Method Article
생체 외 설치류의 삼차 혈관 시스템에서 칼시토닌 유전자 관련 펩타이드의 방출
요약
본 프로토콜은 생체 외 칼시토닌 유전자 관련 펩타이드 (CGRP) 방출 모델 및 설치류의 삼차 혈관계에서 방출되는 CGRP의 양에 대한 약리학 적 제제의 효과를 정량화하는 전략을 설명합니다.
초록
칼시토닌 유전자 관련 펩타이드 (CGRP)는 1980 년대에 칼시토닌 유전자의 스플 라이스 변이체로 처음 발견되었습니다. 발견 이후, 편두통 병태 생리학에서의 역할은 처음에는 강력한 혈관 확장제 특성에 의해, 이후에는 감각 삼차 혈관계에서 신경 전달 물질로서의 존재와 기능에 의해 잘 확립되었습니다. CGRP의 편두통 유발 능력은 제약 산업이 CGRP의 효과를 억제하는 단일 클론 항체 및 길항제를 개발하도록 지원했습니다. 새로운 치료 패러다임이 편두통의 예방 적 치료에 효과적임이 입증되었습니다. 편두통 메커니즘을 더 잘 이해하는 데 유용한 도구 중 하나는 삼차 혈관 시스템에서 CGRP 방출의 생체 외 모델입니다. 새로운 효과적인 편두통 치료법을 더욱 개발하기위한 노하우를 달성하기 위해 다양한 약리학 적 도구와 함께 사용할 수있는 비교적 간단한 방법입니다. 본 프로토콜은 설치류의 삼차 혈관계로부터 방출되는 CGRP의 양에 대한 약리학적 제제의 효과를 정량화하는 CGRP 방출 모델 및 기술을 기술한다. 안락사에서 단백질 수준 측정에 이르는 실험적 접근 방식을 설명하는 절차가 제공됩니다. 생쥐와 쥐 모두에서 삼차 신경절과 삼차 핵 꼬리의 본질적인 분리와 쥐 경막의 준비가 자세히 설명되어 있습니다. 또한 두 종 (쥐와 생쥐)의 대표적인 결과가 제시됩니다. 이 기술은 다양한 약리학 적 화합물과 유전자 변형 동물을 사용하여 편두통 병태 생리학에 관여하는 분자 메커니즘을 조사하는 핵심 도구입니다.
서문
편두통은 WHO에 따르면 10억 명 이상의 사람들에게 영향을 미치는 것으로 추정되는 신경 장애이며 전 세계적으로 장애의 주요 원인 중 하나입니다1. 따라서 편두통은 환자와 사회 모두에 중요한 영향을 미칩니다. CGRP 길항 약물의 최근 임상 적 성공에도 불구하고 많은 환자가 개선 된 치료 옵션을 필요로합니다 2,3,4,5. 새로운 효과적인 치료법으로 이어지는 편두통 병태생리학의 해명이 필요하다. 수막, 삼차 신경절 (TG) 및 삼차 핵 꼬리 (TNC)로 구성된 삼차 혈관 시스템 내의 신호 전달은 편두통 병태 생리학 6,7의 핵심입니다.
37 아미노산 신경 펩티드 칼시토닌 유전자 관련 펩티드 (CGRP)는 Amara와 동료들이 칼시토닌 유전자의 1 차 RNA 전사체를 처리하여 칼시토닌8,9 외에도 CGRP를 암호화하는 mRNA를 제공 할 수 있음을 입증 한 1980 년대 초에 처음 발견되었습니다. 후속 연구는 편두통 병태생리학10에 대한 연관성을 제안했습니다. CGRP는 강력한 혈관 확장 특성 11,12,13,14,15,16,1 7을 가진 신경 전달 물질이며 중추 및 말초 신경계에 널리 분포합니다. 13,14,18,19,20,21,22 . 편두통에 CGRP의 관여는 인간23의 편두통 발작 동안 뇌 외 순환에서 증가 된 CGRP 수준의 발견과 CGRP의 주입이 환자24에서 편두통과 유사한 통증을 유발한다는 사실로 강조되었다. 2 년 후, 편두통 치료에서 CGRP 길항제 olcegepant의 유효성에 대한 최초의 개념 증명 연구가 발표되었습니다25.
CGRP는 TG 21,26, 경막27,28,29 및 TNC30을 자극하는 감각 신경 섬유에서 입증 된 바와 같이 삼차 혈관계에 풍부합니다. 삼차 혈관 시스템에서 CGRP는 TG의 중소 규모 뉴런, 수초가없는 C- 섬유에서 발견되며 TG의 신경 집단의 거의 50 %에서 발현됩니다. CGRP 수용체는 주로 더 큰 뉴런에서 발현되며 수초 Aδ- 섬유31,32에서 발견됩니다. CGRP는 화학적 또는 전기적 자극(33,34)에 의해 뉴런으로부터 방출된다. CGRP의 방출로 이어지는 경로와이 활성화의 위치에 대한 연구는 편두통 병태 생리학을 이해하는 데 중요합니다. 지난 5 년 동안 전임상 연구는 편두통 관련 신호 전달에 대한 광범위한 지식을 얻는 데 기여했으며 새로운 치료법 개발에 기여했습니다35. 혈관 및 신경성 침범을 고려한 많은 방법이 수정되어 편두통 연구에 적용되었습니다. 생물학적 화합물 또는 약리학적 치료(17,36,37) 및 전기 신경-자극(38,39)에 대한 동맥 반응의 생체내 및 시험관내 모델이 언급될 수 있다. 또한, TNC의 활성화 된 뉴런은 c-Fos 발현40,41,42 및이 영역에서의 전기 생리 학적 기록 (43,44)에 의해 검출 될 수있다. 두 방법 모두 머리에서 뇌로 전달되는 통각 신호(예: 경막)를 측정합니다. 단 하나의 전임상 모델을 사용하는 것은 편두통 병태생리학의 전체 그림을 제시하지 않습니다. 따라서 편두통 병태생리학의 여러 측면을 다루는 다양한 모델을 결합하는 것이 중요합니다. 새로운 모델의 지속적인 개발은 편두통 메커니즘의 다양한 측면을 다룰 것이며, 시간이 지나면 편두통 병태생리학의 미스터리가 밝혀질 것입니다.
여기서, CGRP 방출 방법의 상세한 프로토콜이 제시되고, 화학적 자극 후 마우스로부터 단리된 TG 및 TNC에서 생체외로 수행된다. CGRP 방출은 또한 쥐의 경막에서 연구 될 수 있습니다. 따라서, 쥐에 대한 실험 프로토콜에서, 경막은 TG 및 TNC와 함께 기술된다. CGRP 방출 방법의 기초는 1999 년에 처음 기술되었으며, Ebersberger와 동료들은 선구적인 연구를 수행했으며 쥐45에서 경막 구 심성의 화학적 및 전기적 자극 후 CGRP가 경막에서 방출되었음을 발견했습니다. 나중에, 이 접근법은 TG46 및 TNC47로부터의 CGRP 방출로 확장되었다. 이어서, 상기 방법을 마우스에서 TG 및 TNC에 적용하도록 수정하였다. 지금까지 경막에서 CGRP 방출은 마우스에서 어려웠습니다.
프로토콜
모든 동물 관리 및 실험 절차는 동물 관리 및 사용에 대한 유럽 공동체 가이드 (2010 / 63 / UE)에 따라 수행되었습니다. 10주령의 수컷 C57BL/6JBomTac 마우스와 10주령의 수컷 Sprague Dawley 쥐를 사용하여 이 프로토콜을 입증했습니다.
1. 합성 간질액의 제조
- 다음의 제조법에 따라 합성 간질 액 (SIF)을 제조한다 : 108 mM NaCl, 3.48 mM KCl, 3.50 mM MgSO4, 26 mMNaHCO3, 11.70 mM NaH2PO4, 1.50 mM CaCl2, 9.60 mM Na- 글루코 네이트, 5.50 mM 글루코스 및 7.60 mM 자당 (재료 표 참조).
참고: SIF는 자극 대상에 따라 달라질 수 있으며, 예를 들어 칼슘 채널을 연구할 때 칼슘이 없는 용액을 사용할 수 있습니다. - pH를 7.4로 조정하고 카보겐 가스 발생(5% CO2 및 95%O2)46으로 pH를 안정화합니다.
2. 안락사
- 성인 마우스와 쥐를 70 % CO 2 및 30 % O2의 혼합물로 마취시킨다. 한 쌍의 가위를 사용하여 쥐를 참수하고 단두대를 사용하여 쥐를 참수하십시오 (재료 표 참조).
알림: 연구 목적에 맞는 균주와 나이를 사용하십시오. 이 모델에서는 남성과 여성 모두 사용할 수 있습니다. - 척수의 C3-C4 수준에서 머리를 몸에서 분리하십시오.
참고: 안락사는 펜토바르비탈(100-150mg/kg)의 복강 주사로도 수행할 수 있습니다.
3. 해부
- 아래 단계에 따라 쥐 조직을 준비하십시오.
- 가위를 사용하여 머리와 목 주위의 피부와 근육을 제거합니다(그림 1A).
- 뼈 트리머와 가위를 사용하여 아래턱을 머리에서 분리합니다(그림 1B-C).
- 척추의 등쪽 부분에 꼬리로 뼈 트리머를 삽입하여 척수를 열고 척추의 등쪽 부분을 제거하여 척수와 뇌간을 노출시킵니다(그림 1D).
- 소뇌를 노출시키는 이러한 뼈 구조를 제거하기 위해 후두골과 정수리 뼈의 경계로 두개골의 꼬리 부분을 자릅니다(그림 1E).
알림: 척추를 자르고 제거하는 동안 뇌간과 척수를 손상시키지 않는 것이 중요합니다. - 스프링 가위로 뇌간의 등측 부분을 절단하여 양쪽의 브레그마에서 꼬리로 약 13-16mm 떨어진 TNC(Sp5C)를 분리합니다. 왼쪽과 오른쪽 TNC를 SIF에 담그십시오(그림 1E-I).
참고: 설명은 성인 쥐에 해당합니다. - 톱을 사용하여 두개골을 두 개로 나누기 위해 머리를 중간 시상으로 자릅니다(그림 1J-L).
- 주걱을 사용하여 두개골에 부착 된 경막을 건드리지 않고 뇌간으로 들어가는 삼차 신경을 절단하지 않고 조심스럽게 뇌를 제거합니다 (그림 1M-P).
- TG를 분리하려면 시각적 경계 주변의 가지를 포함하여 TG를 자릅니다. 구멍 난소에 들어가는 하악 가지를 자릅니다. 두개골에 들어가는 안과 및 상악 가지가 거시적으로 분할되지 않으므로 잘라냅니다. TG를 해부하는 동안 TG를 덮고 있는 경막을 제거합니다(그림 1Q-T).
- 두개골 반쪽과 TG를 SIF에 담그십시오.
- 아래 단계에 따라 마우스 조직을 준비합니다.
- 작은 가위를 사용하여 머리와 목 주위의 피부와 근육을 제거합니다(그림 2A-B).
- 척추의 등쪽 부분에 꼬리로 작은 가위를 삽입하여 척수를 열고 척추의 등쪽 부분을 제거하여 척수와 뇌간을 노출시킵니다 (그림 2C).
알림: 척추를 자르고 제거하는 동안 척수를 손상시키지 않는 것이 중요합니다. - 소뇌를 노출시키는 이러한 뼈 구조를 제거하기 위해 후두골과 정수리 뼈의 경계로 두개골을 자릅니다(그림 2D-F).
- 그런 다음 정수리 뼈를 시상 중간으로 자르고 뼈를 제거하여 대뇌를 노출시킵니다(그림 2G-I).
- 주걱으로 소뇌를 조심스럽게 제거하여 뇌간을 노출시킵니다 (그림 2J).
- 스프링 가위를 사용하여 뇌간의 TNC 함유 부분을 분리합니다 (그림 2K-N). TIF에 TNC로 뇌간을 담그십시오 (그림 2O).
- 뇌를 제거하고 뇌간으로 들어가는 삼차 신경을 절단합니다 (그림 2P-Q).
- TG를 분리하려면 시각적 경계 주변의 가지를 포함하여 TG를 자릅니다. 구멍 난소에 들어가는 하악 가지를 자릅니다. 두개골에 들어가는 안과 및 상악 가지가 거시적으로 분할되지 않으므로 잘라냅니다. TG를 해부하는 동안 TG를 덮고 있는 경막을 제거합니다(그림 2R-S).
- TG를 SIF에 담그십시오(그림 2T).
4. 세탁
- 두개골 반쪽, TNC 및 TG를 SIF에서 30분 동안 세척하고 실온에서 5분마다 SIF를 교체합니다.
알림: 세척 단계는 쉽게 SIF를 교환할 수 있도록 얇은 명주 그물 뚜껑이 있는 플라스틱 용기에 티슈를 보관하면서 수행할 수 있습니다(그림 3A-B). - 아래 단계에 따라 쥐 조직을 준비하십시오.
- TNC 반쪽을 350μL의 SIF로 분리된 마이크로 원심분리 튜브 캡으로 옮깁니다(그림 3C).
- TG를 마이크로 원심분리 튜브 캡(350μL의 SIF가 포함된 마이크로 원심분리 튜브 캡당 TG 1개)으로 옮깁니다(그림 3C).
- 두개골 반쪽을 점토로 만든 플랫폼 또는 6웰 배양 플레이트에 놓고 두개골에 400μL의 SIF를 채웁니다(그림 3C).
- 아래 단계에 따라 마우스 조직을 준비합니다.
- TNC가 있는 뇌간을 250μL의 SIF가 있는 마이크로 원심분리기 튜브 캡으로 옮깁니다(그림 3D).
- 두 TG를 250μL의 SIF가 있는 마이크로 원심분리 튜브 캡으로 옮깁니다(그림 3D).
알림: 마우스의 조직을 사용할 때 마이크로 원심 분리기 튜브 캡 당 두 개의 TG를 배치하십시오.
- 쥐 두개골과 쥐 조직이 있는 미세 원심분리기 튜브 캡을 37°C의 가습 인큐베이터에 놓습니다. 5분마다 피펫을 사용하여 SIF를 20분 동안 교체합니다.
참고: SIF를 추가 및 제거할 때 티슈를 만지지 않는 것이 중요합니다.
5. 약물 검사
- 기초 CGRP 방출 수준을 결정합니다.
- 마지막 세척 후, 250 μL의 SIF를 마우스 TG 및 TNC에 첨가한다. 쥐 TG 및 TNC에 350μL를 추가하고 각 쥐 두개골에 400μL를 추가합니다.
- 10분 배양 후 미세 원심분리 튜브에서 200μL의 샘플을 수집하고 50μL의 10x EIA 버퍼(CGRP 효소 면역분석 키트와 함께 제공됨, 재료 표 참조)를 추가하여 기저 CGRP 방출을 측정할 수 있도록 합니다(단계 6). 남은 액체는 폐기하십시오.
참고: 배양 시간은 모든 샘플에 대해 동일해야 합니다. - 즉시, 샘플을 -20°C에서 보관한다.
- 기초 CGRP 방출 수준을 샘플링 한 후 다음 세 가지 방법 중 하나를 따르십시오 : (A) 단일 자극 (단계 5.2); (b) 농도-반응 자극(단계 5.3); 및 (C) 자극 억제 (단계 5.4) (그림 4).
알림: 사용 된 테스트 화합물과 농도는 연구 목적에 따라 다릅니다.
- 아래 단계에 따라 단일 자극을 수행하십시오.
- 시험 화합물 또는 비히클을 조직에 첨가하고 10분 동안 그대로 둔다(부피: 마우스 TG 및 TNC의 경우 250 μL, 래트 TG 및 TNC의 경우 350 μL, 및 각 래트 두개골의 경우 400 μL).
- 10분 배양 후 50μL의 10x EIA 버퍼가 있는 미세 원심분리 튜브에서 200μL의 샘플을 수집합니다. 남은 액체를 버리고 즉시 샘플을 -20°C에서 보관하십시오.
참고: 배양 시간은 모든 샘플에 대해 동일해야 합니다.
- 아래 단계에 따라 농도-반응 자극을 수행하십시오.
- 시험 화합물 또는 비히클을 원하는 농도로 희석한다. 가장 낮은 농도부터 시작하여 증가하는 농도로 테스트 화합물을 추가하십시오.
알림: 사용 된 테스트 화합물과 농도는 연구 목적에 따라 다릅니다. 예를 들어, 1 μM, 10 μM, 및 100 μM 수퍼신남알데히드가 본 연구에 사용되었다. - 시험 화합물 및 상응하는 비히클의 최저 농도 (본 연구를 위한 1 μM)를 2개의 동일한 조직 제제에 첨가하고, 10분 동안 인큐베이션한다 (부피: 마우스 조직에 대해 250 μL, 래트 TG 및 TNC에 대해 350 μL, 및 각각의 래트 두개골에 대해 400 μL).
- 10분 배양 후 50μL의 10x EIA 버퍼가 있는 미세 원심분리 튜브에서 200μL의 샘플을 수집합니다.
- 남은 액체를 버리고 두 번째로 낮은 농도 (본 연구의 경우 10 μM)를 조직에 첨가하십시오.
- 즉시, 샘플을 -20°C에서 보관한다.
- 나머지 농도 (본 연구의 경우 100 μM)로이 절차를 반복하십시오.
- 시험 화합물 또는 비히클을 원하는 농도로 희석한다. 가장 낮은 농도부터 시작하여 증가하는 농도로 테스트 화합물을 추가하십시오.
- 아래 단계에 따라 자극 억제를 수행하십시오.
- 차단제 또는 비히클을 조직에 첨가하고 10분 동안 인큐베이션한다 (부피: 마우스 조직의 경우 250 μL, 래트 TG 및 TNC의 경우 350 μL, 및 각각의 래트 두개골에 대해 400 μL).
알림: 사용되는 차단제와 농도는 연구 목적에 따라 다릅니다. 예를 들어, 3 μM 글리벤클라미드를 도 5의 대표적인 결과로 사용하였다. - 10분 배양 후 50μL의 10x EIA 버퍼가 있는 마이크로 원심분리 튜브에서 200μL 샘플을 수집합니다. 남은 액체를 버리고 즉시 샘플을 -20°C에서 보관하십시오.
- 작용제 또는 작용제 + 차단제( 재료 표 참조)를 조직에 추가하고 10분 동안 배양합니다.
알림: 사용되는 작용제, 차단제 및 농도는 연구 목적에 따라 다릅니다. 본 연구에서는 3μM의 글리벤클라미드와 1μM의 캡사이신을 사용했습니다( 그림 5). - 10분 배양 후 50μL의 10x EIA 버퍼가 있는 마이크로 원심분리 튜브에서 200μL 샘플을 수집합니다. 남은 액체를 버리고 즉시 샘플을 -20°C에서 보관하십시오.
- 차단제 또는 비히클을 조직에 첨가하고 10분 동안 인큐베이션한다 (부피: 마우스 조직의 경우 250 μL, 래트 TG 및 TNC의 경우 350 μL, 및 각각의 래트 두개골에 대해 400 μL).
- 실험에 대한 양성 대조군을 수행합니다.
- 적절한 경우, 프로토콜 종료 시 양성 대조군(예: 1-10μM의 캡사이신, 재료 표 참조)을 조직에 추가하고 10분의 배양 기간 후에 50μL의 10x EIA 버퍼가 있는 미세 원심분리 튜브에서 200μL 샘플을 수집합니다.
참고: 설정과 조직이 작동하는지 확인하기 위해 양성 대조군을 포함하는 것이 유리합니다. 캡사이신 48,49,50 또는 칼륨의 탈분극 자극 (KCl의 40-60 mM)46,47,49는 삼차 혈관계에서 CGRP의 방출을 유발하기 위해 일상적으로 사용됩니다. 40-60 mM의 KCl SIF는 NaCl이 등몰 기준으로 KCl로 교환되는 것을 제외하고는 SIF로서 제조된다.
- 적절한 경우, 프로토콜 종료 시 양성 대조군(예: 1-10μM의 캡사이신, 재료 표 참조)을 조직에 추가하고 10분의 배양 기간 후에 50μL의 10x EIA 버퍼가 있는 미세 원심분리 튜브에서 200μL 샘플을 수집합니다.
6. CGRP 농도 분석
- 제조업체의 프로토콜에 따라 효소 면역 분석(EIA) 키트를 사용하여 방출되는 CGRP의 양을 측정합니다( 재료 표 참조).
- 플레이트 광도계를 사용하여 410nm에서 광학 밀도를 측정합니다. 다른 CGRP EIA 키트를 사용하는 경우 제조업체의 프로토콜에 제공된 파장에서 광학 밀도를 측정합니다.
참고: 샘플은 표준 곡선과 일치하도록 희석해야 합니다. - 데이터 분석을 수행합니다.
- 데이터를 절대 농도로 제시하거나 특정 조직에서 기저 CGRP 방출로 정규화하십시오.
결과
이 기술은 편두통과 관련된 CGRP 관련 분자 메커니즘을 조사하는 도구입니다. 그것은 삼차 혈관 시스템의 다른 수준에서 CGRP 방출을 평가하는 장점이 있으며 다양한 약리학 적 화합물과 함께 야생형 및 형질 전환 마우스와 쥐 모두에 적용될 수 있습니다. 여기에서는 랫트의 농도-반응 및 차단 실험과 야생형 및 형질전환 마우스의 농도-반응 결과를 제시합니다.
CGRP 방출 방법은 암컷 자발적 삼차 동종 (STA) 쥐에서 TG 및 경막으로부터의 CGRP 방출에 대한 KATP 채널 억제제 글리벤 클라 미드의 효과를 연구하기 위해 사용되었다. 먼저, 캡사이신의 최적 농도는 농도-반응 연구 설계를 사용하여 발견되었다. 캡사이신 노출은 비히클에 비해 경막 및 TG로부터 상당한 CGRP 방출을 유도했습니다(그림 5). 경막에서, CGRP의 최대 방출은 캡사이신의 1 μM에서 발견되었고, TG에서, 최대 CGRP 방출은 캡사이신의 10 μM에서 발견되었다 (도 5A-B). 농도-반응 실험에 기초하여, 1 μM의 캡사이신 및 3 μM의 글리벤클라미드를 블로킹 실험에 사용하였다. 글리벤클라미드는 일원 ANOVA51로 분석했을 때 경막(P=0.441) 및 TG(P=0.881)로부터의 기저 CGRP 방출에 영향을 미치지 않았다. 글리벤클라마이드는 단방향 ANOVA로 분석했을 때 비히클을 사용한 캡사이신에 비해 경막에서 캡사이신 유도 CGRP 방출을 40%(P=0.031) 및 TG를 39%(P=0.003) 유의하게 감소시켰습니다(그림 5C-D)51.
마우스에서, 프로토콜은 편두통의 GTN 마우스 모델에서 일시적인 수용체 전위 ankyrin 1 (TRPA1) 이온 채널의 관여를 조사하기 위해 사용되었으며, 여기서 GTN 유도 과민증은 TRPA1 채널에 완전히 의존적이었다. TRPA1 작용제 수퍼신남알데히드(SCA)는 1μM, 10μM 및 100μM의 SCA를 사용하여 TG로부터 용량 의존적 방식으로 CGRP를 방출하는 것으로 밝혀졌으며, 그 결과 양방향 분산 분석으로 분석했을 때 비히클에 비해 CGRP의 방출이 각각 9%(P=0.23), 51%(P=0.011) 및 69%(P=0.0097) 증가했습니다. 이러한 방출은 1 μM, 10 μM 및 100 μM의 SCA에 노출된 Trpa1 널 마우스로부터의 TG에서 부재하였으며, 이원 분산 분석으로 분석했을 때, 비히클과 비교하여 CGRP의 방출에서 각각 11% (P > 0.99), -13% (P > 0.99) 및 9% (P=0.97) 퍼센트의 변화가 나타났다. 10μM의 캡사이신(양성 대조군)을 사용한 후속 자극은 모든 조직 샘플이 CGRP를 방출할 수 있음을 보여줍니다(그림 6)50.
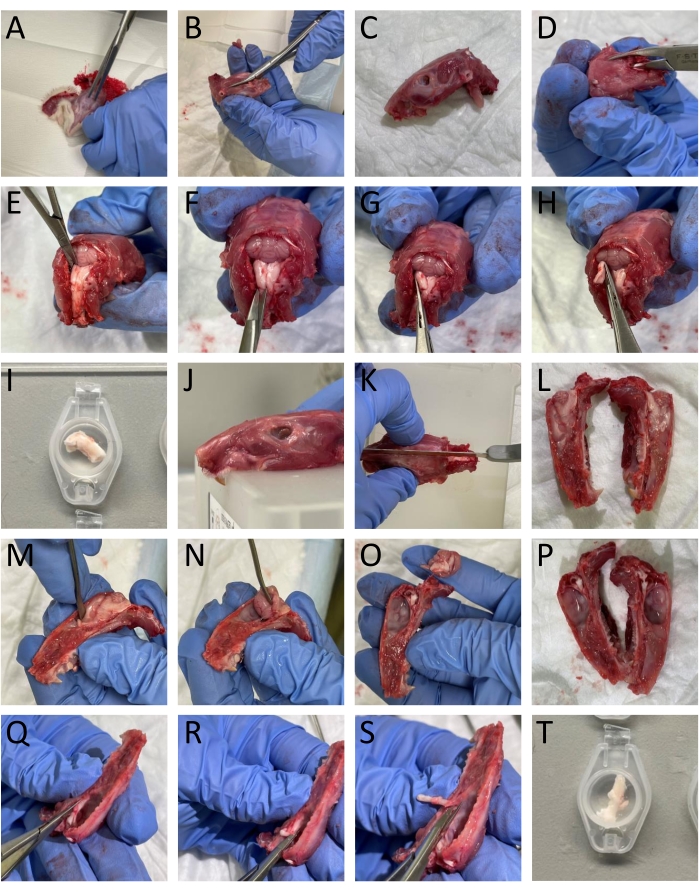
그림 1 : 쥐의 조직을 단계별로 해부합니다. (A-T) 세부 정보는 프로토콜 섹션(3.1단계)에 제공됩니다. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
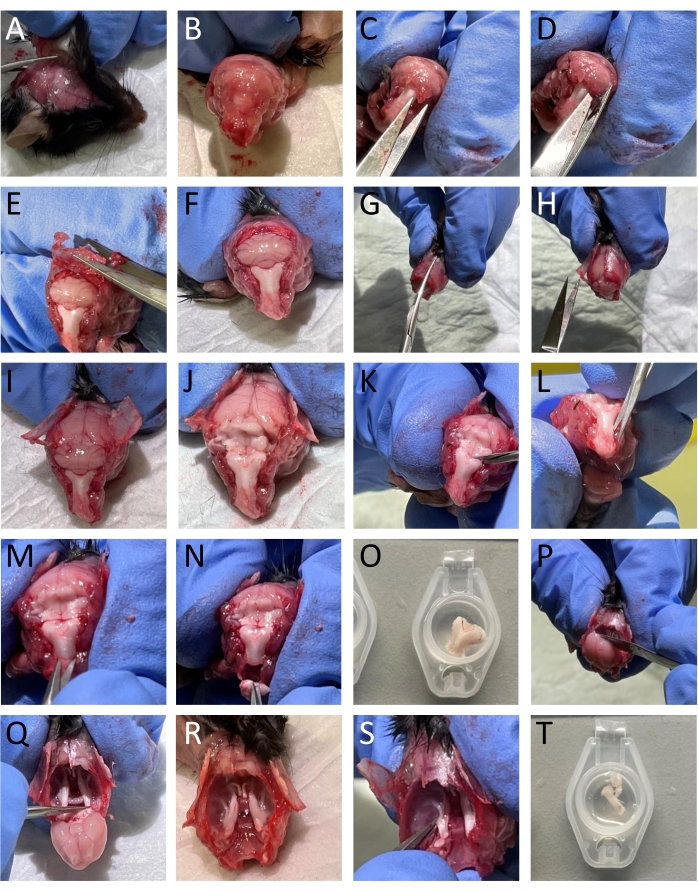
그림 2: 생쥐의 조직을 단계별로 해부합니다. (AT) 세부 정보는 프로토콜 섹션(3.2단계)에 제공됩니다. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
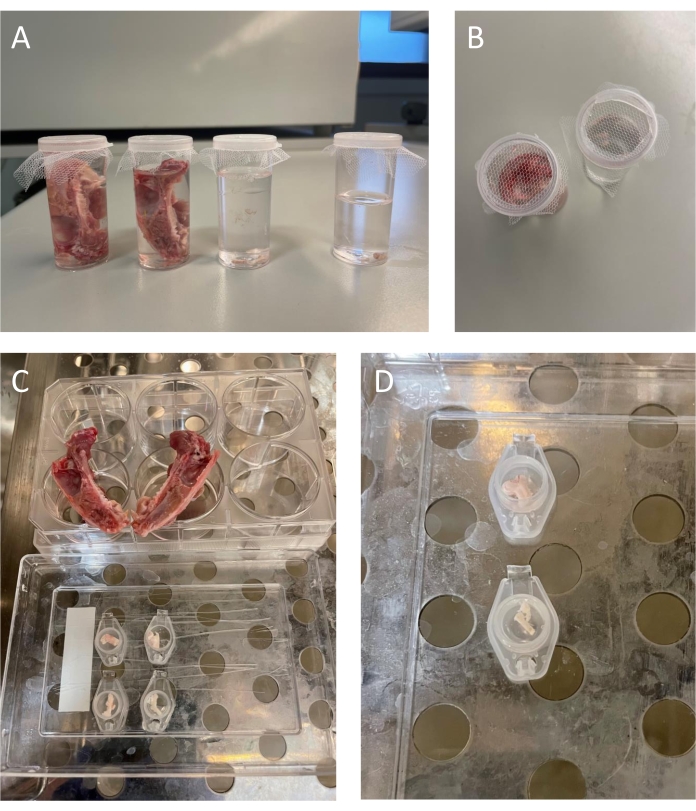
그림 3 : 설치류 조직의 세척 및 배양. (A-B) SIF가 있는 플라스틱 용기에 갓 분리된 조직. 컨테이너는 SIF를 쉽게 변경할 수 있도록 얇은 명주 그물로 덮여 있습니다. (C) 쥐 조직 - 두개골의 내부 안감을 덮는 경막이 있는 두 개의 두개골 반쪽을 6-웰 배양 접시에 놓는다. 오른쪽 및 왼쪽 삼차 핵 꼬리는 별도의 미세 원심 분리기 튜브 뚜껑 (뚜껑의 맨 윗줄)에 있습니다. 개별 미세 원심 분리기 튜브 뚜껑 (뚜껑의 맨 아래 줄)에있는 두 개의 삼차 신경절. (d) 마우스 조직 - 삼차 핵 꼬리-함유 뇌간의 일부를 별도의 미세원심분리 튜브 뚜껑(상단)에 담는다. 두 개의 마우스 삼차 신경절이 하나의 미세 원심 분리 튜브 뚜껑 (하단)에 있습니다. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
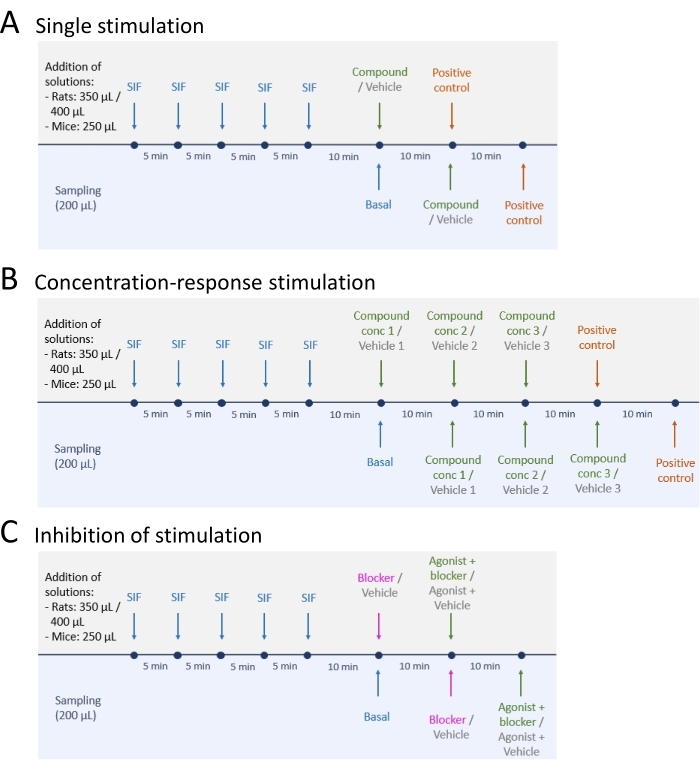
그림 4: CGRP 릴리스를 위한 연구 설계. CGRP 방출 실험을 수행하기 위한 세 가지 다른 프로토콜. 약물은 합성 간질 액 (SIF)으로 희석해야합니다. (A) 단일 자극. (B) 집중 반응 자극. (C) 자극의 억제. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
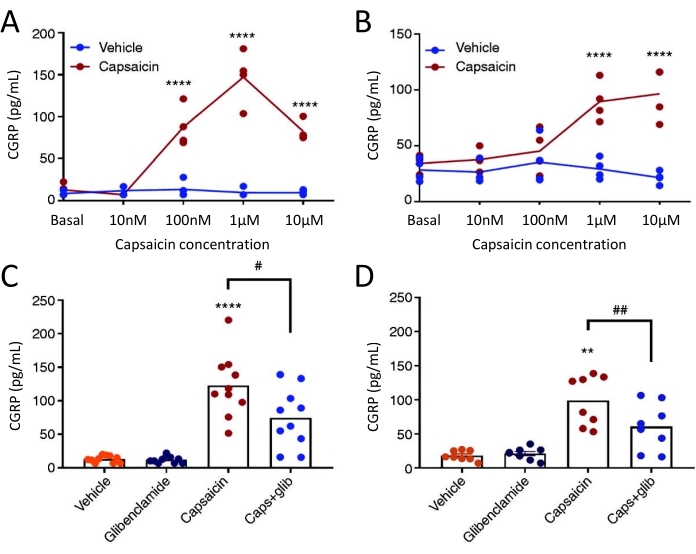
그림 5: 글리벤클라미드는 쥐 경막 및 삼차 신경절에서 캡사이신 유도 CGRP 방출을 억제합니다. 원래 Thomas Jefferson University52에서 공급된 암컷 자발적 삼차 동종(STA) 쥐(215-318g)로부터 분리된 삼차 신경절 및 경막으로부터의 CGRP 수준을 상업용 인간 CGRP EIA 키트로 측정하였다. (A-B) 캡사이신 (10 nM, 100 nM, 1 μM 및 10 μM)의 농도 증가 후 (A) 경막 및 (B) 삼차 신경절로부터의 CGRP 방출 (n = 4). 데이터는 개별 점으로 제시되고 양방향 분산 분석으로 분석되었습니다. p < 0.0001 (CD) 비히클에 10분 노출 후 (C) 경막 및 (D) 삼차 신경절에서 방출된 CGRP 수준, 3μM 글리벤클라미드 (글리브), 1μM 캡사이신 및 1μM 캡사이신 + 3μM glib (n=6-11). 데이터는 개별 점과 평균값으로 제시되며 일원 분산 분석으로 분석되었습니다. *차량과 비교. #캡사이신과 캡사이신 + 글립을 비교한 캡사이신. #P < 0.05, ** 및 ##P < 0.01, ****P < 0.0001입니다. 분석은 Bonferroni의 다중 비교 테스트로 이어졌습니다. 모든 테스트에 대해 상당한 수준의 α = 0.05가 사용되었습니다. 이 수치는 Christensen et al.에서 수정되었습니다. 51. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
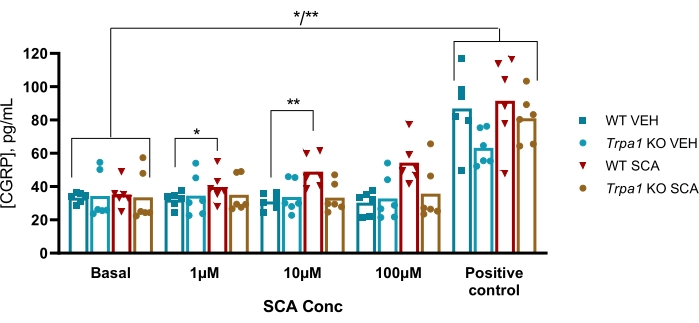
그림 6: SCA 노출은 마우스 삼차 신경절에서 TRPA1 의존성 CGRP 방출을 초래합니다. WT 및 Trpa1 null (Trpa1tm1 / Dpc) 53 수컷 마우스 (8-10 주)에서 분리 된 삼차 신경절로부터 방출 된 CGRP 수준은 양성 대조군으로서 1 μM, 10 μM 및 100 μM에서 수퍼 신남 알데히드 (SCA) 및 10 μM에서 캡사이신에 노출 된 후 래트 CGRP EIA 키트로 측정되었다 (n = 6). 각 마우스의 데이터는 개별 점으로 표시되며 막대는 평균값을 나타냅니다. 통계: 각 농도에서 SCA와 비히클 사이 및 기저 대조군과 양성 대조군 사이의 비교는 양방향 반복 ANOVA로 수행되었다. 상당한 수준의 α = 0.05. *P < 0.05, **P < 0.01. 이 수치는 Christensen et al.에서 수정되었습니다. 50. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
토론
설명 된 방법은 편두통 병태 생리학에서 CGRP의 중요성을 보여주는 연구에 따라 개발되었습니다. 머리 부위의 통증 신호에 중요한 삼차 혈관 시스템에서 CGRP의 방출과 관련된 메커니즘을 조사하는 데 매우 적합합니다. 이 모델에서 얻은 CGRP의 양은 경막, TG 및 TNC를 자극하는 삼차 신경으로부터의 CGRP 방출을 직접 측정합니다. CGRP 방출량은 인간의 열 응고, 고양이 39,55,56의 삼차 자극 및 편두통 발작23 후 혈장에서 측정 된 방출보다 정량적으로 45,54 더 큽니다. 한 가지 설명은 CGRP가 혈액에서 희석되고 분해된다는 것입니다54. 그러나 화학 물질을 사용한 직접 자극이 병태 생리 학적 활성화보다 우수 할 수 있습니다. 추가 장점은 삼차 혈관계 내의 세 가지 다른 부위에서 방출을 찾을 수 있고 약리학 적 조작과 함께 및 유전자 변형 설치류의 조직에서 사용할 수 있다는 것입니다.
최근에, 많은 전임상 설치류 모델은 von Frey 테스트57,58, 찡그린 얼굴59,60,61 또는 가벼운 혐오62,63,64를 사용하여 물질의 전신 투여 및 후속 통증 또는 편두통 관련 판독에 중점을 둡니다. 이 방법은 다양한 물질의 통증 유발 및 통증 완화 특성을 이해하는 데 유용합니다. 그러나 이러한 접근법은 관련된 특정 표적 조직에 대한 정보를 제공하지 않습니다. 본 방법에서, 삼차 혈관 시스템은 경막, TG 및 TNC의 세 가지 구조로 나뉩니다. 이를 통해 각 구조의 국소 노출과 특정 물질의 작용 위치 평가가 가능합니다. 이것은 쥐에서 전압 게이트 칼슘 채널의 역할을 탐구 한 2011 년 연구에서 활용되었으며, 이러한 채널의 억제는 삼차 혈관 경로47의 세 가지 구조에서 다른 것으로 밝혀졌습니다. 신경계의 구조를 해부 할 때, axotomy는 피할 수 없습니다. Axotomy는 다양한 유전자65의 전사를 변경하는 것으로 나타났습니다. 이러한 전사 변화는 너무 느려서 이 방법의 결과에 영향을 미치지 않지만, 생체 내 상황과 비교할 때 인산화의 변화를 배제할 수 없습니다(46). CGRP와 같은 신경 펩티드는 세포 체세포에서 형성되지만 신경 펩티드의 방출 및 작용은 일반적으로 중추 또는 말초 신경 말단에 있습니다. 따라서, 말단을 포함한 손상되지 않은 뉴런에 대한 연구는 신경 펩티드 방출을 연구 할 때 흥미 롭습니다. 따라서 분리 된 신경절에서 뉴런의 배양을 연구하는 방법이 말단의 모델로 사용되도록 확립되었습니다. 그러나, 뉴런 세포 배양은 기계적 해리가 배양물(46)에서 뉴런을 파괴할 수 있기 때문에 몇 가지 문제에 종속된다. 세포의 배양과 관련된 더 긴 시간 프레임은 이 방법을 축리술 및 배양 조건으로 인한 전사체 변화에 민감하게 만든다65. 또한, 성장 인자의 첨가 및 표면 코팅 상의 배양은 전달자 및 수용체 발현66,67,68,69로서 뉴런 특성을 변화시켰다. 이러한 문제는 신경 세포 배양 대신 새로 분리 된 손상되지 않은 신경절을 연구 할 때 피할 수 있습니다.
생체 외 CGRP 방출 방법의 한 가지 과제는 재현 가능한 결과에 필요한 조직의 정확한 해부입니다. 특히 TNC의 정확한 해부는 눈에 보이는 경계가없는 뇌간 내의 구조이기 때문에 어렵습니다. 또한, 경막은 깨지기 쉽기 때문에 손상되지 않은 구조를 보장하기 위해 뇌 제거를 신중하게 수행해야합니다. 이러한 장애는 다양한 조직 크기를 초래할 수 있으며, 따라서 다양한 기저 및 자극 유발 CGRP 수준을 초래할 수 있습니다. 그러나, 이러한 변동은 기초 CGRP 방출에 대한 정규화에 의해 설명될 수 있다. 또한 마우스에서 TNC를 분리 할 때, 뇌간의 전체 하부가 분리되고 쥐에서보다 구체적인 TNC 함유 부분이 아니라는 점에 유의해야합니다. 일반적으로 쥐 조직을 사용하는 것이 유리할 수 있는데, 이는 경막으로부터의 CGRP 방출을 측정하고 TNC를 보다 정밀하게 해부할 수 있기 때문이다. 또한, 조직의 크기는 또한 한 쥐가 두 개의 두개골 반쪽, 두 개의 TG 및 두 개의 TNC를 초래하기 때문에 쥐를 비히클 제어로 사용할 수 있게 하며, 여기서 조직의 한 조각은 물질 자극에 사용되고 다른 하나는 비히클에 사용됩니다. 마우스를 사용할 때 두 TG가 하나의 샘플에 풀링되고 TNC가 하나의 뇌간으로 해부되기 때문에 하나의 실험에 두 마리의 동물이 필요합니다. 따라서 물질 자극에는 2 개의 TG와 1 개의 뇌간이 사용되고 다른 마우스의 2 개의 TG와 1 개의 뇌간이 차량 제어에 사용됩니다. 그 결과 동일한 수의 반복을 얻기 위해 쥐에 비해 두 배 많은 마우스를 사용합니다. 사용되는 마우스의 수를 줄이기 위해, 뇌간 절편으로부터 CGRP 방출을 측정하는 방법이 제안되었다49. 마우스의 사용이 가능하도록 방법이 변형되었다는 장점이 있다. 이를 통해 이미 이용 가능한 많은 형질전환 마우스 균주를 사용할 수 있으며, 이는 예를 들어 신호 전달 경로를 연구하는 데 유용한 도구입니다. 실험에 사용 된 조직이 CGRP를 방출 할 수 있도록 실험 마지막에 양성 대조군을 포함시켜야합니다. 양성 대조군은 TRPV1 작용제 캡사이신 또는 탈분극 자극 칼륨 (KCl) 일 수 있으며, 이는 마우스와 래트46,47,48,49,50 모두에서 삼차 혈관계로부터 CGRP를 방출하는 것으로 밝혀졌습니다. 더욱이, 상기 방법은 또한 편두통 연구70 내에서 큰 관심의 또 다른 펩티드 - 뇌하수체 아데닐레이트 사이클라제-활성화 펩티드 (PACAP)로서 다른 관련 펩티드의 방출을 측정하도록 적응되었다.
상기 방법은 래트 및 마우스의 특정 표적 조직으로부터의 CGRP 방출을 조사하기 위한 유용한 도구를 제공한다. 뉴런 배양과 관련된 문제를 피하는 비교적 빠른 방법입니다. 상기 방법 프로토콜은 다양한 약리학적 화합물에 의한 반응의 농도-반응 관계 또는 억제를 연구하기 위해 용이하게 변형될 수 있다. 생체 외 CGRP 방출 방법은 편두통 병태생리학에서 CGRP 방출과 관련된 CGRP 및 기타 메커니즘의 역할을 연구하는 데 유용한 여러 전임상 방법 중 하나입니다.
공개
저자는 공개 할 것이 없습니다.
감사의 말
이 작업은 캔디 재단에서 자금을 지원했습니다.
자료
| Name | Company | Catalog Number | Comments |
| 6-well culture plate | NUNC | 140675 | |
| Calcium chloride dihydrate | Merck | 1.02382.1000 | For SIF buffer |
| Caps for plastic containers | ThermoFisher Scientific | 536617 | |
| Capsaicin | Merck | M2028 | |
| CGRP kits | AH Diagnostics | A05482.96 | |
| CO2 | Strandmøllen | 4.6 | For carbogen gassing of SIF |
| Delicate Bone Trimmer | Fine Science Tools | 16109-14 | |
| Glibenclamide | Tocris | 911 | |
| Glucose | Merck | G7021 | For SIF buffer |
| Guillotine for rats | Scandidact | NS-802 | |
| Magnesium sulfate heptahydrate | Merck | M5921 | For SIF buffer |
| Microcenrifuge tubes + lids/caps | VWR | 700-5239 | |
| Mini Hacksaw | BAHCO | 208 | |
| O2 | Strandmøllen | 4.5 | For carbogen gassing of SIF |
| Pentobarbital | Glostrup pharmacy | NA | Magistral formula |
| Plastic containers | ThermoFisher Scientific | 536455 | |
| Plate photometer - Infinite M200 | Tecan | NA | Infinite M200 is discontinued. A Infinite 200 PRO is available at Tecan. Software: SW Magellan v.6.3 |
| Potassium chloride | Merck | P9333 | For SIF buffer |
| Scissor | Allgaier Instruments | 307-156-170 | |
| Small scissor | Allgaier Instruments | 04-520-115 | |
| Sodium bicarbonate | Merck | S6014 | For SIF buffer |
| Sodium chloride | Merck | S9888 | For SIF buffer |
| Sodium dihydrogen phosphate monohydrate | Merck | 1.06346.1000 | For SIF buffer |
| Sodium gluconate | Merck | S2054 | For SIF buffer |
| Spatula | Bochem Lab Supply | 3018 | |
| Spring scissor | Fine Science Tools | 15024-10 | |
| Sucrose | Merck | 84097 | For SIF buffer |
| Supercinnamaldehyde | Merck | S3322 | |
| Tulle (fabrics) | NA | NA | Bought in the local fabrics store |
참고문헌
- GBD 2016 Collaborators. Global, regional, and national incidence, prevalence, and years lived with disability for 328 diseases and injuries for 195 countries, 1990-2016: A systematic analysis for the Global Burden of Disease Study. The Lancet. 390 (10100), 1211-1259 (2017).
- Dodick, D. W. CGRP ligand and receptor monoclonal antibodies for migraine prevention: Evidence review and clinical implications. Cephalalgia: An International Journal of Headache. 39 (3), 445-458 (2019).
- Sacco, S., et al. European headache federation guideline on the use of monoclonal antibodies acting on the calcitonin gene related peptide or its receptor for migraine prevention. The Journal of Headache and Pain. 20 (1), 6 (2019).
- Moreno-Ajona, D., Pérez-Rodríguez, A., Goadsby, P. J. Gepants, calcitonin-gene-related peptide receptor antagonists: what could be their role in migraine treatment. Current Opinion in Neurology. 33 (3), 309-315 (2020).
- Khan, S., Olesen, A., Ashina, M. CGRP, a target for preventive therapy in migraine and cluster headache: Systematic review of clinical data. Cephalalgia: An International Journal of Headache. 39 (3), 374-389 (2019).
- Edvinsson, L., Haanes, K. A., Warfvinge, K., Krause, D. N. CGRP as the target of new migraine therapies - successful translation from bench to clinic. Nature Reviews Neurology. 14 (6), 338 (2018).
- Goadsby, P. J., et al. Pathophysiology of migraine: A disorder of sensory processing. Physiological Reviews. 97 (2), 553-622 (2017).
- Amara, S. G., Jonas, V., Rosenfeld, M. G., Ong, E. S., Evans, R. M. Alternative RNA processing in calcitonin gene expression generates mRNAs encoding different polypeptide products. Nature. 298 (5871), 240-244 (1982).
- Rosenfeld, M. G., et al. Production of a novel neuropeptide encoded by the calcitonin gene via tissue-specific RNA processing. Nature. 304 (5922), 129-135 (1983).
- Edvinsson, L., Goadsby, P. J. Discovery of CGRP in relation to migraine. Cephalalgia: An International Journal of Headache. 39 (3), 331-332 (2019).
- Brain, S. D., Williams, T. J., Tippins, J. R., Morris, H. R., MacIntyre, I. Calcitonin gene-related peptide is a potent vasodilator. Nature. 313 (5997), 54-56 (1985).
- Fisher, L. A., et al. Stimulation of noradrenergic sympathetic outflow by calcitonin gene-related peptide. Nature. 305 (5934), 534-536 (1983).
- Hanko, J., Hardebo, J. E., Kåhrström, J., Owman, C., Sundler, F. Calcitonin gene-related peptide is present in mammalian cerebrovascular nerve fibres and dilates pial and peripheral arteries. Neuroscience Letters. 57 (1), 91-95 (1985).
- Uddman, R., Edvinsson, L., Ekblad, E., Håkanson, R., Sundler, F. Calcitonin gene-related peptide (CGRP): perivascular distribution and vasodilatory effects. Regulatory Peptides. 15 (1), 1-23 (1986).
- Edvinsson, L. Functional role of perivascular peptides in the control of cerebral circulation. Trends in Neurosciences. 8, 126-131 (1985).
- Edvinsson, L., Ekman, R., Jansen, I., Ottosson, A., Uddman, R. Peptide-containing nerve fibers in human cerebral arteries: Immunocytochemistry, radioimmunoassay and in vitro pharmacology. Annals of Neurology. 21 (5), 431-437 (1987).
- Edvinsson, L., Fredholm, B. B., Hamel, E., Jansen, I., Verrecchia, C. Perivascular peptides relax cerebral arteries concomitant with stimulation of cyclic adenosine monophosphate accumulation or release of an endothelium-derived relaxing factor in the cat. Neuroscience Letters. 58 (2), 213-217 (1985).
- Brain, S. D., Grant, A. D. Vascular actions of calcitonin gene-related peptide and adrenomedullin. Physiological Reviews. 84 (3), 903-934 (2004).
- Skofitsch, G., Jacobowitz, D. M. Calcitonin gene-related peptide: Detailed immunohistochemical distribution in the central nervous system. Peptides. 6 (4), 721-745 (1985).
- Suzuki, N., Hardebo, J. E., Owman, C. Origins and pathways of cerebrovascular nerves storing substance P and calcitonin gene-related peptide in rat. Neuroscience. 31 (2), 427-438 (1989).
- Uddman, R., Edvinsson, L., Ekman, R., Kingman, T., McCulloch, J. Innervation of the feline cerebral vasculature by nerve fibers containing calcitonin gene-related peptide: trigeminal origin and co-existence with substance P. Neuroscience Letters. 62 (1), 131-136 (1985).
- Warfvinge, K., Edvinsson, L. Distribution of CGRP and CGRP receptor components in the rat brain. Cephalalgia: An International Journal of Headache. 39 (3), 342-353 (2019).
- Goadsby, P. J., Edvinsson, L., Ekman, R. Vasoactive peptide release in the extracerebral circulation of humans during migraine headache. Annals of Neurology. 28 (2), 183-187 (1990).
- Lassen, L. H., et al. CGRP may play a causative role in migraine. Cephalalgia: An International Journal of Headache. 22 (1), 54-61 (2002).
- Olesen, J., et al. Calcitonin gene-related peptide receptor antagonist BIBN 4096 BS for the acute treatment of migraine. New England Journal of Medicine. 350 (11), 1104-1110 (2004).
- Eftekhari, S., et al. Localization of CGRP, CGRP receptor, PACAP and glutamate in trigeminal ganglion. Relation to the blood-brain barrier. Brain Research. 1600, 93-109 (2015).
- Keller, J. T., Marfurt, C. F. Peptidergic and serotoninergic innervation of the rat dura mater. Journal of Comparative Neurology. 309 (4), 515-534 (1991).
- Edvinsson, L., et al. Innervation of the human middle meningeal artery: immunohistochemistry, ultrastructure, and role of endothelium for vasomotility. Peptides. 19 (7), 1213-1225 (1998).
- Lennerz, J. K., et al. Calcitonin receptor-like receptor (CLR), receptor activity-modifying protein 1 (RAMP1), and calcitonin gene-related peptide (CGRP) immunoreactivity in the rat trigeminovascular system: Differences between peripheral and central CGRP receptor distribution. Journal of Comparative Neurology. 507 (3), 1277-1299 (2008).
- Eftekhari, S., Edvinsson, L. Calcitonin gene-related peptide (CGRP) and its receptor components in human and rat spinal trigeminal nucleus and spinal cord at C1-level. BMC Neuroscience. 12, 112 (2011).
- Eftekhari, S., et al. Differential distribution of calcitonin gene-related peptide and its receptor components in the human trigeminal ganglion. Neuroscience. 169 (2), 683-696 (2010).
- Eftekhari, S., Warfvinge, K., Blixt, F. W., Edvinsson, L. Differentiation of nerve fibers storing CGRP and CGRP receptors in the peripheral trigeminovascular system. The Journal of Pain. 14 (11), 1289-1303 (2013).
- Spitzer, M. J. S., Reeh, P. W., Sauer, S. K. Mechanisms of potassium- and capsaicin-induced axonal calcitonin gene-related peptide release: Involvement of L- and T-type calcium channels and TRPV1 but not sodium channels. Neuroscience. 151 (3), 836-842 (2008).
- Evans, A. R., Nicol, G. D., Vasko, M. R. Differential regulation of evoked peptide release by voltage-sensitive calcium channels in rat sensory neurons. Brain Research. 712 (2), 265-273 (1996).
- Gupta, S., Villalón, C. M. The relevance of preclinical research models for the development of antimigraine drugs: Focus on 5-HT 1B/1D and CGRP receptors. Pharmocology & Therapeutics. 128 (1), 170-190 (2010).
- Williamson, D. J., Hargreaves, R. J., Hill, R. G., Shepheard, S. L. Intravital microscope studies on the effects of neurokinin agonists and calcitonin gene-related peptide on dural vessel diameter in the anaesthetized rat. Cephalalgia: An International Journal of Headache. 17 (4), 518-524 (1997).
- Gupta, S., Bhatt, D. K., Boni, L. J., Olesen, J. Improvement of the closed cranial window model in rats by intracarotid infusion of signalling molecules implicated in migraine. Cephalalgia: An International Journal of Headache. 30 (1), 27-36 (2010).
- Knight, Y. E., Edvinsson, L., Goadsby, P. J. Blockade of calcitonin gene-related peptide release after superior sagittal sinus stimulation in cat: a comparison of avitriptan and CP122, 288. Neuropeptides. 33 (1), 41-46 (1999).
- Goadsby, P. J., Edvinsson, L., Ekman, R. Release of vasoactive peptides in the extracerebral circulation of humans and the cat during activation of the trigeminovascular system. Annals of Neurology. 23 (2), 193-196 (1988).
- Tassorelli, C., Joseph, S. A. Systemic nitroglycerin induces Fos immunoreactivity in brainstem and forebrain structures of the rat. Brain Research. 682 (1-2), 167-181 (1995).
- Ramachandran, R., et al. A naturalistic glyceryl trinitrate infusion migraine model in the rat. Cephalalgia: An International Journal of Headache. 32 (1), 73-84 (2012).
- Hoskin, K. L., Zagami, A. S., Goadsby, P. J. Stimulation of the middle meningeal artery leads to Fos expression in the trigeminocervical nucleus: a comparative study of monkey and cat. Journal of Anatomy. 194, 579-588 (1999).
- Charbit, A. R., Akerman, S., Goadsby, P. J. Comparison of the Effects of Central and Peripheral Dopamine Receptor Activation on Evoked Firing in the Trigeminocervical Complex. Journal of Pharmacology and Experimental Therapeutics. 331 (2), 752-763 (2009).
- Koulchitsky, S., Fischer, M., Messlinger, K. Calcitonin gene-related peptide receptor inhibition reduces neuronal activity induced by prolonged increase in nitric oxide in the rat spinal trigeminal nucleus. Cephalalgia: An International Journal of Headache. 29 (4), 408-417 (2009).
- Ebersberger, A., Averbeck, B., Messlinger, K., Reeh, P. W. Release of substance P, calcitonin gene-related peptide and prostaglandin E2 from rat dura mater encephali following electrical and chemical stimulation in vitro. Neuroscience. 89 (3), 901-907 (1999).
- Eberhardt, M., et al. Calcitonin gene-related peptide release from intact isolated dorsal root and trigeminal ganglia. Neuropeptides. 42 (3), 311-317 (2008).
- Amrutkar, D. V., Ploug, K. B., Olesen, J., Jansen-Olesen, I. Role for voltage gated calcium channels in calcitonin gene-related peptide release in the rat trigeminovascular system. Neuroscience. 172, 510-517 (2011).
- Gupta, S., et al. Evidence for CGRP re-uptake in rat dura mater encephali. British Journal of Pharmacology. 161 (8), 1885-1898 (2010).
- Kageneck, C., Nixdorf-Bergweiler, B. E., Messlinger, K., Fischer, M. J. M. Release of CGRP from mouse brainstem slices indicates central inhibitory effect of triptans and kynurenate. Journal of Headache and Pain. 15 (1), 1-9 (2014).
- Christensen, S. L., et al. CGRP-dependent signalling pathways involved in mouse models of GTN- cilostazol- and levcromakalim-induced migraine. Cephalalgia: An International Journal of Headache. 41 (14), 1413-1426 (2021).
- Christensen, S. L., et al. ATP sensitive potassium (KATP) channel inhibition: A promising new drug target for migraine. Cephalalgia: An International Journal of Headache. 40 (7), 650-664 (2020).
- Oshinsky, M. L., et al. Spontaneous trigeminal allodynia in rats: A model of primary headache. Headache. 52 (9), 1336 (2012).
- Kwan, K. Y., et al. TRPA1 contributes to cold, mechanical, and chemical nociception but is not essential for hair-cell transduction. Neuron. 50 (2), 277-289 (2006).
- Eltorp, C., Jansen-Olesen, I., Hansen, A. J. Release of calcitonin gene-related peptide (CGRP) from guinea pig dura mater in vitro is inhibited by sumatriptan but unaffected by nitric oxide. Cephalalgia: An International Journal of Headache. 20 (9), 838-844 (2000).
- Zagami, A. S., Goadsby, P. J., Edvinsson, L. Stimulation of the superior sagittal sinus in the cat causes release of vasoactive peptides. Neuropeptides. 16 (2), 69-75 (1990).
- Goadsby, P. J., Edvinsson, L. The trigeminovascular system and migraine: studies characterizing cerebrovascular and neuropeptide changes seen in humans and cats. Annals of Neurology. 33 (1), 48-56 (1993).
- Bates, E. A., et al. Sumatriptan alleviates nitroglycerin-induced mechanical and thermal allodynia in mice. Cephalalgia: An International Journal of Headache. 30 (2), 170-178 (2010).
- Pradhan, A. A., et al. Characterization of a novel model of chronic migraine. Pain. 155 (2), 269-274 (2014).
- Mogil, J. S., Pang, D. S. J., Silva Dutra, G. G., Chambers, C. T. The development and use of facial grimace scales for pain measurement in animals. Neuroscience and Biobehavioral Reviews. 116, 480-493 (2020).
- Sotocinal, S. G., et al. The rat grimace scale: A partially automated method for quantifying pain in the laboratory rat via facial expressions. Molecular Pain. 7, 55 (2011).
- Langford, D. J., et al. Coding of facial expressions of pain in the laboratory mouse. Nature Methods. 7 (6), 447-449 (2010).
- Mahmoudi, J., et al. Cerebrolysin attenuates hyperalgesia, photophobia, and neuroinflammation in a nitroglycerin-induced migraine model in rats. Brain Research Bulletin. 140, 197-204 (2018).
- Farajdokht, F., Babri, S., Karimi, P., Mohaddes, G. Ghrelin attenuates hyperalgesia and light aversion-induced by nitroglycerin in male rats. Neuroscience Letters. 630, 30-37 (2016).
- Kuburas, A., et al. PACAP Induces Light Aversion in Mice by an Inheritable Mechanism Independent of CGRP. Journal of Neuroscience. 41 (21), 4697-4715 (2021).
- Buschmann, T., et al. Expression of Jun, Fos, and ATF-2 proteins in axotomized explanted and cultured adult rat dorsal root ganglia. Neuroscience. 84 (1), 163-176 (1998).
- Lee, Y. J., Zachrisson, O., Tonge, D. A., McNaughton, P. A. Upregulation of bradykinin B2 receptor expression by neurotrophic factors and nerve injury in mouse sensory neurons. Molecular and Cellular Neuroscience. 19 (2), 186-200 (2002).
- Hari, A., Djohar, B., Skutella, T., Montazeri, S. Neurotrophins and extracellular matrix molecules modulate sensory axon outgrowth. International Journal of Developmental Neuroscience. 22 (2), 113-117 (2004).
- Skoff, A. M., Resta, C., Swamydas, M., Adler, J. E. Nerve Growth Factor (NGF) and Glial Cell Line-Derived Neurotrophic Factor (GDNF) regulate substance P release in adult spinal sensory neurons. Neurochemical Research. 28 (6), 847-854 (2003).
- Lindsay, R. M., Harmar, A. J. Nerve growth factor regulates expression of neuropeptide genes in adult sensory neurons. Nature. 337 (6205), 362-364 (1989).
- Edvinsson, J. C. A., et al. Differences in pituitary adenylate cyclase-activating peptide and calcitonin gene-related peptide release in the trigeminovascular system. Cephalalgia: An International Journal of Headache. 40 (12), 1296-1309 (2020).
재인쇄 및 허가
JoVE'article의 텍스트 или 그림을 다시 사용하시려면 허가 살펴보기
허가 살펴보기더 많은 기사 탐색
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. 판권 소유