고성능 액체 크로마토그래피 (HPLC)
Overview
출처: 폴 바우어 박사 - 퍼듀 대학교
고성능 액체 크로마토그래피(HPLC)는 액체 샘플의 성분을 분리하고 정량화하는 데 일반적으로 사용되는 중요한 분석 방법입니다. 이 기술에서 솔루션(제1 상)은 표면에 결합된 두 번째 위상을 가진 작은 다공성 입자의 포장을 포함하는 열을 통해 펌핑된다. 두 단계에서 샘플 구성 요소의 용해도가 다르면 구성 요소가 서로 다른 평균 속도로 컬럼을 통과하여 이러한 구성 요소를 분리합니다. 펌핑된 솔루션을 이동단계라고 하며 컬럼의 위상을 고정 위상이라고 합니다.
액체 크로마토그래피의 여러 모드가 있습니다, 고정 및 / 또는 모바일 단계의 종류에 따라 고용. 이 실험은 고정 단계가 극적이지 않으며 이동 상이 극성인 반전 위상 크로마토그래피를 사용합니다. 사용되는 고정 단계는 C18 탄화수소 그룹이 3μm 실리카 입자에 접합되는 반면, 이동상은 극성 유기 수정자(acetonitrile)가 첨가된 수성 완충제로 용출 강도를 변화시킵니다. 이 양식에서 실리카는 수용성 샘플에 사용할 수 있어 광범위한 응용 을 제공합니다. 이 실험에서, 다이어트 청량 음료에서 자주 발견 되는 세 가지 구성 요소의 혼합물 (즉 카페인, 벤조아테, 그리고 아스파타메) 분리. 3종의 알려진 양을 포함하는 7개의 준비된 해결책이 이용되고, 그들의 크로마토그램은 그 때 기록됩니다.
Principles
HPLC 실험 중에 고압 펌프는 인젝터를 통해 저수지에서 이동 단계를 수행합니다. 그런 다음 부품 분리를 위해 역상 C18로 포장된 열을 통과합니다. 마지막으로, 이동상은 흡수도가 220nm에서 측정되고 폐병으로 끝나는 검출기 세포로 이동합니다. 구성 요소가 인젝터 포트에서 검출기로 이동하는 데 걸리는 시간을 보존 시간이라고 합니다.
이 실험에서는 역상 컬럼에서 분리가 수행되는 액체 크로마토그래프가 사용됩니다. 컬럼 치수는 3mm(즉, 100mm) x 100mm이며 실리카 패킹(3-μm 입자 크기)은 C18 옥타데실린실레인(ODS)으로 기능성된다. Rheodyne 6 포트 회전 사출 밸브는 처음에 작은 루프에 샘플을 저장하는 데 사용되며 밸브의 회전 시 이동 단계에 샘플을 소개합니다.
검출은 220 nm의 파장에서 흡수 분광법에 의한 것입니다. 이 실험은 검출기가 가변적이지 않은 경우 254nm에서 실행할 수 있습니다. 검출기의 데이터에는 디지털 멀티미터(DMM)를 사용하여 측정되고 데이터 수집 프로그램이 로드된 컴퓨터에서 읽는 아날로그 전압 출력이 있습니다. 생성된 크로마토그램은 샘플의 모든 구성 요소에 대한 피크를 가지고 있습니다. 이 실험을 위해, 세 가지 구성 요소는 모두 5 분 이내에 elute.
이 실험은 동위 동위 제일 상이라고 하는 단일 이동 단계 및 펌프를 사용합니다. 분리하기 어려운 샘플의 경우 그라데이션 모바일 단계를 사용할 수 있습니다. 이는 초기 이동 단계가 주로 수성 단계이며 시간이 지남에 따라 두 번째 유기 적인 모바일 단계가 점차 전체 모바일 단계에 추가되는 경우입니다. 이 방법은 시간이 지남에 따라이 단계의 극성을 제기하여 구성 요소의 보존 시간을 낮추고 가스 크로마토그래프의 온도 그라데이션과 유사하게 작동합니다. 컬럼이 가열되는 경우도 있습니다(일반적으로 40°C)는 주변 온도 변화와 관련된 보존 시간 오류를 없애는 경우가 있습니다.
역상 HPLC에서 컬럼 고정 위상 패킹은 일반적으로 C4, C8 또는 C18 패킹입니다. C4 컬럼은 주로 큰 분자량을 가진 단백질을 위한 반면, C18 컬럼은 펩타이드와 저분자량을 가진 기본 샘플을 위한 것입니다.
흡수 분광법에 의한 검출은 성분의 흡수 스펙트럼이 모두 쉽게 사용할 수 있기 때문에 압도적으로 선택의 검출 방법입니다. 일부 시스템은 전도도 또는 암페어와 같은 전기 화학 적 측정을 검출 방법으로 사용합니다.
이 실험을 위해, 이동상은 주로 20% 아세토닐릴과 80% 정제된 디온화(DI) 물이다. 소량의 아세트산이 첨가되어 이동상pH를 낮추어 고정된 패킹 단계에서 실라놀을 유지하여 비소화 상태로 유지합니다. 이렇게 하면 흡착 피크가 테일링에서 감소하여 더 좁은 피크를 제공합니다. 이어서, pH는 40% 수산화나트륨으로 조정되어 pH를 높이고 성분의 보유 시간을 줄이는 데 도움을 줍니다.
각 그룹은 표준 용액의 상이한 농도를 포함하는 7 개의 바이알 세트를 사용합니다(표 1). 처음 3은 각 피크를 식별하는 데 사용되며 마지막 4는 각 구성 요소에 대한 교정 차트를 만드는 것입니다. 표준 1-3은 교정 차트에도 사용됩니다.
| 수 | 카페인 (mL) | 벤조아테 (mL) | 아스파타메 (mL) |
| 1 | 4 | 0 | 0 |
| 2 | 0 | 4 | 0 |
| 3 | 0 | 0 | 4 |
| 4 | 1 | 1 | 1 |
| 5 | 2 | 2 | 2 |
| 6 | 3 | 3 | 3 |
| 7 | 5 | 5 | 5 |
표 1. 7개의 제공된 작업 표준을 준비하는 데 사용되는 재고 표준의 볼륨(각 표준의 총 부피는 50mL).
Procedure
1. 모바일 단계 만들기
- 약 1.5L의 정제 된 DI 물에 400 mL의 아세토나이트를 추가하여 이동 단계를 준비하십시오.
- 이 용액에 2.4mL의 빙하 아세트산을 조심스럽게 추가하십시오.
- 정제된 DI 물로 볼륨 플라스크에서 총 2.0 L의 부피로 용액을 희석합니다. 결과 솔루션은 2.8에서 3.2 사이의 pH가 있어야 합니다.
- 보정된 디지털 pH 미터를 사용하여 수산화 나트륨40%를 추가하여 pH를 4.2로 조정합니다. pH가 4.0에 도달하면 매우 느리게 추가합니다. 이것은 달성하기 위해 약 50 방울이 소요됩니다.
- 0.47-μm 나일론 66 멤브레인 필터를 통해 이동 단계를 필터링하여 용액을 탈착하고 크로마토그래피 컬럼을 연결할 수 있는 고체를 제거합니다. 기둥 입구의 고정 된 단계에서 공백을 유발하거나 검출기 세포로 작동하여 UV 흡광도로 불안정을 일으킬 수있는 거품을 피하기 위해 이동 단계를 탈염하는 것이 중요합니다.
2. 구성 요소 솔루션 만들기
만들어야 할 세 가지 구성 요소는 카페인 (0.8 mg / mL), 칼륨 벤조아테 (1.4 mg / mL), 아스파타메 (L-aspartyl-L-페닐라닌 메틸 에스테르) (6.0 mg/mL). 이러한 농도는 한때 같은 방식으로 희석되면 소다 샘플에서 발견되는 수준에서 표준을 넣습니다.
- 500mL 체피 플라스크에 0.40 g의 카페인을 넣은 다음 DI 물로 500mL 마크에 희석합니다.
- 벤조아테 0.70g을 500mL 체피플라스크에 넣은 다음 DI 물로 500mL 마크에 희석합니다.
- 100mL 체피 플라스크에 아스파타메 0.60 g을 추가한 다음 DI 물로 100mL 마크에 희석합니다. 보관 시 분해를 방지하기 위해 이 솔루션을 냉장고에 놓습니다.
3. 7가지 표준 솔루션 만들기
세 가지 구성 요소는 모두 서로 다른 분포 계수를 가지며, 이는 각 단계가 모두 상호 작용하는 방식에 영향을 미칩니다. 분포 계수가 클수록 부품이 고정 단계에서 더 많은 시간을 소비하여 검출기에 도달하는 데 시간이 길어집니다.
- 표 1의차트에 따라 각 구성 요소의 적절한 양을 50mL 체적 플라스크로 파이프합니다.
- 각 스톡 솔루션을 볼륨 플라스크의 50mL 마크에 모바일 단계로 희석합니다.
- 각 표준 솔루션을 샘플 랙에 라벨이 부착된 작은 바이알에 붓습니다.
- 50mL 체적 플라스크에 남은 솔루션과 함께 샘플 랙을 냉장고에 보관합니다.
4. HPLC 시스템의 초기 설정 확인
- 폐기물 라인이 폐기물 용기에 있고 이동 단계로 다시 재활용되지 않는지 확인합니다.
- 이동 단계의 유량이 0.5mL/min으로 설정되어 있는지 확인합니다. 이것은 모든 피크가 5 분 이내에 elute에 충분히 높고 좋은 해상도를 허용 할 수있을만큼 느립니다.
- 최소 및 최대 압력 및 유량이 용매 전달 시스템(펌프)의 전면 패널의 올바른 값으로 설정되어 있는지 확인합니다.
- 최소 압력 설정: 250 psi (누출이 발생하는 경우 펌프를 차단하는 것입니다).
- 최대 압력 설정: 4,000 psi(나막신이 형성되는 경우 펌프가 파손되지 않도록 보호하는 것입니다).
- 공백을 설정하려면 검출기의 전면 패널에서 "0"을 눌러 (공백은 순수한 이동 단계입니다).
- 100μL 주사기를 탈온화된 물로 헹구고, 분석해야 할 작업 표준 중 하나의 여러 부피를 분석하고 주사기를 해당 솔루션으로 채웁니다. 관심 있는 각 구성 요소의 피크를 식별할 수 있는 3개의 단일 구성 요소 샘플로 시작합니다.
5. 샘플 및 데이터 수집을 수동으로 삽입
- 인젝터 핸들을 하중 위치에 배치하면 중격 포트를 통해 100 μL의 용액을 천천히 주입하십시오.
- 데이터 수집 프로그램이 300s에 대한 데이터를 수집하도록 설정되어 있는지 확인하여 3개의 피크가 모두 검출기를 통해 엘로테할 수 있는 충분한 시간을 할애할 수 있습니다.
- 평가판을 시작할 준비가 되면 인젝터 핸들을 삽입 위치로 회전(샘플을 모바일 단계에 삽입) 즉시 컴퓨터 데이터 수집 프로그램에서 "평가판 시작"을 클릭합니다. 표준 1-3의 경우 실행 중에 3개의 순차 피크 중 하나만 화면에나타납니다(그림 1).
- 300이 지나면 데이터 수집은 데이터 파일을 저장하는 프롬프트를 보냅니다. 적절한 파일이름(예:STD#1)으로 데이터를 저장합니다.
- 각 평가판의 피크에 대한 몇 초 의 시간을 기록하며, 이 시간은 해당 구성 요소를 식별하는 데 사용됩니다.
- 중격에서 주사기를 제거하고 첫 번째 실행에서 결정된 크로마토그램 당 동일한 시간을 사용하여 나머지 각 작업 표준에 대한 프로세스를 반복합니다.
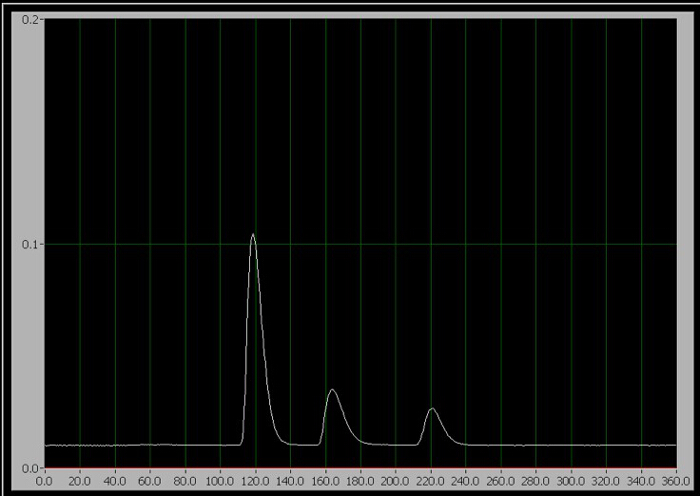
그림 1. 3 성분의 크로마토그램. 왼쪽에서 오른쪽으로, 그들은 카페인, 아스파타메, 벤조아테입니다.
6. 다이어트 탄산음료 샘플
다이어트 콜라, 다이어트 펩시, 콜라 제로는 "미지수"입니다. 그들은 거품이 HPLC 시스템에 좋지 않기 때문에 탄산을 제거하기 위해 하룻밤 동안 열린 용기에 빠져 나왔습니다. 이것은 충분히 샘플의 가스를 제거합니다.
- 다이어트 소다의 약 2mL를 플라스틱 주사기에 넣습니다.
- 필터 팁을 Luer-Lok를 통해 주사기에 부착하여 제자리에 비틀어 놓습니다.
- 주사기의 액체를 필터를 통해 작은 유리 바이알로 밀어 넣습니다. 이렇게 하면 분리 열을 막을 수 있는 원치 않는 미립자를 제거합니다.
- 각 시료를 동일한 양의 DI 물로 희석하여 순도가 50%에 달합니다.
- 샘플의 100 μL을 샘플 루프에 주입하고 표준과 동일한 매개 변수로 시험을 실행합니다.
7. 계산
- 성분 용액의 농도에서 7개의 시료에 대해 만들어진 희석을 기반으로 표준의 모든 성분의 농도를 계산합니다.
- 각 표준에 대한 크로마토그램의 피크 영역과 1/2 높이에서 폭의 피크 높이 시간과 동일한 삼각형 방법에 의해 알려지지 않은 시료를 결정합니다(그림2). 각 구성 요소가 각각의 피크를 표시하는 데 걸리는 시간을 기준으로 각 구성 요소에 해당하는 피크를 결정한 후 이러한 피크 영역을 컴퓨터 스프레드시트에 입력합니다.
- 세 가지 구성 요소에 대한 표준에서 피크 영역 대 농도(mg/L)의 교정 곡선을 만듭니다.
- 각 교정 곡선에 맞는 최소 사각형을 결정합니다.
- 샘플에 대한 HPLC 시험에서 표시된 피크 영역에서 다이어트 소다의 각 성분의 농도를 계산합니다. 다이어트 소다는 HPLC 시스템에 주입하기 전에 2의 요인에 의해 희석되었다는 것을 기억하십시오.
- 다이어트 소다의 각 성분의 mg/L양을 계산합니다.
- 결과에 따라 12 온스의 소다 캔에 있는 각 성분의 밀리그램을 계산합니다. 12 온스 = 354.9 mL을 가정합니다.
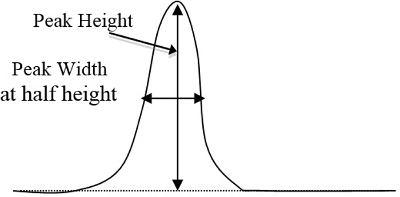
그림 2. 곱해야 하는 곡선의 피크 높이와 너비의 기본 예입니다(높이 시간 폭은 1/2 높이).
Results
HPLC 크로마토그램은 표준의 교정곡선(그림 3)에기초하여 모든 샘플에 대해 각각 3개의 성분을 정량화할 수 있다.
이 실험 세트에서, 이러한 다이어트 소다의 12 온스 캔각각 성분의 다음 금액을 포함 결정 했다:
다이어트 콜라: 50.5 mg 카페인; 217.6 mg 아스파타메; 83.6 mg 벤조아테.
콜라 제로: 43.1 mg 카페인; 124.9 mg 아스파타메; 85.3 mg 벤조아테.
다이어트 펩시: 34.1 mg 카페인; 184.7 mg 아스파타메; 79.5 mg 벤조아테.
당연히, 모든 3 벤조아테의 대략 동일한 금액을 했다, 그것은 단지 방부제. 콜라 제품은 카페인이 조금 더 많았고, 콜라 제로는 다른 두 탄산음료보다 아스파탐이 훨씬 적었으며, 일부 향료에 구연산을 함유하고 있습니다.
다음 숫자는 3 다이어트 소다의 12 온스 캔에 카페인과 아스파타메의 실제 금액 (카페인 함량은 코카콜라와 펩시 웹 사이트에서 얻은. 아스파탐 콘텐츠는 LiveStrong.com 및 DiabetesSelfManagement.com 모두에서 얻었습니다.):
다이어트 콜라: 46 mg 카페인; 187.5 mg 아스파타메
콜라 제로: 34 mg 카페인; 87.0 mg 아스파타메
다이어트 펩시: 35 mg 카페인; 177.0 mg 아스파타메
샘플 계산(표 2):
STD#1의 카페인 농도: 카페인성분용 용액은 0.400g의 카페인을 500mL = 0.500 l → 0.800 g/L = 0.800 mg/mL로 희석했습니다.
STD#1은 이 솔루션의 1mL을 50.0 mL로 희석시켰습니다.
0.800 mg/mL * (1.0 mL / 50.0 mL) = 0.016 mg /mL = 16.0 mg / L.
STD#2는 이 솔루션의 2mL를 50.0 mL로 희석시켰습니다.
0.800 mg/mL * (2.0 mL / 50.0 mL) = 0.032 mg /mL = 32.0 mg / L.
세 가지 교정그래프(그림 4)의결과는 다음 방정식을 산출했습니다.
카페인 피크 지역 = 0.1583*[카페인 mg/L] - 0.574
아스파타메 피크 지역 = 0.02696*[아스파타메 mg/L] - 0.405
벤조아테 피크 지역 = 0.1363*[벤조아테 mg/L] - 1.192
다이어트 콜라: 카페인 피크 지역 = 10.68 = 0.1583*[카페인 mg/L] - 0.574
[카페인 mg/L] = (10.68 + 0.574)/ (0.1583) = 주입된 샘플에서 71.1 mg/L.
샘플은 2의 요인에 의해 희석되었기 때문에, 다이어트 콜라는 141.2 mg / L 카페인을 했다.
12 온스 당 금액 = (141.2 mg/L)(0.3549 mL/12-온스 캔) = 50.5 mg 카페인/캔.
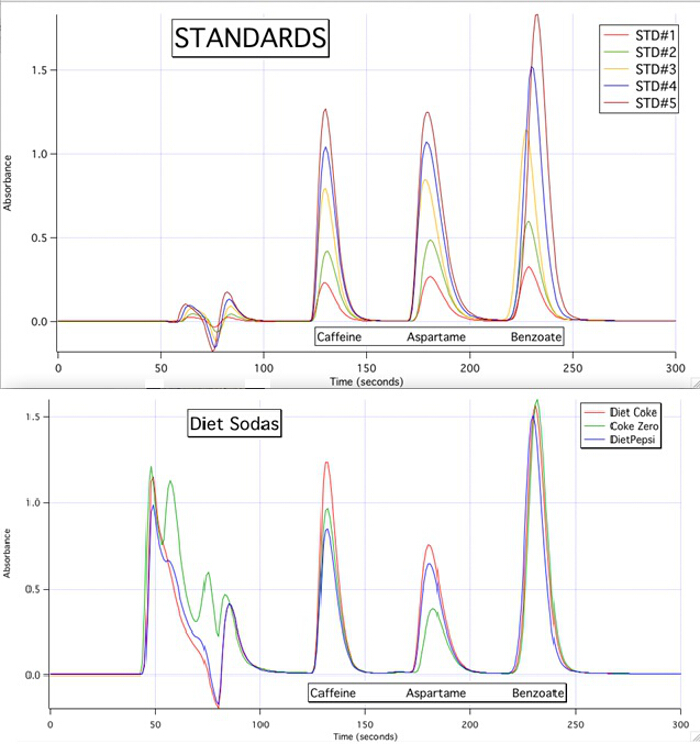
그림 3. 5 가지 표준및 3 개의 샘플의 HPLC 크로마토그램.
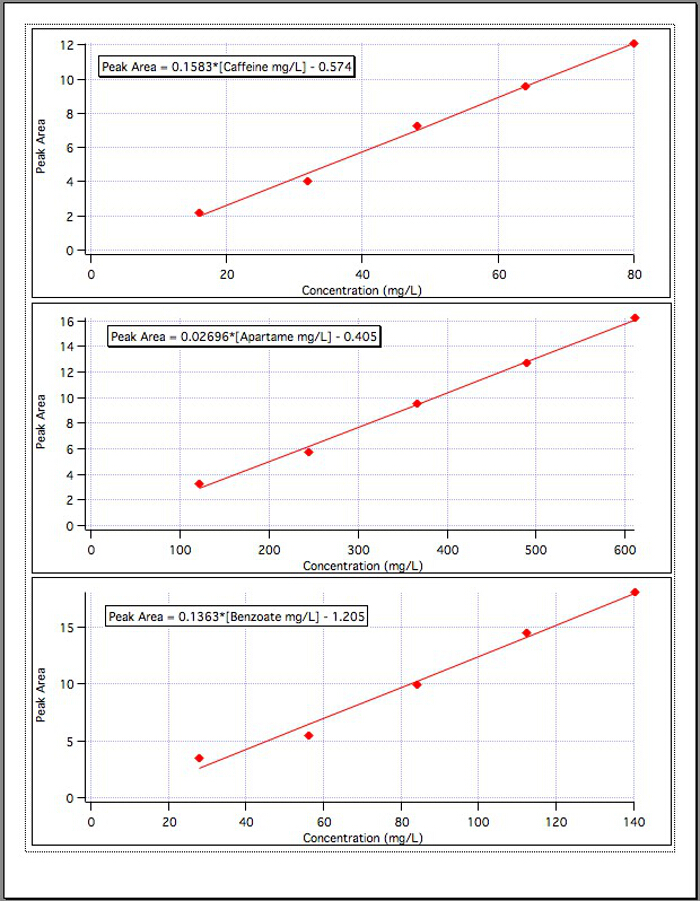
그림 4. 3개의 구성 요소 각각에 대한 보정 곡선입니다.
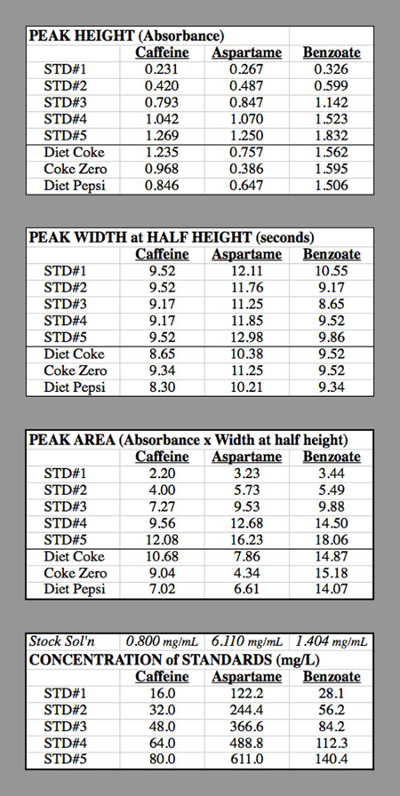
표 2. 교정 곡선을 생성하는 데 사용되는 HPLC 평가판의 데이터 테이블입니다.
Application and Summary
HPLC는 많은 응용 분야에 대한 분리 및 검출에 널리 사용되는 기술입니다. 가스 크로마토그래피(GC)는 시료가 가스 상에 있어야 하기 때문에 비휘발성 화합물에 이상적입니다. 비 휘발성 화합물은 설탕을 포함, 비타민, 약물, 그리고 대사 산물. 또한, 그것은 비 파괴적이다, 이는 각 구성 요소를 수집 할 수 있도록 추가 분석을 위해 (질량 분광법 등). 모바일 단계는 실질적으로 무제한이며, pH의 극성을 변경하여 더 나은 해상도를 달성할 수 있습니다. 그라데이션 모바일 단계를 사용하면 실제 시험 중에 이러한 변경 이 사항이 가능합니다.
인공 감미료 아스파타메와 관련 될 수 있는 가능한 건강 문제에 대 한 우려가 있다. 현재 제품 라벨링은 식이 음료 내부에 이러한 구성 요소의 양을 표시하지 않습니다. 이 방법은 카페인과 벤조아테와 함께 이러한 양을 정량화 할 수 있습니다.
다른 응용 프로그램은 물에 살충제의 양을 결정하는 포함; 진통제 정제에서 아세트아미노펜 또는 이부프로펜의 양을 결정; 선수의 혈 류에 존재 하는 성능 향상 약물 인지 여부를 결정; 또는 단순히 범죄 실험실에서 약물의 존재를 결정. 이러한 샘플의 농도와 종종 구성 요소의 ID를 쉽게 확인할 수 있지만, 한 가지 제한사항은 여러 샘플이 동일한 보존 시간에 가깝게 유지되어 동례를 할 수 있다는 것입니다.
Tags
건너뛰기...
이 컬렉션의 비디오:

Now Playing
고성능 액체 크로마토그래피 (HPLC)
Analytical Chemistry
385.6K Views

분석 특성화를 위한 샘플 준비
Analytical Chemistry
85.1K Views

내부 표준
Analytical Chemistry
205.2K Views

표준 추가 방법
Analytical Chemistry
320.5K Views

교정 곡선
Analytical Chemistry
798.3K Views

자외선 눈에 보이는 (UV-Vis) 분광법
Analytical Chemistry
624.8K Views

화학 분석을 위한 라만 분광법
Analytical Chemistry
51.4K Views

엑스레이 형광 (XRF)
Analytical Chemistry
25.9K Views

화염 이온화 감지를 갖춘 가스 크로마토그래피(GC)
Analytical Chemistry
282.9K Views

이온 교환 크로마토그래피
Analytical Chemistry
264.9K Views

모세관 전기 포레시스 (CE)
Analytical Chemistry
94.3K Views

질량 분광법 소개
Analytical Chemistry
112.8K Views

스캐닝 전자 현미경 검사법 (SEM)
Analytical Chemistry
87.6K Views

전위요스타트/갈바노스타트를 사용하여 지원되는 촉매의 전기화학적 측정
Analytical Chemistry
51.7K Views

순환 볼탐량 (CV)
Analytical Chemistry
125.8K Views
Copyright © 2025 MyJoVE Corporation. 판권 소유