É necessária uma assinatura da JoVE para visualizar este conteúdo. Faça login ou comece sua avaliação gratuita.
Method Article
Produção de nanopartículas metálicas por ablação a laser pulsada em líquidos: uma ferramenta para estudar as propriedades antibacterianas das nanopartículas
Neste Artigo
Resumo
As propriedades antimicrobianas de metais como cobre e prata foram reconhecidas há séculos. Este protocolo descreve a ablação por laser pulsada em líquidos, um método de síntese de nanopartículas metálicas que proporciona a capacidade de afinar as propriedades dessas nanopartículas para otimizar seus efeitos antimicrobianos.
Resumo
O surgimento de bactérias resistentes a múltiplos fármacos é uma preocupação clínica global levando alguns a especular sobre o nosso retorno a uma era de medicamentos "pré-antibióticos". Além dos esforços para identificar novos fármacos antimicrobianos de pequena molécula, tem havido grande interesse no uso de nanopartículas metálicas como revestimentos para dispositivos médicos, curativos para feridas e embalagens de consumo, devido às suas propriedades antimicrobianas. A grande variedade de métodos disponíveis para a síntese de nanopartículas resulta em um amplo espectro de propriedades químicas e físicas que podem afetar a eficácia antibacteriana. Este manuscrito descreve o método de ablação a laser pulsada em líquidos (PLAL) para criar nanopartículas. Esta abordagem permite o ajuste fino do tamanho, composição e estabilidade das nanopartículas usando métodos de pós-irradiação, bem como a adição de surfactantes ou exclusores de volume. Ao controlar o tamanho e a composição das partículas, uma grande variedade de propriedades físicas e químicas da nanopa de metalPodem ser exploradas as partículas que podem contribuir para a sua eficácia antimicrobiana, abrindo assim novas vias para o desenvolvimento antibacteriano.
Introdução
As nanopartículas (NPs) são geralmente definidas como partículas que têm pelo menos uma dimensão com menos de 100 nm de comprimento. Os métodos tradicionais de síntese NP química geralmente requerem agentes redutores perigosos, como boroidridos e hidrazinas. Em contraste, a ablação a laser de alvos de metal sólido imersos em um meio líquido (ablação a laser pulsada em líquidos - PLAL) fornece uma rota ecológica para a síntese NP que satisfaz todos os 12 dos Princípios da Química Verde 1 , 2 . Em PLAL, um alvo de metal submerso é irradiado por pulsos de laser repetidos. À medida que o laser abla o alvo, uma pluma densa de aglomerados atômicos e vapor é liberada no meio líquido em que os NPs se juntam rapidamente. Os NP produzidos por PLAL são finamente dispersos em um meio aquoso e o tamanho, polidispersão e composição dos NPs podem ser facilmente controlados pela variação do líquido aquoso de ablação, bem como do laser parAmostras 1 , 2 , 3 , 4 , 5 , 6 .
As características das nanopartículas podem ser ajustadas ajustando uma série de parâmetros do laser, incluindo: fluência, comprimento de onda e duração do pulso (revisado na referência 7 ). A fluência do laser é calculada como a energia do pulso dividida pela área do ponto do laser na superfície do alvo. Os efeitos precisos da fluência sobre o tamanho e a polidispersão das NPs são algo controversos. Em geral, verificou-se que, para os sistemas de laser pulsado "longos" e "ultra-curtos", existem regimes de fluência baixos e altos que produzem tendências negativas e positivas de tamanho, respectivamente 8 , 9 , 10 , 11 . NP tamanho distributivoOs ons podem ser medidos empiricamente usando técnicas como dispersão de luz dinâmica e microscopia eletrônica de transmissão (TEM), conforme descrito abaixo.
A escolha do comprimento de onda do laser pode afetar os mecanismos físicos pelos quais os NPs são formados. Em comprimentos de onda mais curtos (ultravioleta), os fótons de alta energia são capazes de quebrar as ligações interatômicas 12 . Este mecanismo de foto-ablação é um exemplo de uma síntese de NP de cima para baixo, porque resulta na liberação de fragmentos de material ultra-pequenos que tendem a produzir maiores amostras de polidispersão ao saciar no líquido de submersão 12 , 13 , 14 . Em contraste, a ablação do infravermelho próximo (λ = 1,064 nm) produz um mecanismo de síntese ascendente dominado pela ablação plasmática 12 . A absorção do laser pelo alvo libera elétrons que colidem com e, em seguida, livres, elétrons encadernados. Como cOllisions aumenta, o material é ionizado, inflamando assim um plasma. O líquido circundante limita o plasma, aumenta a sua estabilidade e aumenta ainda mais a absorção 12 . À medida que o plasma em expansão é extinto pelo líquido de confinamento, os NPs são condensados com várias geometrias 4 , 12 , 15 .
A escolha da duração do pulso do laser pode afetar ainda mais o processo de formação de NP. Os lasers de pulsação longa comumente usados, com durações de pulso superiores a alguns picosegundos, incluem todos os milímetros, micro, nano e alguns aeroses pulsados com picosegundo. Neste regime de largura do pulso, a duração do pulso do laser é maior do que o tempo de equilíbrio elétron-fonão, que é normalmente na ordem de alguns picosegundos 4 , 16 , 17 , 18 , 19. Isso resulta em vazamento de energia no meio de ablação circundante e na formação de NPs por mecanismos térmicos, como emissão termiônica, vaporização, ferver e derreter 1 , 20 .
A atividade antibacteriana dos NPs é fortemente influenciada pelo tamanho de partícula 21 , 22 , 23 , 24 . A fim de aumentar a redução de tamanho e a monodispersão, os NPs podem ser irradiados uma segunda vez usando um laser de um comprimento de onda perto da ressonância plasmática de superfície (SPR) do NP. A radiação laser incidente é absorvida pelo NP através da excitação do SPR. A fragmentação do NP pode ocorrer através da evaporação térmica 25 , 26 ou da explosão de Coulomb 27 , 28 . A fotoexcitação aumenta tA temperatura do NP acima do ponto de fusão, resultando no derramamento da camada externa da partícula. Verificou-se que a adição de agentes tais como polivinilpirrolidona (PVP) ou dodecilsulfato de sódio (SDS) à solução pode melhorar grandemente os efeitos pós-irradiação 5 . O impacto da adição de vários solutos foi descrito em vários relatórios 1 , 4 , 6 . A facilidade de manipulação de características de NP por PLAL oferece um novo método para desenvolver novos antimicrobianos baseados em NP.
Protocolo
1. Focando o laser de nanosegundo e fluência de medição
- Montar o aparelho de ablação colocando uma barra de agitação magnética e um estágio de ablação porosa dentro de um copo de vidro de 50 mL.
NOTA: O estágio de ablação consiste em uma plataforma de aço inoxidável de 3,81 cm de diâmetro e 1,6 mm de espessura com dez orifícios de 0,65 cm de diâmetro e seis orifícios de 0,50 cm de diâmetro perfurados no padrão ilustrado na Figura 1 . O objetivo desses buracos é permitir que o líquido se mova através do alvo para que as partículas não se acumulem imediatamente acima do alvo. A mistura insuficiente leva a interações deletérias entre o laser e as partículas já formadas. Além disso, três furos roscados # 29 (8-32) estão localizados perto do perímetro da plataforma para aceitar os parafusos que servem como pernas para elevar a plataforma e fornecer espaço para uma barra de agitação magnética ( Figura 1A ).- Coloque o copo em um magnéticoAgite a placa e coloque a placa de agitação sobre uma fase de conversão xy para permitir o movimento do alvo durante a ablação ( Figura 1A ).
- Defina o laser Nd: YAG para operar no comprimento de onda fundamental de 1.064 nm, com uma duração de impulso de 5 ns e uma taxa de repetição de pulso de 10 Hz. Meça a energia por pulso com um medidor de energia e energia de laser. A energia necessária é 240-250 mJ.
- Focalize o feixe abaixo do alvo no estágio de ablação usando uma lente convergente de comprimento focal de 250 mm (NA = 0,05).
NOTA: O feixe de entrada possui um raio de 4.025 mm e é necessária uma altura da lente de 161 mm para atingir o tamanho do ponto desejado. O tamanho ideal do ponto é determinado empiricamente. Um tamanho de ponto maior é utilizado para reduzir o efeito da proteção por NPs presentes na solução. Isso é equilibrado com o fato de que aumentar o tamanho do ponto requer maior energia para manter fluência adequada. - Determine o tamanho do ponto, colocando um alvo de metal (veja a seçãoN 2) no palco e ablação com vários pulsos de laser. Veja o alvo ablado juntamente com um slide micrométrico em um microscópio de luz equipado com câmera CCD (objetivo 4X) para medir o tamanho do ponto ( Figura 1A ).
NOTA: Para o aparelho aqui, o sistema de ablação produz um tamanho de ponto com uma área média de 5,51 mm 2 . O tamanho do ponto permanece nesta faixa para cada ablação. - Calcule a fluência dividindo a energia do pulso pela área do ponto. Para o aparelho aqui, a fluência é de 4,80 J / cm 2 .
2. Síntese de Nanopartículas de Prata por Ablação com Laser Pulsado em Líquido
- Pesar um alvo de prata plano usando uma microbalança para obter a massa de pré-ablação.
- Aderir ao alvo prateado para o estágio poroso usando fita adesiva de carbono de dupla face. Adicione 40 mL de líquido de ablação ao copo ( Figura 1A ). A altura do líquido acima do alvo é de 11 mm.
NOTA: ablação típica liqUids são soluções aquosas contendo SDS 60 mM ou PVP 2 mM para aumentar a monodispersão. - Sob constante agitação, mova o estágio xy motorizado controlado por computador em um padrão elíptico (dimensões: eixo principal = 2,09 cm, eixo menor = 0,956 cm, área = 1,57 cm 2 ) a uma velocidade de 0,42 cm / s e ablate o alvo Por 20-40 min.
NOTA: A concentração de NPs aumenta com tempos de ablação mais longos. Certifique-se de que a agitação seja suficientemente vigorosa para manter a concentração NP uniforme ao longo da solução para minimizar os efeitos de proteção 7 .
3. Caracterizando Nanopartículas de Metal
- Recolher a solução de nanopartículas do copo por decantação. Confirme a presença de nanopartículas medindo seus espectros de luz visíveis UV (200-1,100 nm).
NOTA: Os NPs têm uma absorção de pico no comprimento de onda de ressonância de plasmon de superfície (SPR). Para prata, o SPR é centrado a 400 nm. NP altamente concentradoAs soluções requerem diluição antes da medição do espectro UV-VIS para garantir que as leituras de absorvância permaneçam dentro da faixa linear do espectrofotômetro. - Medir o diâmetro hidrodinâmico dos NP por dispersão de luz dinâmica (DLS) utilizando um método de análise de distribuição de números 29 .
- Diluir a solução NP 1:40 na solução de ablação e pipetar 1 mL em uma cubeta de plástico de 1 cm. Utilizando um ângulo de medição de 180 ° , mede a dispersão da luz a um comprimento de onda de 633 nm para determinar o diâmetro NP de acordo com a equação de Stokes-Einstein:
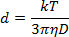
Onde d é o raio hidrodinâmico, k é constante de Boltzmann, T é temperatura absoluta, η é viscosidade e coeficiente de difusão D ou velocidade do movimento browniano.
- Diluir a solução NP 1:40 na solução de ablação e pipetar 1 mL em uma cubeta de plástico de 1 cm. Utilizando um ângulo de medição de 180 ° , mede a dispersão da luz a um comprimento de onda de 633 nm para determinar o diâmetro NP de acordo com a equação de Stokes-Einstein:
- Confirmar o tamanho e a forma de NP usando o microfone eletrônico de transmissãoEscopy (TEM) 30 .
NOTA: O diâmetro hidrodinâmico medido usando DLS é maior do que o tamanho medido usando TEM devido à camada de solvente que envolve os NPs.- Diluir a solução NP 1:40 em água duplamente destilada para remover qualquer excesso de aditivos ( por exemplo, SDS ou PVP) que possam interferir com a imagem. Largue 2 μL da solução em uma grade TEM de cobre pré-revestida com película de carbono lacei / fina (comercialmente disponível, veja a Lista de materiais) e seca durante a noite à temperatura ambiente sob vácuo em um dessecador.
- Imagem dos NP para avaliar o tamanho e a forma, conforme descrito na referência 30 .
- Para calcular a concentração de NP, desalojar quaisquer NPs ligeiramente ligados do alvo de metal ablado (etapa 2.3) colocando o alvo em um banho de água sonicante contendo água destilada durante 1 min.
- Secar o alvo sob uma corrente de ar comprimido durante 1 min. Meça a massa da taRget em uma microbalança. Quantifique a massa de NPs em solução como a diferença de peso antes e depois da ablação, o que é assumido como resultado da ejeção de nanopartículas metálicas na solução.
4. Pós-irradiação
- Diluir os NPs para uma concentração máxima de 100 μg / mL na mesma solução de ablação usada em 2.2. Este limite de concentração é fundamental para garantir uma irradiação uniforme.
- Transferir 15-17 mL das NP diluídas para uma cuvete de quartzo contendo uma barra de agitação ( Figura 1B ). Coloque a cuvete em uma placa de agitação magnética alinhada paralelamente com o laser de entrada.
- Use um sistema laser Nd: YAG para produzir pulsos a laser de 25 ps 532 nm e uma lente de comprimento focal de 75 mm para focalizar o laser no centro da solução. Irradiate a solução por 30 minutos a várias horas, dependendo do tamanho desejado.
NOTA: A energia total entregue depende da concentração da solução e tDe irradiação e pode variar de 0,5 mJ a 3,5 mJ. Para o aparelho aqui, 30 min de pós-irradiação de uma amostra transparente e de baixa concentração (<50 μg / mL) produz NPs de prata com um diâmetro de 10 nm.
5. Medindo as Propriedades Antibacterianas das Nanopartículas
NOTA: A toxicidade de NPs de prata contra ambos os Gram- positivos ( Bacillus subtilis ) e Gram- negativos ( Escherichia coli ) foi testada 31 . O método é facilmente adaptado a qualquer espécie; No entanto, a dose eficaz de nanopartículas pode variar consideravelmente e deve ser determinada empiricamente. Aqui, E. coli é usado como o sistema modelo para a descrição do método.
- Cultivar culturas de E. coli (estirpe MG1655) durante a noite a 37 ° C em Luria Broth (LB) contendo 10 g / L de triptona de Bacto, 5 g / L de extracto de levedura e 10 g / L de cloreto de sódio. Diluir as culturas durante a noite para uma densidade óptica (λ = 600Nm) de 0,01 em LB fresco.
- Se os NPs foram sintetizados em meios de ablação contendo aditivos ( por exemplo, SDS ou PVP), adicione o respectivo produto químico ao LB de tal forma que a concentração permaneça constante ao adicionar os NPs.
NOTA: Por exemplo, em uma experiência típica, um alvo de prata é ablado em uma solução de SDS 60 mM para produzir uma solução de NP de 100 ug / mL. Se a concentração final de NPs nos meios de cultura for de 10 μg / mL, prepare LB contendo SDS 6 mM ( ou seja, 1/10 da concentração de SDS no líquido de ablação). Não há efeito negativo sobre o crescimento da bactéria ao usar essas concentrações. Isso é mostrado no controle -AgNP na Figura 3 . - Adicione os NPs às culturas diluídas em concentrações variando entre 0-50 μg / mL e cultivar as culturas com agitação a 37 ° C durante 2 h adicionais. Como um controle positivo para a toxicidade, tratar E. coli com um antibiótico ( por exemplo, 30 μg / mL de kanamYcin).
- Após as 2 h de incubação, diluir em série as amostras de cultura 1:10 em LB fresco e detectar 10 μL de gotas de cada diluição em placas de agar LB. Tipicamente, 10 4 -10 diluições de 8 vezes são suficientes para ver colônias individuais.
- Uma vez que as gotículas foram absorvidas, incubar as placas durante a noite a 37 ° C e contar as unidades formadoras de colônias (cfu) na manhã seguinte.
Resultados
Usando alvos de prata, os parâmetros de laser descritos acima e SDS de 60 mM no líquido de ablação, NPs de prata são gerados com a absorvância UV-VIS característica no SPR ( Figura 2A ). As medições de TEM e DLS revelam um diâmetro NP médio de aproximadamente 25 nm antes da pós-irradiação ( Figura 2B ). Ablação do alvo de prata por 30 min geralmente produz uma concentração de NP de 200 μg / mL. Ao avaliar a to...
Discussão
Os efeitos antimicrobianos reproduzíveis das NPs requerem produção consistente de NP com tamanhos e concentrações semelhantes. Portanto, é fundamental padronizar os parâmetros do laser, incluindo fluência, comprimento de onda e duração do pulso. Embora a dispersão de luz dinâmica seja um método fácil e rápido para estimar o tamanho de NP, a quantificação precisa da distribuição de tamanho requer medição direta por TEM. Como cada raio laser tem características distintas em termos de perfil de modo e...
Divulgações
Os autores não têm nada a revelar.
Agradecimentos
Este trabalho foi apoiado pela National Science Foundation (NSF premia CMMI-0922946 a DB, CMMI-1300920 a DB e S.O'M., E CMMI-1531789 a S.O'M., DB e EAK) e um Busch Biomedical Research Grant para EAK e S.O'M.
Materiais
| Name | Company | Catalog Number | Comments |
| Nanosecond Nd:YAG laser | Ekspla | NL303 | |
| Motorized xy scanning stage | Standa | 8MTF | |
| UV-VIS spectrophotometer | Agilent | Cary 60 | |
| Dynamic light scattering unit | Malvern | Zetasizer ZS 90 | |
| Microbalance | Maktek | TM 400 | |
| Transmission electron microscope | Zeiss | EM 902 | |
| Silver foil target | Alfa Aesar | 12127 | |
| 250 mm focal length lens | Edmund Optics | 69-624 | |
| Copper TEM grids | Pacific Grid-Tech | Cu-400LD | Lacey/thin film coated grid |
| E. coli MG1655 | ATCC | 47076 | |
| Bacto-tryptone | BD Biosciences | 211705 | |
| Yeast extract | BD Biosciences | 212750 | |
| Sodium chloride | Fisher Scientific | BP3581 | |
| Bacto-agar | BD Biosciences | 214010 | |
| Sodium dodecyl sulfate | Fisher Scientific | BP166-100 | |
| Polyvinylpyrrolidone | Fisher Scientific | BP431-100 | |
| Stainless steel disc (for ablation stage) | Metal Remnants, Inc. | N/A | 1.5 inch diameter, 16 gauge |
| Beaker | Fisher Scientific | 02-540G | |
| Magnetic stir bar | Fisher Scientific | 14-513-57 | |
| Magnetic stir plate | Fisher Scientific | 11-100-49SH | |
| Laser energy and power meter | Coherent | 1098579 | |
| Carbon tape | Shinto Chemitron Co. Ltd. | STR Tape | |
| Sonicating water bath | Branson | 1510 | |
| Air compressor | GMC | Syclone 3010 | For drying ablation target |
| 75 mm focal length lens | Edmund Optics | 34-096 | Focusing lens for post-irradiation |
| Quartz cuvette | Precision Cells Inc | 21UV40 | 50 mm light path (for post-irradiation) |
| Kanamycin | Fisher Scientific | BP906-5 | |
| Light microscope | Nikon | 50i | This microscope is used to focus the laser on the ablation stage. This particular model is no longer available, but any light microscope with a 4X objective will work. |
| CCD camera | AmScope | MT5000-CCD | |
| Micrometer slide | Ted Pella | 2280-70 |
Referências
- Amendola, V., Meneghetti, M. What controls the composition and the structure of nanomaterials generated by laser ablation in liquid solution?. Phys Chem Chem Phys. 15 (9), 3027-3046 (2013).
- Anastas, P., Eghbali, N. Green chemistry: principles and practice. Chem Soc Rev. 39 (1), 301-312 (2010).
- Mafune, F., Kohno, J. Y., Takeda, Y., Kondow, T., Sawabe, H. Formation of Gold Nanoparticles by Laser Ablation in Aqueous Solution of Surfactant. J Phys Chem B. 105 (22), 5114-5120 (2001).
- Rao, S. V., Podagatlapalli, G. K., Hamad, S. Ultrafast laser ablation in liquids for nanomaterials and applications. J Nanosci Nanotechnol. 14 (2), 1364-1388 (2014).
- Tsuji, T., et al. Preparation of silver nanoparticles by laser ablation in polyvinylpyrrolidone solutions. Appl Surf Sci. 254 (16), 5224-5230 (2008).
- Zeng, H., et al. Nanomaterials via laser ablation/irradiation in liquid: a review. Adv Funct Mater. 22 (7), 1333-1353 (2012).
- Naddeo, J. J., et al. Antibacterial Properties of Nanoparticles: A Comparative Review of Chemically Synthesized and Laser-Generated Particles. Adv. Sci. Eng. Med. 7 (12), 1044-1057 (2015).
- Elsayed, K. A., Imam, H., Ahmed, M. A., Ramadan, R. Effect of focusing conditions and laser parameters on the fabrication of gold nanoparticles via laser ablation in liquid. Opt. & Laser Tech. 45, 495-502 (2013).
- Kabashin, A. V., Meunier, M. Synthesis of colloidal nanoparticles during femtosecond laser ablation of gold in water. J Appl Phys. 94 (12), 7941-7943 (2003).
- Nichols, W. T., Sasaki, T., Koshizaki, N. Laser ablation of a platinum target in water I. Ablation mechanisms. J Appl Phys. 100 (11), 114911 (2006).
- Povarnitsyn, M. E., Itina, T. E., Levashov, P. R., Khishchenko, K. V. Mechanisms of nanoparticle formation by ultra-short laser ablation of metals in liquid environment. Phys Chem Chem Phys. 15 (9), 3108-3114 (2013).
- Mortazavi, S. Z., Parvin, P., Reyhani, A., Golikand, A. N., Mirershadi, S. Effect of Laser Wavelength at IR (1064 nm) and UV (193 nm) on the Structural Formation of Palladium Nanoparticles in Deionized Water. J Phys Chem C. 115 (12), 5049-5057 (2011).
- Kim, J., Reddy, D. A., Ma, R., Kim, T. K. The influence of laser wavelength and fluence on palladium nanoparticles produced by pulsed laser ablation in deionized water. Solid State Sci. 37, 96-102 (2014).
- Mortazavi, S. Z., Parvin, P., Reyhani, A., Mirershadi, S., Sadighi-Bonabi, R. Generation of various carbon nanostructures in water using IR/UV laser ablation. J Phys D: Appl Phys. 46 (16), 165303 (2013).
- Hunter, B. M., et al. Highly active mixed-metal nanosheet water oxidation catalysts made by pulsed-laser ablation in liquids. J Am Chem Soc. 136 (38), 13118-13121 (2014).
- Momma, C., et al. Short-pulse laser ablation of solid targets. Opt Commun. 129 (1), 134-142 (1996).
- Sonntag, S., Roth, J., Gaehler, F., Trebin, H. R. Femtosecond laser ablation of aluminium. Appl Surf Sci. 255 (24), 9742-9744 (2009).
- Yamashita, Y., Yokomine, T., Ebara, S., Shimizu, A. Heat transport analysis for femtosecond laser ablation with molecular dynamics-two temperature model method. Fusion Eng Des. 81 (8), 1695-1700 (2006).
- Zhigilei, L. V., Lin, Z., Ivanov, D. S. Atomistic modeling of short pulse laser ablation of metals: connections between melting, spallation, and phase explosion. J Phys Chem C. 113 (27), 11892-11906 (2009).
- Schmidt, M., et al. Lasers in Manufacturing 2011 - Proceedings of the Sixth International WLT Conference on Lasers in Manufacturing Metal Ablation with Short and Ultrashort Laser Pulses. Physics Procedia. 12, 230-238 (2011).
- Azam, A., Ahmed, A. S., Oves, M., Khan, M. S., Memic, A. Size-dependent antimicrobial properties of CuO nanoparticles against Gram-positive and-negative bacterial strains. Int. J. Nanomed. 7, 3527-3535 (2012).
- Ivask, A., et al. Size-dependent toxicity of silver nanoparticles to bacteria, yeast, algae, crustaceans and mammalian cells in vitro. PLoS One. 9 (7), e102108 (2014).
- Kim, T. H., et al. Size-dependent cellular toxicity of silver nanoparticles. J Biomed Mater Res A. 100 (4), 1033-1043 (2012).
- Raghupathi, K. R., Koodali, R. T., Manna, A. C. Size-dependent bacterial growth inhibition and mechanism of antibacterial activity of zinc oxide nanoparticles. Langmuir. 27 (7), 4020-4028 (2011).
- Plech, A., Kotaidis, V., Gresillon, S., Dahmen, C., von Plessen, G. Laser-induced heating and melting of gold nanoparticles studied by time-resolved x-ray scattering. Phys Rev B. 70 (19), 195423 (2004).
- Takami, A., Kurita, H., Koda, S. Laser-Induced Size Reduction of Noble Metal Particles. J Phys Chem B. 103 (8), 1226-1232 (1999).
- Kamat, P. V., Flumiani, M., Hartland, G. V. Picosecond Dynamics of Silver Nanoclusters. Photoejection of Electrons and Fragmentation. J Phys Chem B. 102 (17), 3123-3128 (1998).
- Yamada, K., Tokumoto, Y., Nagata, T., Mafune, F. Mechanism of laser-induced size-reduction of gold nanoparticles as studied by nanosecond transient absorption spectroscopy. J Phys Chem B. 110 (24), 11751-11756 (2006).
- Pecora, R. Dynamic Light Scattering Measurement of Nanometer Particles in Liquids. J. Nanoparticle Res. 2 (2), 123-131 (2000).
- Pyrz, W. D., Buttrey, D. J. Particle size determination using TEM: a discussion of image acquisition and analysis for the novice microscopist. Langmuir. 24 (20), 11350-11360 (2008).
- Ratti, M., et al. Irradiation with visible light enhances the antibacterial toxicity of silver nanoparticles produced by laser ablation. Appl Phys A. 122 (4), 1-7 (2016).
- Sajti, C. L., Sattari, R., Chichkov, B. N., Barcikowski, S. Gram Scale Synthesis of Pure Ceramic Nanoparticles by Laser Ablation in Liquid. J Phys Chem C. 114 (6), 2421-2427 (2010).
- Streubel, R., Barcikowski, S., Gokce, B. Continuous multigram nanoparticle synthesis by high-power, high-repetition-rate ultrafast laser ablation in liquids. Opt Lett. 41 (7), 1486-1489 (2016).
- Streubel, R., Bendt, G., Gokce, B. Pilot-scale synthesis of metal nanoparticles by high-speed pulsed laser ablation in liquids. Nanotechnology. 27 (20), 205602 (2016).
Reimpressões e Permissões
Solicitar permissão para reutilizar o texto ou figuras deste artigo JoVE
Solicitar PermissãoThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Todos os direitos reservados