É necessária uma assinatura da JoVE para visualizar este conteúdo. Faça login ou comece sua avaliação gratuita.
Method Article
Braçadeira de tensão Fluorometria em
Neste Artigo
Resumo
Este artigo descreve um aumento da Fluorometria Voltagem-Clamp convencional (VCF) onde Fluorescente Aminoácidos Não-naturais (fUAA) são usados em vez de corantes maleimida, para sondar rearranjos estruturais em canais iônicos. O procedimento inclui injeção de DNA de oócito de Xenopus , coinjeção de ARN / fUAA e medições simultâneas de corrente e fluorescência.
Resumo
A Fluorometria de Voltage-Clamp (VCF) tem sido a técnica de escolha para investigar a estrutura e função das proteínas de membrana eletrogênicas, onde as medidas em tempo real de fluorescência e correntes relatam simultaneamente rearranjos locais e função global, respectivamente. Enquanto que as técnicas estruturais de alta resolução, como a microscopia de crio-elétrons ou a cristalografia de raios-X, fornecem imagens estáticas das proteínas de interesse, o VCF fornece dados estruturais dinâmicos que nos permitem relacionar os rearranjos estruturais (fluorescência) com dados funcionais dinâmicos (eletrofisiologia). Até recentemente, a química tiol-reactiva utilizada para a marcação fluorescente dirigida ao local das proteínas restringia o âmbito da abordagem porque todas as cisteínas acessíveis, incluindo as endógenas, seriam rotuladas. Foi assim necessário construir proteínas isentas de cisteínas endógenas. A rotulagem também se restringiu a locais acessíveis a partir dolado. Isto mudou com o uso de Aminoácidos Não-naturais Fluorescentes (fUAA) para incorporar especificamente uma pequena sonda fluorescente em resposta à supressão do codão de paragem utilizando um par ortogonal de tRNA e tRNA sintetase 2 . A melhoria do VCF requer apenas um procedimento de injeção de dois passos de injeção de DNA (par tRNA / sintetase) seguido por co-injeção de ARN / fUAA. Agora, a rotulagem tanto intracelular e locais enterrados é possível, eo uso de VCF se expandiu significativamente. A técnica VCF torna-se assim atraente para o estudo de uma vasta gama de proteínas e, mais importante, permite investigar numerosos mecanismos reguladores citosólicos.
Introdução
Mais de 200 aminoácidos não naturais de várias propriedades químicas e físicas foram geneticamente incorporados em proteínas em células de E. coli , leveduras e mamíferos 3 . O aminoácido não natural é incorporado em resposta a um codão de paragem específico através de um par tRNA / sintetase engendrado ortogonalmente. A abordagem genética para modificar proteínas forneceu insights valiosos sobre a estrutura ea função da proteína. Aqui, apresentamos um protocolo para o uso de Fluorometria de Voltagem-Clamp (VCF) em combinação com uma UAA fluorescente.
No VCF, a observação simultânea de dados funcionais e rearranjos estruturais localizados ao redor da sonda fluorescente (~ 5 Å) nos permite obter informações dinâmicas com resolução milissegundo 1 . As sondas fluorescentes alteram o seu estado de extinção ao movimento localizado da proteína. Um movimento de apenas 1-2 Å é suficiente para levar a alterações significativas na fluorescênciaIntensidade 4 . Após a identificação do local de interesse na proteína alvo, o local é mutado por mutação pontual. Classicamente, o resíduo tinha sido mutado para uma cisteína enquanto que agora, um codão de paragem âmbar (TAG) é introduzido para a incorporação genética de fUAA. A proteína é então transcrita in vitro .
Enquanto outros sistemas de expressão ( por exemplo, células de mamíferos) podem ser utilizados 5 , 6 , 7 , os oócitos de Xenopus são preferíveis para estudos de estrutura-função devido ao seu maior tamanho, levando a manipulação mais fácil e maior intensidade de fluorescência (mais fluoróforos) Ruído. Além disso, os oócitos de Xenopus têm baixa formação de proteínas endógenas 2 , 8 , ea pigmentação escura no pólo animal protege contra a fluorescência de fundo de tEle citosol. Os oócitos de Xenopus são removidos cirurgicamente e o ADN que codifica o par tRNA / tRNA-sintetase ortogonal específico para a fUAA é injectado no núcleo dos oócitos. Após um período de incubação de 6-24 h, a proteína ARN é co-injectada com a fUAA no citosol dos oócitos, seguido por um período de incubação de 2-3 dias. A fim de evitar qualquer dano ao fUAA (foto-branqueamento), os procedimentos incluindo Anap têm de ser levados a cabo sob luz vermelha para evitar a excitação do fluoróforo.
Os oócitos são estudados em uma configuração de braçadeira de tensão de oócito cortada aberta, que é montada em um microscópio de fluorescência vertical, e mudanças de corrente elétrica e fluorescência são registradas simultaneamente 9 , 10 . Em alternativa, podem ser utilizadas as configurações de tensão de dois eléctrodos 1 ou de grampo-grampo 11 . A fluorescência é excitada por comprimentos de onda apropriados com baixo Emissão gravada usando um fotodíodo ligado a um amplificador com alta amplificação.
Existem várias vantagens do uso de aminoácidos fluorescentes não naturais (fUAAs) na fluorometria de tensão-braçadeira. Um deles é o acesso ao lado citosólico das proteínas da membrana; Muitos processos reguladores estão localizados aqui ( por exemplo, Ca2 + - ou sítios de ligação de nucleotídeos, inativação rápida e fechada de canais iónicos com voltagem, abertura de poros, acoplamento de módulo). Todos estes processos estão agora acessíveis para rotulagem fluorescente.
Outra vantagem é o pequeno tamanho da sonda levando a menos perturbação da proteína. Até agora, dois pares de tRNA / tRNA sintetase ortogonais para fUAAs foram desenvolvidos 12 , 13 , onde o ácido 3- (6-acetilnaftalen-2-ilamino) -2-aminopropanóico (Anap) é o único fUAA que tem sido utilizado em oócitos de Xenopus 2 ,"Xref"> 8. Anap é um fluoróforo ambientalmente sensível com um peso molecular de 272,3 g / mol e é apenas ligeiramente maior do que o triptofano 12 ( Figuras 1A, 1B ). Devido ao seu pequeno tamanho, é provável que sejam introduzidos menos efeitos estéricos pelo fluoróforo em comparação com os fluoróforos convencionais ligados através de um ligante (tipicamente mais do que 500 g / mol). Além disso, no caso de Anap, o fluoróforo está localizado mais próximo do esqueleto da proteína do que os ligados às cisteínas e, consequentemente, Anap está a testar rearranjos mais localizados. Finalmente, a remoção de cisteínas endógenas em VCF convencional para assegurar a marcação específica de sítio não é mais uma exigência em UAA-VCF e portanto (i) deixa as proteínas em (quase) o seu estado nativo e (ii) permite a aplicação de VCF Para estudar uma gama mais ampla de proteínas em que a função pode ser alterada pela substituição de cisteína.

Figura 1 : Espectro de Anap e Fluorescência. ( A ) Estrutura química de Anap. ( B ) Espectro de absorção normalizado e espectros de emissão para Anap 1 nM, demonstrando a sensibilidade da fluorescência de Anap à hidrofobicidade do solvente. Os espectros de emissão foram obtidos por excitação a 350 nm. Clique aqui para ver uma versão maior desta figura.
Uma desvantagem do uso de UAAs fluorescentes é que uma população heterogénea de proteínas pode resultar de leitura de codão de terminação, reiniciação de tradução, proteínas truncadas de terminal C ou crosstalk com aminoacilação endógena se a quantidade de tRNAs aminoacilados for escassa. Tal expressão de vazamento deve ser sempre verificada na ausência do par de ARNt / tRNA sintetase. A questão da transReinicialização lacional e como evitá-la para locais de inserção N-terminais anteriormente 14 . No entanto, quando a fUAA, tRNA e tRNA sintetase estão presentes em quantidades saturadas, só permanece uma baixa probabilidade de expressão de vazamento.
A principal diferença processual entre fUAA-VCF e VCF convencional é a injecção e manuseamento dos oócitos; A injecção de ADN que codifica o ARNt e a ARNt-sintetase (pAnap) é seguida pela introdução de Anap, que é co-injectado com o ARNm da proteína ou, alternativamente, adicionado à solução de incubação como um éster de acetoximetilo (AM).
Protocolo
As manipulações de rãs foram realizadas de acordo com as diretrizes canadenses e foram aprovadas pelo comitê de ética (CDEA, protocolo # 15-042) da Universidade de Montréal.
1. Preparação de mRNA para incorporação de fUAA
- Escolha um local de interesse na proteína onde mudanças conformacionais são esperadas para ocorrer. Selecione um aminoácido nesta região para substituir o fUAA.
NOTA: A escolha da posição baseia-se nos rearranjos estruturais esperados. Se existir uma estrutura de alta resolução e uma hipótese dos movimentos esperados, o anap deve ser colocado de modo que o ambiente químico altere; Isto pode ser uma mudança na constante dieléctrica (ambiente hidrofóbico versus hidrofílico) ou, mais provavelmente, extinção por outro aminoácido. Os melhores quenchers são triptofanos. Anap deve estar em contato com o extintor em um estado (sobreposição do raio van-der-Waals) e livre deo outro. Se não existirem estruturas ou modelos de alta resolução, seria necessário verificar a região de interesse. Em ambos os casos, é aconselhável selecionar várias localizações próximas para aumentar a probabilidade de obter expressão e sinal de fluorescência. De modo a minimizar os efeitos estéricos durante a maturação e / ou a função da proteína, pode-se escolher substituir aminoácidos grandes e aromáticos (Phe, Trp, Tyr). Os autores, no entanto, experimentaram que a exploração de uma região de interesse para a inserção de fUAA independentemente do aminoácido substituído, é mais produtiva. - Inserir um codão de paragem âmbar (TAG) no local seleccionado utilizando a mutagénese dirigida ao local 15 . Certifique-se de que a proteína de interesse não termina num codão de paragem âmbar (TAG). Se assim for, mutar para um diferente (ocre ou opal stop codon). Amplificar, isolar e sequenciar o DNA. Obter ARNm de proteína com transcrição in vitro 16 e armazenar o mRNA a 20 ° C ou 80 ° C.
- Proceder à cirurgia para obtenção de oócitos da Fase V ou VI de rãs de Xenopus laevis e defolliculate com colagenase como descrito anteriormente 17 .
- Anestesiar sapos com um anestésico apropriado de acordo com o protocolo animal aprovado (aqui: éster etílico do ácido 3-aminobenzóico). Quando eles não conseguem responder a uma pitada suave para uma ponta do pé (perda de reflexo de retirada), então eles são adequadamente anestesiados para a cirurgia.
- Remova imediatamente as râs da solução anestésica e lave bem a pele com água fresca. Este enxaguamento impedirá que o animal caia em níveis mais profundos de anestesia removendo o produto químico não absorvido da superfície da pele.
- Remova os nós do ovário de um lado cirurgicamente e cuidadosamente abra os nós usando dois fórceps. Incubar e agitar os oócitos em "solução padrão de oócito" (SOS) contendo colagenase a 1% (p / v) durante 20-30 minPara defolliculate. Lavar três vezes com solução SOS.
- Selecionar ovócitos grandes e saudáveis individualmente e incubá-los em solução de Barth suplementada com antibióticos (100 U / mL de penicilina, 100 μg / mL de estreptomicina, 10 mg / 100 mL de canamicina) e 5% de soro de cavalo a 18 ºC por pelo menos 4 h antes da injeção .
NOTA: Após 2 a 4 cirurgias com um atraso de 4 meses entre as fases, Xenopus laevis é eutanizado por incubação prolongada (> 1 h) com éster etílico do ácido 3-aminobenzóico.
- Para a injeção nuclear de DNA, prepare uma ponta de injeção longa e fina para poder alcançar o núcleo e evitar danificar o oócito. Encha a ponta da injeção com óleo e monte-a no dispositivo nanoinjetor.
- Instale o nano-injector sob um microscópio estéreo e use fórceps para quebrar a extremidade da ponta. Ejetar o óleo até que não haja bolhas de ar presas dentro da extremidade da ponta.
- Colocar 1 μL de 0,1 μg /# 181; L pAnap em água livre de nuclease contendo NaOH (1% de NaOH 1 N) em um pedaço de parafilme sob um estereoscópio e encher a ponta de injeção com o DNA.
- Transferir 40 oócitos para uma placa de injecção revestida com malha contendo solução de Barth suplementada com antibióticos.
NOTA: Para fazer o prato de injecção revestido com malha, corte uma peça de tamanho apropriado de malha de nylon de 800 μm para encher uma placa de Petri de poliestireno. Adicionar clorofórmio para o centro e, em seguida, coloque a malha na parte superior. Segure a malha plana até que o plástico conjuntos. - Como o núcleo do oócito está localizado no pólo animal (escuro), aponte a ponta da injeção no centro do pólo animal e empalar de forma que a ponta se aproxime do centro do hemisfério animal (ou 2-3x a profundidade em relação à injeção de RNA ). Injectar 9,2 nL de pAnap no núcleo de cada oócito. A ponta fina e o pequeno volume de injeção podem resultar em injeção irregular ou ponta bloqueada. Ocasionalmente verifique se a injeção funciona injetando no ar.
NOTA: Se o DNA é devidamente injetado no núcleo é incerto. Esperar, portanto, 10 - 40% dos oócitos para não expressar o par tRNA / sintetase. Ver Discussão para mais detalhes. - Incubar os oócitos em 2 mL de solução de Barth suplementada com antibióticos e 5% de soro de cavalo (HS) a 18 ° C durante 6-24 h para permitir a expressão robusta de Anap tRNAs específicos e tRNA-sintetases.
NOTA: O tempo de incubação do DNA pode durar vários dias antes da injeção de RNA, mas não aumenta a expressão. - Prepare o nano-injetor para injeção de RNA (o mesmo que o passo 2.2, mas a ponta da injeção não precisa ser tão fina quanto para a injeção de DNA). Trabalhe apenas sob luz vermelha a partir deste ponto para evitar o fotoblanqueio do Anap.
- Misture 1 μl de Anap 1 mM com 1 μL de mRNA 1-2 μg / μL diretamente em um pedaço de parafilme e encha a ponta da injeção com a solução mista. Impala logo abaixo da membrana no(Brilhante) e injectar 46 nL em cada ovocito injectado com pAnap.
NOTA: A concentração de mRNA requerida depende da proteína de interesse. - Incubar os oócitos protegidos da luz em uma caixa ou envolto em folha de alumínio, em solução de Barth suplementado com antibióticos e 5% de soro de cavalo a 18 ° C por 2-3 dias. Troque com a solução fresca de Barth todos os dias e remova os oócitos mortos para evitar contaminação.
- Instale o equipamento de aperto de tensão de oócito cortado aberto como descrito anteriormente 18 .
- Montar o sistema de registro eletrofisiológico em um microscópio de fluorescência vertical, instalando a câmara de gravação em um controle deslizante que permite movê-lo entre o estereoscópio padrão para colocar o oócito eo microscópio para realizar as medições de fluorescência ( Figura 2c ).
NOTA: A geometria da câmara para os oócitos cortados não é adequada para usar a tra normalNsmitted luz para iluminação durante a manipulação. Portanto, uma lâmpada halógena "gooseneck" com filtro vermelho é usada para iluminar lateralmente a partir do topo. O condensador do microscópio pode ser removido fazer espaço para baixar o estágio para a câmara de eletrofisiologia. - Conectar um sistema de detecção de fotodiodo à porta de saída de montagem em C do microscópio de fluorescência ( Figura 2a ). Ligue a leitora de fotocorrente a um segundo canal de entrada no processador de sinal digital (DSP, conversor analógico / digital - digital / analógico).
- Use uma lâmpada de halogéneo de 100 W, 12 V como fonte de luz para a excitação de fluorescência.
NOTA: Em alternativa, podem ser utilizados queimadores de Hg, mas têm de ser reduzidos em intensidade para evitar um foto-branqueamento demasiado rápido durante as gravações. A iluminação por LED só é recomendada se os respectivos LEDs apresentarem uma intensidade significativa na gama de excitação ( por exemplo, ~ 350 nm para Anap). A maioria dos LEDs brancos não atinge muito no espectro UV. - InsErt um obturador controlado eletricamente entre a fonte de luz de excitação e microscópio e conectar seu controle (tipicamente TTL-pulso) a uma saída digital do DSP. Tempo o TTL-pulso no software de gravação (consulte a documentação do fabricante), de modo que o obturador abre ~ 100 ms antes do início da gravação. Desta forma, qualquer vibração durante o processo de abertura não interfere com a gravação. O tempo depende da velocidade e vibração do obturador. Termine o pulso 5ms antes do fim da gravação como mostrado na Figura 4 . Desta forma, o valor para a fluorescência total é também registado.
- Insira um cubo de filtro apropriado (filtro de excitação, espelho dicróico e filtro de emissão) na torreta do cubo do filtro. Para Anap, utilizar Passo de banda Ex: 377/50 nm, passo largo 409 nm dicroico e passo de banda Em: 470/40 nm.
- Seguir os passos de preparação para a tensão de bloqueio de oócito cortada como anteriormente descrito e visualizado 18 (preparação da ponte de ágar, montagem do oócito, permeabilização da saponina). No entanto, trabalhar sob luz vermelha em todos os tempos para evitar o branqueamento do fluoróforo antes de gravações. Ao colocar o oócito, certifique-se de que o pólo animal está voltado para cima. A pigmentação sob a membrana polar animal protege contra a autofluorescência originária do citosol e, portanto, reduz a fluorescência de fundo.
- Deslize a câmara para o microscópio e foco usando um objetivo 4X.
- Empale o oócito com o eletrodo V1 (3 M KCl), mude para o objetivo 40X de imersão em água (NA 0,8 - 0,9). Foco no pólo animal que está enfrentando para cima.
- Desligue a luz vermelha. Selecione o cubo do filtro direito girando a torre do cubo do filtro e a porta de saída óptica conectada ao fotodiodo. Ligue o halogéneoEn lâmpada na maior intensidade e em breve mudar o obturador aberto por 2-5 s para ler a intensidade de fluorescência de fundo originário do oócito. Com a configuração descrita o valor deve ser de cerca de 50-200 pA para Anap.
- Ligue o grampo, rode o interruptor de banho / guarda para ativo e ajuste o potencial de membrana (V1 - V2) ao potencial de comando, rodando o botão na cabeça.
- Selecione o potencial de retenção, o protocolo de passo, o número eo comprimento de pulsos, etc. no software de gravação. Registre as correntes dependentes da tensão e as intensidades de fluorescência Anap.
- Para monitorizar simultaneamente duas localizações na mesma proteína, muta um aminoácido extracelular e acessível em cisteína, e remove outras cisteínas para garantir rotulagem específica com tiol-química.
- Execute a etapa 2.1-2.5.
- Antes das gravações VCF, incubar oócitos em TMR-maleimida 5 μM em solução de rotulagem durante 15 min (ou outro coranteCom espectros não sobrepostos comparados com Anap).
- Lave os oócitos com solução de rotulagem três vezes para remover o excesso de corante.
- Execute a etapa 4.1-4.6.
- Insira um cubo de filtro apropriado para TMR (filtro de excitação, espelho dicróico e filtro de emissão) na torreta do cubo do filtro. Mude para o cubo do filtro TMR girando a torre do filtro.
- Leia a fluorescência de fundo para TMR como descrito para Anap no passo 4.4.
NOTA: O rótulo com a química tiol resulta em alta fluorescência de fundo devido à marcação inespecífica na membrana. Portanto, a fluorescência de fundo TMR pode saturar o amplificador (> 2000 pA). Nesse caso, não diminua a intensidade da luz, mas simplesmente subtraia a fluorescência de fundo adicionando uma corrente de deslocamento ao fotodiodo. Em sistemas comercialmente disponíveis, use o recurso "sample-and-hold" no sistema detector. Observe o valor de fluorescência de fundo (usando um filtro de densidade neutra 10X) em um laboratório jComo este valor não será registrado (saturação). - Registre as correntes dependentes da tensão e as intensidades de fluorescência TMR simultaneamente, como no passo 4.6.
2. Preparação e Injecção de Oócitos
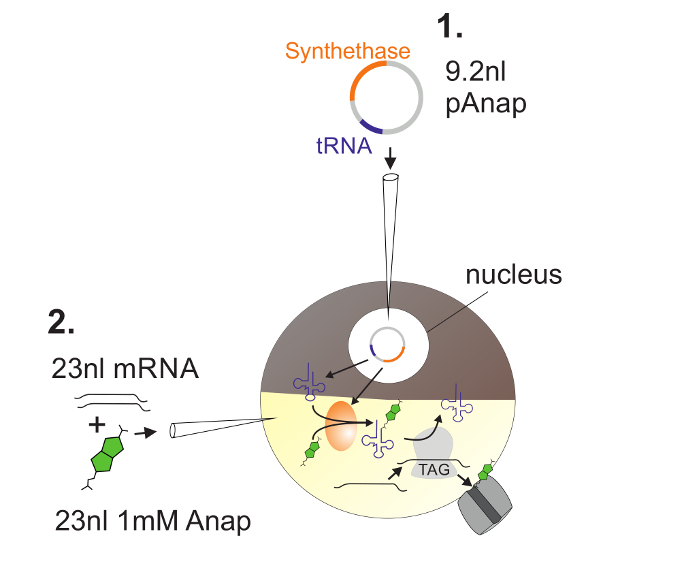
Figura 2 : Ilustra�o da injec�o de ADN e ARN em O�itos de Xenopus para Anap Incorporation.
Primeiro, pAnap é injetado no núcleo do oócito Xenopus ( 1 ). Após 6-24 h, Anap e canal RNA são coinjected no pólo vegetal ( 2 ). O Anap será ortogonalmente aminoacilado com o ARNt portador de um anti-codão de bloqueio âmbar, pela aminoacil-ARNt-sintetase que é codificada por pAnap. Deste modo, os Anap-ARNt aminoacilados são reconhecidos pelo ribossoma no codão de paragem âmbar inserido no canalL de ARN, resultando na supressão do codão de paragem e inserção de Anap. Clique aqui para ver uma versão maior desta figura.
3. Configuração VCF

Figura 3 < / Strong> : configuração VCF. ( A ) Vista lateral da configuração VCF mostrando o caminho da luz dentro do microscópio. O cubo do filtro contém um filtro de excitação, um espelho dicróico e um filtro de emissão. ( B ) As dimensões da câmara de oócito são 3,4 cm para o raio superior da câmara (1), 5,5 cm para o comprimento da câmara inferior (2), 1,4 cm para a largura da câmara inferior (3) e 1,7 cm para a largura da câmara intermédia (4). ( C ) Vista frontal da configuração VCF. O primeiro ocular à esquerda é para montar o oócito na câmara de aperto de tensão aberta e para permeabilização. Em seguida, a câmara é deslizada sob o microscópio no segundo olho para a direita. Aqui, o eléctrodo V1 é inserido no oócito utilizando o objectivo 4X, e a fluorescência é registada utilizando o objectivo 40X de imersão em água. Clique aqui para ver uma versão maior desta figura.
5. Duas cores VCF
Resultados
A Figura 4 mostra um exemplo de gravações de VCF obtidas a partir de um ovócito que expressa canais de Shaker com inactivação rápida removida (IR), L382stop-W434F na presença de pAnap e Anap. A mutação W434F bloqueia as correntes iônicas de potássio, o que torna possível medir os deslocamentos transitórios de carga de gating (correntes de gating). As gravações simultâneas das correntes de passagem (traçado superior) e das alterações de intensidade de f...
Discussão
A aminoacilação in vivo de tRNAs que estão continuamente a ser transcritos em conjunto com a tRNA-sintetase, torna possível obter níveis de expressão elevados para medições de fluorescência. Para a incorporação eficiente de fUAA, é crítico que o pAnap seja corretamente injetado no núcleo. Devido à incerteza da localização exacta do núcleo, espera-se que 10-40% das injecções de ADN falhem, resultando em oócitos que não expressam (ou que expressam fugas). Portanto, é importante verificar a ...
Divulgações
Os autores não têm nada a revelar.
Agradecimentos
PAnap foi um presente amável do Dr. Peter Schultz (Scripps Research Institute). Este trabalho foi financiado pelos Institutos Canadenses de Subsídios de Pesquisa de Saúde MOP-102689 e MOP-136894 (para RB) e Canadian Foundation for Innovation Grant 950-225005.
Materiais
| Name | Company | Catalog Number | Comments |
| Solutions | |||
| Barth's solution | |||
| NaCl | Sigma-Aldrich | S7653 | 90 mM |
| KCl | Fisher Scientific | BP366-500 | 3 mM |
| MgSO4 | Sigma-Aldrich | M-9397 | 0.82 mM |
| CaCl2 | Sigma-Aldrich | C-7902 | 0.41 mM |
| Ca(NO3)2 | Sigma-Aldrich | C-1396 | 0.33 mM |
| HEPES | Sigma-Aldrich | H4034 | 5 mM |
| NaOH hydrate | BDH | BDH7225-4 | pH 7.6 |
| Penicilin | Invitrogen | 15140122 | 100 U/mL |
| Streptomycin | Invitrogen | 15140122 | 100 µg/mL |
| Kanamycin | Invitrogen | 15160054 | 10 mg/100mL |
| Horse Serum (HS) | Invitrogen | 16050122 | 5% |
| SOS Standard Oocyte Solution | |||
| NaCl | Sigma-Aldrich | 746398 | 102 mM |
| KCl | Sigma-Aldrich | 746436 | 3 mM |
| MgCl2 | Sigma-Aldrich | M9272 | 1 mM |
| HEPES | Sigma-Aldrich | H4034 | 5 mM |
| External recording solution | |||
| N-methyl-D-glucamine (NMDG) | Alfa Aesar | L14282 | 115 mM |
| HEPES | Sigma-Aldrich | H4034 | 10 mM |
| Calcium hydroxide | Sigma-Aldrich | 239232 | 2 mM |
| MES hydrate | Sigma-Aldrich | 258105 | pH 7.2 |
| Internal recording solution | |||
| N-methyl-D-glucamine (NMDG) | Alfa Aesar | L14282 | 115 mM |
| HEPES | Sigma-Aldrich | H4034 | 10 mM |
| Ethylenediamine Tetraacetic Acid (EDTA) | Fisher Scientific | E478-500 | 2 mM |
| MES hydrate | Sigma-Aldrich | 258105 | pH 7.2 |
| Labeling solution | |||
| KOH | Fisher Scientific | P250-1 | 115 mM |
| HEPES | Sigma-Aldrich | H4034 | 10 mM |
| Calcium hydroxide | Sigma-Aldrich | 239232 | 2 mM |
| MES hydrate | Sigma-Aldrich | 258105 | pH 7.2 |
| TMR stock solution | |||
| Tetramethylrhodamine-5-maleimide (TMR) | Molcular Probes by Life Technologies | T6027 | 5 mM in DMSO |
| Anap stock solution | |||
| Anap | ABZENA (TCRS) | Custom synthesis TCRS-170 | 1 mM in nuclease-free water and 1% NaOH 1 N |
| Name | Company | Catalog Number | Comments |
| Material/Equipment | |||
| pAnap | Addgene | 48696 | |
| High Performance Oocyte Clamp | Dagan Corporation | CA-1B | |
| Gpatch Acquisition software | Department of Anesthesiology, University of California, Los Angeles | ||
| Analysis software | Department of Anesthesiology, University of California, Los Angeles | ||
| Recording Chamber | Custom machined | ||
| Photo diode detection system | Dagan Corporation | PhotoMax-200/PIN | |
| Electrical shutter driver | UNIBLITZ | VCM-D1 |
Referências
- Mannuzzu, L. M., Moronne, M. M., Isacoff, E. Y. Direct physical measure of conformational rearrangement underlying potassium channel gating. Science. 271 (5246), 213-216 (1996).
- Kalstrup, T., Blunck, R. Dynamics of internal pore opening in K(V) channels probed by a fluorescent unnatural amino acid. Proc Natl Acad Sci U S A. 110 (20), 8272-8277 (2013).
- Xiao, H., Schultz, P. G. At the Interface of Chemical and Biological Synthesis: An Expanded Genetic Code. Cold Spring Harb Perspect Biol. 8 (9), (2016).
- Blunck, R. Chapter 9. Handbook of Ion Channels. , 113-133 (2015).
- Chatterjee, A., Guo, J., Lee, H. S., Schultz, P. G. A genetically encoded fluorescent probe in mammalian cells. J Am Chem Soc. 135 (34), 12540-12543 (2013).
- DeBerg, H. A., Brzovic, P. S., Flynn, G. E., Zagotta, W. N., Stoll, S. Structure and Energetics of Allosteric Regulation of HCN2 Ion Channels by Cyclic Nucleotides. J Biol Chem. 291 (1), 371-381 (2016).
- Shen, B., et al. Genetically encoding unnatural amino acids in neural stem cells and optically reporting voltage-sensitive domain changes in differentiated neurons. Stem Cells. 29 (8), 1231-1240 (2011).
- Aman, T. K., Gordon, S. E., Zagotta, W. N. Regulation of CNGA1 Channel Gating by Interactions with the Membrane. J Biol Chem. 291 (19), 9939-9947 (2016).
- Haddad, G. A., Blunck, R. Mode shift of the voltage sensors in Shaker K+ channels is caused by energetic coupling to the pore domain. J Gen Physiol. 137 (5), 455-472 (2011).
- Batulan, Z., Haddad, G. A., Blunck, R. An intersubunit interaction between S4-S5 linker and S6 is responsible for the slow off-gating component in Shaker K+ channels. J Biol Chem. 285 (18), 14005-14019 (2010).
- Kusch, J., et al. How subunits cooperate in cAMP-induced activation of homotetrameric HCN2 channels. Nat Chem Biol. 8 (2), 162-169 (2012).
- Lee, H. S., Guo, J., Lemke, E. A., Dimla, R. D., Schultz, P. G. Genetic incorporation of a small, environmentally sensitive, fluorescent probe into proteins in Saccharomyces cerevisiae. J Am Chem Soc. 131 (36), 12921-12923 (2009).
- Summerer, D., et al. A genetically encoded fluorescent amino acid. Proc Natl Acad Sci U S A. 103 (26), 9785-9789 (2006).
- Kalstrup, T., Blunck, R. Reinitiation at non-canonical start codons leads to leak expression when incorporating unnatural amino acids. Sci Rep. 5, 11866 (2015).
- Liu, H., Naismith, J. H. An efficient one-step site-directed deletion, insertion, single and multiple-site plasmid mutagenesis protocol. BMC Biotechnol. 8, 91 (2008).
- Beckert, B., Masquida, B. Synthesis of RNA by in vitro transcription. Methods Mol Biol. 703, 29-41 (2011).
- Goldin, A. L. Maintenance of Xenopus laevis and oocyte injection. Methods Enzymol. 207, 266-279 (1992).
- Rudokas, M. W., Varga, Z., Schubert, A. R., Asaro, A. B., Silva, J. R. The Xenopus oocyte cut-open vaseline gap voltage-clamp technique with fluorometry. J Vis Exp. (85), (2014).
- Zhao, J., Blunck, R. The isolated voltage sensing domain of the Shaker potassium channel forms a voltage-gated cation channel. Elife. 5, (2016).
- Posson, D. J., Ge, P., Miller, C., Bezanilla, F., Selvin, P. R. Small vertical movement of a K+ channel voltage sensor measured with luminescence energy transfer. Nature. 436 (7052), 848-851 (2005).
- Chanda, B., Asamoah, O. K., Blunck, R., Roux, B., Bezanilla, F. Gating charge displacement in voltage-gated ion channels involves limited transmembrane movement. Nature. 436 (7052), 852-856 (2005).
- Taraska, J. W., Puljung, M. C., Zagotta, W. N. Short-distance probes for protein backbone structure based on energy transfer between bimane and transition metal ions. Proc Natl Acad Sci U S A. 106 (38), 16227-16232 (2009).
- Baker, B. J., et al. Genetically encoded fluorescent sensors of membrane potential. Brain Cell Biol. 36 (1-4), 53-67 (2008).
- Miranda, P., et al. State-dependent FRET reports calcium- and voltage-dependent gating-ring motions in BK channels. Proc Natl Acad Sci U S A. , (2013).
- Sisido, M., Ninomiya, K., Ohtsuki, T., Hohsaka, T. Four-base codon/anticodon strategy and non-enzymatic aminoacylation for protein engineering with non-natural amino acids. Methods. 36 (3), 270-278 (2005).
- Hohsaka, T., Ashizuka, Y., Murakami, H., Sisido, M. Five-base codons for incorporation of nonnatural amino acids into proteins. Nucleic Acids Res. 29 (17), 3646-3651 (2001).
Reimpressões e Permissões
Solicitar permissão para reutilizar o texto ou figuras deste artigo JoVE
Solicitar PermissãoThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Todos os direitos reservados