Method Article
Sondagem de Propriedades Estruturais e Dinâmicas de Nanoestruturas Subcelulares de Tráfico por Espectroscopia de Flutuação Espiotemporal
Neste Artigo
Resumo
A análise de deslocamento quadrado médio (iMSD) derivada de imagem é aplicada a macropinossos para destacar sua natureza intrínseca em termos de propriedades estruturais e dinâmicas. Os macropinossomos são então comparados aos grânulos secretos de insulina (ISGs) como referência para estruturas subcelulares com propriedades estruturais/dinâmicas médias invariantes.
Resumo
O deslocamento quadrado médio derivado da imagem (iMSD) é usado para abordar as propriedades estruturais e dinâmicas das nanoestruturas subcelulares, como vesículas envolvidas no tráfico endo/exotótico de solútes e biomoléculas. O iMSD conta com imagens padrão de lapso de tempo, é compatível com qualquer configuração óptica e não precisa se debruçar sobre objetos únicos para extrair trajetórias. A partir de cada traço iMSD, um trigêmeo único de parâmetros estruturais e dinâmicos médios (ou seja, tamanho, difusividade local, coeficiente anômulo) é calculado e combinado para construir a "assinatura iMSD" da nanoestrutura em estudo.
A potência dessa abordagem é comprovada aqui com o caso exemplar de macropinossomos. Essas vesículas evoluem no tempo, alterando seu tamanho médio, número e propriedades dinâmicas passando dos estágios iniciais para o final do tráfico intracelular. Como controle, os grânulos secretores de insulina (ISGs) são usados como referência para estruturas subcelulares que vivem em um estado estacionário no qual as propriedades estruturais e dinâmicas médias de toda a população de objetos são invariantes no tempo. A análise do iMSD destaca essas características peculiares quantitativamente e abre caminho para aplicações semelhantes no nível subcelular, tanto nos estados fisiológicos quanto patológicos.
Introdução
As nanoestruturas subcelulares (por exemplo, vesículas endocíticas/secretas, organelas) desempenham um papel fundamental na regulação de sinalizaçãocelular 1. A sintonia adequada de suas características estruturais (por exemplo, tamanho) e/ou dinâmica (por exemplo, difusividade) determina como a célula responde a estímulos internos ou externos 2,3,4. Com base nessas evidências, não é de surpreender que alterações dessas características sejam encontradas em muitas condições patológicas. Exemplos englobam o papel da endocitose mal regulamentada no câncer 2,3, as alterações estruturais e dinâmicas encontradas no nível de ISGs em células β expostas às condições de Diabetes Tipo 25, a desregulamentação das propriedades estruturais e de transporte lysosomal na leucodistrofia de células globoid ou lipidose de galactosylceramida6, e disfuncionalidades na via endo-lyosomal em distúrbios neurodegenerativos (por exemplo, doença de Alzheimer)7.
Nesse contexto, pesquisadores provaram recentemente que o desempenho dos métodos de microscopia óptica padrão pode ser aprimorado, afinando adequadamente a resolução de amostragem espacial e temporal8. Isso, por sua vez, pode fornecer mais informações sobre processos biológicos de relevância. Na prática, isso é possível por um algoritmo de análise de flutuação espiotemporal, que extrai simultaneamente as propriedades estruturais e dinâmicas médias de objetos difundidores diretamente da pilha padrão de imagens de microscopia óptica sem qualquer necessidade de conhecimento preliminar sobre o objeto biológico de interesse e extração de trajetórias de um único objeto. Todas essas informações estão incluídas em uma única saída do método: um traço iMSD9 (detalhes sobre a derivação e análise do traço iMSD são fornecidos no Arquivo Suplementar 1).
O protocolo experimental resultante consiste em alguns passos. Em primeiro lugar, a imagem da região de interesse é realizada em alta resolução temporal. Em seguida, as funções médias de correlação espaço-temporal são calculadas a partir da pilha de imagens. Finalmente, pelo encaixe gaussiano da série de funções de correlação, a "lei de difusão" média é obtida diretamente a partir de imagens e analisada para reconhecer o modo de difusão do objeto. O potencial do método já foi comprovado para uma variedade de objetos biológicos, variando de moléculas a nanopartículas e até organelas/estruturas subcelulares inteiras 9,10,11,12,13,14,15.
Este artigo relata a aplicação do IMSD aos macropinossmos para destacar sua natureza intrínseca e irreversível em termos de suas propriedades estruturais e dinâmicas médias (ou seja, em todo o nível populacional). Além disso, essas vesículas endocíticas são comparadas aos ISGs como referência para estruturas subcelulares em um "estado estacionário", ou seja, um estado em que as propriedades estruturais/dinâmicas médias de toda a população de grânulos permanecem constantes a qualquer momento. A macropinocistose define uma série de eventos iniciados pela extensa reorganização (ou babados) da membrana plasmática para formar uma estrutura macropinocítica externa que é então internalizada16. Os macropinossos em estágio inicial formados são muito semelhantes aos fagosmosos. Ao mesmo tempo, eles podem ser distinguidos de outras formas de vesículas dotícticas devido ao seu tamanho grande característico, heterogeneidade morfológica e falta de estruturas de proteína-revestimento.
Ensaios bioquímicos revelaram que, após a internalização, os macropinosos são progressivamente enriquecidos com marcadores proteicos de outras vias endocíticas, por sua vez, sugerindo que suas identidades estão mudando continuamente durante o tráfico17. Usando anticorpos contra marcadores conhecidos da via endossomal, foi demonstrado que os macropinossos adotam progressivamente características endossomais clássicas: diminuem de tamanho, desenvolvem-se em estruturas endócticas tardias (por exemplo, lysosomes), ou eventualmente perdem sua identidade através da recuperação mediada por membrana de marcadores moleculares específicos (por exemplo, classificando nexins)18,19 . O cenário geral é que cada macropinosome dentro da célula muda irreversivelmente sua identidade estrutural e dinâmica (assim como molecular) durante o tráfico da membrana plasmática para seu destino intracelular final. Como resultado, as propriedades estruturais/dinâmicas/moleculares de toda a população de macropinossomos também estão mudando ao longo do mesmo caminho temporal. Sendo intrinsecamente sensível às propriedades médias de toda a população de objetos observados, o método iMSD retrata quantitativamente a "natureza em evolução" pela quantificação dos principais parâmetros médios, ou seja, a difusividade local e coeficiente anômulo (propriedades dinâmicas) e o tamanho médio dos macropinosos (propriedade estrutural) em qualquer estágio de seu tráfico intracelular.
Para comparação, medidas semelhantes foram realizadas em uma conhecida estrutura intracelular fechada por membrana, o ISG, em um modelo de células β. Assim como os macropinossomos, a regulação das propriedades estruturais e dinâmicas dos ISGs, desde sua gênese na Rede Trans Golgi (TGN) até sua exocitese na membrana plasmática, é fundamental para a execução adequada da função ISG20. No entanto, ao contrário dos macropinossomos, os ISGs vivem em um "estado estacionário" no qual, a qualquer momento, todos os estágios funcionais/estruturais/moleculares da vida útil do ISG estão simultaneamente presentes dentro da célula, e cada um é representado por uma subpopulação específica de ISGs. Isso significa que, embora cada grânulo evolua irreversivelmente da biogênese para a secreção, espera-se que as propriedades estruturais/dinâmicas médias de toda a população de grânulos permaneçam constantes a qualquer momento (a menos que as condições estacionárias do estado sejam alteradas, por exemplo, por estímulos externos como glicose, colesterol e citocinas13). Isso é confirmado pela análise do iMSD.
Protocolo
1. Preparação da amostra
- Antes do experimento da microscopia, células de subcultura em pratos adequados para aplicações de microscopia.
- Lave um prato tratado com 10 cm de tecido-cultura de células confluentes HeLa ou INS 1E (insulinoma β células) duas vezes com 0,01 M 1x PBS, adicione 1 mL de 0,05% de trippsina-EDTA (1x), e coloque-o em uma incubadora de 37 °C, umidificada, 5% CO2 para 5.
- Resuspenque as células separadas adicionando 9 mL de DMEM completo (para células HeLa) ou RPMI 1640 (para células INS-1E) médios, e colete os 10 mL finais em tubos de centrífugas.
- Sementes aproximadamente 2 × 105 células em cada prato de 35 mm x 10 mm em um volume final de 1 mL do meio. Incubar as células por 24 h a 37 °C e 5% de CO2.
- Para rotular fluorescentemente lysosomes, use LysoTracker Red DND-99.
- Diluir a solução de estoque em 1 mL de médio pré-armado para uma concentração final de corante de 70 nM.
- Substitua o meio do prato por meio fresco contendo LysoTracker. Incubar as células em LysoTracker-contendo meio por 20 min a 37 °C em uma atmosfera de 5% de CO2 , e lavá-las duas vezes com meio fresco antes do experimento.
- Para rotular fluorescentemente macropinossomos, use isothiocyanato-dextran de 70 kDa. Lave as células subculturadas três vezes com 0,01 M 1x 1x tamponado de fosfato (PBS), substitua pelo meio contendo dextran (1 mg/mL) e incubar a 37 °C por 30 min. Antes de prosseguir com o experimento de microscopia, lave as células três vezes com meio fresco.
- Para rotular fluorescentemente isgs em células INS-1E, transfez as células usando reagente de transfecção (ver a Tabela de Materiais) e C-peptídeo-enhanced green fluorescent protein (EGFP) plasmid13 de acordo com o protocolo do fabricante, e incubar a 37 °C por 24 h em um CO2 5 % antes do experimento.
2. Aquisição de Dados
- Para deixar o microscópio equilibrar-se na temperatura e atmosfera desejadas, ligue o sistema de controle da incubadora de microscópio pelo menos 2 h antes do experimento.
NOTA: Cada aquisição é uma série de lapso de tempo. - Adquira as imagens usando um microscópio confocal invertido equipado com um objetivo de imersão de água de 60x, 1.2 Numérico (NA).
- Use um laser argon de 488 nm para excitação de EGFP (células transfeminadas) e macropinoss rotulados por fluoresceína. Colete a emissão de fluorescência entre 500 e 600 nm usando um detector de tubo fotomultiplier padrão.
- Use um laser HeNe de 543 nm para excitar Lysotracker e coletar sua emissão de fluorescência entre 555 e 655 nm.
- Ajuste o diâmetro do pinhole de detecção ao tamanho de 1 Airy. Para cada aquisição, colete uma série de 1000 quadros sequenciais. Defina o tempo de pixel-dwell para 2 μs/pixel para um tempo de quadro de 129 ms.
NOTA: Cada quadro consistia de 256 x 256 pixels (16 bits/pixel) com uma dimensão física de 69 nm/pixel, correspondendo aproximadamente a uma área de 17 μm x 17 μm.
3. icálculo msd
NOTA: Para executar corretamente o cálculo, use um software capaz de cálculo numérico e programação de script. O script específico (ou seja, para o arquivo de script 'iMSD.m', ver Arquivo de Suporte 1) deve estar presente no mesmo diretório que contém a série de imagens a ser processada. Cada imagem da série deve ser salva como um arquivo '.tif' distinto.
- Para inicializar adequadamente os parâmetros instrumentais utilizados para as aquisições, abra o iMSD.m com o editor de texto do software e modifique sua primeira seção da seguinte forma.
- Definir N como o número de quadros na série temporal (por exemplo, 1000 neste protocolo).
- Definir px_size: tamanho do pixel, expresso em μm (por exemplo, 0,069 neste protocolo).
- Conjunto f: resolução temporal de cada quadro, expressa em segundos (por exemplo, 0,129 neste protocolo).
- Definir filtro: entrada binária para correção de fundo, definir o valor para '0' para processar imagens brutas ou definir o valor para '1' para executar uma subtração de fundo baseada em limiar.
- Definir av_toll: limiar para correção de fundo; qualquer pixel com intensidade inferior a este valor será definido como 0 se Filter=1.
- Defina o bit como o número inteiro determinando a amostragem de intensidade (por exemplo, 8 bits, 16 bits).
- Salve e execute o arquivo de script editado iMSD.m.
- Verifique a execução do roteiro.
NOTA: O status do processamento do cálculo pode ser verificado na janela de comando; se ocorrer algum problema fatal, o processo será interrompido e uma mensagem de aviso será exibida para mostrar o tipo de erro e o código de linha relacionado. Caso contrário, siga os passos 3.3.1-3.3.3.- Importe a pilha de imagens e subtraia o fundo (se necessário).
- Calcule a função de correlação espiotemporal G (φ,η,τ) utilizando o método Fourier.
- Encaixe a função de correlação espória com uma função gaussiana 2D.
NOTA: Ao final do processo, os valores de saída dos procedimentos de montagem σ2(τ) serão mostrados na janela de comando: médias, erros e bondade correspondente (R2) de encaixe são relatados.
- Verifique a saída gráfica.
NOTA: A curva iMSD e as curvas de encaixe correspondentes são mostradas em três painéis separados, cada um para um tipo diferente de equação de montagem usada: difusão browniana, difusão anômparada ou difusão confinada. Para cada curva, o valor R2 é relatado na legenda do gráfico. - Verifique a saída de texto.
NOTA: No final do processo, um arquivo '.xls' é criado com o mesmo nome do arquivo '.tif' original. A primeira folha contém os valores de φ, η, τ e σ2 calculados para cada atraso de tempo. Os parâmetros de entrada e os principais valores de saída calculados são relatados na segunda folha, ou seja, coeficiente de difusão, coeficiente anômo e eixo y σinterceptação 20.
Resultados
O fluxo de trabalho geral do método é apresentado na Figura 1. Recapitula as principais etapas apresentadas na seção de protocolo, desde a preparação da amostra (Figura 1A) até a imagem de lapso de tempo de nanoestruturas intracelulares (Figura 1B), análise de flutuação para o cálculo da série de funções correlações espaço-estruturais (Figura 1C) e adequação para a derivação das propriedades estruturais/dinâmicas médias do objeto em estudo (Figura 1D).
Um parâmetro crítico é a resolução de tempo adotada para a imagem do objeto de interesse subcelular. Este valor experimental definirá o limite de tempo no qual será medido o deslocamento médio mínimo dos objetos de interesse. No entanto, a condição preferida é definir uma resolução de tempo de imagem em que o objeto de interesse aparece 'imóvel' dentro do quadro capturado, ou seja, ele exibe um tamanho característico que, em média, não é deformado devido à velocidade de imagem. Isso é tecnicamente possível se o objeto de interesse for uma estrutura subcelular ou organela com membrana (como neste caso). Normalmente, estruturas subcelulares exibem coeficientes locais de difusão (D, μm2/s, ver Tabela 1) que são várias ordens de magnitude inferiores às de moléculas isoladas únicas no citoplasma (por exemplo, GFP21). A validação pode ser realizada imobilizando artificialmente a organela de interesse (por exemplo, por fixação química). De fato, essa condição pode servir como uma referência para determinar o tamanho real da organela sob as condições experimentais utilizadas (por exemplo, comprimento de onda de excitação, tamanho do pixel, objetivo).
Aqui, embora os lysosomos tenham sido utilizados como organelas de teste para este procedimento, os resultados são válidos independentemente da estrutura alvo. A Figura 2A mostra uma imagem de um lysosome fixo (ou seja, imóvel) juntamente com uma aquisição realizada em células vivas na resolução temporal apropriada (ou seja, tipicamente abaixo de 100 ms/quadro; por exemplo, 65 ms/quadro no exemplo na Figura 2B) e uma aquisição realizada intencionalmente em resolução temporal muito baixa (por exemplo, 10 s/quadro no exemplo em Figura 2C) e uma aquisição realizada intencionalmente em resolução temporal muito baixa (por exemplo, 10 s/quadro no exemplo em Figura 2C) e uma aquisição realizada intencionalmente em resolução temporal muito baixa (por exemplo, 10 s/quadro no exemplo em Figura 2C) e uma aquisição realizada intencionalmente em resolução temporal muito baixa (por exemplo, 10 s/quadro no exemplo em Figura 2C) e uma aquisição realizada intencionalmente em resolução temporal muito baixa (por exemplo, 10 s/quadro no exemplo em Figura 2C) e uma aquisição realizada intencionalmente em resolução temporal muito baixa (por exemplo, 10 s/quadro no exemplo em Figura 2C) e uma aquisição realizada intencionalmente em resolução temporal muito baixa (por exemplo, 10 s/quadro no exemplo em Figura 2C) ). Para cada condição, o tamanho do objeto difuso é extraído da seguinte forma: i) um perfil de intensidade do local é derivado pela ferramenta de linha no software ImageJ; ii) o perfil de intensidade é plotado e interpolado por uma função gaussiana para calcular a largura total pela metade do valor máximo (FWHM) que, por sua vez, é usado como uma estimativa do diâmetro spot (Figura 2D). Como esperado e mostrado na parcela da Figura 2E, a aquisição em resolução temporal muito alta (ou seja, 65 ms/quadro) rende um tamanho médio da estrutura próxima à obtida na amostra fixa, seja utilizando a ferramenta padrão descrita acima ou extraindo a interceptação iMSD y-eixo. Em vez disso, a aquisição em velocidade lenta produz um aumento no tamanho aparente da estrutura, devido à dinâmica da estrutura natural durante a imagem. Em condições experimentais subótimas, as informações estruturais/dinâmicas extraídas não refletem fielmente as propriedades intrínsecas do objeto em estudo.
Uma vez selecionados os principais parâmetros experimentais, os conjuntos de dados podem ser produzidos para as estruturas intracelulares de destino. Para macropinossomos, após 20 min de incubação das células com dextrans de 70 kDa, séries temporâneas das estruturas intracelulares rotuladas foram adquiridas em diferentes pontos de tempo após o tratamento, de 30 min até aproximadamente 180 min. Curiosamente, é detectada uma mudança gradual nas propriedades estruturais e dinâmicas dos macropinossomos durante o tráfico (Figura 3; distribuições de σ02, Dm, α e N para macropinossos são relatadas nas parcelas à esquerda). Embora não sejam detectadas mudanças óbvias na difusividade local (Dm) de macropinossomos durante o tráfico, tanto o tamanho característico (σ02) quanto o modo geral de movimento (α) evoluem no tempo.
Note-se, uma diminuição no tamanho médio dos macropinossmos é observada durante o tráfico (Figura 3A, à esquerda), juntamente com um aumento concomitante na natureza subdiffusiva de seu movimento (ou seja, denotado como uma diminuição nos valores α, Figura 3C, painel esquerdo). Além disso, o número de macropinossomos foi extraído de cada aquisição: os resultados, relatados na Figura 3D, painel esquerdo, revelam claramente um aumento no número de macropinossos no tempo. Todos esses resultados estão de acordo com as expectativas, pois os macropinosos rotulados pelo Dextran devem se originar como vesículas isoladas e grandes na membrana plasmática (que também são competentes para o movimento ao longo dos componentes citosqueléticos), mas devem se comunicar gradualmente com a via endo-lyosômica composta por uma grande população de estruturas menores e aleatoriamente difusoras.
Como antecipado acima, os resultados para macropinossos contrastam com medições semelhantes realizadas em ISGs (Figura 3, coluna direita). Os grânulos de insulina não mostram uma tendência de evolução temporal dos parâmetros estruturais/dinâmicos derivados do iMSD (e seu número médio dentro da célula) na mesma janela de tempo observada para macropinossomos. Além disso, os valores característicos de σ02, Dm e α são bem diferentes dos de lisesomos, usados novamente como referência. Este resultado confirma a ideia, como antecipado acima, de que os grânulos são sondados em um "estado estacionário" no qual, a qualquer momento, as propriedades estruturais/dinâmicas médias de toda a população de ISGs permanecem inalteradas (ou seja, permanecem constantes, a menos que as condições estacionárias do estado mudem, por exemplo, devido a estímulos externos).
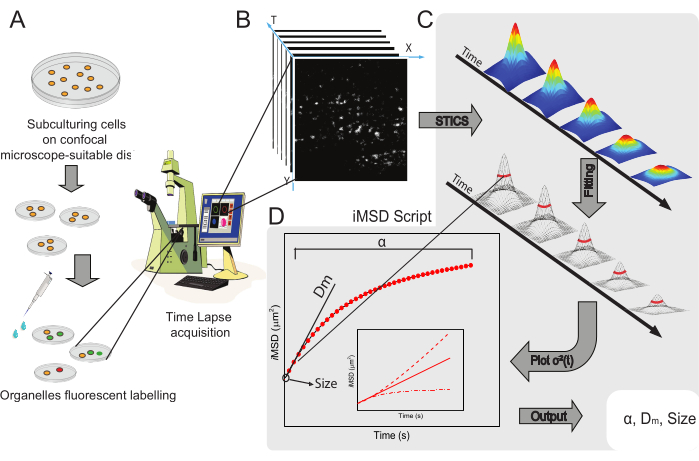
Figura 1: Fluxo de trabalho experimental. (A) As células foram banhadas 24 h (48 h para experimentos de transfecção) antes de experimentos confocal em pratos de células adequados para aplicações microscópicas. As células foram então adequadamente tratadas de acordo com o método de rotulagem (ver protocolo) para manchar a organela citoplasmática de interesse. (B) Uma aquisição confocal típica consiste em uma pilha de imagens (lapso de tempo) de uma porção citoplasmática de uma célula viva, descrevendo a evolução temporal da dinâmica organela rotulada. (C) O filme time-lapse é analisado com um script Matlab personalizado, primeiro calculando a função de correlação de imagem e o encaixe gaussiano para plotar curvas iMSD (D) e parâmetros de montagem extraídos relacionados descrevendo parâmetros de dinâmica estrutural de organelas imageadas. Abreviaturas: iMSD = deslocamento quadrado médio derivado por imagem; STICS = espectroscopia de correlação de imagem espesso; α = coeficiente anômulo de difusão; Dm = difusividade local; σ2(τ) = variância. Clique aqui para ver uma versão maior desta figura.
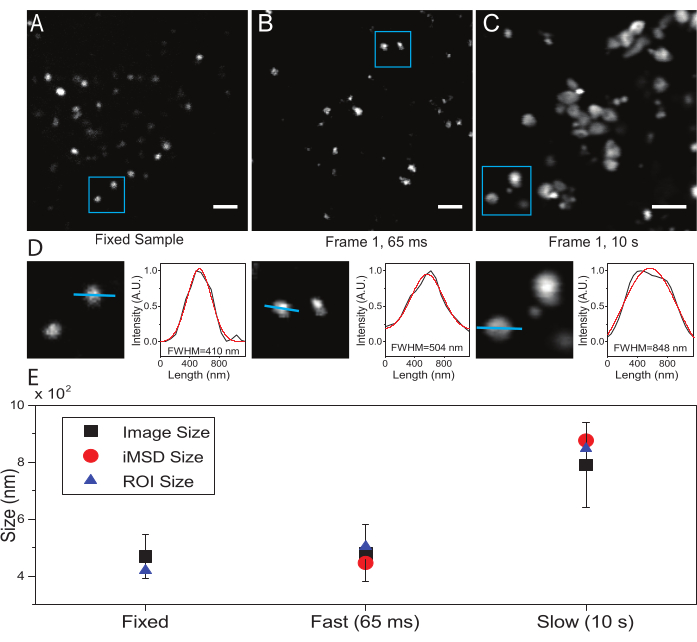
Figura 2: Parâmetros experimentais adequados. (A) Imagem exemplar de lisesomos manchados em uma amostra fixa. Barra de escala = 2 μm. (B) O primeiro quadro de uma pilha de imagens de lisesomos manchados em uma célula viva, adquirido com os parâmetros apropriados. Resolução temporal: 65 ms/quadro. Barra de escala = 2 μm. (C) O primeiro quadro de uma pilha de imagens de lysosos em uma célula viva, adquiridas em baixa velocidade: deformação artefatofato do tamanho aparente de lysososome devido ao movimento da organela durante a imagem é visível. Resolução temporal: 10 s/quadro. Barra de escala = 2 μm. (D) Exemplo de cálculo de tamanho para lysososomes imaged em um ROI azul de (A), (B) e (C). O perfil de intensidade ao longo da linha azul foi equipado com uma função gaussiana para recuperar o FWHM, ou seja, uma estimativa de tamanho spot. Os valores FWHM são reportados para cada montagem. (E) Representação gráfica dos valores de tamanho obtidos pela análise de imagem descrita no painel (D) para todos os lysosomos imaged (quadrado preto, valor médio e desvio padrão), para lisesosomes dentro do ROI azul (triângulo azul) e recuperados pela análise iMSD (círculo vermelho). Este número é de 22. Abreviaturas: ROI = região de interesse; FWHM = largura total a meio máximo; iMSD = deslocamento quadrado médio derivado de imagem. Clique aqui para ver uma versão maior desta figura.
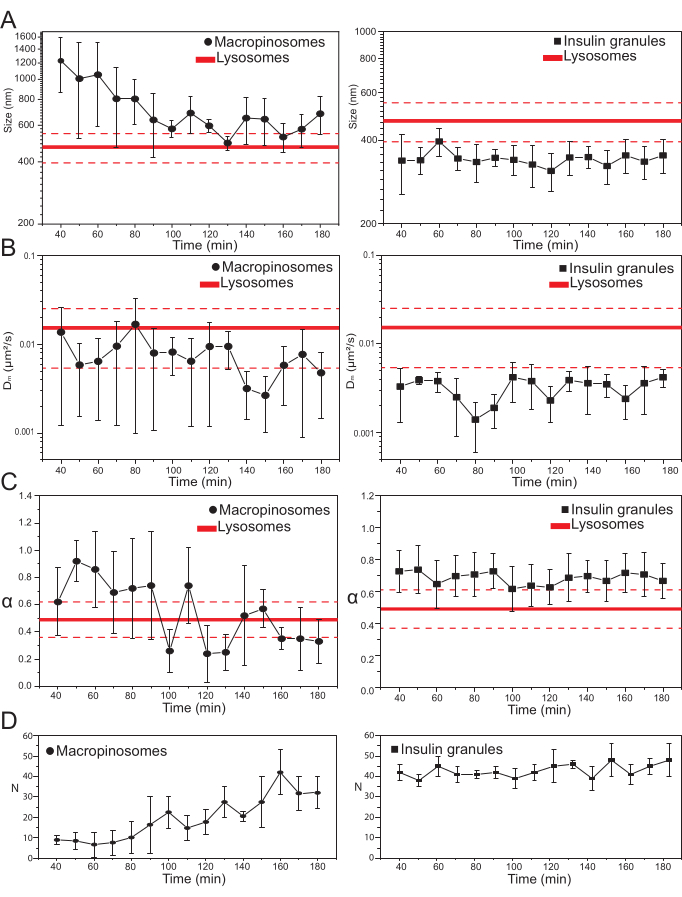
Figura 3: Evolução temporal das organelas rotuladas. (A) Parcelas de valores de tamanho extraídos pelo iMSD versus progressão de tempo de aquisições subsequentes representadas como uma média de valores medidos em aquisições realizadas em uma janela de tempo de 10 minutos. À esquerda, redução progressiva do tamanho médio dos macropinossomos (círculos pretos) e à direita, o tamanho invariante de granulos secretos de insulina (quadrados pretos) em comparação com os lysososomes, representados como valor médio de tamanho (linha vermelha mais espessa) ± desvio padrão (linhas vermelhas tracejadas). (B) e (C) Progressão de tempo de Dm e α coeficientes para macropinossomos (esquerda) e grânulos de insulina (direita) extraídos pela análise iMSD. (D) Evolução temporal dos números de macropinossos rotulados e grânulos de insulina medidos no primeiro quadro de cada filme de lapso de tempo adquirido. Abreviaturas: iMSD = deslocamento quadrado médio derivado por imagem; α = coeficiente anômulo de difusão; Dm = difusividade local, N = número. Clique aqui para ver uma versão maior desta figura.
| Organela | Rotulagem | Linha celular | Tamanho (nm) | Dm ( × 10-3 μm2/s) | α | N | Ref. | ||
| Endosome precoce (EE) | CellLight Early Endosome GFP | Hela | 395±74 | 3.0±2.4 | 1.02±0.20 | 40 | 10 | ||
| Endosome Tardio (LE) | CellLight Late Endosome GFP | Hela | 693±102 | 15.4±10.6 | 0,57±0.16 | 58 | 10 | ||
| Lysosome (LY) | LysoTracker DND-99 | Hela | 471±76 | 15.3±9.0 | 0,49±0.13 | 143 | 10, 14 | ||
| Caveola (CAV) | Caveolin-EGFP | Hela | 405±49 | 3.1±1.8 | 1.00±0.22 | 15 | 10 | ||
| Vescicle Revestido de Clathrin (CCV) | Transferrin-Alexa 488 | Hela | 513±62 | 16.2±9.9 | 0,48±0.17 | 33 | 10 | ||
| Grânulo de insulina (IG) | C-peptídeo-EGFP | INS-1E | 335±56 | 3.0±1.7 | 0,70±0.14 | 107 | 11 | ||
| Macropinosome precoce (EMCR) | Fluoresceíno-Dextran 70 kDa | Hela | 979±423 | 8.3±9 | 0,79±0.27 | 36 | 10 | ||
| Macropinoso intermediário (IMCR) | Fluoresceíno-Dextran 70 kDa | Hela | 702±180 | 13.7±19.9 | 0,60±0.38 | 29 | 10 | ||
| Macropinosome tardio (LMCR) | Fluoresceíno-Dextran 70 kDa | Hela | 592±127 | 5.8±4.7 | 0.39±0.21 | 21 | 10 | ||
Tabela 1: Parâmetros estruturais e dinâmicos extraídos por MSD. A tabela mostra os valores de tamanho, Dm e α coeficiente medido para diferentes organelas, especificando estratégias de rotulagem, a linha celular utilizada e o número de aquisições analisadas. Os valores são relatados como ± desvio padrão. Abreviaturas: iMSD = deslocamento quadrado médio derivado por imagem; α = coeficiente anômulo de difusão; Dm = difusividade local, N = número; GFP = proteína fluorescente verde; EGFP = proteína fluorescente verde aprimorada.
Arquivo Suplementar 1: Detalhes sobre a derivação e análise do traço iMSD. Clique aqui para baixar este Arquivo.
Suporte ao arquivo 1: Clique aqui para baixar este Arquivo.
Discussão
As propriedades e vantagens do iMSD são evidentes quando comparadas com as técnicas disponíveis para recuperar informações análogas. Para informações estruturais, a escolha preferida é a análise de microscopia eletrônica de transmissão (TEM). Por este método, detalhes ultraestruturais em resolução molecular e até além podem ser recuperados, mesmo para nanoestruturas subcelulares. No entanto, a peculiar resolução espacial do TEM é alcançada em detrimento das informações na dimensão temporal, o que é de interesse aqui. Para compensar isso, os recentes avanços nas tecnologias de imagem de células vivas são de particular interesse. Estes incluem novos marcadores fluorescentes com desempenhos aumentados (por exemplo, brilho e fotoestabilidade), procedimentos de rotulagem otimizados e detectores mais sensíveis. Além disso, ferramentas analíticas estão disponíveis para abordar tanto estruturalmente (por exemplo, 'tamanho' por análise baseada em phasor de espectroscopia de correlação de imagem local, PLICS23, agregação/oligomerização pela análise Number&Brightness24) e dinâmica (por exemplo, lei de difusão por rastreamento de partículas únicas, ou seja, (SPT)25,26,27,28 ) parâmetros na escala subcelular. O método SPT permite acesso direto à trajetória do objeto e ao seu MSD. No entanto, a desvantagem é a necessidade de uma baixa densidade da sonda e rótulos muito brilhantes e muitas trajetórias de objeto único a serem medidas para satisfazer critérios estatísticos. Com relação à resolução temporal da medição, sondas inorgânicas e fotostíveis (por exemplo, pontos quânticos ou nanopartículas metálicas) podem aumentar o desempenho do SPT, mas em detrimento de procedimentos complexos de produção e rotulagem.
Em comparação com esses padrões, o método iMSD descrito aqui mostra algumas vantagens fundamentais. Primeiro, essa abordagem pode ser usada em conjunto com tags fluorescentes relativamente fracas, como proteínas fluorescentes geneticamente codificadas (por exemplo, a aplicação aos ISGs). Assim, em comparação com o SPT, é alcançada uma maior resolução temporal (utilizando o mesmo rótulo) devido à menor quantidade de fótonsnecessários 8. Em segundo lugar, o método iMSD é limitado apenas pela resolução temporal, mas não pela difração. De fato, apesar da configuração óptica limitada à difração utilizada, deslocamentos moleculares médios mesmo abaixo do limite de difração podem ser medidos, como já demonstrado para fluxos moleculares usando STICS29. A resolução real na medição dos deslocamentos depende de quão precisamente (em termos de sinal para ruído) a função de correlação pode ser medida, explicando assim por que não é limitada pela difração. Assim, parece claro que o deslocamento mínimo que pode ser medido depende da difusividade do objeto de interesse e da resolução temporal da configuração da imagem.
Nesse sentido, é importante considerar que a aplicação a nanoestruturas subcelulares, como macropinossomos ou grânulos de insulina, com um microscópio de varredura a laser é ótima: a velocidade de digitalização disponível é significativamente maior do que a dinâmica do objeto de interesse. Nesse caso, o movimento dos objetos durante a aquisição é insignificante, e a função de correlação pode ser aproximada por uma função gaussiana. Finalmente, a abordagem iMSD pode ser facilmente aplicada a uma ampla gama de configurações comerciais de microscopia óptica com base em varredura raster ou imagens baseadas em câmeras de campo largo, sem necessidade de calibração do sistema (necessário apenas se uma estimativa precisa do tamanho das partículas precisar ser alcançada). Um parâmetro importante para o método funcionar é a amostragem espacial adequada. Como regra geral, para alcançar uma convergência satisfatória do algoritmo de montagem, o tamanho mínimo da região de interesse para imagem deve ser pelo menos 3 vezes maior do que o deslocamento máximo de juros.
Em conclusão, o método iMSD requer apenas um microscópio equipado para aquisição rápida. A estrutura de interesse pode ser marcada para qualquer fluoróforo geneticamente codificado ou orgânico, permitindo assim imagens multicanais. Prevê-se que a análise cross-iMSD será usada em um futuro próximo para selecionar subpopulações de nanoestruturas subcelulares e revelar suas interações e co-difusão dentro da célula, sendo esta última um tópico quente na biofísica celular. Se algum detalhe for perdido pela análise do iMSD, isso certamente está relacionado com a grande quantidade de informações moleculares dentro de nanoestruturas subcelulares dinâmicas. Essas informações são inevitavelmente mediadas durante a medição devido à má resolução temporal. Teoricamente, porém, não há limite técnico devido à possibilidade de recuperação de informações moleculares, desde que velocidades de aquisição suficientes possam ser alcançadas8. Devido às melhorias contínuas na velocidade/sensibilidade do detector e tecnologias de imagem, prevê-se que informações sobre todo o compartimento subcelular e seus constituintes moleculares serão extraídas de um único conjunto de dados.
Divulgações
Os autores não têm conflito de interesses para declarar.
Agradecimentos
Este trabalho recebeu financiamento do Conselho Europeu de Pesquisa (ERC) no âmbito do Programa de Pesquisa e Inovação Horizon 2020 da União Europeia (acordo de concessão no 866127, projeto CAPTUR3D).
Materiais
| Name | Company | Catalog Number | Comments |
| 100x Penicillin-Streptomycin-Glutamine | Gibco | 10378-016 | Cell medium supplement |
| C-peptide-EGFP | Plasmid | ||
| DMEM High Glucose | Gibco | 31053028 | Cell medium (HeLa) |
| FBS | Gibco | 10082147 | Cell medium supplement |
| Fluorescein isothiocyanate-dextran 70 kDa | Sigma Aldrich | 46945-100MG-F | Reagent |
| HeLa | ATCC | CCL-61 | Cell Line |
| Lipofectamine 2000 | TermoFisher | 11668019 | Trasfection reagent |
| Lysotracker Red DND-99 | Gibco | L7528 | Reagent |
| Matlab | MathWork | Software | |
| Microscope-suitable cell dishes | Willco | GWSt-3522 | Petri dishes |
| Olympus FV1000 | Olympus Japan | Confocal microscope | |
| RPMI 1640 | Gibco | 11835063 | Cell medium (INS-1E) |
Referências
- Murphy, J. E., Padilla, B. E., Hasdemir, B., Cottrell, G. S., Bunnett, N. W. Endosomes: a legitimate platform for the signaling train. Proceedings of the National Academy of Sciences of the United States of America. 106 (42), 17615-17622 (2009).
- Mosesson, Y., Mills, G. B., Yarden, Y. Derailed endocytosis: an emerging feature of cancer. Nature Reviews Cancer. 8 (11), 835-850 (2008).
- Mellman, I., Yarden, Y. Endocytosis and cancer. Cold Spring Harbor Perspectives in Biology. 5 (12), 016949 (2013).
- Di Fiore, P. P. Endocytosis, signaling and cancer, much more than meets the eye. Preface. Molecular Oncology. 3 (4), 273-279 (2009).
- Bogan, J. S., Xu, Y., Hao, M. Cholesterol accumulation increases insulin granule size and impairs membrane trafficking. Traffic. 13 (11), 1466-1480 (2012).
- Ballabio, A., Gieselmann, V. Lysosomal disorders: From storage to cellular damage. Biochimica et Biophysica Acta. 1793 (4), 684-696 (2009).
- Hu, Y. -. B., Dammer, E. B., Ren, R. -. J., Wang, G. The endosomal-lysosomal system: from acidification and cargo sorting to neurodegeneration. Translational Neurodegeneration. 4, 18 (2015).
- Di Rienzo, C., Gratton, E., Beltram, F., Cardarelli, F. Spatiotemporal fluctuation analysis: a powerful tool for the future nanoscopy of molecular processes. Biophysical Journal. 111 (4), 679-685 (2016).
- Di Rienzo, C., Gratton, E., Beltram, F., Cardarelli, F. Fast spatiotemporal correlation spectroscopy to determine protein lateral diffusion laws in live cell membranes. Proceedings of the National Academy of Sciences of the United States of America. 110 (30), 12307-12312 (2013).
- Di Rienzo, C., Gratton, E., Beltram, F., Cardarelli, F. From fast fluorescence imaging to molecular diffusion law on live cell membranes in a commercial microscope. Journal of Visualized Experiments: JoVE. (92), e51994 (2014).
- Digiacomo, L., et al. Dynamic fingerprinting of sub-cellular nanostructures by image mean square displacement analysis. Scientific Reports. 7 (1), 14836 (2017).
- Durso, W., et al. Lysosome dynamic properties during neuronal stem cell differentiation studied by spatiotemporal fluctuation spectroscopy and organelle tracking. International Journal of Molecular Sciences. 21 (9), 3397 (2020).
- Ferri, G., et al. Insulin secretory granules labelled with phogrin-fluorescent proteins show alterations in size, mobility and responsiveness to glucose stimulation in living β-cells. Scientific Reports. 9 (1), 2890 (2019).
- Durso, W., D'Autilia, F., Amodeo, R., Marchetti, L., Cardarelli, F. Probing labeling-induced lysosome alterations in living cells by imaging-derived mean squared displacement analysis. Biochemical and Biophysical Research Communications. 503 (4), 2704-2709 (2018).
- Digiacomo, L., Digman, M. A., Gratton, E., Caracciolo, G. Development of an image Mean Square Displacement (iMSD)-based method as a novel approach to study the intracellular trafficking of nanoparticles. Acta Biomaterialia. 42, 189-198 (2016).
- Swanson, J. A., Watts, C. Macropinocytosis. Trends in Cell Biology. 5 (11), 424-428 (1995).
- Jones, A. T. Macropinocytosis: searching for an endocytic identity and role in the uptake of cell penetrating peptides. Journal of Cellular and Molecular Medicine. 11 (4), 670-684 (2007).
- Falcone, S., et al. Macropinocytosis: regulated coordination of endocytic and exocytic membrane traffic events. Journal of Cell Science. 119, 4758-4769 (2006).
- Kerr, M. C., et al. Visualisation of macropinosome maturation by the recruitment of sorting nexins. Journal of Cell Science. 119, 3967-3980 (2006).
- Rorsman, P., Renstrom, E. Insulin granule dynamics in pancreatic beta cells. Diabetologia. 46 (8), 1029-1045 (2003).
- Di Rienzo, C., Piazza, V., Gratton, E., Beltram, F., Cardarelli, F. Probing short-range protein Brownian motion in the cytoplasm of living cells. Nature Communications. 5 (1), 5891 (2014).
- Ferri, G., et al. Time-lapse confocal imaging datasets to assess structural and dynamic properties of subcellular nanostructures. Scientific Data. 5 (1), 180191 (2018).
- Scipioni, L., Gratton, E., Diaspro, A., Lanzanò, L. Phasor analysis of local ICS detects heterogeneity in size and number of intracellular vesicles. Biophysical Journal. 111 (3), 619-629 (2016).
- Digman, M. A., Dalal, R., Horwitz, A. F., Gratton, E. Mapping the number of molecules and brightness in the laser scanning microscope. Biophysical Journal. 94 (6), 2320-2332 (2008).
- Li, C. H., Bai, L., Li, D. D., Xia, S., Xu, T. Dynamic tracking and mobility analysis of single GLUT4 storage vesicle in live 3T3-L1 cells. Cell Research. 14 (6), 480-486 (2004).
- Donovan, K. W., Bretscher, A. Tracking individual secretory vesicles during exocytosis reveals an ordered and regulated process. Journal of Cell Biology. 210 (2), 181-189 (2015).
- Westphal, V., et al. Video-rate far-field optical nanoscopy dissects synaptic vesicle movement. Science. 320 (5873), 246-249 (2008).
- Tabei, S. M. A., et al. Intracellular transport of insulin granules is a subordinated random walk. Proceedings of the National Academy of Sciences of the United States of America. 110 (13), 4911-4916 (2013).
- Hebert, B., Costantino, S., Wiseman, P. W. Spatiotemporal image correlation spectroscopy (STICS) theory, verification, and application to protein velocity mapping in living CHO cells. Biophysical Journal. 88 (5), 3601-3614 (2005).
Reimpressões e Permissões
Solicitar permissão para reutilizar o texto ou figuras deste artigo JoVE
Solicitar PermissãoThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Todos os direitos reservados