É necessária uma assinatura da JoVE para visualizar este conteúdo. Faça login ou comece sua avaliação gratuita.
Method Article
Padronização de um ensaio citométrico de esferas baseado em anticorpos contra gema de ovo
Neste Artigo
Resumo
Este protocolo descreve uma metodologia para a preparação de esferas de látex para ensaios utilizando anticorpos IgY para detecção de antígenos.
Resumo
Os imunoensaios são testes importantes para a detecção de inúmeros alvos moleculares. Dentre os métodos atualmente disponíveis, o ensaio citométrico de contas tem ganhado destaque nas últimas décadas. Cada microesfera lida pelo equipamento representa um evento de análise da capacidade de interação entre as moléculas em teste. Milhares desses eventos são lidos em um único ensaio, garantindo alta precisão e reprodutibilidade do ensaio. Essa metodologia também pode ser utilizada na validação de novos insumos, como anticorpos IgY, para o diagnóstico de doenças. Esses anticorpos são obtidos através da imunização das galinhas com o antígeno de interesse e, em seguida, da extração da imunoglobulina da gema dos ovos dos animais; Portanto, este é um método indolor e altamente produtivo para a obtenção dos anticorpos. Além de uma metodologia para a validação de alta precisão da capacidade de reconhecimento de anticorpos deste ensaio, este trabalho também apresenta um método para extração desses anticorpos, determinação das melhores condições de acoplamento para os anticorpos e esferas de látex e determinação da sensibilidade do teste.
Introdução
Dentre as técnicas de imunoensaio voltadas para o diagnóstico de doenças, o ensaio citométrico de contas tem emergido como uma abordagem altamente sensível e confiável, pois permite a análise de milhares de partículas em um único ensaio1. Essa técnica, além de apresentar alta produtividade e permitir a utilização de menores volumes de amostras, também apresenta grande flexibilidade, pois permite a detecção de diversas moléculas, como citocinas, moléculas de adesão, isotipos de anticorpos eproteínas2,3.
Diferentes partículas são utilizadas para o desenvolvimento desses ensaios, entre elas esferas de látex, que são um insumo eficaz e de baixo custo. Estas podem apresentar modificações em sua superfície, como a presença de grupos funcionais ou proteínas que permitem o acoplamento covalente ou não covalente de determinadas moléculas 3,4,5.
Esses imunoensaios usam componentes como antígenos e anticorpos para realizar a detecção de marcadores de doenças e comumente requerem anticorpos de mamíferos como camundongos, coelhos e cabras. Isso gera problemas relacionados a questões éticas, uma vez que a imunização de mamíferos geralmente requer muitos animais para obter um bom rendimento, bem como a realização frequente de procedimentos que levam ao sofrimento dos animais 6,7. Uma alternativa a isso é o uso de anticorpos IgY isolados das gemas de ovos de galinhas imunizadas, uma vez que altas concentrações dos anticorpos específicos contra os antígenos inoculados podem ser encontradas nas gemas; A produção de um frango equivale à produção de 4,3 coelhos ao longo de um ano 6,7.
Assim, o objetivo deste protocolo é fornecer um método para avaliar anticorpos IgY obtidos de gemas de ovo de galinha usando citometria de fluxo com esferas de látex. Para isso, propomos um método de padronização para um imunoensaio citométrico de esferas em formato sanduíche utilizando esferas de látex. Como modelo, foram utilizados anticorpos IgY direcionados ao antígeno II da proteína II rica em histidina do Plasmodium falciparum (IgY-Pf HRP2). Descrevemos um método para extração dos anticorpos, discutimos os passos críticos para a definição da concentração de acoplamento destes aos cordões de látex e apresentamos uma avaliação do limite de detecção do antígeno. A alta acurácia da citometria de fluxo, aliada ao baixo custo das esferas de látex, tornam esta técnica aplicável para a análise de ferramentas de imunoensaio, como anticorpos e antígenos. Este método pode ser utilizado para a detecção de diversos alvos.
Protocolo
NOTA: Consulte a Tabela de Materiais para obter detalhes relacionados a todos os materiais, reagentes e instrumentos usados neste protocolo.
1. Extração de IgY de gemas de ovo
- Higienização dos ovos
- Mergulhe os ovos (recém-postos ou até 4 dias após a colocação, da linhagem Gallus gallus Dekalb White) em uma solução diluída a 0,2% de hipoclorito de sódio, enxágue rapidamente em água corrente e limpe suavemente para uso posterior ou imediato.
NOTA: Se não for utilizado imediatamente, manter a 4 °C até 15 dias.
- Mergulhe os ovos (recém-postos ou até 4 dias após a colocação, da linhagem Gallus gallus Dekalb White) em uma solução diluída a 0,2% de hipoclorito de sódio, enxágue rapidamente em água corrente e limpe suavemente para uso posterior ou imediato.
- Separação das gemas
- Quebre o ovo com cuidado e separe a gema da clara com a ajuda de um separador de gema.
- Retire o excesso de branco com a ajuda de papel de filtro. Perfurar a gema e recolher o seu interior num tubo cónico de 50 ml. Conservar a gema a -20 °C durante, pelo menos, 24 h antes da utilização.
OBS: Durante esses experimentos (dados não mostrados), observou-se que o uso de gemas não congeladas anteriormente dificultou o isolamento de imunoglobulinas da porção lipídica das gemas.
- Acidificação das gemas
- Descongelar a gema armazenada e diluí-la na proporção de 1:10 em PBS 1 mM. Ajustar o pH da solução para 5 com 1 N HCl e incubar a solução a 4 °C durante 6-24 horas.
- Centrifugar a solução a 3.000 × g por 40 min, recuperar o sobrenadante e filtrá-lo com um filtro de celulose de 0,7 mm.
- Precipitação de lipídios com ácido caprílico
- Reajustar o pH dos sobrenadantes para 5 e adicionar o ácido caprílico (concentração inicial de ≥98%) a uma concentração final de 8,7% sob agitação constante por 30 min a 4 °C.
NOTA: O volume do sobrenadante pode variar em função da massa lipídica precipitada na etapa 1.3.2. Assim, por exemplo, 3,107 mL de ácido caprílico devem ser adicionados a 35 mL do sobrenadante obtido após filtração. - Centrifugar as amostras por 15 min a 18.600 × g e separar o sobrenadante do material precipitado.
- Reajustar o pH da solução para 7,4 usando NaOH 1 M, quantificar os anticorpos usando o ensaio de Bradford8 e armazenar os anticorpos a -20 °C até o momento de uso.
OBS: Os anticorpos foram obtidos na concentração de 1 μg/μL, o que foi verificado por meio de um gel de SDS-PAGE a 12%.
- Reajustar o pH dos sobrenadantes para 5 e adicionar o ácido caprílico (concentração inicial de ≥98%) a uma concentração final de 8,7% sob agitação constante por 30 min a 4 °C.
2. Curva de saturação de anticorpos IgY contra esferas de látex
- Acoplamento das esferas aos anticorpos IgY
- Adicionar 21 μL de 1-etil-3-(3-dimetilaminopropil)carbodiimida (EDC, concentração inicial de 367 mM) e 21 μL de N-hidroxisuccinimida (NHS, concentração inicial de 50 mM) a 21 μL de esferas de látex (4% p/v) e ajustar para um volume final de 2,1 mL com PBS filtrado de 10 mM.
OBS: A faixa de pH da solução de PBS deve estar entre 7,2 e 7,4, uma vez que neste trabalho foi observada uma alteração negativa no acoplamento e nas demais etapas quando se utiliza uma solução fora desta faixa. - Incubar a 22 °C com agitação rápida durante 3 h.
- Adicionar 4 μg, 2 μg, 1 μg, 0,5 μg, 0,25 μg, 0,125 μg e 0 μg do anticorpo de captura previamente extraído IgY-PfHRP2 (ver passo 1.4.3) a diferentes microtubos contendo 100 μL da solução descrita no passo 2.1.1 (concentração final do cordão de 0,04%) e incubar nas mesmas condições descritas no passo 2.1.2 durante 16 horas.
- Centrifugar as amostras a 857 × g a 15 °C por 5 min, descartar os sobrenadantes e lavar as esferas de látex duas vezes com 500 μL de PBS filtrado 10 mM (0,008% de concentração final do cordão) usando ciclos de centrifugação e ressuspensão.
OBS: Não ultrapassam 857 × g, pois neste trabalho, observou-se que além desta velocidade as contas sofrem deformações que alteram negativamente o resultado do ensaio.
- Adicionar 21 μL de 1-etil-3-(3-dimetilaminopropil)carbodiimida (EDC, concentração inicial de 367 mM) e 21 μL de N-hidroxisuccinimida (NHS, concentração inicial de 50 mM) a 21 μL de esferas de látex (4% p/v) e ajustar para um volume final de 2,1 mL com PBS filtrado de 10 mM.
- Bloqueando as contas
- Ressuspender as amostras em 1 mL de tampão de bloqueio (0,004% de concentração final do talão) (PBS filtrado 10 mM + albumina de soro bovino, BSA, 5%) e incubar nas mesmas condições descritas na etapa 2.1.2 por 2 h.
- Após o bloqueio, lave conforme descrito na etapa 2.1.4 e ressuspenda em buffer PBS de 10 mM.
- Incubação com anticorpos secundários antifrango marcados com Alexa Fluor 488
- Adicionar 100 μL de anticorpo antifrango fluorescente (2 mg/mL) diluído a 1:2.000 em PBS 10 mM + BSA 0,5% a cada microtubo, conforme descrito na etapa 2.1.3.
- Incubar as amostras conforme descrito no passo 2.1.2, desta vez no escuro, durante 30 minutos.
- Lavar as contas como no passo 2.1.4 e voltar a suspender com 250 μL de (0,016% de concentração final do talão) filtrado 10 mM PBS. Efectuar a leitura do citómetro de fluxo conforme descrito na secção 5.
OBS: A partir dos dados de porcentagem de fluorescência obtidos, observar o ponto inicial de formação do platô (1 μg, como observado neste estudo). Recomendamos o uso do segundo ponto do platô (2 μg, como observado aqui) para os próximos passos (Figura 1).
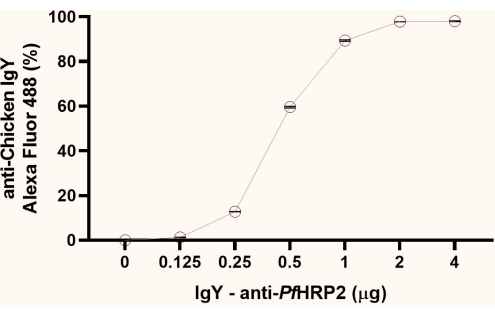
Figura 1: Gráfico da análise por citometria de fluxo para determinação do ponto de saturação do acoplamento do anticorpo IgY-Pf HRP2 às esferas de látex. O eixo x representa a concentração de anticorpos e o eixo Y representa a porcentagem de fluorescência obtida. teste de Kruskal-Wallis, p < 0,0033. Clique aqui para ver uma versão maior desta figura.
3. Ensaio de citometria de fluxo baseado em esferas de látex para detecção de antígenos
- Após a determinação do ponto de saturação dos anticorpos IgY para as esferas de látex, realizar novamente o processo de ativação do cordão de acordo com o passo 2.1.1.
- Emparelhar as esferas na concentração de saturação observada (conforme descrito no passo 2.1.3) e incubar de acordo com o passo 2.1.2.
NOTA: Nos ensaios realizados com o anticorpo IgY-Pf HRP2, a condição de saturação foi de 2 μg para cada 1 μL de esferas de látex.
- Emparelhar as esferas na concentração de saturação observada (conforme descrito no passo 2.1.3) e incubar de acordo com o passo 2.1.2.
- Bloqueie e lave as contas de acordo com o passo 2.2.
- Incubação com o antígeno
- Para determinar o limite de detecção, distribuir o equivalente a 100 μL da preparação de esferas bloqueadas em tubos contendo diferentes quantidades da proteína recombinante Pf HRP2 (1 μg/mL) (r PfHRP2, 10 μg, 1 μg, 0,1 μg, 0,01 μg, 0,001 μg, 0,0001 μg e 0 μg) diluída em 10 mM PBS + 0,5% BSA em triplicata.
OBS: Esta proteína recombinante foi desenvolvida no trabalho de Sousa et al.9. - Incubar as soluções de esferas com a proteína rPfHRP2, conforme descrito no passo 2.1.2, durante 1 h.
- Efectuar as lavagens descritas no ponto 2.1.4 e eliminar o sobrenadante após centrifugação.
- Para determinar o limite de detecção, distribuir o equivalente a 100 μL da preparação de esferas bloqueadas em tubos contendo diferentes quantidades da proteína recombinante Pf HRP2 (1 μg/mL) (r PfHRP2, 10 μg, 1 μg, 0,1 μg, 0,01 μg, 0,001 μg, 0,0001 μg e 0 μg) diluída em 10 mM PBS + 0,5% BSA em triplicata.
- Incubação com o anticorpo primário
- Adicionar 2 μg de anticorpo IgG de camundongo contra a proteína rPfHRP2 diluída em 10 mM PBS + 0,5% BSA para um volume final de 100 μL em cada amostra. Incubar as amostras conforme descrito no passo 2.1.2 e eliminar o sobrenadante após a última centrifugação.
OBS: Este anticorpo foi desenvolvido no trabalho de Sousa et al.9.
- Adicionar 2 μg de anticorpo IgG de camundongo contra a proteína rPfHRP2 diluída em 10 mM PBS + 0,5% BSA para um volume final de 100 μL em cada amostra. Incubar as amostras conforme descrito no passo 2.1.2 e eliminar o sobrenadante após a última centrifugação.
- Incubação com o anticorpo secundário
- Adicionar 100 μL de anticorpo anti-camundongo fluorescente (2 mg/mL) diluído a 1:2.000 em PBS 10 mM + BSA 0,5% a cada amostra. Incubar conforme descrito na etapa 2.1.2 e ressuspender em 250 μL (0,016% de concentração final do cordão) de PBS filtrado de 10 mM. Realizar a leitura de acordo com a seção 5.
4. Leitura do citômetro de fluxo das amostras
- Configuração da citometria: Alinhamento dos parâmetros ópticos do citômetro acoplado a um computador
- Ligue o computador e o citômetro de fluxo e aguarde alguns minutos para que o equipamento se conecte ao computador.
- Clique no software de citometria instalado no computador e faça login nele. No espaço de trabalho do software, selecione Citômetro | Inicialização | Modo de limpeza | Fluidos SIT.
NOTA: Bolhas de ar e obstruções devem ser removidas durante o processo de início do citômetro antes da aquisição da amostra.
- Controle de qualidade
- Use o reagente de controle de qualidade para verificar as tensões dos tubos fotomultiplicadores e avaliar a sensibilidade do citômetro.
- Coloque o reagente de configuração do citômetro e as esferas de rastreamento em um tubo de poliestireno tampado de 12 mm x 75 mm.
- Misture suavemente o tubo por vórtice.
- Preparo das contas de suspensão
- Para definir a linha de base, adicionar 0,5 mL de diluente (PBS filtrado 10 mM, pH 7) e três gotas de contas ao tubo de poliestireno tampado de 12 mm x 75 mm. Vórtice o tubo suavemente antes de usar.
- No espaço de trabalho do software do citômetro, selecione Citômetro | CST e aguarde até que o citômetro se desconecte da interface do software do citômetro e conecte-se à interface CS&T. Observe a seguinte mensagem na barra de status do software do citômetro na parte inferior da tela: Citômetro desconectado.
- Use o tubo de poliestireno tampado de 12 mm x 75 mm contendo o reagente de controle de qualidade e conecte-o à sonda do citômetro de fluxo.
- Verificação da configuração do citômetro
- Na janela Resumo do sistema , verifique se a configuração do citômetro é apropriada para o experimento.
- Configuração para uma verificação de desempenho
- Selecione o ID das contas de configuração correspondente ao lote de contas de pesquisa CS&T.
- Verificação de desempenho
- Conecte o tubo à sonda do citômetro de fluxo e clique na janela Controle de configuração . Selecione Verificar desempenho e clique em Executar.
- Quando a verificação de desempenho estiver concluída, aguarde até que uma caixa de diálogo seja aberta. Siga um destes procedimentos:
- Para visualizar o relatório de desempenho do citômetro , clique em Exibir relatório.
- Para concluir a verificação de desempenho e retornar à visualização de configuração do espaço de trabalho, clique em Concluir.
- Observe o resultado final da análise morfométrica e de sensibilidade à fluorescência que aparece no Resumo do Sistema | Resultado de desempenho do citômetro com o status PASSED.
- Retire o tubo do citômetro. Verifique os resultados de desempenho do citômetro exibidos na janela Resumo do sistema .
5. Análise da amostra por citometria de fluxo
- Faça login no software do citômetro.
- No espaço de trabalho do software do citômetro, selecione Citômetro | Modo de limpeza | Fluidos SIT.
- Ajuste ao espaço de trabalho do software.
- Definir a estratégia de gating com base nas características morfométricas e de fluorescência das partículas de controle negativo (esferas sem fluorescência).
- Para determinar a morfometria celular, escolha Dot Plot Plot Graphic para a análise dos parâmetros do FSC-A usando SSC-A (Figura 1A Suplementar).
- Determinar células únicas por CSC usando Gráfico de Dot Plot para a análise de SSC-H no eixo y e SSC-W no eixo x (Figura 1B Suplementar), e determinar células únicas por FSC usando Gráfico de Gráfico para a análise de FSC-H no eixo y e FSC-W no eixo x (Figura Suplementar 1C).
- Para as análises de fluorescência, escolha FL1 Dot Plot Plots Plots usando FCS-A. Use um tubo de poliestireno com tampa de 12 mm x 75 mm contendo amostras não rotuladas e amostras previamente marcadas com Alexa Fluor 488 de cor única (Figura suplementar 1D, E).
- Adquirir a amostra em citometria de fluxo.
- Utilizar um tubo de poliestireno com tampa de 12 mm x 75 mm contendo as amostras previamente marcadas. Misture o conteúdo do tubo cuidadosamente, conecte-o à sonda do citômetro de fluxo e clique com o botão esquerdo do mouse em Adquirir.
- Para definir a potência dos lasers, clique em Parâmetros, e nas opções abaixo, ajuste a tensão do FSC para 182 V e a tensão do SSC para 236 V. Para definir o limite, clique em Citômetro | Limite, e nas opções abaixo, ajuste o FSC para 500 V.
- Defina a porta de análise para caracterizar partículas por tamanho e complexidade, bem como para realizar análises de célula única.
- Para remover a autofluorescência, analise a amostra sem corante contendo apenas as esferas de látex e ajuste as tensões do detector: nas opções abaixo, ajuste a tensão do FL1 (FITC) para 332 V.
- Defina a porta de análise de fluorescência em formato quadrangular a partir do ponto negativo mostrado no gráfico de gráfico de pontos.
- Após o ajuste das análises morfométricas e fluorescentes, configure o dispositivo para 50.000 eventos: em Aquisição, clique em Registro.
Resultados
A Figura 2 fornece uma representação gráfica do processo de extração dos anticorpos IgY via acidificação, seguido de separação com ácido caprílico (Figura 2).
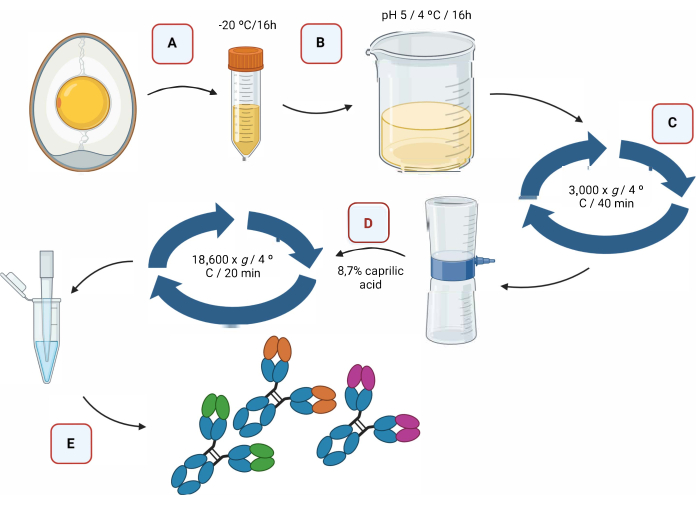
Figura 2: Representação esquemática da etapa de extração dos anticorpos IgY e separaçã...
Discussão
O método de precipitação do anticorpo IgY por redução de pH seguida de separação lipídica utilizando ácido caprílico é eficiente no isolamento de anticorpos totais sem perda de funcionalidade. O método aqui proposto é mais simples e barato do que o relatado por Redwan et al.11, que também utilizaram precipitação por acidificação e ácido caprílico, porém com um protocolo mais complexo e trabalhoso. Esse método também apresenta vantagens sobre as metodologias comumente utiliza...
Divulgações
Os autores declaram não haver conflitos de interesse com relação à pesquisa, autoria e publicação deste artigo.
Agradecimentos
Ao Programa de excelência em pesquisa básica e aplicada em saúde dos laboratórios do Instituto Leônidas e Maria Deane - ILMD/Fiocruz Amazônia-PROEP-LABS/ILMD FIOCRUZ AMAZÔNIA ("Programa de excelência em pesquisa básica e aplicada em saúde dos laboratórios do Instituto Leônidas e Maria Deane - ILMD/Fiocruz Amazônia-PROEP-LABS/ILMD FIOCRUZ AMAZÔNIA"), ao Programa de Pós-Graduação em Biotecnologia (PPGBIOTEC) da Universidade Federal do Amazonas (UFAM), à Coordenação de Aperfeiçoamento de Pessoal de Nível (CAPES) e à Fundação de Amparo à Pesquisa do Estado do Amazonas (FAPEAM) pela concessão das bolsas. A Figura 2 e a Figura 4 foram criadas com biorender.com.
Materiais
| Name | Company | Catalog Number | Comments |
| Anti-Chicken IgY (H+L), highly cross-adsorbed, CF 488A antibody produced in donkey | Sigma-Aldrich | SAB4600031 | |
| Anti-mouse IgG (H+L), F(ab′)2 | Sigma-Aldrich | SAB4600388 | |
| BD FACSCanto II | BD Biosciences | BF-FACSC2 | |
| BD FACSDiva CS&T research beads (CS&T research beads) | BD Biosciences | 655050 | |
| BD FACSDiva software 7.0 | BD Biosciences | 655677 | |
| Bio-Rad Protein Assay Dye Reagent Concentrate | Bio-Rad | #5000006 | |
| Bovine serum albumin | Sigma-Aldrich | A4503 | |
| Caprilic acid | Sigma-Aldrich | O3907 | |
| Centrifuge 5702 R | Eppendorf | Z606936 | |
| Chloride 37% acid molecular grade | NEON | 02618 NEON | |
| CML latex, 4% w/v | Invitrogen | C37253 | |
| Megafuge 8R | Thermo Scientific | TS-HM8R | |
| N-(3-Dimethylaminopropyl)-N′-ethylcarbodiimide Hydrochloride Powder (EDC) | Sigma-Aldrich | E7750-1G | |
| N-Hydroxysuccinimide (NHS) | Sigma-Aldrich | 130672-25G | |
| Phosphate buffered saline | Sigma-Aldrich | 1003335620 | |
| Sodium hydroxide | Acs Cientifica | P.10.0594.024.00.27 | |
| Sodium hypochlorite | Acs Cientifica | R09211000 | |
| Thermo Mixer Heat/Cool | KASVI | K80-120R |
Referências
- Salzer, U., Sack, U., Fuchs, I. Flow cytometry in the diagnosis and follow up of human primary immunodeficiencies. Electronic Journal of the International Federation of Clinical Chemistry and Laboratory. 30 (4), 407 (2019).
- de Figueiredo, A. M., Glória, J. C., Chaves, Y. O., Neves, W. L. L., Mariúba, L. A. M. Diagnostic applications of microsphere-based flow cytometry: A review. Experimental Biology and Medicine. 247 (20), 1852-1861 (2022).
- Morgan, E., et al. Cytometric bead array: A multiplexed assay platform with applications in various areas of biology. Clinical Immunology. 110 (3), 252-266 (2004).
- Graham, H., Chandler, D. J., Dunbar, S. A. The genesis and evolution of bead-based multiplexing. Methods. 158, 2-11 (2019).
- Kellar, K. Multiplexed microsphere-based flow cytometric assays. Experimental Hematology. 30 (11), 1227-1237 (2002).
- Schade, R., et al. Chicken egg yolk antibodies (IgY-technology): A review of progress in production and use in research and human and veterinary medicine. ATLA Alternatives to Laboratory Animals. 33 (2), 129-154 (2005).
- Xu, Y., et al. Application of chicken egg yolk immunoglobulins in the control of terrestrial and aquatic animal diseases: A review. Biotechnology Advances. 29 (6), 860-868 (2011).
- Bradford, M. M. A rapid and sensitive method for the quantitation of microgram quantities of protein utilizing the principle of protein-dye binding. Analytical Biochemistry. 72 (1-2), 248-254 (1976).
- Sousa, L. P., et al. A novel polyclonal antibody-based sandwich ELISA for detection of Plasmodium vivax developed from two lactate dehydrogenase protein segments. BMC Infectious Diseases. 14 (1), 49 (2014).
- Klimentzou, P., et al. Development and immunochemical evaluation of antibodies Y for the poorly immunogenic polypeptide prothymosin alpha. Peptides. 27 (1), 183-193 (2006).
- Redwan, E. M., Aljadawi, A. A., Uversky, V. N. Simple and efficient protocol for immunoglobulin Y purification from chicken egg yolk. Poultry Science. 100 (3), 100956 (2021).
- Lee, H. Y., Abeyrathne, E. D. N. S., Choi, I., Suh, J. W., Ahn, D. U. K. Sequential separation of immunoglobulin Y and phosvitin from chicken egg yolk without using organic solvents. Poultry Science. 93 (10), 2668-2677 (2014).
- Pauly, D., Chacana, P., Calzado, E., Brembs, B., Schade, R. IgY Technology: Extraction of chicken antibodies from egg yolk by polyethylene glycol (PEG) precipitation. Journal of Visualized Experiments. (51), e3084 (2011).
- Chang, H. M., Lu, T. C., Chen, C. C., Tu, Y. Y., Hwang, J. Y. Isolation of immunoglobulin from egg yolk by anionic polysaccharides. Journal of Agricultural and Food Chemistry. 48 (4), 995-999 (2000).
- Ko, K. Y., Ahn, D. U. Preparation of immunoglobulin Y from egg yolk using ammonium sulfate precipitation and ion exchange chromatography. Poultry Science. 86 (2), 400-407 (2007).
- Polson, A. Isolation of IgY from the yolks of eggs by a chloroform polyethylene glycol procedure. Immunological Communications. 19 (3), 253-258 (1990).
- Simonova, M. A., et al. xMAP-based analysis of three most prevalent staphylococcal toxins in Staphylococcus aureus cultures. Analytical and Bioanalytical Chemistry. 406 (25), 6447-6452 (2014).
- Sharma, P., et al. A multiplex assay for detection of staphylococcal and streptococcal exotoxins. PLoS One. 10 (8), e0135986 (2015).
- Merbah, M., et al. Standardization of a cytometric p24-capture bead-assay for the detection of main HIV-subtypes. Journal of Virological Methods. 230, 45-52 (2016).
Reimpressões e Permissões
Solicitar permissão para reutilizar o texto ou figuras deste artigo JoVE
Solicitar PermissãoExplore Mais Artigos
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Todos os direitos reservados