Для просмотра этого контента требуется подписка на Jove Войдите в систему или начните бесплатную пробную версию.
Method Article
Визуализация рецепторов эстрогена в колонах мышей с TNBS-индуцированной болезнью Крона с использованием иммунофлюоресценции
В этой статье
Резюме
Протокол представляет собой полную проверенную модель Murine, индуцированную TNBS, болезнь Крона и методы визуализации рецепторов эстрогена иммуногистохимией с использованием иммунофлюоресценции формалино-фиксированных секций толстой кишки, встроенных в парафин.
Аннотация
Болезнь Крона является наиболее диагностируется тип воспалительных заболеваний кишечника. Хроническое воспаление, развивающаяся в кишечнике, приводит к нарушению перистальции и повреждению слизистой оболочки кишечника и, кажется, связано с повышенным риском неопластической трансформации толстой кишки. Накопление доказательств указывает на то, что эстрогены и рецепторы эстрогена влияют не только на гормоночувствительные ткани, но и на другие ткани, не имеющие прямого отношения к эстрогенам, таким как легкие или толстой кишки. Здесь мы описываем протокол для успешного иммунофлуоресцентного окрашивания рецепторов эстрогена в толстой кишке, полученного от модели мурина болезни Крона, индуцированной TNBS. Предоставляется подробный протокол для индукции болезни Крона у мышей и подготовки кишечника, а также пошаговая иммуногистохимическая процедура с использованием формалино-фиксированного парафин-встроенных секций кишечника. Описанные методы не только полезны для обнаружения рецепторов эстрогена и эстроген сигнализации исследования in vivo, но также могут быть применены к другим белкам, которые могут быть вовлечены в развитие колита.
Введение
Болезнь Крона (CD) является воспалительным заболеванием кишечника (IBD) проявляется как хроническое воспаление кишечника. Этиология CD плохо понимается, но есть несколько основных факторов, которые, как представляется, несут ответственность за развитие компакт-диска, в том числе кишечной микробиоты, и генетические и экологические факторы, такие как диета или стресс1. Для лучшего понимания патогенеза болезни Крона, несколько моделей кишечного воспаления были использованы2,,3,,4,,5,,6,7. В этой статье мы представляем результаты, полученные из 2,4,6-тринитробензенсеновой сульфоновой кислоты (TNBS)-индуцированной модели murine CD.
Было документально подтверждено, что эстрогены способны модулировать хроническое воспаление кишечника8,9,10,11,12. Биологическая активность эстрогенов опосредованается cognate рецепторов, среди которых являются ядерные рецепторы эстрогена (ERs), т.е. ЭРЗ (ген ESR1) и Эр-Эра (ген ESR2), а также G13,14белка связанных рецепторов эстрогена, т.е., GPER (ген GPER1), называется Есть несколько методов для определения уровня рецепторов эстрогена, но лишь немногие из них могут быть использованы для визуализации их в кишечнике.
Иммуногистохимия (IHC) является широко используемым методом в клинических и базовых исследованиях для обнаружения определенных антигенов в клетках или тканях с флюорохром-конъюгированными антителами. IHC, как представляется, является важным методом в визуализации структуры тканей, а также в выявлении и локализации конкретных белков, которые могут иметь решающее значение для понимания развития колита. Здесь мы представляем полный и проверенный протокол для иммуногистохимической визуализации рецепторов эстрогена в кишечнике с использованием иммунофлуоресценции.
протокол
Исследования на животных проводились с согласия Местного комитета по этике (28/29/2016) в соответствии с Директивой 2010/63/ЕС Европейского парламента и Совета от 22 сентября 2010 года и институциональными рекомендациями.
1. TNBS-индуцированной морин модели болезни Крона
ПРИМЕЧАНИЕ: Этот протокол использует самцов BALB/C мышей весом 25-28 г. Животные размещаются при постоянной температуре (22-24 градусов по Цельсию) и, относительная влажность 55 и 5%, и поддерживается в 12 ч свет / темный цикл с бесплатным доступом к стандартным гранулы чау и водопроводной воды ad libitum.
- Поместите мышь в индукционную камеру и плотно закройте крышку. Анестезируйка мыши кратко с изофлуран (25% O2 с O2 скорость потока на 1,5-2 л / мин).
ПРИМЕЧАНИЕ: Дыхательная частота должна оставаться ритмичной и медленнее, чем обычно, и не должна меняться в ответ на вредный стимул. - Привить 4 мг TNBS в 0,1 мл 30% этанола в 0,9% NaCl или 0,1 мл 30% этанола в 0,9% NaCl как управление транспортным средством в дистальной толстой кишки через катетер.
ПРИМЕЧАНИЕ: Катетер должен быть тщательно введен примерно 3 см в анус. - Мониторинг мыши ежедневно с веских по два-восьмого дня для клинических параметров, включая вес тела, ректальное кровотечение, консистенцию стула и смертность.
- На восьмой день, эвтаназии мыши шейки матки дислокации.
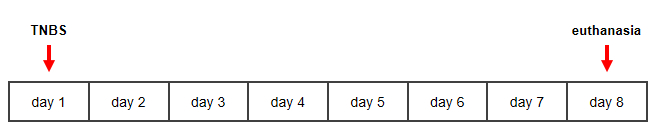
Рисунок 1: Хронология для TNBS-индуцированной модели мурина болезни Крона. Пожалуйста, нажмите здесь, чтобы просмотреть большую версию этой цифры.
2. Разделение и макроскопическая оценка толстой кишки
ПРИМЕЧАНИЕ: За день до разделения толстой кишки, разбавить 100 л антибиотика в 1 мл фосфатного буфера солине (PBS) и оставить на 4 градуса Цельсия на ночь.
- Очистите кожу над животом с помощью 75% этанола и стерильной марли.
- Вырежьте брюшную стенку от грудины до ануса с помощью стерильных ножниц и пинцета.
- Отрежьте толстую кишку как можно ближе к анусу и цекуму.
- Поместите толстую кишку на чашку Петри. Вырежьте толстую кишку вместе с анусом в конце cecum. Чистота и мыть толстой кишки 2-4 раза в холодном растворе антибиотик-PBS.
- Выполните макроскопическую оценку с помощью капика в соответствии с таблицей 1.
ПРИМЕЧАНИЕ: Ткань адгезии и эритема / кровоизлияние,фекальнаякровь и диарея- подлежат визуальной оценке.* * Ткань адгезии оценить с помощью трехточечной шкалы (0: толстой кишки без сливк ткани, 1: толстой кишки с умеренной сливки тканей, 2: толстой кишки с обширной сливки тканей); -на основании отсутствия (0) или наличия (1) эритемы/кровоизлияния, фекальной крови и диареи.
| Адгезия* | Эритема / кровоизлияние# | Фекальнаякровь | Диарея# | Длина язвы | Толщина толстой кишки | Длина толстой кишки |
| очки (0 - 2) | очки (0 - 1) | очки (0 - 1) | очки (0 - 1) | cm/points | мм/точки | cm/points |
| 0 - отсутствует | 0 - отсутствует | 0 - отсутствует | 0 - отсутствует | 0,5 см и 0,5 балла | n мм и n точки | 0 - злт;10% короче, чем контроль |
| 1 - умеренный | 1 - настоящее время | 1 - настоящее время | 0,5 - небольшой/свободный стул | 1 - от 10 до 20% короче, чем контроль | ||
| 2 - настоящее время | 1 - настоящее время | 2 - более чем на 20% короче, чем контроль |
Таблица 1: Макроскопический скоринг кишечника мышей с TNBS-индуцированной модели болезни Крона.
- Преобразуйте длину язвы в сантиметры к точечной шкале, т.е. каждый 0,5 см язвы считается 0,5 балла. Преобразуйте толщину толстой кишки в миллиметрах в точечную шкалу, т.е. каждый н мм соответствует n точкам.
- Преобразуйте длину толстой кишки в сантиметры по трехбалльной шкале. Длина толстой кишки, полученная от каждой мыши с TNBS-индуцированной болезнью Крона оценивается по отношению к средней длине толстой кишки для контрольной группы (0: lt;10% короче, чем контроль, 2: более 20% короче, чем контроль).
- Рассчитайте общий макроскопический балл в соответствии с уравнением: Общая макроскопическая оценка - слив (точки) - эритема/кровоизлияние (точки) - фекальная кровь (точки) - диарея (точки) - длина язвы (точки) - толщина толстой кишки (точки)
3. Подготовка образца толстой кишки
- Разрежьте толстой кишки на 1-2 см фрагментов и поместите каждый на губку в соответствующим образом помечены гистологические кассеты.
ПРИМЕЧАНИЕ: Губки для гистологических кассет предотвращают складывание толстой кишки во время обезвоживания и инкубации в жидком парафине. - Поместите фрагмент толстой кишки в 4% формальдегида и инкубировать, по крайней мере 24 ч при 4 градусах Цельсия.
- Подготовка и программирование процессора тканей для 1 ч инкубации в 50%, 70%, 90%, 95%, 100% этанол, ксилен/100% этанол (1:1; v/v), и ксилен только, а также по крайней мере 3 ч инкубации в жидком парафина.
ПРИМЕЧАНИЕ: Обезвоживание должно быть выполнено в возрастающих концентрациях этанола и ксилена, но концентрация этанола может быть изменена. Смесь ксилена/этанола рекомендуется, но не требуется. - Перенесите фрагмент толстой кишки в гистологическую коробку и поместите в заранее запрограммированный процессор тканей.
- Выполнить процессор ткани.
- После инкубационных ступеней поместите фрагмент толстой кишки в металлическую форму так, чтобы два конца толстой кишки оказались в вертикальном положении и заполнили треть плесени жидким парафином.
- Поместите форму в области охлаждения (-5 градусов по Цельсию) в течение нескольких секунд, а затем переместить форму в зону потепления (70 градусов по Цельсию). Поместите в нижнюю часть гистологического ящика и покройте весь фрагмент толстой кишки жидким парафином.
- Оставьте металлическую форму с фрагментом толстой кишки в парафине в течение нескольких минут в области охлаждения. Удалите металлическую форму из парафиновой блока и инкубируйте, по крайней мере, 24 ч при 4 градусах Цельсия.
- Удалите избыток парафина из блока и вставьте его в полностью автоматизированный вращающийся микротом.
ПРИМЕЧАНИЕ: Парафин блок может храниться при -20 градусов по Цельсию в течение нескольких минут до этого шага. - Разрежьте фрагмент толстой кишки на 5 мкм разделов.
- Перенесите секцию толстой кишки на водяную баню, разогретую до 40 градусов по Цельсию.
- Используйте помеченную стеклянную горку, чтобы удалить секцию толстой кишки из водяной ванны.
ПРИМЕЧАНИЕ: Секции толстой кишки плавают на воде. Положите помечены стеклянные слайд в воде под толстой кишки разделе и снять стеклянную горку тщательно. - Оставьте стеклянную горку на 24 ч при комнатной температуре. Для длительного хранения держите стеклянную горку при температуре в 4 градуса после 24 ч инкубации при комнатной температуре.
4. Иммуногистохимия с иммунофлюоресценцией окрашивания
ПРИМЕЧАНИЕ: Не позволяйте толстой кишки разделе высохнуть на любом этапе во время процедуры.
- Удалите парафин, инкубируя стеклянную горку в ксилене в течение 5 мин. Повторите этот шаг три раза.
- Поместите стеклянную горку в ксилен/100% этанол (1:1; v/v) в течение 5 мин. Повторите этот шаг три раза.
- Регидратировать секцию толстой кишки в серии снижения концентрации этанола, т.е. 70%, 50%, 30% и 10% этанола в течение 5 мин. Повторите каждый шаг три раза.
- Промыть стеклянную горку под проточной водой в течение 5 минут.
- Разогреть буфер извлечения антигена (10 мм натрия цитрат; 0,05% Tween 20, pH 6.0) до 95-98 градусов по Цельсию и нагреть стеклянный слайд в кипящем растворе извлечения антигена в течение 10 мин.
ПРИМЕЧАНИЕ: Шаг поиска антигена является необязательным, но рекомендуется. Разоблаченное решение должно быть оптимизировано в зависимости от антител, используемых в эксперименте. - Нарисуйте круг вокруг толстой кишки раздел с помощью гидрофобной ручкой.
ПРИМЕЧАНИЕ: Этот шаг является необязательным, но рекомендуется. Гидрофобная ручка предотвращает отходы реагентов, удерживая жидкость в небольшом объеме внутри отмеченного круга. - Инкубировать секцию в 3% водного раствора переоксидаза водорода в течение 10 мин.
- Вымойте в стиральном растворе (50 мм Tris-HCl, рН 7,4; 150 мМ NaCl; 0,05% Tween 20) за 5 мин.
- Инкубировать в блокирующем растворе (5% нормальной козьей сыворотки; 50 мм Tris-HCl, pH 7.4; 150 mM NaCl; 0.05% Triton X-100) за 1 ч при комнатной температуре.
ПРИМЕЧАНИЕ: В блокирующем растворе нормальная сыворотка должна быть от того же вида, что и вторичное антитело. В стадиях, когда требуется инкубация, поместите стеклянную горку в камеру влажности, чтобы предотвратить чрезмерное испарение. - Удалите блокирующий раствор и добавьте 20-50 л первичных антител против ЭРЗ, ЭРЗ или GPER, разбавленного в 1% бычьего сывороточного альбумина с 50 мм Tris-HCl, pH 7.4, 150 mM NaCl, 0.05% Triton X-100.
ПРИМЕЧАНИЕ: Рекомендуемые разбавления первичных антител показаны в таблице 2.
| Тип антител | Антитела против | Клональность | Виды хозяев | Реактивность видов | Разбавления |
| Основной | ЭРЗ | Поликлональных | Кролик | Человека | 1:100 |
| Мыши | |||||
| Черепаха | |||||
| Капибара | |||||
| ЕРЗ | Поликлональных | Кролик | Человека | ||
| Обезьяна | |||||
| Крыса | |||||
| Мыши | |||||
| Овец | |||||
| Свинья | |||||
| GPER | Поликлональных | Кролик | Человека | ||
| Крыса | |||||
| Мыши | |||||
| Вторичного | DyLight 650 | Поликлональных | Коза | Кролик | 1:250 |
Таблица 2: Характеристики антител.
- Инкубировать с первичными антителами ночь на 4 градуса по Цельсию в темноте.
- Удалить раствор антитела и промыть в стиральном растворе (50 мм Tris-HCl, рН 7,4; 150 мМ NaCl; 0,05% Tween 20) в течение 5 мин. Повторите этот шаг три раза.
- Добавьте 20-50 л вторичных антител DyLight 650, разбавленных в 1% бычьего сывороточки альбумина (содержащий 50 мм Tris-HCl, рН 7,4, 150 мМ NaCl, 0,05% Triton X-100). Инкубировать вторичными антителами, спрятательными с красителем на 1 ч при комнатной температуре в темноте.
ПРИМЕЧАНИЕ: Рекомендуемое разбавление вторичных антител показано в таблице 2. - Удалить раствор антитела и промыть в стиральном растворе (50 мм Tris-HCl, рН 7,4, 150 мМ NaCl, 0,05% Tween 20) в течение 5 мин. Повторите этот шаг три раза.
- Добавьте 2% DiOC6(3) разбавленный в 50 мм Tris-HCl, рН 7,4, 150 мМ NaCl и инкубировать в течение 10 минут при комнатной температуре в темноте.
- Снимите раствор и промойте в стиральном растворе (50 мм Tris-HCl, рН 7,4, 150 мМ NaCl, 0,05% Tween 20) в течение 5 мин. Повторите этот шаг три раза.
- Добавьте несколько капель жидкости на основе глицерола с DAPI непосредственно на секции толстой кишки и тщательно накройте крышкой слайд. Инкубировать секцию толстой кишки, по крайней мере 24 ч при 4 градусах Цельсия.
ПРИМЕЧАНИЕ: Избегайте пузырьков воздуха при покрытии ткани с крышкой слайд. - Проанализируйте секцию толстой кишки под конфокальный микроскоп с 20x или 63x целей и погружения нефти с помощью специального программного обеспечения.
ПРИМЕЧАНИЕ: В таблице 3 перечислены характеристики флюорохромов, используемых в данном исследовании.
| Тип фторхома | Длина волны (нм) | Красителя | |
| Возбуждения | Выбросов | ||
| ДАПИ | 405 | 460 – 480 | Синий |
| DiOC6 (3) | 485 | 538 – 595 | Зеленый |
| DyLight 650 | 654 | 660 – 680 | Красного |
Таблица 3: Характеристики фторхромов.
Результаты
Макроскопические характеристики толстой кишки у мышей с болезнью Крона, вызванной TNBS
Репрезентативные изображения толстой кишки взяты из контроля и TNBS обработанных мышей показаны на рисунке 2. У мышей с TNBS-индуцированной модели болезни Кро?...
Обсуждение
Существует множество моделей животных для исследования ПАтофизиологии IBD, включая генетические, иммунологические или спонтанные модели, а также химически индуцированные модели15. Среди нескольких типов животных моделей колита, химически индуцированных моделей, таких как...
Раскрытие информации
Авторам нечего раскрывать.
Благодарности
Работа была опубликована благодаря финансовой поддержке властей Лодзинского университета: проректора по научным исследованиям, проректора по национальному и международному сотрудничеству, декана факультета биологии и охраны окружающей среды. Damian Jacenik was supported by grants (2017/24/T/NZ5/00045 and 2015/17/N/NZ5/00336) from National Science Centre, Poland.
Материалы
| Name | Company | Catalog Number | Comments |
| Animals | |||
| BALB/C mice | University of Lodz | NA | |
| Equipment | |||
| Caliper | VWR | 62379-531 | |
| Cardboard block | NA | NA | |
| Confocal microscope - TCS SP8 | Leica Biosystems | NA | |
| Fully automated rotary microtome - RM2255 | Leica Biosystems | NA | |
| Glass slide | Thermo Scientific | J1800BMNT | |
| Heated Paraffin Embedding Module - EG1150 H | Leica Biosystems | NA | |
| Histological box | Marfour | LN.138747 | |
| Hydrophobic pen | Sigma-Aldrich | Z377821 | |
| Laboratory balance | Radwag | WL-104-0048 | |
| LAS X software | Leica Biosystems | NA | |
| Metal mold | Marfour | CP.5105 | |
| Sterile gauze | NA | NA | |
| Sterile scissor | NA | NA | |
| Sterile tweezer | NA | NA | |
| Tissue processor - TP1020 | Leica Biosystems | NA | |
| Reagents | |||
| 2, 4, 6-trinitrobenzene sulfonic acid | Sigma-Aldrich | 92822 | |
| Bovine serum albumin | Sigma-Aldrich | A3294 | |
| DiOC6 (3) | Sigma-Aldrich | 318426 | |
| DyLight 650 secondary antibody | Abcam | ab96886 | |
| ERα primary antibody | Abcam | ab75635 | |
| ERβ primary antibody | Abcam | ab3576 | |
| Ethanol | Avantor Performance Materials Poland | 396480111 | |
| Formaldehyde | Avantor Performance Materials Poland | 432173111 | |
| GPER primary antibody | Abcam | ab39742 | |
| Hydrochloric acid | Avantor Performance Materials Poland | 575283421 | |
| Hydrogen peroxidase | Avantor Performance Materials Poland | 885193111 | |
| isoflurane (forane) | Baxter | 1001936040 | |
| Normal goat serum | Gibco | 16210064 | |
| Paraffin | Leica Biosystems | 39602012 | |
| Petrie dish | Nest Scientific | 705001 | |
| Phosphate buffer saline | Sigma-Aldrich | P3813 | |
| Physiological saline | Sigma-Aldrich | 7982 | |
| Primocin (antibiotic) | Invitrogen | ant-pm-1 | |
| ProLong Diamond Antifage Mountant with DAPI (glycerol-based liquid with DAPI) | Invitrogen | P36971 | |
| Sodium chloride | Chempur | WE/231-598-3 | |
| Sodium citrate | Avantor Performance Materials Poland | 795780429 | |
| Tris | Avantor Performance Materials Poland | 853470115 | |
| Triton X-100 | Sigma-Aldrich | T8787 | |
| Tween 20 | Sigma-Aldrich | P9416 | |
| Xylene | Avantor Performance Materials Poland | BA0860119 |
Ссылки
- Zhang, Y. Z., Li, Y. Y. Inflammatory bowel disease: pathogenesis. World Journal of Gastroenterology. 20 (1), 91-99 (2014).
- Morris, G. P., et al. Hapten-induced model of chronic inflammation and ulceration in the rat colon. Gastroenterology. 96 (3), 795-803 (1989).
- Okayasu, I., et al. A novel method in the induction of reliable experimental acute and chronic ulcerative colitis in mice. Gastroenterology. 98 (3), 694-702 (1990).
- Boirivant, M., Fuss, I. J., Chu, A., Strober, W. Oxazolone colitis: a murine model of T helper cell type 2 colitis treatable with antibodies to interleukin 4. Journal of Experimental Medicine. 188 (10), 1929-1939 (1998).
- Morrissey, P. J., Charrier, K., Braddy, S., Liggitt, D., Watson, J. D. CD4+ T cells that express high levels of CD45RB induce wasting disease when transferred into congenic severe combined immunodeficient mice. Disease development is prevented by cotransfer of purified CD4+ T cells. Journal of Experimental Medicine. 178 (1), 237-244 (1993).
- Kühn, R., Löhler, J., Rennick, D., Rajewsky, K., Müller, W. Interleukin-10-deficient mice develop chronic enterocolitis. Cell. 75 (2), 263-274 (1993).
- Sundberg, J. P., Elson, C. O., Bedigian, H., Birkenmeier, E. H. Spontaneous, heritable colitis in a new substrain of C3H/HeJ mice. Gastroenterology. 107 (6), 1726-1735 (1994).
- Harnish, D. C., et al. Beneficial effects of estrogen treatment in the HLA-B27 transgenic rat model of inflammatory bowel disease. American Journal of Physiology Gastrointestinal and Liver Physiology. 286 (1), 118-125 (2004).
- Pierdominici, M., et al. Linking estrogen receptor β expression with inflammatory bowel disease activity. Oncotarget. 6 (38), 40443-40451 (2015).
- Włodarczyk, M., et al. G protein-coupled receptor 30 (GPR30) expression pattern in inflammatory bowel disease patients suggests its key role in the inflammatory process. A preliminary study. Journal of Gastrointestinal and Liver Diseases. 26 (1), 29-35 (2017).
- Mohammad, I., et al. Estrogen receptor α contributes to T cell-mediated autoimmune inflammation by promoting T cell activation and proliferation. Science Signaling. 11 (526), eaap9415 (2018).
- Jacenik, D., et al. G protein-coupled estrogen receptor mediates anti-inflammatory action in Crohn's disease. Scientific Reports. 9 (1), 6749 (2019).
- Prossnitz, E. R., Barton, M. The G protein-coupled estrogen receptor GPER in health and disease. Nature Review Endocrinology. 7 (12), 715-726 (2011).
- Yaşar, P., Ayaz, G., User, S. D., Güpür, G., Muyan, M. Molecular mechanisms of estrogen-estrogen receptor signaling. Reproductive Medicine and Biology. 16 (1), 4-20 (2016).
- Pizarro, T. T., Arseneau, K. O., Bamias, G., Cominelli, F. Mouse models for the study of Crohn's disease. Trends in Molecular Medicine. 9 (5), 218-222 (2003).
- Neurath, M. F., Fuss, I., Kelsall, B. L., Stüber, E., Strober, W. Antibodies to interleukin 12 abrogate established experimental colitis in mice. Journal of Experimental Medicine. 182 (5), 1281-1290 (1995).
- Ikeda, M., et al. Simvastatin attenuates trinitrobenzene sulfonic acid-induced colitis, but not oxazalone-induced colitis. Digestive Diseases and Sciences. 53 (7), 1869-1875 (2007).
- Thavarajah, R., Mudimbaimannar, V. K., Elizabeth, J., Rao, U. K., Ranganathan, K. Chemical and physical basics of routine formaldehyde fixation. Journal of Oral Maxillofacial Pathology. 16 (3), 400-405 (2012).
Перепечатки и разрешения
Запросить разрешение на использование текста или рисунков этого JoVE статьи
Запросить разрешениеThis article has been published
Video Coming Soon
Авторские права © 2025 MyJoVE Corporation. Все права защищены