Method Article
Hücre ve İlaç Dağıtım Uygulamaları için Enjekte Edilebilir Supramoleküler Polimer-Nanopartikül Hidrojelleri
Bu Makalede
Özet
Bu protokol enjekte edilebilir, supramoleküler polimer-nanopartikül (PNP) hidrojel biyomalzemelerin sentezini ve formülasyonlarını açıklar. Bu malzemelerin ilaç dağıtımı, biyofarmasötik stabilizasyon ve hücre kapsülleme ve teslimi için uygulamaları gösterilmiştir.
Özet
Bu yöntemler, biyomalzeme olarak kullanılmak üzere enjekte edilebilir, supramoleküler polimer-nanopartikül (PNP) hidrojellerin nasıl formüle edilerek kullanılacağı açıklanmaktadır. PNP hidrojelleri iki bileşenden oluşur: ağ polimeri olarak hidrofobik olarak modifiye selüloz ve dinamik, çok değerli etkileşimler yoluyla kovalent olmayan çapraz bağlayıcılar olarak hareket eden kendi kendine monte edilmiş çekirdek kabuk nanopartikülleri. Bu yöntemler, hem nano-prekipitasyon yoluyla kendi kendine monte edilen bu nanopartiküllerin oluşumunu hem de ayarlanabilir mekanik özelliklere sahip hidrojeller oluşturmak için iki bileşenin formülasyonunu ve karıştırılmasını açıklar. Sentezlenen malzemelerin kalitesini karakterize etmek için dinamik ışık saçılım (DLS) ve reoloji kullanımı da ayrıntılı olarak açıklanmıştır. Son olarak, bu hidrojellerin ilaç dağıtımı, biyofarmasötik stabilizasyon ve hücre kapsülleme ve doğumu için faydası, ilaç salınımını, termal stabiliteyi ve hücre yerleştirme ve canlılığını karakterize etmek için in vitro deneylerle gösterilmiştir. Biyouyumluluğu, enjekte edilebilirliği ve hafif jel oluşum koşulları nedeniyle, bu hidrojel sistemi bir dizi biyomedikal uygulama için uygun kolayca tonlanabilir bir platformdur.
Giriş
Enjekte edilebilir hidrojeller, terapötik hücreleri ve ilaçları kontrollü bir şekilde vücuda ulaştırmak için ortaya çıkan bir araçtır1. Bu malzemeler ilaçlar veya hücrelerle yüklenebilir ve yüzeysel dokulara doğrudan enjeksiyon veya derin dokulara kateter teslimatı ile minimal invaziv bir şekilde uygulanabilir. Genel olarak, enjekte edilebilir hidrojeller, geçici, fiziksel etkileşimlerle birbirine birbirine kenemiş su şişmiş polimer ağlarından oluşur. Dinlenme sırasında, bu çapraz bağlantılar jellere katı benzeri bir yapı sağlar, ancak yeterli mekanik kuvvetin uygulanması üzerine bu çapraz bağlantılar geçici olarak bozulur ve malzeme kolayca akabilen sıvı benzeri bir duruma dönüşür2. Fiziksel hidrojellerin kesmesine ve enjeksiyon sırasında küçük iğne çaplarından akmasına izin veren bu reolojiközelliklerdir 3. Enjeksiyondan sonra, malzemenin polimer ağı, kendi kendini iyileştirmesine ve hızla katı benzeri bir jel oluşturmasına izin verir4,5. Bu yapılar, doku yenilenmesi için ilaçlar veya iskeleler için yavaş salınım depoları olarak işlev görür6,7. Bu malzemeler ilaç dağıtım teknolojisi, rejeneratif tıp ve immünomühendislik 1,8 , 9 ,10,11,12'yikapsayan çeşitli uygulamalarda kullanılmıştır.
Hem doğal malzemeler (örneğin, aljinat ve kollajen) hem de sentetik malzemeler (örneğin, poli(etilen glikol) (PEG) veya benzeri hidrofilik polimerler) biyouyumlu enjekte edilebilir hidrojel malzemeler olarak geliştirilmiştir13,14,15. Birçok doğal malzeme, tekrarlanabilirliği etkileyen toplu iş varyasyonu sergiler4,16. Bu malzemeler genellikle fizyolojik sıcaklıklara ulaştıktan sonra iyileşen sıcaklığa duyarlıdır; bu nedenle, bu malzemelerin işlenmesi ek teknik ve lojistik zorluklar doğurur17. Sentetik malzemeler daha hassas kimyasal kontrol ve mükemmel tekrarlanabilirlik sağlar, ancak bu malzemeler bazen biyouyumlarını sınırlayan olumsuz bağışıklık yanıtlarına maruz kalabilir, bu da in vivo terapötik uygulamalar için kritik birözelliktir 6,18,19. Son çabalar, enjekte edilebilir bir hidrojel malzemenin mühendisliğinde mekanik özelliklerin optimize edilmesi, polimer ağ örgü boyutu, biyoaktif moleküler ipuçları, biyobozunurluk ve malzemenin immünojenikliği 20 , 21 , 22 ,23,24,25,26dahil olmak üzere birçok karmaşık tasarım kriteri olduğunu göstermiştir. Tüm bu faktörler, ilginin uygulanmasına bağlı olarak düşünülmelidir, bu da modüler, kimyasal olarak ayarlanabilir bir platformun geniş bir uygulama genişliğini karşılamak için ideal olduğu anlamına gelir.
Mevcut yöntemler, ayarlanabilir mekanik özellikler, yüksek derecede biyouyumluluk ve düşük immünojeniklik sergileyen enjekte edilebilir bir polimer-nanopartikül (PNP) hidrojel platformunun formülasyonunu ve kullanımını açıklar ve biyoaktif moleküler ipuçları 27 ,28 ,29,30,31,32,33'üçağrıştırmak için siteler sunar. Bu PNP hidrojeller hidrofobik modifiye selüloz polimerleri ve bir supramoleküler ağ üretmek için etkileşime giren poli (etilen glikol)-blok-poli (laktik asit) (PEG-PLA)27,34'den oluşan kendi kendine monte edilmiş çekirdek kabuklu nanopartiküllerden oluşur. Daha spesifik olarak, dodecyl modifiye hidroksipropimetil selüloz polimerleri (HPMC-C12),PEG-PLA nanopartiküllerinin yüzeyi ile dinamik olarak etkileşime girer ve bu polimer ağını oluşturmak için bu nanopartiküller arasındaki köprü27,34. Bu dinamik, çok değerli etkileşimler, malzemelerin enjeksiyon sırasında kesmesine ve uygulamadan sonra hızla kendini iyileştirmesine izin verir. PNP hidrojel bileşenleri basit tek pot reaksiyonları ile kolayca imal edilir ve PNP hidrojel, iki bileşenin basit bir şekilde karıştırılmasıyla hafif koşullar altında oluşturulur35. İmalat kolaylığı nedeniyle, bu hidrojel platformu ölçek olarak son derece çevrilebilir. PNP hidrojellerinin mekanik özellikleri ve ağ boyutu, formülasyondaki polimer ve nanopartikül bileşenlerinin ağırlık yüzdesi değiştirilerek kontrol edilir. Bu platform ile yapılan önceki çalışmalar, PNP hidrojellerinin son derece biyouyumlu, biyobozunur ve immünojenik olmayan28,30,31olduğunu göstermektedir. Genel olarak, bu hidrojeller ameliyat sonrası yapışıklık önleme, doku mühendisliği ve rejenerasyon, sürekli ilaç dağıtımı ve immünörineringi kapsayan biyomedikal uygulamalarda geniş fayda sağlar.
Protokol
Bu protokole başlamadan önce, HPMC-C12 ve PEG-PLA'yı daha önce yayınlanan27 , 28,29,30,31,36,37,38yöntemlerini kullanarak sentezlemek gerekir.
1. Nanopartikül (NP) nano prekipitasyon ile sentez
NOT: Bu bölümde, tampon çözeltisinde 250 μL%20 wt NP üreten tek bir NP grubunun sentezi açıklanmaktadır (parti başına 50 mg kuru PEG-PLA polimer). Toplu iş sayısını ölçeklendirme notları ilgili adımlarda sağlanır.
- 8 mL cam scintillation şişesine 50 mg PEG-PLA polimer ölçün ve 1 mL asetonitril ekleyin. Girdap tamamen çözülecek.
NOT: Parti sayısını ölçeklendirmek için, bu adımı doğrusal olarak ölçeklendirin ve tek bir şişede gereken toplam polimer ve çözücü miktarını ekleyin. - Küçük bir karıştırma çubuğu ile 20 mL cam scintillation şişesine 10 mL ultra saf su ekleyin. 600 rpm'ye ayarlanmış bir karıştırma plakası takın.
NOT: Adım 1.1 ölçeklendirilmişse, her eşdeğer toplu iş için çökeltmek için ayrı bir scintillation şişesine sahip olmak gerekir. Örneğin, 4 mL asetonitril içinde çözünmüş 200 mg polimer için 4 x 20 mL scintillation şişeleri hazırlayın. - Nano prekipitasyon ile NP'ler oluşturmak için, 200 μL pipet kullanarak suya damla yönünde 1 mL polimer çözücü çözeltisi ekleyin. 2 dakika karıştırın. PEG-PLA'nın PLA bloğu suda çözünmez ve sonuç olarak, çekirdek kabuk NP'leri çekirdek olarak hidrofobik PLA blokları ve kabuk olarak hidrofilik PEG blokları ile kendiliğinden bir araya gelecektir.
- Dinamik ışık saçılımı (DLS) ile parçacık boyutunu doğrulayın.
NOT: Bu prosedür, ilişkili yazılım paketine sahip ticari olarak kullanılabilen bir plaka okuyucu için özel olarak yazılmıştır (bkz. Malzeme Tablosu). Alternatif aletleri kullanmak için, cihazın üreticisi tarafından açıklanan örnek hazırlama yöntemlerine bakın.- 20 μL NP çözeltisi ile 80 μL ultra saf su ile seyreltin (analiz konsantrasyonu: 1 mg/mL PEG-PLA NP). Net bir alt siyah 384 kuyu plakasına kuyu başına 30 μL ekleyin (üç taraflı olarak analiz edin).
- Yazılım paketindeki önceden ayarlanmış protokol seçeneklerini kullanarak her numunenin hidrodinamik yarıçapını ve polidispersitesini bir DLS plaka okuyucu ile ölçün. Tipik bir protokole örnek olarak, veri toplama parametrelerini toplama başına 2-5 s süre 5-10 DLS ölçümü elde etmek için ayarlayın ve ardından küresel proteinler modelinden hesaplanan kuyu başına ortalama bir parçacık boyutu ve dağılımı bildirin. Tutarlı reolojik özelliklere sahip hidrojeller oluşturmak için, elde edilen parçacıklar 0.2'< bir polidispersite (PD) ile hidrodinamik çapta 30-50 nm olmalıdır.
NOT: NP'ler istenenden daha küçükse, adım 1.1'de% 75 asetonitril /% 25 dimetil sülfit (DMSO) çözeltisi kullanın. Çözücü çözeltideki DMSO yüzdesini artırmak genellikle parçacık boyutunu artıracaktır.
- NP çözeltisini 20 mL scintillation şişesinden bir santrifüj filtre ünitesine aktarın. NP çözeltisini 250 μL'ye < konsantre etmek için 1 saat boyunca 4500 x g'da santrifüj.
- Fosfat tamponlu salin (PBS) gibi istenen tamponda % 20 wt NP'ye yeniden depolanır. Filtreyi durulamak ve tüm NP'lerin toplanmasını sağlamak için az miktarda (50-100 μL) tampon kullanın.
NOT: Toplu işlemler yeniden canlandırma sırasında birikebilir. NP stok çözümleri yaklaşık 1 ay boyunca 4 °C'de saklanabilir. Donmayın. Daha uzun depolama için, kullanmadan önce boyutu ve polidispersiteyi DLS ile doğrulayın.
2. İlaçların veya hücrelerin hidrojel formülasyonu ve kapsüllenmesi
NOT: Bu bölümde 2:10 PNP hidrojel formülasyonunun 1 mL'sinin hazırlanması açıklanmaktadır, 2 wt%HPMC-C12 ve %10 wt NPs (%12 wt toplam katı polimer) ve %88 wt tampon çözeltisi, ilaç kargo çözümü veya hücre süspansiyonu gösterilir. Formülasyon yüzdeleri, çeşitli mekanik özelliklere sahip hidrojeller elde etmek için değiştirilebilir. Örneğin, hücre yerleştirme ve uygulanabilirlik deneysel sonuçları için 1:5 PNP hidrojel kullanıldı.
- PBS'de (veya tercih eden diğer tamponlarda) %6 wt HPMC-C12 stok çözeltisi hazırlayın. Polimerin tamamen dağılmasını sağlamak için 48 saat çözün.
NOT: HPMC-C12 stok çözümü oda sıcaklığında aylarca stabildir. Bununla birlikte, mikrobiyal büyümeyi engellemek için 4 °C'de depolama önerilir. - 1 mL Luer kilit şırıngına 333mg%6 wt HPMC-C 12 stok çözeltisi ekleyin.
- Bir mikrosantrifüj tüpüne 500 μL%20 wt%NP stok çözeltisi ekleyin. Karıştırmak için 167 μL PBS ve pipet ekleyin. Bir iğne kullanarak, seyreltilmiş NP çözeltisi ile başka bir 1 mL Luer kilit şırıngasını doldurun.
NOT: İlaç kargosu yüklemek için, ilacın hidrojeldeki istenen son konsantrasyonu hesaplayın ve uygun miktarı NP'lerle karıştırılan 167 μL PBS'ye yükleyin. İlaç stabilitesini izlemek gibi yerinde bir test için moleküler bir prob gerekliyse, probu ilaç kargosu yüklemek için yukarıda açıklandığı gibi yükleyin. Hücreleri yüklemek için, hidrojelde istenen son hücre konsantrasyonunun hesaplayın ve uygun sayıda hücreyi NP'lerle karıştırılan 167 μL PBS'ye yükleyin. - İki hidrojel bileşeni (HPMC-C12 ve NP' ler) dirsek karıştırma yöntemi35kullanarak karıştırın.
- Luer dirsek konektörünü NP çözeltisi içeren şırınna takın (isteğe bağlı olarak ilaç yükü veya hücreleri de içerir). Menisküs açık uçta görünene kadar NP çözeltisini dirsekten itin. Hafifçe geri çekin ve HPMC-C12 çözümü içeren şırınnayı bağlayın.
NOT: Karıştırma işlemi sırasında hidrojel boyunca kabarcık oluşumunu ve dağılmasını önlemek için dirsek bağlantısındaki havayı en aza indirmek önemlidir. Hücreleri dirsek mikseri ile karıştırırken, çok hızlı karıştırmak hücreleri yüksek kesme kuvvetlerine maruz kalabileceğinden, hücre ölümüne yol olabileceğinden daha hafif bir şekilde karıştırmaya özen edin. - Homojen, opak beyaz bir hidrojel malzeme oluşana kadar iki çözeltiyi yaklaşık 60 döngü boyunca dirsek mikserinde ileri geri pompalayın.
- Tüm hidrojel hacmini tek bir şırında itin. Boş şırınnayı çıkarın ve dirsek konektöründen malzemeyi kurtarmak için pistonu jel yüklü şırınna geri çekin. Bir iğne veya fiş ile kap.
NOT: Karıştırma işlemindeki ölü alan nedeniyle ~300 μL kayıp hidrojel hacmini hesaba katmak gerekir. Örneğin, 700 μL nihai hidrojel hacmi isteniyorsa, 1 mL hidrojel hazırlanmalıdır. Hidrojel formülasyon işlemi daha büyük şırınnalar kullanılarak ölçeklendirilebilir. Bununla birlikte, 2:10 gibi sert hidrojel formülasyonları için, şırınga namlusunun dirsek veya iğne çapına oranının artması nedeniyle hacmi 3 mL'den büyük şırıngalardan karıştırmak ve enjekte etmek zorlaşabilir. - Hidrojelleri şırınnada oda sıcaklığında saklayın. Bununla birlikte, ilaçlar kapsüllenirse, ilaç üreticisi aksini belirtmedikçe 4 °C'de depolanmasınız önerilir. Malzemeyi dondurmayın.
- Luer dirsek konektörünü NP çözeltisi içeren şırınna takın (isteğe bağlı olarak ilaç yükü veya hücreleri de içerir). Menisküs açık uçta görünene kadar NP çözeltisini dirsekten itin. Hafifçe geri çekin ve HPMC-C12 çözümü içeren şırınnayı bağlayın.
3. Hidrojel formülasyonlarının reolojik özelliklerinin ölçülmesi
NOT: Bu protokol özellikle 20 mm tırtıklı plaka geometrisine sahip Malzeme Tablosunda belirtilen ticari reometre ile kullanılır. Diğer aletleri kullanmak için, numune hazırlama için üreticinin talimatlarına bakın.
- Reolojik karakterizasyon için en az 700 μL PNP hidrojel formüle edin.
- Malzemeyi tırtıklı reometre plakasının ortasına enjekte edin. Miktar seçilen geometri boşluğuna bağlı olarak değişecektir. Referans olarak, 700 μm boşluk ~ 400-500 μL malzeme gerektirir.
- Reometreyi trim boşluğuna (500-1000 μm) küt çevirin ve boşluğun eşit ve tamamen doldurulmasını sağlamak için PNP hidrojel ile temas ettiği için üst reometre plakasını yavaşça çevirin.
- PNP hidrojelinin yüklenmesini, tüm reometre plaka yüzeyini kaplar şekilde inceleyin. Plakadan çok hafif bir şişkinliğe sahip olacak şekilde fazla malzemeyi hafifçe kırpmak ve çıkarmak için bir spatula veya plastik düzeltici kullanın.
- Reometreyi son geometri boşluğuna küskün ve numunenin temiz bir şekilde yüklendiğini doğrulayın.
- Genlik veya frekans süpürme gibi salınımlı testleri veya akış süpürmeleri veya adım testleri gibi akış testlerini kullanarak numunenin mekanik özelliklerini ölçün.
NOT: Gösterilen temsili verilerde osilatör genlik testleri 10 rad/s sabit frekansta çalıştırılır. Salınımlı frekans taramaları, genlik süpürmenin doğrusal viskoelastik rejimi içinde sabit bir% 1 suşta çalıştırılır. Akış süpürmeleri yüksek kesme hızlarından düşük kesme hızlarına39'a kadar çalıştırılır. Tüm testler, toplanan on yıllık veri başına 10 puanla ve oda sıcaklığında tamamlanır. Test parametrelerinin formülasyonun özelliklerine bağlı olarak ayarlanması gerekebilir. 2:10 formülasyonları gibi daha sert PNP malzemelerinin yüksek kesme hızlarına tabi tutulması, malzemenin reometre plakalarından atılmasına neden olabilir, bu da yanlış mekanik karakterizasyona neden olabilir ve sonraki testler arasında numunenin yeniden yüklenmesini gerektirebilir. Aşağıda gösterilen temsili veriler, kalite kontrol testi sırasında karşılaştırma için kullanılabilir.
4. In vitro ilaç salınımı karakterize
- Cam kılcal boruları istenilen uzunlukta keserek kılcal borular hazırlayın. Bir fiş oluşturmak için tüpün ucuna az miktarda epoksi itmek için tek kullanımlık bir spatula veya pipet ucu kullanarak her tüpün bir ucunu kapatın. Epoksinin üreticinin önerdiği süreye göre ayar yapmasına izin verin.
NOT: Tüp enjeksiyon iğnesinin uzunluğundan daha kısa olmalıdır. 2-3 μm iç çaplı boru, 2,5 inç uzunluğunda en az 300 μL toplam hacim içerecek şekilde önerilir. - İlgi çekici ilacı içeren bir şırınna en az 500 μL PNP hidrojel malzeme formüle edin. Her örnek grubu ayrı bir şırınna hazırlayın.
- Uzun bir hipodermik iğne (22G, 4 inç) kullanarak her kılcal tüpün altına 100-200 μL PNP hidrojel enjekte edin. Örnek grup başına en az üç tüp (triplikat) hazırlayın.
- (İsteğe bağlı) Hidrojel yüzeyinin düzgün olduğundan emin olmak için doldurulmuş kılcal boruları konik bir santrifüj tüpüne ve santrifüje 1 dakika boyunca 1000 x g'da yerleştirin. Bu adımın tekrarlanması gerekebilir, malzemenin yüzeyini yumuşatmak için zaman ve hızı gerektiği gibi değiştirebilirsiniz.
DİkKAT: Santrifüjün iyi dengelenmiş olduğundan emin olun. - Kılcal borudaki hidrojel üzerine şırınga ve iğne veya pipet kullanarak 200-300 μL PBS'yi dikkatlice doldurun. Hidrojel yüzeyine temas etmeyin veya rahatsız etmeyin. Tüpü bir kapakla kapatın veya en az iki kat parafin filmi ile takın veya örtün.
- (İsteğe bağlı) Vivo koşulları simüle etmek için numuneleri 37 °C'de kuluçkaya yatır.
- PBS'yi hidrojel yüzeyini bozmadan, ilaç salınımının beklenen zaman ölçeğine bağlı olarak seçilen zaman noktalarında bir şırınga ve iğne kullanarak her kılcal damardan dikkatlice çıkarın. Kaldırılan birimi yeni PBS ile değiştirin. Aliquots uygun koşullarda saklayın.
NOT: 4.3, 4.5 ve 4.7 adımlarında önerilen hacimler ve zaman noktaları, malzemeye ne kadar ilaç yüklendiklerine ve süpernatanta ne kadar hızlı salındıklarına bağlı olarak, bir dizi zaman ölçeğinde in vitro ilaç salınımını yakalamak için optimize edilebilir. Seçilen zaman noktalarının bir örneği, yavaş salınan bir ilaç için 6 saat, 1 gün, 3 gün, 1 hafta ve 2 hafta olabilir. Aliquots, depolandığı yerine edinildikçe de analiz edilebilir. - Çalışmanın tamamlanmasıyla, her zaman40 , 41,42noktasında salınan ilaç miktarını ölçmek için ELISA, HPLC veya floresan tahlil gibi uygun bir yöntemle aliquotları analiz edin. Uygun tespit yöntemi, ilgi çekici ilaca bağlı olarak değişecektir.
NOT: In vitro salınım çalışmaları, farklı hidrojel formülasyonları veya ilaç kargoları arasındaki salınımı karşılaştırmak için yararlıdır. In vitro serbest bırakma zaman ölçeği genellikle doğrudan vivo beklenen bir serbest bırakma zaman ölçeğini göstermez.
5. Jel kapsüllenmiş insülinin termal stabilitesinin karakterizei
- Örnek grubu başına en az 1,2 mL PNP hidrojel formüle edin. Bölüm 2.3'te açıklanan prosedürü takiben, PNP hidrojel içine hem insülin (ilaç yükü) hem de thioflavin T (ThT) (moleküler prob) yükleyin.
NOT: Birincil toplama mekanizması ve bu nedenle insülinin inaktivasyonu amiloid fibrillerin oluşumundan geçer. ThT uygun bir moleküler probdur, çünkü amiloid fibrillerin varlığında güçlü bir floresan sinyali üretir ve insülin toplamanın yerinde izlenmesini sağlar. İlgi edilen ilaç kargosunda, toplama farklı yöntemlerle izlenebilir. Gösterilen temsili veriler için, insülin 6.7 veya 10 mg / mL ve ThT son konsantrasyona 25 μM'lik son bir konsantrasyona yüklendi. - 21 G iğne kullanarak, siyah bir 96 kuyu plakasına kuyu başına 200 μL PNP hidrojel enjekte edin. Her örnek grup en az üç taraflı olarak ölçülmelidir. Buharlaşmayı önlemek için optik olarak netleştirilmiş yapışkan plaka contası ile sızdırmaz plaka.
- Plakayı sıcaklık kontrolü, sallama ve kinetik okuma programlama ile donatılmış bir plaka okuyucusuna yerleştirin ve okuma protokolüne başlayın. Temsili veriler, aşağıdaki koşullar kullanılarak piyasada bulunan bir plaka okuyucusu (bkz. Malzeme Tablosu) ile elde edildi:
- Stresli yaşlanma koşulları: 37 °C'de sürekli doğrusal sarsıntı (410 cpm, 5 mm).
- Veri toplama: 20 dakika aralıklarla heyecanlanma/emisyon 450 nm/482 nm
NOT: Sıcaklık kontrolü, çalkalayıcı ve kinetik okuma özelliklerine sahip bir plaka okuyucu mevcut değilse, plaka bir inkübatördeki bir çalkalayıcı plakaya yerlenebilir ve seçilen zaman noktalarındaki dalga boylarının üzerinde manuel olarak okunabilir.
- Verileri her grup için zaman içinde ortalama floresan sinyali olarak çizin. Toplama süresi, rasgele bir sinyal eşiği43tanımlayarak ölçülebilir.
NOT: Aşağıda gösterilen temsili veriler için eşik 750.000 keyfi floresan birimi (AFU) olarak tanımlanmıştır. Bu değer, keskin bir floresan sinyal artışı ile belirtilen toplama başlangıcını yeterince yakalarken ölçülen taban çizgisinin üzerinde olması için seçildi. - Numuneler bir araya geldiğinde veya görsel olarak susuzlaşmaya başladığında tahlilleri sonlandır.
6. Hücre canlılığının değerlendirilmesi
- Yukarıdaki protokolleri izleyerek istenen hücre konsantrasyonu içeren en az 2 mL PNP hidrojel formüle edin (normalde 1 - 5 x 106 hücre/mL). Her örnek grubu ayrı bir şırınna hazırlayın.
- 21G iğne kullanarak, her kuyuya net bir alt 96 kuyu plakasında 150 μL PNP hidrojel enjekte edin; her kuyu bir çoğaltmadır. Her örnek grubun zaman noktası başına 3-5 çoğaltması olmalıdır. Hidrojel kuyuya eşit olarak yaymak için plakayı 2 dakika boyunca 50 x g'da santrifüj edin.
- Hidrojel üzerine 100 μL uygun hücre ortamı ekleyin. Bu ortamı her gün çıkarın ve 100 μL yeni ortam ekleyin.
- 1. Günde, her örnek grup için bu zaman noktası için belirlenen çoğaltmalar için hidrojel üzerindeki ortamı çıkarın. Hidrojellerin üzerine 50 μL 2 mM kalsein çözeltisi ekleyin. 30 dakika kuluçkaya yaslanın.
NOT: Calcein canlı hücreleri tanımlamak ve etiketlemek için kullanılabilir. Canlı hücrelerde, floresan olmayan kalsein, asetoksimetrin ester hidrolizden sonra hücre içi esterazlar tarafından yeşil floresan kalceine dönüştürülür. - Konfokal mikroskop kullanarak her kuyunun merkezini 96 kuyulu bir plakada görüntüleyin. En az 150 μm'ye yayılan bir z yığını ile en az 300 μm2'lik bir alanı inceleyin. Kalsilerin floresanını yakalamak için konfokal dalga boyu ayarlarını kullanın (ekscitasyon/emisyon: 495 nm/515 nm).
- Sonraki her zaman noktası için 6.4 ve 6.5 adımlarını istediğiniz gibi yineleyin.
- Her görüntüyü analiz etmek için, FIJI veya benzer bir yazılım kullanarak tüm z yığını görüntülerini tek bir düzlem maksimum yoğunluklu görüntüye daraltin. Her görüntüdeki floresan hücrelerinin sayısını ölçün. Her zaman noktasında floresan hücre sayısının 1.
7. Hücre yerleşimi değerlendirme
- 5 x 106 hücre/mL'lik son konsantrasyonda 500-700 μL PNP hidrojel formüle etmek için gereken hücre sayısını hesaplayın. 1 mL PBS'deki hücreleri 1 x 106 hücre/mL konsantrasyonda askıya alın. 50 μL 2 mM kalsein ekleyerek hücreleri lekele. Hücreleri boya ile 10 dakika kuluçkaya yatırın.
- Hücreleri uygun koşullarda santrifüj edin, PBS'yi çıkarın ve istenen PNP hidrojelinin 500-700 μL'sini oluşturmak için gereken PBS hacmindeki hücreleri yeniden biriktirin.
NOT: Her bir hücre türünü santrifüj etmek için önerilen hız ve süre genellikle ürün belgelerinde sağlanır. - Protokol bölüm 2'den sonra lekeli hücrelerle (5 x 106 hücre/mL) 500-700 μL PNP hidrojel formüle edin.
- 21G iğne kullanarak, bir cuvette'in altındaki lekeli hücreleri içeren 100-200 μL PNP hidrojel enjekte edin. Her örnek için üç çoğaltma yapılmalıdır. Kabarcık oluşumunu önlemek için enjekte ederken iğneyi cuvette içinde ileri geri hareket ettinin.
- Hemen (zaman t=0), cuvette'in tabanındaki tüm düz cuvette dikdörtgen alanı üzerinde yan yatan cuvetteleri görüntüleyin. Tüm kuyu alanını ve 100 μm derinlikte z yığınını 3D olarak görüntülemek için konfokal karo tarama yeteneklerini kullanın. Daha sonra görselleştirme için, tüm karoları birleştirmek ve geniş alanın tek bir görüntüsünü oluşturmak için maksimum yoğunluk projeksiyonu gerçekleştirmek için konfokal mikroskop yazılımını kullanın veya kişisel bir bilgisayarda FIJI yazılımını kullanın44,45.
- Görüntülemeyi takiben cuvettes dik durun.
- Hücrelerin hidrojel içine yerleşip yerleşmediğini veya askıya alınıp alınmadığını gözlemlemek için 1 saat ve 4 saat görüntü.
NOT: Bu zaman noktaları önerilerdir ve istiridye olarak değiştirilebilir. - Her görüntüyü analiz etmek için tüm z yığını görüntülerini tek bir düzlem maksimum yoğunluklu görüntüye daraltin. FIJI veya benzeri bir yazılım kullanarak, yerleşme derecesini belirlemek için cuvette'in merkez dikey profilinde floresan yoğunluğunu ölçerek hücre dağılımını ölçün.
Sonuçlar
PNP hidrojel imalatı ve karakterizasyonu
PNP hidrojelleri iki ana bileşenin karıştırılmasıyla oluşur - hidrofobik olarak modifiye edilmiş HPMC polimerleri ve PEG-PLA nanopartikülleri (Şekil 1a). Terapötik kargo, hidrojel hazırlamadan önce nanopartikül bileşenini seyreltmek için kullanılan ek tampona kolayca dahil edilir. Aşağı akış biyomedikal karakterizasyon için, iki bileşenin basit ve tekrarlanabilir karıştırılmasını sağlayan bir dirsek karıştırma yöntemi kullanmak uygundur (Şekil 1b). Yeterli karıştırmadan sonra, hidrojel şırıngada sıkı hissetmeli, ancak basınç altında verim vermeli ve standart bir iğneden ekstrüze etmelidir (gösterilen 21G) (Şekil 1c). Enjeksiyondan sonra, hidrojel hızla yerçekiminden gelen akışa direnen katı benzeri bir malzemeye ayarlanmalıdır. Hidrojel'i tam olarak karakterize etmek ve tutarlı toplu ürünler sağlamak için, numuneler bir reometre üzerinde birkaç farklı deney kullanılarak analiz edilmelidir. Jelin kesme inceltme ve kendi kendini iyileştirme yetenekleri, sırasıyla bir akış süpürme protokolü ve adım kesme protokolü kullanılarak kolayca gözlemlenecektir (Şekil 2a,b). 2:10 formülasyonu gibi daha sert jeller için, kullanıcı, kesme oranı enjeksiyon sırasında mekanik koşulları simüle eden 0,1'den 100 s -1'e yükseltildikçe akış süpürme sırasında en az iki büyüklük sırasını azaltmak için viskozite aramalıdır. Adım kesme protokolü, yüksek kesme adımları altında viskozitede büyüklükte bir azalma ve düşük kesme adımları sırasında taban çizgisi viskozitesine hızlı bir dönüş (<5 s kurtarma süresi) göstermelidir. Doğrusal viskoelastik rejimde salınımlı kesme frekansı süpürme deneyi kullanılarak depolama ve kayıp modülünün karakterizasyonu, 0,1-100 rad s-1 (Şekil 2c)frekans aralıklarında katı benzeri özellikleri ortaya çıkaracaktır. Özellikle, genellikle 2:10 hidrojeller gibi daha sert formülasyonlar için düşük frekanslarda gözlemlenebilen kesme depolama ve kayıp modülünün bir geçişi olmamalıdır. Böyle bir çapraz olay, değiştirilmiş HPMC veya PEG-PLA polimerinin başlangıç malzemelerinin kalitesindeki sorunları veya PEG-PLA nanopartiküllerinin boyutunu ve dağılımını gösterebilir. 1:5 hidrojel gibi daha zayıf hidrojel formülasyonları için bir geçit olayının beklenebileceği belirtilmelidir. PNP hidrojellerdeki salınımlı kesme genliği süpürmeleri, malzemelerin yüksek stres değerleri uygulanana kadar verim vermediğini ortaya koymaktadır, bu da bu malzemelerin bir verim stresine, malzemenin akması için gereken bir eşik stres miktarına sahip olduğunu gösterir.
PNP hidrojellerinden salınım kinetiğini karakterize etme
İlaç teslimatı için PNP jelleri tasarlamanın önemli bir adımı, ilaç salınım kinetiğinin seçilen bir formülasyondan tanımlanmasıdır. Bunun için birkaç teknik vardır, ancak basit bir in vitro metodoloji erken formülasyon geliştirme sırasında yararlı veriler sağlar (Şekil 3a). HPMC-C12 veya NP miktarını modüle ederek PNP hidrojellerinin polimer içeriğini değiştirmek, bu hidrojellerin mekanik özelliklerini ve ağ boyutunu ayarlamanın en basit yoludur, bu da polimer ağı üzerinden kargonun yayılması ve malzemelerden salınma oranı üzerinde doğrudan bir etkiye sahip olabilir (Şekil 3b). Dinamik ağ boyutundan (yani yüksek moleküler ağırlık veya büyük hidrodinamik yarıçap) daha büyük olan kargolar için araştırmacılar, hidrojel deposundan kargonun yavaş, çözünme aracılı bir şekilde serbest bırakılmasını beklemelidir. Kargo boyutundan büyük veya buna eşit dinamik ağ boyutlarına sahip formülasyonlar, geleneksel kargo difüzyon modelleri kullanılarak tanımlanabilecek difüzyon aracılı serbest bırakma ve46 , 47,48,49serbest bırakma için izin verecektir. Serbest bırakma eğrisinin şekline bağlı olarak, araştırmacılar hidrojel'i daha yavaş (örneğin, polimer içeriğini artırın) veya daha hızlı (örneğin, polimer içeriğini azaltın) serbest bırakmaya ayarlamak için yeniden biçimlendirebilirler.
Terapötik kargonun stabilitesinin değerlendirilmesi
Bir hidrojel formülasyonunda terapötik yükün stabilitesinin belirlenmesi, klinik öncesi veya hücresel çalışmalara başlamadan önce kritik öneme sahiptir. İlaçları kapsüllemek için diğer sentetik yöntemlerle karşılaştırıldığında, PNP hidrojelleri dökme malzemeye karıştırarak kargoyu nazik bir şekilde içerir ve kapsüllemenin kargoya zarar verme olasılığı düşüktür. Bu çalışmalar, PNP hidrojellerinin ayrıca insülin gibi termal kararsızlığa duyarlı, raf ömrünü önemli ölçüde uzatan ve soğuk depolama ve dağıtıma olan güveni azaltan yükü stabilize edebileceğini göstermektedir (Şekil 4). Yükün durumunun hidrojel içine kapsüllendikten hemen sonra ve uzun depolama sürelerinden sonra değerlendirilmesi önemlidir. Bu veriler, insülin toplamayı ölçmek için basit bir floresan tahlili kullanarak, sürekli termal ve mekanik stres altında 28 günlük depolamadan sonra insülinin hidrojellerde sabit kaldığını göstermektedir. Uygun bir plaka testinin yapılamadığı durumlar için alternatif bir teknik, özellikle protein ilaçlarının ikincil yapısını belirlemek için yararlı olan kargonun dairesel dikroizm ölçümlerini yapmak olacaktır.
PNP hidrojellerinde hücre canlılığının ve dağılımının belirlenmesi
Birçok terapötik hücrenin canlı kalması için yapışma motifleri gerekir ve bu nedenle arginin-glisine-aspartik asit (RGD) peptitleri gibi integrin motiflerinin dahil edilmesi, PNP hidrojellerinin hücresel tedavilere uyarlanması için önemli bir adımdır50. NP'lerden oluşan modüler PEG-PLA polimer, peg koronanın basit "tıklama" kimyaları28,51ile kimyasal işlevselleştirilmesini sağlar. Bu örnekte, PNP hidrojel yapısı ile hücre etkileşimini teşvik etmek için PEG-PLA polimerine hücre yapışkanlı RGD peptitler tutturuldu. Kapsüllenmiş hücreler bu yapışıklık motifleri ile formülasyonlarda kapsüllenmiş hücrelere kıyasla çoğalamadığı için yapışıklık bölgelerinden yoksun formülasyonlar düşük hücre canlılığına sahip olacaktır (Şekil 5a,b). Kapsüllenmiş hücreler, floresan mikroskopla hücre sayımını kolaylaştırmak için kalsein veya başka bir uygun floresan boya (örneğin CFSE) ile etiketlenebilir. Optimizasyon sırasında, integrin fonksiyonel formülasyonlarının gelişmiş canlılık ve çoğalma sağladığına emin olmak için uygulanabilirlik değiştirilmemiş PNP hidrojelleri ile karşılaştırılmalıdır. Integrin fonksiyonelleştirilmiş formülasyonlar değiştirilmemiş hidrojellerle benzer etkinlik sağlıyorsa, bu yapışma motiflerini dahil etmek için kullanılan konjugasyon kimyasında bir arızaya işaret edebilir.
Araştırmacılar, uygun bir hidrojel formülasyonu kullanırken kapsüllenmiş hücrelerin hidrojel ortamına eşit olarak dağılmasını beklemelidir. Bu, hidrojel yönetimi sırasında hücrelerin tutarlı ve öngörülebilir bir şekilde dosing edilmesine izin verecektir ve uygulamadan sonra hidrojeldeki hücrelerin lokal tutulmasına çevrilmelidir. Floresan mikroskopi teknikleri kullanılarak hücrelerin dağılımı kolayca belirlenebilir. Hücreler uygun bir boya ile etiketlenebilir ve daha sonra konfokal mikroskopi kullanılarak görüntülenebilir. Görüntüler görsel olarak değerlendirilebilir (Şekil 5c) ve ayrıca imageJ yazılımı kullanılarak görüntünün dikey ekseni boyunca ortalama floresan yoğunluğunu ölçmek için (veya yerçekimi nedeniyle hangi eksende hücre yerleştirme olması bekleniyorsa) nicel olarak (Şekil 5d). Hidrojel formülasyonu, uzun zaman dilimleri boyunca süspansiyondaki hücreleri desteklemek için çok zayıfsa, Şekil 5'teki1:1 formülasyonunda gözlemlendiği gibi hücre yerleştirme meydana gelecektir. Polimer içeriğinin artırılması, yerleşmeye bağlı olarak inhomogeneöz hücre dağılımı ile ilgili sorunları çözebilir.
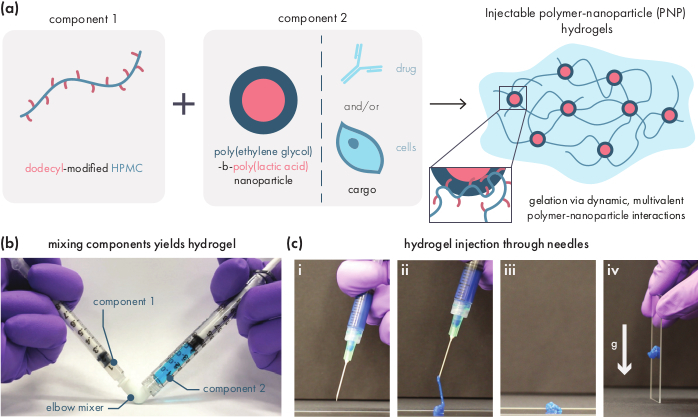
Şekil 1: Polimer-nanopartikül (PNP) hidrojelleri iki bileşen karıştırılarak kolayca oluşturulur. (a) İlk bileşen dodecyl modifiye hidroksipropimetil selüloz çözeltisi (HPMC-C12),ikinci bileşen ise herhangi bir terapötik kargo ile birlikte poli (etilen glikol)-blok-poli(laktik asit) (PEG-PLA) nanopartiküllerinin bir çözeltisidir. Bu iki bileşenin nazik bir şekilde karıştırılması, HPMC-C12 polimerlerinin PEG-PLA nanopartikülleri ile dinamik, çok değerli etkileşimlerle fiziksel olarak birbirine bağlı olduğu enjekte edilebilir bir hidrojel sağlar. (b) Her biri PNP hidrojelinin bir bileşenini içeren iki şırınna ile karıştırılarak jel formülasyonunun gösterildiği fotoğraf. İki şırınnayı bir Luer-lock dirsek konektörü ile bağlayarak, iki bileşen steril koşullar altında kolayca karıştırılarak, anında kullanım için bir şırıncaya önceden yüklenmiş kabarcıksız bir hidrojel elde edilebilir. NP çözümü gösteri amacıyla maviye boyanır. (c) PNP hidrojellerinin enjeksiyonunun ve yeniden katılaşmasının gösterimi. (i) PNP hidrojel bağlı bir şırınga içinde 21G iğne. (ii) Enjeksiyon, hidrojelleri polimer ve nanopartiküller arasındaki etkileşimleri geçici olarak bozan kesmenin altına yerleştirir ve sıvı benzeri bir kıvam oluşturur. (iii) Enjeksiyon sonrası, dinamik polimer-nanopartikül etkileşimleri hızla reform yaparak hidrojelin kendi kendine iyileşmesine izin verir. (iv) Katı hidrojel, yerçekimi gibi verim stresinden daha zayıf kuvvetler altında akmaz. PNP hidrojel gösteri amacıyla maviye boyanmıştır. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.
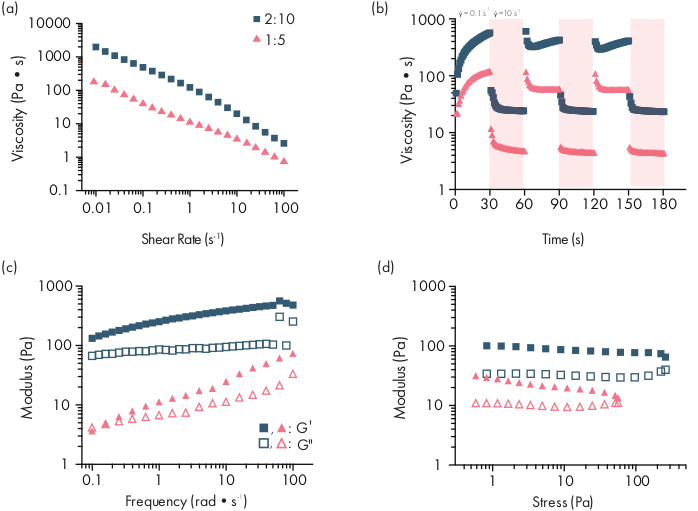
Şekil 2: İki PNP hidrojel formülasyonunun reolojik karakterizasyonu. Formülasyonlar polimer wt.%: NP wt.%olarak gösterilir. (a)Sabit kesme akışı, PNP hidrojellerinin düşükten yüksek kesme hızına kadar süpürülür. Kesme hızının bir fonksiyonu olarak viskozite, kesme inceltme özelliklerini karakterize eder. (b)PNP hidrojellerinin kendi kendini iyileştiren özelliklerini gösteren düşük kesme hızları (beyaz arka plan; 0,1 s−1)ile yüksek kesme hızları (kırmızı arka plan; 10 s−1)arasındaki kesme hızlarını salınma işlevinin viskozitesi. Kesme oranları her biri 30 s için uygulanır. (c) Elastik depolama modülü G′ ve viskoz kayıp modülü G" çeşitli PNP hidrojel formülasyonları için sabit bir% 1 suşta frekans fonksiyonu olarak. (d) Genlik, PNP hidrojellerinin elastik depolama modülü G′ ve viskoz kayıp modülü G" yi stresin bir fonksiyonu olarak karakterize etmek için 10 rad / s sabit bir frekansta süpürür. Bu reolojik karakterizasyon, kalite kontrolü için karşılaştırma olarak kullanılabilir. Bu rakam Grosskopf ve ark.28'den uyarlanmıştır.
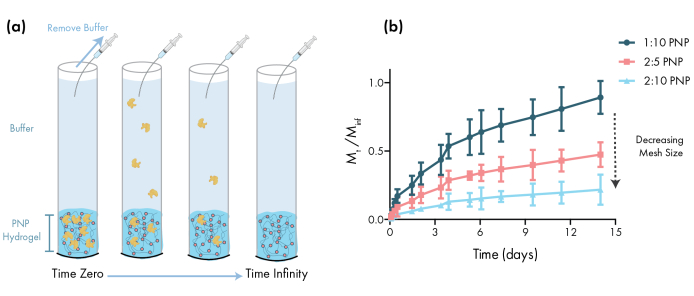
Şekil 3: PNP hidrojellerinden sığır serum albüminin (BSA) in vitro salınımı. Formülasyonlar polimer wt.%: NP wt.%olarak gösterilir. (a)Deneysel in vitro salınım protokolünü açıklayan şematik. Aliquots zamanla PNP hidrojel yüklü kılcal borulardan çıkarılır. (b) BSA'nın 1:10 PNP, 2:5 PNP ve 2:10 PNP'den in vitro salınımı, belirtilen zaman noktası tarafından toplanan kütlenin test sırasında toplanan toplam kütleye bölünmesi olarak rapor edilir (SD'± ortalama olarak gösterilen veriler; n = 3). Absorbans ölçümleri ile BSA tespit edildi. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.
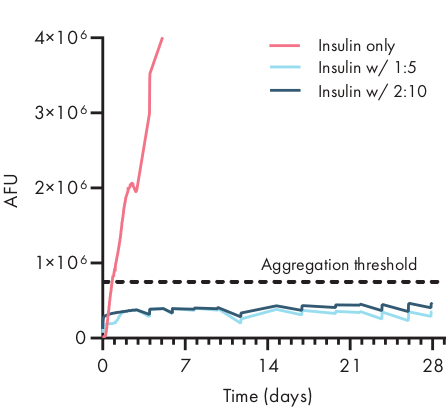
Şekil 4: PNP hidrojellerinde kapsüllenen insülinin termal stabilitesi ThT tahlili ile. Formülasyonlar polimer wt.%: NP wt.%olarak gösterilir. Hem 1:5 hem de 2:10 PNP hidrojelde kapsüllenen insülin, 37 °C'lik stresli yaşlanma koşullarında ve sürekli ajitasyonda 28 günden fazla bir süre boyunca kontrolsüz kaldı. PBS'de formüle edilen insülin toplama süresi 20 ± 4 saatti (ortalama ± SD, toplama eşiği 750.000 AFU). Ortalama olarak sunulan veriler n = 4 deneysel kopya (AFU, keyfi floresan birimleri). Bu rakam Meis ve ark.38'den uyarlanmıştır.
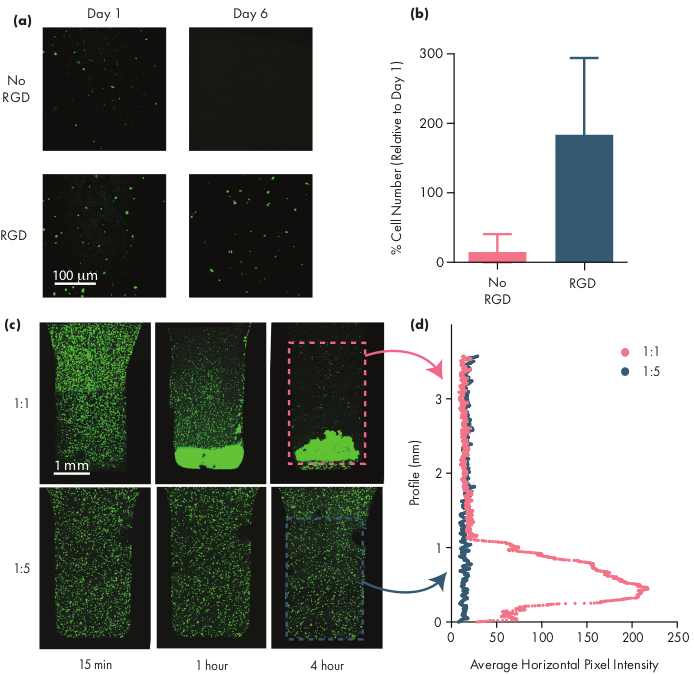
Şekil 5: PNP hidrojellerinde hücre canlılığı ve hücre yerleşimi. (a,b) PNP hidrojellerinde insan mezenkimal kök hücreli hücre canlılığı çalışmaları (hMSC'ler). (a)PEG-PLA NP'lerine konjuge edilen hücre yapışkan arginin-glisine-aspartik asit (RGD) motifi ile 1:5 PNP hidrojellerde uygulanabilir hMSC'lerin temsili görüntüleri konfokal görüntülemeden önce 30 dakika boyunca kalsenin lekeliydi. Ölçek çubuğu 100 μm'yi temsil eder. (b) 6. günde hücre canlılığı, 1. günde floresan hücre sayısına göre görüntüdeki floresan hücre sayısı olarak tanımlanır (veriler SD ± ortalama olarak gösterilir; n = 3). (c,d) HMSC'lerle hücre kapsülleme ve yerleştirme deneyleri. (c) Hücre yerleşimini ölçmek için 4 saat boyunca 1:1 PNP hidrojel (üst sıra) ve 1:5 PNP hidrojel (alt sıra) kapsüllenmiş kalsenin lekeli hMSC'lerin maksimum yoğunluklu görüntüleri. Ölçek çubuğu 1 mm' dir. (d) Hidrojelin dikey profili boyunca hMSC'lerin ortalama yatay piksel yoğunluğunu temsil eder. Bu rakam Grosskopf ve ark.28'den uyarlanmıştır.
Tartışmalar
Polimer-Nanopartikül (PNP) hidrojelleri kolayca imal edilir ve terapötik hücrelerin ve ilaçların doğrudan enjeksiyon veya kateter teslimatı yoluyla minimal invaziv uygulama yoluyla uzun süreli yerel olarak teslim edilmesini sağlar. Bu protokoller PNP hidrojellerinin formülasyonunu ve elde eden malzemelerin kalitesini güvence altına alma için karakterizasyon yöntemlerini açıklar. Supramoleküler PNP hidrojeller üretilebilir ve modifiye selüloz polimerleri ve polimerik çekirdek kabuklu nanopartiküllerin basit bir şekilde karıştırılmasıyla oluşur. Bu yöntemler, basit dirsek karıştırma protokolleri aracılığıyla şırıngamlara önceden yüklenmiş jeller oluşturmak için facile prosedürlerini açıklar. NP boyutunu ve dağıtımını izlemek için DLS gibi bileşen parçalarının her birinin kalite kontrol ölçümleri sayesinde, tutarlı reolojik özelliklere sahip PNP hidrojel malzemeleri yeniden formüle edilebilir. HPMC-C12 veya NP miktarını değiştirerek, elde edilen PNP hidrojelinin ağ boyutunu ve sertliğini modüle edebilirsiniz. Bu özellikler belirli bir biyomedikal uygulamaya en uygun şekilde ayarlanabilir ve burada ayrıntılı olarak açıklanan reolojik yöntemlerle araştırmacılar, platformu özel uygulamaları için optimize ettikleri için PNP hidrojellerinin kesme inceltme ve kendi kendini iyileştirme özelliklerini karakterize edebilir. Tüp bebek salınım çalışmaları için yöntemler de açıklanmıştır; araştırmacılar bu çalışmaları, gelecekteki in vivo çalışmaları bilgilendirerek, ilgi çekici ilaçların serbest bırakılmasının göreceli zaman ölçeğini karakterize etmek için kullanabilirler. Araştırmacılar, stabilite çalışmalarını kullanarak, biyoterapötiklerin soğuk zincir bağımlılığını azaltmak için zorlayıcı potansiyel uygulamalarla, hassas biyoterapötiklerin biyolojik yapısını ve stabilitesini zaman içinde ve aşırı sıcaklıklarda korumaya yardımcı olmak için bu malzemelerin yeteneğini de değerlendirebilirler. Son olarak, basit hücre canlılığı tahlilleri ile hücre büyümesi ve PNP malzemeleri içindeki göç, hücre tedavileri ve iskelelerdeki potansiyel uygulamalarla değerlendirilebilir.
Grubumuz PNP hidrojel platformu27için birçok zorlayıcı uygulama buldu. PNP hidrojelleri, antijenlerin ve yardımcıların eşleşen kinetik salınım profillerinin humoral immün yanıtın büyüklüğünü, süresini ve kalitesini artırmak için mümkün olan alt ünvan aşılarının yavaş teslimi için kullanılmıştır31. PNP hidrojellerinin en sık kullanılan hidrojellerden daha küçük bir ağ boyutuna sahip olduğu bulunmuştur, bu nedenle difüzyonu yavaşlatmada ve moleküler yükü yavaşça serbest bırakmada etkilidirler. PNP hidrojellerin benzersiz doku yapışma özellikleri ve mekanik özellikleri, hidrojellerin ameliyattan sonra organların geniş yüzey alanlarına püskürtülerek ameliyattan kaynaklanan yapışıklıkları önlemek için fiziksel bariyerler oluşturmak için de kullanılmıştır30. PNP hidrojellerinin de etkili hücre dağıtım araçları olduğu gösterilmiştir ve mekanik özellikler aslında enjeksiyon sırasında şırınga iğnesinde meydana gelen mekanik kuvvetlerden hücreleri korur, hücre canlılığını artırır29. NP'ler bir hücre yapışkan peptidi ile eşlendiğinde, hücreler uygulanabilir kalmak için PNP matrisini takabilir ve bunlarla etkileşime girebilir. Bu yaklaşımı kullanarak, PNP hidrojellerinin sıvı araçları kullanan yöntemlere kıyasla enjekte edilen kök hücrelerin lokal tutulmasını iyileştirdiği gösterilmiştir28. Ek olarak, PNP hidrojellerinin, sert stresli yaşlanma koşullarında bile kapsüllenmiş insülinin termal olarak indüklenen toplanmasını önlediği gösterilmiştir, bu da bu malzemelerin sıcaklığa duyarlı ilaçları soğutma ihtiyacını azaltabileceğini düşündürmektedir38.
Genel olarak, burada açıklanan metodolojiler, araştırma gruplarının PNP hidrojellerini biyomalzeme olarak üretip keşfetmelerine izin verecektir. Bu protokoller, hem in vitro hem de in vivo çalışmaları sürdürmek için yeterli hidrojel malzemeyi imal etmek için laboratuvar ölçeğinde sentez teknikleri sağlar. Yukarıda açıklanan çalışmalar, bu malzemelerin dinamik çapraz bağlantılarının, moleküler kargonun pasif difüzyonunu kısıtlarken, tuzaklı hücrelerin aktif hareketliliğine izin vererek bir dizi biyomedikal uygulama için uygun olmasını sağladığını göstermektedir. Araştırmacıların PNP platformunu kontrollü ilaç dağıtımı yoluyla klinik sonuçları iyileştirmek ve hücre alımı ve mekanobiyoloji gibi temel biyolojik mekanizmaları incelemek için erişilebilir ve güçlü bir araç bulmaları bekmektedir.
Açıklamalar
Bu yazarların açıklayacak bir şeyi yok.
Teşekkürler
Bu araştırma Bill & Melinda Gates Vakfı (OPP1113682) ve Bill & Melinda Gates Vakfı (OPP1211043) ile İnsan Sistemleri İmmünoloji Merkezi tarafından finansal olarak desteklendi. C.M.M. Stanford Lisansüstü Bursu ve Stanford Bio-X William ve Lynda Steere Bursu tarafından desteklendi. A.K.G. Ulusal Bilim Vakfı Lisansüstü Araştırma Bursu ve Stanford Fen ve Mühendislik Lisansüstü Bursu Gabilan Bursu için minnettardır. S.C., Ulusal Sağlık Enstitüleri Ulusal Kanser Enstitüsü tarafından F32CA247352 Ödül Numarası altında desteklendi. Yazarlar ayrıca Dr. Gillie Roth, Dr. Anthony Yu, Dr. Lyndsay Stapleton, Dr. Hector Lopez Hernandez, Dr. Andrea d'Aquino, Dr. Julie Baillet, Celine Liong, Ben Ou, Emily Meany, Emily Gale ve Dr. Anton Smith gibi Appel Lab üyelerini, Appel Lab'ın bu protokolleri geliştirmesine yardımcı olma çabaları ve zamanları için sıcak bir şekilde kabul etmek istiyor.
Malzemeler
| Name | Company | Catalog Number | Comments |
| 21G needles | BD | 305165 | PNP hydrogel injection |
| 22G, 4 in hypodermic needles | Air-Tite | N224 | In vitro release studies |
| 384-well plates, black, clear bottom | Corning | 3540 | Dynamic light scattering (DLS) |
| 96-well plates, black | Fisher Scientific | 07-200-627 | Biostability studies |
| 96-well plates, clear | Corning | 3599 | Cell viability and settling studies |
| Calcein AM | Thermo Fisher Scientific | C3100MP | Cell viability and settling studies |
| Capillary tubes | McMaster-Carr | 8729K66 | In vitro release studies |
| Centrifugal filter units | Fisher Scientific | UFC901024 | NP concentration |
| Cuvettes | Millipore Sigma | BR759015-100EA | Cell viability and settling studies |
| DLS Plate Reader | Wyatt Technology | DynaPro II Plate Reader | Dynamic light scattering (DLS) |
| Epoxy | VWR International | 300007-392 (EA) | In vitro release studies |
| Hypodermic needles | Air-Tite | 8300015027 | In vitro release studies |
| Luer elbow connector | Cole-Parmer | EW-30800-12 | PNP hydrogel formulation |
| Luer lock syringe | Fisher Scientific | 14-955-456 | PNP hydrogel formulation |
| Phosphate Buffered Saline (1x) | Fisher Scientific | 10010049 | PNP hydrogel formulation |
| Plastic Spatula | Thomas Scientific | 1229F13 | Rheological characterization |
| Plate Reader | BioTek | Synergy H1 Hybrid Multi-Mode Plate Reader | Biostability studies |
| Plate seals | Excel Scientific | TS-RT2-100 | Biostability studies |
| Recombinant human insulin | Gibco | A11382II | Biostability studies |
| Rheometer | TA Instruments | DHR-2 Rheometer | Rheological characterization |
| Thioflavin T | Sigma-Aldrich | T3516-5G | Biostability studies |
Referanslar
- Mandal, A., Clegg, J. R., Anselmo, A. C., Mitragotri, S. Hydrogels in the clinic. Bioengineering Translational Medicine. 5 (2), 10158 (2020).
- Appel, E. A., del Barrio, J., Loh, X. J., Scherman, O. A. Supramolecular polymeric hydrogels. Chemical Society Reviews. 41 (18), 6195-6214 (2012).
- Mann, J. L., Yu, A. C., Agmon, G., Appel, E. A. Supramolecular polymeric biomaterials. Biomaterials Science. 6 (1), 10-37 (2018).
- Foster, A. A., Marquardt, L. M., Heilshorn, S. C. The diverse roles of hydrogel mechanics in injectable stem cell transplantation. Current Opinion in Chemical Engineering. 15, 15-23 (2017).
- Aguado, B. A., Mulyasasmita, W., Su, J., Lampe, K. J., Heilshorn, S. C. Improving viability of stem cells during syringe needle flow through the design of hydrogel cell carriers. Tissue Engineering Part A. 18 (7-8), 806-815 (2012).
- Marquardt, L. M., Heilshorn, S. C. Design of injectable materials to improve stem cell transplantation. Current Stem Cell Reports. 2 (3), 207-220 (2016).
- Guvendiren, M., Burdick, J. A. Engineering synthetic hydrogel microenvironments to instruct stem cells. Current Opinion in Biotechnology. 24 (5), 841-846 (2013).
- Marquardt, L. M., et al. Designer, injectable gels to prevent transplanted Schwann cell loss during spinal cord injury therapy. Science Advances. 6 (14), 1039 (2020).
- Stephan, S. B., et al. Biopolymer implants enhance the efficacy of adoptive T-cell therapy. Nature Biotechnology. 33 (1), 97-101 (2015).
- Tuladhar, A., et al. Injectable hydrogel enables local and sustained co-delivery to the brain: two clinically approved biomolecules, cyclosporine and erythropoietin, accelerate functional recovery in rat model of stroke. Biomaterials. 235, 119794 (2020).
- Pakulska, M. M., Miersch, S., Shoichet, M. S. Designer protein delivery: From natural to engineered affinity-controlled release systems. Science. 351 (6279), (2016).
- Gupta, D., Tator, C. H., Shoichet, M. S. Fast-gelling injectable blend of hyaluronan and methylcellulose for intrathecal, localized delivery to the injured spinal cord. Biomaterials. 27 (11), 2370-2379 (2006).
- Verbeke, C. S., Mooney, D. J. Injectable, pore-forming hydrogels for in vivo enrichment of immature dendritic cells. Advanced Healthcare Materials. 4 (17), 2677-2687 (2015).
- Tous, E., Purcell, B., Ifkovits, J. L., Burdick, J. A. Injectable acellular hydrogels for cardiac repair. Journal of Cardiovascular Translational Research. 4 (5), 528-542 (2011).
- Zhao, X., et al. Antibacterial anti-oxidant electroactive injectable hydrogel as self-healing wound dressing with hemostasis and adhesiveness for cutaneous wound healing. Biomaterials. 122, 34-47 (2017).
- Johnson, T. D., Christman, K. L. Injectable hydrogel therapies and their delivery strategies for treating myocardial infarction. Expert Opinion on Drug Delivery. 10 (1), 59-72 (2013).
- Kleinman, H. K., Martin, G. R. . Seminars in Cancer Biology. , 378-386 (2005).
- Hickey, J. W., et al. Engineering an artificial T-cell stimulating matrix for immunotherapy. Advanced Materials. 31 (23), 1807359 (2019).
- Baumann, M. D., et al. An injectable drug delivery platform for sustained combination therapy. Journal of Controlled Release. 138 (3), 205-213 (2009).
- Trappmann, B., et al. Matrix degradability controls multicellularity of 3D cell migration. Nature Communications. 8 (1), 1-8 (2017).
- Figueiredo, L., et al. Assessing glucose and oxygen diffusion in hydrogels for the rational design of 3D stem cell scaffolds in regenerative medicine. Journal of Tissue Engineering and Regenerative Medicine. 12 (5), 1238-1246 (2018).
- Daly, A. C., Riley, L., Segura, T., Burdick, J. A. Hydrogel microparticles for biomedical applications. Nature Reviews Materials. , 1-24 (2019).
- Chaudhuri, O., et al. Substrate stress relaxation regulates cell spreading. Nature Communications. 6 (1), 1-7 (2015).
- Cai, L., Dewi, R. E., Heilshorn, S. C. Injectable hydrogels with in situ double network formation enhance retention of transplanted stem cells. Advanced Functional Materials. 25 (9), 1344-1351 (2015).
- Fisher, S. A., Baker, A. E., Shoichet, M. S. Designing peptide and protein modified hydrogels: selecting the optimal conjugation strategy. Journal of the American Chemical Society. 139 (22), 7416-7427 (2017).
- Li, R. H., Altreuter, D. H., Gentile, F. T. Transport characterization of hydrogel matrices for cell encapsulation. Biotechnology and Bioengineering. 50 (4), 365-373 (1996).
- Appel, E. A., et al. Self-assembled hydrogels utilizing polymer-nanoparticle interactions. Nature Communications. 6 (6295), (2015).
- Grosskopf, A. K., et al. Injectable supramolecular polymer-nanoparticle hydrogels enhance human mesenchymal stem cell delivery. Bioengineering and Translational Medicine. 5 (1), 10147 (2020).
- Lopez Hernandez, H., Grosskopf, A. K., Stapleton, L. M., Agmon, G., Appel, E. A. Non-newtonian polymer-nanoparticle hydrogels enhance cell viability during injection. Macromolecular Bioscience. 19 (1), (2019).
- Stapleton, L. M., et al. Use of a supramolecular polymeric hydrogel as an effective post-operative pericardial adhesion barrier. Nature Biomedical Engineering. 3 (8), 611-620 (2019).
- Roth, G. A., et al. Injectable hydrogels for sustained codelivery of subunit vaccines enhance humoral immunity. ACS Central Science. , (2020).
- Steele, A. N., et al. A biocompatible therapeutic catheter-deliverable hydrogel for in situ tissue engineering. Advanced Healthcare Materials. 8 (5), 1801147 (2019).
- Fenton, O. S., et al. Injectable polymer-nanoparticle hydrogels for local immune cell recruitment. Biomacromolecules. 20 (12), 4430-4436 (2019).
- Yu, A. C., Smith, A. A., Appel, E. A. Structural considerations for physical hydrogels based on polymer-nanoparticle interactions. Molecular Systems Design & Engineering. 5 (1), 401-407 (2020).
- Wisdom, K., Chaudhuri, O., Koledova, Z. . 3D Cell Culture: Methods and Protocols. , 29-37 (2017).
- Lohmeijer, B. G., et al. Guanidine and amidine organocatalysts for ring-opening polymerization of cyclic esters. Macromolecules. 39 (25), 8574-8583 (2006).
- Cheng, J., et al. Formulation of functionalized PLGA-PEG nanoparticles for in vivo targeted drug delivery. Biomaterials. 28 (5), 869-876 (2007).
- Meis, C. M., et al. Self-assembled, dilution-responsive hydrogels for enhanced thermal stability of insulin biopharmaceuticals. ACS Biomaterials Science & Engineering. , (2020).
- Franck, A., Germany, T. Viscoelasticity and dynamic mechanical testing. TA Instruments. , (1993).
- Appel, E. A., et al. Self-assembled hydrogels utilizing polymer-nanoparticle interactions. Nature Communications. 6, 6295 (2015).
- Gallastegui, A., et al. Controlled release of antibiotics from photopolymerized hydrogels: kinetics and microbiological studies. Materials Science and Engineering: C. 102, 896-905 (2019).
- Qiao, M., Chen, D., Ma, X., Liu, Y. Injectable biodegradable temperature-responsive PLGA-PEG-PLGA copolymers: synthesis and effect of copolymer composition on the drug release from the copolymer-based hydrogels. International Journal of Pharmaceutics. 294 (1-2), 103-112 (2005).
- Schlein, M. Insulin Formulation Characterization-The Thioflavin T Assays. The AAPS Journal. 19 (2), 397-408 (2017).
- Preibisch, S., Saalfeld, S., Tomancak, P. Globally optimal stitching of tiled 3D microscopic image acquisitions. Bioinformatics. 25 (11), 1463-1465 (2009).
- Sakas, G., Grimm, M., Savopoulos, A. . EUROGRAPHICS workshop on Rendering Techniques. , 51-63 (1995).
- Axpe, E., et al. A multiscale model for solute diffusion in hydrogels. Macromolecules. 52 (18), 6889-6897 (2019).
- Peppas, N., Bures, P., Leobandung, W., Ichikawa, H. Hydrogels in pharmaceutical formulations. European Journal of Pharmaceutics and Biopharmaceutics. 50 (1), 27-46 (2000).
- Ritger, P. L., Peppas, N. A. A simple equation for description of solute release I. Fickian and non-fickian release from non-swellable devices in the form of slabs, spheres, cylinders or discs. Journal of Controlled Release. 5 (1), 23-36 (1987).
- Reinhart, C. T., Peppas, N. A. Solute diffusion in swollen membranes. Part II. Influence of crosslinking on diffusive properties. Journal of Membrane Science. 18, 227-239 (1984).
- Salinas, C. N., Anseth, K. S. The influence of the RGD peptide motif and its contextual presentation in PEG gels on human mesenchymal stem cell viability. Journal of Tissue Engineering and Regenerative. 2 (5), 296-304 (2008).
- Smith, A. A., et al. Nanoparticles presenting potent TLR7/8 agonists enhance anti-PD-L1 immunotherapy in cancer treatment. Biomacromolecules. 21 (9), 3704-3712 (2020).
Yeniden Basımlar ve İzinler
Bu JoVE makalesinin metnini veya resimlerini yeniden kullanma izni talebi
Izin talebiDaha Fazla Makale Keşfet
This article has been published
Video Coming Soon
JoVE Hakkında
Telif Hakkı © 2020 MyJove Corporation. Tüm hakları saklıdır