Se requiere una suscripción a JoVE para ver este contenido. Inicie sesión o comience su prueba gratuita.
Method Article
Virus pseudotipados como herramienta molecular para monitorizar las respuestas inmunitarias humorales contra el SARS-CoV-2 mediante ensayo de neutralización
* Estos autores han contribuido por igual
En este artículo
Resumen
Los virus pseudotipados (PV) son viriones con replicación defectuosa que se utilizan para estudiar las interacciones huésped-virus en condiciones más seguras que la manipulación de virus auténticos. Aquí se presenta un protocolo detallado que muestra cómo se pueden usar los PV del SARS-CoV-2 para probar la capacidad neutralizante del suero de los pacientes después de la vacunación contra el COVID-19.
Resumen
Los virus pseudotipados (PV) son herramientas moleculares que se pueden utilizar para estudiar las interacciones huésped-virus y para probar la capacidad neutralizante de muestras de suero, además de su uso más conocido en terapia génica para la administración de un gen de interés. Los PV son defectuosos en la replicación porque el genoma viral se divide en diferentes plásmidos que no se incorporan a los PV. Este sistema seguro y versátil permite el uso de fotovoltaicos en laboratorios de nivel 2 de bioseguridad. Aquí, presentamos una metodología general para producir PVs lentivirales basada en tres plásmidos como se menciona aquí: (1) el plásmido de la columna vertebral que lleva el gen reportero necesario para monitorear la infección; (2) el plásmido de empaquetamiento que transporta los genes de todas las proteínas estructurales necesarias para generar las PV; (3) el plásmido de expresión de glicoproteínas de la superficie de la envoltura que determina el tropismo del virus y media la entrada del virus en la célula huésped. En este trabajo, la espícula del SARS-CoV-2 es la glicoproteína de la envoltura utilizada para la producción de lentivirus pseudotipados no replicativos del SARS-CoV-2.
Brevemente, las células de empaquetamiento (HEK293T) se transfectaron conjuntamente con los tres plásmidos diferentes utilizando métodos estándar. Después de 48 h, el sobrenadante que contenía los PV se recolectó, filtró y almacenó a -80 °C. La infectividad de los PV del SARS-CoV-2 se probó mediante el estudio de la expresión del gen reportero (luciferasa) en una línea celular diana 48 h después de la infección. Cuanto mayor sea el valor de las unidades de luminiscencia relativa (RLU), mayor será la tasa de infección/transducción. Además, los PV infecciosos se añadieron a las muestras de suero diluidas en serie para estudiar el proceso de neutralización de la entrada de los pseudovirus en las células diana, medido como la reducción de la intensidad de RLU: valores más bajos correspondientes a una alta actividad neutralizante.
Introducción
Los virus pseudotipados (PV) son herramientas moleculares utilizadas en microbiología para estudiar las interacciones huésped-virus y patógeno-patógeno 1,2,3,4. Los PV constan de una parte interna, el núcleo viral que protege el genoma viral, y una parte externa, las glicoproteínas de la envoltura en la superficie del virus que define el tropismo5. Un pseudovirus es incompetente para la replicación en la célula diana porque no contiene toda la información genética necesaria para generar nuevas partículas virales. Esta combinación de características peculiares hace que los PV sean una alternativa segura a un virus de tipo salvaje. Los virus de tipo salvaje, por otro lado, son altamente patógenos y no se pueden utilizar en los laboratorios BSL 2 para su análisis6.
La infectividad de las PV puede ser monitoreada por un gen reportero, generalmente codificando una proteína fluorescente (GFP, RFP, YFP) o una enzima que produce productos quimioluminiscentes (luciferasa). Este está contenido en uno de los plásmidos utilizados para la producción de PV e incorporado en el genoma del pseudovirus7.
Actualmente existen varios tipos de núcleos fotovoltaicos, incluidas las partículas derivadas de lentivirus basadas en el genoma del VIH-1. La gran ventaja de las PV basadas en VIH-1 frente a otras plataformas es su proceso de integración intrínseca en el genoma de la célula diana8. Aunque el VIH-1 es un virus altamente contagioso y es el agente causal del SIDA, estos vectores lentivirales son seguros de usar debido a los extensos pasos de optimización a lo largo de los años. Las condiciones óptimas de seguridad se lograron con la introducción de vectores lentivirales de2ª generación, en los que los genes virales se agotaron sin influir en las capacidades de transducción9. La3ª y4ª generación contribuyeron a aumentar la seguridad del manejo de vectores lentivirales con la división adicional del genoma viral en plásmidos separados10,11. Las últimas generaciones de PV se emplean generalmente para producir vectores lentivirales para la terapia génica.
Los PV se pueden utilizar para estudiar las interacciones entre los virus y las células huésped, tanto durante la fase de producción como durante la infección. Los PV se emplean especialmente en ensayos de neutralización de pseudovirus (PVNA). Los PVNA están ampliamente validados para evaluar el potencial de neutralización del suero o el plasma al dirigirse a la glicoproteína viral en la envoltura del PV12,13. La actividad de neutralización, expresada como la concentración inhibitoria 50 (IC50), se define como la dilución de suero/plasma que bloquea el 50% de la entrada de partículas virales14. En este protocolo, describimos la configuración de un PVNA para probar la actividad de anticuerpos contra el Síndrome Respiratorio Agudo Severo - Coronavirus 2 (SARS-CoV-2) en sueros recolectados antes y después de recibir una dosis de vacuna de refuerzo.
Protocolo
El presente protocolo ha sido aprobado y sigue las directrices del Comité de Ética de la Universidad de Verona (protocolo de aprobación número 1538). Se obtuvo el consentimiento informado por escrito de los sujetos humanos que participaron en el estudio. Se recolectaron muestras de sangre entera de trabajadores de la salud voluntarios que estaban en proceso de recibir vacunas contra el SARS-CoV-2. Estas muestras fueron colectadas en tubos de plástico que contenían anticoagulantes para el posterior aislamiento del suero15.
Todos los procesos siguientes deben realizarse en una campana biológica de Clase 2, trabajando en condiciones estériles. El manejo de virus debe realizarse con cuidado y todos los productos de desecho deben neutralizarse en una solución de lejía diluida. En la Figura 1 se muestra una descripción general del protocolo.
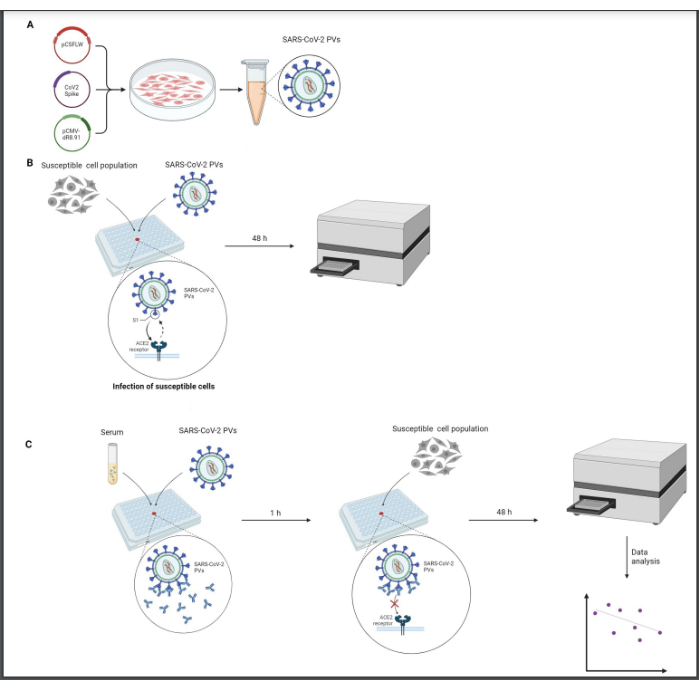
Figura 1: Representación gráfica de un ensayo de neutralización. (A) producción de energía fotovoltaica, (B) valoración de energía fotovoltaica y (C) ensayo de neutralización. Todos los procedimientos se realizan en una campana biológica de clase 2 en condiciones estériles. Es necesario realizar el paso de valoración (B) para estandarizar los niveles de infectividad de los PV antes de su uso en el ensayo de neutralización (C). Esta figura fue creada con BioRender. Haga clic aquí para ver una versión más grande de esta figura.
1. Prueba de producción e infectividad de PVs del SARS-CoV-2
- Siembre 5 x 105 células HEK293T en el medio Eagle modificado completo de Dulbecco (DMEM, alto contenido de glucosa, 10 % de suero fetal bovino (FBS), 1 % de L-glutamina, 1 % de penicilina/estreptomicina) en una placa de 6 pocillos (6WP) para alcanzar una densidad celular adecuada compatible con el reactivo de transfección utilizado. En el caso de realizar la transfección con polietilenimina (PEI) (preparar el reactivo siguiendo las instrucciones del fabricante), asegúrese de que las células alcancen el 40-60% de densidad el día de la transfección (paso 1.3). Mantener las células en una incubadora humidificada a 37 °C y 5% de CO2.
- Antes de la transfección, reemplace el medio celular gastado con medio fresco sin antibióticos (DMEM, alto contenido de glucosa, 10% de FBS, 1% de L-glutamina) para lograr una mayor eficiencia de transfección.
NOTA: Al día siguiente de la siembra, HEK293T células están listas para ser transfectadas. - Transfecte las células HEK293T adherentes con un reactivo de transfección adecuado de acuerdo con las instrucciones del fabricante. Si usa PEI, prepare dos mezclas y siga los pasos a continuación.
- Para preparar la mezcla A, agregue 500 ng de plásmido de empaque16 de pCMV-dR8.91, 750 ng de plásmido reportero de pCSFLW16 y 450 ng de plásmido que expresa la espícula del SARS-CoV-2 en 100 μL de medio sérico reducido.
- Para preparar la mezcla B, añadir 17,5 μL de PEI (concentración: 1 mg/mL) a 100 μL del medio sérico reducido.
- Deje que ambas mezclas se incuben a temperatura ambiente (RT) durante 5 minutos. A continuación, mezcle el contenido de ambos tubos añadiendo la mezcla B de PEI a la mezcla de ADN A.
- Incuba el tubo durante 20-30 min a RT. Mueve el tubo suavemente cada 3-4 min para mejorar la mezcla. Finalmente, agregue la mezcla a las HEK293T celdas.
- 16-20 h después de la transfección, sustituya el medio de cultivo por DMEM fresco y completo. Incubar a 37 °C y 5% de CO2, para permitir la producción de PV por células transfectadas.
- 72 h después de la transfección, cosechar el sobrenadante que contiene PVs. A continuación, centrifugar a 1600 x g durante 7 min a temperatura ambiente para eliminar los restos celulares y las células muertas y filtrarlos a través de un filtro de acetato de celulosa de 0,45 μm.
- PASO OPCIONAL: Para aumentar el rendimiento final del título fotovoltaico, realice múltiples transfecciones, agrupe los medios celulares que contienen PV y concéntrelos utilizando tubos concentradores.
- Proceda directamente con los siguientes pasos ("Valoración de PVs", sección 2) o alícuota el medio que contiene PV en tubos adecuados para almacenarlo a -80 °C hasta su uso. Preparar una alícuota adicional (400-500 μL) que se utilizará para la valoración.
NOTA: La realización de múltiples alícuotas garantizará la reproducibilidad entre experimentos al evitar ciclos excesivos de descongelación y congelación.
2. Valoración de los PV
- Utilice el medio fresco que contiene PV para los siguientes pasos o descongele la alícuota de prueba (paso 1.7) para realizar la valoración de la nueva cepa viral. La congelación de las alícuotas del mismo stock fotovoltaico garantizará la reproducibilidad.
- Añadir 50 μL de DMEM completo (o medio completo compatible con la línea celular objetivo en uso) en todos los pocillos de una placa de 96 pocillos (96WP) necesaria para probar por duplicado el stock fotovoltaico, dejando vacía la fila "A". Agregue 100 μL de material de PV a la fila "A". En función del número de preparados que se vayan a analizar, deje una columna sin el virus como control de "solo células" (Figura 2).
- Pipetear 50 μL desde la fila A hasta la fila B y repetir este proceso hasta la fila G para obtener diluciones seriadas del stock inicial. Deseche el exceso de volumen de la última fila.
- Separar las células utilizando tripsina/ácido etilendiaminotetraacético 1x (EDTA) en solución salina tampón fosfato de Dulbecco 1x (DPBS 1x), después de retirar el medio gastado y lavar las células con DPBS 1x dos veces. Prepare las células a una densidad de 4 x 105 células/ml.
NOTA: En este protocolo, la infección por PVs se probó en la línea celular susceptible HEK293T/ACE2; dichas células se derivaron de HEK293T, transducidas utilizando un vector lentiviral para expresar el receptor ACE2. - Agregue 50 μL de la suspensión celular en cada pocillo para asegurar un recuento celular de 2 x 104 celdas por pocillo.
- Incubar a 37 °C y 5% de CO2, durante 48 h.
- Después de la incubación, realice el ensayo de luciferasa para obtener la lectura según las instrucciones del fabricante. Añadir 100 μL del reactivo luciferasa a los pocillos e incubar en la oscuridad a RT durante 2 min. Mueva el contenido de cada pocillo a una placa negra de 96 pocillos (compatible con el lector de placas disponible) y lea las placas en un lector de placas de 96 pocillos.
NOTA: El luminómetro utilizado para la lectura de la luciferasa producirá un archivo de hoja de cálculo con los datos sin procesar sin procesar que se utilizarán para el análisis posterior (en este caso, un archivo de Excel). La infectividad del virus se expresará como unidades de luminiscencia relativa (UGR) (descritas en el punto 4.1).
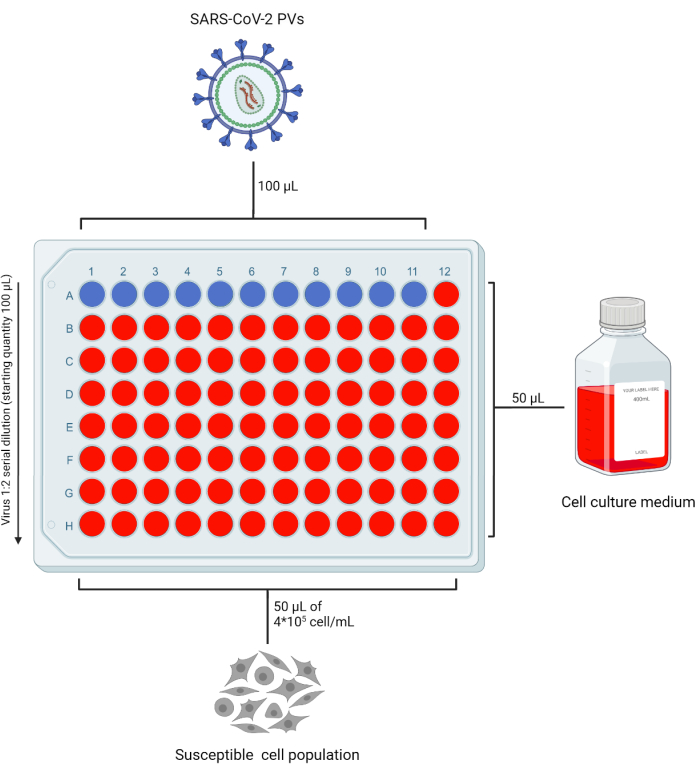
Figura 2: Diseño representativo de una placa de 96 pocillos para la valoración de fotovoltaicos. Se agrega un volumen fijo de sobrenadante que contiene PV a la fila A, columnas 1-11, y se diluye en serie. La última columna se deja como el control de "solo celda". Esta figura fue creada con BioRender. Haga clic aquí para ver una versión más grande de esta figura.
3. Ensayo de neutralización
- Descongele los sueros de los pacientes en hielo. Inactivar las muestras de suero incubándolas a 56 °C durante 30 min.
- En una placa de 96 pocillos, añadir 50 μL del DMEM fresco y completo (o medio completo compatible con la línea celular diana utilizada) en cada uno de los pocillos siguientes: desde la fila B (columnas 1-10) hasta la fila H (columnas 1-10). Coloque 95 μL del DMEM fresco y completo en la fila A (columnas 1-10). Agregue 50 μL y 100 μL de DMEM completo en los pocillos de las columnas 11 y 12, respectivamente. Estos serán los controles infectados (control de virus, o VC) y no infectados (solo célula, o CC), respectivamente (Figura 3).
- Añadir 5 μL de muestras de suero/plasma inactivado por calor en la fila A (columnas 1-10). Cada muestra estará duplicada. Con una pipeta multicanal, mezcle las muestras en la primera fila y mueva 50 μL de medio que contenga suero de la fila A a la fila B. Repita este proceso hasta la última fila (Figura 3). Deseche los 50 μL restantes.
- Descongelar el número necesario de alícuotas de PV y diluir a ≥ 104 RLU/mL. Añadir 50 μl del medio diluido que contiene PV a cada pocillo (de la columna 1 a la columna 11) utilizando una pipeta multicanal para alcanzar una dilución 1:1 de suero/plasma inactivado por calor al virus. Incubar a 37 °C y 5% de CO2, durante 1 h para permitir que los anticuerpos de las muestras de suero se unan a la proteína de la espícula del SARS-CoV-2 en los PV.
- Prepare al menos 5 ml de suspensión de células susceptibles (HEK293T/ACE2) a una densidad celular de 4 x 105 células/ml. Añadir 50 μL de la suspensión celular a cada pocillo e incubar a 37 °C y 5% de CO2, durante 48 h.
- Después de la incubación, realice la lectura del ensayo de luciferasa de acuerdo con las instrucciones del fabricante, como se describe en el paso 2.7.
NOTA: El luminómetro utilizado para la lectura de la luciferasa producirá un archivo de hoja de cálculo (en este caso, .xlsx) con los datos sin procesar que se utilizarán para el análisis posterior (el archivo de ensayo de luciferasa).
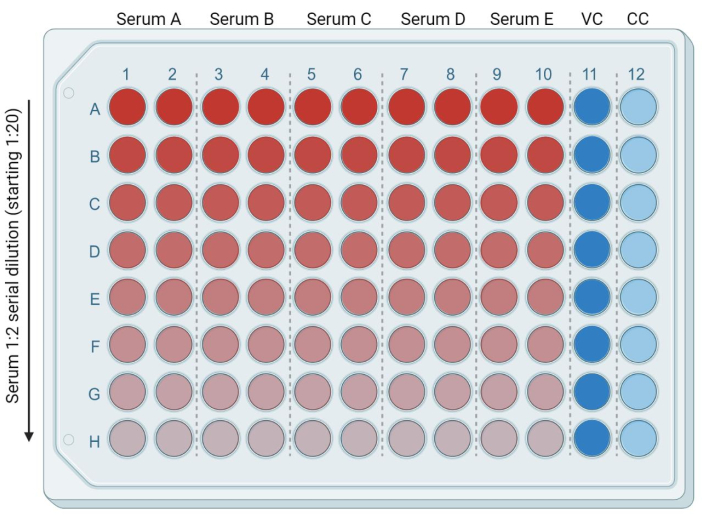
Figura 3: Representación en placa basada en la dilución sérica. El rojo brillante corresponde a una mayor cantidad de suero, y el azul brillante (columna 11) corresponde al control de células infectadas (VC, control de virus). El carril azul claro (columna 12) corresponde a las células no infectadas (CC, control de células). Esta figura fue creada con BioRender. Haga clic aquí para ver una versión más grande de esta figura.
4. Análisis de valoración
- En el archivo de ensayo de luciferasa, asigne los nombres/títulos a las muestras correspondientes.
- Multiplique la medida de RLU por los factores de dilución (de arriba a abajo de la cuadrícula: 20x, 40x, 80x, 160x, 320x, 640x, 1,280x, 2,560x) para obtener RLU/mL. Si se utilizan diferentes factores de dilución, cambie los factores de multiplicación en consecuencia.
- Calcule el promedio de RLU/mL para cada preparación fotovoltaica.
5. Análisis del ensayo de neutralización de PVs
- En el archivo de hoja de cálculo del ensayo de luciferasa (en este caso, .xlsx), asigne los títulos correspondientes a las muestras analizadas. Introduzca el factor de dilución de la muestra (40s, 80x, 160x, 320x, 640x, 1.280x, 2.560x, 5.120x). Calcular el Log10 de los factores de dilución.
- Calcule la RLU promedio de los controles no infectados e infectados (Figura 3, columnas 11 y 12, respectivamente). Estos valores serán útiles para la normalización en el paso 5.5.
- Abra un nuevo documento para el análisis de datos. Seleccione el análisis X/Y, ingrese X como Números e Y como Ingrese 2 valores de replicación en subcolumnas una al lado de la otra.
- Introduzca los valores de Log10 (dilución) como números X. Introduzca la RLU duplicada de las muestras.
- Vaya a Analizar > normalizar > marcar todas las muestras en la misma hoja. Introduzca los valores medios de VC y CC en ¿Cómo se define el 0%?, y ¿Cómo se define el 100%?, respectivamente. Haga clic en Aceptar.
- En la hoja de datos normalizada, vaya a Analizar análisis > XY > Análisis no lineales (ajuste de curva). Marque todas las muestras y haga clic en Aceptar. Para la dosis-respuesta - Inhibición, seleccione log(inhibidor) frente a respuesta normalizada - pendiente variable.
- En Constreñir, cambie HillSlope a Debe ser menor que 0.
- En Salida, marque Crear tabla de resumen y gráfico. Haga clic en Aceptar para obtener los análisis finales. En el Archivo Complementario 1 se proporciona una hoja de trabajo con una plantilla para el análisis.
Resultados
Este protocolo describe la producción de VP del SARS-CoV-2 y una aplicación posterior de estos PV para analizar la actividad neutralizante del suero/plasma de sujetos que reciben la vacuna anti-COVID-1917. Además, este protocolo se puede aplicar para producir pseudotipos de cada variante preocupante (VOC) del SARS-CoV-2 para probar la evolución de la respuesta neutralizante. A pesar de que este protocolo facilita el estudio de la respuesta inmune humoral después de la vacunación contra la CO...
Discusión
A pesar de que el uso de un virus de tipo salvaje simula la infección real, los PV lentivirales son una opción más segura para estudiar los mecanismos asociados con la entrada e infección viral sin los estrictos requisitos de seguridad necesarios para trabajar con virus patógenos 4,20,21. Los PV están compuestos por un núcleo viral de replicación defectuosa rodeado por la glicoproteína de la envoltura superficial de un ...
Divulgaciones
Los autores declaran no tener ningún conflicto de intereses.
Agradecimientos
Reconocemos la contribución de los trabajadores de la salud voluntarios. Este proyecto contó con el apoyo del Departamento de Excelencia 2023/2027, MUR, Italia. AR y DZ recibieron el apoyo de PRIN2022 (financiación de la UE; NextGenerationEU)
Materiales
| Name | Company | Catalog Number | Comments |
| 0.45 μm filter | SARSTEDT | 83 1826 | |
| 6-well plate | SARSTEDT | 83 3920 | |
| 96-well plate | SARSTEDT | 8,33,924 | |
| Amicon Ultra-15 Centrifugal Filter Units | Merck | 10403892 | |
| Black Opaque 96-well Microplate | Perkin Elmer | 60005270 | |
| Dulbecco's Modified Eagle Medium | SIGMA-ALDRICH | D6546 - 500ML | |
| Dulbecco's phosphate buffered saline (PBS 1x) | AUROGENE | AU-L0615-500 | |
| Foetal Bovine Serum | AUROGENE | AU-S1810-500 | |
| Graphpad Prism version 7 | graphpad dotmatics | NA | In the manuscript, we replace the commercial name with 'data analysis program' |
| HEK293T cells | ATCC | CRL-3216 | |
| HEK293T/ACE2 cells | ATCC | CRL-3216 | HEK293T has been transduced to overexpress ACE2 with a lentiviral vector. |
| L-glutamine | AUROGENE | AU-X0550-100 | |
| Luminometer - Victor3 | Perkin Elmer | HH35000500 | In the manuscript, we replace the commercial name with 'luminometer' |
| Opti-MEM | Thermo Fisher Scientific | 11058021 | In the manuscript, we replace the commercial name with 'reduced serum medium' |
| p8.91 packaging plasmid | Di Genova et al., 2021 | A kind gift from Prof. Nigel Temperton (ref 16.) | |
| pCSFLW reporter plasmid | Di Genova et al., 2021 | A kind gift from Prof. Nigel Temperton (ref 16.) | |
| Penicillin/streptomycin | AUROGENE | AU-L0022-100 | |
| Polyethylenimine, branched (PEI) (25 kDa) | SIGMA-ALDRICH | 408727 | |
| RRL.sin.cPPT.SFFV/Ace2.IRES-puro.WPRE (MT126) | Addgene | 145839 | This plasmid was used to generate HEK293Tcells/ACE2 |
| SARS-CoV-2 Spike expressing plasmid | Addgene | pGBW-m4137382 | |
| steadylite plus Reporter Gene Assay System | Perkin Elmer | 6066759 | In the manuscript, we replaced the commercial name with 'luciferase reading reagent' |
| Trypsin EDTA 1x | AUROGENE | AU-L0949-100 |
Referencias
- Ozaki, D. A., et al. International technology transfer of a GCLP-compliant HIV-1 neutralizing antibody assay for human clinical trials. Plos One. 7 (1), e30963 (2012).
- Pouget, M., et al. Generation of liposomes to study the effect of Mycobacterium tuberculosis lipids on HIV-1 cis- and trans-infections. International Journal of Molecular Sciences. 22 (4), 1945 (2021).
- McKay, L. G. A., et al. The HCV envelope glycoprotein down-modulates NF-κB signalling and associates with stimulation of the host endoplasmic reticulum stress pathway. Frontiers in Immunology. 13, 831695 (2022).
- Xiang, Q., Li, L., Wu, J., Tian, M., Fu, Y. Application of pseudovirus system in the development of vaccine, antiviral-drugs, and neutralizing antibodies. Microbiological Research. 258, 126993 (2022).
- Li, Q., Liu, Q., Huang, W., Li, X., Wang, Y. Current status on the development of pseudoviruses for enveloped viruses. Reviews in Medical Virology. 28, e1963 (2018).
- D'Apice, L., et al. Comparative analysis of the neutralizing activity against SARS-CoV-2 Wuhan-Hu-1 strain and variants of concern: Performance evaluation of a pseudovirus-based neutralization assay. Frontiers in Immunology. 13, 981693 (2022).
- Falzarano, D., Groseth, A., Hoenen, T. Development and application of reporter-expressing mononegaviruses: current challenges and perspectives. Antiviral Research. 103, 78-87 (2014).
- Gutierrez-Guerrero, A., Cosset, F. -. L., Verhoeyen, E. Lentiviral vector pseudotypes: Precious tools to improve gene modification of hematopoietic cells for research and gene therapy. Viruses. 12, 1016 (2020).
- Zufferey, R., Nagy, D., Mandel, R. J., Naldini, L., Trono, D. Multiply attenuated lentiviral vector achieves efficient gene delivery in vivo. Nature Biotechnology. 15 (9), 871-875 (1997).
- Dull, T. A third-generation lentivirus vector with a conditional packaging system. Journal of Virology. 72 (11), 8463-8471 (1998).
- Berkhout, B. A Fourth generation lentiviral Vector: Simplifying genomic gymnastics. Molecular Therapy. 25 (8), 1741-1743 (2017).
- Wu, X. Development and evaluation of a pseudovirus-luciferase assay for rapid and quantitative detection of neutralizing antibodies against Enterovirus 71. Plos One. 8 (6), e64116 (2013).
- Ferrara, F., et al. Development of lentiviral vectors pseudotyped with Influenza B hemagglutinins: application in vaccine immunogenicity, mAb potency, and sero-surveillance studies. Frontiers in Immunology. 12, 661379 (2021).
- Hu, J., et al. Development of cell-based pseudovirus entry assay to identify potential viral entry inhibitors and neutralizing antibodies against SARS-CoV-2. Genes & Diseases. 7 (4), 551-557 (2020).
- Dalle Carbonare, L., et al. Serology study after BTN162b2 vaccination in participants previously infected with SARS-CoV-2 in two different waves versus naïve. Communications Medicine. 1 (1), 38 (2021).
- Di Genova, C., et al. Production, titration, neutralisation, storage and lyophilisation of severe acute respiratory syndrome coronavirus 2 (SARS-CoV-2) lentiviral pseudotypes. Bio-protocol. 11 (21), e4236 (2021).
- Chmielewska, A. M., Czarnota, A., Bieńkowska-Szewczyk, K., Grzyb, K. Immune response against SARS-CoV-2 variants: The role of neutralization assays. NPJ Vaccines. 6 (1), 1-8 (2021).
- Chen, Q., et al. Development and optimization of a sensitive pseudovirus-based assay for HIV-1 neutralizing antibodies detection using A3R5 cells. Human Vaccines & Immunotherapeutics. 14 (1), 199-208 (2018).
- Gauger, P. C., Vincent, A. L. Serum virus neutralization assay for detection and quantitation of serum neutralizing antibodies to influenza A virus in swine. Methods in Molecular Biology (Clifton, N.J). 2123, 321-333 (2020).
- Miglietta, R., Pastori, C., Venuti, A., Ochsenbauer, C., Lopalco, L. Synergy in monoclonal antibody neutralization of HIV-1 pseudoviruses and infectious molecular clones. Journal of Translational Medicine. 12 (1), 346 (2014).
- Chen, M., Zhang, X. -. E. Construction and applications of SARS-CoV-2 pseudoviruses: A mini review. International Journal of Biological Sciences. 17 (6), 1574-1580 (2021).
- Zipeto, D., et al. Induction of human immunodeficiency virus neutralizing antibodies using fusion complexes. Microbes and Infection. 8 (6), 1424-1433 (2006).
- WHO Coronavirus (COVID-19) Dashboard. Available from: https://covid19.who.int (2022)
- Zhou, P. A pneumonia outbreak associated with a new coronavirus of probable bat origin. Nature. 579 (7798), 270-273 (2020).
- Chen, X., Huang, H., Ju, J., Sun, R., Zhang, J. Impact of vaccination on the COVID-19 pandemic in U.S. states. Scientific Reports. 12 (1), 1554 (2022).
- Stefani, C., Fantoni, T., Bissoli, M., Thomas, J., Ruggiero, A. HIV and SARS-CoV-2 Co-Infection: From Population Study Evidence to In Vitro Studies. Life. 12 (12), 2089 (2022).
- Watson, O. J., et al. Global impact of the first year of COVID-19 vaccination: a mathematical modelling study. The Lancet Infectious Diseases. 22 (9), 1293-1302 (2022).
- Cantoni, D. Analysis of antibody neutralisation activity against SARS-CoV-2 variants and seasonal human coronaviruses NL63, HKU1, and 229E induced by three different COVID-19 vaccine olatforms. Vaccines. 11 (1), 58 (2023).
- Siracusano, G., et al. Different decay of antibody response and VOC sensitivity in naïve and previously infected subjects at 15 weeks following vaccination with BNT162b2. Journal of Translational Medicine. 20 (1), 22 (2022).
- Ruggiero, A. SARS-CoV-2 vaccination elicits unconventional IgM specific responses in naïve and previously COVID-19-infected individuals. eBioMedicine. 77, (2022).
- Piubelli, C. Subjects who developed SARS-CoV-2 specific IgM after vaccination show a longer humoral immunity and a lower frequency of infection. eBioMedicine. 89, 104471 (2023).
- Zhang, G. F. Infectivity of pseudotyped SARS-CoV-2 variants of concern in different human cell types and inhibitory effects of recombinant spike protein and entry-related cellular factors. Journal of Medical Virology. 95 (1), e28437 (2023).
- da Costa, K. A. S. Influenza A (N1-N9) and Influenza B (B/Victoria and B/Yamagata) neuraminidase pseudotypes as tools for pandemic preparedness and improved influenza vaccine design. Vaccines. 10 (9), 1520 (2022).
- Condor Capcha, J. M. Generation of SARS-CoV-2 spike pseudotyped virus for viral entry and neutralization assays: a 1-week protocol. Frontiers in Cardiovascular Medicine. 7, 618651 (2021).
- Diomede, L., et al. Doxycycline inhibition of a pseudotyped virus transduction does not translate to inhibition of SARS-CoV-2 infectivity. Viruses. 13 (9), 1745 (2021).
Reimpresiones y Permisos
Solicitar permiso para reutilizar el texto o las figuras de este JoVE artículos
Solicitar permisoExplorar más artículos
This article has been published
Video Coming Soon
ACERCA DE JoVE
Copyright © 2025 MyJoVE Corporation. Todos los derechos reservados