Bu içeriği görüntülemek için JoVE aboneliği gereklidir. Oturum açın veya ücretsiz deneme sürümünü başlatın.
Method Article
π-π İstifleme etkileşimlerle Stabilize blok kopolimer miselleri hazırlanması için bir amfifilik kopolimerin anyonik polimerizasyonu
Bu Makalede
Özet
Metoksi-polietilen glikol (MPEG-b -PPheGE) üzerine fenil glisidil eter (PheGE) anyonik polimerizasyon yaşayan önemli adımlar anlatılmıştır. Elde edilen blok kopolimer miseller (BCMS) fizyolojik olarak uygun koşulları elde edildi altında 4 gün boyunca doksorubisin% 14 (% ağırlık) ve ilacın sürekli bırakılmasını sağlar ile yüklendi.
Özet
Bu çalışmada, fenil grubu ile bir çekirdek-oluşturucu blok içeren bir amfifilik kopolimerin metoksi-polietilen glikol (MPEG-B -PPheGE) hakkında fenil glisidil eter (PheGE) anyonik polimerizasyonunu canlı sentezlendi. Kopolimerin karakterizasyonu dar bir molekül dağılımı (PDI <1.03) ortaya çıktı ve mPEG 122 polimerizasyon derecesi teyit - B - (PheGE) 15. kopolimerin kritik misel konsantrasyonu, dinamik ışık saçılımı ve iletim elektronik mikroskopi ile değerlendirildi çekiş davranışı ile oluşturulmuş bir floresans yöntemi kullanılarak değerlendirildi. İlaç verme uygulamalarında kullanım için kopolimerin potansiyeli, in vitro biyolojik uyumluluk, yükleme ve hidrofobik bir anti-kanser ilaç doksorubisin (DOX) serbest bırakılması da dahil olmak üzere bir ön şekilde değerlendirilmiştir. DOX stabil bir misel formülasyonu% 14 (ağırlık olarak%), effici ilaç yüklemesi kadar ilaç yükleme seviyeleri elde edilmiştirasetatlara>% 60 fizyolojik olarak ilgili koşullar (asidik ve nötral pH albümin varlığı) altında 4 gün boyunca ilacın özelliğine ve sürekli bırakmaya (a / a). Yüksek ilaç yükü seviyesi ve sürekli salınan DOX ve misellerin çekirdek oluşturucu blok arasında π-π etkileşimleri stabilize ilişkilendirilir.
Giriş
sulu ortam içinde, amfifilik blok kopolimerleri bir hidrofilik kabuk veya korona ile çevrili bir hidrofobik çekirdeğin oluşur nano-boyutlu blok kopolimer miselleri (BCMS) oluşturmak için bir araya getirin. misel temel hidrofobik ilaçlar dahil edilmesi için bir rezervuar olarak hizmet edebilir; birlikte, hidrofilik korona iç ve dış ortam arasında bir arabirim sağlar. Poli (etilen glikol) (PEG) ve bunun türevleri, polimerler en önemli sınıflarından birini ve en çok ilaç formülasyonunda kullanılan bulunmaktadır. 1-3 BCMS birçok formülasyonları bu dayanarak bir değerli ilaç verme platformu olduğu kanıtlanmıştır Teknoloji artık geç aşama klinik geliştirme. 4. En sık olarak, kopolimerin hidrofobik blok polikaprolakton, poli (D, L-laktid), poli (propilen oksit) veya poli (β-benzil-L-aspartat) oluşur. 5 -9
Kataoka grubu in- b oluşan küresel misellerin incelenmiştir -PBLA Ve poli (etilen oksit) -. B - raporlarında doksorubisin doğum (DOX) 10,11 için (poliaspartik asit-konjuge doksorubisin), bu polimer konjuge ilaç veya PBLA arasındaki π-π etkileşimler olduğunu ortaya koydu ve ücretsiz DOX ilaç yüklemesi ve saklama artışlar sonucunda misel çekirdeği stabilize etmek için hareket ederler. Bir ilaç ve çekirdek oluşturan blok arasındaki uyumluluk veya etkileşimleri kurulmuş olan anahtar performans ile ilgili parametrelerin belirleyicileri. DOX ek olarak 12, kanser tedavi bir dizi kendi çekirdek yapısı (örneğin, metotreksat, olaparib, SN içinde aromatik halkalar içeren -38).
Sonuç olarak çekirdek oluşturucu blok benzil halkaları içerir kopolimerlerin sentezi önemli bir ilgi vardır. PEG ve türevlerinin Anyonik halka-açma polimerizasyon molekül ağırlığı üzerinde kontrol sağlayan ve iyi bir verimle düşük poli dispersiteye sahip malzeme ile sonuçlanır. 13,14 etilenfenil glisidil eter (PheGE) veya stiren oksit ile NE oksit (SO) hidrofobik ilaçlar çözünürleştirme için miseller oluşturan blok kopolimerler oluşturmak için polimerize (ko) olabilir. 15-18 mevcut rapor fenil anyonik polimerizasyonunu yaşam için gerekli adımları açıklamaktadır makrobaşlatıcı olarak mPEG-OH üzerinde eter monomer glisidil (Şekil 1). Elde edilen blok kopolimer ve agrega daha sonra ilaç iletiminde kullanım açısından özellikleri açısından karakterize edilir.
Access restricted. Please log in or start a trial to view this content.
Protokol
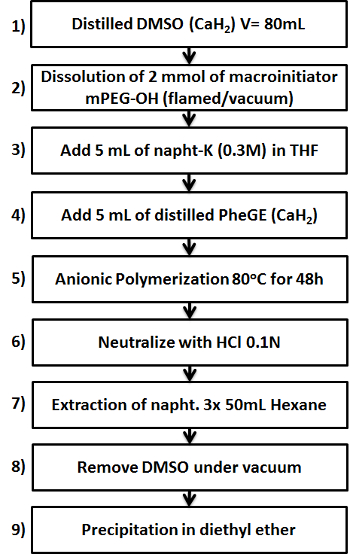
MPEG-b -PPheGE kopolimeri hazırlanmasında dokuz kilit adımları gösteren Şekil 1. Şematik. Bu rakamın büyük halini görmek için lütfen buraya tıklayınız.
Kuru Koşullarında Reaktiflerin hazırlanması 1.
- Reaktiflerin hazırlanması.
- Kullanımdan önce 48 saat boyunca vakum altında bir fırın içinde 50 ° C 'de, mPEG-5K (Mn = 5400 g / mol, KAE 1.03) ve yeri 15 g tartılır.
- Kuru, 200, 30 dakika boyunca vakum altında dimetilsülfoksit, kalsiyum hidrid üzerinde (DMSO) (CAH 2) (yaklaşık 1 gr), yeri mi, argon altında, boşaltma ve kullanımdan önce 48 saat boyunca karıştırılmıştır.
- Kuru ve temiz bir şişeye (100 mi) içinde PheGE monomer 50 ml koyun, argon altında, buz üzerinde 15 dakika boyunca vakum altında CaH 2 tasfiye contasını 1 grve kullanımdan önce argon altında 24 saat boyunca karışmaya bırakılmaktadır.
Potasyum Naphthalenin 2. Hazırlık
- Dikkatle, fazla mineral yağ çıkarmak ve tetrahidrofuran (THF) (v = 500 mi) ihtiva eden yuvarlak bir şişeye ilave heksan ile kurutulmuş sodyum (~ 1.5 g) küçük parçalara kesilir.
NOT: sodyum topakları nedeniyle yangın riski uzun süre havaya maruz bırakılmamalıdır. - argon ile benzofenon (~ 5 gr), tasfiye ekleme ve cam tıpa yuvarlak şişeye (2 boyunları) mühür.
- 24 saat argon altında karıştırılarak ardından, bir damıtma aparatı (Şekil 2) yuvarlak dipli bir şişeye bağlamak geri akışta argon altında koyu çözelti distile (örneğin, geri-akışa 2 saat süre ile çözelti rengi mavi olana sonra). (Damıtma cihazının ortasında bulunan) sol vanası kapatılarak ~ 150 ml THF istenen ses toplamaya başlar.
NOT: Bu çözüm mavi dönmezse, imbikten durdurmakyon, oda sıcaklığında (RT) soğumasını ve daha benzofenon veya sodyum eklemek ve damıtma yeniden başlatın. Bu THF de su içeren bir göstergesidir. - Kuru bir Erlenmeyer olarak, damıtılmış THF (v = 100 mi) ekleyin ve naftalinin 3.9 g çözülür.
NOT: damıtma Dur oda sıcaklığında soğumaya ve THF hacmini aktarmak için doğru vanasını açın. - alanına 2.1'de tarif edildiği gibi, potasyum (1,1 g), küçük parçalar kesildi ve naftalen (nihai konsantrasyon ~ 0.3 mol / L) ihtiva eden çözeltiye ilave edin. üstünde bir bölme ile (açık / kapalı) bir yıkama adaptörü (T) ile Erlenmeyer Seal ve argon ile temizleyin.
- 24 saat argon altında karıştırılarak ardından homojen koyu yeşil renk olarak potasyum naftalen baz elde edilen solüsyon izleyin.
- atıl koşullar altında, bir şırınga ile şişeden bazik bir solüsyon 5 ml'lik bir şişe çıkarın ve damıtılmış su, 10 ml ekle. Daha sonra bu çözüm fenolftalein göstergesinin 1-2 damla,hangi çözüm fuşya rengi döner.
- çözelti renksiz olana kadar, standart bir hidroklorik asit solüsyonu (0.1 N) ile, potasyum naftalen titre etmek için bir büret kullanarak.
3. Malzemeler ve Etkili Yaşam Anyonik Polimerizasyon için gerekli önlemler
- Sistem argon / vakum manifoldu.
NOT: Şekil 2'de açıklandığı gibi, içi boş cam stopcocks ile çift cam manifoldu cam argon teslimat ve vakum koşulları arasında geçiş yapmak için kullanılır.- kuru bir kurutucu kolonuna ve atıl kauçuk tüp kullanarak manifoldu hattına (manometre) ile argon tankı bağlayın. Argon hattının diğer ucunda, bir kabarcık (mineral yağ ihtiva eden) bağlanır.
- Cam stopcocks için esnek atıl tüpleri ve iğneler bağlayın. manifold diğer satır için, yüksek bir vakum pompasına (buz / su ya da sıvı nitrojen ile doldurulur) soğuk bir Dewar şişesi içinde daldırılmış camdan bir tuzak bağlayın.
- monomer ve DMSO damıtma için cihaz.
Not: (her birinde, yani) uygun bir yüksek vakum damıtma aygıtı (Şekil 2) kullanılmaktadır. Kuru cam yüksek vakum valfleri ile yapılan ve yerleşik kondansatörler bir iç soğutmalı kafa ile bir.- Soğutma birimi (letter) girişine (A) ve çıkış (B) su akışının bağlayın. Argon / vakum için çift manifolduna diğer giriş / çıkış (C) bağlayın. Ekle ve teslimat / çıkarma limanında bir septum (metal teller) mühür ve (üst / döngü at) hava duyarlı sıvıların transferi (D) bir paslanmaz çelik kanül bağlayın.
- Polimerizasyondan önce, 100 ° C de yarım küre ısıtma gömleği üzerine PheGE ve DMSO damıtılır ve 70 ° C, sırasıyla, karıştırma ile, vakum altında 2 saat karıştırıldı. DMSO kaynama noktası (1 atm) 189 ° C ise PheGE monomer kaynama noktası 254 ° C'dir.
- anyonik polimerleştirme için Züccaciyeiyon.
- damıtma sistemine ek olarak, (imalatçı tarafından onaylı) alt şişeler yuvarlak dahil olmak üzere yalnızca yüksek vakum dayanıklı cam kullanın, kanüller, septa ve septa mühür, metal teller (çözücü, baz ve monomer birimlerin transferi için) silindir mezun oldu.
Not: (vakum altında) dikkatli bir polimerizasyonu, ısı yaşayan ve kullanımdan önce, argon akımı altında, tüm cam soğutmak için. cam dan ~ bir mesafede 10 cm ısı tabancası tutun.
- damıtma sistemine ek olarak, (imalatçı tarafından onaylı) alt şişeler yuvarlak dahil olmak üzere yalnızca yüksek vakum dayanıklı cam kullanın, kanüller, septa ve septa mühür, metal teller (çözücü, baz ve monomer birimlerin transferi için) silindir mezun oldu.
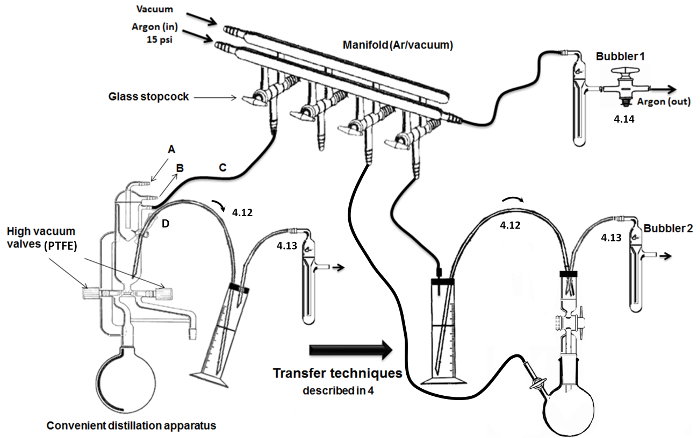
Şekil 2. Montaj ve anahtar damıtma / aktarma adımlar. Bu rakamın büyük halini görmek için lütfen buraya tıklayınız.
4. Yaşam Anyonik Polimerizasyon Önemli Adımlar açıklaması: Distilasyon ve Transferi
- kuru f mPEG-5K (2 mmol, 10 g) tartılırLASK / savurma üstünde bir bölme ile (açık / kapalı) (fırın), bir karıştırma çubuğu içeren ve yıkama adaptörü (T) mühür.
- manifolduna şişeyi bağlayın ve argon basması ile 2-3 dakika boyunca şişeyi temizlemek. şişeyi temizlemek için vakum pozisyonuna vanayı çevirin.
- elle şişeyi çevirin ve bir darbe kurutma makinesi (ısı tabancası) mPEG-5K eriyene kadar ile homojen reaksiyon kabı kurutun.
NOT: şişeden ~ bir mesafede 10 cm ısı tabancası tutun. - 1 dakika sonra, birkaç hızlı enstantane ile argon pozisyonuna doğru manifoldu vanayı çevirerek vakum kırmak.
NOT: sürekli bir argon akışı kabarcık olarak dikkate alınmalıdır. Akış sürekli olduğunda, valf argon konumuna kalır. Tekrarlayın ısıtma ve soğutma aşamaları iki kere nem tüm izlerini silmek için. - Reaksiyon başlamadan önce yaklaşık 2 saat boyunca argon altında, vakum altında polimer makroinisiyatör tutun.
- İki yüksek vakum damıtma cihazları başlık altında Dağı (Şekure 2); DMSO damıtılması için bir ve monomer (PheGE) damıtılması için.
- iki cihaz DMSO ve monomer içeren ayrı şişeler takın ve yarım küre ısıtma mantosu her gerekmektedir (ya da bir yağ banyosu içinde). (Giriş / çıkış) ve manifoldu (argon / vakum) ile aparatın üstüne soğuk su bağlayın.
- Her cihaz güvenli ve iyi mühürlü olduğundan emin olun. valf üzerinden vakum Engage.
NOT:. Adım 3.3 anlatıldığı gibi, nem tüm izlerini silmek için iki kez ısıtma ve soğutma adımları tekrarlayın. - Bir sıcaklık kontrol yoluyla ısıtma ayarlayın ve çözümleri karıştırma başlayın. DMSO dolaşımı / damıtma 2 saat sonra, çözelti, yaklaşık 20 ml toplamak (damıtma aygıtı ortasında bulunan) yüksek vakum vanasını kapatmak (cihazının içini yıkamak). Sonra, balona fraksiyonu bırakın ve istenen fraksiyonun saflığı c sağlamak için bir kez daha işlemi tekrarlayınDaha sonra ollected.
- polimer kadar ısı tabancası ile (vakum altında) mPEG-5K içeren şişeyi ısıtın (mPEG-5K) erir. argon ile tekrar temizleyin.
NOT: Prosedür DMSO transferinden sonra dağılmasına yardımcı olacaktır. - 2 saat sonra, yüksek vakum vanasını kapatmak ve çözücünün hacmi (V DMSO = ~ 100 mi) toplanır. ısıtma durdurun ve manifoldu gelen vakum kırmak. Yukarıda açıklandığı gibi hazneye (enstantane) tarafından argon serbest bırakın.
- pozitif argon basıncı altında, dereceli bir silindire (düzeneğin vana bulundurulan) kanülün bir yan bağlamak ya da doğrudan mPEG-5K (damıtma aygıtı varsa Bitirme) ihtiva eden bir şişeye, diğer ucu batırmak dikkatle taze damıtılmış fraksiyonu içine.
- argon basıncı kullanılarak, reaksiyon şişesi içine kanül yoluyla DMSO sürücü. inci bağlı cam musluğunu (ölçüm için gerekirse veya silindir) ekstra bir şişeye bubbler bağlayın ve kapatmakManifoldun karşı tarafında e kabarcık.
Not: bir kanülün bir yan transferi için kaldırıldığında, positif argon basıncı uygulandığında olduğundan emin olun. - , Argon basıncı ile meydana gelebilecek kazalara karşı 1-2 saniye cam stopcock açmak ve tam devir tamamlanıncaya kadar (0.5 dakika başına bir kez yinelenen) DMSO akışını devam tekrar kapama için. Bittiğinde musluğunu açın.
NOT: Aynı prosedür şimdi monomer damıtma ve toplanması için takip edilmelidir. Çözücü monomer aynı zamanda toplanan edilemez. - Aktarım yerleştirilmiş kanül bir septum (loop) ile kapatılmış bir dereceli silindir içinde kanül yoluyla 0.3 M naftalen potasyum 5 mi.
NOT: Aynı önlem NOT 4.13 açıklandığı gibi. Positif argon basıncı hava / su kirlenmesini önlemek için, reaksiyon şişesine silindir birinci silindire naftalen potasyum şişesi ve muhafaza edilmelidir. - manifo başka iğneyisilindirin (argon) içine ld. dikkatli bir şekilde, damıtma sistemine bağlı kanülün çıkarın ve reaksiyon şişesi içine hızlı bir şekilde yerleştirin.
NOT: taban ve monomer transferi için bu tekniği kullanın. - Çözelti koyu hale gelinceye kadar damla damla taban ekleyin. Koyu renk tekrar görünene kadar renk yavaş kaybolması ardından, başka bir bölümü eklemek ve tam transferi kadar tekrarlayın.
- PPheGE ~ polimerizasyonu n = 18-20 derecesine ulaşmak için monomer istenilen hacmi (V PheGE = 5 ml) aktarın.
- Tam polimerizasyonu sağlamak için sabit karıştırma ile, argon atmosferi altında, 80 ° C'de 48 saat boyunca reaksiyona bırakın.
- metanol içinde HCl 1 N damlalar (turnusol kağıdı (nötr pH) ile ölçülmüştür) ve bir renkli kaybolması ile gözlenen ilave reaksiyonu söndürün.
- heksan (3 x 50 mi) ile DMSO çözeltisinden naftalen ekstrakte edin. ~, Vakum altında damıtma yoluyla 70 ml (aynı cihaz) DMSO kaldır. mırıldanmakBulamaç çözeltisi aşağı L 50 ml THF ilave edin.
- 10 dakika için 5000 x g'de santrifüjleme ile bulamaç çözeltiden tuz çıkarın. süpernatant aktarın ve soğuk dietil eter, 500 ml damla damla ilave edin.
- 24-48 st için 30 ° C (% 85 verim) vakum altında süzme ya da santrifüjleme (iki kez) ve kuru ile çökeltiyi toplamak.
NOT: kopolimer şimdi karakterizasyonu için hazırdır.
Kopolimerlerin 5. Karakterizasyonu
- bir alüminyum numune kabına kopolimeri (kayıt gerçek kütle) 5-10 mg ağırlığında ve alüminyum kapak ile hava geçirmez bir şekilde kapatmak. diferansiyel taramalı kalorimetre yükleyin örnek tava ve referans tavası (boş).
- Program bir yöntem olup ( "sıcak / soğuk / sıcak") döngüsü: 100 ° C ile 40 ° C arasında 1) ısı 10 ° C / dakika, 2) 10 ° C / dakika ile -70 ° C'ye soğutun, 3), ısı 10 ° C / dakika ile 100 ° C arasındadır. Tekrarlayın 2) ve 3) iki kez. Erime noktası (Tm), kristalleştirme belirlemekÜçüncü devinim termal izlerinden allization (Tc) ve cam geçiş sıcaklığı (Tg) ve füzyon (AH f) ısı (varsa).
- THF polimerler (2 mg / ml) içinde çözülür ve 0.2 mikron PTFE filtresinden filtre. Bir jel nüfuziyet kromatografi sistemi (50 ul) halinde örnek enjekte edilir ve bir örnek için tutma süresini kullanımı ve bir kalibrasyon eğrisi polimerin moleküler ağırlığı belirlemek için polistiren standartlarına bir dizi üretilmiştir. 19
- 1H NMR spektroskopisi analizi için d6 DMSO (ko) polimerleri (15 mg / ml) içinde çözülür. 19
- Floresans 1,6-difenil-1,3,5-hexatriene (DPH) ile kopolimerin kritik misel konsantrasyonu (CMC) belirler. 9
- Karanlıkta THF içinde DPH stok çözelti hazırlayın (2.32 mg / L) hazırlanması ve şişeler bir dizi her biri, bu stok çözeltinin 100 ul ilave edin.
- PrepaTHF içinde kopolimer stok çözeltisi yeniden ve bir dizi şişe eşit hacimde (2 mi) hacimde ilave 0.01 ilâ 1,000 ug kopolimer / ml aralığında nihai kopolimer konsantrasyonları ile sonuçlanan (DPH stok çözeltisi bir kısım ihtiva eden) ekstrakte edildi.
- Daha sonra, girdap kopolimer-DPH çözeltiler ve bar karıştırılarak iki kez damıtılmış 10 ml su damla damla ilave edin. çözeltiler, daha sonra THF yavaş buharlaşmaya yeterli olacak bir azot akımı altında 48 saat süreyle kuvvetli bir şekilde karanlıkta karıştırılmalıdır. Her bir çözelti içinde DPH nihai konsantrasyonu 0.232 mg / L'dir.
- Çift tarama mikroplak spektroflorometre ve arsa floresan kullanarak 430 nm (λ ex = 350 nm) numunelerin floresan emisyonunu ölçün karşı [polimer] açın. İki doğrusal yamaçları arasındaki kesişme kopolimeri için CMC değer sağlar.
BCMS içine Doksorubisin Yükleme 6. Prosedürü
- ACE 1 ml DOX 12 mg çözülürtonitrile, 2 saat boyunca karanlıkta çözeltinin karışmasını trietilamin 10 ul ekleyin ve bildirin.
- 1 ml THF içinde kopolimeri (45 mg) içinde çözülür ve aynı zaman dönemi boyunca karıştırın. DOX çözeltisine kopolimer solüsyonu eklenir ve THF ilave hacim (0.5 mi) ile arta kalan kopolimer içeren vial yıkayın.
- karıştırılarak tuz 15 ml% 0.9 (NaCl) içeren bir şişeye (20 mi) kopolimer-ilaç karışımı (2.5 mi) damla damla ilave edin.
- Bir diyaliz torbasına (3.5 kDa kesilmiş) çözüm aktarın ve tuzlu su karşısında% 0.9 oranında (500 ml) dialyze.
Not: 6 saat sonra, dış tuzlu değiştirme ve diyaliz, oda sıcaklığında karanlıkta karıştırılarak 24 saat devam etmesine izin. - 15 dakika boyunca 5.000 xg'de 50 ml tüp ve santrifüj diyalizatı aktarın.
- bir diyaliz membranı (10 kDa kesilmiş) ihtiva eder (10 mi kapasiteli) bir ultrafiltrasyon sistemi süpernatant aktarın. Ultrafiltrasyon sistemi içine karıştırarak adaptörü koymak kapağını kapatın ve şekilde açıkazot Team,.
- 4 ml'lik bir hacme BCM çözelti konsantre edin ve taze tuzlu çözelti 6 ml ilave edilir ve iki kez prosedürü tekrarlayın.
- 4 ml BCM çözeltisi konsantre, tuz, 0.5 ml odası yıkayın ve çözeltiye ilave edin. Koyu önce daha kullanımda oda sıcaklığında kahverengi şişelerde saklayın.
DOX-BCMS doksorubisin Yükleme 7. Değerlendirme
- miseller bozabilir ve (900 ul 0.1 N HCl, 100 ul) ve değerlendirmeden önce bir sulu HCI solüsyonu (0.1 N) seyreltilmesi dimetilformamid DOX-BCM (400 ul 100 ul) içinde çözülür.
- bir tezgah üstü mikroplaka spektrofotometrik sistemi kullanılarak 490 nm'de ilaç yükleme ölçün. ilaç yüklemesi kapasitesi (DLC) ve ilaç yükleme verimliliğini (DLE) belirlemek için aşağıdaki denklemleri kullanın:
DLC (ağırlık%) = 100 x (% ilacın ağırlığı BCMS / toplam ağırlığı yüklü)
DLE (%) = (ilacın ağrılık besleme ilaç / ağırlık yüklü) x% 100
8. DeğerlendirmeDOX-BCMS gelen DOX İn Vitro duyurusunda
- PBS pH karşı 0.1 M fosfat tamponlu tuz (PBS, pH 7.4) içinde 7.4% 0.1, 37 ° C'de BCMS gelen Dox Bırakılmanın incelenmesi (ağ / hac) Tween 80, PBS karşı BCMS + BSA'da (50 mg / ml) pH 7.4 ve pH 0.1 M asetat tampon = 5.5. 20,21
- diyaliz torbasında Dox ≈ 0.6-0.7 mg toplam miktarına neden olmak için seçilen tampon (2.3 mL) 'de BCM-DOX formülasyonu (700 ul) ile seyreltilir.
- , Diyaliz torbaya çözüm yerleştirin klipler ile mühür ve ilgili dış ortama 200 ml içine torbayı batırmayın.
- önceden tespit edilmiş bir zaman noktalarında Diyaliz çantasının dışında çözeltisi 2 mi çıkarın ve taze, aynı hacimde tampon ile değiştirin.
- Önceki UV-Vis spektrofotometre ile analiz -20 ° C'de çıkarıldı alikotları (Abs 490 nm) saklayın. (E R) salınan ilacın kümülatif yüzde aşağıdaki denklem kullanılarak hesaplanabilir:

Not: m DOX BCMS doks miktarını temsil eder, V 0 salım ortamı (200 mi) toplam hacmi, V T ikame ortam hacmi (VT = 2 mi) ise, Cı konsantrasyonudur düzeltme öncesi ve Cı n numunesinde DOX konsantrasyonunu temsil eder.
Access restricted. Please log in or start a trial to view this content.
Sonuçlar
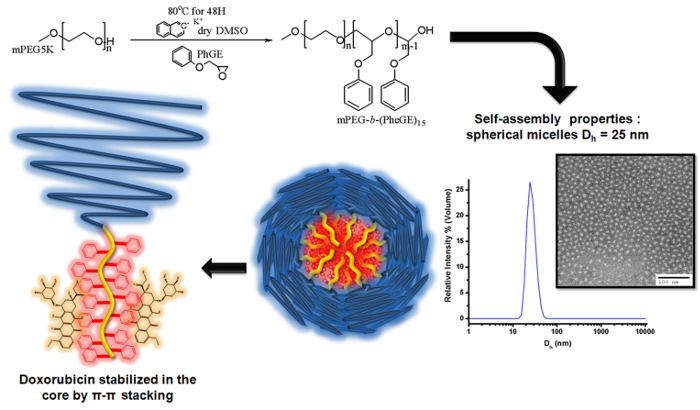
Doksorubisinin yüklenmesi için blok kopolimer misellerinin hazırlanması için (PheGE) 15 şematik bir naftalen potasyum ile MPEG hidroksil grubunun deprotonasyon görüntülemektedir - MPEG makrobaşlatıcı ilgili fenil glisidil eter anyonik polimerizasyonu Şekil 3. Çizim MPEG B
Access restricted. Please log in or start a trial to view this content.
Tartışmalar
Bağlı anyonik polimerizasyon molekül ağırlığı üzerinde sağladığı iyi kontrol etmek için, oksiran monomerler (PEG ve PEG) göre polimerlerin hazırlanması için sanayide en çok kullanılan süreçlerden biridir. Başarılı bir polimerizasyon elde edilmesi için en uygun ve sıkı koşullar kullanılmalıdır. Tüm reaktifler ve uygun düzeneğin titiz saflaştırma sentezi oturma karakteri için önemlidir. Geçerli kurulum Sınırlamalar çoğunlukla kanülasyon dayanır transfer tekniği ile ilişkilid...
Access restricted. Please log in or start a trial to view this content.
Açıklamalar
The authors have nothing to disclose.
Teşekkürler
CA acknowledges a Discovery grant from the Natural Sciences and Engineering Research Council of Canada. CA acknowledges a Chair in Pharmaceutics and Drug Delivery from GSK. The authors declare no competing financial interest.
Access restricted. Please log in or start a trial to view this content.
Malzemeler
| Name | Company | Catalog Number | Comments |
| DMEM/HAMF12 | Gibco, Life Technologies | 12500 | Supplemented with 10% FBS. Warm in 37 °C water bath. |
| Trypsin-EDTA (0.25%) | Sigma-Aldrich | T4049 | Warm in 37 °C water bath |
| Fetal bovine serum (FBS) | Sigma-Aldrich | F1051 | Canada origin |
| MDA-MB-468 cell line | ATCC | HTB-132 | |
| MTS tetrazolium reagent | PROMEGA | G111B | |
| Phenazine ethosulfate (PES) | Sigma-Aldrich | P4544 | >95% |
| mPEG5K (Mn 5,400 g/mol) | Sigma-Aldrich | 81323 | PDI=1.02 |
| Dimethylsolfoxide (DMSO) | Sigma-Aldrich | D4540 | >99.5% |
| Naphthalene | Sigma-Aldrich | 147141 | >99% |
| Phenyl glycidyl ether | Sigma-Aldrich | A32608 | >85% |
| Benzophenone | Sigma-Aldrich | 427551 | >99% |
| Potassium | Sigma-Aldrich | 451096 | >98% |
| Tetrahydrofuran | Caledon Laboratory Chemicals | 8900 1 | ACS |
| Hexane | Caledon Laboratory Chemicals | 5500 1 | ACS |
| Calcium hydride (CaH2) | ACP | C-0460 | >99.5% |
| Diethyl Ether | Caledon Laboratory Chemicals | 1/10/4800 | ACS |
| Microplate reader | BioTek Instruments | ||
| Differential scanning calorimetry (DSC) | TA Instruments Inc | DSC Q100 | |
| Gel permeation chromatography (GPC) | Waters | 2695 separation moldule / 2414 detector | 2 Columns: Agilent Plgel 5 µm Mixed-D |
| NMR spectroscopy | Varian Mercury 400MHz | ||
| Chloroform-d | Sigma-Aldrich | 151858 | 99.96% |
| DMSO-d | Sigma-Aldrich | 156914 | 99.96% |
| Vaccum pump | Gardner Denver Welch Vacuum Tech, Inc. | Ultimate pressure 1x10-4 torr | |
| Drierit with indicator, 8 mesh | Sigma-Aldrich | 238988 | Regenerated at 230 °C for 2 hr |
Referanslar
- Dickerson, T. J., Reed, N. N., Janda, K. D. Soluble Polymers as Scaffolds for Recoverable Catalysts and Reagents. Chemical Reviews. 102, 3325-3344 (2002).
- van Heerbeek, R., Kamer, P. C. J., van Leeuwen, P. W. N. M., Reek, J. N. H. Dendrimers as Support for Recoverable Catalysts and Reagents. Chemical Reviews. 102 (10), 3717-3756 (2002).
- Knop, K., Hoogenboom, R., Fischer, D., Schubert, U. S. Poly(ethylene glycol) in Drug Delivery: Pros and Cons as Well as Potential Alternatives. Angewandte Chemie International Edition. 49 (36), 6288-6308 (2010).
- Eetezadi, S., Ekdawi, S. N., Allen, C. The challenges facing block copolymer micelles for cancer therapy: In vivo barriers and clinical translation. Advanced Drug Delivery Reviews. 91, 7-22 (2015).
- Attwood, D., Booth, C., Yeates, S. G., Chaibundit, C., Ricardo, N. Block copolymers for drug solubilisation: Relative hydrophobicities of polyether and polyester micelle-core-forming blocks. International Journal of Pharmaceutics. 345 (1-2), 35-41 (2007).
- Matsumura, Y., Kataoka, K. Preclinical and clinical studies of anticancer agent-incorporating polymer micelles. Cancer Science. 100 (4), 572-579 (2009).
- Chan, A. S., Chen, C. H., Huang, C. M., Hsieh, M. F. Regulation of particle morphology of pH-dependent poly(epsilon-caprolactone)-poly(gamma-glutamic acid) micellar nanoparticles to combat breast cancer cells. Journal of Nanoscience and Nanotechnology. 10 (10), 6283-6297 (2010).
- Diao, Y. Y., et al. Doxorubicin-loaded PEG-PCL copolymer micelles enhance cytotoxicity and intracellular accumulation of doxorubicin in adriamycin-resistant tumor cells. International Journal of Nanomedicine. 6, 1955-1962 (2011).
- Mikhail, A. S., Allen, C. Poly(ethylene glycol)-b-poly(ε-caprolactone) Micelles Containing Chemically Conjugated and Physically Entrapped Docetaxel: Synthesis, Characterization, and the Influence of the Drug on Micelle Morphology. Biomacromolecules. 11 (5), 1273-1280 (2010).
- Kataoka, K., Harada, A., Nagasaki, Y. Block copolymer micelles for drug delivery: design, characterization and biological significance. Advanced Drug Delivery Reviews. 47 (1), 113-131 (2001).
- Nakanishi, T., et al. Development of the polymer micelle carrier system for doxorubicin. Journal of Controlled Release. 74 (1-3), 295-302 (2001).
- Liu, J., Xiao, Y., Allen, C. Polymer-drug compatibility: A guide to the development of delivery systems for the anticancer agent, ellipticine. Journal of Pharmaceutical Sciences. 93 (1), 132-143 (2004).
- Flory, P. J. Molecular Size Distribution in Ethylene Oxide Polymers. Journal of the American Chemical Society. 62 (6), 1561-1565 (1940).
- Kazanskii, K. S., Solovyanov, A. A., Entelis, S. G. Polymerization of ethylene oxide by alkali metal-naphthalene complexes in tetrahydrofuran. European Polymer Journal. 7 (10), 1421-1433 (1971).
- Crothers, M., et al. Micellization and Gelation of Diblock Copolymers of Ethylene Oxide and Styrene Oxide in Aqueous Solution. Langmuir. 18 (22), 8685-8691 (2002).
- Taboada, P., et al. Block Copolymers of Ethylene Oxide and Phenyl Glycidyl Ether: Micellization, Gelation, and Drug Solubilization. Langmuir. 21 (12), 5263-5271 (2005).
- Taboada, P., et al. Micellization and Drug Solubilization in Aqueous Solutions of a Diblock Copolymer of Ethylene Oxide and Phenyl Glycidyl Ether. Langmuir. 22 (18), 7465-7470 (2006).
- Attwood, D., Booth, C. Colloid Stability. , Wiley-VCH Verlag GmbH & Co. KGaA. 61-78 (2010).
- Le Devedec, F., et al. Postalkylation of a Common mPEG-b-PAGE Precursor to Produce Tunable Morphologies of Spheres, Filomicelles, Disks, and Polymersomes. ACS Macro Letters. 5 (1), 128-133 (2016).
- Chtryt, V., Ulbrich, K. Conjugate of Doxorubicin with a Thermosensitive Polymer Drug Carrier. Journal of Bioactive and Compatible Polymers. 16 (6), 427-440 (2001).
- Kataoka, K., et al. Doxorubicin-loaded poly(ethylene glycol)-poly(β-benzyl-l-aspartate) copolymer micelles: their pharmaceutical characteristics and biological significance. Journal of Controlled Release. 64 (1-3), 143-153 (2000).
- Cammas, S., Matsumoto, T., Okano, T., Sakurai, Y., Kataoka, K. Design of functional polymeric micelles as site-specific drug vehicles based on poly (α-hydroxy ethylene oxide-co-β-benzyl l-aspartate) block copolymers. Materials Science and Engineering: C. 4 (4), 241-247 (1997).
- Lv, S., et al. Doxorubicin-loaded amphiphilic polypeptide-based nanoparticles as an efficient drug delivery system for cancer therapy. Acta Biomaterialia. 9 (12), 9330-9342 (2013).
- Kim, J. O., Oberoi, H. S., Desale, S., Kabanov, A. V., Bronich, T. K. Polypeptide nanogels with hydrophobic moieties in the cross-linked ionic cores: synthesis, characterization and implications for anticancer drug delivery. Journal of Drug Targeting. 21 (10), 981-993 (2013).
- Zhao, C. L., Winnik, M. A., Riess, G., Croucher, M. D. Fluorescence probe techniques used to study micelle formation in water-soluble block copolymers. Langmuir. 6 (2), 514-516 (1990).
- Wilhelm, M., et al. Poly(styrene-ethylene oxide) block copolymer micelle formation in water: a fluorescence probe study. Macromolecules. 24 (5), 1033-1040 (1991).
- Cammas, S., Kataoka, K. Functional poly[(ethylene oxide)-co-(β-benzyl-L-aspartate)] polymeric micelles: block copolymer synthesis and micelles formation. Macromolecular Chemistry and Physics. 196 (6), 1899-1905 (1995).
- Kwon, G., et al. Micelles based on AB block copolymers of poly(ethylene oxide) and poly(.beta.-benzyl L-aspartate). Langmuir. 9 (4), 945-949 (1993).
- Ahmed, F., Discher, D. E. Self-porating polymersomes of PEG-PLA and PEG-PCL: hydrolysis-triggered controlled release vesicles. Journal of Controlled Release. 96 (1), 37-53 (2004).
- Uhrig, D., Mays, J. W. Experimental techniques in high-vacuum anionic polymerization. Journal of Polymer Science Part A: Polymer Chemistry. 43 (24), 6179-6222 (2005).
- Parker, A. J. The effects of solvation on the properties of anions in dipolar aprotic solvents. Quarterly Reviews, Chemical Society. 16 (2), 163-187 (1962).
- Cram, D. J. Fundamentals o] Carbanion Chemistry. , (1965).
- Szwarc, M. ACS Symposium Series. 166, American chemistry society. 1-15 (1981).
- Cho, Y. W., Lee, J., Lee, S. C., Huh, K. M., Park, K. Hydrotropic agents for study of in vitro paclitaxel release from polymeric micelles. Journal of Controlled Release. 97, 249-257 (2004).
- Dewhurst, P. F., Lovell, M. R., Jones, J. L., Richards, R. W., Webster, J. R. P. Organization of Dispersions of a Linear Diblock Copolymer of Polystyrene and Poly(ethylene oxide) at the Air−Water Interface. Macromolecules. 31 (22), 7851-7864 (1998).
- Opanasopit, P., et al. Block Copolymer Design for Camptothecin Incorporation into Polymeric Micelles for Passive Tumor Targeting. Pharmaceutical Research. 21 (11), 2001-2008 (2004).
- Allen, G., Booth, C., Price, C. VI-The physical properties of poly(epoxides). Polymer. 8, 414-418 (1967).
- Jada, A., Hurtrez, G., Siffert, B., Riess, G. Structure of polystyrene-block-poly(ethylene oxide) diblock copolymer micelles in water. Macromolecular Chemistry and Physics. 197 (11), 3697-3710 (1996).
- Attwood, D., Florence, A. T. Surfactant systems : their chemistry, pharmacy, and biology. , Chapman and Hall. (1983).
- Rekatas, C. J., et al. The effect of hydrophobe chemical structure and chain length on the solubilization of griseofulvin in aqueous micellar solutions of block copoly(oxyalkylene)s. Physical Chemistry Chemical Physics. 3 (21), 4769-4773 (2001).
- Encyclopædia Britannica Online. , http://www.britannica.com/EBchecked/topic/479680/protein/72559/Proteins-of-the-blood-serum (2015).
Access restricted. Please log in or start a trial to view this content.
Yeniden Basımlar ve İzinler
Bu JoVE makalesinin metnini veya resimlerini yeniden kullanma izni talebi
Izin talebiThis article has been published
Video Coming Soon
JoVE Hakkında
Telif Hakkı © 2020 MyJove Corporation. Tüm hakları saklıdır