Bu içeriği görüntülemek için JoVE aboneliği gereklidir. Oturum açın veya ücretsiz deneme sürümünü başlatın.
Method Article
T Hücrelerinin Viral Transdüksiyonu için Kuru Makrogözenekli Aljinat İskelelerinin İmalatı ve Kullanımı
Bu Makalede
Özet
Burada, CAR-T hücre tedavisi için T hücreleri de dahil olmak üzere T hücrelerinin genetik mühendisliğinde kullanılmak üzere verimli viral gen transferine aracılık eden kuru makrogözenekli aljinat iskeleleri oluşturmak için bir protokol bulunmaktadır. İskelelerin aktive olmuş primer T hücrelerini %>85 transdüksiyonla transdüksiyon yaptığı gösterilmiştir.
Özet
CAR-T hücre tedavisi için T hücrelerinin genetik mühendisliği, son birkaç yılda kanser tedavisinde ön plana çıkmıştır. CAR-T hücreleri, T hücrelerine viral gen transferi ile üretilir. Viral gen transferinin mevcut altın standardı, pahalı ve zaman alıcı olan retronektin kaplı plakaların spinokülasyonunu içerir. CAR-T hücreleri üretmek için verimli ve uygun maliyetli yöntemlere önemli bir ihtiyaç vardır. Burada açıklanan, aktif T hücrelerinin viral transdüksiyonunu etkili bir şekilde teşvik eden Drydux iskeleleri olarak bilinen ucuz, kuru makrogözenekli aljinat iskelelerinin üretilmesi için bir yöntemdir. İskeleler, virüsle tohumlanmış retronektin kaplı plakaların altın standart spinokülasyonu yerine kullanılmak üzere tasarlanmıştır ve hücrelerin dönüştürülmesi işlemini basitleştirir. Aljinat, kalsiyum-D-glukonat ile çapraz bağlanır ve iskeleleri oluşturmak için gece boyunca dondurulur. Dondurulmuş iskeleler, kuru makrogözenekli iskelelerin oluşumunu tamamlamak için 72 saat boyunca bir liyofilizatörde dondurularak kurutulur. İskeleler, virüs ve aktive olmuş T hücreleri, genetiği değiştirilmiş hücreler üretmek için iskelenin üzerine birlikte tohumlandığında viral gen transferine aracılık eder. İskeleler, retronektin kaplı plakalarda spinokülasyonun transdüksiyon verimliliği ile karşılaştırılabilir olan% >85 primer T hücre transdüksiyonu üretir. Bu sonuçlar, kuru makrogözenekli aljinat iskelelerinin geleneksel transdüksiyon yöntemine daha ucuz ve daha uygun bir alternatif olarak hizmet ettiğini göstermektedir.
Giriş
İmmünoterapi, tümörleri spesifik olarak hedefleme, hedef dışı sitotoksisiteyi sınırlama ve nüksetmeyi önleme kabiliyeti nedeniyle devrim niteliğinde bir kanser tedavisi paradigması olarak ortaya çıkmıştır. Özellikle kimerik antijen reseptörü T (CAR-T) hücre tedavisi, lenfoma ve lösemi tedavisindeki başarısı nedeniyle popülerlik kazanmıştır. FDA, 2017 yılında ilk CAR-T hücre tedavisini onayladı ve o zamandan beri dört CAR-T hücre terapisini daha onayladı 1,2,3,4,5. CAR'lar genellikle tümörle ilişkili bir antijen 3,4 için spesifik olan bir monoklonal antikorun tek zincirli değişken fragmanından oluşan bir antijen tanıma alanına sahiptir. Bir CAR, tümörle ilişkili antijeniyle etkileşime girdiğinde, CAR-T hücreleri aktive olur ve sitokin salınımı, sitolitik degranülasyon, transkripsiyon faktörü ekspresyonu ve T hücresi proliferasyonunu içeren bir antitümör yanıta yol açar. CAR-T hücrelerini üretmek için, T hücrelerini elde etmek için hastadan kan toplanır. CAR'lar genetik olarak bir virüs kullanılarak hastanın T hücrelerine eklenir. CAR-T hücreleri in vitro olarak büyütülürve hastaya 2,3,4,6 geri verilir. CAR-T hücrelerinin başarılı bir şekilde üretilmesi, genetik olarak CAR-T hücrelerine dönüştürülen T hücrelerinin sayısını tanımlayan iletim verimliliği ile belirlenir.
Şu anda, CAR-T hücre üretimi için altın standart, retronektin kaplı plakalar 7,8 üzerinde aktive edilmiş T hücrelerinin ve virüsün spinokülasyonudur. Transdüksiyon, viral parçacıklar T hücrelerinin yüzeyine girdiğinde başlar. Retronektin, viral parçacıklar ve hücreler arasındaki bağlanma verimliliğini artırarak virüs ve hücrelerin kolokalizasyonunu teşvik eder ve transdüksiyonu arttırır 7,8. Retronektin kendi başına iyi çalışmaz ve viral parçacıkları yoğunlaştırarak ve T hücresinin yüzey geçirgenliğini artırarak gen transferini artıran ve daha kolay viral enfeksiyona izin veren spinokülasyonun eşlik etmesi gerekir8. Retronektin kaplı plakalarda spinokülasyonun başarısına rağmen, çoklu spin döngüleri ve pahalı reaktifler gerektiren karmaşık bir işlemdir. Bu nedenle, viral gen transferi için daha hızlı ve daha ucuz olan alternatif yöntemler oldukça arzu edilir.
Aljinat, düşük maliyeti, iyi güvenlik profili ve iki değerli katyonlar 9,10,11,12 ile karıştırıldığında hidrojel oluşturma kabiliyeti nedeniyle biyomedikal endüstrisinde yaygın olarak kullanılan doğal bir anyonik polisakkarittir. Aljinat, GMP uyumlu bir polimerdir ve genellikle FDA13 tarafından güvenli (GRAS) olarak kabul edilir. Aljinatın katyonlarla çapraz bağlanması, yara iyileşmesinde, küçük kimyasal ilaçların ve proteinlerin verilmesinde ve hücre taşınmasında sıklıkla kullanılan stabil hidrojeller oluşturur 9,10,11,12,14,15,16. Mükemmel jelleşme özellikleri nedeniyle, aljinat10,17 dondurarak kurutularak gözenekli iskeleler oluşturmak için tercih edilen malzemedir. Aljinatın bu özellikleri, aktif hücrelerin viral gen transferine aracılık edebilecek bir iskele üretmek için çekici bir aday olmasını sağlar.
Burada tarif edilen, Drydux iskeleleri olarak bilinen kuru makrogözenekli aljinat iskeleleri yapmak için kullanılan ve T hücrelerini viral gen transferi ile statik olarak dönüştüren bir protokoldür17,18. Bu iskelelerin yapım süreci Şekil 1'de gösterilmiştir. Bu iskeleler, retronektin kaplı plakaların spinokülasyonu ihtiyacını ortadan kaldırır. Makrogözenekli aljinat iskeleleri, mühendislik ürünü T hücrelerinin işlevselliğini ve yaşayabilirliğini etkilemeden tek bir adımda verimli gen transferini sağlamak için viral parçacıkların ve T hücrelerinin etkileşimini teşvik eder17. Doğru takip edildiğinde, bu makrogözenekli aljinat iskeleleri en az% 80'lik bir transdüksiyon verimliliğine sahiptir ve viral iletim sürecini basitleştirir ve kısaltır.
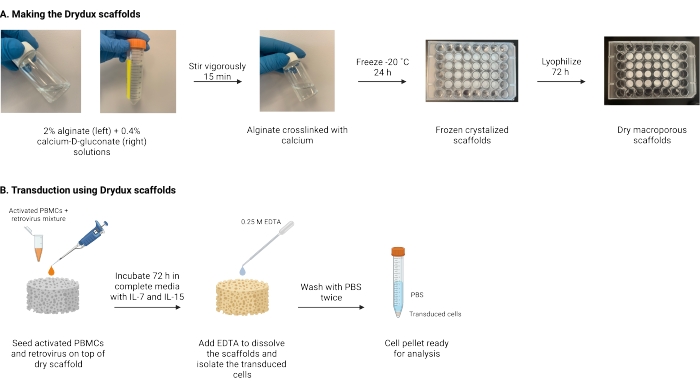
Şekil 1: Protokolün şeması ve zaman çizelgesi. (A) Kuru makrogözenekli aljinat iskelelerinin yapılması için zaman çizelgesi. Aljinat, kalsiyum-D-glukonat ile çapraz bağlanır ve gece boyunca dondurulur. Dondurulmuş iskeleler, Drydux iskelelerini oluşturmak için 72 saat boyunca liyofilize edilir. (B) Aktif hücrelerin viral transdüksiyonu için zaman çizelgesi. Aktif hücreler ve virüs (MOI 2) iskelenin üzerine ekilir ve IL-7 ve IL-15 ile desteklenmiş tam ortamda inkübe edilir. İskeleler karışımı emer ve viral gen transferini teşvik eder. EDTA, iskeleleri çözmek ve dönüştürülmüş hücreleri izole etmek için kullanılır. PBS ile iki kez yıkandıktan sonra, hücre peleti analiz için kullanılabilir. Kısaltmalar: PBS = fosfat tamponlu salin; PBMC'ler = periferik kan mononükleer hücreleri. Bu şeklin daha büyük bir versiyonunu görüntülemek için lütfen buraya tıklayın.
Protokol
İnsan önceliği hücrelerini ve retroviral vektörleri içeren tüm prosedürler, Kuzey Carolina Eyalet Üniversitesi'nin Biyolojik Güvenlik yönergelerine uygun olarak gerçekleştirildi ve Çevre Sağlığı ve Güvenliği Ofisi tarafından onaylandı. İnsan periferik kan mononükleer hücreleri, ticari kaynaklardan buffy paltolar olarak satın alındı. Birincil insan hücreleri, insan buffy ceket fraksiyonlarından izole edilmeli ve Biyogüvenlik Seviye 2 temizliği ve ayrıntılı standart çalışma prosedürleri ve işin yapılacağı kurumdan onay gerektirmelidir. Dahaönce tarif edildiği gibi hazırlanan transdüksiyon için kullanılan retroviral vektör süpernatantları da dahil olmak üzere viral vektörler, kodlanmış proteine bağlı olarak Biyogüvenlik Seviye 1 veya Biyogüvenlik Seviye 2 olarak sınıflandırılabilir ve ilgili kurumsal biyogüvenlik komitesinden onay gerektirir.
1. Makrogözenekli aljinat iskelelerinin yapılması
- Bir beherdeki kalsiyum D glukonata steril filtrelenmiş deiyonize su ekleyerek% 0.4'lük (hacim başına ağırlık) kalsiyum D glukonatlık bir stok çözeltisi hazırlayın. Kalsiyum glukonat çözünene kadar (~ 1.5 saat), steril filtre olana kadar orta hızda karıştırın ve oda sıcaklığında saklayın.
NOT: Çözeltinin pH'ını kontrol etmek gerekli değildir. - Bir vidalı kapak şişesinde veya beherinde% 2'lik (hacim başına ağırlık) bir alginat çözeltisi hazırlayın. Ultra saf aljinatı dikkatlice kaba ekleyin ve aljinata steril filtrelenmiş deiyonize su ekleyin. Karıştırmayı engellemeyecek mümkün olan en büyük karıştırma çubuğunu seçin ve kaba ekleyin.
NOT: Bu protokol için kullanılan ultra saf aljinat türü hakkında bilgi Malzeme Tablosunda ve Novamatrix web sitesi20'de bulunabilir. Bu iskeleler için farklı aljinatlar araştırılmamıştır, çünkü iskelelerin gözenekliliğinde ve biyouyumluluğunda istenmeyen değişikliklere yol açabilirler 9,10,11. - Aljinat eriyene kadar çözeltiyi yüksek hızda karıştırın (~ 1 saat). Geminin yanlarında büyük kümeler varsa, gemiyi yerinden çıkarmak için eğin. Yanlardaki az miktarda aljinat karıştırılırken çözülür ve endişe kaynağı olmaz.
NOT: Çözeltinin pH'ını kontrol etmek gerekli değildir. - Aljinat çözündüğünde, karıştırma hızını azaltın, çapraz bağlanma kümelerinin oluşmasını önlemek için aljinat çözeltisine yavaşça% 0.4 kalsiyum D glukonat eşit hacimde ekleyin ve 15 dakika boyunca kuvvetlice karıştırın.
- Oluşmuş olabilecek kümeleri çıkarmak için beheri veya şişeyi yana doğru eğin.
NOT: Bir homojenizatör kullanılması tavsiye edilir. Nihai çözüm optik olarak açık olmalıdır. - Çözeltinin istenen hacmini 48 delikli bir plakanın veya 24 delikli plakanın her bir kuyucuğuna pipetleyin. 48 delikli bir plaka için 300 μL / kuyu ve 24 delikli bir plaka için 1 mL / kuyu kullanın. Yavaşça dökün ve uçları sık sık değiştirin, çünkü çözelti viskoz olacak ve uca yapışacaktır.
- Plakaları kapaklarla örtün ve -20 ° C'de gece boyunca dondurun.
- Kapağı çıkararak ve üstünü mendil ve lastik bantlarla sabitleyerek liyofilizatör için plakayı hazırlayın. Plakaları 750 mL ila 2.000 mL liyofilizatör şişelerine yerleştirin ve 72 saat boyunca liyofilizatöre yerleştirin.
- 72 saat sonra, plakayı liyofilizatörden çıkarın ve kapağı değiştirin. Plakayı kapatın ve 4 ° C'de saklayın. Uzun süreli depolama için, 4 ° C'de saklamadan önce plakayı vakumla kapatın. Gerekene kadar kuru tutun.
NOT: Hacim hatası nedeniyle ekstra kalsiyum-aljinat çözeltisi yapın (şişenin duvarlarına bazı yapışırlar, pipet uçları). Örneğin, 24 delikli bir plakada dört iskele yapmak için, 4 mL kombine çözelti (2 mL aljinat + 2 mL kalsiyum D glukonat) gereklidir, ancak 2.5 mL% 2 aljinat çözeltisi ve 2.5 mL% 0.4 kalsiyum D glukonat çözeltisi hazırlanması önerilir.
2. Transdüksiyon
- 100 kDa filtreler kullanılarak viral süpernatant konsantrasyonu
- Santrifüj filtreyi 1 mL 1x fosfat tamponlu salin (PBS) ile 2 dakika boyunca nemlendirin. PBS'yi atın.
- 2 mL viral süspansiyon (1 × 106 TU/mL) ekleyerek ve sallanan bir kova rotorunda 10 dakika boyunca 1.500 × g'da santrifüj filtreden geçirerek viral süspansiyonu konsantre edin.
NOT: İskele başına bir ila iki yüz mikrolitre konsantre virüs gereklidir. - Konsantre virüs süspansiyon hacmi 200 μL'den büyükse birkaç dakika daha döndürün.
- Her iskele için 2.1.1-2.1.3 arasındaki adımları yineleyin.
NOT: Büyük bir virüs stoğunu konsantre etmek ve konsantre stoktan 100-200 μL alikot almak da kabul edilebilir.
- Tohumla aktive olmuş hücreler ve virüs bir arada.
- Her iskele için, 50 μL tam hücre kültürü ortamında (250 mL Click'in ortamı + 250 mL RPMI1640 media + 50 mL fetal sığır serumu + 5 mL glutamin ikamesi + 5 mL glutamin ikamesi + 5 mL penisilin / streptomisin) 1 × 10 6 aktive periferik kan mononükleer hücresini (PBMC) askıya alarak bir aliquot hazırlayın.
NOT: PBMC'lerin nasıl etkinleştirileceğine ilişkin bir protokol için Ek Dosya 1'e bakın. - Konsantre viral süpernatantı (~ 2 × 106 TU, MOI 2) hücre süspansiyonuna ekleyin. Hücre-virüs süspansiyonunun toplam hacmi, 48 kuyulu bir iskele için 200 μL'yi veya 24 delikli bir iskele için 350 μL'yi geçmemelidir.
- Hücre-virüs karışımını damla damla kuru iskelenin üstüne ekleyin. Negatif kontrol deneyleri için, konsantre virüs yerine tam hücre kültürü ortamı kullanın. Hücre süspansiyonunu kuru iskelenin üstüne ekleyin.
- Her iskele için 2.2.1-2.2.3 arasındaki adımları yineleyin.
- İskeleleri bir hücre kültürü inkübatöründe 37 ° C'de 45-60 dakika boyunca inkübe edin. İskeleleri inkübatörden çıkarın; iskeleler bu süre zarfında çözeltiyi tamamen emecektir.
- Proliferasyonu indüklemek için, her bir kuyucuğa IL-15 (5 ng / mL) ve IL-7 (10 ng / mL) ile desteklenmiş tam hücre kültürü ortamı ekleyin; IL-2 de kullanılabilir. Her 48 kuyulu iskeleye 500 μL veya her 24 kuyulu iskeleye 1 mL ekleyin.
- İskeleleri 72 saat boyunca 37 ° C'de inkübe edin. Hücreler çoğaldıkça, medya turuncuya dönecektir.
- Her iskele için, 50 μL tam hücre kültürü ortamında (250 mL Click'in ortamı + 250 mL RPMI1640 media + 50 mL fetal sığır serumu + 5 mL glutamin ikamesi + 5 mL glutamin ikamesi + 5 mL penisilin / streptomisin) 1 × 10 6 aktive periferik kan mononükleer hücresini (PBMC) askıya alarak bir aliquot hazırlayın.
- Hücreleri analiz için iskelelerden izole edin.
- 1x PBS'de 0,5 M EDTA'yı 0,25 M EDTA'ya seyreltin.
- Her bir kuyucuktan fazla ortamı çıkarın ve ayrı 15 mL santrifüj tüplerinde toplayın.
- Hücreleri iskeleden izole etmek için, her iskeleye 0,25 M EDTA ekleyin. 48 kuyulu iskelelere 300 μL veya 24 delikli iskelelere 1 mL ekleyin. Tabağın oturmasına izin verin veya 3-4 dakika boyunca hafifçe çalkalayın.
- İskele çoğunlukla çözüldükten sonra, kuyunun içine yavaşça girip çıkın. İskeleyi tamamen çözmek için birkaç giriş ve çıkış pipetleme adımı gerekebilir. 10 dakika içinde çözünmezse, 200 μL 0.25 M EDTA daha ekleyin.
- İskele tamamen çözündükten sonra, çözeltiyi 15 mL'lik bir santrifüj tüpüne aktarın.
- Her iskele için 2.3.4 ve 2.3.5 numaralı adımları yineleyin.
- Her santrifüj tüpüne 12 mL PBS ekleyerek ve 5 dakika boyunca 400 × g'da santrifüj yaparak hücreleri iki kez yıkayın. Her tüpün dibinde bir hücre peleti oluşacaktır. Süpernatantı aspire edin ve yıkamayı tekrarlayın. Tüm EDTA'yı çıkarmak çok önemli olduğundan, süpernatantı her yıkamada tamamen aspire etmeye dikkat edin.
- PBS ile ikinci yıkamadan sonra, hücre peleti artık analiz için hazırdır. Analiz için gereken uygun protokolü izleyin.
Sonuçlar
Bu makrogözenekli aljinat iskelelerinin yapımı kolaydır ve liyofilizatörden gözenekli, kabarık ve beyaz diskler olarak çıkmalıdır. Bu deneyde çalışılmamış olmasına rağmen, kalsiyum-aljinat çözeltisi, kullanıcının ihtiyaçlarına bağlı olarak farklı şekillerde iskeleler oluşturmak için farklı kalıplara dökülebilir 9,10. İskeleler elektrostatiktir ve iyi plakanın kapağına veya eldivenli bir parmağa yapışabilir.
Tartışmalar
CAR-T hücre tedavisi hem araştırma hem de ticari uygulamalar için ilgi görmeye devam etmektedir. CAR-T hücre tedavisinin kan kanserlerinin tedavisinde elde ettiği başarıya rağmen, prosedürün yüksek maliyeti kullanımını sınırlar. Burada sunulan protokol, retronektin kaplı plakaların spinokülasyonuna gerek kalmadan T hücrelerinin viral gen transferi için yeni bir yöntem sunmaktadır. Transdüksiyona aracılık etmek için kuru makrogözenekli aljinat iskeleleri üretmek nispeten basittir ve geleneks...
Açıklamalar
P.A. ve Y.B., CAR-T hücre terapötiklerinin üretimi için biyomalzemelerin kullanımı ile ilgili patentler üzerinde mucitlerdir. Y.B., CAR-T hücre terapötik teknolojisi ile ilgili endüstri destekli bir araştırma hibesi alır (bu çalışmayla ilgisi yoktur). Diğer tüm yazarlar rakip çıkarları olmadığını beyan ederler.
Teşekkürler
Bu çalışma, Ulusal Sağlık Enstitüleri tarafından R37-CA260223, R21CA246414 Hibe Ödül Numaraları ile desteklenmiştir. NCSU flow cytometry core'a flow cytometry analizi konusunda eğitim ve rehberlik için teşekkür ederiz. Şemalar Biorender.com ile oluşturuldu
Malzemeler
| Name | Company | Catalog Number | Comments |
| 0.5 M EDTA | Invitrogen | 15575-038 | UltraPure, pH 8.0 |
| 1x DPBS | Gibco | 14190-144 | No calcium chloride or magnesium chloride |
| 3% Acetic Acid with Methylene Blue | Stemcell Technologies Inc | 07060 | |
| Activated Periphreal Blood Mononuclear Cells | - | - | Fresh or frozen |
| Calcium-D-Gluconate | Alfa Aesar | A11649 | |
| CD28.2 Antibody | BD | 555725 | 1 mg/mL |
| CD3 Antibody | Miltenyi | 130-093-387 | 100 μg/mL |
| Click's Media | FUJIFILM IRVINE SCIENTIFIC MS | 9195 | |
| DI Water | - | - | |
| Glutamax | Gibco | 35-050-061 | |
| HyClone FBS | Cytvia | SH3039603 | |
| HyClone RPMI 1640 Media | Cytvia | SH3009601 | |
| Penicillin-streptomycin (P/S) | Gibco | 15-140-122 | |
| Peripheral Blood Mononuclear Cells | - | - | Fresh or frozen |
| PRONOVA UP MVG | NovaMatrix | 4200101 | Sodium alginate |
| Recombinant Human IL-15 | Peprotech | 200-15 | 5 ng/mL |
| Recombinant Human IL-7 | Peprotech | 200-07 | 10 ng/mL |
| Retrovirus | - | - | 1 x 106 TU/mL |
Referanslar
- Prinzing, B. L., Gottschalk, S. M., Krenciute, G. C. A. R. T-cell therapy for glioblastoma: ready for the next round of clinical testing. Expert Review of Anticancer Therapy. 18 (5), 451-461 (2018).
- Bagley, S. J., Desai, A. S., Linette, G. P., June, C. H., O'Rourke, D. M. CAR T-cell therapy for glioblastoma: recent clinical advances and future challenges. Neuro-oncology. 20 (11), 1429-1438 (2018).
- Nair, R., Westin, J. CAR T cells. Advances in Experimental Medicine and Biology. 1342, 297-317 (2021).
- Jackson, H. J., Rafiq, S., Brentjens, R. J. Driving CAR T-cells forward. Nature Reviews. Clinical Oncology. 13 (6), 370-383 (2016).
- Sterner, R. C., Sterner, R. M. CAR-T cell therapy: current limitations and potential strategies. Blood Cancer Journal. 11 (4), 69 (2021).
- Miliotou, A. N., Papadopoulou, L. C. CAR T-cell therapy: A new era in cancer immunotherapy. Current Pharmaceutical Biotechnology. 19 (1), 5-18 (2018).
- Lee, H. -. J., et al. Retronectin enhances lentivirus-mediated gene delivery into hematopoietic progenitor cells. Biologicals: Journal of the International Association of Biological Standardization. 37 (4), 203-209 (2009).
- Rajabzadeh, A., Hamidieh, A. A., Rahbarizadeh, F. Spinoculation and retronectin highly enhance the gene transduction efficiency of Mucin-1-specific chimeric antigen receptor (CAR) in human primary T cells. BMC Molecular and Cell Biology. 22 (1), 57 (2021).
- Sun, J., Tan, H. Alginate-based biomaterials for regenerative medicine applications. Materials. 6 (4), 1285-1309 (2013).
- Nayak, A. K., Mohanta, B. C., Hasnain, M. S., Hoda, M. N., Tripathi, G. Chapter 14 - Alginate-based scaffolds for drug delivery in tissue engineering. Alginates in Drug Delivery. , 359-386 (2020).
- Lee, K. Y., Mooney, D. J. Alginate: properties and biomedical applications. Progress in Polymer Science. 37 (1), 106-126 (2012).
- Kuo, C. K., Ma, P. X. Ionically crosslinked alginate hydrogels as scaffolds for tissue engineering: part 1. Structure, gelation rate and mechanical properties. Biomaterials. 22 (6), 511-521 (2001).
- Soccol, C., et al. Probiotic nondairy beverages. Handbook of Plant-Based Fermented Food and Beverage Technology, Second Edition. , 707-728 (2012).
- Moody, C. T., et al. Restoring carboxylates on highly modified alginates improves gelation, tissue retention and systemic capture. Acta Biomaterialia. 138, 208-217 (2022).
- Brudno, Y., et al. Replenishable drug depot to combat post-resection cancer recurrence. Biomaterials. 178, 373-382 (2018).
- Moody, C. T., Palvai, S., Brudno, Y. Click cross-linking improves retention and targeting of refillable alginate depots. Acta Biomaterialia. 112, 112-121 (2020).
- Agarwalla, P., et al. Scaffold-mediated static transduction of T Cells for CAR-T Cell therapy. Advanced Healthcare Materials. 9 (14), 2000275 (2020).
- Agarwalla, P., et al. Bioinstructive implantable scaffolds for rapid in vivo manufacture and release of CAR-T cells. Nature Biotechnology. 40 (8), 1250-1258 (2022).
- Vera, J., et al. T lymphocytes redirected against the kappa light chain of human immunoglobulin efficiently kill mature B lymphocyte-derived malignant cells. Blood. 108 (12), 3890-3897 (2006).
- . PRONOVA UP MVG. IFF Nutrition Norge AS Available from: https://novamatrix.biz/store/pronova-up-mvg/ (2022)
- Zappasodi, R., Budhu, S., Abu-Akeel, M., Merghoub, T. In vitro assays for effector T cell functions and activity of immunomodulatory antibodies. Methods in Enzymology. 631, 43-59 (2020).
- Kong, B. S., Lee, C., Cho, Y. M. Protocol for the assessment of human T cell activation by real-time metabolic flux analysis. STAR Protocols. 3 (1), 101084 (2022).
- Bio-Rad cell activation protocols. Bio-Rad Available from: https://www.bio-rad-antibodies.com/cell-activation.html?JSESSIONID_STERLING=D6E538F76818E53C29884D6CC7334F24 (2022)
- Lin, H. -. R., Yeh, Y. -. J. Porous alginate/hydroxyapatite composite scaffolds for bone tissue engineering: Preparation, characterization, andin vitro studies. Journal of Biomedical Materials Research. 71 (1), 52-65 (2004).
- Wu, J., Zhao, Q., Sun, J., Zhou, Q. Preparation of poly(ethylene glycol) aligned porous cryogels using a unidirectional freezing technique. Soft Matter. 8 (13), 3620 (2012).
Yeniden Basımlar ve İzinler
Bu JoVE makalesinin metnini veya resimlerini yeniden kullanma izni talebi
Izin talebiThis article has been published
Video Coming Soon
JoVE Hakkında
Telif Hakkı © 2020 MyJove Corporation. Tüm hakları saklıdır