Bu içeriği görüntülemek için JoVE aboneliği gereklidir. Oturum açın veya ücretsiz deneme sürümünü başlatın.
Method Article
Amfifilik DNA Nanoyapılarından Sentetik Kondensatlar ve Hücre Benzeri Mimariler
Bu Makalede
Özet
Kurucu DNA oligonükleotidlerinden başlayarak amfifilik DNA nanoyıldızlarından oluşan sentetik biyomoleküler kondensatların hazırlanması için bir protokol sunuyoruz. Kondensatlar, tek bir nanostar bileşeninden veya iki bileşenden üretilir ve gömülü bir DNA şablonundan RNA'nın in vitro transkripsiyonunu sürdürmek için modifiye edilir.
Özet
Sentetik damlacıklar ve kondensatlar, bölümlere ayırma oluşturmak ve yaşam benzeri tepkileri sürdürmek için kullanılabilecekleri gelişmiş biyomimetik sistemlerin ve sentetik hücrelerin giderek daha yaygın bileşenleri haline gelmektedir. Sentetik DNA nanoyapıları, programlanabilir şekilleri, kimyasal işlevselleştirmeleri ve kendi kendine montaj davranışları nedeniyle yoğuşma oluşturan yapı taşları olarak önemli bir potansiyel göstermiştir. Son zamanlarda, DNA bağlantılarının hidrofobik kısımlarla etiketlenmesiyle elde edilen amfifilik DNA "nanostarlarının" özellikle sağlam ve çok yönlü bir çözüm oluşturduğunu gösterdik. Elde edilen amfifilik DNA kondensatları, karmaşık, çok bölmeli iç mimarileri sergilemek, çeşitli dış uyaranlara yapısal olarak yanıt vermek, makromolekülleri sentezlemek, yükleri yakalamak ve serbest bırakmak, morfolojik dönüşümlere uğramak ve canlı hücrelerle etkileşime girmek üzere programlanabilir. Burada, kurucu DNA oligonükleotidlerinden başlayarak amfifilik DNA kondensatlarının hazırlanması için protokoller gösteriyoruz. (i) Tek tip kondensatlar oluşturan tek bileşenli sistemleri, (ii) çekirdek-kabuk kondensatları oluşturan iki bileşenli sistemleri ve (iii) kondensatların RNA nanoyapılarının in vitro transkripsiyonunu desteklemek için modifiye edildiği sistemleri ele alacağız.
Giriş
Sentetik hücreler, mevcut biyolojik hücrelerin işlevlerini ve yapılarını çoğaltmak için aşağıdan yukarıya doğru yapılmış mikrometre ölçekli (10-50 μm) cihazlardır 1,2. Sentetik hücreler genellikle lipid çift katmanlı veziküller 3,4,5,6,7, polimeromlar 8,9 veya proteinozomlar 10,11'den yapılmış zarlarla bağlanır ve bunlar ayrıca iç bölümlendirme12,13 oluşturmak için de kullanılabilir. Canlı hücrelerde çeşitli işlevleri sürdürdüğü bilinen zarsız organellerden14 ilham alan polimer koaservatlar, biyomoleküler kondensatlar ve hidrojeller gibi yapılar, sentetik hücrelerde hem dış hem de iç bölümlendirme oluşturmak için çok yönlü ve sağlam alternatifler olarak ilgi görmektedir 15,16,17,18.
DNA nanoteknolojisinin19 çok yönlü araç setinden yararlanarak, boyutu, şekli, işlevselliği, değerliği ve karşılıklı etkileşimleri hassas bir şekilde programlanabilen yapay DNA nanoyapılarının kendi kendine montajından sentetik damlacıklar ve yoğunlaşmalar tasarlamak için çoklu çözümler geliştirilmiştir20. DNA damlacıkları veya yoğunlaşmaları biyouyumludur ve hem sentetik hücreler hem de organeller için iskele görevi görebilir, kimyasal ve biyomoleküler reaksiyonlara ev sahipliği yapabilir21, bilgi hesaplama22,23, kargoları yakalama ve serbest bırakma24,25 ve yapısal tepkilerisürdürme 26.
Yoğunlaşma oluşturan DNA nanoyapılarının çeşitli tasarımları arasında, C-yıldızları olarak adlandırılan amfifilik DNA nanoyıldızlarının sağlam ve çok yönlü olduğu kanıtlanmıştır27. C-yıldızları, çift sarmallı (ds)DNA kollarının çıktığı sabit bir DNA bağlantısından (tipik olarak dört yönlü) oluşan basit dallı motiflerdir28. Kollar daha sonra hidrofobik kısımlarla, tipik olarak kolesterolle uçlandırılır, bu da nanoyapıları amfifilik hale getirir ve basit bir tek kap tavlamanın ardından yoğunlaşmalarını sağlar. C-yıldız kondensatları, çok bölmeli mimariler 29,30 oluşturma, DNA ve katyon tetikleyicilerine yapısal olarak yanıt verme31, makromolekülleri sentezleme29, yükleri yakalama ve serbest bırakma32 ve canlı hücrelerle etkileşim33 dahil olmak üzere hassas yapısal ve işlevsel programlanabilirlik sağlar. Aşağıda, bileşen oligonükleotidlerinden başlayarak C-yıldız kondensatları üretmek için protokolleri tanımlayacağız ve tartışacağız.
Protokol, üç farklı C-yıldız tasarımı (Şekil 1) kullanarak tekli (tek bileşenli) ve ikili (iki bileşenli) kondensatların hazırlanmasını özetler - "Yanıt vermeyen", "TMSD'ye duyarlı" ve "RNA şablonlama". "Yanıt vermeyen" C-yıldızı (panel A), dört kavşağı oluşturan farklı dizilere sahip dört "çekirdek iplikçikten" oluşur. Dört özdeş kolesterol modifiye oligonükleotid, her bir kolun sonunda bir kolesterol molekülünün bulunmasını sağlamak için bağlantıya bağlanır. Yanıt vermeyen C-yıldızları, tekli ve ikili yoğunlaşmalar için basit, inert iskeleler oluşturur. "TMSD'ye duyarlı" C-yıldızında (panel B), kolesterolize iplikler ile bağlantı noktası arasındaki bağlantı, sarkan tek sarmallı (ss)DNA "ayak parmağı" alanına sahip bir "Toehold köprüsü" ipliği ile sağlanır. Tamamlayıcı bir ayak parmağı alanına sahip bir istilacı DNA zincirinin varlığında, ayak parmağı aracılı bir iplik yer değiştirme reaksiyonutetiklenebilir 34, bu sayede istilacı Toehold köprüsünün yerini alır, bağlantı noktası ile hidrofobik parçalar arasındaki bağlantıyı koparır ve DNA ağınınparçalanmasını tetikler 32. Son olarak, "RNA şablonlama" C-yıldızı (panel C), bir "Köprü" ipliğine tamamlayıcı bir "Baz" modifikasyonu içerir, ikincisi Brokoli aptamer29 için kopyalanabilir ssDNA şablonunu birbirine bağlar. Burada bahsedilen üç tip C-yıldız tasarımı için kurucu oligonükleotidlerin dizi ayrıntıları Ek Tablo 1'de ve önceki çalışmalarda 29,30,32'de bulunabilir.
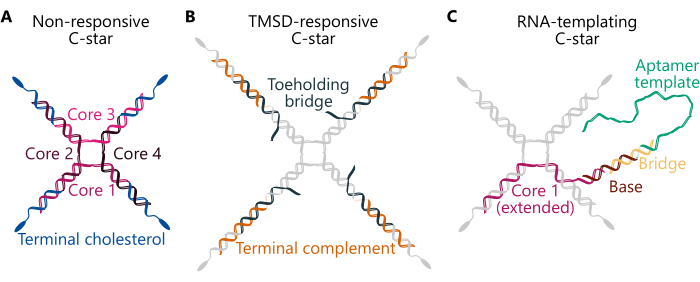
Şekil 1. Amfifilik DNA nanoyıldızlarının (C-yıldızları) üç farklı tasarımının şemaları. Burada tarif edilen C-yıldızlarının çeşitli örnekleri için oligonükleotid dizileri Ek Tablo 1'de bulunabilir. (A) "Çekirdek 1", "Çekirdek 2", "Çekirdek 3", "Çekirdek 4" (pembe tonlarında renkli) ve "Terminal kolesterol" (mavi renkli) bileşen oligonükleotid iplikleri ile yanıt vermeyen kondensatlar oluşturmak üzere tasarlanmış bir C-yıldızının şeması. Her benzersiz renk, benzersiz dizilimin bir oligonükleotid zincirini temsil eder. "Çekirdek 1" ve "Çekirdek 3"ün her biri "Çekirdek 2" ve "Çekirdek 4"ü kısmen tamamlar, ancak birbirini tamamlayıcı değildir. (B) Önceki çalışma32'de açıklandığı gibi, ayak parmağı aracılı iplik yer değiştirmesi yoluyla istilacı bir ipliğin eklenmesi üzerine parçalanmak üzere tasarlanmış bir C-yıldızının şeması. Bu C-yıldızı, "Çekirdek" ve "Terminal kolesterol" ipliklerinden (gri renkli), ayrıca bir "Terminal tamamlayıcı" (turuncu renkle gösterilmiştir) ve bir "Toeholding köprüsü" iplikçiğinden (koyu deniz mavisi ile gösterilmiştir) oluşur. Sonuncusu, uygun şekilde tasarlanmış bir istilacı ipliğin bağlanabileceği ve ardından "Toehold köprüsü" ipliğini tamamen değiştirebileceği altı nükleotidli bir çıkıntı içerir, bu da merkezi nanostar bağlantısının ("Çekirdek 1, 2, 3 ve 4"ten oluşur) "Terminal tamamlayıcısı" ve "Terminal kolesterol" ipliklerinden oluşan dublekslerden ayrılmasına neden olur. (C) Bir RNA aptameri için bir DNA şablonu ile işlevselleştirilmiş bir C-yıldızının şeması. Bu da "Terminal kolesterol" ipliği ve "Çekirdek 2, 3 ve 4" (tümü gri renkle gösterilmiştir) ve ayrıca "Çekirdek 1" ipliğinin genişletilmiş bir versiyonundan (pembe ile gösterilmiştir), bir "Baz" ipliğinden (kahverengi), bir "Köprü" ipliğinden (sarı) ve "Aptamer şablonundan" (yeşil) oluşur. Son iki iplikten oluşan DNA dupleksi, transkripsiyon başlangıç bölgesini işaretleyen T7 polimeraz promotör bölgesini oluşturur. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.
C-yıldız kondensatları, burada sunulan protokolde yüksek en-boy oranlı dikdörtgen kesitli sızdırmaz cam kılcal damarlar içinde gerçekleştirilen bileşen oligonükleotidlerin termal tavlanması üzerine oluşur. Bu kaplar çok sayıda önemli avantaj sunar: i) Sızdırmazlık, (bazen yavaş) tavlama adımlarında buharlaşmanın tamamen önlenmesini sağlar; ii) Kılcal damarların optik kalitesinde düz tabanı, kendi kendine montaj (veya sökme) geçici durumunun görüntülenmesini sağlar; iii) Kılcal damarların yüksek en-boy oranı, ağır yoğuşmaların geniş, düz bir alana yerleşmesini sağlayarak, kama şeklindeki kaplarda (örneğin, mikrosantrifüj tüpleri) meydana gelecek olan kendi kendine montaj geçici olayının sonraki aşamalarında birleşme ve toplanma olasılığını azaltır ve nispeten monodispers yoğuşma popülasyonları üretir; iv) Tavlamanın uzatılmış bir cam kılcal damarda gerçekleştirilmesi, numunenin, amfifilik kolesterolize oligonükleotidleri işe alarak kendi kendine montajı bozduğu gözlemlenen hidrofobik arayüzlere (hava, plastik veya yağ) maruz kalmasını en aza indirir. Montaj protokolü tamamlandıktan sonra, ek reaktifler içeren daha ileri deneyler için kondensatlar cam kılcal damarlardan ekstrakte edilebilir.
Protokol
NOT: Protokol üç bölüme ayrılmıştır. Bölüm 1, DNA oligonükleotidlerinin ve cam kılcal damarların hazırlanması da dahil olmak üzere ön koşul adımlarını açıklamaktadır. Bölüm 2, bir ve iki bileşenli tasarımlar dahil olmak üzere çeşitli tasarımlardaki C-yıldız kondensatlarının hazırlanmasını ve bunların cam kılcal damarlardan çıkarılmasını açıklar. Bölüm 3, bir RNA aptamerinin sentezi için tek bileşenli RNA şablonlama C-yıldız kondensatlarının kullanımını açıklar. Kullanıcı, baştan sona iyi laboratuvar uygulamalarını takip etmeli, gerekli tüm risk değerlendirmelerinin ve hafifletmelerin yapıldığından emin olmalı ve eldivenler, koruyucu gözlükler ve laboratuvar önlüğü dahil olmak üzere uygun kişisel koruyucu ekipman (KKD) giymelidir. Cam kılcal tüplerin temizlenmesi, önce bir yüzey aktif madde çözeltisinde ve ikinci olarak izopropanol veya etanolde sonikasyonlarını gerektirir. Kılcal borulardan C-yıldız kondensatlarının ekstraksiyonu, camı çentiklemek ve kırmak için bir elmas çizme kaleminin kullanılmasını gerektirir ve buna bağlı olarak cam parçalarından kaynaklanan yaralanma riski vardır. Kullanılan temel malzemeler, ekipman ve reaktifler Malzeme Tablosunda listelenmiştir. İşlevselleştirilmemiş oligonükleotidlerin çoğu, poliakrilamid jel elektroforezi (PAGE) saflaştırması ile sipariş edilen "genişletilmiş Core 1" ve "Aptamer şablonu" iplikleri hariç, tedarikçi tarafından standart tuzdan arındırma kullanılarak saflaştırılır. Kolesterolü modifiye edilmiş oligonükleotidler, ters fazlı yüksek performanslı sıvı kromatografisi (HPLC) kullanılarak tedarikçi tarafından saflaştırılır.
1. Ön Koşullar
NOT: Aşağıdaki çözeltiler ultra saf (Tip I) suda hazırlanmalı ve 0.22 μm şırınga filtreleri kullanılarak filtrelenmelidir: pH ~8.0'da 10 mM Tris, 1 mM EDTA içeren Tris-EDTA (TE) tamponu; 2 M NaCl ile desteklenmiş TE tamponu; ve 0.3 M NaCl ile desteklenmiş TE tamponu. Tampon çözeltiler hazırlandıktan sonra 2 hafta içinde kullanılmalı ve kullanılmadığı zaman 4 °C'de saklanmalıdır. Ek olarak, cam kılcal damarları temizlemek için ultra saf su içinde hacimce %1'lik bir alkali optik deterjan çözeltisi kullanılacaktır.
- DNA oligonükleotidlerinin liyofilize halden hazırlanması
- Liyofilize DNA oligonükleotid tüplerini kısaca santrifüjleyin (10-30 s boyunca 2000 x g ), liyofilize DNA topaklarının altta toplanmasını sağlamak için.
NOT: Santrifüjleme oda sıcaklığında (RT) 10-30 s yapılır. Burada kullanılan mini santrifüj varsayılan olarak 2000 x g'dir (6000 rpm). - Her bir oligonükleotidi 100 μM'de yeniden oluşturmak için uygun miktarda TE tamponu ekleyin. Tam çözünmeyi sağlamak için iyice sarın, ardından adım 1.1.1'e göre tüm sıvıyı toplamak için tüpleri döndürün.
- Her stok çözeltisi için, 260 nm'de absorbansı ölçün ve test edilen oligonükleotid dizisinin sönme katsayısını kullanarak nihai konsantrasyonu hesaplayın.
NOT: Belirli bir oligonükleotid dizisi için sönme katsayısı genellikle tedarikçinin Veri Sayfasında bulunur, ancak en yakın komşu model35 veya tek tek nükleotidlerin36 sönme katsayısının tablo haline getirilmiş değerleri kullanılarak çevrimiçi araçlarla da hesaplanabilir. - Rehidre edilmiş oligonükleotidleri kısa süreler için 4 °C'de (1 haftaya kadar) veya daha uzun süreli depolama için (6 aya kadar) -20 °C'de saklayın.
- Liyofilize DNA oligonükleotid tüplerini kısaca santrifüjleyin (10-30 s boyunca 2000 x g ), liyofilize DNA topaklarının altta toplanmasını sağlamak için.
- Cam kılcal boruların temizlenmesi
- Deiyonize sudaki optik bileşenler için% 1 alkali optik deterjan içinde sonikat.
- Temizlenecek gerekli sayıda cam kılcal tüpü alın ve kılcal damarlar kabın tabanında düz durmayacak şekilde uzun, dar bir kaba (örneğin bir beher veya 15/50 mL santrifüj tüpü) yerleştirin.
- Deterjanı kabın içine ekleyin ve kılcal boruların seviyesinin hemen üzerinde doldurun. Kılcal boruların içinde sıkışmış hava kabarcığı olmadığından emin olun - gerekirse çıkarmak için hafifçe vurun. Kabı gevşek bir şekilde kapatın (örn. kalay folyoda veya santrifüj tüpü kapağını kullanarak, sıkıca kapatılmadığından emin olun).
- Sonikasyon su banyosunu 40 °C'ye ayarlayın, kapalı kabı banyoya dik olarak yerleştirin ve 30 dakika boyunca sonikasyon yapın. Folyonun, kullanılıyorsa, sonikasyon banyosundaki su ile temas etmediğinden emin olun.
NOT: Bu çalışmada kullanılan sonikasyon banyosu varsayılan olarak 60 Hz'lik bir sonikasyon frekansına ve 150 W'lık bir sonikasyon gücüne sahiptir.
DİKKAT: Koşarken asla sonikasyon banyosuna ürün eklemeyin veya çıkarmayın; Her zaman önce protokolü duraklatın. - Sonikasyon tamamlandıktan sonra, sonikasyon su banyosunun ısıtma elemanını kapatın, ardından kaptaki kılcal damarları deiyonize veya ultra saf suyla iyice durulayın - en az beş kez, her seferinde durulama suyunu atın.
- Deiyonize sudaki optik bileşenler için% 1 alkali optik deterjan içinde sonikat.
- İzopropanol veya etanol içinde sonikat.
- Temizleme kabındaki cam kılcal borulara, kılcal boruların seviyesinin hemen üzerine kadar doldurarak izopropanol veya etanol (en az% 70) ekleyin. Adım 1.2.1.2'de olduğu gibi, kılcal borularda sıkışmış hava kabarcıkları olmadığından emin olun ve kabı gevşek bir şekilde kapatın.
- Kabı dik olarak sonikasyon banyosuna yerleştirin ve 15-30 dakika boyunca sonikasyon yapın.
DİKKAT: İzopropanol ve etanol yanıcıdır ve parlama noktaları RT'nin altındadır. Uygun boyutta bir kap seçerek temizlik sırasında kullanılan çözücülerin hacimlerini en aza indirin, kapların gevşek bir şekilde örtüldüğünden emin olun ve bu aşamada sonikasyon banyosunu gözetimsiz bırakmayın. - Sonikasyon tamamlandıktan sonra, izopropanol veya etanolü uygun şekilde atın ve kılcal damarları azot altında kurutun, tüy bırakmayan bir doku ile ele alın.
2. C-yıldız kondensatlarının hazırlanması ve ekstraksiyonu (Şekil 2)

Şekil 2: C-star karışımlarının yüklenmesi ve cam kılcal borulardan kondensatların çıkarılması. Tüm panellerde, C-star karışımı, görünürlüğe yardımcı olmak için sulu bir 25 mM kalsein çözeltisi ile değiştirilmiştir. (A-E) Tavlamadan önce atılması gereken temel adımlar, protokol bölüm 2.1 ve 2.2'ye karşılık gelir. (F-J) Tavlamadan sonra atılması gereken temel adımlar, protokol bölüm 2.3'e karşılık gelir. Ekstraksiyon sırasında (paneller (I-J)), mikrosantrifüj tüpü dikey olarak depolandığı sürece DNA kondensatları kılcal damardan tampon rezervuarına çökelecektir. Yoğuşma suyu çıplak gözle görülemez. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.
- Tek bileşenli kondensatlar için C-star karışımlarının hazırlanması
NOT: Tek bileşenlerin çeşitli tasarımları için sıra ayrıntıları Ek Tablo 1'de ve önceki çalışmalarda 29,30,32'de bulunabilir. Adım 2.1.9 ve 2.2.2'de tanımlanan yavaş tavlama protokolleri, nanostar ağlarının37 güçlü sıcaklığa bağlı reolojik özellikleri göz önüne alındığında, nanostar ağlarının kompakt morfolojilere gevşemesini sağlamak için geliştirilmiştir.- Oligonükleotid ve tampon bileşenleri, istenen C-yıldız tasarımına bağlı olarak değişecektir. Yanıt vermeyen dört kollu C-yıldızı, TMSD'ye duyarlı C-yıldızı veya RNA-şablonlayan C-yıldızı için 5 μM konsantrasyonda 60 μL'lik tek bileşenli C-yıldız kondensatları karışımı hazırlayın.
- Her tasarım için, Ek Tablo 2'de listelenen uygun bileşenleri ayrı bir mikrosantrifüj tüpüne pipetleyin ve pipetleme yoluyla iyice karıştırın.
NOT: Tüm oligonükleotid stok çözeltilerinin TE'de 100 μM konsantrasyonda olduğu varsayılmaktadır. - 60 μL'lik C-star solüsyonunun tamamını geri çekin ve karışımı Şekil 2A'da gösterildiği gibi temizlenmiş, kuru cam kılcal tüpe enjekte etmek için hava kabarcıklarının girmesini önlemeye dikkat ederek dikkatlice pipetleyin.
- Bir pipet kullanarak, kılcal borunun her iki ucuna yaklaşık 9-12 μL mineral yağ enjekte edin ve numuneyi C-yıldız çözeltisi ile hava arasında serbest bir arayüz olmayacak şekilde kapatın (bkz. Şekil 2B). Ardından, kılcal boruyu dışarıda yağ bulunmadığından emin olmak için kağıt mendille dikkatlice kurulayın (Şekil 2C), mineral yağı veya C-star solüsyonunu kılcal borudan dışarı atmamaya dikkat edin. Nihai sonuç Şekil 2D'de gösterilmiştir.
- Kılcal borunun her iki ucunu düz tarafı aşağı bakacak şekilde bir cam kapak kızağına yapıştırmak için küçük bir parti halinde iki parçalı epoksi yapıştırıcı hazırlayın. Tüpün açıklıklarının tamamen tutkalla kaplandığından ve Şekil 2E'de gösterildiği gibi sürekli bir sızdırmazlık oluşturduğundan emin olun.
- En az 3 saat, ancak tercihen gece boyunca kürlenmesi için bir kenara koyun.
- ~ 30 dakikalık kürlemeden sonra, tutkal tabakasında contada hava kabarcıklarının neden olduğu boşlukların olup olmadığını kontrol edin. Bunlar varsa, az miktarda yapıştırıcı kullanarak kapatın.
- Lameli üzerine yapıştırılmış kılcal boruyu kalay folyoya sarın ve folyonun cam kapak kızağının alt tarafında düz tutulduğundan emin olun. Folyo, aynı ve termal döngüleyicinin ısıtma elemanı arasında iyi bir termal temas sağlar (bir sonraki adıma bakın).
- Sarılmış numuneyi bir termal döngüleyiciye yerleştirin ve aşağıdaki protokolü kullanarak tavlayın: 95 °C'de 30 dakika tutun, ardından -0,04 °C·min-1'de 85 °C'den 50 °C'ye soğutun ve ardından 50 °C'den -0,5 °C·dk-1'de RT'ye soğutun.
- Tavlanmış C-star kondensatlarını 4 °C'de veya RT'de kılcal damar kapalı kaldığı sürece uzun süreler (aylar) boyunca saklayın, çünkü termal tavlama numuneyi etkili bir şekilde sterilize eder ve nükleazları denatüre eder. Yoğuşmaların bir uca doğru çökelmesini ve toplanmasını önlemek için depolama ve taşıma sırasında kılcal damarı düz tutun.
- İkili kondensatlar için C-star karışımlarının hazırlanması
NOT: İkili sistemler için C-yıldızı popülasyonlarının seçimi hakkında bilgi vermek için, ikili C-yıldızı yoğunlaşmalarının30 tasarım kurallarını ve beklenen faz davranışını açıklayan Malouf ve arkadaşlarının çalışmasına bakın.- İkili kondensatları hazırlamak için, yukarıdaki adım 2.1'de açıklanan 30 μL hacimdeki C-yıldız karışımlarını toplam 60 μL'lik bir hacme birleştirin, iyice karıştırın, kılcal damarlara yükleyin ve 2.1.4-2.1.8 adımlarını izleyin.
- Sarılmış numuneyi bir termal döngüleyiciye yerleştirin ve aşağıdaki protokolü kullanarak tavlayın: 95 °C'de 30 dakika tutun, ardından -0,01 °C·min-1'de 85 °C'den 40 °C'ye soğutun ve ardından -0,1 °C·min-1'de 40 °C'den RT'ye soğutun.
- Kılcal borulardan C-yıldız kondensatlarının ekstraksiyonu.
- TE tamponunda 60 μL 0.3 M NaCl içeren büyük (1.5 mL veya 2.0 mL) bir mikrosantrifüj tüpü hazırlayın.
- Kılcal numuneyi açın ve yapıştırılmış alanın her bir iç ucunda lamel alt tarafını çentiklemek için bir elmas karalama kalemi kullanın (Şekil 2F). Bu bölgedeki lamel kırın ve uygun şekilde atın.
- Kılcal boruları etanol ile iyice temizleyin ve kurulayın.
- Kılcal boruların her iki ucunu elmas çizik kalemle, önce alt tarafı ile (Şekil 2G), ardından tüpleri "sağ tarafı yukarı" çevirerek ve puanlayarak çizin.
- Skor çizgilerinin yağ-su arayüzü ile örtüşmediğinden emin olun. Ekstrakte edilen numunede yağ kalmasını önlemek için sulu bölge içinde olmaları gerekir.
- Kılcal boruların uçlarını koparın (Şekil 2H), tüpün orta kısmını koruyun ve geri kalanını atın. Kesilen kılcal boruyu, kılcal borunun tabanının tampon çözeltisi ile temas ettiğinden emin olarak adım 2.3.1'de hazırlanan mikrosantrifüj tüpüne yerleştirin (Şekil 2I).
- Yoğuşmalar, yerçekimi yoluyla tüpten tampon rezervuarına çökelecektir; bunun en az 10 dakika sürmesine izin verin (Şekil 2J). Kesilen kılcal boruyu çıkarın ve uygun şekilde atın. Bu nazik ekstraksiyon yaklaşımı, yoğuşma suyu agregasyonu riskini sınırlar.
3. RNA şablonlayan C-yıldız kondensatlarından bir RNA aptamerinin transkripsiyonu
NOT: Brokoli RNA aptamerinin üretimi için, bir difloro-4-hidroksibenziliden imidazolidinon (DFHBI) çözeltisi gereklidir - DFHBI tozu ilk olarak dimetil sülfoksit (DMSO) içinde 10 mM'de bir stok çözeltisi olarak hazırlanır, daha sonra RNaz ve DNaz içermeyen suda 600 μM'ye seyreltilir.
- RNA şablonlu C-yıldız kondensatlarının yıkanması
NOT: RNA şablonlu C-yıldız kondensatları, bağlanmamış şablon oligonükleotidlerinin çıkarılmasını sağlamak için üç kez yıkanır.- Ekstrakte edilen kondensatların çözeltisinin en az 5 dakika çökmesine izin verin ve ardından süpernatantın hacminin yaklaşık yarısını çıkarın.
- 60 μL'lik bir ekstrakte edilmiş kondensat hacmi için, 25-30 μL arasında süpernatanı çıkarın.
- Bu adımda çıkarılan yoğuşma sayısını en aza indirmek için sıvı seviyesinin üstünden pipetleyin.
- Çıkarılan süpernatantın yerini almak için aynı hacimde 0,3 M NaCl'yi TE'ye ekleyin ve pipetleme ile karıştırın.
- Toplam üç döngü için önceki iki adımı tekrarlayın.
- Ekstrakte edilen kondensatların çözeltisinin en az 5 dakika çökmesine izin verin ve ardından süpernatantın hacminin yaklaşık yarısını çıkarın.
- T7 transkripsiyon karışımının hazırlanması
NOT: T7 transkripsiyon karışımı, CellScript T7-FlashScribe Transkripsiyon Kiti kullanılarak hazırlanmıştır. Adım 3.2.2, üreticinin protokolünde yapılan bir değişikliktir ve burada bulunabilir38. Burada, bağlanma üzerine DFHBI'de floresanı indükleyen Brokoli RNA aptamerinin transkripsiyonunu açıklıyoruz. Diğer ışıklı aptamerler için, adım 3.2.2'de açıklanan DFHBI hacmini uygun florojen ile değiştirin. Diğer transkriptler için bu bileşeni tamamen kaldırın.- DMSO'da 10 mM DFHBI'lik bir stok çözeltisi hazırlayın, ardından RNaz ve DNaz içermeyen su kullanarak bir alikotu 600 μM'lik bir son konsantrasyona seyreltin.
- Transkripsiyon kiti bileşenlerini buz üzerinde çözün ve ardından aşağıdakileri steril pipet uçları kullanarak oda sıcaklığında otoklavlanmış bir mikrosantrifüj tüpüne pipetleyin: 2 μL 10x T7-Transkripsiyon Tamponu (transkripsiyon kitinde sağlanır), 1.8 μL 100 mM ATP, 1.8 μL 100 mM CTP, 1.8 μL 100 mM UTP, 1.8 μL 100 mM GTP, 2 μL 100 mM DTT, 2 μL 600 μM DFHBI, 0.5 μL RNaz inhibitörü, 2 μL T7-enzim çözeltisi (transkripsiyon kitinde sağlanır).
- Çözeltiyi pipetleyerek yavaşça karıştırın.
- Hazırladıktan hemen sonra adım 3.3 (RNA transkriptinin sentezi) için transkripsiyon karışımını kullanın.
- RNA transkriptinin sentezi
- Mikroskopi görüntüleme için uygun bir odaya, RNA şablonlayan C-yıldızlarından hazırlanan yıkanmış kondensatların 3.3 μL'sini pipetleyin ve daha önce hazırlanan transkripsiyon karışımının toplam hacmini ekleyin.
- Transkripsiyon karışımını kondensatlara ekledikten hemen sonra başlayarak 18 saatlik bir süre boyunca mikroskopi görüntüleri elde edin.
NOT: Mikroskopi ayarları, hazırlanan sisteme bağlı olacaktır. Numunedeki herhangi bir florofor için uygun uyarma ve emisyon ayarlarının kullanıldığından ve transkripsiyon ilerledikçe doygunluğa yol açmayacak maruz kalma sürelerinin kullanıldığından emin olun. Herhangi bir hızlandırılmış çekimde olduğu gibi, iyi bir sinyal için yeterince yüksek bir lazer veya LED gücü arasında bir uzlaşma bulunmalı ve aynı zamanda foto ağartma riskini en aza indirmelidir. LED tabanlı sistemlerde lazer tabanlı sistemlere kıyasla uzun süreler boyunca foto ağartma en aza indirilecektir. Önerilen görüntüleme aralıkları: İlk 2 saat için 20 dakika ve daha sonra 30 dakika.
Sonuçlar
Tavlamadan sonra, C-yıldız kondensatları, oluşumlarını doğrulamak için doğrudan kılcal boruda veya ekstraksiyondan sonra görüntülenebilir. Tüm C-yıldızı tasarım varyasyonları için, çapı yaklaşık 10-50 μm olan farklı küresel veya çok yüzlü kondensatlar gözlemlenmelidir, ikincisi kristalleşme meydana geldiğinde oluşur28,32. Tek bileşenli kondensatlar için, kondensatlar görünüşte ayrık ve tekdüze olmalıdır ve kullanılan C...
Tartışmalar
Burada açıklanan protokol, amfifilik DNA nanoyıldızlarından bir veya iki bileşenli kondensatların hazırlanması için, kondensatlara farklı tepkiler vermek için tasarım varyasyonları ile bir yaklaşım sağlar. Verilen protokol, TE'de 0.3 M NaCl'lik bir tampon çözeltisinde kondensatlar üretir, ancak tampon koşulları, yukarıda listelenen hacimler uygun şekilde değiştirilerek değiştirilebilir. Önceki çalışmalar, TE'de 0.2 M NaCl ve TE'de 0.1 M NaCl'de ve fosfat tamponlu salin (PBS) içinde C-yıl...
Açıklamalar
Herhangi bir çıkar çatışması beyan edilmedi.
Teşekkürler
LM, LDM ve DT, Horizon 2020 Araştırma ve İnovasyon Programı (ERC-STG No 851667 - NANOCELL) kapsamında Avrupa Araştırma Konseyi'nden (ERC) destek aldı. LDM, Royal Society Araştırma Bursları Araştırma Bursu'ndan (RGF/R1/180043) ve Royal Society Üniversitesi Araştırma Bursu'ndan (UF160152, URF/R/221009) destek alır.
Malzemeler
| Name | Company | Catalog Number | Comments |
| 0.22 μm syringe filters | Sigma-Aldrich | SLGVR33RB | |
| 24 x 60 mm #1.5 Rectangular cover glasses, Menzel Gläser | VWR | 631-0853 | |
| 2-Propanol | Sigma-Aldrich | 34683 | |
| 6 L Ultrasonic Cleaner with Digital Timer and Heat, 230 VAC | Cole-Parmer | WZ-08895-11 | |
| Araldite Rapid Adhesive 2 Part Epoxy Glue | RS | ARA-400005 | |
| Bio-Rad C1000 thermal cycler | Bio-Rad | 1851197 | |
| Brand Microcentrifuge Tube 2 mL with Locking Lid | Fisher Scientific | 15338665 | 2 mL microcentrifuge tubes for the extraction of C-star condensates |
| Diamond Scribing Pen | RS | 394-217 | |
| Difluoro-4-hydroxybenzylidene imidazolidinone (DFHBI) | Sigma-Aldrich | SML1627 | |
| Dimethyl sulfoxide (DMSO) | Sigma-Aldrich | 472301 | |
| Eppendorf PCR Clean Colorless Safe-Lock Centrifuge Tubes | Fisher Scientific | 0030123301 | 0.5 mL microcentrifuge tubes for the preparation of C-star mixtures |
| Ethanol Absolute 99.8+% | Fisher Scientific | 10437341 | 70% ethanol is sufficient for cleaning purposes |
| Fisherbrand ZX4 IR Vortex Mixer | Fisherbrand | 13284769 | |
| Hellmanex III | Hellma | 9-307-011-4-507 | |
| Hollow Rectangle Capillaries ID 0.40 x 4.00 mm, 50 mm in length | CM Scientific | 2540-50 | |
| Mineral oil | Sigma-Aldrich | 69794 | |
| Mini Centrifuge, 230 V | PRISM(TM) | Z763128 | |
| NaCl | Sigma-Aldrich | S3014 | |
| NanoDrop One Spectrophotometer | Thermo Fisher Scientific | ND-ONE-W | Used to measure absorbance of oligonucleotides for concentration calculations |
| Oligonucleotides | Integrated DNA Technologies | Custom | Oligonucleotide sequences are unique to the C-star design required. |
| ScriptGuard RNase inhibitor | CELLSCRIPT | C-SRI6310K | RNase inhibitor |
| T7-FlashScribe Transcription Kit | Cambio | C-ASF3507 | |
| Tris-EDTA buffer, 100x stock solution | Sigma-Aldrich | 574793 | |
| UltraPure DNase/RNase-Free Distilled Water | Invitrogen | 10977035 | |
| VWR Spec-Wipe 3 Wipers | VWR | 21914-758 |
Referanslar
- Buddingh', B. C., Hest, J. C. M. v. Artificial cells: Synthetic compartments with life-like functionality and adaptivity. Acc Chem Res. 50 (4), 769-777 (2017).
- Fanalista, F., et al. Shape and size control of artificial cells for bottom-up biology. ACS Nano. 13 (5), 5439-5450 (2019).
- Dora Tang, T. -. Y., et al. Fatty acid membrane assembly on coacervate microdroplets as a step towards a hybrid protocell model. Nat Chem. 6 (6), 527-533 (2014).
- Deshpande, S., et al. Spatiotemporal control of coacervate formation within liposomes. Nat Commun. 10 (1), 1800 (2019).
- Rubio-Sánchez, R., et al. Thermally driven membrane phase transitions enable content reshuffling in primitive cells. J Am Chem Soc. 143 (40), 16589-16598 (2021).
- Jahnke, K., Huth, V., Mersdorf, U., Liu, N., Göpfrich, K. Bottom-up assembly of synthetic cells with a DNA cytoskeleton. ACS Nano. 16 (5), 7233-7241 (2022).
- Tran, M. P., et al. A DNA segregation module for synthetic cells. Small. 19 (13), 2202711 (2023).
- Mason, A. F., Buddingh', B. C., Williams, D. S., Hest, J. C. M. v. Hierarchical self-assembly of a copolymer-stabilized coacervate protocell. J Am Chem Soc. 139 (48), 17309-17312 (2017).
- Gumz, H., et al. Toward functional synthetic cells: In-depth study of nanoparticle and enzyme diffusion through a cross-linked polymersome membrane. Adv Sci. 6 (7), 1801299 (2019).
- Huang, X., Patil, A. J., Li, M., Mann, S. Design and construction of higher-order structure and function in proteinosome-based protocells. J Am Chem Soc. 136 (25), 9225-9234 (2014).
- Booth, R., Qiao, Y., Li, M., Mann, S. Spatial positioning and chemical coupling in coacervate-in-proteinosome protocells. Angew Chem Int Ed Engl. 58 (27), 9120-9124 (2019).
- Hindley, J. W., et al. Light-triggered enzymatic reactions in nested vesicle reactors. Nat Commun. 9 (1), 1093 (2018).
- Zubaite, G., Hindley, J. W., Ces, O., Elani, Y. Dynamic reconfiguration of subcompartment architectures in artificial cells. ACS Nano. 16 (6), 9389-9400 (2022).
- Hirose, T., et al. A guide to membraneless organelles and their various roles in gene regulation. Nat Rev Mol Cell Biol. 24 (4), 288-304 (2023).
- Guindani, C., Silva, L. C. d., Cao, S., Ivanov, T., Landfester, K. Synthetic cells: From Simple Bio-Inspired Modules to Sophisticated Integrated Systems. Angew Chem Int Ed Engl. 61 (16), e202110855 (2022).
- Adamala, K. P., et al. Present and future of synthetic cell development. Nat Rev Mol Cell Biol. 25 (3), 162-167 (2023).
- Allen, M. E., et al. Biomimetic behaviors in hydrogel artificial cells through embedded organelles. Proc Natl Acad Sci U S A. 120 (35), e2307772120 (2023).
- Cook, A. B., Novosedlik, S., Hest, J. C. M. v. Complex coacervate materials as artificial cells. Acc Mater Res. 4 (3), 287-298 (2023).
- Seeman, N. C., Sleiman, H. F. DNA nanotechnology. Nat Rev Mater. 3, 17068 (2018).
- Takinoue, M. DNA droplets for intelligent and dynamical artificial cells: from the viewpoint of computation and non-equilibrium systems. Interface Focus. 13 (5), 20230021 (2023).
- Liu, W., Lupfer, C., Samanta, A., Sarkar, A., Walther, A. Switchable hydrophobic pockets in DNA protocells enhance chemical conversion. J Am Chem Soc. 145 (13), 7090-7094 (2023).
- Wilner, O. I., Willner, I. Functionalized DNA nanostructures. Chem Rev. 112 (4), 2528-2556 (2012).
- Gong, J., Tsumura, N., Sato, Y., Takinoue, M. Computational DNA droplets recognizing miRNA sequence inputs based on liquid-liquid phase separation. Adv Funct Mater. 32, 2202322 (2022).
- Jeon, B. -. J., Nguyen, D. T., Saleh, O. A. Sequence-controlled adhesion and microemulsification in a two-phase system of DNA liquid droplets. J Phys Chem. 124 (40), 8888-8895 (2020).
- Sato, Y., Sakamoto, T., Takinoue, M. Sequence-based engineering of dynamic functions of micrometer-sized DNA droplets. Sci Adv. 6 (23), 3471 (2020).
- Saleh, O. A., et al. Vacuole dynamics and popping-based motility in liquid droplets of DNA. Nat Commun. 14 (1), 3574 (2023).
- Rubio-Sánchez, R., Fabrini, G., Cicuta, P., Michele, L. D. Amphiphilic DNA nanostructures for bottom-up synthetic biology. Chem Commun. 57 (95), 12725-12740 (2021).
- Brady, R. A., Brooks, N. J., Cicuta, P., Di Michele, L. Crystallization of amphiphilic DNA C-Stars. Nano Lett. 17 (5), 3276-3281 (2017).
- Leathers, A., et al. Reaction-diffusion patterning of DNA-based artificial cells. J Am Chem Soc. 144 (38), 17468-17476 (2022).
- Malouf, L., et al. Sculpting DNA-based synthetic cells through phase separation and phase-targeted activity. Chem. 9 (11), 3347-3364 (2023).
- Fabrini, G., Minard, A., Brady, R. A., Antonio, M. D., Michele, L. D. Cation-responsive and photocleavable hydrogels from noncanonical amphiphilic DNA nanostructures. Nano Lett. 22 (2), 602-611 (2022).
- Brady, R. A., Brooks, N. J., Foderà, V., Cicuta, P., Di Michele, L. Amphiphilic-DNA platform for the design of crystalline frameworks with programmable structure and functionality. J Am Chem Soc. 140 (45), 15384-15392 (2018).
- Walczak, M., et al. Responsive core-shell DNA particles trigger lipid-membrane disruption and bacteria entrapment. Nat Commun. 12 (1), 4743 (2021).
- Zhang, D. Y., Winfree, E. Control of DNA strand displacement kinetics using Toehold exchange. J Am Chem Soc. 131 (47), 17303-17314 (2009).
- . Integrated DNA Technologies OligoAnalyzer Tool Available from: https://www.idtdna.com/pages/products/custom-dna-rna/dna-oligos/custom-dna-oligos (2024)
- Cavaluzzi, M. J., Borer, P. N. Revised UV extinction coefficients for nucleoside-5'-monophosphates and unpaired DNA and RNA. Nucleic Acids Res. 32 (1), e13 (2004).
- Lattuada, E., Caprara, D., Piazza, R., Sciortino, F. Spatially uniform dynamics in equilibrium colloidal gels. Sci Adv. 7 (49), (2021).
- . T7-FlashScribeTM Transcription Kit Available from: https://www.cellscript.com/products/018pl0617CS.pdf (2017)
- Zadeh, J. N., et al. NUPACK: Analysis and design of nucleic acid systems. J Comput Chem. 32 (1), 170-173 (2011).
- Walczak, M., Brady, R. A., Leathers, A., Kotar, J., Di Michele, L. Influence of hydrophobic moieties on the crystallization of amphiphilic DNA nanostructures. The Journal of Chemical Physics. 158 (8), 084501 (2023).
Yeniden Basımlar ve İzinler
Bu JoVE makalesinin metnini veya resimlerini yeniden kullanma izni talebi
Izin talebiThis article has been published
Video Coming Soon
JoVE Hakkında
Telif Hakkı © 2020 MyJove Corporation. Tüm hakları saklıdır