A subscription to JoVE is required to view this content. Sign in or start your free trial.
Method Article
توليد خطوط خلايا خروج المغلوب المرتبطة بالسنترومير Protein-E CENP-E-/- باستخدام نظام كريسبر / كاس 9
In This Article
Summary
تشير هذه المقالة إلى بناء خلايا خروج المغلوب المرتبطة بالبروتين E (CENP-E) باستخدام نظام CRISPR / Cas9 وثلاث استراتيجيات فحص قائمة على النمط الظاهري. لقد استخدمنا خط الخلايا الضربة القاضية CENP-E لإنشاء نهج جديد للتحقق من خصوصية وسمية مثبطات CENP-E ، وهو أمر مفيد لتطوير الأدوية والبحوث البيولوجية.
Abstract
برز نظام كريسبر (التكرارات العنقودية القصيرة المتباعدة بانتظام) / Cas9 كأداة قوية لتحرير الجينات بدقة وكفاءة في مجموعة متنوعة من الكائنات الحية. البروتين E المرتبط بالسنترومير (CENP-E) هو كينيسين موجه بنهاية زائد مطلوب لالتقاط الأنابيب الدقيقة الحركية ، ومحاذاة الكروموسوم ، ونقطة تفتيش تجميع المغزل. على الرغم من أن الوظائف الخلوية لبروتينات CENP-E قد تمت دراستها جيدا ، فقد كان من الصعب دراسة الوظائف المباشرة لبروتينات CENP-E باستخدام البروتوكولات التقليدية لأن استئصال CENP-E يؤدي عادة إلى تنشيط نقطة تفتيش تجميع المغزل ، وتوقف دورة الخلية ، وموت الخلايا. في هذه الدراسة ، قمنا بإخراج جين CENP-E تماما في خلايا HeLa البشرية ونجحنا في إنشاء خلايا CENP-E-/- HeLa باستخدام نظام CRISPR / Cas9.
تم إنشاء ثلاث استراتيجيات فحص محسنة قائمة على النمط الظاهري ، بما في ذلك فحص مستعمرة الخلايا ، والأنماط الظاهرية لمحاذاة الكروموسومات ، وشدة الفلورسنت لبروتينات CENP-E ، والتي تعمل بشكل فعال على تحسين كفاءة الفحص ومعدل النجاح التجريبي لخلايا CENP-E بالضربة القاضية. الأهم من ذلك ، أن حذف CENP-E يؤدي إلى اختلال الكروموسوم ، والموقع غير الطبيعي لبروتينات نقطة التفتيش الانقسامية BUB1 سيرين / ثريونين كيناز B (BubR1) ، والعيوب الانقسامية. علاوة على ذلك ، استخدمنا نموذج خلية HeLa بالضربة القاضية CENP-E لتطوير طريقة تحديد مثبطات CENP-E المحددة.
في هذه الدراسة ، تم وضع نهج مفيد للتحقق من خصوصية وسمية مثبطات CENP-E. علاوة على ذلك ، تقدم هذه الورقة بروتوكولات تحرير الجينات CENP-E باستخدام نظام CRISPR / Cas9 ، والذي يمكن أن يكون أداة قوية للتحقيق في آليات CENP-E في انقسام الخلايا. علاوة على ذلك ، سيساهم خط الخلايا الضربة القاضية CENP-E في اكتشاف مثبطات CENP-E والتحقق من صحتها ، والتي لها آثار مهمة على تطوير الأدوية المضادة للأورام ، ودراسات آليات انقسام الخلايا في بيولوجيا الخلية ، والتطبيقات السريرية.
Introduction
يتوسط تحرير الجينوم الهندسي التعديلات المستهدفة للجينات في مجموعة متنوعة من الخلايا والكائنات الحية. في حقيقيات النوى ، يمكن إدخال طفرات خاصة بالموقع من خلال تطبيقات النيوكليازات الخاصة بالتسلسل التي تحفز إعادة التركيب المتماثل للحمض النوويالمستهدف 1. في السنوات الأخيرة ، تم تصميم العديد من تقنيات تحرير الجينوم ، بما في ذلك نوكلياز إصبع الزنك (ZFNs) 2,3 ، والنوكليازات المستجيبة الشبيهة بمنشط النسخ (TALENs) 4,5 ، و meganucleases 6,7 ، لشق الجينومات في مواقع محددة ، ولكن هذه الأساليب تتطلب هندسة بروتين معقدة وإجراءات تجريبية زائدة عن الحاجة. أظهرت الدراسات أن النوع الثاني من بدائية النواة العنقودية المتجمعة بانتظام بين التكرارات القصيرة المتباعدة (CRISPR) / Cas هي تقنية فعالة لتحرير الجينات ، والتي تتوسط على وجه التحديد انقسام الحمض النووي الموجه بالحمض النووي الريبي والموقع في مجموعة واسعة من الخلايا والأنواع8،9،10،11. أحدثت تقنية الضربة القاضية الجينية CRISPR / Cas9 ثورة في مجالات البيولوجيا الأساسية والتكنولوجيا الحيوية والطب12.
طورت البكتيريا ومعظم العتائق نظاما مناعيا تكيفيا قائما على الحمض النووي الريبي يستخدم بروتينات كريسبر وكاس لتحديد وتدمير الفيروسات والبلازميدات13. العقدية المقيحة يحتوي Cas9 (SpCas9) endonuclease على محلول تقاطع هوليداي الشبيه ب RuvC (RuvC) ومجال His-Asn-His (HNH) ، والذي يمكنه التوسط بكفاءة في الفواصل ذات التسلسل المزدوج (DSBs) من خلال توفير الحمض النووي الريبي أحادي التوجيه الاصطناعي (sgRNA) الذي يحتوي على CRISPR RNAs (crRNA) و crRNA المنشط (tracrRNA) 14،15،16. يمكن إصلاح DSBs من خلال مسار الانضمام النهائي غير المتماثل (NHEJ) أو مسار الإصلاح الموجه بالتماثل (HDR) ، والذي يقدم طفرات متعددة ، بما في ذلك عمليات الإدراج أو الحذف أو بدائل النوكليوتيدات المفردة الخالية من الندبات ، في خلايا الثدييات 1,8. يمكن استخدام كل من NHEJ المعرض للخطأ ومسار HDR عالي الدقة للتوسط في خروج المغلوب الجيني من خلال عمليات الإدراج أو الحذف ، والتي يمكن أن تسبب طفرات إزاحة الإطار وكودونات التوقف المبكرة10.
مطلوب Kinesin-7 CENP-E لربط الأنابيب الدقيقة الحركية ومحاذاة الكروموسوم أثناء انقسام الخلايا17،18،19. الحقن المجهري للأجسام المضادة20،21 ، استنفاد siRNA22،23 ، التثبيط الكيميائي24،25،26 ، والحذف الجيني27،28،29 من CENP-E يؤدي إلى اختلال الكروموسوم ، وتنشيط نقطة تفتيش تجميع المغزل والعيوب الانقسامية ، مما يؤدي إلى اختلال الصيغة الصبغية وعدم استقرار الكروموسومات19,30. في الفئران ، يؤدي حذف CENP-E إلى نمو غير طبيعي وفتك جنيني في المراحل المبكرة جدا من التطور27،29،31. عادة ما يؤدي الحذف الجيني ل CENP-E إلى اختلال الكروموسوم وموت الخلايا26،27،29 ، وهو ما يمثل عقبة في دراسة وظائف وآليات بروتينات CENP-E.
أنشأت دراسة حديثة خط خلية خروج المغلوب CENP-E مشروطا باستخدام طريقة تحرير الجينات CRISPR / Cas9 القابلة للحث على الأوكسين32 ، والتي تتيح التدهور السريع لبروتينات CENP-E في وقت قصير نسبيا33. ومع ذلك ، حتى الآن ، لم يتم إنشاء خطوط خلايا خروج المغلوب CENP-E مستقرة ، وهو تحد تقني لم يتم حله في بيولوجيا CENP-E. بالنظر إلى المتانة الجينية34 ، واستجابات التعويض الجيني35،36،37 ، والبيئات المعقدة داخل الخلايا ، حيث أن العواقب المباشرة للحذف الكامل ل CENP-E قد تكون معقدة ولا يمكن التنبؤ بها ، فمن المهم إنشاء خطوط خلايا CENP-E للتحقيق في آليات محاذاة الكروموسوم ، ونقطة تفتيش تجميع المغزل ، ومسارات إشارات المصب.
يعد اكتشاف مثبطات CENP-E وتطبيقاتها أمرا مهما لعلاج السرطان. حتى الآن ، تم العثور على سبعة أنواع من مثبطات CENP-E وتوليفها ، بما في ذلك GSK923295 ومشتقاته24,25 ، PF-2771 38,39 ، مشتقات سقالة إيميدازو [1,2-a]بيريدين 40,41 ، مركب-A42,43 ، سينتيلين44,45 ، UA6278446 ، ومشتقات بنزو بيرولو [2,1-ب] ثيازول47. من بين هذه المثبطات ، GSK923295 هو مثبط CENP-E الخيفي والفعال الذي يرتبط بالمجال الحركي ل CENP-E ويثبط نشاط ATPase المحفز بالأنابيب الدقيقة CENP-E مع Ki من 3.2 ± 0.2 نانومتر24,25. ومع ذلك ، بالمقارنة مع الآثار المثبطة ل GSK923295 على الخلايا السرطانية المستزرعة ، فإن الآثار العلاجية ل GSK923295 في مرضى السرطان السريري ليست مثالية48,49 ، مما أثار أيضا مخاوف بشأن خصوصية GSK923295 ل CENP-E. علاوة على ذلك ، فإن الخصوصية والآثار الجانبية لمثبطات CENP-E الأخرى على بروتينات CENP-E هي قضايا رئيسية في أبحاث السرطان.
في هذه الدراسة ، قمنا بإخراج جين CENP-E تماما في خلايا HeLa باستخدام نظام CRISPR / Cas9. تم إنشاء ثلاث استراتيجيات فحص محسنة قائمة على النمط الظاهري ، بما في ذلك فحص مستعمرة الخلايا ، والأنماط الظاهرية لمحاذاة الكروموسومات ، وكثافة الفلورسنت لبروتينات CENP-E ، لتحسين كفاءة الفحص ومعدل نجاح تحرير الجينات CENP-E. علاوة على ذلك ، يمكن استخدام خطوط خلايا CENP-E لاختبار خصوصية المركبات المرشحة ل CENP-E.
Protocol
1. بناء ناقلات الضربة القاضية الجينية CRISPR / Cas9
- حدد تسلسل الحمض النووي الجينومي المستهدف على جين CENP-E البشري (GenBank Accession No. NM_001286734.2) وتصميم sgRNA باستخدام أداة تصميم CRISPR عبر الإنترنت (http://crispor.tefor.net/).
- أدخل تسلسلا جينوميا واحدا ، وحدد جينوم "Homo sapiens-human-UCSC Dec 2013 (مجموعة تحليل hg38) + تعدد أشكال النوكليوتيدات المفردة (SNPs): dbSNP148" ، وحدد الشكل المجاور للفضاء الأولي "20 bp-NGG-spCas9". اختر تسلسلين دليليين ، بما في ذلك sgRNA-1 و 5'-CGGCCGCACTCGCACGCAGA-3' و sgRNA-2 5'-TTCTTTAGAGACGCGGGCTC-3' ، وفقا لدرجات الخصوصية50 ، والكفاءة المتوقعة10 ، والحد الأدنى من الأهداف.
- ترتيب وتوليف oligonucleotides الحمض النووي واحد تقطعت بهم السبل (ssODNs). تمييع ssODNs في ddH2O إلى تركيز نهائي من 100 ميكرومتر. لفسفرة وتلدين أوليغوس sgRNA ، أضف 1 ميكرولتر من oligo الأمامي ، و 1 ميكرولتر من oligo العكسي ، و 0.5 ميكرولتر من T4 polynucleotide kinase ، و 1 μL من T4 polynucleotide kinase buffer ، و 6.5 μL من الماء الخالي من RNase في أنبوب تفاعل البوليميراز المتسلسل (PCR) ، واحتضان الأنبوب عند 37 درجة مئوية لمدة 30 دقيقة ، و 95 درجة مئوية لمدة 5 دقائق ؛ ثم انزل إلى 25 درجة مئوية عند 5 درجات مئوية دقيقة -1.
- هضم البلازميد pX458 باستخدام إنزيم تقييد Bbs
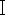 . أضف 1 ميكروغرام من بلازميد pX458 ، و 2 ميكرولتر من 10x buffer G ، و 1 ميكرولتر من Bbs
. أضف 1 ميكروغرام من بلازميد pX458 ، و 2 ميكرولتر من 10x buffer G ، و 1 ميكرولتر من Bbs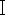 ، وأضف ddH2O الخالي من RNase إلى 20 ميكرولتر في أنبوب طرد مركزي سعة 1.5 مل. احتضان الأنبوب عند 37 درجة مئوية لمدة 2 ساعة. بعد ذلك ، قم بتنقية البلازميد الخطي باستخدام مجموعة استخراج هلام الحمض النووي للعمود وفقا لبروتوكولات الشركة المصنعة.
، وأضف ddH2O الخالي من RNase إلى 20 ميكرولتر في أنبوب طرد مركزي سعة 1.5 مل. احتضان الأنبوب عند 37 درجة مئوية لمدة 2 ساعة. بعد ذلك ، قم بتنقية البلازميد الخطي باستخدام مجموعة استخراج هلام الحمض النووي للعمود وفقا لبروتوكولات الشركة المصنعة. - اربط أوليغوس sgRNA في بلازميد pX458 (pSpCas9 (BB) -2A-بروتين الفلورسنت الأخضر (GFP) بلازميد ، Addgene ID. 48138). أضف 1 ميكرولتر من قليل النوكليوتيدات الملدن ، و 25 نانوغرام من البلازميد الخطي ، و 1 ميكرولتر من 10x T4 عازلة لربط الحمض النووي ، و 0.5 ميكرولتر من T4 DNA ligase (350 U / μL) وتكوين ما يصل إلى 10 ميكرولتر مع ddH2O في أنبوب طرد مركزي 1.5 مل. احتضان محلول الربط عند 16 درجة مئوية لمدة 2 ساعة.
- احتضان 10 ميكرولتر من البلازميد المبني مع خلايا DH5α المختصة على الجليد لمدة 30 دقيقة ، وصدمة حرارية عند 42 درجة مئوية لمدة 45 ثانية ، ووضعها على الفور على الجليد لمدة 5 دقائق. أضف 500 ميكرولتر من وسط لوريا بيرتاني (LB) وزرع الخلايا على صفيحة LB تحتوي على الأمبيسلين (100 ميكروغرام / مل). احتضانها عند 37 درجة مئوية لمدة 16 ساعة وفحص المستنسخة المقاومة.
- حدد 5-10 مستعمرات مفردة بطرف ماصة معقم وانقلها إلى مزرعة 1 مل من وسط LB مع الأمبيسلين (100 ميكروغرام / مل). احتضان الثقافة عند 37 درجة مئوية ورجها عند 180 دورة في الدقيقة لمدة 12-16 ساعة.
- عزل الحمض النووي البلازميد باستخدام مجموعة استخراج البلازميد وفقا لبروتوكولات الشركة المصنعة. تحقق من صحة الحمض النووي البلازميد لكل مستعمرة عن طريق تسلسل سانجر من موقع المروج U6 باستخدام التمهيدي U6-Fwd 5'-GAGGGCCTATTTCCCATGATTCC-3'.
- استخرج ونقي البلازميدات باستخدام مجموعة الحمض النووي البلازميد الخالية من الإندو وفقا لبروتوكولات الشركة المصنعة.
2. نقل وعزل وفحص خلايا هيلا بالضربة القاضية CENP-E
- استزراع خلايا هيلا في وسط النسر المعدل Dulbecco (DMEM) المكمل ب 10٪ مصل بقري جنيني و 1٪ بنسلين / ستربتومايسين في حاضنة مرطبة عند 37 درجة مئوية مع 5٪ CO2.
- احتضان خلايا هيلا باستخدام 0.25٪ تريبسين / إيثيلين ديامين حمض رباعي الخليك (EDTA) عند 37 درجة مئوية لمدة 2-3 دقائق ، وفصل الخلايا عن طريق السحب برفق ، ثم زرع الخلايا في صفائح جديدة بنسبة تخفيف 1: 4 لمرور الخلية.
- زرع الخلايا في لوحة 12 بئرا ، وثقافة التقاء 60-70 ٪ قبل النقل. نقل بلازميدات pX458-sgRNA إلى خلايا HeLa باستخدام الكواشف المشار إليها وفقا لبروتوكولات الشركة المصنعة (انظر جدول المواد).
- امزج بلطف 1 ميكروغرام من بلازميد pX458-sgRNA المصدق عليه و 50 ميكرولتر من وسط المصل المختزل في الأنبوب A. بعد ذلك ، امزج برفق 2 ميكرولتر من كاشف النقل و 50 ميكرولتر من وسط المصل المختزل في الأنبوب B. احتضان الأنابيب A و B بشكل منفصل في درجة حرارة الغرفة لمدة 5 دقائق.
- امزج كل من الأنبوب A والأنبوب B برفق واحتضانه في درجة حرارة الغرفة لمدة 5 دقائق. أضف الخليط إلى طبق من 12 بئرا ، واحتضن الخلايا لمدة 6 ساعات ، واستبدل الوسط بوسط DMEM جديد.
- افحص خلايا هيلا بعد 24 ساعة أو 48 ساعة باستخدام مجهر مضان لكفاءة النقل. بعد النقل لمدة 48 ساعة ، قم بفصل خلايا HeLa المنقولة تماما باستخدام 0.25٪ trypsin / EDTA عند 37 درجة مئوية لمدة 3-5 دقائق ، واحسب عدد الخلايا باستخدام غرفة Neubauer أو عداد الخلايا الآلي ، وقم بتقسيم الخلايا إلى ثلاث لوحات منفصلة من 96 بئرا لكل مجموعة منقولة وفقا لطرق التخفيف التسلسلي10.
- أعد الخلايا إلى حاضنة مرطبة ثم استزراعها لمدة 1-2 أسابيع أخرى. قم بتغيير وسط الثقافة مرة كل 3 أيام. للفحص القائم على النمط الظاهري والتحقق من خروج المغلوب CENP-E ، قم بفصل الخلايا وتوسيعها في 24 بئرا أو 12 لوحة بئر لمدة 5-7 أيام.
- افحص الخلايا الطافرة بأقطار مستعمرة خلايا أصغر باستخدام مجهر مقلوب مزود بعدسات موضوعية 10x و 20x.
ملاحظة: عادة ما تؤدي طفرات CENP-E إلى زيادة كبيرة في عدد الخلايا المنقسمة في مستعمرات الخلايا ، والتي يمكن أن تكون أحد المؤشرات الرئيسية لفحص الخلايا الطافرة CENP-E . - حصاد الخلايا لاستخراج الحمض النووي باستخدام مجموعة استخراج الحمض النووي الجينومي الحيواني وفقا لبروتوكولات الشركة المصنعة. قم بإعداد تفاعلات تفاعل البوليميراز المتسلسل على النحو التالي: 0.25 ميكرولتر من Taq polymerase ، 5 ميكرولتر من المخزن المؤقت 10x (Mg2+ plus) ، 4 ميكرولتر من مخاليط dNTP ، 500 نانوغرام من قالب الحمض النووي ، 1 ميكرولتر من oligo الأمامي ، 1 ميكرولتر من oligo العكسي ، واضبط ddH2O إلى 50 ميكرولتر. استخدم إعدادات برنامج تفاعل البوليميراز المتسلسل التالية لتضخيم الجينات: 98 درجة مئوية ، 10 ثوان ؛ 98 درجة مئوية ، 10 ثوان ، 55 درجة مئوية ، 30 ثانية ، 72 درجة مئوية ، 60 ثانية لمدة 33 دورة ؛ 72 درجة مئوية ، 10 دقائق ، ثم امسك عند 4 درجات مئوية.
ملاحظة: ترد قائمة بالمواد الأولية المحددة لاستنساخ الموضع المستهدف على النحو التالي: الهدف F1 من CENP-E ، 5'-GAGGGTCCTGGCCATTTTCCTG-3'؛ الهدف CENP-E R1 ، 5'-AGATCTCCGATCCTCCCCTGTC-3 '؛ الهدف CENP-E F2 ، 5'-TGGTAACTGCATTTTGGTGTTCTAC-3 '؛ الهدف CENP-E R2 ، 5'-CCTGTTGCAACGTGAGGGAAG-3'. - اربط الحمض النووي المستهدف في ناقل pMD18-T وفقا لبروتوكولات الشركة المصنعة. نقل البلازميد المربوط إلى خلايا DH5α المختصة وثقافة لاختيار المستنسخة.
- قم بإجراء تسلسل سانجر لتحديد أنواع خروج المغلوب CENP-E . عزل الحمض النووي البلازميد باستخدام مجموعة استخراج البلازميد وفقا لبروتوكولات الشركة المصنعة. قم بإجراء تسلسل سانجر للحمض النووي البلازميد لكل مستعمرة باستخدام الاشعال الأمامية والخلفية M13. M13F التمهيدي، 5'-TGTAAAACGACGGCCAGT-3'; M13R التمهيدي ، 5'-CAGGAAACAGCTATGACC-3'.
- قم بزرع خلايا HeLa الطافرة من النوع البري و CENP-E على أغطية زجاجية مقاس 12 مم في صفيحة من 24 بئرا ، على التوالي. قم بإزالة وسط DMEM الكامل وثبت الخلايا في محلول مثبت 4٪ بارافورمالدهايد / محلول ملحي مخزن بالفوسفات (PBS) في درجة حرارة الغرفة لمدة 10 دقائق.
- تلطيخ النوى بمحلول 4 '، 6-دياميدينو -2-فينيليندول (DAPI) في درجة حرارة الغرفة لمدة 5 دقائق. فحص الخلايا الطافرة CENP-E والتحقق من صحتها بناء على النمط الظاهري لمحاذاة الكروموسوم باستخدام مجهر مضان مزود بخطة فلور 40x / الفتحة العددية (NA) 0.75 الهدف.
- فحص خلايا خروج المغلوب CENP-E والتحقق من صحتها باستخدام تلطيخ وتحليل التألق المناعي (انظر القسم 3) لبروتينات CENP-E.
3. تلطيخ المناعي والفحص المجهري متحد البؤر عالي الدقة
- ثبت الخلايا بمحلول مثبت بارافورمالدهايد / PBS بنسبة 4٪ في درجة حرارة الغرفة لمدة 10 دقائق وانغمس لمدة 2 × 5 دقائق في 1x PBS.
ملاحظة: تأكد من أن الخلايا في حالة صحية وأن الخلايا يتم جمعها وتثبيتها برفق لتجنب انفصال الخلايا الطورية. - قم بتخلل الخلايا بنسبة 0.25٪ Triton X-100 / PBS في درجة حرارة الغرفة لمدة 10 دقائق واغمرها في 1x PBS لمدة 2 × 5 دقائق.
- قم بحظر الخلايا باستخدام 1٪ BSA / PBST (0.1٪ Tween 20 في PBS) في درجة حرارة الغرفة لمدة ساعة واحدة. تمييع الأجسام المضادة الأولية بنسبة 1٪ BSA / PBST واحتضان العينات عند 4 درجات مئوية لمدة 12 ساعة.
- تجاهل محاليل الأجسام المضادة الأولية ، وشطف الخلايا 3 × 5 دقائق مع 1x PBS ، واحتضان الخلايا مع الأجسام المضادة الثانوية المخففة في درجة حرارة الغرفة لمدة 2 ساعة.
- تخلص من الأجسام المضادة الثانوية واشطف الخلايا في 1x PBS لمدة 3 × 5 دقائق.
- تلطيخ النوى مع DAPI في درجة حرارة الغرفة لمدة 5 دقائق. قم بتركيب الشرائح باستخدام وسيط التثبيت. ختم الشرائح مع طلاء الأظافر.
- مراقبة وتسجيل الصور الفلورية باستخدام مجهر المسح متحد البؤر مزود بهدف 63x / NA 1.40.
4. إعداد كروموسوم وتحليل النمط النووي
- استزراع خلايا النوع البري وخلايا CENP-E-/- HeLa في وسط DMEM الكامل المكمل بمصل بقري جنيني بنسبة 10٪ و 1٪ بنسلين / ستربتومايسين لمدة 24 ساعة ثم احتضان خلايا CENP-E-/- HeLa من النوع البري مع 300 نانومتر كولشيسين لمدة 5 ساعات.
- احتضان الخلايا بنسبة 0.25٪ تربسين / EDTA عند 37 درجة مئوية لمدة 3 دقائق وجمع الخلايا في أنابيب طرد مركزي سعة 1.5 مل.
- قم بطرد الخلايا عند 1000 × جم لمدة 5 دقائق في درجة حرارة الغرفة ، وتخلص من المواد الطافية ، وأضف 1.2 مل من محلول KCl 0.075 مول / لتر ، واحتضانها عند 37 درجة مئوية لمدة 20 دقيقة.
- قم بطرد الخلايا عند 1000 × جم لمدة 5 دقائق في درجة حرارة الغرفة ، وتخلص من المواد الطافية ، وأضف 0.2 مل من المحلول المثبت (الميثانول: حمض الخليك الجليدي = 3: 1) للبادئة ، واخلطها برفق لمدة دقيقة واحدة.
- قم بطرد الخلايا عند 1000 × جم لمدة 5 دقائق في درجة حرارة الغرفة ، وجمع الكريات ، وإضافة 1.5 مل من المحلول المثبت في درجة حرارة الغرفة لمدة 10 دقائق ، ثم الطرد المركزي عند 1000 × جم لمدة 5 دقائق في درجة حرارة الغرفة.
- تخلص من المواد الطافية ، وأضف 0.6 مل من المحاليل المثبتة ، وقم بإعداد تعليق خلوي. أضف 3-5 قطرات من تعليق الخلية من ارتفاع 35-40 سم على شرائح الجليد.
ملاحظة: حافظ على الارتفاع لتحرير تعليق الخلية على الشرائح عند 35-40 سم ؛ خلاف ذلك ، قد تكون الكروموسومات مشتتة للغاية أو غير منفصلة عن بعضها البعض. - قم بتجفيف الشرائح على الفور باستخدام مصباح كحولي ، وقم بتلطيخ العينات بمحلول تلطيخ Giemsa بنسبة 10٪ لمدة 7 دقائق ، واشطف الشرائح بالماء الجاري لمدة 2 دقيقة ، وراقب العينات باستخدام مجهر ضوئي مجهز بهدف Plan Fluor 40x / NA 0.75.
5. مقايسة تشكيل مستعمرة الخلية
- قم بإعداد معلقات الخلايا في ألواح 6 آبار بكثافة خلية تتراوح بين 1000 و 2000 خلية / بئر. هز الألواح برفق لتوزيع الخلايا بالتساوي.
- ضع الألواح المكونة من 6 آبار في حاضنة CO2 واحتضانها لمدة 2-3 أسابيع عند 37 درجة مئوية مع 5٪ CO2. تغيير وسط الثقافة مرة واحدة كل 5 أيام. سجل الصور باستخدام مجهر مقلوب مزود بعدسات موضوعية 10x و 20x. احصد الخلايا عندما تكون المستعمرات مرئية (مئات الخلايا داخل استنساخ).
- لدراسة تأثيرات GSK923295 ، قم بزراعة الخلايا في ألواح 6 آبار لمدة 24 ساعة ، وأضف 2 مل من GSK923295 بتركيزات نهائية تبلغ 10 و 25 و 50 و 100 و 200 نانومتر.
ملاحظة: لا تحرك طبق الاستزراع في المرحلة المبكرة من تكوين الاستنساخ لتجنب تساقط الخلايا ، والتي يمكن أن تشكل استنساخا جديدا وتؤثر على فحص الخلايا المنقولة. - تخلص من وسط الاستزراع وقم بإصلاح الخلايا بنسبة 1٪ PFA في درجة حرارة الغرفة لمدة 10 دقائق. تلطيخ المستعمرات بمحلول تلطيخ بنفسجي بلوري بنسبة 0.1٪ في درجة حرارة الغرفة لمدة 15 دقيقة. شطف العينات مع 1x PBS ثلاث مرات. سجل صور مستعمرات الخلايا وحدد أقطار كل مستعمرة باستخدام برنامج ImageJ. اختر أداة تحديد الخط المستقيم ، انقر تحليل، اختر قياس، وسجل الطول.
- شطف المستعمرات مع 1 مل من محلول حمض الخليك 10 ٪ لمدة 5 دقائق. نقل 200 ميكرولتر من المحاليل الطافية في صفيحة 96 بئرا ، وقياس قيم الامتصاص باستخدام مقياس الطيف الضوئي للصفائح الدقيقة عندA 600 نانومتر.
6. فحص صلاحية الخلية
- قم بزرع الخلايا في ألواح 24 بئرا واستزرع الخلايا بكثافة 48 ساعة إلى 80-90٪.
- احتضان الخلايا ب 100 ميكرولتر من 0.25٪ تربسين / EDTA عند 37 درجة مئوية لمدة 3 دقائق.
- مزيج 400 ميكرولتر من PBS مع الخلايا مع بندقية ماصة. نقل 100 ميكرولتر من معلقات الخلية إلى لوحة 96 بئر.
- أضف 20 ميكرولتر من محلول MTS في كل بئر بتركيز نهائي يبلغ 317 ميكروغرام / مل واخلطه برفق وفقا لبروتوكولات الشركة المصنعة. احتضان العينات عند 37 درجة مئوية لمدة 1-3 ساعات في حاضنة CO2 .
- سجل قيم الامتصاص لكل بئر عند ذروة الامتصاص البالغة490 نانومتر باستخدام مقياس الطيف الضوئي للصفائح الدقيقة. استخدم طولا موجيا مرجعيا يبلغA 630 نانومتر لطرح الخلفية التي يساهم بها حطام الخلية والامتصاص غير المحدد (صلاحية الخلية = A490nm- A630 نانومتر).
النتائج
تم إنشاء خلايا CENP-E-/- HeLa بنجاح باستخدام نظام CRISPR / Cas9 (الشكل 1). يوضح الشكل 1 الجدول الزمني والخطوات التجريبية الحرجة لهذه الطريقة. أولا ، قمنا بتصميم وتوليف sgRNAs الخاصة ب CENP-E ، وقمنا بتلدين وربط sgRNAs في بلازميد pX458 ، ونقل البلازميد إلى خلايا HeLa ، و?...
Discussion
Kinesin-7 CENP-E هو منظم رئيسي في محاذاة الكروموسوم ونقطة تفتيش تجميع المغزل أثناء انقسام الخلايا17،19،20. عادة ما يؤدي الحذف الجيني ل CENP-E إلى تنشيط نقطة تفتيش تجميع المغزل ، وإيقاف دورة الخلية ، وموت الخلايا27،29،...
Disclosures
ليس لدى المؤلفين أي تضارب في المصالح للكشف عنه.
Acknowledgements
نشكر جميع أعضاء مختبر الهيكل الخلوي في جامعة فوجيان الطبية على المناقشات المفيدة. نشكر جون جين لين ، وتشي هونغ هوانغ ، ولينغ لين ، ولي لي بانغ ، ولين يينغ تشو ، وشي لين ، ومين شيا وو في مركز خدمات التكنولوجيا العامة ، جامعة فوجيان الطبية على مساعدتهم الفنية. نشكر Si-Yi Zheng و Ying Lin و Qi Ke في مركز التدريس التجريبي للعلوم الطبية الأساسية في جامعة فوجيان الطبية على دعمهم. تم دعم هذه الدراسة من خلال المنح التالية: المؤسسة الوطنية للعلوم الطبيعية في الصين (رقم المنحة 82001608 و 82101678) ، ومؤسسة العلوم الطبيعية بمقاطعة فوجيان ، الصين (رقم المنحة 2019J05071) ، والصناديق المشتركة لابتكار العلوم والتكنولوجيا ، مقاطعة فوجيان ، الصين (رقم المنحة 2021Y9160) ، ومشروع تمويل بدء البحث العلمي للمواهب عالية المستوى بجامعة فوجيان الطبية (رقم المنحة XRCZX2017025).
Materials
| Name | Company | Catalog Number | Comments |
| 0.25% Trypsin-EDTA | Gibco | 25200056 | |
| 1.5 mL centrifuge tube | Axygen | MCT-150-C | |
| 24-well plate | Corning | 3524 | |
| 4S Gelred, 10,000x in water | Sangon Biotech (Shanghai) | A616697 | |
| 50 mL centrifuge tube | Corning | 430828 | |
| 6 cm Petri dish | Corning | 430166 | |
| 95% ethanol | Sinopharm Chemical Reagent | 10009164 | |
| 96-well plate | Corning | 3599 | |
| Acetic acid | Sinopharm Chemical Reagent | 10000218 | Dissolve in H2O to prepare a 10% working solution. |
| Agarose | Sangon Biotech (Shanghai) | A620014 | |
| Alexa Fluor 488-labeled Goat Anti-Mouse IgG(H+L) | Beyotime | A0428 | For immunofluorescence. Dissolve in 1% BSA/PBST. 1:500 dilution. |
| Alexa Fluor 488-labeled Goat Anti-Rabbit IgG(H+L) | Beyotime | A0423 | For immunofluorescence. Dissolve in 1% BSA/PBST. 1:500 dilution. |
| Alexa Fluor 555-labeled Donkey Anti-Mouse IgG(H+L) | Beyotime | A0460 | For immunofluorescence. Dissolve in 1% BSA/PBST. 1:500 dilution. |
| Anhydrous ethanol | Sinopharm Chemical Reagent | 100092690 | |
| Anti-BubR1 rabbit monoclonal antibody | Abcam | ab254326 | For immunofluorescence. Dissolve in 1% BSA/PBST. 1:100 dilution |
| Anti-CENP-B mouse monoclonal antibody | Santa Cruz Biotechnology | sc-376392 | For immunofluorescence. Dissolve in 1% BSA/PBST. 1:50 dilution. |
| Anti-CENP-E rabbit monoclonal antibody | Abcam | ab133583 | For immunofluorescence. Dissolve in 1% BSA/PBST. 1:100 dilution. |
| Anti-fade mounting medium | Beyotime | P0131 | Slowing down the quenching of fluorescent signals. |
| Anti-α-tubulin mouse monoclonal antibody | Abcam | ab7291 | For immunofluorescence. Dissolve in 1% BSA/PBST. 1:100 dilution. |
| Biotek Epoch Microplate Spectrophotometer | Biotek Instruments | Biotek Epoch | |
| Bovine Serum Albumin (BSA) | Sinopharm Chemical Reagent | 69003435 | |
| BpiI (BbsI) | Thermo Fisher Scientific | ER1011 | |
| CellTiter 96 aqueous one solution cell proliferation assay | Promega | G3580 | |
| Centrifuge | Eppendorf | 5424BK745380 | |
| Colchicine | Sinopharm Chemical Reagent | 61001563 | |
| Confocal scanning microscope | Leica | Leica TCS SP8 | |
| Coverslip | CITOTEST | 80344-1220 | |
| DAPI | Beyotime | C1006 | |
| DH5α competent cells | Sangon Biotech (Shanghai) | B528413 | |
| DL2000 DNA marker | TaKaRa | 3427A | |
| Dulbecco's Modified Eagle Medium (DMEM) | Gibco | C11995500BT | |
Endo-free plasmid mini kit  | Omega | D6950 | |
| Ezup Column Animal Genomic DNA Purification Kit | Sangon Biotech (Shanghai) | B518251 | |
| Fetal bovine serum | Zhejiang Tianhang Biotechnology | 11011-8611 | |
| Gentian violet | Sinopharm Chemical Reagent | 71019944 | Dissolve in PBS to prepare 0.1% gentian violet/PBS. |
| Giemsa staining solution | Sinopharm Chemical Reagent | 71020260 | |
| GraphPad Prism version 8.0 software | GraphPad | www.graphpad.com | Statistical analysis. |
| GSK923295 | MedChemExpress | HY-10299 | |
| HeLa cell line | ATCC | CCL-2 | |
| Humidified incubator | Heal Force | HF90/HF240 | |
| Image J software | National Institutes of Health | https://imagej.nih.gov/ij/ | Image processing and analysis. |
| Inverted microscope | Nanjing Jiangnan Novel Optics | XD-202 | |
| LB agar powder | Sangon Biotech (Shanghai) | A507003 | |
| Lipo6000 transfection reagent | Beyotime | C0526 | |
| Nikon Ti-S2 microscope | Nikon | Ti-S2 | |
| Opti-MEM reduced serum medium | Gibco | 31985070 | |
| Paraformaldehyde | Sinopharm Chemical Reagent | 80096618 | Dissolve in PBS to prepare 4% paraformaldehyde/PBS. |
| Penicillin-streptomycin solution | HyClone | SV30010 | |
| SanPrep column DNA gel extraction kit | Sangon Biotech (Shanghai) | B518131 | |
| SanPrep column plasmid mini-preps kit | Sangon Biotech (Shanghai) | B518191 | |
| T4 DNA ligase | TaKaRa | 2011A | |
| T4 polynucleotide kinase | TaKaRa | 2021A | |
| TaKaRa Ex Taq | TaKaRa | RR001A | |
| Triton X-100 | Sinopharm Chemical Reagent | 30188928 | Dissolve in PBS to prepare 0.25% Triton X-100/PBS. |
| Tween 20 | Sinopharm Chemical Reagent | 30189328 | Dissolve in PBS to prepare 0.1% Tween 20/PBS. |
References
- Jiang, W., Bikard, D., Cox, D., Zhang, F., Marraffini, L. A. RNA-guided editing of bacterial genomes using CRISPR-Cas systems. Nature Biotechnology. 31 (3), 233-239 (2013).
- Bibikova, M., Beumer, K., Trautman, J. K., Carroll, D. Enhancing gene targeting with designed zinc finger nucleases. Science. 300 (5620), 764 (2003).
- Urnov, F. D., Rebar, E. J., Holmes, M. C., Zhang, H. S., Gregory, P. D. Genome editing with engineered zinc finger nucleases. Nature Reviews Genetics. 11 (9), 636-646 (2010).
- Joung, J. K., Sander, J. D. TALENs: a widely applicable technology for targeted genome editing. Nature Reviews Molecular Cell Biology. 14 (1), 49-55 (2013).
- Wood, A. J., et al. Targeted genome editing across species using ZFNs and TALENs. Science. 333 (6040), 307 (2011).
- Stoddard, B. L. Homing endonuclease structure and function. Quarterly Reviews of Biophysics. 38 (1), 49-95 (2005).
- Pâques, F., Duchateau, P. Meganucleases and DNA double-strand break-induced recombination: perspectives for gene therapy. Current Gene Therapy. 7 (1), 49-66 (2007).
- Cong, L., et al. Multiplex genome engineering using CRISPR/Cas systems. Science. 339 (6121), 819-823 (2013).
- Shmakov, S., et al. Discovery and functional characterization of diverse class 2 CRISPR-Cas systems. Molecular Cell. 60 (3), 385-397 (2015).
- Ran, F. A., et al. Genome engineering using the CRISPR-Cas9 system. Nature Protocols. 8 (11), 2281-2308 (2013).
- Jia, N., Patel, D. J. Structure-based functional mechanisms and biotechnology applications of anti-CRISPR proteins. Nature Reviews Molecular Cell Biology. 22 (8), 563-579 (2021).
- Hsu, P. D., Lander, E. S., Zhang, F. Development and applications of CRISPR-Cas9 for genome engineering. Cell. 157 (6), 1262-1278 (2014).
- Horvath, P., Barrangou, R. CRISPR/Cas, the immune system of bacteria and archaea. Science. 327 (5962), 167-170 (2010).
- Gasiunas, G., Barrangou, R., Horvath, P., Siksnys, V. Cas9-crRNA ribonucleoprotein complex mediates specific DNA cleavage for adaptive immunity in bacteria. Proceedings of the National Academy of Sciences of the United States of America. 109 (39), E2579-E2586 (2012).
- Jinek, M., et al. A programmable dual-RNA-guided DNA endonuclease in adaptive bacterial immunity. Science. 337 (6096), 816-821 (2012).
- Jackson, S. A., et al. CRISPR-Cas: Adapting to change. Science. 356 (6333), eaal5056 (2017).
- Wood, K. W., Sakowicz, R., Goldstein, L. S., Cleveland, D. W. CENP-E is a plus end-directed kinetochore motor required for metaphase chromosome alignment. Cell. 91 (3), 357-366 (1997).
- Craske, B., Welburn, J. P. I. Leaving no-one behind: how CENP-E facilitates chromosome alignment. Essays in Biochemistry. 64 (2), 313-324 (2020).
- Yu, K. W., Zhong, N., Xiao, Y., She, Z. Y. Mechanisms of kinesin-7 CENP-E in kinetochore-microtubule capture and chromosome alignment during cell division. Biology of the Cell. 111 (6), 143-160 (2019).
- Schaar, B. T., Chan, G. K., Maddox, P., Salmon, E. D., Yen, T. J. CENP-E function at kinetochores is essential for chromosome alignment. Journal of Cell Biology. 139 (6), 1373-1382 (1997).
- McEwen, B. F., et al. CENP-E is essential for reliable bioriented spindle attachment, but chromosome alignment can be achieved via redundant mechanisms in mammalian cells. Molecular Biology of the Cell. 12 (9), 2776-2789 (2001).
- Yao, X., Abrieu, A., Zheng, Y., Sullivan, K. F., Cleveland, D. W. CENP-E forms a link between attachment of spindle microtubules to kinetochores and the mitotic checkpoint. Nature Cell Biology. 2 (8), 484-491 (2000).
- Kim, Y., Heuser, J. E., Waterman, C. M., Cleveland, D. W. CENP-E combines a slow, processive motor and a flexible coiled coil to produce an essential motile kinetochore tether. Journal of Cell Biology. 181 (3), 411-419 (2008).
- Qian, X., et al. Discovery of the first potent and selective inhibitor of Centromere-Associated Protein E: GSK923295. ACS Medicinal Chemistry Letters. 1 (1), 30-34 (2010).
- Wood, K. W., et al. Antitumor activity of an allosteric inhibitor of centromere-associated protein-E. Proceedings of the National Academy of Sciences of the United States of America. 107 (13), 5839-5844 (2010).
- Pisa, R., Phua, D. Y. Z., Kapoor, T. M. Distinct mechanisms of resistance to a CENP-E inhibitor emerge in near-haploid and diploid cancer cells. Cell Chemical Biology. 27 (7), 850.e6-857.e6 (2020).
- Putkey, F. R., et al. Unstable kinetochore-microtubule capture and chromosomal instability following deletion of CENP-E. Developmental Cell. 3 (3), 351-365 (2002).
- Weaver, B. A., Silk, A. D., Montagna, C., Verdier-Pinard, P., Cleveland, D. W. Aneuploidy acts both oncogenically and as a tumor suppressor. Cancer Cell. 11 (1), 25-36 (2007).
- Silk, A. D., et al. Chromosome missegregation rate predicts whether aneuploidy will promote or suppress tumors. Proceedings of the National Academy of Sciences of the United States of America. 110 (44), E4134-E4141 (2013).
- Guo, Y., Kim, C., Ahmad, S., Zhang, J., Mao, Y. CENP-E-dependent BubR1 autophosphorylation enhances chromosome alignment and the mitotic checkpoint. Journal of Cell Biology. 198 (2), 205-217 (2012).
- Weaver, B. A., Cleveland, D. W. Aneuploidy: instigator and inhibitor of tumorigenesis. Cancer Research. 67 (21), 10103-10105 (2007).
- Nishimura, K., Fukagawa, T. An efficient method to generate conditional knockout cell lines for essential genes by combination of auxin-inducible degron tag and CRISPR/Cas9. Chromosome Research. 25 (3-4), 253-260 (2017).
- Owa, M., Dynlacht, B. A non-canonical function for Centromere-associated protein-E controls centrosome integrity and orientation of cell division. Communications Biology. 4 (1), 358 (2021).
- Barabási, A. L., Oltvai, Z. N. Network biology: understanding the cell's functional organization. Nature Reviews Genetics. 5 (2), 101-113 (2004).
- Rossi, A., et al. Genetic compensation induced by deleterious mutations but not gene knockdowns. Nature. 524 (7564), 230-233 (2015).
- Ma, Z., et al. PTC-bearing mRNA elicits a genetic compensation response via Upf3a and COMPASS components. Nature. 568 (7751), 259-263 (2019).
- El-Brolosy, M. A., et al. Genetic compensation triggered by mutant mRNA degradation. Nature. 568 (7751), 193-197 (2019).
- Kung, P. P., et al. Chemogenetic evaluation of the mitotic kinesin CENP-E reveals a critical role in triple-negative breast cancer. Molecular Cancer Therapeutics. 13 (8), 2104-2115 (2014).
- Kim, J. H., et al. Development of a novel HAC-based "gain of signal" quantitative assay for measuring chromosome instability (CIN) in cancer cells. Oncotarget. 7 (12), 14841-14856 (2016).
- Hirayama, T., et al. Synthetic studies of centromere-associated protein-E (CENP-E) inhibitors: 1. Exploration of fused bicyclic core scaffolds using electrostatic potential map. Bioorganic & Medicinal Chemistry. 21 (17), 5488-5502 (2013).
- Hirayama, T., et al. Synthetic studies on Centromere-associated protein-E (CENP-E) inhibitors: 2. Application of electrostatic potential map (EPM) and structure-based modeling to Imidazo[1,2-a]pyridine derivatives as anti-tumor agents. Journal of Medicinal Chemistry. 58 (20), 8036-8053 (2015).
- Ohashi, A., et al. A novel time-dependent CENP-E inhibitor with potent antitumor activity. PLoS One. 10 (12), e0144675 (2015).
- Ohashi, A., et al. Aneuploidy generates proteotoxic stress and DNA damage concurrently with p53-mediated post-mitotic apoptosis in SAC-impaired cells. Nature Communications. 6, 7668 (2015).
- Ding, X., et al. Probing CENP-E function in chromosome dynamics using small molecule inhibitor syntelin. Cell Research. 20 (12), 1386-1389 (2010).
- Liu, X., et al. Phase separation drives decision making in cell division. Journal of Biological Chemistry. 295 (39), 13419-13431 (2020).
- Henderson, M. C., et al. UA62784, a novel inhibitor of centromere protein E kinesin-like protein. Molecular Cancer Therapeutics. 8 (1), 36-44 (2009).
- Yamane, M., et al. Identification of benzo[d]pyrrolo[2,1-b]thiazole derivatives as CENP-E inhibitors. Biochemical and biophysical research communications. 519 (3), 505-511 (2019).
- Lock, R. B., et al. Initial testing of the CENP-E inhibitor GSK923295A by the pediatric preclinical testing program. Pediatric Blood & Cancer. 58 (6), 916-923 (2012).
- Chung, V., et al. First-time-in-human study of GSK923295, a novel antimitotic inhibitor of centromere-associated protein E (CENP-E), in patients with refractory cancer. Cancer Chemotherapy and Pharmacology. 69 (3), 733-741 (2012).
- Hsu, P. D., et al. DNA targeting specificity of RNA-guided Cas9 nucleases. Nature biotechnology. 31 (9), 827-832 (2013).
- Weaver, B. A., Cleveland, D. W. Decoding the links between mitosis, cancer, and chemotherapy: The mitotic checkpoint, adaptation, and cell death. Cancer Cell. 8 (1), 7-12 (2005).
- Manchado, E., Guillamot, M., Malumbres, M. Killing cells by targeting mitosis. Cell Death and Differentiation. 19 (3), 369-377 (2012).
- Dang, Y., et al. Optimizing sgRNA structure to improve CRISPR-Cas9 knockout efficiency. Genome Biology. 16, 280 (2015).
- Ratz, M., Testa, I., Hell, S. W., Jakobs, S. CRISPR/Cas9-mediated endogenous protein tagging for RESOLFT super-resolution microscopy of living human cells. Scientific Reports. 5, 9592 (2015).
- Koch, B., et al. Generation and validation of homozygous fluorescent knock-in cells using CRISPR-Cas9 genome editing. Nature Protocols. 13 (6), 1465-1487 (2018).
- Yan, Q., et al. Multiplex CRISPR/Cas9-based genome engineering enhanced by Drosha-mediated sgRNA-shRNA structure. Scientific Reports. 6, 38970 (2016).
- Cheng, Y., et al. CRISPR/Cas9-mediated chicken TBK1 gene knockout and its essential role in STING-mediated IFN-β induction in chicken cells. Frontiers in Immunology. 9, 3010 (2019).
- Zhou, Y., et al. High-throughput screening of a CRISPR/Cas9 library for functional genomics in human cells. Nature. 509 (7501), 487-491 (2014).
- Zeng, W., Guo, L., Xu, S., Chen, J., Zhou, J. High-throughput screening technology in industrial biotechnology. Trends in Biotechnology. 38 (8), 888-906 (2020).
- Tsai, S. Q., et al. GUIDE-seq enables genome-wide profiling of off-target cleavage by CRISPR-Cas nucleases. Nature Biotechnology. 33 (2), 187-197 (2015).
- Kim, D., et al. Genome-wide analysis reveals specificities of Cpf1 endonucleases in human cells. Nature Biotechnology. 34 (8), 863-868 (2016).
- Komor, A. C., Kim, Y. B., Packer, M. S., Zuris, J. A., Liu, D. R. Programmable editing of a target base in genomic DNA without double-stranded DNA cleavage. Nature. 533 (7603), 420-424 (2016).
- Nishimasu, H., et al. Engineered CRISPR-Cas9 nuclease with expanded targeting space. Science. 361 (6408), 1259-1262 (2018).
- Wang, H., et al. One-step generation of mice carrying mutations in multiple genes by CRISPR/Cas-mediated genome engineering. Cell. 153 (4), 910-918 (2013).
- Ablain, J., Durand, E. M., Yang, S., Zhou, Y., Zon, L. I. A CRISPR/Cas9 vector system for tissue-specific gene disruption in zebrafish. Developmental Cell. 32 (6), 756-764 (2015).
- Pickar-Oliver, A., Gersbach, C. A. The next generation of CRISPR-Cas technologies and applications. Nature Reviews Molecular Cell Biology. 20 (8), 490-507 (2019).
- Nalawansha, D. A., Gomes, I. D., Wambua, M. K., Pflum, M. K. H. HDAC inhibitor-induced mitotic arrest is mediated by Eg5/KIF11 acetylation. Cell Chemical Biology. 24 (4), 481.e5-492.e5 (2017).
- Kavalapure, R. S., et al. Design, synthesis, and molecular docking study of some 2-((7-chloroquinolin-4-yl) amino) benzohydrazide Schiff bases as potential Eg5 inhibitory agents. Bioorganic Chemistry. 116, 105381 (2021).
- Calligaris, D., Lafitte, D. Chemical inhibitors: the challenge of finding the right target. Chemistry & Biology. 18 (5), 555-557 (2011).
- Łomzik, M., et al. Metal-dependent cytotoxic and kinesin spindle protein inhibitory activity of Ru, Os, Rh, and Ir half-sandwich complexes of Ispinesib-derived ligands. Inorganic Chemistry. 59 (20), 14879-14890 (2020).
- Ferro, L. S., et al. Structural and functional insight into regulation of kinesin-1 by microtubule-associated protein MAP7. Science (New York, N.Y.). 375 (6578), 326-331 (2022).
- Atherton, J., et al. The mechanism of kinesin inhibition by kinesin-binding protein. eLife. 9, e61481 (2020).
Reprints and Permissions
Request permission to reuse the text or figures of this JoVE article
Request PermissionExplore More Articles
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. All rights reserved