このコンテンツを視聴するには、JoVE 購読が必要です。 サインイン又は無料トライアルを申し込む。
Method Article
CRISPR/Cas9システムを用いたセントロメア関連プロテイン-E CENP-E-/-ノックアウト細胞株の作製
要約
本稿では、CRISPR/Cas9システムと3つの表現型ベースのスクリーニング戦略を用いたセントロメア関連プロテインE(CENP-E)ノックアウト細胞の構築について報告します。私たちは、 CENP-Eノックアウト細胞株を利用して、CENP-E阻害剤の特異性と毒性を検証するための新しいアプローチを確立し、医薬品開発や生物学研究に有用です。
要約
CRISPR(clustered regular interspaced short palindromic repeats)/Cas9システムは、さまざまな生物において正確かつ効率的な遺伝子編集のための強力なツールとして登場しました。セントロメア関連プロテインE(CENP-E)は、動原体微小管の捕捉、染色体アライメント、および紡錘体アセンブリチェックポイントに必要なプラス末端指向性キネシンです。CENP-Eタンパク質の細胞機能は十分に研究されていますが、CENP-Eアブレーションは通常、紡錘体アセンブリチェックポイントの活性化、細胞周期の停止、および細胞死につながるため、従来のプロトコルを使用してCENP-Eタンパク質の直接的な機能を研究することは困難でした。本研究では、ヒトHeLa細胞の CENP-E 遺伝子を完全にノックアウトし、CRISPR/Cas9システムを用いて CENP-E-/- HeLa細胞を作製することに成功しました。
細胞コロニースクリーニング、染色体アライメント表現型、CENP-Eタンパク質の蛍光強度など、3つの最適化された表現型ベースのスクリーニング戦略が確立され、 CENP-E ノックアウト細胞のスクリーニング効率と実験成功率を効果的に向上させました。重要なことに、 CENP-Eの 欠失は、染色体のミスアライメント、BUB1有糸分裂チェックポイントセリン/スレオニンキナーゼB(BubR1)タンパク質の異常な位置、および有糸分裂欠損をもたらします。さらに、 CENP-E ノックアウトHeLa細胞モデルを用いて、CENP-E特異的阻害剤の同定法を開発しました。
この研究では、CENP-E阻害剤の特異性と毒性を検証するための有用なアプローチが確立されました。さらに、この論文では、細胞分裂におけるCENP-Eのメカニズムを調査するための強力なツールとなる可能性のあるCRISPR/Cas9システムを使用した CENP-E 遺伝子編集のプロトコルを提示します。さらに、 CENP-Eノックアウト細胞株は、抗腫瘍薬の開発、細胞生物学における細胞分裂メカニズムの研究、および臨床応用に重要な意味を持つCENP-E阻害剤の発見と検証に貢献します。
概要
遺伝子操作によるゲノム編集は、さまざまな細胞や生物の遺伝子の標的修飾を媒介します。真核生物では、標的DNAの相同組換えを刺激する配列特異的ヌクレアーゼの応用により、部位特異的な突然変異誘発を導入することができます1。近年、ジンクフィンガーヌクレアーゼ(ZFN)2,3、転写活性化因子様エフェクターヌクレアーゼ(TALEN)4,5、ホーミングメガヌクレアーゼ6,7など、いくつかのゲノム編集技術が特定の部位でゲノムを切断するように設計されていますが、これらのアプローチには複雑なタンパク質工学と冗長な実験手順が必要です。研究によると、II型原核生物クラスター化規則的インタースペース短回文反復(CRISPR)/Casシステムは、さまざまな細胞および種8,9,10,11においてRNA誘導部位特異的DNA切断を特異的に媒介する効率的な遺伝子編集技術であることが示されています8,9,10,11。CRISPR/Cas9遺伝子ノックアウト技術は、基礎生物学、バイオテクノロジー、医学の分野に革命をもたらしました12。
バクテリアとほとんどの古細菌は、CRISPRとCasタンパク質を使用してウイルスとプラスミドを識別して破壊するRNAベースの適応免疫システムを進化させました13。化膿連鎖球菌Cas9(SpCas9)エンドヌクレアーゼには、RuvC様Holliday junction resolvase(RuvC)およびHis-Asn-His(HNH)ドメインが含まれており、CRISPR RNA(crRNA)とトランス活性化crRNA(tracrRNA)を含む合成シングルガイドRNA(sgRNA)を提供することにより、配列特異的な二本鎖切断(DSB)を効率的に媒介することができます14,15,16。.DSBは、哺乳類細胞に挿入、欠失、または瘢痕のない一塩基置換を含む複数の変異を導入するインデル形成非相同末端結合(NHEJ)または相同性指向性修復(HDR)経路を介して修復することができます1,8。エラーが発生しやすいNHEJ経路と忠実度の高いHDR経路の両方を使用して、挿入または欠失を介して遺伝子ノックアウトを媒介することができ、フレームシフト変異および早期停止コドンを引き起こす可能性がある10。
キネシン-7 CENP-Eは、細胞分裂中の動原体-微小管の付着と染色体アライメントに必要です17,18,19。CENP-Eの抗体マイクロインジェクション20,21、siRNA枯渇22,23、化学的阻害24,25,26、および遺伝子欠失27,28,29は、染色体のミスアライメント、紡錘体アセンブリチェックポイントの活性化、および有糸分裂欠損を引き起こし、異数性および染色体不安定性をもたらす19,30.マウスでは、CENP-Eの欠失により、発生のごく初期段階で異常な発育と胚致死が生じます27,29,31。CENP-Eの遺伝子欠失は、通常、染色体のミスアライメントと細胞死26,27,29を引き起こし、CENP-Eタンパク質の機能とメカニズムを研究する上で障害となる。
最近の研究では、オーキシン誘導性CRISPR/Cas9遺伝子編集法32を用いて、比較的短時間でCENP-Eタンパク質の迅速な分解を可能にする条件付きCENP-Eノックアウト細胞株が確立されました33。しかし、今日まで、安定したCENP-Eノックアウト細胞株は確立されておらず、これはCENP-E生物学における未解決の技術的課題です。遺伝的頑健性34、遺伝的代償応答35、36、37、および複雑な細胞内環境を考慮すると、CENP-Eの完全な欠失の直接的な結果は複雑で予測不可能である可能性があるため、染色体アライメント、紡錘体アセンブリチェックポイント、および下流シグナル伝達経路のメカニズムを調査するためにCENP-Eノックアウト細胞株を確立することが重要です。
CENP-E阻害剤の発見と応用は、がん治療にとって重要です。現在までに、GSK923295とその誘導体24,25、PF-277138,39、イミダゾ[1,2-a]ピリジン足場誘導体40,41、化合物-A42,43、シンテリン44,45、UA6278446、ベンゾ[d]ピロロ[2,1-b]チアゾール誘導体47を含む7種類のCENP-E阻害剤が発見され、合成されている.これらの阻害剤の中で、GSK923295は、CENP−Eの運動ドメインに結合し、3.2±0.2nMのKiを有するCENP−E微小管刺激ATPアーゼ活性を阻害するアロステリックで効率的なCENP−E阻害剤である24,25。しかし、培養がん細胞に対するGSK923295の阻害効果と比較すると、臨床がん患者におけるGSK923295の治療効果は理想的ではなく48,49、CENP-EのGSK923295の特異性についても懸念が生じました。さらに、CENP-Eタンパク質に対する他のCENP-E阻害剤の特異性と副作用は、がん研究における重要な問題です。
本研究では、CRISPR/Cas9システムを用いてHeLa細胞の CENP-E 遺伝子を完全にノックアウトしました。CENP-E遺伝子編集のスクリーニング効率と成功率を向上させるために、細胞コロニースクリーニング、染色体アライメント表現型、CENP-Eタンパク質の蛍光強度など、3つの最適化された表現型ベースのスクリーニング戦略が確立されています。さらに、 CENP-E ノックアウト細胞株を使用して、CENP-Eの候補化合物の特異性を試験することができます。
プロトコル
1. CRISPR/Cas9遺伝子ノックアウトベクターの構築
- ヒト CENP-E 遺伝子上の標的ゲノムDNA配列を選択します(GenBank Accession No.NM_001286734.2)を作成し、オンラインCRISPRデザインツール(http://crispor.tefor.net/)を使用してsgRNAを設計します。
- ゲノム配列を1つ入力し、"Homo sapiens-human-UCSC Dec 2013 (hg38 analysis set) + single nucleotide polymorphisms (SNPs): dbSNP148"のゲノムを選択し、プロトスペーサー隣接モチーフ"20 bp-NGG-spCas9"を選択します。特異度スコア50、予測効率10、および最小のオフターゲットに従って、sgRNA-1、5'-CGGCCGCACTCGCACGCAGA-3' および sgRNA-2 5'-TTCTTTAGAGACGCGGCTC-3' の 2 つのガイド配列を選択します。
- 一本鎖DNAオリゴヌクレオチド(ssODN)を注文して合成します。ddH2O中のssODNを最終濃度100μMに希釈します。sgRNAオリゴをリン酸化してアニーリングするには、ポリメラーゼ連鎖反応(PCR)チューブにフォワードオリゴ1μL、リバースオリゴ1μL、T4ポリヌクレオチドキナーゼ0.5μL、T4ポリヌクレオチドキナーゼバッファー1μL、RNaseフリー水6.5μLを加え、チューブを37°Cで30分間、95°Cで5分間インキュベートします。その後、5°C min-1で25°Cまで下げます。
- Bbs
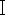 制限酵素を用いてpX458プラスミドを消化します。pX458プラスミド1 μg、10倍バッファーG2 μL、Bbs1
制限酵素を用いてpX458プラスミドを消化します。pX458プラスミド1 μg、10倍バッファーG2 μL、Bbs1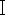 μLを添加し、RNaseフリーddH2Oを1.5 mL遠心チューブに20 μL添加します。チューブを37°Cで2時間インキュベートします。次に、カラムDNAゲル抽出キットを使用して、メーカーのプロトコルに従って直鎖状プラスミドを精製します。
μLを添加し、RNaseフリーddH2Oを1.5 mL遠心チューブに20 μL添加します。チューブを37°Cで2時間インキュベートします。次に、カラムDNAゲル抽出キットを使用して、メーカーのプロトコルに従って直鎖状プラスミドを精製します。 - sgRNAオリゴをpX458プラスミド(pSpCas9(BB)-2A-緑色蛍光タンパク質(GFP)プラスミド、Addgene ID. 48138)にライゲーションします。アニーリングしたオリゴヌクレオチド 1 μL、直鎖プラスミド 25 ng、10 x T4 DNA ライゲーションバッファー 1 μL、T4 DNA リガーゼ 0.5 μL(350 U/μL)を加え、1.5 mL の遠心チューブに ddH2O で最大 10 μL を作ります。ライゲーション溶液を16°Cで2時間インキュベートします。
- 構築したプラスミド10 μLをコンピテントDH5α細胞とともに氷上で30分間インキュベートし、42°Cで45秒間ヒートショックし、すぐに氷上に5分間置きます。500 μLのLuria-Bertani(LB)培地を添加し、アンピシリン(100 μg/mL)を含むLBプレートに細胞を播種します。37°Cで16時間インキュベートし、耐性クローンをスクリーニングします。
- 滅菌したピペットチップで5〜10個の単一コロニーを選択し、アンピシリン(100 μg/mL)を含むLB培地の1 mL培養物に移します。培養液を37°Cでインキュベートし、180rpmで12〜16時間振とうします。
- プラスミド抽出キットを使用して、メーカーのプロトコルに従ってプラスミドDNAを単離します。U6-Fwd プライマー 5'-GAGGGCCTATTTCCCATGATTCC-3' を使用して、U6 プロモーター部位からのサンガーシーケンシングにより、各コロニーのプラスミド DNA を検証します。
- エンドフリープラスミドDNAキットを使用して、メーカーのプロトコルに従ってプラスミドを抽出および精製します。
2. CENP-E ノックアウトHeLa細胞のトランスフェクション、単離、スクリーニング
- 10%ウシ胎児血清と1%ペニシリン/ストレプトマイシンを添加したDulbecco Modified Eagle's Medium(DMEM)でHeLa細胞を、加湿インキュベーターで37°C、5%CO2で培養します。
- 0.25%トリプシン/エチレンジアミン四酢酸(EDTA)を使用して37°Cで2〜3分間HeLa細胞をインキュベートし、ピペッティングで穏やかに細胞を解離した後、細胞継代用に希釈比1:4で新しいプレートに細胞を播種します。
- トランスフェクション前に細胞を12ウェルプレートに播種し、60〜70%のコンフルエントになるまで培養します。pX458-sgRNAプラスミドを、メーカーのプロトコルに従って参照試薬を使用してHeLa細胞にトランスフェクションします( 材料表を参照)。
- 1 μgのバリデーション済みpX458-sgRNAプラスミドと50 μLの還元血清培地をチューブAで穏やかに混合します。次に、チューブBにトランスフェクション試薬2μLと還元血清培地50μLを静かに混合し、チューブAとBを別々に室温で5分間インキュベートします。
- チューブAとチューブBの両方を穏やかに混合し、室温で5分間インキュベートします。混合物を12ウェルプレートに加え、細胞を6時間インキュベートし、培地を新しいDMEM培地と交換します。
- 24時間後または48時間後に蛍光顕微鏡を使用してHeLa細胞を検査し、トランスフェクション効率を確認します。48時間トランスフェクションした後、0.25%トリプシン/EDTAを用いて37°Cで3〜5分間トランスフェクションしたHeLa細胞を完全に解離し、ノイバウアーチャンバーまたは自動セルカウンターを使用して細胞数をカウントし、段階希釈法10に従って、トランスフェクションした集団ごとに細胞を3つの別々の96ウェルプレートに播種します。
- 細胞を加湿したインキュベーターに戻し、さらに1〜2週間培養します。培地は3日に1回交換してください。 CENP-E ノックアウトの表現型ベースのスクリーニングおよびバリデーションでは、24ウェルまたは12ウェルプレートで細胞を5〜7日間解離および増殖させます。
- 10倍および20倍の対物レンズを備えた倒立顕微鏡を使用して、細胞コロニーの直径が小さい変異細胞をスクリーニングします。
注: CENP-E 変異は、通常、細胞コロニー内の分裂細胞の数の有意な増加をもたらし、これは CENP-E 変異細胞をスクリーニングするための重要な指標の1つとなり得る。 - カラム動物ゲノムDNA抽出キットを使用して、DNA抽出用の細胞をメーカーのプロトコルに従って回収します。PCR反応を次のようにセットアップします:0.25 μLのTaqポリメラーゼ、5 μLの10xバッファー(Mg2+ plus)、4 μLのdNTP混合物、500 ngのDNAテンプレート、1 μLのフォワードオリゴ、1 μLのリバースオリゴ、ddH2Oを50 μLに調整します。 遺伝子増幅には、以下のPCRプログラム設定を使用します。 98 °C、10秒;98 °C、10 秒、55 °C、30 秒、72 °C、60 秒、33 サイクル。72°C、10分間、その後4°Cで保持します。
注:標的遺伝子座のクローニングのための特異的プライマーは、以下のようにリストされている: CENP-EターゲットF1 、5'-GAGGGTCCTGGCCATTTTCCTG-3'; CENP-EターゲットR1 、5'-AGATCTCCGATCCTCCCCTGTC-3'; CENP-EターゲットF2 、5'-TGGTAACTGCATTTTGGTGTTCTAC-3'; CENP-EターゲットR2 、5'-CCTGTTGCAACGTGAGGGAAG-3'。 - メーカーのプロトコールに従って、ターゲットDNAをpMD18-Tベクターにライゲーションします。ライゲーションしたプラスミドをコンピテントDH5α細胞にトランスフェクションし、クローンを選択するために培養します。
- サンガーシーケンシングを実施して、 CENP-E ノックアウトの種類を決定します。プラスミド抽出キットを使用して、メーカーのプロトコルに従ってプラスミドDNAを単離します。M13フォワードプライマーおよびリバースプライマーを使用して、各コロニーのプラスミドDNAのサンガーシーケンシングを実施します。M13Fプライマー、5'-TGTAAAACGACGGCCAGT-3';M13Rプライマー、5'-CAGGAAACAGCTATGACC-3'。
- 野生型および CENP-E 変異体HeLa細胞を、それぞれ24ウェルプレート内の12 mmガラスカバーガラスに播種します。完全なDMEM培地を除去し、細胞を4%パラホルムアルデヒド/リン酸緩衝生理食塩水(PBS)固定液中で室温で10分間固定します。
- 核を4',6-ジアミジノ-2-フェニルインドール(DAPI)溶液で室温で5分間染色します。Plan Fluor 40x/開口数(NA)0.75対物レンズを装着した蛍光顕微鏡を用いて、染色体アライメントの表現型に基づいて CENP-E 変異細胞をスクリーニングし、検証します。
- CENP-Eタンパク質の免疫蛍光染色および分析(セクション3を参照)を用いて、CENP-Eノックアウト細胞をスクリーニングし、検証します。
3. 免疫蛍光染色と高分解能共焦点顕微鏡
- 細胞を4%パラホルムアルデヒド/PBS固定液で室温で10分間固定し、1x PBSに2 x 5分間浸漬します。
注:細胞が健康な状態にあり、中期の細胞剥離を避けるために細胞が収集され、穏やかに固定されていることを確認してください。 - 細胞を0.25% Triton X-100/PBSで室温で10分間透過処理し、1x PBSに2 x 5分間浸漬します。
- 細胞を1% BSA/PBST(0.1% Tween 20 in PBS)で室温で1時間ブロッキングします。一次抗体を1% BSA/PBSTで希釈し、サンプルを4°Cで12時間インキュベートします。
- 一次抗体溶液を廃棄し、1x PBSで細胞を3 x 5分間リンスし、希釈した二次抗体とともに細胞を室温で2時間インキュベートします。
- 二次抗体を廃棄し、細胞を1x PBSで3 x 5分間すすぎます。
- 核をDAPIで室温で5分間染色します。スライドを封入剤で取り付けます。スライドをマニキュアで密封します。
- 63倍/NA 1.40の対物レンズを装備した走査型共焦点顕微鏡を使用して、蛍光画像を観察し、記録します。
4. 染色体調製と核型解析
- 10%ウシ胎児血清および1%ペニシリン/ストレプトマイシンを添加した完全DMEM培地で野生型および CENP-E-/- HeLa細胞を24時間培養した後、野生型および CENP-E-/- HeLa細胞を300 nMコルヒチンで5時間インキュベートします。
- 細胞を0.25%トリプシン/EDTAと37°Cで3分間インキュベートし、細胞を1.5 mLの遠心チューブに集めます。
- 細胞を室温で1,000 × g で5分間遠心分離し、上清を廃棄し、1.2 mLの0.075 mol/L KCl溶液を加え、37°Cで20分間インキュベートします。
- 細胞を室温で1,000 × g で5分間遠心分離し、上清を捨て、0.2 mLの固定液(メタノール:氷酢酸=3:1)を加えてプレフィケーションし、1分間穏やかに混合します。
- 細胞を室温で1,000×gで5分間遠心分離し、ペレットを回収し、1.5mLの固定液を室温で10分間添加した後、室温で1,000×gで5分間遠心分離します。
- 上清を捨て、0.6 mLの固定液を加え、細胞懸濁液を調製します。氷のスライドに35〜40 cmの高さから3〜5滴の細胞懸濁液を追加します。
注:細胞懸濁液をスライドに放出する高さは35〜40cmに保ちます。そうしないと、染色体が分散しすぎているか、互いに分離していない可能性があります。 - スライドを直ちにアルコールランプで乾燥させ、サンプルを10%ギムザ染色溶液で7分間染色し、スライドを流水で2分間すすぎ、Plan Fluor 40x/NA 0.75対物レンズを装着した光学顕微鏡でサンプルを観察します。
5. 細胞コロニー形成アッセイ
- 細胞懸濁液を6ウェルプレートで1,000-2,000細胞/ウェルの細胞密度で調製します。プレートを静かに振って、細胞を均等に分散させます。
- 6ウェルプレートをCO2 インキュベーターに入れ、37°Cで5%CO2で2〜3週間インキュベートします。培地は5日に1回交換してください。10倍と20倍の対物レンズを備えた倒立顕微鏡を使用して画像を記録します。コロニーが見えたら細胞を採取します(クローン内の数百の細胞)。
- GSK923295の影響を調べるには、6ウェルプレートで細胞を24時間培養し、最終濃度10、25、50、100、および200 nMで2 mLのGSK923295を加えます。
注:新しいクローンを形成し、トランスフェクションされた細胞のスクリーニングに影響を与える可能性のある細胞脱落を避けるために、クローン形成の初期段階で培養皿を動かさないでください。 - 培地を廃棄し、細胞を1%PFAで室温で10分間固定します。コロニーを0.1%クリスタルバイオレット染色液で室温で15分間染色します。サンプルを1x PBSで3回すすぎます。細胞コロニーの画像を記録し、ImageJソフトウェアを使用して各コロニーの直径を定量化します。 [直線 ] 選択ツールを選択して [解析] をクリックし、[ 計測] を選択して、長さを記録します。
- コロニーを1 mLの10%酢酸溶液で5分間すすぎます。上清溶液200μLを96ウェルプレートに移し、マイクロプレート分光光度計を用いてA600 nmの吸光度値を測定します。
6. 細胞生存率アッセイ
- 24ウェルプレートに細胞を播種し、48時間から80〜90%の密度で細胞を培養します。
- 細胞を100 μLの0.25%トリプシン/EDTAとともに37°Cで3分間インキュベートします。
- 400 μLのPBSをピペットガンで細胞と混合します。100 μL の細胞懸濁液を 96 ウェルプレートに移します。
- 最終濃度が 317 μg/mL になるように各ウェルに 20 μL の MTS 溶液を添加し、メーカーのプロトコルに従って穏やかに混合します。サンプルを37°CでCO2 インキュベーターで1〜3時間インキュベートします。
- マイクロプレート分光光度計を使用して、A490 nmの吸光度ピークにおける各ウェルの吸光度値を記録します。細胞破片と非特異的吸光度(細胞生存率 =A 490nm-A 630 nm)に寄与するバックグラウンドを差し引くには、A630 nmの参照波長を使用します。
結果
CENP-E-/- HeLa細胞は、CRISPR/Cas9システムを用いて作製に成功しました(図1)。この分析法のタイムラインと重要な実験ステップを図 1 に示します。まず、CENP-E特異的sgRNAを設計・合成し、sgRNAをアニーリングしてpX458プラスミドにライゲーションし、プラスミドをHeLa細胞にトランスフェクションし、48時間培養しました。トランスフ?...
ディスカッション
キネシン-7 CENP-Eは、細胞分裂中の染色体アライメントと紡錘体アセンブリチェックポイントにおける重要な調節因子です17,19,20。CENP-Eの遺伝子欠失は、通常、紡錘体アセンブリチェックポイントの活性化、細胞周期停止、および細胞死をもたらします27,29,51,52
開示事項
著者には開示すべき利益相反はありません。
謝辞
有益な議論をしてくれた福建医科大学細胞骨格研究所のすべてのメンバーに感謝します。福建医科大学公共技術サービスセンターのJun-Jin Lin氏、Zhi-Hong Huang氏、Ling Lin氏、Li-Li Pang氏、Lin-Ying Zhou氏、Xi Lin氏、Min-Xia Wu氏の技術支援に感謝します。福建医科大学基礎医学実験教育センターのSi-Yi Zheng氏、Ying Lin氏、Qi Ke氏のご支援に感謝します。本研究は、中国国家自然科学基金会(助成金番号82001608および82101678)、中国福建省自然科学基金会(助成金番号2019J05071)、中国福建省科学技術イノベーション共同基金(助成金番号2021Y9160)、福建医科大学ハイレベル人材科学研究立ち上げ資金プロジェクト(助成金番号XRCZX2017025)の支援を受けて行われました。
資料
| Name | Company | Catalog Number | Comments |
| 0.25% Trypsin-EDTA | Gibco | 25200056 | |
| 1.5 mL centrifuge tube | Axygen | MCT-150-C | |
| 24-well plate | Corning | 3524 | |
| 4S Gelred, 10,000x in water | Sangon Biotech (Shanghai) | A616697 | |
| 50 mL centrifuge tube | Corning | 430828 | |
| 6 cm Petri dish | Corning | 430166 | |
| 95% ethanol | Sinopharm Chemical Reagent | 10009164 | |
| 96-well plate | Corning | 3599 | |
| Acetic acid | Sinopharm Chemical Reagent | 10000218 | Dissolve in H2O to prepare a 10% working solution. |
| Agarose | Sangon Biotech (Shanghai) | A620014 | |
| Alexa Fluor 488-labeled Goat Anti-Mouse IgG(H+L) | Beyotime | A0428 | For immunofluorescence. Dissolve in 1% BSA/PBST. 1:500 dilution. |
| Alexa Fluor 488-labeled Goat Anti-Rabbit IgG(H+L) | Beyotime | A0423 | For immunofluorescence. Dissolve in 1% BSA/PBST. 1:500 dilution. |
| Alexa Fluor 555-labeled Donkey Anti-Mouse IgG(H+L) | Beyotime | A0460 | For immunofluorescence. Dissolve in 1% BSA/PBST. 1:500 dilution. |
| Anhydrous ethanol | Sinopharm Chemical Reagent | 100092690 | |
| Anti-BubR1 rabbit monoclonal antibody | Abcam | ab254326 | For immunofluorescence. Dissolve in 1% BSA/PBST. 1:100 dilution |
| Anti-CENP-B mouse monoclonal antibody | Santa Cruz Biotechnology | sc-376392 | For immunofluorescence. Dissolve in 1% BSA/PBST. 1:50 dilution. |
| Anti-CENP-E rabbit monoclonal antibody | Abcam | ab133583 | For immunofluorescence. Dissolve in 1% BSA/PBST. 1:100 dilution. |
| Anti-fade mounting medium | Beyotime | P0131 | Slowing down the quenching of fluorescent signals. |
| Anti-α-tubulin mouse monoclonal antibody | Abcam | ab7291 | For immunofluorescence. Dissolve in 1% BSA/PBST. 1:100 dilution. |
| Biotek Epoch Microplate Spectrophotometer | Biotek Instruments | Biotek Epoch | |
| Bovine Serum Albumin (BSA) | Sinopharm Chemical Reagent | 69003435 | |
| BpiI (BbsI) | Thermo Fisher Scientific | ER1011 | |
| CellTiter 96 aqueous one solution cell proliferation assay | Promega | G3580 | |
| Centrifuge | Eppendorf | 5424BK745380 | |
| Colchicine | Sinopharm Chemical Reagent | 61001563 | |
| Confocal scanning microscope | Leica | Leica TCS SP8 | |
| Coverslip | CITOTEST | 80344-1220 | |
| DAPI | Beyotime | C1006 | |
| DH5α competent cells | Sangon Biotech (Shanghai) | B528413 | |
| DL2000 DNA marker | TaKaRa | 3427A | |
| Dulbecco's Modified Eagle Medium (DMEM) | Gibco | C11995500BT | |
Endo-free plasmid mini kit  | Omega | D6950 | |
| Ezup Column Animal Genomic DNA Purification Kit | Sangon Biotech (Shanghai) | B518251 | |
| Fetal bovine serum | Zhejiang Tianhang Biotechnology | 11011-8611 | |
| Gentian violet | Sinopharm Chemical Reagent | 71019944 | Dissolve in PBS to prepare 0.1% gentian violet/PBS. |
| Giemsa staining solution | Sinopharm Chemical Reagent | 71020260 | |
| GraphPad Prism version 8.0 software | GraphPad | www.graphpad.com | Statistical analysis. |
| GSK923295 | MedChemExpress | HY-10299 | |
| HeLa cell line | ATCC | CCL-2 | |
| Humidified incubator | Heal Force | HF90/HF240 | |
| Image J software | National Institutes of Health | https://imagej.nih.gov/ij/ | Image processing and analysis. |
| Inverted microscope | Nanjing Jiangnan Novel Optics | XD-202 | |
| LB agar powder | Sangon Biotech (Shanghai) | A507003 | |
| Lipo6000 transfection reagent | Beyotime | C0526 | |
| Nikon Ti-S2 microscope | Nikon | Ti-S2 | |
| Opti-MEM reduced serum medium | Gibco | 31985070 | |
| Paraformaldehyde | Sinopharm Chemical Reagent | 80096618 | Dissolve in PBS to prepare 4% paraformaldehyde/PBS. |
| Penicillin-streptomycin solution | HyClone | SV30010 | |
| SanPrep column DNA gel extraction kit | Sangon Biotech (Shanghai) | B518131 | |
| SanPrep column plasmid mini-preps kit | Sangon Biotech (Shanghai) | B518191 | |
| T4 DNA ligase | TaKaRa | 2011A | |
| T4 polynucleotide kinase | TaKaRa | 2021A | |
| TaKaRa Ex Taq | TaKaRa | RR001A | |
| Triton X-100 | Sinopharm Chemical Reagent | 30188928 | Dissolve in PBS to prepare 0.25% Triton X-100/PBS. |
| Tween 20 | Sinopharm Chemical Reagent | 30189328 | Dissolve in PBS to prepare 0.1% Tween 20/PBS. |
参考文献
- Jiang, W., Bikard, D., Cox, D., Zhang, F., Marraffini, L. A. RNA-guided editing of bacterial genomes using CRISPR-Cas systems. Nature Biotechnology. 31 (3), 233-239 (2013).
- Bibikova, M., Beumer, K., Trautman, J. K., Carroll, D. Enhancing gene targeting with designed zinc finger nucleases. Science. 300 (5620), 764 (2003).
- Urnov, F. D., Rebar, E. J., Holmes, M. C., Zhang, H. S., Gregory, P. D. Genome editing with engineered zinc finger nucleases. Nature Reviews Genetics. 11 (9), 636-646 (2010).
- Joung, J. K., Sander, J. D. TALENs: a widely applicable technology for targeted genome editing. Nature Reviews Molecular Cell Biology. 14 (1), 49-55 (2013).
- Wood, A. J., et al. Targeted genome editing across species using ZFNs and TALENs. Science. 333 (6040), 307 (2011).
- Stoddard, B. L. Homing endonuclease structure and function. Quarterly Reviews of Biophysics. 38 (1), 49-95 (2005).
- Pâques, F., Duchateau, P. Meganucleases and DNA double-strand break-induced recombination: perspectives for gene therapy. Current Gene Therapy. 7 (1), 49-66 (2007).
- Cong, L., et al. Multiplex genome engineering using CRISPR/Cas systems. Science. 339 (6121), 819-823 (2013).
- Shmakov, S., et al. Discovery and functional characterization of diverse class 2 CRISPR-Cas systems. Molecular Cell. 60 (3), 385-397 (2015).
- Ran, F. A., et al. Genome engineering using the CRISPR-Cas9 system. Nature Protocols. 8 (11), 2281-2308 (2013).
- Jia, N., Patel, D. J. Structure-based functional mechanisms and biotechnology applications of anti-CRISPR proteins. Nature Reviews Molecular Cell Biology. 22 (8), 563-579 (2021).
- Hsu, P. D., Lander, E. S., Zhang, F. Development and applications of CRISPR-Cas9 for genome engineering. Cell. 157 (6), 1262-1278 (2014).
- Horvath, P., Barrangou, R. CRISPR/Cas, the immune system of bacteria and archaea. Science. 327 (5962), 167-170 (2010).
- Gasiunas, G., Barrangou, R., Horvath, P., Siksnys, V. Cas9-crRNA ribonucleoprotein complex mediates specific DNA cleavage for adaptive immunity in bacteria. Proceedings of the National Academy of Sciences of the United States of America. 109 (39), E2579-E2586 (2012).
- Jinek, M., et al. A programmable dual-RNA-guided DNA endonuclease in adaptive bacterial immunity. Science. 337 (6096), 816-821 (2012).
- Jackson, S. A., et al. CRISPR-Cas: Adapting to change. Science. 356 (6333), eaal5056 (2017).
- Wood, K. W., Sakowicz, R., Goldstein, L. S., Cleveland, D. W. CENP-E is a plus end-directed kinetochore motor required for metaphase chromosome alignment. Cell. 91 (3), 357-366 (1997).
- Craske, B., Welburn, J. P. I. Leaving no-one behind: how CENP-E facilitates chromosome alignment. Essays in Biochemistry. 64 (2), 313-324 (2020).
- Yu, K. W., Zhong, N., Xiao, Y., She, Z. Y. Mechanisms of kinesin-7 CENP-E in kinetochore-microtubule capture and chromosome alignment during cell division. Biology of the Cell. 111 (6), 143-160 (2019).
- Schaar, B. T., Chan, G. K., Maddox, P., Salmon, E. D., Yen, T. J. CENP-E function at kinetochores is essential for chromosome alignment. Journal of Cell Biology. 139 (6), 1373-1382 (1997).
- McEwen, B. F., et al. CENP-E is essential for reliable bioriented spindle attachment, but chromosome alignment can be achieved via redundant mechanisms in mammalian cells. Molecular Biology of the Cell. 12 (9), 2776-2789 (2001).
- Yao, X., Abrieu, A., Zheng, Y., Sullivan, K. F., Cleveland, D. W. CENP-E forms a link between attachment of spindle microtubules to kinetochores and the mitotic checkpoint. Nature Cell Biology. 2 (8), 484-491 (2000).
- Kim, Y., Heuser, J. E., Waterman, C. M., Cleveland, D. W. CENP-E combines a slow, processive motor and a flexible coiled coil to produce an essential motile kinetochore tether. Journal of Cell Biology. 181 (3), 411-419 (2008).
- Qian, X., et al. Discovery of the first potent and selective inhibitor of Centromere-Associated Protein E: GSK923295. ACS Medicinal Chemistry Letters. 1 (1), 30-34 (2010).
- Wood, K. W., et al. Antitumor activity of an allosteric inhibitor of centromere-associated protein-E. Proceedings of the National Academy of Sciences of the United States of America. 107 (13), 5839-5844 (2010).
- Pisa, R., Phua, D. Y. Z., Kapoor, T. M. Distinct mechanisms of resistance to a CENP-E inhibitor emerge in near-haploid and diploid cancer cells. Cell Chemical Biology. 27 (7), 850.e6-857.e6 (2020).
- Putkey, F. R., et al. Unstable kinetochore-microtubule capture and chromosomal instability following deletion of CENP-E. Developmental Cell. 3 (3), 351-365 (2002).
- Weaver, B. A., Silk, A. D., Montagna, C., Verdier-Pinard, P., Cleveland, D. W. Aneuploidy acts both oncogenically and as a tumor suppressor. Cancer Cell. 11 (1), 25-36 (2007).
- Silk, A. D., et al. Chromosome missegregation rate predicts whether aneuploidy will promote or suppress tumors. Proceedings of the National Academy of Sciences of the United States of America. 110 (44), E4134-E4141 (2013).
- Guo, Y., Kim, C., Ahmad, S., Zhang, J., Mao, Y. CENP-E-dependent BubR1 autophosphorylation enhances chromosome alignment and the mitotic checkpoint. Journal of Cell Biology. 198 (2), 205-217 (2012).
- Weaver, B. A., Cleveland, D. W. Aneuploidy: instigator and inhibitor of tumorigenesis. Cancer Research. 67 (21), 10103-10105 (2007).
- Nishimura, K., Fukagawa, T. An efficient method to generate conditional knockout cell lines for essential genes by combination of auxin-inducible degron tag and CRISPR/Cas9. Chromosome Research. 25 (3-4), 253-260 (2017).
- Owa, M., Dynlacht, B. A non-canonical function for Centromere-associated protein-E controls centrosome integrity and orientation of cell division. Communications Biology. 4 (1), 358 (2021).
- Barabási, A. L., Oltvai, Z. N. Network biology: understanding the cell's functional organization. Nature Reviews Genetics. 5 (2), 101-113 (2004).
- Rossi, A., et al. Genetic compensation induced by deleterious mutations but not gene knockdowns. Nature. 524 (7564), 230-233 (2015).
- Ma, Z., et al. PTC-bearing mRNA elicits a genetic compensation response via Upf3a and COMPASS components. Nature. 568 (7751), 259-263 (2019).
- El-Brolosy, M. A., et al. Genetic compensation triggered by mutant mRNA degradation. Nature. 568 (7751), 193-197 (2019).
- Kung, P. P., et al. Chemogenetic evaluation of the mitotic kinesin CENP-E reveals a critical role in triple-negative breast cancer. Molecular Cancer Therapeutics. 13 (8), 2104-2115 (2014).
- Kim, J. H., et al. Development of a novel HAC-based "gain of signal" quantitative assay for measuring chromosome instability (CIN) in cancer cells. Oncotarget. 7 (12), 14841-14856 (2016).
- Hirayama, T., et al. Synthetic studies of centromere-associated protein-E (CENP-E) inhibitors: 1. Exploration of fused bicyclic core scaffolds using electrostatic potential map. Bioorganic & Medicinal Chemistry. 21 (17), 5488-5502 (2013).
- Hirayama, T., et al. Synthetic studies on Centromere-associated protein-E (CENP-E) inhibitors: 2. Application of electrostatic potential map (EPM) and structure-based modeling to Imidazo[1,2-a]pyridine derivatives as anti-tumor agents. Journal of Medicinal Chemistry. 58 (20), 8036-8053 (2015).
- Ohashi, A., et al. A novel time-dependent CENP-E inhibitor with potent antitumor activity. PLoS One. 10 (12), e0144675 (2015).
- Ohashi, A., et al. Aneuploidy generates proteotoxic stress and DNA damage concurrently with p53-mediated post-mitotic apoptosis in SAC-impaired cells. Nature Communications. 6, 7668 (2015).
- Ding, X., et al. Probing CENP-E function in chromosome dynamics using small molecule inhibitor syntelin. Cell Research. 20 (12), 1386-1389 (2010).
- Liu, X., et al. Phase separation drives decision making in cell division. Journal of Biological Chemistry. 295 (39), 13419-13431 (2020).
- Henderson, M. C., et al. UA62784, a novel inhibitor of centromere protein E kinesin-like protein. Molecular Cancer Therapeutics. 8 (1), 36-44 (2009).
- Yamane, M., et al. Identification of benzo[d]pyrrolo[2,1-b]thiazole derivatives as CENP-E inhibitors. Biochemical and biophysical research communications. 519 (3), 505-511 (2019).
- Lock, R. B., et al. Initial testing of the CENP-E inhibitor GSK923295A by the pediatric preclinical testing program. Pediatric Blood & Cancer. 58 (6), 916-923 (2012).
- Chung, V., et al. First-time-in-human study of GSK923295, a novel antimitotic inhibitor of centromere-associated protein E (CENP-E), in patients with refractory cancer. Cancer Chemotherapy and Pharmacology. 69 (3), 733-741 (2012).
- Hsu, P. D., et al. DNA targeting specificity of RNA-guided Cas9 nucleases. Nature biotechnology. 31 (9), 827-832 (2013).
- Weaver, B. A., Cleveland, D. W. Decoding the links between mitosis, cancer, and chemotherapy: The mitotic checkpoint, adaptation, and cell death. Cancer Cell. 8 (1), 7-12 (2005).
- Manchado, E., Guillamot, M., Malumbres, M. Killing cells by targeting mitosis. Cell Death and Differentiation. 19 (3), 369-377 (2012).
- Dang, Y., et al. Optimizing sgRNA structure to improve CRISPR-Cas9 knockout efficiency. Genome Biology. 16, 280 (2015).
- Ratz, M., Testa, I., Hell, S. W., Jakobs, S. CRISPR/Cas9-mediated endogenous protein tagging for RESOLFT super-resolution microscopy of living human cells. Scientific Reports. 5, 9592 (2015).
- Koch, B., et al. Generation and validation of homozygous fluorescent knock-in cells using CRISPR-Cas9 genome editing. Nature Protocols. 13 (6), 1465-1487 (2018).
- Yan, Q., et al. Multiplex CRISPR/Cas9-based genome engineering enhanced by Drosha-mediated sgRNA-shRNA structure. Scientific Reports. 6, 38970 (2016).
- Cheng, Y., et al. CRISPR/Cas9-mediated chicken TBK1 gene knockout and its essential role in STING-mediated IFN-β induction in chicken cells. Frontiers in Immunology. 9, 3010 (2019).
- Zhou, Y., et al. High-throughput screening of a CRISPR/Cas9 library for functional genomics in human cells. Nature. 509 (7501), 487-491 (2014).
- Zeng, W., Guo, L., Xu, S., Chen, J., Zhou, J. High-throughput screening technology in industrial biotechnology. Trends in Biotechnology. 38 (8), 888-906 (2020).
- Tsai, S. Q., et al. GUIDE-seq enables genome-wide profiling of off-target cleavage by CRISPR-Cas nucleases. Nature Biotechnology. 33 (2), 187-197 (2015).
- Kim, D., et al. Genome-wide analysis reveals specificities of Cpf1 endonucleases in human cells. Nature Biotechnology. 34 (8), 863-868 (2016).
- Komor, A. C., Kim, Y. B., Packer, M. S., Zuris, J. A., Liu, D. R. Programmable editing of a target base in genomic DNA without double-stranded DNA cleavage. Nature. 533 (7603), 420-424 (2016).
- Nishimasu, H., et al. Engineered CRISPR-Cas9 nuclease with expanded targeting space. Science. 361 (6408), 1259-1262 (2018).
- Wang, H., et al. One-step generation of mice carrying mutations in multiple genes by CRISPR/Cas-mediated genome engineering. Cell. 153 (4), 910-918 (2013).
- Ablain, J., Durand, E. M., Yang, S., Zhou, Y., Zon, L. I. A CRISPR/Cas9 vector system for tissue-specific gene disruption in zebrafish. Developmental Cell. 32 (6), 756-764 (2015).
- Pickar-Oliver, A., Gersbach, C. A. The next generation of CRISPR-Cas technologies and applications. Nature Reviews Molecular Cell Biology. 20 (8), 490-507 (2019).
- Nalawansha, D. A., Gomes, I. D., Wambua, M. K., Pflum, M. K. H. HDAC inhibitor-induced mitotic arrest is mediated by Eg5/KIF11 acetylation. Cell Chemical Biology. 24 (4), 481.e5-492.e5 (2017).
- Kavalapure, R. S., et al. Design, synthesis, and molecular docking study of some 2-((7-chloroquinolin-4-yl) amino) benzohydrazide Schiff bases as potential Eg5 inhibitory agents. Bioorganic Chemistry. 116, 105381 (2021).
- Calligaris, D., Lafitte, D. Chemical inhibitors: the challenge of finding the right target. Chemistry & Biology. 18 (5), 555-557 (2011).
- Łomzik, M., et al. Metal-dependent cytotoxic and kinesin spindle protein inhibitory activity of Ru, Os, Rh, and Ir half-sandwich complexes of Ispinesib-derived ligands. Inorganic Chemistry. 59 (20), 14879-14890 (2020).
- Ferro, L. S., et al. Structural and functional insight into regulation of kinesin-1 by microtubule-associated protein MAP7. Science (New York, N.Y.). 375 (6578), 326-331 (2022).
- Atherton, J., et al. The mechanism of kinesin inhibition by kinesin-binding protein. eLife. 9, e61481 (2020).
転載および許可
このJoVE論文のテキスト又は図を再利用するための許可を申請します
許可を申請さらに記事を探す
This article has been published
Video Coming Soon
Copyright © 2023 MyJoVE Corporation. All rights reserved