Method Article
衣藻中心粒单粒子重建的分离与荧光成像
摘要
我们已经制定了一个战略, 以净化和图像大量的中心粒在不同的方向, 适合超分辨率显微镜和单粒子平均。
摘要
中心粒是大型大分子组件重要的基本细胞生物学过程的正确执行, 如细胞分裂, 细胞运动, 或细胞信号。绿色藻类衣藻衣藻已被证明是研究中心粒建筑, 功能和蛋白质组成的一个有洞察力的模型。尽管在了解 centriolar 体系结构方面取得了巨大进展, 但目前面临的挑战之一是确定中心粒结构区域内 centriolar 组件的精确定位, 以便更好地了解它们在中心粒合成。一个主要的局限性在于荧光显微术的分辨率, 它使该细胞器中蛋白质定位的解释复杂化, 其尺寸接近衍射极限。为了解决这个问题, 我们提供了一种用超分辨率显微镜对大量的衣藻中心粒进行纯化和成像的方法。该技术允许通过荧光单粒子平均 (荧光 SPA) 对数据进行进一步处理, 因为获得的中心粒数量很大。荧光温泉在不同的方向上产生染色的衣藻中心粒的平均值, 从而促进了 centriolar 亚区域不同蛋白质的定位。重要的是, 这种方法可以应用于其他物种或其他大型大分子组件的图像中心粒。
引言
中心粒是一个进化保守的细胞器, 位于中心体的核心, 并可以作为一个基本的身体 (称为中心粒以后) 模板纤毛或鞭毛在许多真核生物1,2。因此, 中心粒对从主轴组件到细胞信号等基本细胞生物学过程至关重要。因此, 中心粒装配或功能上的缺陷与一些人类病理, 包括 ciliopathies 和癌症3有关。
中心粒是九倍, 对称, 微管三重基圆柱结构, 通常, 约 450 nm 长和 ~ 250 nm 宽4,5,6,7。从不同种类的中心粒的常规电子显微镜和低温电子层析显示, 中心粒是沿其长轴极化与三个不同区域: 近区, 中心核心, 和远端区域5,7,8,9,10,11. 重要的是, 每个区域都显示出具体的结构特征。首先, 100 纳米长的近端区域的流明包含了通过针头元素12连接到微管三重的车轮结构。第二, 300–400纳米长中部地区包含管腔内的纤维密度和微管内表面的结构特征: Y 形链接器、C 小管尾和 A 管存根9。最后, 50–100 nm 远端区域展出的远端和远端附属物, 环绕的远端部分的中心粒5,13。
在过去的两年中, 发现了越来越多的 centriolar 蛋白, 导致目前估计约100种不同的蛋白质是中心粒14,15,16的一部分,17. 尽管取得了这些进展, 这些蛋白质在中心粒中的精确定位仍然是难以捉摸的, 特别是在结构的分区域内。重要的是, 为中心粒的结构区域指定精确的定位, 对于更好地理解它们的功能至关重要。在这方面, C. 衣藻中心粒在这两方面都发挥了作用, 首先 delimitating 了圆柱9、18、19的不同结构特征, 然后允许研究人员将荧光显微术对蛋白质子集的定位与亚结构区域相关。这包括, 例如, 蛋白质 Bld12p 和 Bld10p, 在近端区域本地化, 并在车轮结构, 特别是20,21,22,23。子结构局部化蛋白的列表还包括 POB15 和 POC16, 两种新的蛋白质由质谱鉴定, 以修饰衣藻中心粒17的内中心核心区域。
本文对衣藻中心粒的分离和成像方法进行了完整的描述, 并给出了超分辨率显微镜和单粒子平均法。为了实现这一目标, 必须界定需要克服的技术限制。首先, 中心粒净化可以影响整体结构, 车轮结构往往在隔离9的各个步骤中丢失。其次, 中心粒的尺寸与光学显微镜的衍射极限非常接近。事实上, 可在共焦显微镜中获得的横向分辨率约为200毫微米24, 类似于中心粒的直径, z轴的分辨率约为2–3x 低, 导致各向异性体积。第三, 抗体标记的异质性和中心粒定向可能会限制特定 centriolar 子区域内蛋白质定位所需的解释。最后, 中心粒只存在于每个单元格的两个副本中, 因此很难获得大量的图像并找到一个明确的中心粒方向。为了规避这些技术问题, 我们开发了一种方法, 它依靠应用超分辨率显微镜对大量的孤立中心粒采取各种方向。我们将首先描述一个净化C. 衣藻中心粒的协议, 它能够净化含有车轮的结构完整的中心粒和 procentrioles。然后, 我们将描述一步一步的协议, 集中的中心粒在盖玻片成像的常规或超分辨率荧光显微镜。这一重要步骤允许在多个方向上增加中心粒映像的数量。最后, 我们将描述一个程序, 以执行单粒子平均的数据获得的荧光显微镜, 有利于检测中心粒在不同的方向。该方法可应用于不同种类或其他大型大分子组件的图像中心粒。
研究方案
1.衣藻文化和中心粒隔离的媒体准备
-
培养基衣藻细胞的制备
注: 以下步骤描述了为1x 自来水 (三乙酸磷酸酯) 培养基制备库存溶液的方法。- 准备一个磷酸盐缓冲 (pH 值 7), 通过混合250毫升1米 k2HPO4 (174.2 克 2 HPO4补充到 1 L 与蒸馏水) 与 ~ 170 毫升 1 M 的的米的的, 2 po 4 (136.09 g的 2 po4在 1 L)。调整混合物达到 pH 值7。
- 通过混合96.8 克三, 40 毫升磷酸缓冲液 (pH 7) 和40毫升醋酸, 将溶液 A (40x), 用蒸馏水调整溶液为1升。
- 用16克 NH4氯, 2 克 CaCl2, 4 克 MgSO4制备溶液 B (40x)。在将 CaCl2在蒸馏水中加入其他组分之前, 要小心地将其溶解。用蒸馏水将溶液调整为1升。
- 准备 Hutner 的跟踪元素缓冲区25 , 如下所示。
- 对于 1 L 的缓冲, 溶解每个化合物在指定的水量: EDTA 二钠盐 (50 克在250毫升), ZnSO4. 7H2O (22 克在100毫升), H3BO3 (11.4 毫升在 200 ml), MnCl2. 4H2O (5.06 ml 50 毫升), CoCl26H2O (1.61 克50毫升), 丘索4. 5H2o (1.57 g 在50毫升), (NH4) 6Mo7o24. 4H2o (1.10 g 在50毫升) 和 FeSO4o (2 g 在4.99 毫升)。
注: EDTA 应在沸水中溶解, FeSO4应在最后准备, 以避免氧化。 - 混合所有的解决方案, 除了 EDTA 一起, 并带来沸腾。然后加入 EDTA, 溶液应该变绿。溶解一切后, 冷却溶液到70摄氏度。在这个温度下, 加入85毫升的热 20% KOH 溶液 (20 克在100毫升)。室温 (RT) 用蒸馏水将溶液调整为1升。
- 添加一个棉花插头的烧瓶, 让解决方案站立1或2周, 摇晃它一天1x。溶液最初应该是绿色的, 然后变成紫色, 留下锈褐色沉淀;使用过滤纸除去沉淀, 直到溶液清晰为止。冷冻整除数, 贮存在摄氏-20 摄氏度。
- 对于 1 L 的缓冲, 溶解每个化合物在指定的水量: EDTA 二钠盐 (50 克在250毫升), ZnSO4. 7H2O (22 克在100毫升), H3BO3 (11.4 毫升在 200 ml), MnCl2. 4H2O (5.06 ml 50 毫升), CoCl26H2O (1.61 克50毫升), 丘索4. 5H2o (1.57 g 在50毫升), (NH4) 6Mo7o24. 4H2o (1.10 g 在50毫升) 和 FeSO4o (2 g 在4.99 毫升)。
- 通过混合以下组件, 准备1x 分路培养基以生长衣藻细胞:25 毫升溶液 a (40x) 和25毫升溶液 B (40x), 1 毫升的 Hutner 的微量元素缓冲25, 并用蒸馏水调整混合物为1升。使用0.4 µm 过滤器消毒混合物。
-
中心粒净化介质的制备
- 用5% 蔗糖在10毫米 HEPES (pH 7) 上准备一个 deflagellation 缓冲液, 在最后的体积上用蒸馏水调整500毫升。
- 准备250毫升的0.5 米乙酸。
- 先加入50毫升的 H2O 以溶解管状粉末, 然后加入 10 N KOH, 直到溶液开始变得清晰为止, 准备250毫升的1米 K 管的库存溶液 (pH 7.2)。滴定到 pH 值7.2 与 10 n 和 1 n KOH 并且调整解答到最后容量 250 mL 与 H2O。
- 准备5蔗糖溶液 (w/w) 如下。
注: 所有蔗糖溶液都需要过滤后, 使用0.4 µm 过滤器插入注射器。请注意, 60% 和70% 蔗糖溶液是很难溶解, 应该放在水浴预热60摄氏度, 以促进增溶。混合每10分钟, 直到蔗糖完全溶解。- 要准备25% 蔗糖, 重25克蔗糖和调整重量为100克通过增加10毫米 K 管子 (pH 7.2)。
- 要准备60% 蔗糖, 重60克蔗糖并且调整重量到 100 g 与10毫米 K 管子 (pH 7.2)。
- 为蔗糖梯度准备蔗糖溶液。通过称量40克蔗糖, 用10毫米 K 管 (pH 7.2) 将溶液调整为100克, 制备40% 蔗糖。同样, 准备 50% (w/w) 和 70% (w/w) 蔗糖。
- 将解决方案存储在摄氏-20 摄氏度。在解冻后要小心并用重悬蔗糖溶液。
- 通过混合1毫米 HEPES (pH 7), 0.5 毫米氯化镁2, 和 1% NP-40, 准备100毫升的裂解缓冲液, 并保持在4摄氏度。在实验当天总是准备好这个缓冲区。在中心粒隔离日添加抗蛋白酶片。
- 通过混合8克氯化钠制备1x 磷酸盐缓冲盐水 (PBS) (pH 值 7.4), 2 克氯化钾, 1.44 克的 Na2HPO4, 0.24 克的, 在2毫升的蒸馏 4 mL 800 o. 用HCl 调整 pH 值为 2. 把混合物的体积调到 7.4我用蒸馏的 H2O。
2.衣藻中心粒的分离
注: 见图 1。
-
衣藻细胞的培养与扩增
- 在晚上1天, 接种一个cw15菌株从一个坚实的板块到一个文化锥形瓶包含10毫升1x 水龙头。生长在白色荧光灯下的细胞 (60 µE/米2s) 为2–3天在23摄氏度。
- 在3天, 稀释文化 10x (到100毫升) 在1x 轻拍并且生长细胞在光之下为2–3天在23°c。
- 在6天, 稀释文化10x 在1x 轻拍获取 1 L 文化。将细胞在光下生长23摄氏度, 直到文化达到深绿色, 表明大约细胞密度为 ~ 1 x 107细胞/mL26 (天 9–10)。
-
衣藻中心粒的纯化
- 离心cw15细胞在 600 x g 10 分钟50毫升圆锥管。用50毫升 1x PBS 清洗细胞的颗粒 1x, 并将其旋转 600 x g , 以10分钟的并用重悬在室温 deflagellation 缓冲器的100毫升内用吸管。
- Deflagellate 的细胞与 pH 值休克通过缓慢添加0.5 米醋酸下降到最终4.5–4.7 的 pH 值的磁性搅拌器和孵化细胞2分钟. 缓慢添加 1 N KOH 的下降, 以恢复 pH 值为7.0。
- 离心细胞在 600 x g 10 分钟, 以去除任何分离鞭毛。取出上清液并将小球储存在冰上。用50毫升 1x PBS 预换热器在4摄氏度清洗颗粒2x。然后, 旋转颗粒在 600 x g 10 分钟在4摄氏度。
- 并用重悬30毫升 1x PBS 中的颗粒, 慢慢地将悬浮液载到20毫升的 25%-蔗糖垫子上, 不混合 (图 1B)。
- 旋转在 600 x g 15 分钟在4°c 去除剩余的鞭毛在上清;细胞分布在25% 蔗糖 (图 1C)。只保留底部-最20毫升 (红色箭头,图 1C), 通过小心地吸上清液使用吸。
- 通过添加20毫升的冷 1x PBS, 清洗剩余的20毫升。旋转样品在 600 x g 10 分钟在4°c。并用重悬10毫升冷 1x PBS (4 摄氏度) 的颗粒。确保没有团簇, 使以下溶解一次击中所有的细胞。
- 将悬浮颗粒转移到一个新的250毫升瓶。添加100毫升的裂解缓冲液, 辅以5000单位的 DNase 细胞。将裂解缓冲液添加到细胞中是很重要的, 而不是用另一种方法来解决。在4摄氏度孵育混合物1小时, 并仔细混合, 每15分钟反转瓶子, 而不形成任何气泡。
- 将裂解细胞离心在 600 x g 10 分钟, 在50毫升圆锥管中4摄氏度, 以去除任何细胞碎片。如果溶解已经正确地执行, 细胞颗粒应该是白色的 (图 1D)。用吸管收集上清液并将其装入30毫升的圆底管, 其中含有 60%-蔗糖垫, 放在冰上。然后, 旋转管在 1万 x g 30 分钟在4摄氏度。
注: 可能需要几个圆底管 (材料表), 这取决于上清液的体积。 - 将上清液吸入1毫升以上的蔗糖垫。注意1毫升的剩余上清和2毫升的蔗糖垫之间的黄色界面。用切 P1000 尖轻轻地将蔗糖和剩余的上清液混合。不要在这一步旋涡;否则, procentrioles 可以在这个阶段丢失。把所有的蔗糖垫子放在冰上储存起来。
- 在薄壁38.5 毫升聚丙烯管中, 通过轻轻添加3毫升70% 蔗糖 (在4°c), 再加3毫升 50%, 最后, 3 毫升的蔗糖来制备 40%-70%-蔗糖梯度。将池内的接口加载到40% 到 70%-蔗糖梯度上;慢慢地做, 因为冷的蔗糖是非常粘性的。平衡管与10毫米 K 管缓冲 (pH 7.2) 和离心他们在 68320 x g (例如, 与 SW32Ti 转子) 1 小时和15分钟在4°c。
- 收集 12x 500 µL 分数在4°c 通过使一个孔在底部的管与0.8 毫米针, 而不扰乱不同的蔗糖层。用切 P200 吸管尖, 准备额外的10µL 整除数从每个分数, 将用于以下免疫荧光。将液态氮中的分数冻结。
注意: 通过电子显微镜可以分析分离中心粒, 以确保中心粒的整体超微结构得到保留。
3. 盖玻片中孤立中心粒的量化: 离心和免疫荧光
注: 见图 2。
-
准备管子和盖玻片
- 使用1玻璃圆底管 (15 毫升) 每分数分析 centriolar 分数 (总共12管)。
- 将自定义盖玻片支持适配器 (以后称为适配器) 插入到圆底管中。将不育的12毫米盖玻片放入圆底管内。
注: 在这里我们使用了12毫米盖玻片, 但该协议可以适应18毫米盖玻片使用30毫升的圆底管。 - 添加5毫升预冷10毫米 K 管 (pH 7.2) 在4摄氏度。请确保盖玻片没有浮动, 并停留在适配器上。把管子放在冰上。
-
离心中心粒
- 稀释每10µL 分数与100µL 冷10毫米 K 管 (pH 7.2)。并用重悬稀释好, 直到蔗糖的完全消失 (图 2A)。将每个稀释的分数装入一个圆底管。
- 旋转管在 1万 x g 10 分钟 (例如, 与 JS-13.1 摆动斗转子) 在4°c。
- 通过将手工挂钩设备插入适配器的开槽边缘中的孔中, 并轻轻提起, 以恢复盖玻片。
注: 该手工钩装置可以用注射器针手动钩和模压到自制的棍子 (图 2 b-2 d)。 - 到达圆底管顶部时, 用戴手套的手指将适配器的边缘盖玻片, 用镊子将其取下。小心记住盖玻片的哪一边包含中心粒。继续治疗盖玻片免疫荧光。
-
孤立性衣藻中心粒的免疫荧光染色及影像学研究
注: 见图 2。- 准备免疫荧光染色材料如下。
- 在水晶聚苯乙烯传输实验室盒中准备一个盖玻璃染色架 (长度为60毫米, 宽度为50毫米, 高度为43毫米)。用100% 甲醇填充, 并将其存储在-20 摄氏度。
- 准备一个潮湿的房间。为此, 通过放置一个水湿润的组织在正方形培养皿的内侧边缘 (图 2E), 组装潮湿的房间。在免疫荧光过程中, 添加一个实验室密封包装 (见材料表) 到培养皿的中间, 抗体混合将放置在该方法 (步骤 3.3. 2–3.3 3)。用铝箔盖住盖子和潮湿的房间以保护它不受光线的侵害。
- Immunostain 隔离的中心粒如下所示。
- 在离心 (步骤 3.2.4) 后直接用中心粒固定盖玻片, 在装满-20 °c 甲醇 (步骤 3.3.1.1) 的盒子中孵化5分钟。
- 用镊子取出盖玻片, 并将其放在透明的实验室箱内 (见材料表), 填充50毫升 1x PBS, 在室温下清洗5分钟。
- 吸管60µL 的原抗体混合 [主要抗体稀释1% 牛血清白蛋白 (BSA) 和 0.05% Tween-20 在 PBS] 在实验室密封包装在潮湿的房间。小心地将盖玻片放在抗体组合的顶端, 中心粒直接面对下落。用主要抗体孵化盖玻片45分钟。
注: 用于生成代表性结果的主要抗体为兔多克隆 Bld12 (1:300) 和小鼠α蛋白 (DM1A) (1:300)。 - 卸下盖玻片并在 1x PBS 中清洗5分钟, 如步骤3.3.2.2 中所述。在 PBS 中孵化45分钟的盖玻片, 其中含有 1% BSA 和 0.05% Tween-20 的二级抗体。
注: 用于生成代表性结果的二次抗体是山羊抗鼠结合到 alexa 488 (1:1, 000) 和山羊抗兔结合到 alexa 568 (1:1, 000)。 - 卸下盖玻片并在 1x PBS 中清洗5分钟, 如步骤3.3.2.2 中所述。
- 通过在幻灯片上添加3µL 安装介质, 并小心地将盖玻片放在顶部 (中心粒面对安装介质), 将盖玻片安装在玻璃滑梯上。用指甲油封住盖玻片的边缘。
- 在63X 油目标的共聚焦显微镜上, 用1.4 的反褶积27 (见材料表) 将隔离中心粒成像。
注: 在这里, 使用了以下设置: 500–545 nm 为 alexa 488 和 580–635 nm 568。
- 准备免疫荧光染色材料如下。
4. 中心粒集中到盖玻片中心
注: 见图 3。
-
材料制备
- 在冰上准备一个15毫升玻璃圆底管, 一个定制的盖玻片支持适配器 (称为适配器以后,. stl 文件作为补充文件 1), 一个自定义集中器 (. stl 文件提供补充文件 2) 和10毫米 K 管 (pH 值7.2) 在4摄氏度。
- 制备聚 d-赖氨酸 (PDL) 涂层盖玻片。稀释 10x 1 毫克/毫升的 PDL 股票溶液与 H2O。首先, 用70% 乙醇洗盖玻片, 取出乙醇, 让盖玻片干。用 PDL 盖玻片, 在室温下孵化30分钟。用清水冲洗盖玻片 3x, 让它们晾干。
注: 将盖玻片与 PDL 一起涂上, 以增加连接到盖玻片的隔离中心粒的数量。
-
离心
- 将无菌的12毫米盖玻片放到选矿厂的凹槽底端, 使 PDL 外套朝下。将适配器直接放在顶部, 将盖玻片盖上。反转圆底管并将其放在选矿厂、盖玻片和适配器上。
- 用镊子轻轻推, 直到它到达底部的圆底管, 并反转管。将10毫米的 K 管缓冲器 (pH 7.2) 添加到圆底管, 直到它来到选矿厂的顶端。确保选矿厂中央气缸内不存在气泡。
- 轻轻地添加100µL 10 毫米 K 管缓冲 (pH 7.2) 到一个整除含有丰富的中心粒分数, 并彻底混合的体积。
- 从选矿厂空心中心移除100µL 10 毫米 k 管缓冲器 (ph 7.2), 并在10毫米 K 管缓冲器 (ph 7.2) 中加入100µL 的富集 centriolar 馏分, 并注意其内容留在空心中心。
- 离心机在 1万 x g为10分钟 (例如, 与一个 JS-13.1 摆动的铲斗转子) 在一个预冷离心机在4°c。
- 用镊子拆卸选矿厂。
- 通过将手工挂钩设备插入适配器的开槽边缘中的孔中, 并轻轻提起, 以恢复盖玻片。到达圆底管顶部时, 用戴手套的手指将适配器的边缘盖玻片, 用镊子将其取下。小心记住盖玻片的哪一边包含中心粒。继续治疗盖玻片免疫荧光。
注: 手工钩接装置可以用注射器针手工钩住并模压到自制棒上 (图 2B D)。 - 对浓缩中心粒进行固定和免疫荧光染色, 步骤 3.3. 2–3.3 4。
5. 单粒子平均
注: 见图 4。
- 单粒子平均成像
- 使用常规防褪色安装介质在幻灯片上安装盖玻片。使用 CFI 复消色差 TIRF 目标 (100X, NA 1.49, WD 0.12mm) 和背面照明的 EM CCD 相机执行结构化光照显微镜 (2D SIM) 成像。
注: 采集时间设置为100毫秒, 相机读取 3 MHz。2.5X 透镜用于 SIM 成像。
注: 此处提供的数据集是在3维 SIM 显微镜 (见材料表) 上获得的。 - 图像中心粒通过获取包含总中心粒信号的一大堆图像, 分别在中心粒信号的上方和下方设置 Z 堆栈的顶部和底部位置。继续按步骤5.2 和5.3 进行项目堆栈并执行单粒子平均。
- 使用常规防褪色安装介质在幻灯片上安装盖玻片。使用 CFI 复消色差 TIRF 目标 (100X, NA 1.49, WD 0.12mm) 和背面照明的 EM CCD 相机执行结构化光照显微镜 (2D SIM) 成像。
- 堆栈的投影
- 用 ImageJ 打开图像堆栈。然后点击 "图像→栈→ Z 项目"。将投影类型设置为 "最大强度"。
- 通过点击 "编辑→反转"来反转图像。保存生成的投影 (. tif 格式)。
- 单粒子对准与 Scipion
- 通过按页面顶部的红色 "创建项目"按钮, 在 Scipion 中创建一个新项目。在左面板上, 双击 "导入" → "导入显微照片"。
- 根据数据目录和名称填充 "文件目录"和 "模式"字段。保留默认参数。单击 "执行"。
- 双击"粒子→采摘→ xmipp3-手工采摘 (步骤 1)"。单击靠近"输入显微图像"字段的放大镜图标, 然后从步骤5.3.1 中选择导入的显微照片。单击 "执行"。
- 在新打开的窗口中, 从不同的显微照片中选择粒子, 点击它们。完成每一个显微图像, 点击红色按钮' + 坐标 '。
- 双击"粒子→萃取→ xmipp3-萃取粒子"。单击靠近"输入坐标"字段的放大镜图标, 然后从步骤5.3.4 中选择选取的坐标。根据颗粒尺寸填充"粒子盒尺寸 (px)" 。在"预处理"选项卡上, 设置除尘: No (它可以生成工件);反转对比: No (黑色颗粒, 白色背景);相位翻转: No (与 "与"。正常化: 是。
- 然后, 单击 "执行"。完成作业后, 通过选择作业框 (边框变厚) 检查提取的粒子, 然后单击 "分析结果" (主菜单左下角)。
- 双击"2D →对齐→ xmipp3-与 cl2d 对齐"。点击放大玻璃图标接近' 输入粒子 '的领域, 并选择从步骤5.3.5 提取的粒子。不要使用引用图像。单击 "执行"。
- 双击"2D →对齐→更多→ xmipp3-应用对齐 2d"。单击靠近"输入粒子"字段的放大镜图标, 然后从步骤5.3.7 中选择对齐的粒子。
- 在步骤5.3.6 中单击 "执行" 。通过在选择作业框后单击"分析结果"可以检查结果。
- 双击"粒子→掩码→ xmipp3-应用2d 掩码"。
- 单击靠近"输入粒子"字段的放大镜图标, 然后从步骤5.3.9 中选择对齐的粒子。"掩码源"设置为"几何图形"。然后, 将掩码的参数设置为掩码类型: 圆形;半径 (px): 寻找一个粒子 (中心粒) 没有任何周围的东西, 点击左侧的 "魔术棒"图标打开一个窗口, 以帮助找到完美的价值;移位中心: No (如果粒子是完全居中的) 或 Yes (如果粒子被转移);X 中心偏移: 根据粒子位置;Y 中心偏移量: 根据粒子位置。单击 "执行"。
- 使用"分析结果"按钮检查掩码是否正确应用。如果没有, 右键单击"应用掩码 2d"作业, 然后选择"编辑"。修改掩码的参数 (大小和/或移位), 并使用"执行"按钮再次运行它。
- 双击"2D →分类→ xmipp3-cl2d"。
- 单击靠近"输入粒子"字段的放大镜图标, 然后从步骤5.3.11 中选择遮罩粒子。类的数量应该是获得大约50微粒每类。单击 "执行"。
- 点击"分析结果"按钮检查结果。在打开的窗口中, 单击 "要显示的内容" 旁边的 "眼睛"图标。
- 通过在"块"菜单中选择"Classes2D" , 新窗口允许对生成的类进行检查。通过在同一菜单中选择"Class00N_Particles"来检查每个类的内容。检查每个类以确定哪些只包含坏粒子。返回到"Classes2D"视图, 然后通过单击每个来选择具有良好粒子的类。通过在选定内容中按下"Ctrl"键, 可以选择多个类。
- 当所有具有良好粒子的类都被选中后, 单击"+ 粒子"以创建与这些粒子的子集。
- 在同一窗口中, 选择几组表示粒子不同方向的类。通过单击"+ 平均值"创建一个新子集。
- 对于选定的每个方向/平均值, 请按如下所示进行。
- 双击"2D →对齐→ xmipp3-与 cl2d 对齐"。
- 点击放大玻璃图标接近' 输入粒子 '的领域, 并选择良好的粒子从步骤5.3.17。将"使用引用图像"设置为"是"。单击靠近"参考图像"字段的放大镜图标, 然后单击 "从步骤 5.3.18创建子集"作业左侧的白色箭头, 然后选择要用作参考的图像。双击对象以在单独的窗口中打开它, 并检查它是哪个对象。单击 "执行"。
- 双击"2D →对齐→更多→ xmipp3-应用对齐 2d"。单击靠近"输入粒子"字段的放大镜图标, 然后从步骤5.3.19.2 中选择对齐的粒子。
- 单击 "执行"。
- 检查对齐结果 ("分析结果");它将显示排列的粒子和这些粒子的平均值。
- 如果平均是好的和粒子都是以同样的方式, 通过点击"高级→ ImageJ"保存的平均值, 并保存图像与 ImageJ。
- 如果可以提高平均值, 请选择所有面向良好的图像, 并使用"+ 粒子"按钮创建一个新子集。重申步骤 5.3. 19.1–5.3. 19.4 直到子集被清洗 (所有坏微粒被去除)。每次执行对齐 (步骤 5.3.19.2) 时, 引用都设置为最后生成的平均值 (从迭代到迭代, 平均质量增加)。
结果
C. 衣藻中心粒隔离:
为了隔离中心粒, cw15衣藻细胞在液体培养中生长了数天, 在光照下, 随后以 600 x g的离心颗粒为10分钟. 颗粒细胞被洗涤1x 与 PBS 和悬浮在一个deflagellation 缓冲在 deflagellation 之前通过执行 ph 值冲击使用 0.5 M 乙酸到最后 pH 值的4.5–4.7 为2分钟 (图 1a)。添加 1 N KOH 用于恢复 pH 值为7.0。为了分离分离的鞭毛从细胞体, deflagellated 细胞首先离心去除大部分鞭毛。然后在30毫升的 pbs 中用 pbs 和悬浮洗净颗粒, 然后在 25%-蔗糖的垫子上慢慢地加载它 (图 1B)。该管被纺在 600 x g 15 分钟4摄氏度, 以消除大多数分离鞭毛。离心后, 细胞体被分散在蔗糖垫层 (图 1c), 并通过除去大约30毫升的上清 (直到图 1c中的红色箭头) 来恢复。由此产生的20毫升洗涤细胞, 然后悬浮20毫升的冷 PBS 和离心 600 x g 10 分钟。接着, 上清液被丢弃, 细胞在10毫升的 PBS 中完全悬浮。细胞被转移到一个250毫升瓶和溶解缓冲被添加到悬浮细胞一次。DNase 添加到裂解和孵化1小时, 在4摄氏度。在离心步骤去除细胞碎片 (参见图 1D中的白色颗粒) 后, 将上清液收集并仔细地装到2毫升 60%-蔗糖缓冲垫上, 然后在 1万 x g处离心, 30 摄氏度。请注意, 对于100毫升的裂解, 8 管15毫升用于执行这一步骤, 对应于12.5 毫升的裂解缓冲负载在2毫升蔗糖每管。离心后, 大部分上清液被除去在垫子上方1毫升。1毫升剩余的上清, 然后收集2毫升垫, 然后混合和汇集, 以获得最终的体积24毫升。水池然后被装载了 40%-, 50%, 70%-蔗糖梯度和纺在 68320 x g为 1 h 和15分钟在4°c。最后, 通过用针在离心管的底部做一个孔, 并在 12 x 500 µL 馏分中收集了中心粒, 收集了隔离的分离器。由于不同的蔗糖的高密度, 下落非常慢慢地形成了在开始 (70% 蔗糖) 和然后更加迅速地 (40% 蔗糖)。
孤立中心粒的免疫荧光研究
为了评估隔离过程的质量, 在使用盖玻片支持适配器 (图 2A-2D) 的情况下, 将每个收集到的渐变分数的10µL 离心到盖玻片上。重要的是, 为了安全地删除盖玻片, 设计了一个自定义挂钩设备 (图 2B)。其次, 对盖玻片进行免疫荧光分析。本研究采用抗 CrSAS 6 (Bld12p) 抗体, 表明车轮结构和α蛋白 (DMA1) 的存在, 突出 centriolar 壁。通过计算每个中心粒的 CrSAS-6 和α蛋白的阳性数, 然后计算每个分数中心粒的总数, 可以确定哪些分数被浓缩为孤立中心粒 ( 图 2F-2H)。有趣的是, 6 个分数被丰富的中心粒 (图 2F和2G, 分数 #1 –6), 一个峰值的分数 #3, 而最后的分数没有, 表明纯化工作。请注意, 在这个特定的实验中, 95% 的总中心粒是阳性的 CrSAS-6 和α蛋白在分数 #3。这表明大多数孤立的中心粒保留了它们的车轮。如果在第一个分数中未观察到中心粒的富集, 则隔离过程不起作用, 应该重复。请注意, 一些鞭毛的部分可以观察到, 主要是在没有中心粒的分数。
接下来, 要计算每个µL 的中心粒总数, 每个视场的中心粒数应乘以图 2H所示的比例。由此产生的数字应除以用于免疫荧光的分数的体积, 以获得每µL 中心粒的数量。在这个特殊的隔离过程中, 最丰富的分数包含约37中心粒的面积为0.00846 毫米2 (与视野的 92 x 92 µm2)。管截面的表面为7.5 毫米半径, 总表面为176毫米2。相应的比例是然后 176/0.00846 = 20803.8, 所以总共769740中心粒 (37x20,803.8) 在10µL。因此, 中心粒在1µL 的数量是76974。
盖玻片中孤立中心粒的浓度:
增加中心粒的数量增加了检测明确的中心粒方向的机会, 并增加了检测类似的方向, 可用于进一步的粒子平均程序的机会。由于中心粒从集中的组分仍然是稀疏的在盖玻片, 我们开发了离心配件集中中心粒在盖玻片中间 (图 3a) 命名选矿厂。请注意, 具有3维打印精度的. stl 文件与本手稿一起提供。
首先, 在选矿厂安装了一个 12 mm 的盖玻片 (图 3B)。该适配器被放置在盖玻片的顶部, 圆底管倒置, 并放置在组装的适配器和选矿厂。圆底管然后轻轻地倒置, 从而允许加载的样本 (协议步骤 4.2)。中心粒然后离心在 1万 x g 10 分钟在4°c。之后, 中心粒被免疫荧光和染色 CrSAS-6/Bld12p 和α蛋白 (图 3C-3E)。重要的是, 没有选矿厂, 每个视野 (图 3C) 看到大约30中心粒, 而在使用选矿机时, 每个视场上都看到183中心粒 (图 3D-3F)。注意, 中心粒在盖玻片的中间只覆盖了直径4毫米的圆盘。这一结果表明, 浓度步骤的工作和允许6倍丰富的中心粒在定义的区域盖玻片, 从而减轻他们的检测和成像。
孤立的荧光单粒子平均C. 衣藻中心粒:
在这里, 使用可以达到约 120 nm 分辨率的 SIM 显微镜, 中心粒染色的 monoglutamylated 蛋白 (GT335,图 4), 蛋白修饰目前在 centriolar 微管, 被成像24。衣藻中心粒约 500 nm 长, 总是成对, 经常发现与相关的, 新复制的 probasal 体 (称为 procentrioles 以后) 和横纹肌微管相关纤维19。因此, 这个最后的大会是大约1µm 大。出于这个原因, 为了完整地描述中心粒, 我们建议在孤立的中心粒上获取一个 Z 堆栈。
在这里, 收购后, 通过执行最大强度投影使用 ImageJ28 (图像/栈/Z 项目/最大强度投影,图 4B) 生成最终图像。从这些图像中, 采用低温电子显微软件对中心粒类进行了单粒子分析, 进行了相似方向的分类, 然后进行了平均化。为此, 首先反转图像颜色, 以便更好地可视化对象 (图 4C)。中心粒是在每个粒子的一个盒子里手工挑选的, 使用自由可用的 Scipion 软件29集成了几个电子显微软件程序, 如 Xmipp3 (图 4D)。请注意, 该框的大小必须由用户定义。在这里, 使用了一个像素大小为 31.84 nm 的 50 x 50 像素的盒子。接下来, 所有粒子都被提取 (图 4E) 并使用 Xmipp3 对齐 (图 4F)。接下来, 应用半径为12个像素的圆形掩码将每个中心粒从 centriolar 对 (图 4G) 中分离出来。然后, 使用 Xmipp3 对粒子进行分类, 生成几个平均值。只保留了同质类平均值, 这意味着从类平均值偏离的粒子被手动排除。这一步是重复的, 以便为每个选定的方向产生近乎完美的平均值。在五次迭代之后, 生成了两类平均值: 从63个对象 (图 4H) 的顶部视图和从98个粒子 (图 4I) monoglutamylated 中心粒的侧面视图。通过测量沿 monoglutamylation 信号的强度图剖面峰之间的距离, 确定了目标的尺寸。
重要的是, 侧面视图类平均值的长度为260毫微米, 直径为 250 nm, 可与被测到的 monoglutamylated 蛋白信号相比较, 显示为在中心粒17的核心范围内定位到286英寸 33 nm 的区域。
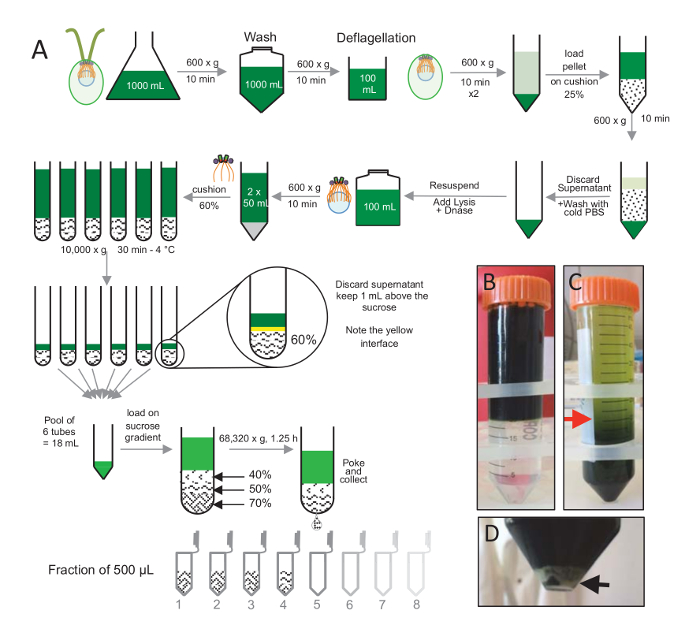
图 1: 纯化的C. 衣藻中心粒.(a) 这是导致隔离C. 衣藻中心粒的每一步的示意图表示。它包括了在 25%-蔗糖梯度离心后 (B) 之前和 (C) 议定书的代表性步骤。C面板中的红色箭头表示离心后保持的最小体积。(D) 本小组在离心后显示裂解细胞的白色颗粒。黑色箭头指示颗粒。请单击此处查看此图的较大版本.
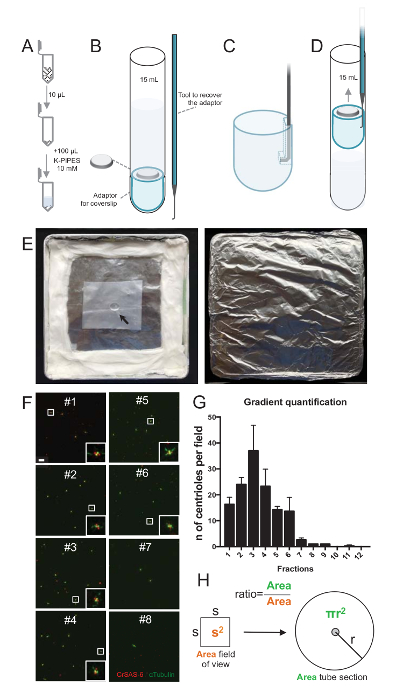
图 2: 离心设置, 对孤立的中心粒进行免疫荧光.(A) 每个收集到的分数的10µL 在100µL 10mM K 管中首先被稀释 (pH 7.2)。(B) 这是离心装置的示意图, 包括15毫升的圆底管、12毫米盖玻片、盖玻片的适配器, 以及一种自定义的钩式装置, 用于在离心后恢复盖玻片。面板C和D显示图纸解释如何恢复盖玻片后离心。(C) 将挂钩工具放入适配器的开槽边上的孔中, (D) 轻轻拉。(E) 这些是执行免疫荧光成像所需的潮湿室的图片。箭头指示12毫米盖玻片。(F) 这些是具有代表性的共焦图像, 在 63X (变焦 2) 的梯度分数 #1-8, 收集在纯化过程中和染色的 CrSAS-6 (红色) 和α蛋白 (绿色)。嵌入对应于较低放大视图中由白色框表示的区域。刻度条 = 10 µm. (G) 这是一个图, 代表每个分数中每个视场的 CrSAS-6 和α蛋白的中心粒阳性数。注意分数的浓缩 #1-6。每个分数中每个字段的平均中心粒数: #1 = 16.3 4.7, #2 = 24.0 @ 4.6, #3 = 37.0 @ 17.0, #4 = 23.3 11.4, #5 = 14.3 @ 2.1, #6 = 13.7 @ 9.3, #7 = 2.7 @ 1.2, #8 = 1.0 @ 0.0, #9 = 1.0 @ 0.0, #10 = 0.0 @ 0.0, #11 = 0.3 @ 0.6, #12 = 0.0 @ 0.0。对于每一个分数, 3 个随机字段进行了成像。请注意, 当计数最丰富的分数 #3, 我们发现, 95% 的中心粒是积极的 CrSAS-6 和α蛋白 (n = 205 中心粒)。(H) 显微照片测量区域中中心粒的数量比率用于计算管区内中心粒的总数量。每个µL 的中心粒数可以从最初离心分数的10µL 计算出来。请单击此处查看此图的较大版本.
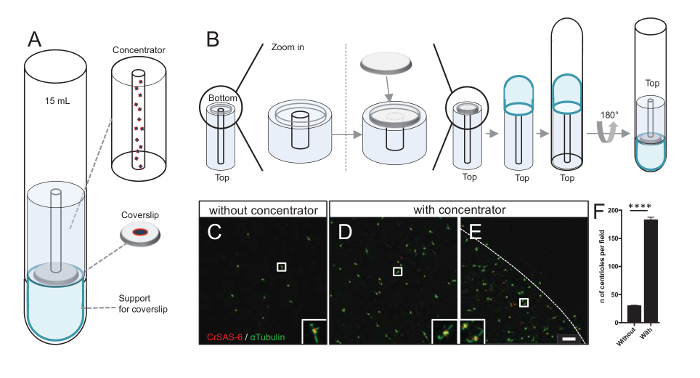
图 3: 使用聚光器离心隔离中心粒.(A) 本小组展示了在免疫荧光之前将中心粒浓缩到盖玻片所需的离心装置, 包括15毫升圆底管、选矿厂、12毫米盖玻片和一个支承适配器装置。(B) 本小组展示了组装离心装置的步骤。面板CE显示共焦图像的中心粒染色的 CrSAS-6 (红色) 和α-蛋白 (绿色) (C) 没有或 (DE) 与选矿厂。嵌入对应于较低放大视图中由白色框表示的区域。刻度条为10µm. 请注意, 中心粒在盖玻片的中间富集 (虚线代表集中区域的边界)。(F) 此图表示没有和与选矿厂的每个视野中心粒的数量。分析了五种随机视场。中心粒的平均数量是, 没有选矿厂, 29.8 @ 2.9, 并且与选矿厂, 182.6 @ 11.5, P < 0.0001。统计意义由一个配对t检验评估。请单击此处查看此图的较大版本.
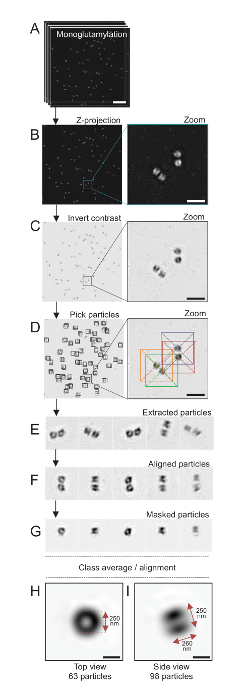
图 4: 孤立的单粒子平均C. 衣藻中心粒.(A) 此面板显示中心粒染色的 Z 堆栈图像, 并使用 SIM 显微镜获取 GT335。(B) 这些面板显示堆叠图像的最大强度 Z 投影。刻度条 = 1 µm. (C) 这些面板显示具有反对比的代表性图像。该嵌入表示放大, 以更好地可视化中心粒。(D) 这些面板显示颗粒采摘。插入物指示粒子是如何被采摘的。(E) 这些是5个提取粒子的例子。(F) 本小组在对齐后显示粒子。(G) 本小组在应用口罩后显示粒子。面板h和I显示两个类平均值: (H) 一个顶部视图 (63 粒子) 和 (I) 侧面视图 (98 粒子)。双箭头表示 GT335 信号的尺寸。刻度条 = 250 毫微米。请单击此处查看此图的较大版本.
补充文件 1.请单击此处下载此文件.
补充文件 2.请单击此处下载此文件.
讨论
生物学的一个挑战是在建筑环境中破译蛋白质的精确定位。中心粒是应用这些方法的理想结构, 因为它的体系结构已经使用了低温电子层析成像, 揭示了其长度的有趣的超微结构特征。然而, 由于它的尺寸接近光学显微学的分辨率极限, 很难精确地将蛋白质通过免疫荧光定位到中心粒的结构子区域, 使用常规显微镜30。
光学显微镜下的分辨率受光衍射的限制, 在光学显微镜24中大致可以得到 200 nm 的侧向最大分辨率。然而, 这一限制是过去20年在光学显微术中取得的重大突破之一: 超分辨率方法的发明。这些方法在不同的决议可能超出衍射极限的图像: 120 毫微米为 SIM, 大约50毫微米为被刺激的放射损耗 (STED) 和20–40毫微米为单分子定位显微镜 (SMLM)24。随着超分辨率显微技术的新发展, 中心粒的结构子区是可达到的。然而, 在实践中, 很难准确确定蛋白质的定位为一个结构元素, 主要原因是成熟的中心粒只存在于每个细胞的2拷贝和有随机方向, 这使得解释本地化困难。基于这个原因, 建立了一个协议, 允许研究人员通过超分辨率的大量中心粒来图像, 增加了观察非模糊方向的机会。重要的是, 由于这种方法依赖于孤立中心粒的使用, 我们提供了一种纯化完整的衣藻中心粒的方法, 它含有成熟的中心粒和 procentrioles。
最后, 由于该协议可以成像的中心粒方向范围, 单粒子分析可以应用电子显微软件。这将导致在特定方向上生成中心粒的平均类。重要的是, 这些产生的2维图像然后可以用来评估一个特定的蛋白质的本地化沿中心粒。事实上, 这种方法可以应用于双色超分辨率图像, 一种颜色可以用来揭示中心粒骨架 (如蛋白), 而另一种颜色则可归因于特定的 centriolar 蛋白。通过减去用一种颜色或两种颜色获得的平均值, 在中心粒 (近端、中心或远端) 上注册蛋白质变得更加容易。请注意, 这两个通道应该准确地对准, 以防止任何误导性的解释。此外, 最高视图的平均值将有助于破译在 centriolar 腔内, 沿微管壁, 或中心粒外的蛋白质本地化。
这种方法具有一定的优势, 以确定特定的蛋白质本地化可能难以本地化, 否则由于异构标签。请注意, 其他的方法来映射中心粒中的蛋白质已被描述在相关的3维 SIM/SMLM, 例如, 评估的具体方向, 形成一个圆环环的椭圆轮廓围绕中心粒通过 SIM 成像。使用这个参数, 可以将蛋白质本地化为第4-5 nm30的精度。还请注意, 此处描述的方法使用独立的中心粒和完整的 procentrioles, 这表明中心粒体系结构很可能基本上是守恒的。然而, 我们不能排除一些建筑特性在净化过程中受到干扰, 例如中心粒直径随价阳离子浓度的变化而被放大, 而人类中心体5的隔离。
这里提出的协议的关键步骤之一是获得足够集中的孤立中心粒在不同的方向, 荧光水疗。要做到这一点, 首先要保证中心粒隔离程序的纯度和效率。低浓度的孤立中心粒将防止正确的成像和进一步的图像处理。为此, 我们提供了一种方法, 以丰富每个视野中心粒的数量。根据所用分数中的中心粒数, 应调整集中器中加载的体积, 最大容积为250µL。
重要的是, 这种方法已经发展为细胞壁减去cw15 衣藻细胞。在这种菌株中, 细胞壁的脆弱性允许细胞的适当溶解, 从而释放其内容。该协议对野生型衣藻细胞没有效率, 因为细胞壁防止了适当的裂解。替代的战略, 如超声波或预先孵化的细胞与 autolysin, 一种酶, 可以降低细胞壁31, 将必须到位, 以改变细胞壁之前, 应用所提出的隔离协议。
这种设置可用于不同类型的显微镜, 从传统的共焦显微镜到高吞吐量专用超分辨率显微镜。请注意, 在进行 SMLM 时, 需要一个特殊的缓冲区来进行正确的成像, 因此, 应使用盖玻片顶部的缓冲区来适应12毫米盖玻片的房间。随后的成像将用倒置显微镜进行。如果显微镜的设置不允许12毫米盖玻片, 这里提出的协议可以应用到18毫米盖玻片使用30毫升的圆底管和修改后的适配器和选矿厂。还必须注意的是, SMLM 的最终重建质量将取决于染色的质量和所使用的原抗体, 以及固定方法。
总之, 我们提供了一种方法, 可以应用于图像众多的中心粒后, 荧光 SPA, 将产生中心粒的平均不同的方向, 从而帮助本地化 centriolar 蛋白质与精度。重要的是, 这种方法可以更广泛地应用于孤立的中心粒从其他物种, 其他细胞器, 或大型大分子组件。最后, 本文给出了样品制备方法, 结合最近对荧光 SMLM 数据32单粒子分析的算法开发, 可以进一步改进大型大分子分子制图组件。
披露声明
作者没有什么可透露的。
致谢
我们感谢皮埃尔 Gönczy 和 BioImaging & 光学平台 (BIOP) 在高等理工 Fédérale de 洛桑 (EPFL), 瑞士洛桑, 那里的 SIM 图像的中心粒被收购。尼古拉 Klena 和达维德 Gambarotto 得到欧洲研究理事会 (紧急救济) 启动赠款 (StG) 715289 (口音) 和索菲特塔西提玛依瓦乐 Guennec, 保罗吉夏尔体育场, 和 Virginie 的支持, 由瑞士国家科学基金会 (SNSF) PP00P3_157517。Susanne Borgers 得到了日内瓦大学的支持。
材料
| Name | Company | Catalog Number | Comments |
| Mouse monoclonal anti-apha tubulin (clone DM1A) | Abcam | ab7291 | dilution 1:300 |
| DNaseI | Roche | 10104159001 | |
| 12 mm coverslips | Roth | YX03.1 | |
| 18 mm coverslips | Roth | LH23.1 | |
| K2HPO4 | Fluka | 60355 | |
| KH2PO4 | Fluka | 60230 | |
| Tris base | Biosolve Chimie SARL | 0020092391BS | |
| acetic acid | Carlo Erba Reagents | 524520 | |
| NH4Cl | Sigma | A-4514 | |
| CaCl2 | Sigma | C-7902 | |
| MgSO4 | Sigma | 63140-500G-F | |
| steritop filter | Millipore | SCGPT05RE | |
| sucrose | Sigma | S7903-1KG | |
| HEPES | AppliChem PanReac | A3724,0250 | |
| PIPES | Sigma | P6757-500G | |
| MgCl2 | ACROS ORGANICS | 197530010 | |
| NP-40 | AppliChem PanReac | A1694,0250 | |
| Round-bottom (Kimble) tubes 15 mL | Fisherscientific | 09-500-34 | |
| Round-bottom (Kimble) tubes 30 mL | Fisherscientific | 09-500-37 | |
| cover glass staining rack | Thomas scientific | 8542E40 | |
| crystal polystyrene transmission lab box | FISHERS | 11712944 | |
| Methanol | VWR | 20864.32 | |
| BSA | Roche | 10735086001 | |
| Triton X100 | Roth | 3051.3 | |
| goat anti-mouse coupled to Alexa 488 | invitrogen | A11029 | dilution 1:1,000 |
| goat anti-rabbit coupled to Alexa 568 | invitrogen | A11036 | dilution 1:1,000 |
| mounting medium | abcam | ab188804 | |
| Tube, thinwall polypropylene | Beckman Coulter | 326823 | |
| Poly-D-Lysine 1 mg/mL | SIGMA | A-003-E | |
| Mouse monoclonal anti-Polyglutamylation modification mAb (GT335) | Adipogen | AG-20B-0020 | dilution 1:1,000 |
| glycerol mounting medium with DAPI and DABCO | Abcam | ab188804 | |
| 50 mL conical tubes | Falcon | 14-432-22 | |
| Eppendorf 5810R centrifuge | Eppendorf | 5811000622 | |
| Beckman JS-13.1 swinging bucket rotor | Beckman Coulter | 346963 | |
| Beckman SW 32Ti rotor | Beckman Coulter | 369694 | |
| parafilm | Bemis | 13-374-10 | |
| Leica TCS SP8 with Hyvolution mode | Leica | ||
| OSRAM L18W/954 LUMILUX | Luxe Daylight/ OSRAM | ||
| Whatman filter paper | Sigma | WHA1001325 | |
| CrSAS-6/Bld12 antibody | dilution 1:300 (Hamel el al., 2014) | ||
| Scipion | http://scipion.i2pc.es/ | ||
| EM CCD camera (Andor iXON DU897) | Andor |
参考文献
- Bornens, M. The centrosome in cells and organisms. Science. 335 (6067), 422-426 (2012).
- Nigg, E. A., Holland, A. J. Once and only once: mechanisms of centriole duplication and their deregulation in disease. Nature Reviews Molecular Cell Biology. 19 (5), 297-312 (2018).
- Nigg, E. A., Raff, J. W. Centrioles, centrosomes, and cilia in health and disease. Cell. 139 (4), 663-678 (2009).
- Gönczy, P. Towards a molecular architecture of centriole assembly. Nature Reviews Molecular Cell Biology. 13 (7), 425-435 (2012).
- Paintrand, M., Moudjou, M., Delacroix, H., Bornens, M. Centrosome organization and centriole architecture: their sensitivity to divalent cations. Journal of Structural Biology. 108 (2), 107-128 (1992).
- Winey, M., O'Toole, E. Centriole structure. Philosophical Transactions of the Royal Society of London. Series B, Biological Sciences. 369 (1650), (2014).
- Dippell, R. V. The development of basal bodies in paramecium. Proceedings of the National Academy of Sciences of the United States of America. 61 (2), 461 (1968).
- Allen, R. D. The morphogenesis of basal bodies and accessory structures of the cortex of the ciliated protozoan Tetrahymena pyriformis. The Journal of Cell Biology. 40 (3), 716-733 (1969).
- Li, S., Fernandez, J. -. J., Marshall, W. F., Agard, D. A. Three-dimensional structure of basal body triplet revealed by electron cryo-tomography. The EMBO Journal. 31 (3), 552-562 (2012).
- Guichard, P., Chrétien, D., Marco, S., Tassin, A. -. M. Procentriole assembly revealed by cryo-electron tomography. The EMBO Journal. 29 (9), 1565-1572 (2010).
- Guichard, P., et al. Native architecture of the centriole proximal region reveals features underlying its 9-fold radial symmetry. Current Biology. 23 (17), 1620-1628 (2013).
- Hirono, M. Cartwheel assembly. Philosophical Transactions of the Royal Society of London. Series B, Biological Sciences. 369 (1650), (2014).
- Bornens, M., Paintrand, M., Berges, J., Marty, M. C., Karsenti, E. Structural and chemical characterization of isolated centrosomes. Cell Motility and the Cytoskeleton. 8 (3), 238-249 (1987).
- Keller, L. C., Romijn, E. P., Zamora, I., Yates, J. R., Marshall, W. F. Proteomic analysis of isolated chlamydomonas centrioles reveals orthologs of ciliary-disease genes. Current Biology. 15 (12), 1090-1098 (2005).
- Kilburn, C. L., et al. New Tetrahymena basal body protein components identify basal body domain structure. The Journal of Cell Biology. 178 (6), 905-912 (2007).
- Bauer, M., Cubizolles, F., Schmidt, A., Nigg, E. A Quantitative analysis of human centrosome architecture by targeted proteomics and fluorescence imaging. The EMBO Journal. 35 (19), 1-15 (2016).
- Hamel, V., et al. Identification of Chlamydomonas Central Core Centriolar Proteins Reveals a Role for Human WDR90 in Ciliogenesis. Current Biology. 27 (16), 2486-2498 (2017).
- Cavalier-Smith, T. basal body and flagellar development during the vegetative cell cycle and the sexual cycle of Chlamydomonas reinhardii. Journal of Cell Science. 16 (3), 529 (1974).
- Geimer, S., Melkonian, M. The ultrastructure of the Chlamydomonas reinhardtii basal apparatus: identification of an early marker of radial asymmetry inherent in the basal body. Journal of Cell Science. 117, 2663-2674 (2004).
- Nakazawa, Y., Hiraki, M., Kamiya, R., Hirono, M. SAS-6 is a cartwheel protein that establishes the 9-fold symmetry of the centriole. Current Biology. 17 (24), 2169-2174 (2007).
- Hamel, V., et al. Correlative multicolor 3D SIM and STORM microscopy. Biomedical Optics Express. 5 (10), 3326 (2014).
- Guichard, P., et al. Cell-free reconstitution reveals centriole cartwheel assembly mechanisms. Nature Communications. 8, 14813 (2017).
- Hiraki, M., Nakazawa, Y., Kamiya, R., Hirono, M. Bld10p constitutes the cartwheel-spoke tip and stabilizes the 9-fold symmetry of the centriole. Current Biology. 17 (20), 1778-1783 (2007).
- Sahl, S. J., Hell, S. W., Jakobs, S. Fluorescence nanoscopy in cell biology. Nature Reviews Molecular Cell Biology. 18 (11), 685-701 (2017).
- Hutner, S. H., Provasoli, L., Schatz, A., Haskins, C. P. Some Approaches to the Study of the Role of Metals in the Metabolism of Microorganisms. Proceedings of the American Philosophical Society. 94 (2), 152-170 (1950).
- Keller, L. C., Marshall, W. F. Isolation and proteomic analysis of chlamydomonas centrioles. Methods in Molecular Biology. 432 (1), 289-300 (2008).
- Borlinghaus, R. T., Kappel, C. HyVolution-the smart path to confocal super-resolution. Nature Methods. 13 (3), (2016).
- Schneider, C. A., Rasband, W. S., Eliceiri, K. W. NIH Image to ImageJ: 25 years of image analysis. Nature Methods. 9 (7), 671-675 (2012).
- de la Rosa-Trevín, J. M., et al. Scipion: A software framework toward integration, reproducibility and validation in 3D electron microscopy. Journal of Structural Biology. 195 (1), 93-99 (2016).
- Gartenmann, L., et al. A combined 3D-SIM/SMLM approach allows centriole proteins to be localized with a precision of ∼4-5 nm. Current Biology. 27 (19), 1054-1055 (2017).
- Jaenicke, L., Kuhne, W., Spessert, R., Wahle, U., Waffenschmidt, S. Cell-wall lytic enzymes (autolysins) of Chlamydomonas reinhardtii are (hydroxy)proline-specific proteases. European Journal of Biochemistry. 170 (1-2), 485-491 (1987).
- Salas, D., et al. Angular reconstitution-based 3D reconstructions of nanomolecular structures from superresolution light-microscopy images. Proceedings of the National Academy of Sciences of the United States of America. 114 (35), 9273-9278 (2017).
转载和许可
请求许可使用此 JoVE 文章的文本或图形
请求许可探索更多文章
This article has been published
Video Coming Soon
版权所属 © 2025 MyJoVE 公司版权所有,本公司不涉及任何医疗业务和医疗服务。