需要订阅 JoVE 才能查看此. 登录或开始免费试用。
Method Article
一种使用纳米草本封装精油的抗菌织物
摘要
抗菌实验室外套可防止病原体积聚和意外生物溢出的交叉污染。在这里,我们描述了使用纳米草药封装和改良标准测试开发皮肤友好型抗菌织物的方案,以精确评估实验室外套典型用途的功效和适用性。
摘要
实验室外套广泛用于生物危害实验室和医疗机构,作为防护服,以防止直接接触病原体、溢出物和烧伤。这些棉基保护层因其多孔性、保湿能力和从用户体内保持温暖而为微生物生长和附着部位提供了理想的条件。一些研究表明,医院服装和实验室外套上的致病菌存活,是微生物传播的载体。
解决这些问题的常见方法是在纺织品整理中使用抗菌剂,但由于许多合成化学品的毒性和环境影响,人们提出了担忧。持续的大流行也为研究有效的抗菌剂和环保无毒配方打开了一扇窗。这项研究使用两种天然生物活性化合物,香芹酚和百里酚,封装在壳聚糖纳米颗粒中,保证有效保护四种人类病原体,减少多达4个对数(99.99%)。这些病原体经常在生物危害实验室使用的实验室外套中检测到。
经过处理的织物还可以抵抗多达 10 次洗涤循环,微生物减少 90%,足以满足预期用途。我们对现有的标准织物测试进行了修改,以更好地代表实验室外套使用的典型场景。这些改进可以更准确地评估抗菌实验室涂层的有效性,并模拟必须在短时间内中和的任何意外微生物泄漏的命运。建议进一步研究,以调查与常规防护外套相比,抗菌实验室外套上病原体随时间推移的积累。
引言
白大褂防护是微生物实验室和医疗机构的强制性个人防护装备 (PPE),可防止直接接触病原体、溢出物和烧伤。由于许多因素,这些棉大衣促进了微生物的生长 - 机织织物提供附着部位和通气,制造过程中使用的棉花和淀粉以及来自用户的脱落上皮细胞提供营养,并且靠近用户提供温暖和水分。微生物在纺织品上的积累也会导致健康问题,例如过敏和院内感染、难闻的气味和织物变质1.
与普通衣服不同,防护服很少清洗或消毒,正如许多调查所发现的那样2,3。许多研究表明,实验室外套是微生物传播的载体,在医疗保健环境中存在院内感染的风险2,4,特别是耐药菌株3,例如耐甲氧西林金黄色葡萄球菌(MRSA);因此,它们引起了个人防护装备的健康问题,而个人防护装备旨在防止微生物污染。在生物安全2级(BSL-2)设施或微生物学教学实验室的背景下,没有足够的关于实验室外套相关感染的横断面研究,但许多监管机构限制在遏制级别内使用实验室外套。然而,由于实际限制,北美的许多学术机构都在努力满足要求,例如在设施内清洗和存放,在自助餐厅和图书馆等公共区域穿着实验室外套的事件很常见。解决这些问题的一个实用解决方案是在纺织品整理中使用抗菌剂。
抗菌织物在运动服、运动服和袜子中越来越受欢迎,主要是为了减少体味。然而,这些织物在个人防护装备开发中并不常见,除了一些镀银棉口罩和保健服装5。我们报告了一种用于实验室外套的抗菌织物的开发,该织物可抑制BSL-2实验室中发现的常见病原体,并有效防止常见病原体的交叉污染。
目前,市场上有各种抗菌织物和整理剂,但其中大多数使用重金属胶体颗粒(例如银、铜、锌)、有机金属化合物或合成化学品,例如三氯生和季铵化合物,这些化合物对环境不友好1 并可能导致健康问题,例如皮肤刺激和过敏6.由于非目标微生物,例如正常菌群或诱导抗菌素耐药性(AMR),一些合成配方会引起关注。美国食品和药物管理局(FDA)对商业抗菌织物进行监管,这些织物必须对用户无毒且无生态毒性。因此,基于抑制广谱微生物的天然杀菌剂的抗菌织物是优选的。精油(EO)被广泛用作抗菌剂和治疗剂,但由于其耐用性6,7,8,它们在抗菌整理中的使用受到限制。根据我们对纳米草药整理8的知识和市场研究,没有基于草药的抗菌织物可供市售。这是因为合成涂料易于制造且具有较长的耐用性。一些仅用于研究目的的纳米草药涂层纺织品包括印楝7,辣木9和咖喱叶9。
本研究使用从牛至EO中提取的两种生物活性成分,香芹酚和百里酚,它们对多种细菌病原体和病毒有效,但通常被认为对人类安全10。然而,这些生物活性成分是挥发性的,因此如果直接应用于织物,它们的抗菌潜力是短暂的。纳米草药封装是将生物活性成分或药物装载在聚合物外壳内的过程,可保护核心免受环境降解,从而延长保质期。此外,聚合物颗粒的小尺寸(通常范围为10 nm至100 nm)提高了应用的功效并减缓了生物活性化合物在织物上的释放。这些生物活性化合物用于各种目的,例如食品保鲜10,但不用于纺织品涂层。
在许多聚合物灌封剂中,壳聚糖因其许多属性(例如无毒、生物降解性、粘液粘附性和生物相容性)而成为有吸引力的候选者11。它是一种天然多糖,通过几丁质的脱乙酰过程获得,甲壳素存在于贝壳和真菌细胞壁中。它用于生化和食品保鲜应用,例如药物或蛋白质递送11、12、13、控释 14 和抗菌膜 10。壳聚糖不易溶于水,但在酸性介质中形成胶体悬浮液。生物活性分子通过简单的两步离子凝胶方法14,15,16加载到壳聚糖纳米颗粒(NPs)中。在此过程中,疏水性生物活性化合物如香芹酚和麝香草酚形成水包油乳液,其由表面活性剂吐温80辅助。随后,使用聚阴离子化合物三聚磷酸五钠(TPP)在沿聚阳离子聚合物分子的氨基和TPP分子的磷酸基团之间形成交联以稳定复合物。这种络合过程固化了壳聚糖基质内的生物活性化合物,随后将其纯化并涂覆到棉板上以生产抗菌织物。
纳米配方在应用于织物之前,必须首先测试乳液形式的抗菌效果。这可以通过定性方法方便地进行评估,例如柯比-鲍尔盘扩散、孔扩散和圆柱板测定。然而,圆筒板测定17 提供了加载不同体积的制剂和比较间隙区域的灵活性。在该方法中,将抗菌制剂装入不锈钢圆筒中并放置在软琼脂层上,该层接种有测试微生物或病原体。针对测试生物体产生的清除区的直径与抗菌制剂的抑制潜力成正比,因此可用作肉汤稀释方法的替代方法。然而,除非保持特定的标准,否则净区的大小只是特定板块内的比较或定性措施。抗菌剂通过抑制病原体的生长(生物静态)或杀死细胞(生物杀灭剂)来对抗病原体,这可以通过最小抑制浓度(MIC)和最小杀菌浓度(MBC)分别进行量化。然而,生物活性化学品的功效和行为在其配方(液态)和涂覆在诸如织物的基材上时是不同的18。这是因为多种因素在功效中起作用,例如抗菌剂对织物的粘附稳定性、水分含量、底物类型和微生物的粘附性。如果预期目的只是抑菌活性,则诸如“平行条纹法”19 之类的定性测定可以提供相对快速和容易的扩散抗菌制剂评估。但是,如果要确定杀菌效果,则可以采用“纺织材料抗菌整理剂评估”20 ,从而减少加标病原体的对数。
Access restricted. Please log in or start a trial to view this content.
研究方案
1. 纳米颗粒的制备
- 纳米草药封装
- 准备 50 mL 的 1% (v/v) 乙酸。
注意:冰醋酸是一种刺激物,会导致严重的皮肤灼伤和眼睛损伤。穿上全身实验室外套、丁腈手套和护目镜,并在通风橱下工作。 - 通过将0.6g壳聚糖薄片(中等分子量)溶解在50mL的1%乙酸(上述制备)中来制备壳聚糖溶液(1.2% w / v)。在室温(R / T)下搅拌过夜(O / N),以获得均匀的乳液。
- 加入0.5g吐温80,并在60°C下搅拌(1,000rpm)2小时以获得均匀的溶液。在添加生物活性化合物(香芹酚或百里酚)之前,将溶液带到R / T。
- 滴加0.75g香芹酚(或百里酚),滴加或逐渐加入,同时在R / T下搅拌(1,000rpm)混合物20分钟。壳聚糖与生物活性化合物的重量比为1:1.25。
- 在以R / T搅拌的同时,将50mL(0.5%w / v)的TPP滴加到混合物中,继续搅拌30分钟以获得均匀的乳液。
- 按照相同的程序制备阴性对照,但不添加生物活性化合物。
- 准备 50 mL 的 1% (v/v) 乙酸。
- 纯化
- 将乳液在4°C下以10,000× g 离心30分钟,并在倾析上清液后收集形成的NP(沉淀)。保留上清液以测试包封功效。
- 使用吐温80水溶液(1%v / v)洗涤颗粒(从步骤1.2.1),用两倍体积的颗粒去除未结合或游离的生物活性化合物。确保通过涡旋来干扰颗粒,直到在每个洗涤步骤中形成均匀的溶液。
- 用去离子水洗涤颗粒(从步骤1.2.2开始)两次以去除杂质。
- 通过将沉淀(从步骤1.2.3)重悬于30mL去离子水中来重建NP。将NPs在4°C下储存长达6个月。
注意:实验可以在此阶段暂停。
- 表征
- 在去离子水中稀释NP,直到250至400nm之间的紫外可见(UV-Vis)读数落在该范围内(吸光度>1)。
- 使用紫外-可见分光光度计记录NP在250至400nm波长范围内的紫外-可见吸收光谱。
- 将等分试样 (1 mL) NPs 在 R/T 下储存一段时间(例如 1 至 6 个月),并通过圆柱板法与新鲜样品一起测试抗菌效果。
- 织物涂层
- 使用垫干固化方法在机织棉织物上施用NPs7,21。
- 将织物样本浸入含有NPs的溶液中与织物粘合剂混合3分钟,直至浸泡。然后,将色板通过双辊实验室垫片以去除多余的液体。
- 将色板在100°C烘干30分钟,并在130°C下固化10分钟。
- 最后,在超声波浴中洗涤色板15分钟以去除未结合的NP。
注意:或者,请按照下面描述的简化方法进行操作。
- 将棉织物(或实验室外套色板)切成 10 厘米 x 10 厘米的正方形。
- 将切割的碎片浸入 2 mL 合成的 NP (10%) 中,在塑料容器 (12 cm x 12 cm) 中以 R/T 的速度浸入 2 分钟。 通过风干除去多余的液体。
- 在100°C下加热3分钟以结合NPs。
- 通过在吐温80水溶液(2%w / v)中冲洗并在100°C的烤箱中干燥30分钟来除去未结合的NP。
注意:这种抗菌织物可以在R / T下储存2年。
- 使用垫干固化方法在机织棉织物上施用NPs7,21。
- 耐洗性
- 将织物切成 50 毫米 x 50 毫米的方形色板。
- 将色板放入玻璃/塑料容器中的50mL温自来水(40°C)中,并加入两滴常规洗涤剂(非抗菌剂)。
- 在摇床摇床或磁力搅拌器上冲洗30分钟。
- 风干或在60°C孵育2小时,并测试抗菌功效。
2. 用于筛选纳米颗粒的圆筒板测定
- 根据制造商的说明制备胰蛋白酶大豆琼脂(TSA),胰蛋白酶大豆肉汤(TSB),抗生素碱琼脂(ABA)和抗生素种子琼脂(ASA),并通过在121°C下在15psi下高压灭菌15分钟来灭菌培养基。
- 通过三向条纹板法在新鲜制备的TSA板(或任何适当的培养基)上传代培养感兴趣的微生物(来自库存),并孵育以生产纯度板。(推荐物种: 金黄色葡萄球菌、 大肠杆菌、 铜绿假单胞菌和 白色念珠菌。
- 从TSB(10mL管)中的新鲜纯度板中接种培养物,在35°C O / N下适度振荡(100-200rpm)。
- 在每个试管中等分 5.0 mL 熔融 ASA。管的数量对应于测试的微生物数量。
- 将 20 mL 预灭菌的熔融 ABA 无菌倒入每个培养皿 (100 mm x 20 mm) 中以形成基层。琼脂平板的数量对应于要测试的微生物的数量。等到介质凝固。
- 基底层凝固后,用步骤2.3(1.0mL,预热至35°C)中的过夜培养物接种每个熔融的ASA,并立即将内容物(ASA和培养物的混合物)转移到ABA板的表面。旋转平板以使熔融琼脂层均匀分布。确保种子层看起来光滑,没有肿块或气泡。
- 使用一对无菌镊子,每个琼脂平板将多达六个不锈钢圆筒(6 mm x 6 mm x 10 mm;预高压灭菌)均匀分布在每个琼脂平板上(图1)。
- 用不同体积(30 μL、50 μL、75 μL 和 100 μL)合成的 NP 加载气瓶,以筛选抗菌效果。阴性对照是没有任何生物活性化合物的对照。
- 将常见的细菌病原体(例如, 大肠杆菌, 金黄色葡萄球菌, 铜绿假单胞菌)在35°C孵育24小时,将真菌物种(例如 白色念珠菌)在R / T孵育3天。
- 测量净区的直径并比较合成NPs的有效性。
注意:此测试可用于预先筛选要涂在织物上的最佳NP。
3. 平行条纹法(根据 AATCC 147 修改)
- 材料准备
- 将NP处理过的织物切成50毫米x 25毫米的色板。
- 根据制造商的说明制备Mueller-Hinton琼脂(MHA),TSA和TSB,并通过在121°C下以15 psi高压灭菌15分钟来灭菌培养基。
- 通过三向条纹板法在新制备的TSA板(或任何适当的培养基)上传代培养感兴趣的微生物(来自库存),并孵育2天用于细菌污渍,并在R / T下孵育5天用于真菌菌株以产生纯度板。(推荐物种: 金黄色葡萄球菌、 大肠杆菌、 铜绿假单胞菌和 白色念珠菌。
- 微生物培养物的加标
- 从TSB(10mL管)中的新鲜纯度板中接种培养物,在35°C O / N下适度振荡(100-200rpm)。
- 将 O/N 培养物稀释至 1.5 × 108 菌落形成单位 (CFU)/mL 或相当于 0.5 McFarland 标准品的浊度(对于大多数健康培养物,通常为 1/10 至 1/20 稀释度)。
- 使用4mm无菌环接种上述稀释的培养物,如下所示。根据 图2,加载一圈肉汤培养物,并通过制作五条平行条纹将其转移到MHA琼脂平板的表面,每条条纹长6厘米,相距1厘米。不要重新填充循环。
- 使用无菌刮刀在五条条纹上轻轻按压织物色板,使织物位于中心并接触所有五条条纹线。在35°C孵育24小时。
- 抗菌效果的定性评估
- 检查孵育板是否沿着织物边缘以外的条纹中断生长(透明区域表示生长抑制)。
- 使用公式 (1) 计算沿织物色板两侧条纹线 (W) 的抑制区的平均宽度。
W = (T - D)/2 (1)
W = 净区宽度;T = 净区的总长度,包括色板宽度;D = 织物样本的宽度 (25 mm)。
4. 定量对数减少法(根据AATCC 100修改)
- 实验准备
- 将织物切成 50 毫米 x 50 毫米的方形色板。
- 根据制造商的说明制备 TSA、TSB、Letheen 肉汤和磷酸盐缓冲盐水 (PBS),并通过高压灭菌对培养基进行灭菌。
- 通过在无菌TSB中接种纯度板中的分离菌落并在35°C下孵育18-24小时,制备感兴趣的微生物的O / N培养物,并对其进行功效测试。 (推荐物种: 金黄色葡萄球菌, 大肠杆菌, 铜绿假单胞菌和 白色念珠菌。
- 微生物培养物的加标
- 将O / N培养物稀释至1.5×108CFU /mL或相当于0.5麦克法兰标准品的浊度(对于大多数健康培养物,通常为1/10至1/20稀释度)。
- 通过测量织物的持液能力来确定用于加标的适当培养物体积,如下所示。
- 将一系列体积的稀释肉汤培养物(例如,100-500 μL)添加到织物样本(在单独的培养皿中)上,并选择体积,使织物样本完全吸收水分并且不留下残留/游离液体。液体保持能力与织物的类型和厚度不同。对于普通的棉质实验室外套,它大约是 200 μL。
- 将每种培养物的体积(上面确定的液体保持容量[例如,200μL])加标到放置在无菌培养皿中的样本上。色板的数量对应于测试次数(例如,立即测试的织物和洗涤后[以及测试的洗涤周期]),以及在接触时间内测试的抗菌效果(在设定的时间/天后[例如,30分钟,2小时,第1-3天])。
注意:使用带有气溶胶过滤器吸头的微量移液器(以防止在后续使用中污染移液器)以均匀分布的方式接种色板上的培养物。 - 对于阴性对照,使用相同类型的未经处理的织物样本。对每种相应的测试微生物种类、接触期、不同的织物和洗涤周期进行阴性对照。
- 通过活菌板计数回收微生物
- 允许接种的色板(处理和未处理)在培养皿内以R / T风干(盖子半开),以测试所需的接触期(例如,0分钟,30分钟,60分钟等,甚至几天的长期影响)。始终包括“0分钟”以表示立竿见影和中和功效。
- 无菌地将色板转移到分离的无菌离心管(50 mL)中,然后拧紧盖子。
- 加入Letheen肉汤(任何相关的中和缓冲液)进行1/100稀释(例如,200 μL的接种物为19.8 mL)。
- 用螺旋盖紧紧关闭离心管,并以中速涡旋1分钟。
- 在随后的1/10稀释液中用无菌PBS连续稀释悬浮液,使得“未处理”组的菌落计数变得太低而无法计数(TLTC)。
- 将稀释液 (0.1 mL) 接种在适当的培养基板上,以支持微生物的生长(例如,细菌的 TSA 或真菌的 Sabouraud 葡萄糖琼脂 [SDA])或任何优化生长并提供良好对比度以使菌落计数准确的培养基。
- 将细菌板在35°C孵育2天,将真菌板在R / T孵育5天。
- 使用菌落计数器或使用成像软件(例如 CFU AI)直接计数活的 CFU。
- 使用公式(2)计算由于抗菌织物引起的微生物对数减少(R):
R =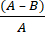 × 100 (2)
× 100 (2)
A = 从未处理的织物中回收的 CFU 数量的对数值;B = 从处理过的织物中回收的 CFU 数量的日志值。
Access restricted. Please log in or start a trial to view this content.
结果
合成NPs的初步筛选
按照两步水包油乳液技术16,生物活性化合物(香芹酚和百里酚)成功地包封在壳聚糖中。紫外-可见分光光度法证实了这一点,与对照组(不含任何生物活性化合物的壳聚糖NPs)相比,各个生物活性化合物的峰吸收。所构成的NPs在4 °C下12个月内均质且稳定。 通过气缸板法验证了抗菌效果的初步筛选(图1)。这是一种定性?...
Access restricted. Please log in or start a trial to view this content.
讨论
杀菌剂的抗菌功效通常通过定量测定进行测试,例如最小抑菌浓度(MIC)和最小杀菌浓度(MBC),其中将细菌浸入抗菌液体中24小时。然而,这些测定不适用于涂层织物,其中缺乏液体界面,杀菌剂沿着织物纤维缓慢扩散。因此,已经建立了许多标准的织物测试,例如AATCC 147,ISO 20645,AATCC 100和JIS L 1902。Pinho等人对这些标准的比较研究23 承认,对于使用最合适的方法尚未达成共?...
Access restricted. Please log in or start a trial to view this content.
披露声明
作者没有利益冲突。
致谢
这项研究由加拿大百年学院的“应用研究,创新和创业服务”(ARIES)资助。
Access restricted. Please log in or start a trial to view this content.
材料
| Name | Company | Catalog Number | Comments |
| Acetic acid | Millipore Sigma | 64-19-7 | |
| Antibiotic base agar | BD Difco | DF0270-17-4 | Also known as Antibiotic Medium 2 |
| Antibiotic seed agar | BD Difco | DF0263-17-3 | Also known as Antibiotic Medium 1 |
| Blood Agar (Nutrient Agar with 5% Sheep Blood) | Donated by CFIA | ||
| Bromcresol Purple Lactose Agar | Donated by CFIA | ||
| Candida albicans | ATCC The Global Bioresource Center | ATTC 10231 | |
| Carvacrol | Millipore Sigma | 282197 (CAS# 499-75-2) | |
| Centrifuge Allergra X-22R Centrifuge | Beckman Coulter | Model # X-22R | Refrigerated. Wait at least 20 min or until the temperature reach the set low value (e.g., 4 °C) as the refrigeration takes time. |
| Chitosan Medium Molecular Weight (CS) | Millipore Sigma | 448877 (CAS # 9012-76-4) | |
| Clamshell Heat Press | Intiva | IM1200 | |
| Escherichia coli (E. coli) | ATCC The Global Bioresource Center | ATTC 23725 | |
| Incubator | Thermo Scientific | 1205M34 | |
| Letheen Broth | BD Difco | DF0681-17-7 | Used to neutralize antimicrobial effects. Product from different manufacturers may require to add Polysorbate 80, which is already added in Difco product. |
| Milli Q water | Millipore Sigma | ZR0Q16WW | Deionized water |
| Mueller-Hinton Agar | BD Difco | DF0252-17-6 | |
| Pentasodium tripolyphosphate (TPP) | Millipore Sigma | 238503 (CAS# 7758-29-4) | |
| Phospahte Buffered Saline (PBS) | Thermo Scientific | AM9624 | |
| Pseudomonas aeruginosa | ATCC The Global Bioresource Center | ATTC 9027 | |
| Sabouraud Dextrose Agar | BD Difco | DF0109-17-1 | |
| Shaking incubator/ Thermo shaker | VWR | Model# SHKA2000 | |
| Staphylococcus aureus | ATCC The Global Bioresource Center | ATTC 6538 | |
| Thymol | Millipore Sigma | T0501 (CAS# 89-83-8) | |
| Trypticase Soy Agar | BD Difco | 236950 | |
| Trypticase Soy Broth | BD Difco | 215235 | |
| Tween 80 | Millipore Sigma | STS0204 (CAS # 9005-65-6) | |
| UV-Vis Spectrophometer | Thermo Scientific | GENESYS 30 (840-277000) |
参考文献
- Schmidt-Emrich, S., et al. Rapid assay to assess bacterial adhesion on textiles. Materials. 9 (4), 249(2016).
- Qaday, J., et al. Bacterial contamination of medical doctors and students white coats at Kilimanjaro Christian Medical Centre, Moshi, Tanzania. International Journal of Bacteriology. 2015, 507890(2015).
- Treakle, A. M., et al. Bacterial contamination of health care workers' white coats. American Journal of Infection Control. 37 (2), 101-105 (2009).
- Wong, D., Nye, K., Hollis, P. Microbial flora on doctors' white coats. BMJ. 303 (6817), 1602-1604 (1991).
- Gouveia, I. C. Nanobiotechnology: A new strategy to develop non-toxic antimicrobial textiles for healthcare applications. Journal of Biotechnology. (150), 349(2010).
- Joshi, M., Ali, S. W., Purwar, R., Rajendran, S. Ecofriendly antimicrobial finishing of textiles using bioactive agents based on natural products. Indian Journal of Fibre and Textile Research. 34, 295-304 (2009).
- Ahmed, H. A., Rajendran, R., Balakumar, C. Nanoherbal coating of cotton fabric to enhance antimicrobial durability. Elixir Applied Chemistry. 45, 7840-7843 (2012).
- Morais, D. S., Guedes, R. M., Lopes, M. A. Antimicrobial approaches for textiles: From research to market. Materials. 9 (6), 498(2016).
- Venkatraman, P. D., Sayed, U., Parte, S., Korgaonkar, S. Development of advanced textile finishes using nano-emulsions from herbal extracts for organic cotton fabrics. Coatings. 11 (8), 939(2021).
- Martínez-Hernández, G. B., Amodio, M. L., Colelli, G. Carvacrol-loaded chitosan nanoparticles maintain quality of fresh-cut carrots. Innovative Food Science & Emerging Technologies. 41, 56-63 (2017).
- Zhang, H. L., Wu, S. H., Tao, Y., Zang, L. Q., Su, Z. Q. Preparation and characterization of water-soluble chitosan nanoparticles as protein delivery system. Journal of Nanomaterials. 2010, 1-5 (2010).
- Patel, R., Gajra, B., Parikh, R. H., Patel, G. Ganciclovir loaded chitosan nanoparticles: preparation and characterization. Journal of Nanomedicine & Nanotechnology. 7 (6), 1-8 (2016).
- Merodio, M., Arnedo, A., Renedo, M. J., Irache, J. M. Ganciclovir-loaded albumin nanoparticles: characterization and in vitro release properties. European Journal of Pharmaceutical Sciences. 12 (3), 251-259 (2001).
- Hsieh, W. C., Chang, C. P., Gao, Y. L. Controlled release properties of Chitosan encapsulated volatile Citronella Oil microcapsules by thermal treatments. Colloids and Surfaces B: Biointerfaces. 53 (2), 209-214 (2006).
- Yoksan, R., Jirawutthiwongchai, J., Arpo, K. Encapsulation of ascorbyl palmitate in chitosan nanoparticles by oil-in-water emulsion and ionic gelation processes. Colloids and Surfaces B: Biointerfaces. 76 (1), 292-297 (2010).
- Keawchaoon, L., Yoksan, R. Preparation, characterization and in vitro release study of carvacrol-loaded chitosan nanoparticles. Colloids and Surfaces B: Biointerfaces. 84 (1), 163-171 (2011).
- Cazedey, E. C. L., Salgado, H. R. N. Development and validation of a microbiological agar assay for determination of orbifloxacin in pharmaceutical preparations. Pharmaceutics. 3 (3), 572-581 (2011).
- Jayapriya, S., Bagyalakshmi, G. Textile antimicrobial testing and standards. International Journal of Textile and Fashion Technology. 4 (1), 2250-2378 (2013).
- AATCC 100. Antibacterial Finishes on Textile Materials: Assessment of Developed from American Association of Textile Chemists and Colorists. AATCC 100. , (2004).
- AATCC 147. Antimicrobial Activity Assessment of Textile Materials: Parallel Streak Method from American Association of Textile Chemists and Colorists. AATCC 147. , (2004).
- Ortelli, S., Costa, A. L., Dondi, M. TiO2 nanosols applied directly on textiles using different purification treatments. Materials. 8 (11), 7988-7996 (2015).
- Poole, K. Pseudomonas aeruginosa: resistance to the max. Frontiers in Microbiology. 2, 65(2011).
- Pinho, E., Magalhães, L., Henriques, M., Oliveira, R. Antimicrobial activity assessment of textiles: standard methods comparison. Annals of Microbiology. 61 (3), 493-498 (2010).
- Venkatraman, P. D., Sayed, U., Parte, S., Korgaonkar, S. Novel antimicrobial finishing of organic cotton fabrics using nano-emulsions derived from Karanja and Gokhru plants. Textile Research Journal. 92 (23-24), 5015-5032 (2022).
Access restricted. Please log in or start a trial to view this content.
转载和许可
请求许可使用此 JoVE 文章的文本或图形
请求许可探索更多文章
This article has been published
Video Coming Soon
版权所属 © 2025 MyJoVE 公司版权所有,本公司不涉及任何医疗业务和医疗服务。