需要订阅 JoVE 才能查看此. 登录或开始免费试用。
Method Article
使用基因编码的钙指示剂对病毒感染的人肠道类器官单层进行活体钙成像
摘要
该协议描述了一种在病毒感染的人肠道类器官中进行钙成像的方法,并提供了一种分析方法。
摘要
钙信号传导是几乎每个组织不可或缺的调节剂。在肠上皮细胞内,钙参与分泌活性、肌动蛋白动力学、炎症反应、干细胞增殖和许多其他未表征的细胞功能的调节。因此,绘制肠上皮内的钙信号动力学可以深入了解稳态细胞过程,并揭示对各种刺激的独特反应。人肠道类器官 (HIO) 是一种用于研究肠上皮的高通量人源模型,因此代表了研究钙动力学的有用系统。本文描述了一种使用基因编码钙指示剂 (GECI) 稳定转导 HIO 的方案,进行实时荧光显微镜检查,并分析成像数据以有意义地表征钙信号。作为代表性示例,用慢病毒转导三维 HIO 以稳定表达 GCaMP6s,这是一种基于绿色荧光蛋白的胞质 GECI。然后将工程化的HIO分散到单细胞悬浮液中,并作为单层接种。分化后,HIO单层感染轮状病毒和/或用已知刺激钙反应的药物治疗。装有温控加湿活体成像室的落射荧光显微镜可以对受感染或药物治疗的单层进行长期成像。成像后,使用免费提供的分析软件ImageJ分析采集的图像。总体而言,这项工作建立了一个适应性强的管道,用于表征HIO中的细胞信号转导。
引言
钙是一种广泛保守的第二信使,在调节细胞生理学中起着关键作用1。鉴于其电荷强、体积小、在生理条件下溶解度高,钙是蛋白质构象的理想操纵剂。这使得钙成为将电化学信号转导为酶促、转录或转录后改变的有力手段。内质网 (ER) 和质膜上严格的钙浓度梯度产生了高驱动力,允许胞质钙浓度快速变化。多种机制,包括缓冲和主动运输,都紧紧地维持了这种梯度。虽然这种维持对于正常的细胞功能是必要的,但这种维持在能量上是昂贵的,使其在压力状态下特别容易受到 影响 2.
因此,胞质溶胶内钙的失调是多种细胞应激的近乎普遍的信号。代谢紊乱、毒素、病原体、机械损伤和遗传扰动都会破坏钙信号传导。无论刺激如何,在全细胞水平上,胞质钙的持续、不受控制的升高都会促进细胞凋亡并最终导致坏死 3,4。然而,较低振幅或较高频率的胞质钙水平的改变具有不同的影响2。同样,钙波动的结果可能因发生钙波动的空间微域而异5.因此,监测钙水平可以深入了解动态信号转导过程,但这需要具有相对较高的时间和空间分辨率的采样。
基因编码钙指示剂 (GECI) 是在活细胞系统中连续采样的有力工具6。一些使用最广泛的 GECI 是基于 GFP 的钙反应性荧光蛋白,称为 GCaMPs7。经典 GCaMP 是三个不同蛋白质结构域的融合:环状置换 GFP (cpGFP)、钙调蛋白和 M136。钙调蛋白结构域在结合钙时发生构象变化,使其与 M13 相互作用。钙调蛋白-M13 相互作用诱导 cpGFP 的构象变化,从而在激发时增加其荧光发射。因此,钙浓度的增加与GCaMP荧光强度的增加有关。这些传感器可以是胞质的,也可以是靶向特定的细胞器8。
与大多数组织类似,钙调节胃肠上皮内的各种功能。肠上皮是营养和液体吸收不可或缺的一部分,但也必须形成紧密的屏障和免疫界面,以避免病原体入侵或毒性侮辱。钙依赖性途径几乎影响所有这些重要功能9,10,11。然而,肠上皮内的钙信号传导仍然是一个未被充分探索的前沿领域,具有作为治疗靶点的潜力。虽然在体内监测肠上皮内的钙动力学继续面临挑战,但人肠道类器官 (HIO) 为实验提供了适应性强的离体系统12。HIO 是源自人类肠道干细胞的 3 维 (3D) 球体,在分化后概括了天然肠上皮细胞的大部分细胞多样性 12。
该协议描述了设计表达GECI的HIO的综合方法,然后将工程HIO制备为用于活细胞钙成像的单层。它提供了病毒感染作为破坏钙信号传导的病理操作的一个例子,并提供了一种分析方法来量化这些变化。
研究方案
本方案和代表性实验中使用的所有人类肠道类器官(HIO)均来源于德克萨斯医学中心消化疾病类肠核心获得和维护的人体组织。所有样本均根据贝勒医学院机构审查委员会批准的方案收集。
1.材料和试剂的制备
- 对于类器官维持,收集细胞培养处理的 24 孔板、基底膜基质 (BMM)、15 mL 锥形管和 1.5 mL 锥形管。
- 为了制备不含生长因子 (CMGF-) 的完整培养基,向 500 mL 高级 DMEM F12 中加入 5 mL 1M HEPES、5 mL 100x 抗生素-抗真菌剂、5 mL 100x 谷氨酰胺补充剂。
- 要制备含 Wnt、R-spondin 和 Noggin 的 (WRNE) 培养基,混合等量的 CMGF 和 Wnt 条件培养基,加入 Noggin 条件培养基(按体积计 10%)、R-spondin 条件培养基(按体积计 20%)、50 ng/mL 人表皮生长因子、10 mM 烟酰胺、10 nM [Leu15]-胃泌素 I、500 nM A-83-01、10 μM SB202190、1x B27 添加剂、1x N2 添加剂和 1 mM N-乙酰半胱氨酸。
- 对于慢病毒转导,制备胎牛血清 (FBS)、0.05% 胰蛋白酶-EDTA 在 1x 磷酸盐缓冲盐水 (PBS) 中、CMGF-和 10% FBS、无菌 1x PBS、聚布苯乙烯、10 μM Y-27632、慢病毒、高 Wnt WRNE + 10 μM Y-27632
- 为了生成类器官单层,制备玻璃底10孔细胞培养玻片,FBS,胶原IV(1mg / mL在去离子(di)H 2O中),基底膜基质,0.5mM EDTA在1x PBS中,5mM EDTA在1x PBS中,酶解离缓冲液,CMGF-与10%FBS,WRNE + 10μM Y-27632。
- 对于类器官单层的病毒感染,制备胰蛋白酶,轮状病毒原液,CMGF-,25G针头,无菌1x PBS和无酚红分化培养基。
- 要制备无酚红分化培养基,取 500 mL 无酚红细胞培养基,加入 5 mL 100x MEM 非必需氨基酸、5 mL 100x L-谷氨酰胺、5 mL 100 nM 丙酮酸钠和 7.5 mL 1M HEPES。
- 对于类器官的免疫荧光染色,制备4%甲醛(16%甲醛在1x PBS中稀释),Triton X-100(0.1%Triton X-100在1x PBS中),牛血清白蛋白(1x PBS中的3%牛血清白蛋白),NH4Cl溶液(50mM),DAPI(1 μg/ mL DAPI溶液在1x PBS中)。
2. 工程类器官表达基因编码的钙传感器
注意:本方案描述了在24孔板13上转导30μL基底膜基质(BMM)中的单孔3D人肠道类器官的步骤。大多数管线每孔将包含约 400,000 个细胞。应包括第二个非转导孔作为对照。将所有试剂和细胞悬液放在冰上。
- 从最后一次传代2-5天后,从HIO的两个孔中除去维持WRNE培养基。每孔用 300 μL 0.05% 胰蛋白酶-EDTA 代替,轻轻上下移液 5 次以将 BMM 从板上分离。置于37°C培养箱中4分钟。
- 每孔加入 500 μL CMGF- + 10% FBS。通过上下移液 2 次,将 1 mL FBS 上下移液,用 FBS 预涂 1 mL 低结合度移液器吸头。使用预涂层吸头,将 HIO 上下移液 10 次。
- 将每个孔的内容物转移到其自己的预包被的 1.5 mL 微量离心管中。用额外的 500 μL CMGF- 冲洗每个孔,并将洗涤液添加到相应的试管中。
- 在4°C下,在摆动桶离心机中以100× g 离心管5分钟。 除去上清液和任何残留的BMM。
- 重悬于 1 mL 的 1x PBS 中。将每个试管分成两个微量离心管,共 4 个试管。在4°C下以100× g 离心管5分钟。 除去上清液。
- 将每个管在1x PBS中再重悬一次,并在4°C下以100× g 离心5分钟。
- 制备400μL转导培养基和对照培养基(表1)。将 2 个试管重悬于 200 μL 对照培养基中,将 2 个试管重悬于 200 μL 转导培养基中。
- 在37°C细胞培养箱中孵育24小时。通过定期用涂层吸头上下移液(例如,转导后 2 小时 (hpt)、12 hpt、18 hpt)重悬,以促进均匀转导。
- 24小时后,将管在4°C下以100× g 离心5分钟。 除去上清液。
- 将沉淀重悬于500μL 1x PBS中进行洗涤。在4°C下以100× g 离心5分钟。 除去上清液。
- 使用冰冷的 200 μL 移液器吸头,将 4 个沉淀中的每一个重悬于 30 μL BMM 中。轻轻上下移液,使其均匀分散。
- 将每个试管的内容物板板放入24孔板上自己的孔中。在加入500μL HighWnt WRNE + 10μM Y-27632之前,在37°C下孵育10分钟以使BMM固化。
- 让转导的 HIO 生长 1 周,每隔一天刷新培养基 (HighWnt WRNE + 10 μM Y-27632)。1周后,通过显微镜检查荧光指示剂的表达。如果信号很强,就开始选择药物。如果信号较弱,请重复上述转导。
- 建立谱系后,通过激动剂处理验证荧光指示剂的功能。100nM ADP 是用于 GCaMP 验证的可靠激动剂。测试 3D 类器官进行初始验证,如下所述。
- 传代后,在单独的成像底板上将 BMM 中的孔(或多个)类器官铺板。将类器官板化为正常密度的约1/3,以避免成像时过度重叠。激动剂治疗后不要继续传出这些HIO,因为很难确保无菌。
- 等待 2-3 天让 HIO 在通过后恢复。成像前,将培养基切换到不含酚红的分化培养基。
- 使用荧光显微镜,设置3分钟的运行,使用488nm激发和FITC / GFP滤光片组每5秒采集一次图像。成像 30 秒后,添加 100 nM ADP 或载体对照。继续成像,直到信号恢复到接近基线,~2 分钟。ADP 处理后 GCaMP 荧光瞬时增加 ~2 倍表明转导和生物传感器功能成功。为了更精确地估计转导效率,使用通过第 3 部分描述的过程生成的单层重复激动剂测试和成像。
3. 用于实时荧光成像的HIO单层的制备
- 用胶原蛋白IV涂覆10孔成像底室载玻片的所有孔。为此,将 34 μL 1 mg/mL IV 胶原蛋白与 960 μL 无菌去离子水混合。向每个孔中加入95μL稀释的胶原IV溶液,并在37°C孵育0.5-2小时。
- 从 4 个 3D HIO 孔中取出 WRNE 维持培养基。HIO 应在最后一次通过后 5-7 天。
注意:1 个 10 孔板通常需要 ~1.25 x 106 个细胞。这通常需要 2-4 个孔的 3D HIO,每个孔接种在 30 μL BMM 中,但会根据密度而变化。 - 每孔加入 500 μL 1x PBS + 0.5 mM EDTA。使用预涂层的 1 mL 吸头,轻轻上下移液以将 BMM 从板上分离。将悬浮液转移到预涂的 15 mL 锥形管中,将孔状组合到同一管中。
- 用额外的 500 μL PBS + 0.5 mM EDTA 冲洗每个孔。在4°C下以300× g 离心5分钟。 除去上清液和残留的BMM。
- 使用预包被的吸头,将剩余的沉淀重悬于3mL PBS + 5 mM EDTA中(请注意,这比第一次洗涤的EDTA多10倍)。
- 在4°C下以300× g 离心5分钟。 除去上清液和残留的BMM。将沉淀重悬于2 mL酶解离缓冲液中。
- 在37°C珠子/水浴中孵育5分钟。加入 3 mL CMGF- + 10% FBS,轻轻移液混合。
- 在4°C下以300× g 离心5分钟。 除去上清液。加入 1 mL CMGF-。
- 用预涂层吸头 80x-100x 用力上下移液,以机械方式将 HIO 分解成单个细胞。在4°C下以300× g 离心5分钟。 除去上清液。
- 重悬于 1 mL WRNE + 10 μM Y-27632 中。获得 1 mL 悬浮液的细胞计数。
- 用 WRNE + 10μM Y-27632 稀释细胞悬液,以达到 1.25 x 105 个细胞/100 μL (1.25 x 106 个细胞/mL) 的浓度。
- 使用 200 μL 移液管,从步骤 1 中制备的平板中取出胶原蛋白溶液,因为胶原蛋白现已沉降到孔底。避免用移液器吸头接触孔底。
- 使用预包被的200μL移液器吸头,每孔加入步骤3.11(1.25×105 个细胞)中的100μL细胞溶液。
- 在37°C细胞培养箱中孵育24小时。24小时后,从所有孔中除去培养基,并用每孔100μL分化培养基代替。
注意:此时,细胞应粘附在板上。请注意,单层可能不会汇合或完全平面。 - 将载玻片放回37°C细胞培养箱中。每24小时刷新一次分化培养基,直到单层汇合。这通常需要 3-5 天的电镀时间。在此之后,单层产品就可以用于下游应用了。
4. HIO单层病毒感染
- 准备病毒接种物。如有必要,胰蛋白酶激活病毒原液。对于轮状病毒,将10μg/ mL沃辛顿胰蛋白酶加入病毒储备液中,并在37°C下孵育1小时。
- 使用以下两种方法之一稀释活化的病毒原液。
- 如果仅使用一种病毒株获得最大数量的感染细胞,则将 50 μL 活化的病毒储备液与 50 μL CMGF- 混合。
- 如果比较多种菌株,请准备接种物以达到等效的感染多样性 (MOI)。使用以下公式确定所需 MOI 所需的每孔病毒储备量。将CMGF-添加到计算的病毒原液体积中,以达到每孔100μL的最终体积。
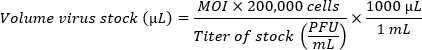
注:在直径为 5.46 mm(96 孔板)的孔中接种的单个 HIO 单层包含约 200,000 个细胞。由于单层感染效率低,因此首选高MOI(每个细胞100-100万个病毒颗粒)。最佳 MOI 必须根据经验确定。
- 使用 200 mL 移液管轻轻去除 HIO 单层培养基,感染单层。用 100 mL 病毒接种物或模拟接种物代替。
- 由于大多数轮状病毒储备在 MA104 细胞中繁殖,因此使用未感染的 MA104 细胞裂解物作为模拟接种物。使用相当于用于感染孔的病毒储备体积的体积,并添加CMGF-,使每孔的最终体积为100 mL。
- 对于基底外侧感染细胞的病毒,例如轮状病毒14,请使用 25G 针头对单层进行刻痕。最容易在单层的长度上,从井的底部到顶部进行一次划痕。轻轻地将针头以斜面朝上的角度压入单层,与运动方向相反,然后将其拖过单层的长度以形成疤痕(图2A)。
- 在37°C培养箱中孵育2小时。去除病毒并模拟接种。用 1x PBS 洗涤单层一次。
- 加入 100 μL 无酚红分化培养基。将载玻片置于37°C培养箱中,直至准备好成像。最佳成像窗口将根据病毒感染的动力学而变化。对于轮状病毒,在感染后 6-8 小时开始成像。
- 使用以下两种方法之一稀释活化的病毒原液。
5. Ca2+ :受感染单层的成像
- 将台顶培养箱预热至37°C。 以 0.02 L/min 的速度运行加湿的 CO2 。将载有受感染单层的载玻片放入培养箱室并密封盖子。
- 使用明场 (BF) 照明和 20 倍物镜,选择要成像的单层内视场的 X 和 Y 坐标。最好选择带有划痕区域的点,因为大多数受感染的细胞将靠近划痕。
- 优化成像参数并使用 488 nm 激发获取图像。为最大限度地减少光毒性,请将光源设置为 50% 功率,曝光时间为 50 毫秒。适当的采集参数可能会有所不同,应通过采集多次采集来优化。确保没有像素饱和。根据需要调整曝光时间和光功率,以确保可以检测到荧光钙传感器的整个动态范围。
- 如果使用其他荧光基团(例如,荧光标记的病毒),请在这些通道上重复优化。设置成像环路,并在 1 分钟环路中在每个选定的 X、Y 坐标处采集 488 nm 图像。连续对此循环进行成像。使用荧光标记病毒时,每 10个 循环(即 1 张图像/10 分钟)在适当的通道上采集图像。
- 收集图像 ~18 小时。如果使用没有荧光标签的病毒,请固定单层并进行免疫荧光染色以识别受感染的细胞。在完成映像运行后执行此操作,如下所述。
- 取出成像介质,并用 100 μL 4% 甲醛的 1x PBS 溶液代替。在室温下孵育 30 分钟。
- 去除固定剂并用100μL50mM NH4Cl淬火10分钟。 除去NH4Cl。 用100μL0.1%Triton X-100在1x PBS中在室温下或在4°C下过夜的单层透化1小时。
- 去除透化缓冲液。用 100 μL 3% 牛血清白蛋白在 1x PBS 中封闭 1 小时。
- 取出封闭溶液。在 1x PBS 中加入稀释至推荐/优化浓度的一抗。每孔加入 100 μL 抗体溶液。
- 在4°C下轻轻摇动孵育过夜。去除一抗。用 1x PBS 洗涤 3 次。
- 加入在 1x PBS 中稀释至推荐/优化浓度的荧光偶联二抗。每孔加入 100 μL。在室温下孵育2小时。
注意:FPBase15 是一个很好的资源,可以帮助选择在多路复用时避免渗漏的次级。大多数次级药物在 1x PBS 中以 1:1000 的稀释度有效。 - 去除二抗。在 1x PBS 中制备 1 μg/mL DAPI 溶液,每孔加入 100 μL。孵育 20 分钟。 去除 DAPI。用 1x PBS 洗涤 3 次。
- 将固定单层保存在 100 μL 1x PBS 中进行成像。将载玻片放回显微镜载物台上,从实时成像运行中重新加载 X 和 Y 坐标,然后对通道上与用于染色的二抗相对应的每个多点进行成像。参考实时成像运行中的图像,以确保捕获相同的点。
6. 细胞间钙波的定量
- 确保 Fiji is Just ImageJ (FIJI) 安装了以下插件:Bio-Formats(应预装在 FIJI 中,但不会安装在 ImageJ 中);说明书:要安装,请从 FIJI 菜单转到“帮助 >更新”>“管理更新站点”。检查 食谱。重新启动斐济。
- 将实时成像运行中的数据文件拆分为多个文件,将每个 X、Y 坐标分隔开来。在Nikon NES Elements中,选择 “文件”>“导入/导出”>“拆分多点”。选择要导出的文件夹和适当的前缀。
- 打开斐济。从拆分的多点加载单个文件。如果使用多通道图像,请拆分通道。选择包含 488 nm 通道 (GCaMP) 图像的窗口。
- 运行 DeltaF Up 函数以确定每个像素值从一个时间点到下一个时间点的变化。为此,请选择“ 说明书”>“T-Functions”>“Delta F Up”。
- 滚动浏览堆栈,直到找到带有钙波的图像。在钙波的视野中,通过单击 图像>调整阈值来设置阈值>。调整下限以最小化不属于波形的信号量,使其超过阈值。对于使用上述参数获取的 16 位图像,请从较低的阈值 600 开始,并根据需要进行调整。
- 运行粒子分析仪,通过单击 “分析”>“分析粒子”来分割波。通过调整范围设置波的最小尺寸(以 μm2 为单位)。它在基线处设置为 0-无穷大。对于使用20倍物镜采集的MA104细胞图像,首先将下限增加到10,000μm2 ,并根据需要进行调整。
- 选中 “显示结果”和 “清除结果”框。从“显示”下拉菜单中,选择“ 大纲”,然后单击 “确定”。这应该会产生 2 个输出:一个窗口“结果”将列出检测到的每个波、波的面积及其平均值、最小强度和最大强度值(基于增量 F)。另一个窗口,标题为 [file name] 的绘图,将包括一个带有分段波浪轮廓的新堆栈。使用它来验证波检测。如果需要,调整阈值和大小范围,并重新检查波次调用。
- 对于批处理,请使用随附的宏脚本(补充编码文件 1)。要利用此功能,请按照下述步骤操作。
- 按照步骤 6.2 中的说明将多点拆分为单个文件。打开斐济。选择 “处理”>“批处理”>宏“。在“输入”框中,提供包含拆分多点文件的文件夹的映射。将“输出”框留空。
- 将 补充编码文件 1 中的脚本粘贴到框中。调整脚本中的强度阈值和大小阈值,以反映步骤 6.5 和 6.6 中的优化参数。
- 单击 “处理”。根据计算机的多点数量和处理速度,处理所有图像可能需要 30 分钟或更长时间。完成后,数据将被写入桌面上名为“写入后重命名我”的新电子表格文件中。输出文件应包含每个多点的波数和波度量(面积、平均强度、最小和最大强度以及强度密度)。
结果
图 1A 显示了包含 3 维人肠道类器官的 BMM 圆顶,这些类器官已被转导以稳定表达 GCaMP6。 图1B 显示了在接种后24、48和72小时重新铺板为单层的相同类器官系。为了验证GCaMP6s的功能,每2秒用荧光显微镜对单层进行成像4分钟,并在~20秒后向培养基中加入100nM ADP。图 1C绘制了每次曝光时在488nm通道上检测到的荧光强度。迹线显示基线荧...
讨论
胞质 Ca2+ 水平的改变可能是上皮内病理的原因和结果 10,16,17。胞质钙的增加可以通过激活钙依赖性氯离子通道直接驱动分泌TMEM16A18,19。响应于 Ca2+ 的 TMEM16A 激活允许氯化物的顶端流出,建立促进液体分泌的渗透梯度20,21。?...
披露声明
作者没有相互竞争的经济利益需要披露。
致谢
这项工作得到了美国国立卫生研究院 (NIH) 的 R01DK115507 和 R01AI158683 (PI: J. M. Hyser) 的资助。受训者支持由 NIH 资助 F30DK131828 (PI: J.T. Gebert)、F31DK132942 (PI: F. J. Scribano) 和 F32DK130288 (PI: K.A. Engevik) 提供。我们要感谢德克萨斯医学中心消化系统疾病肠类核心提供类器官维持培养基。
材料
| Name | Company | Catalog Number | Comments |
| Advanced DMEM F12 | Gibco | 12634028 | |
| [Leu15]-Gastrin I | Sigma-Aldrich | G9145 | |
| 0.05% Trypsin EDTA | Gibco | 25300054 | |
| 0.05% Trypsin EDTA | Gibco | 25300054 | |
| 1.5mL microcentrifuge tubes | Fisherbrand | 5408137 | |
| 15mL conical tubes | Thermofisher Scientific | 0553859A | |
| 16% formaldehyde | Thermofisher Scientific | 28906 | |
| 1M HEPES | Gibco | 15630080 | |
| 1M HEPES | Gibco | 15630080 | |
| 1X PBS | Corning | 21-040-CV | |
| 25 gauge needle | Thermofisher Scientific | 1482113D | |
| A-83-01 | Tocris | 2939 | |
| ADP | Sigma-Aldrich | A2754 | |
| Advanced DMEM F12 | Gibco | 12634028 | |
| Antibiotic-antimycocytic | Gibco | 15240062 | |
| Antibiotic-antimycotic | Gibco | 15240062 | |
| B27 Supplement | Gibco | 17504-044 | |
| Bovine serum albumin | FisherScientific | BP1600100 | |
| CellView Cell Culture Slide, PS, 75/25 MM, Glass Bottom, 10 compartments | Greiner | 543979 | |
| Collagen IV | Sigma Aldrich | C5533 | |
| DAPI | Thermofisher Scientific | D1306 | |
| EDTA | Corning | 46-034-CI | |
| Fetal bovine serum | Corning | 35010CV | |
| Fetal bovine serum | Corning | 35010CV | |
| Fluorobrite | Gibco | A1896701 | |
| GlutaMAX | Gibco | 35050079 | |
| GlutaMAX | Gibco | 35050079 | |
| Human epidermal growth factor | ProteinTech | HZ-1326 | |
| Lentivirus | VectorBuilder | (variable) | |
| Matrigel | BD Biosceicen | 356231/CB40230C | |
| N2 Supplement | Gibco | 17502-048 | |
| N-acetylcysteine | Sigma-Aldrich | A9165-5G | |
| NH4Cl | Sigma-Aldrich | A9434 | |
| Nicotinamide | Sigma-Aldrich | N0636 | |
| Nunc Cell Culture Treated 24-well Plates | Thermofisher Scientific | 142475 | |
| Polybrene | MilliporeSigma | TR1003G | |
| SB202190 | Sigma-Aldrich | S70767 | |
| Triton X-100 | Fisher BioReagents | BP151100 | |
| TrypLE Express Enzyme, no phenol red | Thermofisher Scientific | 12604013 | |
| Trypsin | Worthington Biochemical | NC9811754 | |
| Y-27632 | Tocris | 1254 |
参考文献
- Bootman, M. D., Bultynck, G. Fundamentals of cellular calcium signaling: A primer. Cold Spring Harb Perspect Biol. 12 (1), a038802 (2020).
- Clapham, D. E. Calcium signaling. Cell. 131 (6), 1047-1058 (2007).
- Danese, A., et al. Cell death as a result of calcium signaling modulation: A cancer-centric prospective. Biochim Biophys Acta Mol Cell Res. 1868 (8), 119061 (2021).
- Harr, M. W., Distelhorst, C. W. Apoptosis and autophagy: Decoding calcium signals that mediate life or death. Cold Spring Harb Perspect Biol. 2 (10), a005579 (2010).
- Barak, P., Parekh, A. B. Signaling through Ca2+ microdomains from store-operated CRAC channels. Cold Spring Harb Perspect Biol. 12 (7), a035097 (2020).
- Nakai, J., Ohkura, M., Imoto, K. A high signal-to-noise Ca(2+) probe composed of a single green fluorescent protein. Nat Biotechnol. 19 (2), 137-141 (2001).
- Erofeev, A. I., Vinokurov, E. K., Vlasova, O. L., Bezprozvanny, I. B. GCaMP, a family of single-fluorophore genetically encoded calcium indicators. J Evol Biochem Phys. 59 (4), 1195-1214 (2023).
- Suzuki, J., Kanemaru, K., Iino, M. Genetically encoded fluorescent indicators for organellar calcium imaging. Biophys J. 111 (6), 1119-1131 (2016).
- Nászai, M., Cordero, J. B. Intestinal stem cells: Got calcium. Curr Biol. 26 (3), R117-R119 (2016).
- Barrett, K. E. Calcium-mediated chloride secretion in the intestinal epithelium: Significance and regulation. Curr Top Membr. 53, 257-282 (2002).
- Xu, J., et al. Calcium-sensing receptor regulates intestinal dipeptide absorption via Ca2+ signaling and IKCa activation. Physiol Rep. 8 (1), e14337 (2020).
- Clevers, H. Modeling development and disease with organoids. Cell. 165 (7), 1586-1597 (2016).
- Lin, S. C., Haga, K., Zeng, X. L., Estes, M. K. Generation of CRISPR–Cas9-mediated genetic knockout human intestinal tissue–derived enteroid lines by lentivirus transduction and single-cell cloning. Nat Protoc. 17 (4), 1004-127 (2022).
- Crawford, S. E., Ramani, S., Blutt, S. E., Estes, M. K. Organoids to dissect gastrointestinal virus-host interactions: What have we learned. Viruses. 13 (6), 999 (2021).
- Lambert, T. J. FPbase: a community-editable fluorescent protein database. Nat Methods. 16 (4), 277-278 (2019).
- Lai, Y., et al. Inhibition of calcium-triggered secretion by hydrocarbon-stapled peptides. Nature. 603 (7903), 949-956 (2022).
- Chang-Graham, A. L., et al. Rotavirus induces intercellular calcium waves through ADP signaling. Science. 370 (6519), eabc3621 (2020).
- Lee, B., et al. Anoctamin 1/TMEM16A controls intestinal Cl− secretion induced by carbachol and cholera toxin. Exp Mol Med. 51 (8), 1-14 (2019).
- Saha, T., et al. Intestinal TMEM16A control luminal chloride secretion in a NHERF1 dependent manner. Biochem Biophys Rep. 25, 100912 (2021).
- Mroz, M. S., Keely, S. J. Epidermal growth factor chronically upregulates Ca2+-dependent Cl− conductance and TMEM16A expression in intestinal epithelial cells. J Physiol. 590 (8), 1907-1920 (2012).
- Sui, J., et al. Dual role of Ca2+-activated Cl− channel transmembrane member 16A in lipopolysaccharide-induced intestinal epithelial barrier dysfunction in vitro. Cell Death Dis. 11 (5), 404 (2020).
- Bellono, N. W., et al. Enterochromaffin cells are gut chemosensors that couple to sensory neural pathways. Cell. 170 (1), 185-198.e16 (2017).
- Paradis, T., Bègue, H., Basmaciyan, L., Dalle, F., Bon, F. Tight junctions as a key for pathogens invasion in intestinal epithelial cells. Int J Mol Sci. 22 (5), 2506 (2021).
- Samak, G., et al. Calcium/Ask1/MKK7/JNK2/c-Src signalling cascade mediates disruption of intestinal epithelial tight junctions by dextran sulfate sodium. Biochem J. 465 (3), 503-515 (2015).
- Deng, H., Gerencser, A. A., Jasper, H. Signal integration by Ca2+ regulates intestinal stem cell activity. Nature. 528 (7581), 212-217 (2015).
- Saurav, S., Tanwar, J., Ahuja, K., Motiani, R. K. Dysregulation of host cell calcium signaling during viral infections: Emerging paradigm with high clinical relevance. Mol Aspects Med. 81, 101004 (2021).
- Chang-Graham, A. L., et al. Rotavirus calcium dysregulation manifests as dynamic calcium signaling in the cytoplasm and endoplasmic reticulum. Sci Rep. 9 (1), 10822 (2019).
- Hyser, J. M., Collinson-Pautz, M. R., Utama, B., Estes, M. K. Rotavirus disrupts calcium homeostasis by NSP4 viroporin activity. mBio. 1 (5), e00265-e00310 (2010).
- Pham, T., Perry, J. L., Dosey, T. L., Delcour, A. H., Hyser, J. M. The Rotavirus NSP4 viroporin domain is a calcium-conducting ion channel. Sci Rep. 7, 43487 (2017).
- Crawford, S. E., Hyser, J. M., Utama, B., Estes, M. K. Autophagy hijacked through viroporin-activated calcium/calmodulin-dependent kinase kinase-β signaling is required for rotavirus replication. Proc Natl Acad Sci U S A. 109 (50), E3405-E3413 (2012).
- Crawford, S. E., Criglar, J. M., Liu, Z., Broughman, J. R., Estes, M. K. COPII vesicle transport is required for Rotavirus NSP4 interaction with the autophagy protein LC3 II and trafficking to viroplasms. J Virol. 94 (1), e01341 (2019).
- Pando, V., Iša, P., Arias, C. F., Ló Pez, S. Influence of calcium on the early steps of Rotavirus infection. Virology. 295 (1), 190-200 (2002).
- Hyser, J. M., Estes, M. K. Pathophysiological consequences of calcium-conducting viroporins. Annu Rev Virol. 2 (1), 473-496 (2015).
- Strtak, A. C., et al. Recovirus NS1-2 has viroporin activity that induces aberrant cellular calcium signaling to facilitate virus replication. mSphere. 4 (5), e00506-e00519 (2019).
- In, J. G., Foulke-Abel, J., Clarke, E., Kovbasnjuk, O. Human colonoid monolayers to study interactions between pathogens, commensals, and host intestinal epithelium. J Vis Exp. (146), 59357 (2019).
- Hirota, A., AlMusawi, S., Nateri, A. S., Ordóñez-Morán, P., Imajo, M. Biomaterials for intestinal organoid technology and personalized disease modeling. Acta Biomater. 132, 272-287 (2021).
- Cevallos Porta, D., López, S., Arias, C. F., Isa, P. Polarized rotavirus entry and release from differentiated small intestinal cells. Virology. 499, 65-71 (2016).
- Mirabelli, C., et al. Human Norovirus efficiently replicates in differentiated 3D-human intestinal enteroids. J Virol. 96 (22), e0085522 (2022).
- Icha, J., Weber, M., Waters, J. C., Norden, C. Phototoxicity in live fluorescence microscopy, and how to avoid it. Bioessays. 39 (8), 28749075 (2017).
- Li, J., et al. Engineering of NEMO as calcium indicators with large dynamics and high sensitivity. Nat Methods. 20 (6), 918-924 (2023).
转载和许可
请求许可使用此 JoVE 文章的文本或图形
请求许可探索更多文章
This article has been published
Video Coming Soon
版权所属 © 2025 MyJoVE 公司版权所有,本公司不涉及任何医疗业务和医疗服务。