Se requiere una suscripción a JoVE para ver este contenido. Inicie sesión o comience su prueba gratuita.
Method Article
Obtención de imágenes de calcio en vivo de monocapas de organoides intestinales humanos infectadas por virus utilizando indicadores de calcio codificados genéticamente
En este artículo
Resumen
Este protocolo describe un enfoque para la realización de imágenes de calcio en organoides intestinales humanos infectados por virus y ofrece un enfoque para el análisis.
Resumen
La señalización del calcio es un regulador integral de casi todos los tejidos. Dentro del epitelio intestinal, el calcio está involucrado en la regulación de la actividad secretora, la dinámica de la actina, las respuestas inflamatorias, la proliferación de células madre y muchas otras funciones celulares no caracterizadas. Como tal, el mapeo de la dinámica de señalización del calcio dentro del epitelio intestinal puede proporcionar información sobre los procesos celulares homeostáticos y revelar respuestas únicas a diversos estímulos. Los organoides intestinales humanos (HIO) son un modelo de alto rendimiento derivado del ser humano para estudiar el epitelio intestinal y, por lo tanto, representan un sistema útil para investigar la dinámica del calcio. Este artículo describe un protocolo para transducir de manera estable HIOs con indicadores de calcio codificados genéticamente (GECIs), realizar microscopía de fluorescencia en vivo y analizar datos de imágenes para caracterizar significativamente las señales de calcio. Como ejemplo representativo, las OHIO tridimensionales se transducieron con lentivirus para expresar de forma estable GCaMP6s, una GECI citosólica verde fluorescente basada en proteínas. A continuación, las OHIO modificadas se dispersaron en una suspensión unicelular y se sembraron como monocapas. Después de la diferenciación, las monocapas de HIO se infectaron con rotavirus y/o se trataron con fármacos que se sabe que estimulan una respuesta de calcio. Un microscopio de epifluorescencia equipado con una cámara de imágenes en vivo humidificada y con temperatura controlada permitió obtener imágenes a largo plazo de monocapas infectadas o tratadas con medicamentos. Después de la obtención de imágenes, las imágenes adquiridas se analizaron utilizando el software de análisis disponible gratuitamente, ImageJ. En general, este trabajo establece una línea adaptable para caracterizar la señalización celular en HIO.
Introducción
El calcio es un segundo mensajero ampliamente conservado que desempeña un papel fundamental en laregulación de la fisiología celular. Dada su fuerte carga, su pequeño tamaño y su alta solubilidad en condiciones fisiológicas, el calcio es un manipulador ideal de la conformación de las proteínas. Esto hace que el calcio sea un medio poderoso para transducir señales electroquímicas en alteraciones enzimáticas, transcripcionales o postranscripcionales. Los estrictos gradientes de concentración de calcio a través del retículo endoplásmico (RE) y las membranas plasmáticas crean una alta fuerza impulsora que permite cambios rápidos en la concentración de calcio citosólico. Múltiples mecanismos, incluyendo tanto la amortiguación como el transporte activo, mantienen estrechamente este gradiente. Si bien es necesario para las funciones celulares normales, este mantenimiento es energéticamente costoso, lo que lo hace particularmente susceptible en estados de estrés 2.
Como tal, la desregulación del calcio dentro del citosol es una señal casi universal de muchos tipos de estrés celular. Las alteraciones metabólicas, las toxinas, los patógenos, los daños mecánicos y las perturbaciones genéticas pueden alterar la señalización del calcio. Independientemente del estímulo, a nivel de toda la célula, los aumentos sostenidos e incontrolados del calcio citosólico pueden promover la apoptosis y, finalmente, la necrosis 3,4. Sin embargo, las alteraciones en los niveles citosólicos de calcio de menor amplitud o mayor frecuencia tienen efectos variables2. Del mismo modo, los resultados de las fluctuaciones de calcio pueden diferir en función del microdominio espacial en el que se producen5. Por lo tanto, el monitoreo de los niveles de calcio puede ofrecer información sobre los procesos de señalización dinámica, pero esto requiere un muestreo con una resolución temporal y espacial relativamente alta.
Los indicadores de calcio codificados genéticamente (GECI) son herramientas poderosas para el muestreo continuo en sistemas de células vivas6. Algunos de los GECI más utilizados son las proteínas fluorescentes sensibles al calcio basadas en GFP conocidas como GCaMPs7. El GCaMP canónico es una fusión de tres dominios proteicos distintos: una GFP permutada circularmente (cpGFP), calmodulina y M136. El dominio calmodulina sufre un cambio de conformación al unirse al calcio, lo que permite su interacción con M13. La interacción calmodulina-M13 induce un cambio conformacional en el cpGFP que aumenta su emisión fluorescente tras la excitación. Como tal, un aumento en la concentración de calcio se correlaciona con un aumento en la intensidad de fluorescencia de GCaMP. Estos sensores pueden ser citosólicos o dirigidos a orgánulos específicos8.
Al igual que la mayoría de los tejidos, el calcio regula una variedad de funciones dentro del epitelio gastrointestinal. El epitelio intestinal es fundamental para la absorción de nutrientes y líquidos, pero también debe formar una barrera hermética y una interfaz inmunitaria para evitar la invasión de patógenos o las agresiones tóxicas. Las vías dependientes del calcio influyen en casi todas estas funciones vitales 9,10,11. Sin embargo, la señalización del calcio dentro del epitelio intestinal sigue siendo una frontera poco explorada con un potencial prometedor como diana terapéutica. Si bien el monitoreo de la dinámica del calcio dentro del epitelio intestinal in vivo sigue presentando desafíos, los organoides intestinales humanos (HIO) ofrecen un sistema ex vivo adaptable para la experimentación12. Los HIO son esferoides tridimensionales (3D) derivados de células madre intestinales humanas y, al diferenciarse, recapitulan gran parte de la diversidad celular del epitelio intestinal nativo12.
Este protocolo describe métodos integrales para diseñar HIO que expresan GECI y luego preparar HIO diseñadas como monocapas para la obtención de imágenes de calcio de células vivas. Ofrece la infección viral como ejemplo de una manipulación patológica que interrumpe la señalización del calcio y proporciona un enfoque analítico para cuantificar estos cambios.
Protocolo
Todos los organoides intestinales humanos (HIO) utilizados en este protocolo y los experimentos representativos se derivaron de tejido humano obtenido y mantenido por el Centro Enteroide de Enfermedades Digestivas del Centro Médico de Texas. Todas las muestras se recolectaron de acuerdo con un protocolo aprobado por la Junta de Revisión Institucional de Baylor College of Medicine.
1. Preparación de materiales y reactivos
- Para el mantenimiento de organoides, reúna placas de 24 pocillos tratadas con cultivos celulares, matriz de membrana basal (BMM), tubos cónicos de 15 ml y tubos cónicos de 1,5 ml.
- Para preparar medios completos sin factores de crecimiento (CMGF-), a 500 mL de DMEM F12 avanzado agregue 5 mL de 1M HEPES, 5 mL de antibiótico-antimicótico 100x, 5 mL de suplemento de glutamina 100x.
- Para preparar medios que contengan Wnt, R-espondina y Noggin (WRNE), mezcle partes iguales de medios acondicionados con CMGF y Wnt, agregue medio acondicionado con Noggin, 10 % en volumen, medio acondicionado con R-espondina, 20 % en volumen, 50 ng/ml de factor de crecimiento epidérmico humano, 10 mM de nicotinamida, 10 nM de [Leu15]-gastrina I, 500 nM de A-83-01, 10 μM de SB202190, 1 suplemento de B27, 1 suplemento de N2 y 1 mM de N-acetilcisteína.
- Para la transducción lentiviral, prepare suero fetal bovino (FBS), 0,05% de tripsina-EDTA en solución salina tamponada con fosfato (PBS), CMGF- con 10% de FBS, estéril 1x PBS, polibreno, 10 μM Y-27632, lentivirus, WRNE de alto Wnt + 10 μM Y-27632
- Para generar monocapas de organoides, prepare un portaobjetos de cultivo celular de 10 pocillos con fondo de vidrio, FBS, Colágeno IV (1 mg/mL en (di)H2O desionizado), matriz de membrana basal, EDTA 0,5 mM en 1x PBS, EDTA 5 mM en 1x PBS, tampón de disociación enzimática, CMGF- con FBS al 10%, WRNE + 10 μM Y-27632.
- Para la infección viral de monocapas de organoides, prepare tripsina, caldo de rotavirus, CMGF, aguja 25G, PBS estéril 1x y medios de diferenciación libres de rojo de fenol.
- Para preparar medios de diferenciación sin rojo de fenol, tome 500 ml de medios de cultivo celular sin rojo de fenol, agregue 5 ml de aminoácidos no esenciales MEM 100x, 5 ml de L-glutamina 100x, 5 ml de piruvato de sodio 100 nM y 7,5 ml de HEPES 1M.
- Para la tinción por inmunofluorescencia de organoides, prepare formaldehído al 4 % (formaldehído al 16 % diluido en 1x PBS), Triton X-100 (Triton X-100 al 0,1 % en 1x PBS), albúmina sérica bovina (albúmina sérica bovina al 3 % en 1x PBS), solución de NH4Cl (50 mM), DAPI (solución de DAPI de 1 μg/ml en 1x PBS).
2. Ingeniería de organoides para expresar sensores de calcio codificados genéticamente
NOTA: Este protocolo describe los pasos para transducir un solo pocillo de organoides intestinales humanos tridimensionales sembrados en 30 μL de matriz de membrana basal (BMM) en una placa de 24 pocillos13. La mayoría de las líneas contendrán alrededor de 400.000 células por pocillo. Se debe incluir un segundo pocillo no transducido como control. Mantenga todos los reactivos y suspensiones celulares en hielo.
- Después de 2 a 5 días desde el último paso, retire el medio WRNE de mantenimiento de dos pocillos de HIO. Reemplácelo con 300 μL de tripsina-EDTA al 0,05% por pocillo y pipetee suavemente hacia arriba y hacia abajo 5 veces para separar el BMM de la placa. Colocar en una incubadora a 37 °C durante 4 min.
- Agregue 500 μL de CMGF- + 10% de FBS por pocillo. Recubra previamente una punta de pipeta de baja adherencia de 1 ml con FBS pipeteando 1 ml de FBS hacia arriba y hacia abajo 2 veces. FBS se puede reutilizar en varias puntas. Con la punta prerrevestida, pipetee las OHIO hacia arriba y hacia abajo 10 veces.
- Transfiera el contenido de cada pocillo a su propio tubo de microcentrífuga de 1,5 ml prerrevestido. Enjuague cada pocillo con 500 μL adicionales de CMGF y agregue el lavado al tubo respectivo.
- Centrifugar los tubos a 100 x g en una centrífuga de cubo oscilante durante 5 min a 4 °C. Elimine el sobrenadante y cualquier residuo de BMM.
- Vuelva a suspender en 1 ml de 1x PBS. Divida cada tubo en dos tubos de microcentrífuga para un total de 4 tubos. Centrifugar los tubos a 100 x g durante 5 min a 4 °C. Retire el sobrenadante.
- Vuelva a suspender cada tubo una vez más en 1x PBS y centrifugue a 100 x g durante 5 min a 4 °C.
- Preparar 400 μL de medio de transducción y medio de control (Tabla 1). Resuspender 2 tubos en 200 μL del medio de control y 2 tubos en 200 μL del medio de transducción.
- Incubar en una incubadora de cultivo celular a 37 °C durante 24 h. Vuelva a suspender pipeteando hacia arriba y hacia abajo con una punta recubierta periódicamente (p. ej., 2 h después de la transducción [hpt], 12 hpt, 18 hpt) para fomentar una transducción uniforme.
- Después de 24 h, centrifugue los tubos a 100 x g durante 5 min a 4 °C. Retire el sobrenadante.
- Vuelva a suspender el pellet en 500 μL de 1x PBS para lavar. Centrifugar a 100 x g durante 5 min a 4 °C. Retire el sobrenadante.
- Con una punta de pipeta de 200 μL helada, vuelva a suspender cada uno de los 4 gránulos en 30 μL de BMM. Pipetear suavemente hacia arriba y hacia abajo para dispersar uniformemente.
- Coloque el contenido de cada tubo en su propio pocillo en una placa de 24 pocillos. Incubar durante 10 min a 37 °C para permitir que BMM se solidifique antes de añadir 500 μL de HighWnt WRNE + 10μM Y-27632.
- Deje que las OHIO transducidas crezcan durante 1 semana, actualizando el medio (HighWnt WRNE + 10 μM Y-27632) cada dos días. Después de 1 semana, verifique la expresión del indicador fluorescente por microscopía. Si la señal es fuerte, comience la selección de fármacos. Si la señal es débil, repita la transducción como se ha descrito anteriormente.
- Una vez establecida la línea, verifique la función del indicador de fluorescencia mediante tratamiento con agonistas. El ADP de 100 nM es un agonista fiable para la validación de GCaMP. Pruebe organoides 3D para la validación inicial como se describe a continuación.
- Después de un pasaje, coloque un pocillo (o varios) de organoides en BMM en una placa inferior de imágenes separada. Coloque los organoides en aproximadamente 1/3 de la densidad normal para evitar una superposición excesiva al obtener imágenes. No continúe con estos HIO después del tratamiento con agonistas, ya que es difícil asegurar la esterilidad.
- Espere de 2 a 3 días para que las OHIO se recuperen después del paso. Antes de la obtención de imágenes, cambie el medio a un medio de diferenciación sin rojo de fenol.
- Con un microscopio fluorescente, configure una ejecución de 3 minutos con imágenes adquiridas cada 5 s utilizando una excitación de 488 nm y un juego de filtros FITC/GFP. Después de 30 s de imágenes, agregue 100 nM ADP o control del vehículo. Continúe con la obtención de imágenes hasta que la señal vuelva a la línea de base, ~2 min. Un aumento transitorio de ~2 veces en la fluorescencia de GCaMP con el tratamiento con ADP indica una transducción exitosa y una función del biosensor. Para una estimación más precisa de la eficiencia de la transducción, repita la prueba de agonistas con imágenes utilizando monocapas generadas a través del proceso descrito en la parte 3.
3. Preparación de monocapas HIO para imágenes de fluorescencia en vivo
- Cubra todos los pocillos de un portaobjetos de cámara inferior de 10 pocillos con Colágeno IV. Para ello, mezcle 34 μL de 1 mg/mL de Colágeno IV con 960 μL de agua desionizada estéril. Añadir 95 μL de solución intravenosa de colágeno diluido a cada pocillo e incubar a 37 °C durante 0,5-2 h.
- Retire el medio de mantenimiento WRNE de 4 pocillos de OHIO 3D. Las HIO deben transcurrir entre 5 y 7 días desde su última pasada.
NOTA: 1 placa de 10 pocillos generalmente requiere ~ 1.25 x 106 celdas. Por lo general, esto requiere de 2 a 4 pocillos de HIO 3D recubiertos en 30 μL de BMM cada uno, pero variará según la densidad. - Agregue 500 μL de 1x PBS + 0,5 mM de EDTA por pocillo. Con una punta de 1 ml prerrevestida, pipetee suavemente hacia arriba y hacia abajo para separar el BMM de la placa. Transfiera la suspensión a un tubo cónico de 15 ml prerrevestido, combinando pocillos similares en el mismo tubo.
- Enjuague cada pocillo con 500 μL adicionales de PBS + 0,5 mM de EDTA. Centrifugar a 300 x g durante 5 min a 4 °C. Retire el sobrenadante y el BMM residual.
- Con una punta prerrevestida, vuelva a suspender el gránulo restante en 3 ml de PBS + 5 mM de EDTA (tenga en cuenta que esto es 10 veces más EDTA que el primer lavado).
- Centrifugar a 300 x g durante 5 min a 4 °C. Retire el sobrenadante y el BMM residual. Resuspender el gránulo en 2 mL de tampón de disociación enzimática.
- Incubar en perlas a 37 °C al baño maría durante 5 min. Añadir 3 ml de CMGF- + 10% FBS y pipetear suavemente para mezclar.
- Centrifugar a 300 x g durante 5 min a 4 °C. Retire el sobrenadante. Agregue 1 mL de CMGF-.
- Pipetear vigorosamente hacia arriba y hacia abajo con una punta prerrevestida 80x-100x para romper mecánicamente las OHIO en células individuales. Centrifugar a 300 x g durante 5 min a 4 °C. Retire el sobrenadante.
- Resuspender en 1 mL de WRNE + 10 μM Y-27632. Obtenga un recuento de células para la suspensión de 1 ml.
- Diluir la suspensión celular con WRNE + 10μM Y-27632 para lograr una concentración de 1,25 x 105 células/100 μL (1,25 x 106 células/mL).
- Con una pipeta de 200 μL, retire la solución de colágeno de la placa preparada en el paso 1, ya que el colágeno se ha depositado en el fondo del pocillo. Evite tocar el fondo del pocillo con la punta de la pipeta.
- Con una punta de pipeta de 200 μL prerrevestida, añadir 100 μL de la solución celular del paso 3.11 (1,25 x 105 células) por pocillo.
- Incubar durante 24 h en una incubadora de cultivo celular a 37 °C. Después de 24 h, retire el medio de cultivo de todos los pocillos y reemplácelo con 100 μL de medio de diferenciación por pocillo.
NOTA: En este punto, las células deben estar adheridas a la placa. Tenga en cuenta que es probable que la monocapa no sea confluente o completamente plana. - Vuelva a colocar el portaobjetos en la incubadora de cultivo celular a 37 °C. Refresque el medio de diferenciación cada 24 h hasta que la monocapa sea confluente. Por lo general, esto requiere de 3 a 5 días desde el enchapado. Después de este punto, las monocapas están listas para aplicaciones posteriores.
4. Infección viral de monocapas de HIO
- Prepare el inóculo del virus. Si es necesario, la tripsina activa el stock de virus. En el caso del rotavirus, añadir 10 μg/ml de tripsina de Worthington a las existencias de virus e incubar a 37 °C durante 1 h.
- Diluya el stock de virus activado utilizando uno de los dos métodos siguientes.
- Si se busca el máximo número de células infectadas utilizando una sola cepa viral, mezcle 50 μL del stock viral activado con 50 μL de CMGF-.
- Si se comparan varias cepas, prepare los inóculos para lograr multiplicidades equivalentes de infección (MOI). Utilice la siguiente fórmula para determinar el volumen de existencias de virus por pocillo necesario para el MOI deseado. Agregue CMGF- al volumen de stock de virus calculado para lograr un volumen final de 100 μL por pocillo.
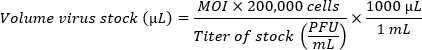
NOTA: Una sola monocapa HIO recubierta en un pocillo con un diámetro de 5,46 mm (placa de 96 pocillos) contiene unas 200.000 células. Debido a la escasa eficiencia de la infección en monocapas, se prefiere un MOI alto (100-1 millón de partículas virales por célula). El MOI óptimo debe determinarse empíricamente.
- Infecte las monocapas retirando suavemente el medio de la monocapa HIO con una pipeta de 200 ml. Reemplace con 100 ml de inóculo de virus o inóculo simulado.
- Dado que la mayoría de las cepas de rotavirus se propagan en células MA104, utilice un lisado de células MA104 no infectadas para el inóculo simulado. Utilice un volumen equivalente al volumen de stock de virus utilizado para los pocillos infectados y agregue CMGF- para un volumen final de 100 ml por pocillo.
- En el caso de los virus que infectan las células por vía basolateral, como el rotavirus14, utilice una aguja de 25G para marcar la monocapa. Es más fácil hacer una sola marca a lo largo de la monocapa, desde la parte inferior hasta la parte superior del pozo. Presione suavemente la aguja en la monocapa en ángulo con el lado biselado hacia arriba, en dirección opuesta al movimiento, y arrástrela a lo largo de la monocapa para crear una cicatriz (Figura 2A).
- Incubar en una incubadora a 37 °C durante 2 h. Eliminar el virus y simular el inóculo. Lave las monocapas una vez con 1x PBS.
- Añadir 100 μL de medio de diferenciación libre de rojo de fenol. Coloque el portaobjetos en una incubadora a 37 °C hasta que esté listo para la obtención de imágenes. La ventana de imagen óptima variará en función de la cinética de la infección viral. En el caso del rotavirus, comience a tomar imágenes a las 6-8 h después de la infección.
- Diluya el stock de virus activado utilizando uno de los dos métodos siguientes.
5. Imágenes de Ca2+ de monocapas infectadas
- Precaliente la incubadora de la parte superior de la etapa a 37 °C. Haga funcionar elCO2 humidificado a 0,02 L/min. Coloque el portaobjetos con las monocapas infectadas en la cámara de la incubadora y selle la tapa.
- Utilizando la iluminación de campo claro (BF) y un objetivo de 20x, seleccione las coordenadas X e Y de los campos de visión dentro de la monocapa de la que se va a obtener la imagen. Lo mejor es seleccionar puntos con la región marcada a la vista, ya que la mayoría de las células infectadas estarán cerca del rasguño.
- Optimice los parámetros de imagen y adquiera una imagen utilizando una excitación de 488 nm. Para minimizar la fototoxicidad, ajuste la fuente de luz al 50% de potencia con un tiempo de exposición de 50 ms. Los parámetros de adquisición apropiados pueden variar y deben optimizarse mediante la adquisición de múltiples adquisiciones. Asegúrese de que no haya píxeles saturados. Ajuste el tiempo de exposición y la potencia de la luz según sea necesario para garantizar que se pueda detectar todo el rango dinámico del sensor de calcio fluorescente.
- Si utiliza otros fluoróforos (por ejemplo, virus marcados con fluorescencia), repita la optimización en estos canales. Configure el bucle de imágenes y adquiera una imagen de 488 nm en cada coordenada X, Y seleccionada en un bucle de 1 minuto. Visualice este bucle continuamente. Cuando utilice un virus marcado con fluorescencia, adquiera una imagen en el canal apropiado cada 10bucles (es decir, 1 imagen/10 minutos).
- Recopile imágenes durante ~ 18 h. Si usa virus sin etiquetas fluorescentes, fije las monocapas y realice la tinción de inmunofluorescencia para identificar las células infectadas. Realice esto después de completar la ejecución de imágenes como se describe a continuación.
- Retire el medio de imagen y reemplácelo con 100 μl de formaldehído al 4 % en 1x PBS. Incubar a temperatura ambiente durante 30 min.
- Retirar el fijador y enfriar con 100 μL de 50mM de NH4Cl durante 10 min. Eliminar NH4Cl. Permeabilizar las monocapas con 100 μL de Triton X-100 al 0,1% en 1x PBS durante 1 h a temperatura ambiente o toda la noche a 4 °C.
- Retire el tampón de permeabilización. Bloquear con 100 μL de albúmina sérica bovina al 3% en 1x PBS durante 1 h.
- Retire la solución de bloqueo. Añadir anticuerpos primarios diluidos a la concentración recomendada/optimizada en 1x PBS. Añadir 100 μL de solución de anticuerpos por pocillo.
- Incubar durante la noche a 4 °C con un suave balanceo. Eliminar los anticuerpos primarios. Lavar 3 veces con 1x PBS.
- Añadir anticuerpos secundarios conjugados con fluorescencia diluidos a la concentración recomendada/optimizada en 1x PBS. Añadir 100 μL por pocillo. Incubar durante 2 h a temperatura ambiente.
NOTA: FPBase15 es un gran recurso para ayudar a seleccionar secundarias que evitarán el sangrado al multiplexar. La mayoría de los secundarios son efectivos a una dilución de 1:1000 en 1x PBS. - Eliminar los anticuerpos secundarios. Prepare una solución DAPI de 1 μg/ml en 1x PBS y agregue 100 μl por pocillo. Incubar durante 20 min. Retire DAPI. Lavar 3 veces con 1x PBS.
- Mantenga monocapas fijas en 100 μL de 1x PBS para la obtención de imágenes. Vuelva a colocar el portaobjetos en la platina del microscopio, vuelva a cargar las coordenadas X e Y de la ejecución de imágenes en vivo y obtenga imágenes de cada multipunto del canal que corresponda al anticuerpo secundario que se utilizó para la tinción. Haga referencia a las imágenes de la ejecución de imágenes en directo para asegurarse de que se capturan los mismos puntos.
6. Cuantificación de las ondas de calcio intercelulares
- Asegúrese de que Fiji is Just ImageJ (FIJI) esté instalado con los siguientes complementos: Bio-Formats (debe estar preinstalado en FIJI pero no estará en ImageJ); Libro de recetas: Para instalarlo, en el menú FIJI, vaya a Ayuda > actualizaciones > Administrar sitios de actualización. Revisa el libro de cocina. Reinicie FIJI.
- Divida el archivo de datos de la ejecución de imágenes en vivo en varios archivos, separando cada coordenada X e Y. En Nikon NES Elements, seleccione Archivo > Importar/Exportar > Dividir multipuntos. Seleccione una carpeta para exportar y un prefijo adecuado.
- Abre FIJI. Cargue un solo archivo desde los multipuntos divididos. Si utiliza una imagen multicanal, divida los canales. Seleccione la ventana con las imágenes del canal de 488 nm (GCaMP).
- Ejecute la función DeltaF Up para determinar el cambio en cada valor de píxel de un punto de tiempo al siguiente. Para ello, seleccione Libro de recetas > funciones T > Delta F Up.
- Desplácese por la pila hasta que encuentre una imagen con una onda de calcio. Con la onda de calcio a la vista, establezca un umbral haciendo clic en Imagen > Ajustar > umbral. Ajuste el límite inferior para minimizar la cantidad de señal que no forma parte de la onda que supera el umbral. Para imágenes de 16 bits adquiridas con los parámetros descritos anteriormente, comience con un umbral inferior de 600 y ajústelo según sea necesario.
- Ejecute el analizador de partículas para segmentar las ondas haciendo clic en Analizar > Analizar partículas. Establezca el tamaño mínimo de la onda en μm2 ajustando el rango. Se establece en 0-infinito en la línea de base. Para las imágenes de células MA104 adquiridas con un objetivo de 20x, comience aumentando el límite inferior a 10.000 μm2 y ajústelo según corresponda.
- Marque las casillas Mostrar resultados y Borrar resultados. En el menú desplegable "Mostrar", selecciona Contornos y, a continuación, haz clic en Aceptar. Esto debería dar como resultado 2 salidas: Una ventana, Resultados, enumerará cada onda detectada, el área de la onda y sus valores de intensidad media, mínima y máxima (basados en delta F). La otra ventana, titulada Dibujo de [nombre del archivo], incluirá una nueva pila con los contornos de las ondas segmentadas. Utilícelo para verificar la detección de ondas. Ajuste los valores de umbral y el rango de tamaño si es necesario, y vuelva a verificar las llamadas de onda.
- Para el procesamiento por lotes, utilice el script de macros incluido (Archivo de codificación suplementario 1). Para utilizar esto, siga los pasos que se describen a continuación.
- Divida los multipuntos en archivos individuales como se describe en el paso 6.2. Abre FIJI. Seleccione Procesar > Lote > Macro. En el cuadro "entrada", proporcione el mapa a la carpeta que contiene los archivos multipunto divididos. Deje el cuadro de "salida" vacío.
- Pegue el script del archivo de codificación suplementario 1 en el cuadro. Ajuste el umbral de intensidad y el umbral de tamaño en el script para reflejar los parámetros optimizados de los pasos 6.5 y 6.6.
- Haga clic en Procesar. Dependiendo del número de multipuntos y de la velocidad de procesamiento del ordenador, el procesamiento de todas las imágenes puede tardar 30 minutos o más. Una vez completados, los datos se escribirán en un nuevo archivo de hoja de cálculo llamado "Cambiar el nombre después de escribir" en el escritorio. El archivo de salida debe contener, para cada multipunto, un recuento de olas y métricas de olas (área, intensidad media, intensidad mínima y máxima y densidad de intensidad).
Resultados
La Figura 1A muestra una cúpula de BMM que contiene organoides intestinales humanos tridimensionales que han sido transducidos para expresar de forma estable GCaMP6s. La Figura 1B muestra la misma línea de organoide resarvida como monocapa a las 24, 48 y 72 h después de la siembra. Para validar la función de GCaMP6s, se obtuvieron imágenes de la monocapa mediante microscopía de fluorescencia cada 2 s durante 4 min, y se añadieron 100 nM de ADP al medio de...
Discusión
Las alteraciones en los niveles citosólicos de Ca2+ pueden ser tanto causa como efecto de patologías dentro del epitelio 10,16,17. Los aumentos en el calcio citosólico pueden impulsar directamente la secreción a través de la activación del canal de cloruro dependiente de calcio TMEM16A18,19. La activación de TMEM16A en respuesta a Ca2+ permit...
Divulgaciones
Los autores no tienen intereses financieros contrapuestos que revelar.
Agradecimientos
Este trabajo fue apoyado por subvenciones R01DK115507 y R01AI158683 (PI: J. M. Hyser) de los Institutos Nacionales de Salud (NIH). El apoyo de los aprendices fue proporcionado por el F30DK131828 de subvenciones de los NIH (PI: J.T. Gebert), F31DK132942 (PI: F. J. Scribano) y F32DK130288 (PI: K.A. Engevik). Nos gustaría agradecer al Centro Enteroide de Enfermedades Digestivas del Centro Médico de Texas por proporcionar los medios de mantenimiento de organoides.
Materiales
| Name | Company | Catalog Number | Comments |
| Advanced DMEM F12 | Gibco | 12634028 | |
| [Leu15]-Gastrin I | Sigma-Aldrich | G9145 | |
| 0.05% Trypsin EDTA | Gibco | 25300054 | |
| 0.05% Trypsin EDTA | Gibco | 25300054 | |
| 1.5mL microcentrifuge tubes | Fisherbrand | 5408137 | |
| 15mL conical tubes | Thermofisher Scientific | 0553859A | |
| 16% formaldehyde | Thermofisher Scientific | 28906 | |
| 1M HEPES | Gibco | 15630080 | |
| 1M HEPES | Gibco | 15630080 | |
| 1X PBS | Corning | 21-040-CV | |
| 25 gauge needle | Thermofisher Scientific | 1482113D | |
| A-83-01 | Tocris | 2939 | |
| ADP | Sigma-Aldrich | A2754 | |
| Advanced DMEM F12 | Gibco | 12634028 | |
| Antibiotic-antimycocytic | Gibco | 15240062 | |
| Antibiotic-antimycotic | Gibco | 15240062 | |
| B27 Supplement | Gibco | 17504-044 | |
| Bovine serum albumin | FisherScientific | BP1600100 | |
| CellView Cell Culture Slide, PS, 75/25 MM, Glass Bottom, 10 compartments | Greiner | 543979 | |
| Collagen IV | Sigma Aldrich | C5533 | |
| DAPI | Thermofisher Scientific | D1306 | |
| EDTA | Corning | 46-034-CI | |
| Fetal bovine serum | Corning | 35010CV | |
| Fetal bovine serum | Corning | 35010CV | |
| Fluorobrite | Gibco | A1896701 | |
| GlutaMAX | Gibco | 35050079 | |
| GlutaMAX | Gibco | 35050079 | |
| Human epidermal growth factor | ProteinTech | HZ-1326 | |
| Lentivirus | VectorBuilder | (variable) | |
| Matrigel | BD Biosceicen | 356231/CB40230C | |
| N2 Supplement | Gibco | 17502-048 | |
| N-acetylcysteine | Sigma-Aldrich | A9165-5G | |
| NH4Cl | Sigma-Aldrich | A9434 | |
| Nicotinamide | Sigma-Aldrich | N0636 | |
| Nunc Cell Culture Treated 24-well Plates | Thermofisher Scientific | 142475 | |
| Polybrene | MilliporeSigma | TR1003G | |
| SB202190 | Sigma-Aldrich | S70767 | |
| Triton X-100 | Fisher BioReagents | BP151100 | |
| TrypLE Express Enzyme, no phenol red | Thermofisher Scientific | 12604013 | |
| Trypsin | Worthington Biochemical | NC9811754 | |
| Y-27632 | Tocris | 1254 |
Referencias
- Bootman, M. D., Bultynck, G. Fundamentals of cellular calcium signaling: A primer. Cold Spring Harb Perspect Biol. 12 (1), a038802 (2020).
- Clapham, D. E. Calcium signaling. Cell. 131 (6), 1047-1058 (2007).
- Danese, A., et al. Cell death as a result of calcium signaling modulation: A cancer-centric prospective. Biochim Biophys Acta Mol Cell Res. 1868 (8), 119061 (2021).
- Harr, M. W., Distelhorst, C. W. Apoptosis and autophagy: Decoding calcium signals that mediate life or death. Cold Spring Harb Perspect Biol. 2 (10), a005579 (2010).
- Barak, P., Parekh, A. B. Signaling through Ca2+ microdomains from store-operated CRAC channels. Cold Spring Harb Perspect Biol. 12 (7), a035097 (2020).
- Nakai, J., Ohkura, M., Imoto, K. A high signal-to-noise Ca(2+) probe composed of a single green fluorescent protein. Nat Biotechnol. 19 (2), 137-141 (2001).
- Erofeev, A. I., Vinokurov, E. K., Vlasova, O. L., Bezprozvanny, I. B. GCaMP, a family of single-fluorophore genetically encoded calcium indicators. J Evol Biochem Phys. 59 (4), 1195-1214 (2023).
- Suzuki, J., Kanemaru, K., Iino, M. Genetically encoded fluorescent indicators for organellar calcium imaging. Biophys J. 111 (6), 1119-1131 (2016).
- Nászai, M., Cordero, J. B. Intestinal stem cells: Got calcium. Curr Biol. 26 (3), R117-R119 (2016).
- Barrett, K. E. Calcium-mediated chloride secretion in the intestinal epithelium: Significance and regulation. Curr Top Membr. 53, 257-282 (2002).
- Xu, J., et al. Calcium-sensing receptor regulates intestinal dipeptide absorption via Ca2+ signaling and IKCa activation. Physiol Rep. 8 (1), e14337 (2020).
- Clevers, H. Modeling development and disease with organoids. Cell. 165 (7), 1586-1597 (2016).
- Lin, S. C., Haga, K., Zeng, X. L., Estes, M. K. Generation of CRISPR–Cas9-mediated genetic knockout human intestinal tissue–derived enteroid lines by lentivirus transduction and single-cell cloning. Nat Protoc. 17 (4), 1004-127 (2022).
- Crawford, S. E., Ramani, S., Blutt, S. E., Estes, M. K. Organoids to dissect gastrointestinal virus-host interactions: What have we learned. Viruses. 13 (6), 999 (2021).
- Lambert, T. J. FPbase: a community-editable fluorescent protein database. Nat Methods. 16 (4), 277-278 (2019).
- Lai, Y., et al. Inhibition of calcium-triggered secretion by hydrocarbon-stapled peptides. Nature. 603 (7903), 949-956 (2022).
- Chang-Graham, A. L., et al. Rotavirus induces intercellular calcium waves through ADP signaling. Science. 370 (6519), eabc3621 (2020).
- Lee, B., et al. Anoctamin 1/TMEM16A controls intestinal Cl− secretion induced by carbachol and cholera toxin. Exp Mol Med. 51 (8), 1-14 (2019).
- Saha, T., et al. Intestinal TMEM16A control luminal chloride secretion in a NHERF1 dependent manner. Biochem Biophys Rep. 25, 100912 (2021).
- Mroz, M. S., Keely, S. J. Epidermal growth factor chronically upregulates Ca2+-dependent Cl− conductance and TMEM16A expression in intestinal epithelial cells. J Physiol. 590 (8), 1907-1920 (2012).
- Sui, J., et al. Dual role of Ca2+-activated Cl− channel transmembrane member 16A in lipopolysaccharide-induced intestinal epithelial barrier dysfunction in vitro. Cell Death Dis. 11 (5), 404 (2020).
- Bellono, N. W., et al. Enterochromaffin cells are gut chemosensors that couple to sensory neural pathways. Cell. 170 (1), 185-198.e16 (2017).
- Paradis, T., Bègue, H., Basmaciyan, L., Dalle, F., Bon, F. Tight junctions as a key for pathogens invasion in intestinal epithelial cells. Int J Mol Sci. 22 (5), 2506 (2021).
- Samak, G., et al. Calcium/Ask1/MKK7/JNK2/c-Src signalling cascade mediates disruption of intestinal epithelial tight junctions by dextran sulfate sodium. Biochem J. 465 (3), 503-515 (2015).
- Deng, H., Gerencser, A. A., Jasper, H. Signal integration by Ca2+ regulates intestinal stem cell activity. Nature. 528 (7581), 212-217 (2015).
- Saurav, S., Tanwar, J., Ahuja, K., Motiani, R. K. Dysregulation of host cell calcium signaling during viral infections: Emerging paradigm with high clinical relevance. Mol Aspects Med. 81, 101004 (2021).
- Chang-Graham, A. L., et al. Rotavirus calcium dysregulation manifests as dynamic calcium signaling in the cytoplasm and endoplasmic reticulum. Sci Rep. 9 (1), 10822 (2019).
- Hyser, J. M., Collinson-Pautz, M. R., Utama, B., Estes, M. K. Rotavirus disrupts calcium homeostasis by NSP4 viroporin activity. mBio. 1 (5), e00265-e00310 (2010).
- Pham, T., Perry, J. L., Dosey, T. L., Delcour, A. H., Hyser, J. M. The Rotavirus NSP4 viroporin domain is a calcium-conducting ion channel. Sci Rep. 7, 43487 (2017).
- Crawford, S. E., Hyser, J. M., Utama, B., Estes, M. K. Autophagy hijacked through viroporin-activated calcium/calmodulin-dependent kinase kinase-β signaling is required for rotavirus replication. Proc Natl Acad Sci U S A. 109 (50), E3405-E3413 (2012).
- Crawford, S. E., Criglar, J. M., Liu, Z., Broughman, J. R., Estes, M. K. COPII vesicle transport is required for Rotavirus NSP4 interaction with the autophagy protein LC3 II and trafficking to viroplasms. J Virol. 94 (1), e01341 (2019).
- Pando, V., Iša, P., Arias, C. F., Ló Pez, S. Influence of calcium on the early steps of Rotavirus infection. Virology. 295 (1), 190-200 (2002).
- Hyser, J. M., Estes, M. K. Pathophysiological consequences of calcium-conducting viroporins. Annu Rev Virol. 2 (1), 473-496 (2015).
- Strtak, A. C., et al. Recovirus NS1-2 has viroporin activity that induces aberrant cellular calcium signaling to facilitate virus replication. mSphere. 4 (5), e00506-e00519 (2019).
- In, J. G., Foulke-Abel, J., Clarke, E., Kovbasnjuk, O. Human colonoid monolayers to study interactions between pathogens, commensals, and host intestinal epithelium. J Vis Exp. (146), 59357 (2019).
- Hirota, A., AlMusawi, S., Nateri, A. S., Ordóñez-Morán, P., Imajo, M. Biomaterials for intestinal organoid technology and personalized disease modeling. Acta Biomater. 132, 272-287 (2021).
- Cevallos Porta, D., López, S., Arias, C. F., Isa, P. Polarized rotavirus entry and release from differentiated small intestinal cells. Virology. 499, 65-71 (2016).
- Mirabelli, C., et al. Human Norovirus efficiently replicates in differentiated 3D-human intestinal enteroids. J Virol. 96 (22), e0085522 (2022).
- Icha, J., Weber, M., Waters, J. C., Norden, C. Phototoxicity in live fluorescence microscopy, and how to avoid it. Bioessays. 39 (8), 28749075 (2017).
- Li, J., et al. Engineering of NEMO as calcium indicators with large dynamics and high sensitivity. Nat Methods. 20 (6), 918-924 (2023).
Reimpresiones y Permisos
Solicitar permiso para reutilizar el texto o las figuras de este JoVE artículos
Solicitar permisoExplorar más artículos
This article has been published
Video Coming Soon
ACERCA DE JoVE
Copyright © 2025 MyJoVE Corporation. Todos los derechos reservados