需要订阅 JoVE 才能查看此. 登录或开始免费试用。
Method Article
通过基于 SV40 的人游离体内易结构 DNA 重复序列的电泳分析进行复制
摘要
在这里,我们概述了使用 2 维凝胶电泳通过致病性、易结构重复分析复制进程的程序。
摘要
二维中性/中性凝胶电泳 (2DGE) 成为分析通过自然障碍进行 DNA 复制的基准技术。该方案描述了如何通过人类细胞中基于猿猴病毒 40 (SV40) 的附加体内易结构、可扩增的 DNA 重复序列分析复制叉进程。简而言之,在质粒转染到人细胞中后,通过改良的 Hirt 方案分离复制中间体,并用 DpnI 限制性内切酶处理以去除未复制的 DNA。然后用适当的限制性内切酶消化中间体,将目标重复序列置于 3-5 kb 长的 DNA 片段的起点远端半部分内。复制中间体分为两个垂直维度,首先按大小,然后按形状。在 Southern 印迹杂交之后,这种方法允许研究人员在复制 Y 弧的下半部分观察到各种结构形成重复的叉停滞。此外,stall 站点的这种定位允许可视化重复介导的 fork stalling 的各种结果,例如分叉反转、收敛分叉的出现和重组分叉重启。
引言
短串联重复序列 (STR) 是小的、通常为 2-9 个碱基对 (bp) 的重复 DNA 序列,约占人类基因组的 3%1。STR 在基因调控中起重要作用2;然而,它们的重复组成使它们容易形成非经典 DNA 二级结构并随后出现遗传不稳定性 3,4。从左旋螺旋到发夹/十字形,再到三链和四链螺旋,这些替代 DNA 结构对复制体造成了内在挑战。二级结构形成的自然先决条件是 DNA 解旋,这是 DNA 复制的先决条件。这给基因组功能带来了一个独特的难题,因为许多这些结构会在复制过程中形成,阻碍复制体的进展,并最终导致复制叉停滞 5,6,7,或者在严重的情况下,导致叉崩溃和 DNA 断裂 8,9。停滞分叉的重新启动和 DNA 修复途径已被证明都会导致重复不稳定性,例如重复扩增10,11 和复杂基因组重排 (CGR) 12,13。这些事件可导致大约 60 种被称为重复扩增障碍的人类疾病的发展,包括脆性 X 综合征、亨廷顿病、弗里德赖希共济失调等14,15 以及 CGR 疾病,如伊曼纽尔综合征16。因此,为了更好地了解重复不稳定性驱动的人类疾病机制,必须研究通过这些重复的复制叉进展的细节。
一种研究复制过程的技术出现在 1980 年代中期,当时 Brewer 和 Fangman 试图提供直接证据,证明 酿酒 酵母的复制起始发生在自主复制序列(通常称为 ARS)元件17。在此过程中,他们分离了琼脂糖中酵母复制中间体的结构,采用了 Bell 和 Byers 的早期方法,称为二维中性/中性凝胶电泳 (2DGE)18。该技术利用了非线性 DNA 在琼脂糖凝胶中的移动方式与相同质量的线性当量不同的事实。更具体地说,在 2DGE 中,分离的 DNA 在两个垂直维度上分离,首先主要按大小分离,然后主要按形状分离,以在特定目标区域创建全面的复制图谱。在他们的原始论文中,Brewer 和 Fangman 将其证明为由"简单 Y"结构或复制叉组成的弧线,将未复制的 DNA 与复制的 DNA 连接起来。他们进一步将其他观察到的中间体描述为 "气泡" 和 "双 Y",分别代表复制起点和收敛分叉。
2DGE 可用于研究给定时间 DNA 复制中间体的相对群体。因此,如果一个中间体群体比另一个群体更普遍,这在可视化时就会很明显。这使得 2DGE 成为通过具有挑战性的序列(如结构形成重复序列)研究复制进程的特别有用的工具。例如,如果分析的区域包含能够诱导复制叉停滞的序列,这将表现为弧上的凸起(图 1A),表明复制叉在该基因座的积累。这可以从酵母中发夹形成重复序列 19,20,21 和人类细胞中三链形成重复序列的复制中看出 22,23,24。除了停滞之外,2DGE 还可用于观察不符合复制过程中形成的标准简单 Y 的 DNA 结构,如重组中间体25。这些中间体具有更重、更支化的 X 形结构,因此在第一维和第二维的移动速度都比标准复制叉慢。在复制叉反转 20,24,26 中也可以观察到类似的结果。为了应对强大的复制应激,真核细胞已被证明可以利用复制叉反转来挽救停滞的叉。这些反向叉子具有与停滞叉子相似的分子量;然而,相对于它们的 Y 形互补体,它们的鸡脚结构导致第二维的电泳迁移率较慢,从而导致电弧向上和向外延伸。
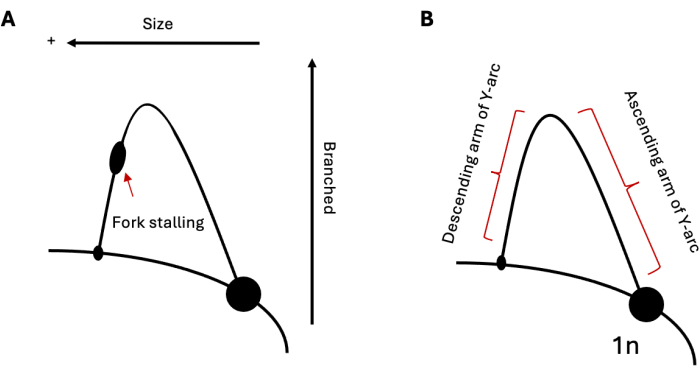
图 1:DNA 复制的 2D 凝胶电泳分析。 (A) 典型 2DGE 的示意图,它通过能够诱导叉停滞的结构形成重复序列进行复制。中等尺寸和结构会影响电泳迁移率。(B) 分别标记了上升臂和下降臂的 Y 轴样本。缩写:2DGE = 二维中性/中性凝胶电泳。 请单击此处查看此图的较大版本。
当然,2DGE 最重要的方面之一涉及复制中间体的质量和数量。然而,对于哺乳动物细胞中内源性基因座复制的 2DGE 分析对于人类基因组中 6 ×10 bp 9 bp 二倍体人类基因组内的单拷贝靶序列是不够的,尽管已经对多拷贝基因进行了解析,例如大量扩增的 DHFR 基因座27 或核糖体 RNA28。基于 SV40 的复制是研究真核细胞复制的一种有效且特征明确的方法29。它提供了一种可靠的真核复制模型,利用大多数宿主复制体机制来复制病毒基因组,病毒基因组在感染后被打包到核小体中 30,31。哺乳动物复制体的两个显著例外是 T 抗原 (Tag) 而不是宿主 CMG 复合物,用作复制 DNA 解旋酶,并且 DNA 聚合酶 delta 合成前导和滞后 DNA 链32。我们利用该系统,将 SV40 复制起点下游的致病性结构形成重复序列放置在最初在 Massimo Lopes 实验室22 中创建的质粒中。重要的是,该质粒还包含编码 Tag 本身的基因,因此在转染到各种培养的人类细胞中时,其产生组成型和极其有效的复制。这一特性产生了大量的产物,非常适合对人类细胞中致病性重复序列复制过程中和响应过程中形成的中间体进行 2DGE 分析。在这里,我们描述了一种使用 2 维凝胶电泳可视化基于 SV40 的人游离体内结构形成重复序列复制的详细方法。
研究方案
注意:为我们在哺乳动物细胞中概述的 2DGE 分析而设计的质粒应包含易结构重复序列上游几 kb 的 SV40 复制起点(图 2)。在选择相对于起始点的方向时,应牢记先导合成和滞后合成,重复序列应克隆到质粒中。

图 2:用于 2DGE 分析的含重复序列质粒的消化。 结构易重复序列描绘在右移动复制叉下游几 kb 处。使用独特的切割器 1 和 2 进行消化会将重复序列放在 Y 弧的下降臂上,因为序列超出了消化片段的中点。缩写:2DGE = 二维中性/中性凝胶电泳。 请单击此处查看此图的较大版本。
1. 质粒转染到哺乳动物细胞中
- 转染前,在 10 cm 组织培养板中接种 600,000 HEK293T 个细胞。让细胞在 37 °C 下恢复过夜。
注:本实验可以使用许多细胞系,但建议使用含有 SV40 标签的细胞以获得最佳结果。注意:HEK293T细胞被视为 BSL-2,所有培养工作都应在生物安全柜中使用适当的无菌技术和适当的 PPE 进行。 - 当细胞达到 60% 汇合度时,根据制造商的方案,使用适当的转染试剂将 8 μg 含重复序列的质粒 DNA 转染到接种的细胞中。
- 如果此时未分离中间体,请吸出旧培养基并在 24 小时后更换为 10 mL 新鲜培养基。
- 转染后 24-48 小时开始收集细胞。
- 吸出培养基并用 10 mL 磷酸盐缓冲盐水 (PBS) 小心洗涤。使用 0.5 mL 胰蛋白酶分离并收集细胞,并以 340 × g 离心 4 分钟。
- 吸出上清液并用 PBS 洗涤细胞沉淀。再次以 340 × g 离心 4 分钟并吸出上清液。
注意:可以通过在 -80 °C 下冷冻细胞沉淀来在此处暂停实验。 我们发现转染后 48 小时分离复制中间体的最佳分辨率;然而,24 h 已经产生了可行的结果。
2. 复制中间体的分离
- 在 50 mL 锥形管中,将细胞重悬于 1.5 mL 改良的 Hirt 裂解缓冲液 [10 mM tris-HCl (pH 7.5)、10 mM 乙二胺四乙酸 (EDTA)] 中,然后开始细胞裂解。
- 添加终浓度为 0.6% 的十二烷基硫酸钠 (SDS)(约 650 μL 2% SDS 储备液)和终浓度为 100 μg/mL(约 10 μL 20 mg/mL 蛋白酶 K 储备液)的蛋白酶 K,以去除核酸酶。
- 通过移液轻轻混合直至均匀,并将混合物在 37 °C 下孵育至少 90 分钟。
- 将 NaCl 浓度增加到 1 M(约 540 μL 5 M NaCl 储备液)并轻轻混合直至均匀。在 4 °C 下孵育过夜(18-24 小时),以便通过盐析沉淀细胞碎片、RNA 和蛋白质。
注意:混合物会非常粘稠,因此在充分混合时要小心并耐心。 - 第二天,将 DNA 与细胞碎片、RNA 和蛋白质分离。
- 将混合物在 4 °C 下以 29,500 × g 离心 45 分钟。
- 转移含有 DNA 的上清液,加入一体积的苯酚:氯仿:异戊醇 25:24:1 (v/v),并短暂混合直至均匀。
注意:苯酚:氯仿:异戊醇是一种有害物质,应在化学通风橱中使用适当的个人防护装备进行处理。 - 在室温下再次以 15,000 × g 离心 5 分钟。将水性层转移到新的锥形管中。
- 沉淀并洗涤分离的 DNA。
- 加入一体积的纯异丙醇,并在室温下孵育至少 5 分钟。在 4 °C 下以 15,000 × g 离心 DNA 30 分钟。
- 倒出上清液,用 70% 冷乙醇洗涤沉淀,以去除多余的盐。
- 在 4 °C 下再次以 15,000 × g 旋转 30 分钟,风干,然后将沉淀轻轻重悬于 Tris-EDTA (TE) 缓冲液(10 mM Tris-HCl,1 mM EDTA)中。
注意:实验可以在此处暂停,样品可以在 -20 °C 下冷冻;但是,应避免冻融循环,因为这会降低 DNA 复制中间体的质量。
3. 样品制备和 2 维凝胶电泳
- 消化质粒复制的分离中间体。
- 向样品中加入 100 单位的适当限制性内切酶以消化质粒 DNA,特异性地将包含重复序列的序列放在线性片段的起点-远端一半上(图 2)。此外,添加 DpnI 以切割甲基化 DNA,从而去除任何在培养的人细胞中未完全复制的质粒 DNA。
注:为获得最佳结果,限制性内切酶应为独特的切割剂,可产生 3-5 kb 片段,将易构建序列置于 Y 弧的下降臂上。 - 将样品在 37 °C 下孵育 6-10 小时,以允许质粒完全消化。
- 用 2.5 体积的冷纯乙醇沉淀 DNA,并在 -20 °C 下孵育过夜,或加入 1 体积的异丙醇并在室温下孵育 5 分钟。
- 将消化和沉淀的样品在 4 °C 下以 15,000 × g 离心 30 分钟。
- 倒出上清液,用 70% 冷乙醇洗涤样品。在 4 °C 下以 15,000 × g 再次旋转 30 分钟。
- 倒出上清液,风干 10 分钟,然后将样品重悬于 15 μL TE 缓冲液中。
- 向样品中加入 100 单位的适当限制性内切酶以消化质粒 DNA,特异性地将包含重复序列的序列放在线性片段的起点-远端一半上(图 2)。此外,添加 DpnI 以切割甲基化 DNA,从而去除任何在培养的人细胞中未完全复制的质粒 DNA。
- 在 1x Tris-硼酸盐-EDTA(TBE)(89 mM tris 碱、89 mM 硼酸、2 mM EDTA)中制备 0.4-0.5% 的第一维琼脂糖凝胶。让溶液凝固至少 1 小时。
- 开始将样本加载到第一维中。
- 将梯子加载到相对于凝胶最左边缘的前 3 cm 内。然后,加载所有准备好的样品,确保每对之间有 3 厘米的距离。
- 将凝胶在 1x TBE 中以 0.85 V/cm 运行19-24 h,以根据其大小分离中间体。确保腔室被覆盖以保护样品避光,否则可能会损坏 DNA。
- 第二天,从缓冲液中取出凝胶,并使用尺子估计消化的线性片段的位置。
- 切除含有分子量标准品的凝胶的前 3 cm,并在含有 0.3 μg/mL 溴化乙锭的 1x TBE 中对凝胶段染色 10-15 分钟。使用凝胶成像系统对分子量标准进行可视化。
- 在估计位置增加 1.3 cm,得到值 a。然后,从值 a 中减去 7.5 cm,得到值 b。将尺子对准第一维凝胶,并在值 a 和 b 处水平切割。然后,垂直切下为每个样品保留的 3 cm 空间。有关可视化原理图,请参阅 图 3 。
- 在新的铸造托盘中,顺时针旋转段并将它们放置在样品孔的位置(图 3)。
- 在 1x TBE 中制备浓度为 1-1.3% 的 0.3 μg/mL 溴化乙锭的第二维琼脂糖凝胶。
- 冷却至约 55 °C 后,将第二维凝胶倒在旋转的第一维段上,并使其固化至少 1 小时。
- 将第二维转移到含有 0.3 μg/mL 溴化乙锭的 1x TBE 的腔室中,并让凝胶平衡至少 30 分钟。
- 再次盖上凝胶,在 4 °C 下以 4.23 V/cm 运行凝胶 9-10 小时,以根据其形状分离中间体。
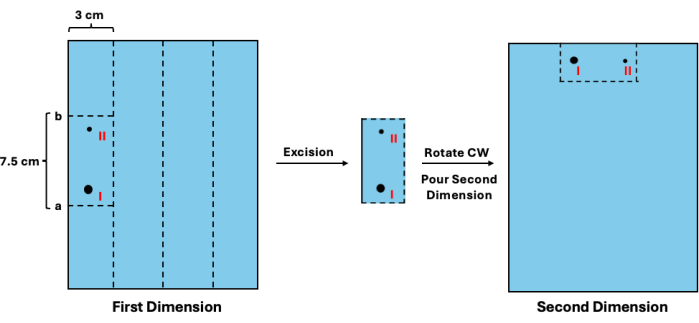
图 3:在第二维分离之前切除第一维中间体。 在阶梯可视化之后,可以估计未复制片段的迁移率。(I) 然后可以使用该值来确定合适的切割位点 (a 和 b) 以切除它及其复制的对应物 (II)。然后应旋转凝胶切片并放置在孔的位置以进行第二维分离。缩写:CW = 顺时针。 请单击此处查看此图的较大版本。
4. Southern 印迹和放射性标记探针杂交
- 从腔室中取出第二维凝胶,并在 0.24 M HCl 溶液中轻轻摇动脱嘌呤 DNA 片段 10 分钟。用去离子水冲洗凝胶,并将其浸泡在 0.4 M NaOH 中 10-15 分钟。
注意:HCl 和 NaOH 具有腐蚀性,应在化学通风橱中使用适当的 PPE 进行处理。 - 开始组装 Southern 印迹,以促进分离的中间体从凝胶转移到膜上。有关全面的原理图,请参阅 图 4 。
- 用 1 L 0.4 M NaOH 填充足够大小的容器。
- 将一块长玻璃片对准容器,并垂直于玻璃片上折叠(沿长度)两张长色谱纸,延伸到 NaOH 容器中。
- 用 NaOH 润湿纸张顶部,并小心去除其表面下的任何气泡。
- 用 NaOH 浸泡三张色谱纸,然后将它们放在折叠的纸上,再次去除任何气泡。
- 将第二维凝胶倒置并将其转移到纸张上。
- 用去离子水润湿带正电荷的尼龙膜(孔径 0.45 μm),然后将其放在凝胶上。
- 最后,在膜上再添加三张用去离子水润湿的纸。
- 用保鲜膜覆盖底部容器中的任何暴露的 NaOH 以防止蒸发。将一叠餐巾纸或纸巾放在印迹上,确保其高度为 0.3-0.5 m。在顶部放置一个重物,压缩整个印迹,以促进紧密的毛细管作用。至少需要 2 天,让 DNA 转移到膜上。
注:色谱纸和膜的长度和宽度取决于用于第二维的琼脂糖凝胶的大小。为了获得最有效的转印效果,请使用与凝胶尺寸相同的纸张和膜。
- 转移后,使用 UV 交联剂以 120 μJ/cm2 的浓度将 DNA 交联到膜上,持续 1 分钟。
注意:通过将膜置于室温下密封、干燥和干净的片材保护器中,可以在此处暂停实验。 - 用 2x 盐水柠檬酸钠(SSC 缓冲液)(0.3 M NaCl,0.03 M 柠檬酸钠)洗涤膜 2 次,每次 5 分钟。
- 在65°C下,用0.18 mL/cm2 的Church & Gilbert杂交缓冲液[1 mM EDTA,1%牛血清白蛋白(BSA),0.5 M磷酸钠,7% SDS]预杂交膜,在杂交培养箱中旋转至少2小时。
注:膜可能会预杂交数天。 - 根据制造商的方案,使用 α-32P dATP 或 dCTP 和 DNA 标记试剂盒制备放射性标记探针。
注意:放射性标记的 dNTP 是危险的,处理它们时应穿戴适当的 PPE。所有放射性工作都应在屏蔽后进行,并且应使用剂量计监测受过培训的人员的辐射吸收情况。- 设计一个与限制性酶切序列互补的 400-900 bp 线性 DNA 片段(图 2),并使用聚合酶链反应 (PCR) 扩增片段。
注:我们建议使用 50-100 ng/μL 的 PCR 储备片段 - 将 100 ng 互补 PCR 片段与 DNA Pol I、Klenow 片段 (3' 5' exo-) 缓冲液和随机十核苷酸寡核苷酸混合。
- 将片段在 100 °C 下变性 10 分钟。
- 向样品中加入 5 单位的 DNA Pol I、Klenow 片段 (3' 5' exo-)、50 μCi 的 α-32P dNTP 和 30-50 μmol 缺乏放射性标记的 dNTP 混合物。
- 在 37 °C 下孵育 10 分钟,以允许聚合和放射性标记的 dNTP 掺入。
- 向样品中加入 30-50 μmol 先前不存在的 dNTP 类型,并在 37 °C 下孵育 10 分钟。
- 使用离心柱以 3,000 × g 纯化放射性标记的片段 2 分钟。
- 设计一个与限制性酶切序列互补的 400-900 bp 线性 DNA 片段(图 2),并使用聚合酶链反应 (PCR) 扩增片段。
- 将放射性标记探针添加到 50 mL 杂交缓冲液中,并在 65 °C 下与膜一起在杂交培养箱中旋转孵育过夜。
- 第二天,取下探针,在42°C下用洗涤缓冲液1(0.1x SSC,0.1%SDS)洗涤膜2次,在65°C下用洗涤缓冲液2(2x SSC,0.1%SDS)洗涤2次。
注意:所有洗涤都应在培养箱中快速旋转 15 分钟。 - 将膜干燥 10 分钟,然后将其放入薄而透明的片材保护膜中。将密封膜储存在带有荧光粉敏感屏幕的受控、抗辐射盒中。让膜暴露在筛网上 1-10 天。
- 使用设置为荧光粉成像的生物分子成像仪可视化结果。必要时清洗并重新暴露。
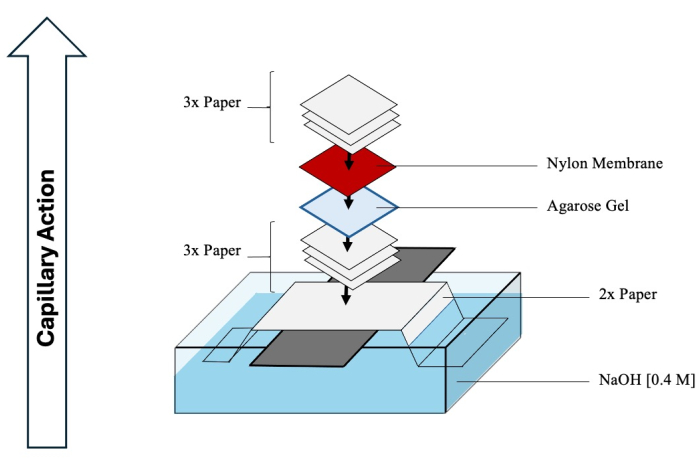
图 4:Southern 印迹的组装。 用于将中间体从第二维 Southern 印迹转移到尼龙膜上的典型装置的综合示意图。 请单击此处查看此图的较大版本。
结果
如果成功,在可视化时,可以观察到复制叉的尖弧从巨大的 1n 点向上和向外延伸(图 5A)。片段的大小或复制的百分比决定了片段在第一维中的移动性。随着中间体发展出更紧密的结构,它们将开始在第二维度中更缓慢地移动。因此,如果中间体在两个维度上都缓慢移动,则可以断言它是一个高度复制的分子,与传统复制叉具有显着的连接变化。?...
讨论
2DGE 提供了特定序列复制过程中出现的中间体相对群体的半定量和综合图像。鉴于在整个过程中必须保持复制叉的脆弱分子结构,因此应非常小心地防止物理剪切和化学变性。因此,强烈建议在质粒分离过程中避免任何碱性处理。为避免这种情况,我们和其他人实施了 Hirt 于 1967 年建立的 Hirt DNA 分离的改良形式33。在这里,通过在 4 °C 下用 1 M NaCl 处理?...
披露声明
作者没有需要披露的利益冲突。
致谢
我们感谢 Jorge Cebrian 和 Anastasia Rastokina 在我们的实验室开始开发这种方法,感谢 Massimo Lopes 为我们提供 pML113 质粒和宝贵的建议,感谢 Ylli Doksani 的深入讨论,以及 Mirkin 实验室成员的支持。Mirkin 实验室的工作得到了美国国家普通医学科学研究所 [R35GM130322] 和 NSF-BSF [2153071] 的支持。
材料
| Name | Company | Catalog Number | Comments |
| 10x TBE Buffer | Bio Rad | 1610733 | |
| 20x SSC Buffer | Fisher Scientific | BP1325-1 | |
| 293T cells | ATCC | CRL-3216 | |
| a-32P dATP, 3000 Ci/mmol | Revvity | BLU512H250UC | |
| Agarose | Fisher Scientific | BP160-500 | |
| Amersham Hybond-N+ | Fisher Scientific | RPN303B | |
| BAS Storage Phosphor Screens | Fisher Scientific | 28956482 | |
| Church and Gibert's hybriddization buffer | Fisher Scientific | 50-103-5408 | |
| DecaLabel DNA labeling kit | ThermoFisher Scientific | K0622 | |
| DMEM, high gluctose, GltaMAX Supplement, pyruvate | ThermoFisher Scientific | 10569010 | |
| DpnI | New England Biolabs | R0176S | Additional restriction enzymes will need to be purchased as well |
| EDTA 0.5 M, pH 8 | Fisher Scientific | BP2482500 | |
| Ethanol, 70% | Fisher Scientific | BP82031GAL | |
| Fetal Bovine Serum | VWR | 97068-085 | |
| Hydrochloric acid solution, 12 M | Millipore Sigma | 13-1683 | |
| Isopropanol | Fisher Scientific | BP26184 | |
| jetPRIME DNA and siRNA Transfection Reagent with Buffer | VWR | 101000027 | |
| MycoZap Plus-CL | VWR | 75870-448 | |
| NaCl | Millipore Sigma | 746398-500G | |
| Nalgene Oak Ridge High-Speed Centrifuge Tubes | ThermoFisher Scientific | 3139-0050 | |
| Phosphate Buffer Saline, pH 7.4 | ThermoFisher Scientific | 10010023 | |
| Phosphate Buffer Saline, pH 7.5 | ThermoFisher Scientific | 10010024 | |
| Proteinase K | ThermoFisher Scientific | EO0491 | |
| Proteinase K | ThermoFisher Scientific | EO0492 | |
| Pure Cellulose Chromatography Paper | Fisher Scientific | 05-714-4 | |
| Pure Cellulose Chromatography Paper | Fisher Scientific | 05-714-5 | |
| Ruler | Fisher Scientific | 09-016 | |
| Scalpel | Fisher Scientific | 12-460-451 | |
| Sodium dodecyl sulfate | Millipore Sigma | 436143-25G | |
| Sodium hydroxide | Fisher Scientific | S25548 | |
| Sorval LYNX 4000 Superspeed Centrifuge | ThermoFisher Scientific | 75006580 | |
| Sub-cell Horizontal Electrophoresis System | Bio Rad | 1704401 | |
| TH13-6 x 50 Swinging Bucket Rotor | ThermoFisher Scientific | 75003010 | |
| Tris-HCl 1 M, pH 7.5 | Fisher Scientific | BP1757-500 | |
| Trypsin-EDTA (0.25%), phenol red | ThermoFisher Scientific | 25200056 |
参考文献
- Liao, X., et al. Repetitive DNA sequence detection and its role in the human genome. Commun Biol. 6 (1), 1-21 (2023).
- Fotsing, S. F., et al. The impact of short tandem repeat variation on gene expression. Nat Genet. 51 (11), 1652-1659 (2019).
- Fan, H., Chu, J. -. Y. A brief review of short tandem repeat mutation. GPB. 5 (1), 7-14 (2007).
- Khristich, A. N., Mirkin, S. M. On the wrong DNA track: Molecular mechanisms of repeat-mediated genome instability. J Biol Chem. 295 (13), 4134-4170 (2020).
- Samadashwily, G. M., Raca, G., Mirkin, S. M. Trinucleotide repeats affect DNA replication in vivo. Nat Genet. 17 (3), 298-304 (1997).
- Khristich, A. N., Armenia, J. F., Matera, R. M., Kolchinski, A. A., Mirkin, S. M. Large-scale contractions of Friedreich's ataxia GAA repeats in yeast occur during DNA replication due to their triplex-forming ability. Proc Natl Acad Sci USA. 117 (3), 1628-1637 (2020).
- Shishkin, A. A., et al. Large-scale expansions of Friedreich's ataxia GAA repeats in yeast. Mol Cell. 35 (1), 82-92 (2009).
- Sundararajan, R., Gellon, L., Zunder, R. M., Freudenreich, C. H. Double-strand break repair pathways protect against CAG/CTG repeat expansions, contractions and repeat-mediated chromosomal fragility in Saccharomyces cerevisiae. Genetics. 184 (1), 65-77 (2010).
- Kim, H. -. M., et al. Chromosome fragility at GAA tracts in yeast depends on repeat orientation and requires mismatch repair. EMBO J. 27 (21), 2896-2906 (2008).
- Polleys, E. J., House, N. C. M., Freudenreich, C. H. Role of recombination and replication fork restart in repeat instability. DNA Repair. 56, 156-165 (2017).
- Gold, M. A., et al. Restarted replication forks are error-prone and cause CAG repeat expansions and contractions. PLoS Genet. 17 (10), e1009863 (2021).
- Lambert, S., et al. Homologous recombination restarts blocked replication forks at the expense of genome rearrangements by template exchange. Mol Cell. 39 (3), 346-359 (2010).
- Burssed, B., Zamariolli, M., Bellucco, F. T., Melaragno, M. I. Mechanisms of structural chromosomal rearrangement formation. Mol Cytogenet. 15 (1), 23 (2022).
- Paulson, H. Repeat expansion diseases. Handb Clin Neurol. 147, 105-123 (2018).
- Malik, I., Kelley, C. P., Wang, E., Todd, P. Molecular mechanisms underlying nucleotide repeat expansion disorders. Nat Rev Mol Cell Biol. 22 (9), 589-607 (2021).
- Emanuel, B. S., Zackai, E. H., Medne, L., Adam, M. P. Emanuel Syndrome. GeneReviews®. , (1993).
- Brewer, B. J., Fangman, W. L. The localization of replication origins on ARS plasmids in S. cerevisiae. Cell. 51 (3), 463-471 (1987).
- Bell, L., Byers, B. Separation of branched from linear DNA by two-dimensional gel electrophoresis. Anal Biochem. 130 (2), 527-535 (1983).
- Voineagu, I., Narayanan, V., Lobachev, K. S., Mirkin, S. M. Replication stalling at unstable inverted repeats: Interplay between DNA hairpins and fork stabilizing proteins. Proc Natl Acad Sci USA. 105 (29), 9936-9941 (2008).
- Nguyen, J. H. G., et al. Differential requirement of Srs2 helicase and Rad51 displacement activities in replication of hairpin-forming CAG/CTG repeats. Nucleic Acids Res. 45 (8), 4519-4531 (2017).
- Krasilnikova, M. M., Mirkin, S. M., Kohwi, Y. Analysis of triplet repeat replication by two-dimensional gel electrophoresis. Trinucleotide Repeat Protocols. , (2004).
- Follonier, C., Oehler, J., Herrador, R., Lopes, M. Friedreich's ataxia-associated GAA repeats induce replication-fork reversal and unusual molecular junctions. Nat Struct Mol Biol. 20 (4), 486-494 (2013).
- Chandok, G. S., Patel, M. P., Mirkin, S. M., Krasilnikova, M. M. Effects of Friedreich's ataxia GAA repeats on DNA replication in mammalian cells. Nucleic Acids Res. 40 (9), 3964-3974 (2012).
- Rastokina, A., et al. Large-scale expansions of Friedreich's ataxia GAA•TTC repeats in an experimental human system: role of DNA replication and prevention by LNA-DNA oligonucleotides and PNA oligomers. Nucleic Acids Res. 51 (16), 8532-8549 (2023).
- Giannattasio, M., et al. Visualization of recombination-mediated damage-bypass by template switching. Nat Struct Mol Biol. 21 (10), 884-892 (2014).
- Hisey, J. A., et al. Pathogenic CANVAS (AAGGG)n repeats stall DNA replication due to the formation of alternative DNA structures. Nucleic Acids Res. 52 (8), 4361-4374 (2024).
- Kalejta, R. F., Lin, H. B., Dijkwel, P. A., Hamlin, J. L. Characterizing replication intermediates in the amplified CHO dihydrofolate reductase domain by two novel gel electrophoretic techniques. Mol Cell Biol. 16 (9), 4923-4931 (1996).
- Little, R. D., Platt, T. H., Schildkraut, C. L. Initiation and termination of DNA replication in human rRNA genes. Mol Cell Biol. 13 (10), 6600-6613 (1993).
- Fanning, E., Zhao, K. SV40 DNA replication: From the A gene to a nanomachine. Virology. 384 (2), 352-359 (2009).
- Sogo, J. M., Stahl, H., Koller, T., Knippers, R. Structure of replicating simian virus 40 minichromosomes: The replication fork, core histone segregation and terminal structures. J Mol Biol. 189 (1), 189-204 (1986).
- Weisshart, K., Taneja, P., Fanning, E. The replication protein A binding site in simian virus 40 (SV40) T antigen and its role in the initial steps of SV40 DNA replication. J Virol. 72 (12), 9771-9781 (1998).
- Sowd, G. A., Fanning, E. A Wolf in sheep's clothing: SV40 co-opts host genome maintenance proteins to replicate viral DNA. PLoS Pathog. 8 (11), e1002994 (2012).
- . BLAST: Basic Local Alignment Search Tool Available from: https://blast.ncbi.nlm.nih.gov/Blast.cgi (2024)
- Hirt, B. Selective extraction of polyoma DNA from infected mouse cell cultures. J Mol Biol. 26 (2), 365-369 (1967).
- Lopes, M., Foiani, M., Sogo, J. M. Multiple mechanisms control chromosome integrity after replication fork uncoupling and restart at irreparable UV lesions. Mol Cell. 21 (1), 15-27 (2006).
转载和许可
请求许可使用此 JoVE 文章的文本或图形
请求许可探索更多文章
This article has been published
Video Coming Soon
版权所属 © 2025 MyJoVE 公司版权所有,本公司不涉及任何医疗业务和医疗服务。