このコンテンツを視聴するには、JoVE 購読が必要です。 サインイン又は無料トライアルを申し込む。
Method Article
SV40ベースのヒトエピソーム内での構造性DNAリピートを介した複製の電気泳動解析
要約
ここでは、2次元ゲル電気泳動を使用して、病原性の構造が取りやすいリピートによる複製進行を解析する手順について概説します。
要約
二次元中性/中性ゲル電気泳動(2DGE)は、自然障害を介したDNA複製を解析するためのベンチマーク技術として登場しました。このプロトコルでは、ヒト細胞内のサルウイルス40(SV40)ベースのエピソーム内で、構造が形成しやすく拡張可能なDNAリピートを介した複製フォークの進行を解析する方法について説明します。簡単に言うと、ヒト細胞へのプラスミドトランスフェクションでは、複製中間体を改良Hirtプロトコルで単離し、DpnI制限酵素で処理して非複製DNAを除去します。次に、中間体を適切な制限酵素によって消化し、目的のリピートを3〜5 kb長のDNAフラグメントの起源-遠位半分内に配置します。複製中間体は、最初にサイズによって、次に形状によって、2つの垂直な次元に分割されます。サザンブロットハイブリダイゼーションに続いて、このアプローチにより、研究者はレプリケーションY弧の下降する半分のさまざまな構造形成リピートでのフォークストールを観察することができます。さらに、このストールサイトの配置により、フォークの反転、収束フォークの出現、リコンビネーションフォークの再起動など、反復媒介フォークストールのさまざまな結果を視覚化できます。
概要
ショートタンデムリピート(STR)は小さく、通常は2〜9塩基対(bp)のDNAの反復配列で、ヒトゲノムの約3%を占めています1。STRは遺伝子調節において重要な役割を果たします2;しかし、それらの反復的な組成は、非標準的なDNA二次構造の形成とそれに続く遺伝的不安定性を引き起こしやすい3,4。左巻きヘリックスからヘアピン/十字形、3本鎖および4本鎖ヘリックスまで、これらの代替DNA構造はレプリソームに固有の課題を引き起こします。二次構造形成の自然な前提条件は、DNA複製の前提条件であるDNAの巻き戻しです。これは、これらの構造の多くが複製中に形成され、レプリソームの進行を妨げ、最終的に複製フォークのストール5,6,7を引き起こし、深刻な場合にはフォークの崩壊とDNAの切断8,9を引き起こす可能性があるため、ゲノム機能にとってユニークな難問を示しています。停止したフォークの再開とDNA修復経路の両方が、反復拡張10,11や複雑ゲノム再構成(CGR)12,13などの反復不安定性につながることが示されています。これらの事象は、脆弱X症候群、ハンチントン病、フリードライヒ運動失調症などを含む反復拡大障害として知られる約60のヒト疾患14,15、およびエマニュエル症候群16などのCGR疾患を発症する可能性があります。したがって、反復不安定性によって引き起こされるヒト疾患のメカニズムをよりよく理解するためには、それらの反復による複製フォーク進行の詳細を研究することが不可欠です。
複製進行を研究する技術は、1980年代半ばにBrewerとFangmanが 、出芽酵母 の複製開始が自律的な複製配列(一般にARSとして知られている)要素17で起こるという直接的な証拠を提供しようとしたときに登場しました。その際、彼らはアガロース中で酵母複製中間体の構造を分離し、2次元中性/中性ゲル電気泳動(2DGE)として知られるBell and Byersの以前の方法を適応させた18。この手法は、非線形DNAがアガロースゲル中を同じ質量の線形同等物とは異なる方法で移動するという事実を利用しました。より具体的には、2DGEでは、単離されたDNAが2つの垂直な次元で分離され、最初は主にサイズによって、次に主に形状によって分離され、特定の関心領域での複製の包括的なマップが作成されます。Brewer氏とFangman氏は、これを「単純なY」構造または複製されていないDNAと複製されたDNAを橋渡しする複製フォークで構成される弧として示しました。さらに、他の観測された中間体を「バブル」と「ダブルY」と表現し、それぞれ複製の起源と収束するフォークを表している。
2DGEは、特定の時間におけるDNA複製中間体の相対的な集団を研究するために使用できます。したがって、中間体の1つの集団が他の集団よりも一般的である場合、これは視覚化すると明らかになります。そのため、2DGEは、構造形成リピートなどの困難な配列による複製進行を研究するのに特に便利なツールとなります。たとえば、分析された領域にレプリケーションフォークのストールを誘発できるシーケンスが含まれている場合、これはアーク上のバルジとして表示され(図1A)、その遺伝子座にレプリケーションフォークが蓄積していることを示します。これは、酵母19,20,21におけるヘアピン形成反復配列およびヒト細胞22,23,24における三重形成反復配列の両方の複製で見ることができる。失速に加えて、2DGEは、組換え中間体25の場合のように、複製中に形成される標準的な単純Ysに適合しないDNA構造を観察するために用いることができる。これらの中間体は、より重く、より分岐したX字型の構造を持っているため、標準的なレプリケーションフォークよりも1次元と2次元の両方でゆっくりと移動します。同様の結果は、レプリケーションフォークの反転20,24,26に関しても観察できます。強い複製ストレスに応答して、真核細胞は複製フォークの反転を利用して停止したフォークを救助することが示されています。これらの逆フォークは、ストールフォークと同様の分子量を持っています。しかし、その鶏足構造は、Y字型の補体に比べて2次元での電気泳動移動度が遅くなり、円弧から伸びます。
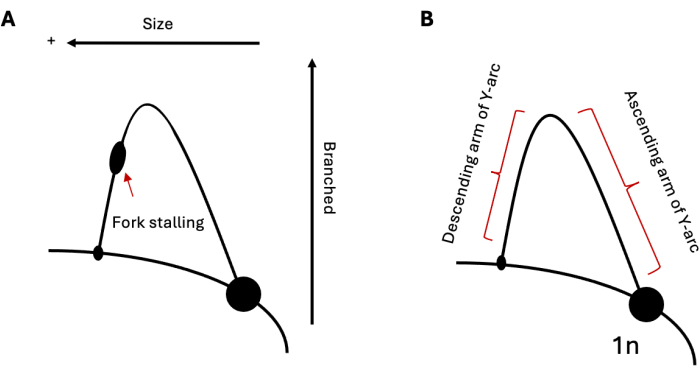
図1:DNA複製の2Dゲル電気泳動解析 (A)フォークストールを誘発できる構造形成リピートを介した複製を示す典型的な2DGEの概略図。中間サイズと構造は、電気泳動の移動性に影響を与えます。(B)上昇アームと下降アームがそれぞれラベル付けされたサンプルYアーク。略語:2DGE = 二次元中性/中性ゲル電気泳動。 この図の拡大版を表示するには、ここをクリックしてください。
当然のことながら、2DGEの最も重要な側面の1つは、複製中間体の質と量に関係しています。しかし、哺乳類細胞における内因性遺伝子座を介した複製の2DGE解析の分解能は、6 × 109 bp二倍体ヒトゲノム内の単一コピー標的配列には不十分であるが、重度に増幅されたDHFR遺伝子座27やリボソームRNA28などのマルチコピー遺伝子に対しては行われている。SV40ベースの複製は、真核細胞における複製を研究するための効率的で十分に特徴付けられた手段である29。これは、感染時にヌクレオソームに分割されるウイルスゲノムを複製するために宿主のレプリソーム機構の大部分を利用する真核生物複製の信頼性の高いモデルを提供する30,31。哺乳類のレプリソームからの2つの注目すべき例外は、宿主CMG複合体の代わりにT抗原(Tag)が複製DNAヘリカーゼとして機能し、DNAポリメラーゼデルタが先行DNA鎖と遅延DNA鎖の両方を合成することである32。このシステムを利用して、Massimo Lopes研究室で最初に作成されたプラスミド内に、SV40の複製起点の下流に病原性の構造形成リピートを配置しました22。重要なことに、このプラスミドにはTag自体をコードする遺伝子も含まれているため、さまざまな培養ヒト細胞へのトランスフェクション時にその構成的で非常に強力な複製がもたらされます。この特徴により、ヒト細胞における病原性反復反応の複製中およびそれに応答して形成される中間体の2DGE分析に最適な大量の製品が生まれます。ここでは、2次元ゲル電気泳動を用いて、SV40ベースのヒトエピソーム内での構造形成リピートの複製を可視化する詳細な方法について説明します。
Access restricted. Please log in or start a trial to view this content.
プロトコル
注:哺乳類細胞における2DGE分析のために設計されたプラスミドは、構造が起こりやすいリピートの数kb上流にSV40の複製起点を含んでいる必要があります(図2)。リード合成と遅延合成は、リピートをプラスミドにクローニングする原点に対する向きを選択する際に留意する必要があります。

図2:2DGE分析のためのリピート含有プラスミドの消化。 構造が不安定なリピートは、右に移動するレプリケーションフォークから数kb下流に描かれています。独自のカッター 1 と 2 による分解では、分解されたフラグメントの中間点を超えるシーケンスが与えられ、リピート シーケンスが Y アークの下降アームに配置されます。略語:2DGE = 二次元中性/中性ゲル電気泳動。 この図の拡大版を表示するには、ここをクリックしてください。
1. 哺乳動物細胞へのプラスミドトランスフェクション
- トランスフェクションの前に、10 cmの組織培養プレートで600,000個のHEK293T細胞を播種します。細胞を37°Cで一晩回復させます。
注:この実験には多くの細胞株を使用できますが、最適な結果を得るにはSV40タグを含む細胞が推奨されます。注意:HEK293T細胞はBSL-2と見なされ、すべての培養作業は、適切な無菌技術と適切なPPEを使用してバイオセーフティキャビネットで実施する必要があります。 - 細胞のコンフルエンシーが60%に達したら、メーカーのプロトコールに従って適切なトランスフェクション試薬を使用して、8 μgのリピート含有プラスミドDNAを播種細胞にトランスフェクションします。
- この時点で中間体を単離していない場合は、古い培地を吸引し、24時間後に10 mLの新鮮な培地と交換します。
- トランスフェクションの24〜48時間後に細胞の収集を開始します。
- 培地を吸引し、10 mLのリン酸緩衝生理食塩水(PBS)で慎重に洗浄します。0.5 mLのトリプシンを使用して細胞を剥離して収集し、340 × g で4分間スピンダウンします。
- 上清を吸引し、細胞ペレットをPBSで洗浄します。再度340 × g で4分間回転させ、上清を吸引します。
注:ここでは、細胞ペレットを-80°Cで凍結することにより、実験を一時停止することができます。 トランスフェクションの48時間後に複製中間体を単離する最良の分解能が見つかりました。しかし、24時間では実行可能な結果が得られています。
2. レプリケーション中間体の単離
- 50 mLコニカルチューブ内の1.5 mLの改変Hirt溶解バッファー[10 mM tris-HCl(pH 7.5)、10 mMエチレンジアミン四酢酸(EDTA)]に細胞を再懸濁し、細胞溶解を開始します。
- ドデシル硫酸ナトリウム(SDS)を最終濃度0.6%(ストック2%SDSの約650μL)まで添加し、プロテイナーゼKを最終濃度100μg/mL(プロテイナーゼKストック20mg/mL約10μL)まで添加してヌクレアーゼを除去します。
- ピペッティングで均質になるまで穏やかに混合し、混合物を37°Cで少なくとも90分間インキュベートします。
- NaCl濃度を1 M(ストック5 M NaClの約540 μL)に増やし、均一になるまで穏やかに混合します。4°Cで一晩(18-24時間)インキュベートし、塩析により細胞破片、RNA、およびタンパク質が沈殿するのを待ちます。
注:混合物は非常に粘性が高いため、よく混合しながら注意して忍耐強くください。 - 翌日、細胞の破片、RNA、およびタンパク質からDNAを分離します。
- 混合物を29,500 × g で45分間、4°Cで遠心分離します。
- DNAを含む上清を移し、フェノール:クロロホルム:イソアミルアルコール25:24:1(v / v)を1容量加え、均一になるまで短時間混合します。
注意:フェノール:クロロホルム:イソアミルアルコールは危険物であり、化学ドラフト内で適切なPPEで取り扱う必要があります。 - 再び15,000 × g で室温で5分間遠心分離します。水性層を新しい円錐管に移します。
- 単離されたDNAを沈殿させて洗浄します。
- 1容量の純粋なイソプロパノールを加え、室温で少なくとも5分間インキュベートします。DNAを15,000 × g で4°Cで30分間スピンダウンします。
- 上清をデカントし、ペレットを冷たい70%エタノールで洗って余分な塩分を取り除きます。
- もう一度 15,000 × g で 4 °C で 30 分間遠心し、風乾させてから、ペレットを Tris-EDTA (TE) バッファー (10 mM Tris-HCl、1 mM EDTA) に穏やかに再懸濁します。
注:実験はここで一時停止でき、サンプルは-20°Cで凍結できます。ただし、凍結融解サイクルはDNA複製中間体の品質を低下させる可能性があるため、避ける必要があります。
3. サンプル調製と2次元ゲル電気泳動
- プラスミド複製の単離された中間体を消化します。
- 適切な制限酵素を100ユニットをサンプルに加えてプラスミドDNAを消化し、特に反復を含む配列を線状フラグメントの起源-遠位半分に配置します(図2)。さらに、DpnIを添加してメチル化DNAを切断し、培養ヒト細胞で完全に複製されなかったプラスミドDNAを除去します。
注:最良の結果を得るためには、制限酵素は、Yアークの下降アーム上に構造が進行しやすい配列を配置する3〜5 kbのフラグメントを生成するユニークなカッターである必要があります。 - サンプルを37°Cで6〜10時間インキュベートして、完全なプラスミド分解を可能にします。
- 2.5容量の冷清純エタノールでDNAを沈殿させ、-20°Cで一晩インキュベートするか、または1容量のイソプロパノールを添加して室温で5分間インキュベートします。
- 分解および沈殿したサンプルを 15,000 × g で 4 °C で 30 分間遠心分離します。
- 上清をデカンタントし、サンプルを冷たい70%エタノールで洗浄します。再度、15,000 × g で4°Cで30分間遠心します。
- 上清をデカンタントし、10分間風乾させてから、サンプルを15 μLのTEバッファーに再懸濁します。
- 適切な制限酵素を100ユニットをサンプルに加えてプラスミドDNAを消化し、特に反復を含む配列を線状フラグメントの起源-遠位半分に配置します(図2)。さらに、DpnIを添加してメチル化DNAを切断し、培養ヒト細胞で完全に複製されなかったプラスミドDNAを除去します。
- 1x トリス-ホウ酸-EDTA(TBE)(89 mMトリス塩基、89 mMホウ酸、2 mM EDTA)で0.4-0.5%の1次元アガロースゲルを調製します。溶液が少なくとも1時間固化するのを待ちます。
- サンプルを 1 次元に読み込み始めます。
- はしごをゲルの左端に対して最初の3cm以内にロードします。次に、準備したサンプル全体をロードし、各ペアの間隔を3cm確保します。
- ゲルを1x TBEで0.85 V/cmで19-24時間泳動し、中間体をそのサイズに対して分離します。DNAに損傷を与える可能性のある光からサンプルを保護するために、チャンバーが覆われていることを確認してください。
- 翌日、ゲルをバッファーから取り出し、定規を使用して消化された線状フラグメントの位置を推定します。
- はしごを含むゲルの最初の3 cmを切除し、0.3 μg/mLの臭化エチジウムを含む1x TBEでゲルセグメントを10〜15分間染色します。ゲルドキュメンテーションシステムを使用してラダーを視覚化します。
- 推定位置に 1.3 cm を加算すると、値 a が得られます。次に、値 aから7.5cmを引くと、値 bが得られます。定規を1次元のゲルに合わせ、 値a と bで水平にカットします。次に、各サンプル用に確保された3cmのスペースを垂直に切り取ります。視覚的な回路図については、 図3 を参照してください。
- 新しいキャスティングトレイで、セグメントを時計回りに回転させ、サンプルウェルの位置に置きます(図3)。
- 2次元アガロースゲルを1x TBE中、0.3 μg/mLのエチジウムブロマイド溶液中で1〜1.3%の濃度で調製します。
- 約55°Cに冷却した後、回転した1次元セグメントに2次元ゲルを注ぎ、少なくとも1時間固化させます。
- 2 次元目を 1x TBE のチャンバーに 0.3 μg/mL のエチジウムブロマイドで移し、ゲルを少なくとも 30 分間平衡化させます。
- 再び蓋をしたゲルを4.23 V/cm、4°Cで9〜10時間泳がせ、中間体をその形状に対して分離します。
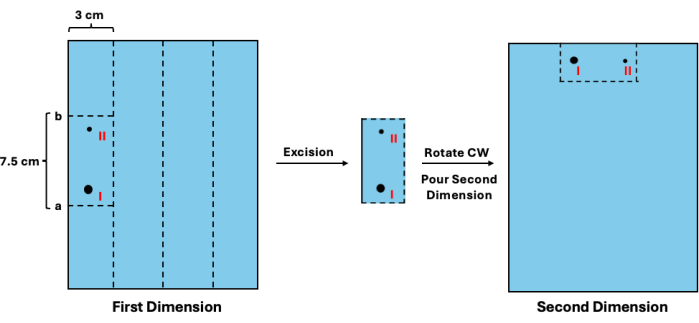
図3:2次元分離前の1次元中間体の切除。 ラダーを可視化した後、複製されていないフラグメントの移動度を推定できます。(I)この値は、それとそれに複製された対応物(II)を切除するための適切なカットサイト(a および b)を決定するために使用できます。次に、ゲルの切片を回転させ、2次元分離のためにウェルの位置に配置する必要があります。略語:CW =時計回り。 この図の拡大版を表示するには、ここをクリックしてください。
4. 放射性標識プローブによるサザンブロッティングとハイブリダイゼーション
- 2次元ゲルをチャンバーから取り出し、0.24 M HCl溶液中でDNA断片を10分間、穏やかに揺さぶって脱精製します。ゲルを脱イオン水ですすぎ、0.4 M NaOHに10〜15分間浸します。
注意:HClとNaOHは腐食性があるため、化学薬品ドラフトで適切なPPEを使用して取り扱う必要があります。 - サザンブロットの組み立てを開始して、分離した中間体をゲルからメンブレンに移すのを容易にします。包括的な回路図については、 図4 を参照してください。
- 十分な大きさの容器に0.4 M NaOHの1 Lを満たします。
- 長いガラスシートを容器全体に整列させ、2枚の長いクロマトグラフィー紙をガラスシートを垂直に折ります(長さに沿って)NaOHの容器に伸びます。
- 紙の上部をNaOHで濡らし、表面の下の気泡を慎重に取り除きます。
- クロマトグラフィーペーパーを3枚NaOHに浸し、折りたたんだペーパーの上に置き、再び気泡を取り除きます。
- 2次元ゲルを逆さまにして、紙の上に転写します。
- 正に帯電したナイロンメンブレン(孔径0.45μm)をDI水で濡らし、ゲルの上に置きます。
- 最後に、DI水で濡らした紙をさらに3枚、メンブレンの上に加えます。
- 底の容器に露出したNaOHをプラスチックラップで覆い、蒸発を防ぎます。ナプキンまたはペーパータオルをブロットの上に重ねて置き、ブロットの高さが0.3〜0.5mであることを確認します。上部に重りを置き、ブロット全体を圧縮して、キャピラリーのタイトな作用を促進します。DNAがメンブレンに移動するまで少なくとも2日かかります。
注:クロマトグラフィーペーパーとメンブレンの長さと幅は、2次元目に使用されるアガロースゲルのサイズによって異なります。最も効率的な転写のためには、ゲルと同じ寸法の紙とメンブレンを使用してください。
- 移載後、UVクロスリンカーを用いて120 μJ/cm2 でDNAをメンブレンに架橋します。
注:実験は、メンブレンを室温で気密性があり、乾燥した清潔なシートプロテクターに置くことにより、ここで一時停止することができます。 - メンブレンを2倍生理食塩水クエン酸ナトリウム(SSCバッファー)(0.3 M NaCl、0.03 Mクエン酸ナトリウム)で5分間2回洗浄します。
- 0.18 mL/cm2 のChurch & Gilbert's hybridization buffer[1 mM EDTA, 1% boly serum albumin (BSA), 0.5 M sodium phosphate, 7% SDS]を65°Cでメンブレンにプレハイブリダイズし、ハイブリダイゼーションインキュベーター内で少なくとも2時間回転させます。
注:メンブレンは数日間プレハイブリダイズすることがあります。 - α-32P dATPまたはdCTPとDNA標識キットを使用して、メーカーのプロトコルに従って放射性標識プローブを調製します。
注意: 放射性標識されたdNTPは危険であり、取り扱うときは適切なPPEを着用する必要があります。すべての放射性作業はシールドの背後で実施されるべきであり、訓練を受けた個人は線量計を使用して放射線の取り込みを監視する必要があります。- 制限酵素消化配列に相補的な400-900 bpの直鎖状DNAフラグメントを設計し(図2)、ポリメラーゼ連鎖反応(PCR)を使用してフラグメントを増幅します。
注:ストックPCRフラグメントを50-100 ng/μLにすることをお勧めします - 100 ngの相補的PCRフラグメントをDNA Pol I、Klenowフラグメント(3' 5' exo-)バッファー、およびランダムデカヌクレオチドオリゴと組み合わせます。
- フラグメントを100°Cで10分間変性させます。
- 5ユニットのDNA Pol I、Klenowフラグメント(3' 5' exo-)、50 μCiのα-32P dNTP、および放射性標識dNTPタイプが欠損した30-50 μmolのdNTPミックスをサンプルに加えます。
- 37°Cで10分間インキュベートし、重合と放射性標識dNTPの取り込みを行います。
- 以前に存在しないdNTPタイプを30〜50 μmolサンプルに加え、37°Cで10分間インキュベートします。
- 放射性標識フラグメントをスピンカラムを用いて3,000 × g で2分間精製します。
- 制限酵素消化配列に相補的な400-900 bpの直鎖状DNAフラグメントを設計し(図2)、ポリメラーゼ連鎖反応(PCR)を使用してフラグメントを増幅します。
- 放射性標識プローブを50 mLのハイブリダイゼーションバッファーに加え、ハイブリダイゼーションインキュベーター内でメンブレンを65°C回転させて一晩インキュベートします。
- 翌日、プローブを取り外し、メンブレンを洗浄バッファー1(0.1x SSC、0.1% SDS)で42°Cで2回、洗浄バッファー2(2x SSC、0.1% SDS)で65°Cで2回洗浄します。
注:すべての洗浄は、インキュベーター内で15分間高速回転で行う必要があります。 - メンブレンを10分間乾燥させ、薄くて透明なシートプロテクターに入れます。密封されたメンブレンは、蛍光体に敏感なスクリーンを備えた制御された耐放射線性カセットに保管します。メンブレンを1〜10日間スクリーンにさらします。
- 蛍光体イメージングに設定された生体分子イメージャーを使用して、結果を可視化します。必要に応じて洗浄し、再度露出させます。
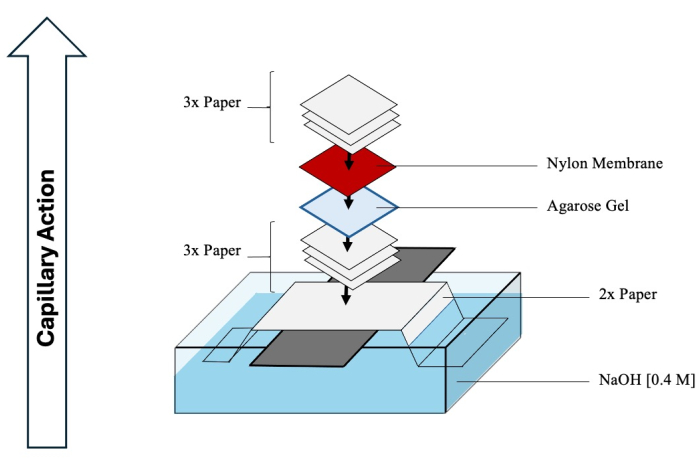
図4:サザンブロットの組み立て。 二次元からナイロン膜への中間体のサザンブロット転写に使用される典型的な装置の包括的な概略図。 この図の拡大版を表示するには、ここをクリックしてください。
Access restricted. Please log in or start a trial to view this content.
結果
成功した場合、視覚化すると、レプリケーションフォークの鋭い弧が巨大な1nスポットから上下に伸びていることが観察できます(図5A)。フラグメントのサイズ、またはレプリケートされる割合によって、最初の次元でのフラグメントの移動性が決まります。中間体がより接合された構造を発達させると、中間体は2次元でよりゆっくりと移動し?...
Access restricted. Please log in or start a trial to view this content.
ディスカッション
2DGEは、特定の配列の複製中に生じる中間体の相対的な集団の半定量的かつ包括的なイメージを提供します。複製フォークの壊れやすい分子構造は、この手順全体を通して維持する必要があることを考えると、物理的なせん断と化学的変性を防ぐために細心の注意を払う必要があります。したがって、プラスミド単離中はアルカリ性処理を避けることを強くお勧めし?...
Access restricted. Please log in or start a trial to view this content.
開示事項
著者には、開示すべき利益相反はありません。
謝辞
私たちの研究室でこのアプローチの開発を始めたJorge Cebrian氏とAnastasia Rastokina氏、pML113プラスミドと貴重なアドバイスを提供してくださったMassimo Lopes氏、洞察に満ちた議論をしてくださったYlli Doksani氏、そしてサポートしてくださったMirkin研究室のメンバーに感謝します。Mirkin研究室での研究は、National Institute of General Medical Sciences[R35GM130322]およびNSF-BSF[2153071]の支援を受けています。
Access restricted. Please log in or start a trial to view this content.
資料
| Name | Company | Catalog Number | Comments |
| 10x TBE Buffer | Bio Rad | 1610733 | |
| 20x SSC Buffer | Fisher Scientific | BP1325-1 | |
| 293T cells | ATCC | CRL-3216 | |
| a-32P dATP, 3000 Ci/mmol | Revvity | BLU512H250UC | |
| Agarose | Fisher Scientific | BP160-500 | |
| Amersham Hybond-N+ | Fisher Scientific | RPN303B | |
| BAS Storage Phosphor Screens | Fisher Scientific | 28956482 | |
| Church and Gibert's hybriddization buffer | Fisher Scientific | 50-103-5408 | |
| DecaLabel DNA labeling kit | ThermoFisher Scientific | K0622 | |
| DMEM, high gluctose, GltaMAX Supplement, pyruvate | ThermoFisher Scientific | 10569010 | |
| DpnI | New England Biolabs | R0176S | Additional restriction enzymes will need to be purchased as well |
| EDTA 0.5 M, pH 8 | Fisher Scientific | BP2482500 | |
| Ethanol, 70% | Fisher Scientific | BP82031GAL | |
| Fetal Bovine Serum | VWR | 97068-085 | |
| Hydrochloric acid solution, 12 M | Millipore Sigma | 13-1683 | |
| Isopropanol | Fisher Scientific | BP26184 | |
| jetPRIME DNA and siRNA Transfection Reagent with Buffer | VWR | 101000027 | |
| MycoZap Plus-CL | VWR | 75870-448 | |
| NaCl | Millipore Sigma | 746398-500G | |
| Nalgene Oak Ridge High-Speed Centrifuge Tubes | ThermoFisher Scientific | 3139-0050 | |
| Phosphate Buffer Saline, pH 7.4 | ThermoFisher Scientific | 10010023 | |
| Phosphate Buffer Saline, pH 7.5 | ThermoFisher Scientific | 10010024 | |
| Proteinase K | ThermoFisher Scientific | EO0491 | |
| Proteinase K | ThermoFisher Scientific | EO0492 | |
| Pure Cellulose Chromatography Paper | Fisher Scientific | 05-714-4 | |
| Pure Cellulose Chromatography Paper | Fisher Scientific | 05-714-5 | |
| Ruler | Fisher Scientific | 09-016 | |
| Scalpel | Fisher Scientific | 12-460-451 | |
| Sodium dodecyl sulfate | Millipore Sigma | 436143-25G | |
| Sodium hydroxide | Fisher Scientific | S25548 | |
| Sorval LYNX 4000 Superspeed Centrifuge | ThermoFisher Scientific | 75006580 | |
| Sub-cell Horizontal Electrophoresis System | Bio Rad | 1704401 | |
| TH13-6 x 50 Swinging Bucket Rotor | ThermoFisher Scientific | 75003010 | |
| Tris-HCl 1 M, pH 7.5 | Fisher Scientific | BP1757-500 | |
| Trypsin-EDTA (0.25%), phenol red | ThermoFisher Scientific | 25200056 |
参考文献
- Liao, X., et al. Repetitive DNA sequence detection and its role in the human genome. Commun Biol. 6 (1), 1-21 (2023).
- Fotsing, S. F., et al. The impact of short tandem repeat variation on gene expression. Nat Genet. 51 (11), 1652-1659 (2019).
- Fan, H., Chu, J. -Y. A brief review of short tandem repeat mutation. GPB. 5 (1), 7-14 (2007).
- Khristich, A. N., Mirkin, S. M. On the wrong DNA track: Molecular mechanisms of repeat-mediated genome instability. J Biol Chem. 295 (13), 4134-4170 (2020).
- Samadashwily, G. M., Raca, G., Mirkin, S. M. Trinucleotide repeats affect DNA replication in vivo. Nat Genet. 17 (3), 298-304 (1997).
- Khristich, A. N., Armenia, J. F., Matera, R. M., Kolchinski, A. A., Mirkin, S. M. Large-scale contractions of Friedreich's ataxia GAA repeats in yeast occur during DNA replication due to their triplex-forming ability. Proc Natl Acad Sci USA. 117 (3), 1628-1637 (2020).
- Shishkin, A. A., et al. Large-scale expansions of Friedreich's ataxia GAA repeats in yeast. Mol Cell. 35 (1), 82-92 (2009).
- Sundararajan, R., Gellon, L., Zunder, R. M., Freudenreich, C. H. Double-strand break repair pathways protect against CAG/CTG repeat expansions, contractions and repeat-mediated chromosomal fragility in Saccharomyces cerevisiae. Genetics. 184 (1), 65-77 (2010).
- Kim, H. -M., et al. Chromosome fragility at GAA tracts in yeast depends on repeat orientation and requires mismatch repair. EMBO J. 27 (21), 2896-2906 (2008).
- Polleys, E. J., House, N. C. M., Freudenreich, C. H. Role of recombination and replication fork restart in repeat instability. DNA Repair. 56, 156-165 (2017).
- Gold, M. A., et al. Restarted replication forks are error-prone and cause CAG repeat expansions and contractions. PLoS Genet. 17 (10), e1009863(2021).
- Lambert, S., et al. Homologous recombination restarts blocked replication forks at the expense of genome rearrangements by template exchange. Mol Cell. 39 (3), 346-359 (2010).
- Burssed, B., Zamariolli, M., Bellucco, F. T., Melaragno, M. I. Mechanisms of structural chromosomal rearrangement formation. Mol Cytogenet. 15 (1), 23(2022).
- Paulson, H. Repeat expansion diseases. Handb Clin Neurol. 147, 105-123 (2018).
- Malik, I., Kelley, C. P., Wang, E., Todd, P. Molecular mechanisms underlying nucleotide repeat expansion disorders. Nat Rev Mol Cell Biol. 22 (9), 589-607 (2021).
- Emanuel, B. S., Zackai, E. H., Medne, L. Emanuel Syndrome. GeneReviews®. Adam, M. P. , University of Washington. Seattle, Seattle, WA. (1993).
- Brewer, B. J., Fangman, W. L. The localization of replication origins on ARS plasmids in S. cerevisiae. Cell. 51 (3), 463-471 (1987).
- Bell, L., Byers, B. Separation of branched from linear DNA by two-dimensional gel electrophoresis. Anal Biochem. 130 (2), 527-535 (1983).
- Voineagu, I., Narayanan, V., Lobachev, K. S., Mirkin, S. M. Replication stalling at unstable inverted repeats: Interplay between DNA hairpins and fork stabilizing proteins. Proc Natl Acad Sci USA. 105 (29), 9936-9941 (2008).
- Nguyen, J. H. G., et al. Differential requirement of Srs2 helicase and Rad51 displacement activities in replication of hairpin-forming CAG/CTG repeats. Nucleic Acids Res. 45 (8), 4519-4531 (2017).
- Krasilnikova, M. M., Mirkin, S. M. Analysis of triplet repeat replication by two-dimensional gel electrophoresis. Trinucleotide Repeat Protocols. Kohwi, Y. , Humana Press. Totowa, NJ. (2004).
- Follonier, C., Oehler, J., Herrador, R., Lopes, M. Friedreich's ataxia-associated GAA repeats induce replication-fork reversal and unusual molecular junctions. Nat Struct Mol Biol. 20 (4), 486-494 (2013).
- Chandok, G. S., Patel, M. P., Mirkin, S. M., Krasilnikova, M. M. Effects of Friedreich's ataxia GAA repeats on DNA replication in mammalian cells. Nucleic Acids Res. 40 (9), 3964-3974 (2012).
- Rastokina, A., et al. Large-scale expansions of Friedreich's ataxia GAA•TTC repeats in an experimental human system: role of DNA replication and prevention by LNA-DNA oligonucleotides and PNA oligomers. Nucleic Acids Res. 51 (16), 8532-8549 (2023).
- Giannattasio, M., et al. Visualization of recombination-mediated damage-bypass by template switching. Nat Struct Mol Biol. 21 (10), 884-892 (2014).
- Hisey, J. A., et al. Pathogenic CANVAS (AAGGG)n repeats stall DNA replication due to the formation of alternative DNA structures. Nucleic Acids Res. 52 (8), 4361-4374 (2024).
- Kalejta, R. F., Lin, H. B., Dijkwel, P. A., Hamlin, J. L. Characterizing replication intermediates in the amplified CHO dihydrofolate reductase domain by two novel gel electrophoretic techniques. Mol Cell Biol. 16 (9), 4923-4931 (1996).
- Little, R. D., Platt, T. H., Schildkraut, C. L. Initiation and termination of DNA replication in human rRNA genes. Mol Cell Biol. 13 (10), 6600-6613 (1993).
- Fanning, E., Zhao, K. SV40 DNA replication: From the A gene to a nanomachine. Virology. 384 (2), 352-359 (2009).
- Sogo, J. M., Stahl, H., Koller, T., Knippers, R. Structure of replicating simian virus 40 minichromosomes: The replication fork, core histone segregation and terminal structures. J Mol Biol. 189 (1), 189-204 (1986).
- Weisshart, K., Taneja, P., Fanning, E. The replication protein A binding site in simian virus 40 (SV40) T antigen and its role in the initial steps of SV40 DNA replication. J Virol. 72 (12), 9771-9781 (1998).
- Sowd, G. A., Fanning, E. A Wolf in sheep's clothing: SV40 co-opts host genome maintenance proteins to replicate viral DNA. PLoS Pathog. 8 (11), e1002994(2012).
- National Library of Medicine: National Center for Biotechnology Information. BLAST: Basic Local Alignment Search Tool. , https://blast.ncbi.nlm.nih.gov/Blast.cgi (2024).
- Hirt, B. Selective extraction of polyoma DNA from infected mouse cell cultures. J Mol Biol. 26 (2), 365-369 (1967).
- Lopes, M., Foiani, M., Sogo, J. M. Multiple mechanisms control chromosome integrity after replication fork uncoupling and restart at irreparable UV lesions. Mol Cell. 21 (1), 15-27 (2006).
Access restricted. Please log in or start a trial to view this content.
転載および許可
このJoVE論文のテキスト又は図を再利用するための許可を申請します
許可を申請さらに記事を探す
This article has been published
Video Coming Soon
Copyright © 2023 MyJoVE Corporation. All rights reserved