Zum Anzeigen dieser Inhalte ist ein JoVE-Abonnement erforderlich. Melden Sie sich an oder starten Sie Ihre kostenlose Testversion.
Method Article
Ein Uniform Shear Assay für menschliche Platelets und Zelloberflächen per Cone-plate Viscometry
In diesem Artikel
Zusammenfassung
Wir beschreiben eine In-Solation-Methode, mit der mittels der Vonenplattenviskometrie einheitliche Schere auf Plattenoberflächen aufgetragen werden kann. Diese Methode kann auch breiter verwendet werden, um Schere auf andere Zelltypen und Zellfragmente aufzutragen und muss nicht auf ein bestimmtes Liga-Rezeptor-Paar zielen.
Zusammenfassung
Viele biologische Zellstoffe spüren die mechanischen Eigenschaften ihrer lokalen Umgebung durch Mechanorezeptoren, Proteine, die auf Kräfte wie Druck oder mechanische Störungen reagieren können. Mechaniker erkennen ihre Reize und übertragen Signale über eine Vielzahl von Mechanismen. Einige der häufigsten Rollen für Mechanorezeptoren sind in neuronalen Reaktionen, wie Berührung und Schmerz, oder Haarzellen, die im Gleichgewicht und Hören funktionieren. Das Mechanosensation ist auch wichtig für Zelltypen, die regelmäßig Scherkelsteinen ausgesetzt sind, wie Endothelzellen, die Blutgefäße säumen, oder Blutkörperchen, die im normalen Kreislauf Schere erleben. Viscometer sind Geräte, die die Viskosität von Flüssigkeiten erkennen. Rotationsviskometer können auch verwendet werden, um eine bekannte Scherkraft auf Flüssigkeiten anzuwenden. Die Fähigkeit dieser Instrumente, eine gleichmäßige Schere zu Flüssigkeiten einzuführen, wurde genutzt, um viele biologische Flüssigkeiten einschließlich Blut und Plasma zu untersuchen. Die Viscometrie kann auch verwendet werden, um die Schere auf die Zellen in einer Lösung aufzutragen und die Wirkung der Schere auf bestimmte Liga-Rezeptor-Paare zu testen. Hier verwenden wir die Visometrie der Kegelplatte, um die Auswirkungen der endogenen Scherkräbellenstress auf die Blutplättchen zu testen, die mit Antikörpern gegen den Plattenmechanosensoren-Rezeptor-Komplex GPIb-IX behandelt werden.
Einleitung
Mechanorezeptoren sind Proteine, die auf mechanische Reize reagieren, wie Druck oder mechanische Störungen/Verformung. Bei einigen Mechanorezeptoren ist das Empfinden dieser mechanischen Störungen explizit für die Funktion der Zelltypen, in denen sie ausgedrückt werden. Nehmen wir zum Beispiel die Stretchrezeptoren in Baroreceptor-Neuronen; Diese mechanoempfindlichen Ionenkanäle regulieren den Blutdruck, indem sie Gefäß-"Dehnung" 1,2wahrnehmen. Im Innenohr erkennen Ionenkanäle an Haarzellen mechanische Verformungen,die durch Schallwellen 3 verursacht werden, und kutane niedrige Schwellenmechanorezeptoren (LTMR) erleichtern die Übertragungvon taktilen Informationen 4. In anderen Fällen liefern Mechanorezeptoren wichtige Informationen an die Zelle für die Herstellung von Haftung oder Wachstum. Zellen können die Starrheit ihrer lokalen Umgebung spüren und können sich auf Kontrahenzkräfte über das Aktin-Zytoskelett und Integrine verlassen, um Wachstum zu diktieren odersichzu verbreiten 5,6.
Bei der Untersuchung von Rezeptor-Ligak-und Wechselwirkungen in Zell-oder Gewebemodellen gibt es gängige Assays, die schnell und präzise die Auswirkungen von Temperaturveränderungen, pH-Wert, Ligakonkonzentration, Tonizität, Membranpotenzial und vielen anderen Parametern melden können. Die in vivo variieren kann. Diese Untersuchungen können jedoch zu kurz kommen, wenn es darum geht, den Beitrag mechanischer Kraft zur Aktivierung des Rezeptors zu erkennen. Ob Zellen ihre Mikroumgebung spüren, Schallwellen erkennen oder auf Dehnung reagieren, eines haben die genannten Mechanorezeptoren gemeinsam, dass sie an Interaktionen teilnehmen, in denen der Ligand, der Rezeptor oder beides zu einem oberfläche. Die zur Untersuchung der Auswirkungen mechanischer Kräfte auf die Interaktionen der Rezeptoren entwickelten Assays spiegeln dieses Paradigma oft wider. Mikrofluidik und Strömungskammern werden verwendet, um die Auswirkungen des Scherflusses auf Zellen und Rezeptoren7,8zu untersuchen. Diese Experimente haben den Vorteil, dass die Scherfrequenz über etablierte Strömungsgeschwindigkeiten verfeinert werden kann. Andere Techniken verwenden fluoreszierende molekulare Sonden, um Kräfte zu erkennen, die von Zellen auf ligandreichen Oberflächen angewendet werden, und ergeben eine genaue Auslesung der Größe und der Orientierung der Kräfte,die an der Interaktion 9,10beteiligtsind.
Neben dem Mechanosensation, bei dem ein oder beide Partner an einer Oberfläche verankert sind, kann Scherspannung Proteine und Zellen in der Lösung beeinflussen. Dies wird oft bei Blutzellenproteinen beobachtet, die sich ständig im Kreislauf befinden, und kann sich durch die Aktivierung von Mechanorezeptoren manifestieren, die normalerweise 11 überlagert sind, oder durch die Exposition von Zielsequenzen, die unter Statische Bedingungen12. Allerdings wird die Wirkung der Scherkraft auf die Partikel in der Lösung relativ weniger Techniken untersucht. Einige in der Lösung befindliche Ansätze führen Schere über Wirbelzellen in Flüssigkeitsaufhängung mit unterschiedlichen Geschwindigkeiten und Längen ein, obwohl diese Ansätze möglicherweise keine sehr genaue Bestimmung der erzeugten Scherspannung erlauben. Rotationsviskometer messen die Viskosität, indem sie eine bestimmte Scherkraft auf Flüssigkeiten anwenden. Hierin beschreiben wir eine angewandte Methode zur Bestimmung der Wirkung bestimmter laminarer Schere auf Zellen oder Zellfragmente in der Lösung.
Eines der am stärksten ausgedrückten Proteine auf der Plattenoberfläche ist der Glykoprotein (GP) Ib-IX-Komplex. GPIb-IX ist der primäre Rezeptor für das Plasma-Protein von Willebrand Factor (VWF). Zusammen ist dieses Rezeptor-Ligandpaar längst als Fundament der Plattenreaktion auf Scherspannung13anerkannt. Im Falle von Gefäßschäden bindet der VWF in der subendothelialen Matrix14exponierte Kollagen und rekrutiert so über die VWF-GPIb-IX-Interaktion Blutplättchen an den Verletzungsort. VWF-Engagement an seiner Bindungsstelle in der GPIbα Untereinheit, wenn GPIb-IX unter physiologischer Schere Stress die Entfaltung einer Membran-proximalen mechanosensorischen Domäne (MSD) bewirkt, die wiederum GPIb-IX15aktiviert. In einer aktuellen Studie haben wir gezeigt, dass Antikörper gegen GPIbα, wie sie bei vielen Immunthrombozytopenie-Patienten (ITP) erzeugt werden, auch in der Lage sind, Blutplättenssignale über MSD zu induzieren,die sich unter Scherstress 11 entfaltet. Im Gegensatz zu VWF, das die Shear-induzierte GPIb-IX-Aktivierung erleichtert, indem der Komplex unter normaler Zirkulation immobilisiert wird, sind die bivalenten Antikörper jedoch in der Lage, die Platelets über GPIb-IX zu kreuzen und die MSD im Umlauf zu entfalten. Auf diese Weise kann ein Mechanorektor, der normalerweise durch Oberflächen-Immobilisierung unter Schere aktiviert wird, in Lösung aktiviert werden. Im vorliegenden Bericht werden wir zeigen, wie ein viskometerbasierter einheitlicher Scherenuntersuchung verwendet wurde, um die Auswirkungen bestimmter Scherkräterbelastungen auf die Rezeptor-Aktivierung in der Lösung zu erkennen.
Protokoll
Alle Methoden, die von Spendern abgeleitete menschliche Blutplättchen verwenden, wurden vom Institutional Review Board der Emory University/Children es Healthcare of Atlanta genehmigt.
1. Blutverlosung und Platzverungrank-Isolation
- Ziehen Sie menschliches Blut von einvernehmlichen gesunden erwachsenen Spendern über Venipunktion am Tag des Experiments in 3,8% Trisodium Citrate. Ein 4,5 mL Blutrohr reicht aus, um genügend plateletreiches Plasma (PRP) für 20-25 Bedingungen bei Spendern zu liefern, deren Plattenzählungen bei fast 250 x 103 pro μL liegen.
Hinweis: Vermeiden Sie es, Blut über Schmalspurnadeln zu ziehen (kleiner als 21 G). - Bereiten Sie PRP über Zentrifugation bei 22 ° C und 140 x g für 12 min mit einer langen Bremse vor. Dies führt zu zwei verschiedenen Schichten, mit roten Blutkörperchen unten und dem hellfarbenen PRP an der Spitze.
- Isolieren Sie die obere, wolkige, gelbe Schicht von PRP durch sorgfältiges Pipettieren durch eine Pipette-Spitze, die in einem 45 °-Winkel geschnitten wird, und erhalten Sie die Plattenzählung über ein komplettes Blutbild (CBC).
- Bei Bedarf in der Anwesenheit von Prostaglandin E1 (PGE1) die Platten in PIPES-gepufferter Saline (150 mM NaCl, 20 mM PIPES) waschen und im Tirode-Puffer wiederbeleben (134 mM NaCl, 0.34 mM Na2HPO4, 2,9 mM KCl, 1 mM MgCl2,5mM Glukose, 12 mM NaHCO 3,20mM HEPES, pH 7.35) mit 5 mM Glukose, ansonsten auf Schritt 1,5. Die folgenden Schritte beschreiben das Waschen kurz.
- Passen Sie das PRP-Volumen auf 10 mL mit PIPES-gepufferter Saline an und fügen Sie 0,6 μM PGE1 hinzu.
- Zentrifuge für 8 min bei 1.900 x g,dann abwerfen supernatant und lassen Sie das Plattenpellet in 400 μL von Tyrode es und Glukose-Lösung für 5 min sitzen.
- Das Platelet Pellet vorsichtig wiederbeleben und 30 Minuten ungestört halten.
- Stellen Sie die Platte auf ca. 250 x 103 Platten pro μL mit gebündeltem, platelettarmem Plasma (PPP) ein und halten Sie die Aufhängung bei 22 ° C ungestört oder unter sanfter Rotation.
2. Ligand-und einheitliche Scherbehandlung
Achtung: Alle Schritte in Abschnitt 2, die Pipettieren erfordern, sollten langsam durchgeführt werden, um keine Schere einzuführen.
- Den gewünschten Antikörper oder Ligand in den PRP oder gewaschene Blutplättchen geben und vorsichtig vermischen, indem man auf-und abkneift oder mit einer Pipette-Spitze rühren. Lassen Sie es bei Raumtemperatur für 5-10 min ungestört.
- Schalten Sie den Von-Platte-Viskometer ein, stellen Sie die Platte auf 22 ° C und lassen Sie sich Zeit, um die Platte diese Temperatur erreichen zu lassen.
- Die behandelte PRP oder gewaschene Blutplättchen direkt in der Mitte der Platte auf den temperaturgesteuerten Kegelplatten-Viskometer piptieren. Stellen Sie sicher, dass die gesamte Probe zwischen Kegel und Platte an der Stelle des Kontakts abgelagert wird, und nicht auf der Außenseite des Kegels.
- In angemessener Geschwindigkeit und Dauer erklingen die Ohren.
- Berechnen Sie die Schere, wie sie im Viscometer-Handbuch angegeben ist,oder wie zuvor 15,16gezeigt.
- Bestimmen Sie die Schere von der Viskosität und der gewünschten Schear-Stress durch Newtons Viskositätsgesetz;
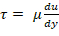 ; Die Plasma-Viskosität beträgt 1,5-1,6 centipoise (cP)17. Zum Beispiel ist ein normaler Scherbereich für den menschlichen Kreislauf 5-30 dyn/cm 2 und die Schere sollte auf der einstelligen Minutenzeit aufgetragen werden.
; Die Plasma-Viskosität beträgt 1,5-1,6 centipoise (cP)17. Zum Beispiel ist ein normaler Scherbereich für den menschlichen Kreislauf 5-30 dyn/cm 2 und die Schere sollte auf der einstelligen Minutenzeit aufgetragen werden.
- Heben Sie den Kegel der Platte leichter (~ 2 mm), so dass die Probe in Kontakt mit der Platte und Kegel bleibt, und verwenden Sie eine Gel-Loadung oder eine andere lange Pipette-Spitze, um 5-10 μL aus der Mitte des Probenvolumens zu sammeln.
- Die geschirmen Proben mit den gewünschten Markierungen 20 min bei Raumtemperatur einweichen. Für Phosphatidylserine, β-Galactose-und P-Selectin-Belichtung verwenden die Lactadherin C2-Domäne (LactC2) bei 0,08 μM 18, Erythrina cristagalli lectin (ECL) bei 6,25 μg/mL und Anti-P-selectin Antikörper (20 μg/mL).
- Fixieren Sie Proben in 2% Paraformaldehyd für 20 Minuten bei RT vor der Verdünnung oder Kühllagerung, und gehen Sie zu Schritt 3.1 oder speichern Sie Proben bei 4 ° C für nicht länger als 12 Stunden.
3. Erkennung von Oberflächenmarkierungen und Vernetzung über Strömungszytometrie
- Analysieren Sie die Probe über die Strömungszytometrie und sammeln Sie mindestens 20.000 Ereignisse für jede Erkrankung.
- Quantitatsignalstärke der fluoreszierenden Marker, die den Höhenwert für die Intensität jedes Fluorophors oder die geometrische mittlere Fluoreszenzintensität (MFI) verwenden.
- Wenn Sie nach der Scherbehandlung eine Platelet-Vernetzung erkennen wollen, analysieren Sie die Probe auf einem bildfähigen Strömungszytometer und quantitieren Sie die Vernetzung nach Flächen-und Seitenverhältnis-Parametern.
- Plot ein Histogramm der Fläche and/oder Seitenverhältnis.
- Verwenden Sie eine negative Steuerung mit Rinder-Serum Albumin (BSA) oder Fahrzeug, um ein Tor zu zeichnen, das die meisten kreisförmigen Ereignisse ausschließt (dieses Tor wird in der Regel mit einem Seitenverhältnis ~ 0,819,20gezeichnet) und den Prozentsatz der Ereignisse innerhalb dieses Tores zu bestimmen. Ereignisse mit einem niedrigeren Seitenverhältnis sind eher miteinander verknüpft.
Ergebnisse
Abbildung 1 skizziert, wie das Triggermodell der GPIb-IX-Aktivierung, das ursprünglich eingeführt wurde, um die schiearabhängige Rezeptor-Aktivierung zu erklären, wenn es an der Gefäßwand verankert ist, kann auch die Aktivierung von Platten unterstützen, die durch einen multivalenten Ligand miteinander verbunden sind. Abbildung 2 zeigt Auslesungen der Aktivierung menschlicher Blutplättchen, die von zwei Antikörpern behandelt werden, die auf die N-Termin...
Diskussion
Das in diesem Manuskript beschriebene Protokoll ermöglicht eine schnelle und vielseitige Beurteilung der Wirkung von Laminarschere auf Platelets und Zelloberflächen. Die hier vorgestellten spezifischen repräsentativen Ergebnisse unterstreichen, wie die Auswirkungen multimerischer oder bivalenter Liganden durch den Scherfluss beeinflusst werden können. Zusätzlich zu dieser Anwendung hat ein einheitlicher Scherenansatz breite Anwendungen in der Beobachtung von schierabhängigen Effekten. In Ermangelung eines bekannten...
Offenlegungen
Die Autoren haben nichts zu offenbaren.
Danksagungen
Die Arbeit, die für diese Studie relevant ist, wurde zum Teil von National Institutes of Health (NIH) National Heart, Lung und Blood Institute, HL082808, HL123984 (R.L.) und F31HL134241 (M.E.Q.), unterstützt. Die Finanzierung auch durch das NIH-Nationale Institut für Allgemeine medizinische Wissenschaften gewährt T32GM008367 (M.E.Q.); Und Pilotzuschüsse von Children es Healthcare of Atlanta und der Emory University Pediatric Flow Cytometry Core. Die Autoren danken Dr. Hans Deckmyn für die gemeinsame Nutzung des 6B4-Antikörpers und des Emory Children es Pediatric Research Center Flow Cytometry Core für die technische Unterstützung.
Materialien
| Name | Company | Catalog Number | Comments |
| APC anti-human CD62P (P-Selectin) | BioLegend | 304910 | |
| Brookfield Cap 2000+ Viscometer | Brookfield | - | |
| FITC-conjugated Erythrina cristagalli lectin (ECL) | Vector Labs | FL-1141 | |
| Pooled Normal Human Plasma | Precision Biologic | CCN-10 | |
| Vacutainer Light Blue Blood Collection Tube (Sodium Citrate) | BD | 369714 | |
| Vacutainer Blood Collection Set, 21G x ¾" Needle | BD | 367287 |
Referenzen
- Sullivan, M. J., et al. Non-voltage-gated Ca2+ influx through mechanosensitive ion channels in aortic baroreceptor neurons. Circulation Research. 80 (6), 861-867 (1997).
- Lansman, J. B., Hallam, T. J., Rink, T. J. Single stretch-activated ion channels in vascular endothelial cells as mechanotransducers. Nature. 325 (6107), 811-813 (1987).
- Fettiplace, R. Hair Cell Transduction, Tuning, and Synaptic Transmission in the Mammalian Cochlea. Comprehensive Physiology. 7 (4), 1197-1227 (2017).
- Zimmerman, A., Bai, L., Ginty, D. D. The gentle touch receptors of mammalian skin. Science. 346 (6212), 950-954 (2014).
- Nelson, C. M., et al. Emergent patterns of growth controlled by multicellular form and mechanics. Proceedings of the National Academy of Sciences USA. 102 (33), 11594-11599 (2005).
- Yu, C. H., Law, J. B., Suryana, M., Low, H. Y., Sheetz, M. P. Early integrin binding to Arg-Gly-Asp peptide activates actin polymerization and contractile movement that stimulates outward translocation. Proceedings of the National Academy of Sciences USA. 108 (51), 20585-20590 (2011).
- Wen, L., et al. A shear-dependent NO-cGMP-cGKI cascade in platelets acts as an auto-regulatory brake of thrombosis. Nature Communications. 9 (1), 4301 (2018).
- Marki, A., Gutierrez, E., Mikulski, Z., Groisman, A., Ley, K. Microfluidics-based side view flow chamber reveals tether-to-sling transition in rolling neutrophils. Scientific Reports. 6, 28870 (2016).
- Brockman, J. M., et al. Mapping the 3D orientation of piconewton integrin traction forces. Nature Methods. 15 (2), 115-118 (2018).
- Wang, X., et al. Constructing modular and universal single molecule tension sensor using protein G to study mechano-sensitive receptors. Scientific Reports. 6, 21584 (2016).
- Quach, M. E., et al. Fc-independent immune thrombocytopenia via mechanomolecular signaling in platelets. Blood. 131 (7), 787-796 (2018).
- Cao, W., Krishnaswamy, S., Camire, R. M., Lenting, P. J., Zheng, X. L. Factor VIII accelerates proteolytic cleavage of von Willebrand factor by ADAMTS13. Proceedings of the National Academy of Sciences USA. 105 (21), 7416-7421 (2008).
- Kroll, M. H., Hellums, J. D., McIntire, L. V., Schafer, A. I., Moake, J. L. Platelets and shear stress. Blood. 88 (5), 1525-1541 (1996).
- Pareti, F. I., Niiya, K., McPherson, J. M., Ruggeri, Z. M. Isolation and characterization of two domains of human von Willebrand factor that interact with fibrillar collagen types I and III. Journal of Biological Chemistry. 262 (28), 13835-13841 (1987).
- Deng, W., et al. Platelet clearance via shear-induced unfolding of a membrane mechanoreceptor. Nature Communications. 7, 12863 (2016).
- Ikeda, Y., et al. The role of von Willebrand factor and fibrinogen in platelet aggregation under varying shear stress. Journal of Clinical Investigation. 87 (4), 1234-1240 (1991).
- Westerhof, N., Stergiopulos, N., Noble, M. I. . Snapshots of hemodynamics: an aid for clinical research and graduate education. , (2010).
- Liang, X., et al. Specific inhibition of ectodomain shedding of glycoprotein Ibalpha by targeting its juxtamembrane shedding cleavage site. Journal of Thrombosis and Haemostasis. 11 (12), 2155-2162 (2013).
- Samsel, L., et al. Imaging flow cytometry for morphologic and phenotypic characterization of rare circulating endothelial cells. Cytometry Part B: Clinical Cytometry. 84 (6), 379-389 (2013).
- Basiji, D. A., Ortyn, W. E., Liang, L., Venkatachalam, V., Morrissey, P. Cellular image analysis and imaging by flow cytometry. Clinics in Laboratory Medicine. 27 (3), 653-670 (2007).
- Quach, M. E., Chen, W., Li, R. Mechanisms of platelet clearance and translation to improve platelet storage. Blood. 131 (14), 1512-1521 (2018).
Nachdrucke und Genehmigungen
Genehmigung beantragen, um den Text oder die Abbildungen dieses JoVE-Artikels zu verwenden
Genehmigung beantragenThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Alle Rechte vorbehalten