Method Article
Kombination von 3D-Druck und Elektrospinnen zur Herstellung biomimetischer Herzklappenbroschüren
In diesem Artikel
Zusammenfassung
Die vorgestellte Methode bietet eine innovative Möglichkeit, biomimetische Faserstrukturen in dreidimensionalen (3D) Gerüsten (z.B. Herzklappenbeilagen) zu konstruieren. Zur Bestimmung von Form und Abmessungen wurden 3D-gedruckte, leitfähige Geometrien verwendet. Faserausrichtung und -eigenschaften wurden für jede Schicht individuell einstellbar. Mehrere Muster können in einem Setup hergestellt werden.
Zusammenfassung
Das Elektrospinnen ist zu einer weit verbreiteten Technik im kardiovaskulären Tissue Engineering geworden, da es die Möglichkeit bietet, (Mikro-)faserige Gerüste mit einstellbaren Eigenschaften herzustellen. Ziel dieser Studie war es, mehrschichtige Gerüste herzustellen, die die architektonischen Fasereigenschaften menschlicher Herzklappenblätter mit leitfähigen 3D-gedruckten Kollektoren nachahmen.
Modelle von Aortenklappenspitzen wurden mit kommerzieller CAD-Software (Computer-Aided Design) erstellt. Leitfähige Polymilchsäure wurde verwendet, um 3D-gedruckte Beipackzettelschablonen herzustellen. Diese Spitzennegative wurden in einen speziell entwickelten, rotierenden Elektrospinndorn integriert. Drei Schichten Polyurethan wurden auf den Kollektor geschleudert und ahmen die Faserorientierung menschlicher Herzklappen nach. Die Oberflächen- und Faserstruktur wurde mit einem Rasterelektronenmikroskop (REM) beurteilt. Der Einsatz von Fluoreszenzfarbstoff ermöglichte zusätzlich die mikroskopische Visualisierung der mehrschichtigen Faserstruktur. Zugversuche wurden durchgeführt, um die biomechanischen Eigenschaften der Gerüste zu beurteilen.
Der 3D-Druck wesentlicher Teile für das Elektrospinngerät war in kurzer Zeit für ein geringes Budget möglich. Die nach diesem Protokoll entstandenen Aortenklappenhöcker waren dreischichtig mit einem Faserdurchmesser von 4,1 ± 1,6 μm. Die REM-Bildgebung zeigte eine gleichmäßige Verteilung der Fasern. Die Fluoreszenzmikroskopie zeigte einzelne Schichten mit unterschiedlich ausgerichteten Fasern, wobei jede Schicht genau die gewünschte Faserkonfiguration erreichte. Die produzierten Gerüste zeigten eine hohe Zugfestigkeit, insbesondere entlang der Ausrichtung. Die Druckdateien für die verschiedenen Collectors sind als Supplemental File 1, Supplemental File 2, Supplemental File 3, Supplemental File 4 und Supplemental File 5 verfügbar.
Mit einem hochspezialisierten Setup- und Workflow-Protokoll ist es möglich, Gewebe mit komplexen Faserstrukturen über mehrere Schichten nachzuahmen. Das direkte Spinnen auf 3D-gedruckten Kollektoren schafft eine beträchtliche Flexibilität bei der Herstellung von 3D-Formen bei niedrigen Produktionskosten.
Einleitung
Herz-Kreislauf-Erkrankungen sind die häufigste Todesursache in westlichen Ländern 1. Obwohl auf diesem Gebiet umfangreiche Forschungen durchgeführt werden, wird geschätzt, dass die Belastung durch degenerative Herzklappenerkrankungen in den nächsten Jahren noch weiter zunehmen wird2. Als therapeutische Option ist ein operativer oder interventioneller Herzklappenersatz möglich. An dieser Stelle stehen mechanische und bioprothetische Herzklappen zur Verfügung, beide mit individuellen Nachteilen. Mechanische Ventile sind thrombogen und erfordern eine lebenslange Antikoagulation. Obwohl biologische Ventile keine Antikoagulation erfordern, zeigen sie einen Mangel an Umbau, eine hohe Verkalkungsrate und einen gleichzeitigen Abbau3.
Tissue-engineered Herzklappen könnten in der Lage sein, diese Nachteile zu beheben, indem sie ein mikrofaseriges Gerüst in den Körper einführen, das einen In-vivo-Umbau ermöglicht. Verschiedene Methoden, z.B. Elektrospinnen (ESP), Dezellularisierung, Micromolding, Spray, Dip-Coat und 3D-Bioprinting, stehen zur Verfügung. Diese Methoden können gewählt werden, um bestimmte Eigenschaften zu erstellen, billiger und schneller zu sein, oder einfach nur aufgrund fehlender Alternativen. Methoden und Materialien können sogar kombiniert werden, um komplexere Strukturenzu schaffen 4. Zum Beispiel war ESP eine Standardtechnik für die Herstellung von Gerüsten im Tissue Engineering, die die Kombination verschiedener Materialien und die Einstellung von Faserdurchmessern, Faserorientierungen und Porositätenermöglicht 4. Darüber hinaus ermöglichen eine Vielzahl von Nachbearbeitungstechniken einen optimierten Gewebeumbau, eine verbesserte Hämokompatibilität und einen einstellbaren biologischen Abbau von elektrogesponnenen Gerüsten 5,6,7.
Basic ESP verwendet entweder statische oder rotierende Kollektoren, die einen direkten Einfluss auf den Grad der Faserausrichtung und die erhaltenen Faserdurchmesser8 haben. Aufgrund von Herstellungsbeschränkungen bestehen klassische ESP-Drehkollektoren aus rotierenden Trommeln, Scheiben, Drähten oder Metallstäben. Die Einführung des 3D-Drucks ermöglicht die Erstellung individuellerer Kollektorgeometrien, die nicht durch traditionelle Fertigungstechniken eingeschränkt sind. Diese Individualisierung ist besonders nützlich für die Erstellung von 3D-Konstrukten wie Herzklappenbroschüren.
Die natürliche dreischichtige (Fibrosa, Spongiosa, Ventricularis) Architektur menschlicher Herzklappenblätter ist die Reaktion des Gewebes auf die mechanischen Kräfte und Schubspannungen, denen es während des Herzzyklus ausgesetzt ist 9,10. Die Fasern der Lamina fibrosa sind umlaufend ausgerichtet, während die Fasern der Lamina spongiosa zufällig und die der Lamina ventricularis radial ausgerichtet sind. Es wird daher eine Dreischicht mit den entsprechenden Faserorientierungen vorgeschlagen, um die Eigenschaften dieser Ventile in einem gewebetechnischen Gerüst nachzuahmen.
Das Workflow-Protokoll beschreibt eine innovative Methode zur Herstellung dreischichtiger 3D-Herzklappenbroschüren mittels 3D-Druck und Elektrospinning. Zusätzlich wird ein Qualitätskontrollschritt vorgestellt, um eine genaue Faserorientierung in jeder Schicht zu gewährleisten.
Protokoll
1. Vorarbeiten
- 3D-Druck
HINWEIS: Die folgenden Schritte erfordern den Download der "Standard Triangle Language" (STL) -Dateien, die als Supplemental File 1, Supplemental File 2, Supplemental File 3, Supplemental File 4 und Supplemental File 5 mit diesem Manuskript bereitgestellt werden. Kollektorteile werden als STL-Dateien bereitgestellt. Der Anschlussflansch wird als STEP-Datei (STandard for the Exchange of Product Model Data) bereitgestellt, um die Anpassung des Kollektors an individuelle Setups zu ermöglichen. Des Weiteren wird eine technische Zeichnung für die zentralen Metallstäbe für die konventionelle Fertigung als Supplemental File 6 zur Verfügung gestellt.- Öffnen Sie die Schneidesoftware (siehe Materialtabelle) und konfigurieren Sie den aktiven Druckkopf für nicht leitende Polymilchsäure (PLA) und eine 0,4-mm-Düse.
HINWEIS: Schneidesoftware, Filament und Düsendurchmesser können je nach verfügbarem 3D-Drucker variieren. - Laden Sie die STL-Dateien Specimen_mount_A (Supplemental File 3) und Speciment_mount_B (Supplemental File 4) in die Slicing-Software hoch.
- Drehen Sie die Modelle, so dass die dreieckigen Flächen auf der Bauplatte platziert werden.
- Markieren Sie alle Teile, klicken Sie mit der rechten Maustaste, und wählen Sie Ausgewählte Modelle multiplizieren aus. Geben Sie 1 in die Eingabeaufforderung Anzahl der Kopien ein und klicken Sie auf OK. Legen Sie insgesamt vier Modelle auf die Bauplatte.
- Legen Sie die Schnittdicke auf 0,1 mm, die Wandstärke auf 1 mm, die Fülldichte auf 40 % fest, und deaktivieren Sie das Kontrollkästchen Unterstützung generieren .
- Klicken Sie auf die Schaltfläche Slice | Unter Wechselmedien speichern, um die Druckdatei auf einem USB-Laufwerk zu speichern.
- Laden Sie die nicht leitende PLA in den Drucker und starten Sie die Druckdatei.
- Nachdem der Druck abgeschlossen ist, entfernen Sie die Modelle von der Bauplatte und überprüfen Sie, ob sie sich an den unteren Ecken verziehen.
- Behalten Sie in der Schneidesoftware die Materialparameter bei und ersetzen Sie die Modelle durch Collector_Flange (Supplemental File 1 und Supplemental File 5) und Leaflet_Template (Supplemental File 2).
- Drehen Sie den Flansch, so dass die ebene kreisförmige Oberfläche gegen die Bauplatte liegt. Drehen Sie zusätzlich die Prospektvorlage, sodass die quadratische Oberfläche direkt auf der Bauplatte platziert wird.
- Markieren Sie den Flansch, und multiplizieren Sie das Modell wie in Schritt 1.1.4. Geben Sie 1 ein, um 1 Kopie und 1 Original des Flanschmodells auf der Bauplatte zu erhalten.
- Markieren Sie das Prospektmodell und multiplizieren Sie es mit 8, um insgesamt neun Prospektmodelle zu erhalten, indem Sie die in 1.1.4 beschriebenen Schritte ausführen.
- Legen Sie die Schnittdicke auf 0,1 mm, die Wandstärke auf 1 mm , die Fülldichte auf 80 % fest, und deaktivieren Sie das Kontrollkästchen Unterstützung generieren .
- Klicken Sie auf die Schaltfläche Slice | In Wechselmedien speichern, um die neue Druckdatei auf einem USB-Laufwerk zu speichern.
- Laden Sie leitfähiges PLA in den Drucker und starten Sie den Druckvorgang.
- Entfernen Sie nach Abschluss des Drucks die Modelle von der Bauplatte. Entfernen Sie einzelne Filamentfasern an der Unterseite des Prospektnegativs vorsichtig mit einem Drahtschneider, wenn diese in den Prospektmodellen vorhanden sind (da keine Stützstrukturen verwendet wurden).
- Öffnen Sie die Schneidesoftware (siehe Materialtabelle) und konfigurieren Sie den aktiven Druckkopf für nicht leitende Polymilchsäure (PLA) und eine 0,4-mm-Düse.
- Spinning-Lösung
ACHTUNG: Tetrahydrofuran (THF) und Dimethylformamid (DMF) sind schädliche Lösungsmittel, die nicht eingeatmet werden oder die Haut berühren sollten. Es wird dringend empfohlen, beim Umgang mit ihnen lösemittelbeständige Handschuhe und Schutzbrillen zu tragen. Arbeiten Sie beim Umgang mit ihnen unter einer Dunstabzugshaube, da sie extrem flüchtig sind.- Legen Sie eine Waage unter die Dunstabzugshaube und positionieren Sie eine 200 ml Schraubverschluss-Glasflasche darauf. Tare die Skala.
- Gießen Sie 50 mL DMF und 50 mL THF in die Glasflasche. Beachten Sie das Gewicht der Lösungsmittel.
- Legen Sie eine Magnetstange in die Flasche, legen Sie die Flasche auf einen Magnetrührer und schalten Sie sie ein.
- Multiplizieren Sie das notierte Gewicht mit 0,15 (= 15% w/v) und geben Sie die entsprechende Menge Polyurethan (PU) langsam in die Glasflasche mit dem Lösungsmittelgemisch (DIN 1310).
- Schließen Sie die Flasche und rühren Sie mindestens 12 h bei Raumtemperatur, um eine homogene Lösung zu erhalten.
2. Elektrospinnen-Setup
- Versammlung
HINWEIS: Da die mit dem vorgestellten Kollektor erstellten Prospektgerüste relativ klein sind, wird die optionale Verwendung eines Trommeldorns mit großem Durchmesser (T: 110 mm) empfohlen. Dies ermöglicht die Schaffung größerer, mehrschichtiger Gerüste, die für mikroskopische, biokompatible und biomechanische Bewertung von Vorteil sind.- Montieren Sie den Kollektor mit den 3D-gedruckten Teilen und sechs M3 x 15-Schrauben.
- Verwenden Sie drei Schrauben, um die Metallstangen an einem der Flansche zu befestigen.
- Schieben Sie einen Specimen_mount_B zwischen die Metallstangen. Stellen Sie sicher, dass die Leerzeichen für Vorlagen in die entgegengesetzte Richtung des Flansches zeigen.
- Füllen Sie die drei Steckplätze des Specimen_mount_B mit Herzklappen-Prospektvorlagen.
- Platzieren Sie Specimen_mount_A oben und füllen Sie die Leerzeichen mit Vorlagen.
- Schieben Sie eine weitere Specimen_mount_A hinein und füllen Sie die Leerzeichen mit Vorlagen.
- Fixieren Sie die Vorlagen, indem Sie die zweite Specimen_mount_B oben platzieren.
- Setzen Sie den zweiten Flansch oben auf und verwenden Sie die M3-Schrauben, um ihn zu sichern.
HINWEIS: Stellen Sie sicher, dass die Beipackzettelvorlagen alle in die gleiche Richtung ausgerichtet sind (gerader Rand der Packungsbeilage parallel zu den Metallstäben). - Setzen Sie den montierten Prospektsammler in die Elektrospinneinrichtung und befestigen Sie die Flansche fest an der Motorachse (d. h. M6-Schrauben und Flügelmuttern) (Abbildung 1).
ACHTUNG: Da leitfähiges PLA spröder ist als normales PLA, verwenden Sie einen Drehmomentschlüssel bei 1,4 Nm, wenn Sie Schrauben befestigen, die Druck auf das Material ausüben, um ein Einrasten zu vermeiden. - Legen Sie einen Nadelhalter 30 cm vom Kollektor entfernt.
- Befestigen Sie eine 14 Gauge (G) Nadel mit einer flachen Spitze im Nadelhalter und fixieren Sie sie auf Höhe der Kollektorachse.
- Schließen Sie ein flexibles, lösungsmittelbeständiges (z. B. Polytetrafluorethylen (PTFE)) Rohr an den Luer-Lock-Port der Nadel an.
HINWEIS: DMF und THF lösen viele Kunststoffe auf. Bei der Arbeit mit diesen Lösungsmitteln müssen lösemittelbeständige Materialien verwendet werden, z. B. Metall- und Glaswerkzeuge. Wenn Kunststoffwerkzeuge erforderlich sind (z. B. Spritzen oder Schläuche), achten Sie darauf, lösungsmittelbeständige Materialien zu verwenden. - Führen Sie den Schlauch zur Spritzenpumpe für den späteren Anschluss der polymergefüllten Spritze.
- Anschluss des Netzteils (PSU)
ACHTUNG: Stellen Sie während der Einrichtung sicher, dass das Netzteil von der Hauptstromquelle getrennt ist.- Schließen Sie zwei geschirmte Hochspannungskabel an die Anode und Kathode des Netzteils an.
- Verbinden Sie mit einem Krokodilklemmer das mit der Kathode verbundene Kabel (-stange) mit der 14-G-Nadel. Überprüfen Sie die Verbindung zwischen Clip und Nadel. Als nächstes führen Sie das Hochspannungskabel so, dass es außerhalb des Drehbereichs verläuft, um Interferenzen zu vermeiden.
- Verbinden Sie den Kollektor mit einem Krokodilclip und dem zweiten Hochspannungskabel mit der Anode (+ Pol). Verwenden Sie einen Schleifring oder einen Schleifkontakt mit einem abisolierten Kabel, um Kontakt am Kollektorflansch herzustellen.
- Vorbereitung der Spritze
HINWEIS: Dieser Schritt sollte unmittelbar vor Beginn des Spinnvorgangs ausgeführt werden.- Füllen Sie eine 20 ml Luer-Lock-Spritze mit der in Schritt 1.2 hergestellten Spinnlösung.
- Verbinden Sie die Spritze mit dem lösungsmittelbeständigen Schlauch und drücken Sie die Lösung manuell in das Schlauchsystem, bis ein Tröpfchen an der Nadelspitze sichtbar ist.
- Legen Sie die Spritze in die Spritzenpumpe. Geben Sie nach dem Einschalten der Pumpe die folgenden Parameter ein: Durchmesser: 19.129 mm; Volumen: 5 ml; Geschwindigkeit 3 ml/h.
3. Elektrospinnenverfahren
- Motor-Testlauf
HINWEIS: Die Herstellung des Kollektors im 3D-Druck kann zu einer außermittigen Bewegung des Kollektors führen. Daher ist ein Testlauf mit niedrigeren Drehzahlen, aber ohne Hochspannung sehr zu empfehlen.- Öffnen Sie die Motorsteuerungssoftware, indem Sie auf das Symbol auf dem Computer doppelklicken.
- Stellen Sie eine Verbindung zur Motorsteuerung her, indem Sie auf die Schaltfläche Verbinden klicken.
- Wählen Sie nach dem Herstellen der Verbindung den Betriebsmodus Profilgeschwindigkeit und klicken Sie auf die Registerkarte Operation in der oberen linken Ecke des Bildschirms.
- Wählen Sie die Registerkarte Profilgeschwindigkeit unter der Schaltfläche Schnellstopp aus, die von einer roten Linie umrahmt wird. Geben Sie die folgenden Einstellungen ein: Zielgeschwindigkeit: 200 U/min; Profilbeschleunigung: 100; Profilentschleunigung: 200; Schnellstopp: 5000.
HINWEIS: Die Drehrichtung sollte auf der Nadelseite nach oben gerichtet sein, was durch Ändern des Vorzeichens im Feld "Zielgeschwindigkeit" von "+" auf "-" eingestellt werden kann. - Starten Sie den Testlauf und überprüfen Sie den Kollektor auf Unregelmäßigkeiten. Wenn der Kollektor reibungslos läuft, fahren Sie mit dem Protokoll fort. Andernfalls stoppen Sie den Motor und stellen Sie den Kollektor wie in Schritt 2.1.9 beschrieben wieder ein.
- Stoppen Sie den Motor, indem Sie auf die Schaltfläche Aktiviert einschalten klicken und die Zielgeschwindigkeit auf 2.000 U/min ändern.
- Herstellungsprozess
HINWEIS: Elektrospinnen ist ein Prozess mit einer hohen Abhängigkeit von Umweltparametern. Optimale Elektrospinnergebnisse wurden zwischen 15-20% relativer Luftfeuchtigkeit bei einer Temperatur zwischen 21 und 24 °C erzielt.- Erste Schicht
HINWEIS: Während der Aufbauphase könnte sich an der Spitze der Nadel ein getrockneter PU-Tröpfchen gebildet haben. Entfernen Sie das Tröpfchen bei Bedarf mit einem langen, nicht leitenden Werkzeug.- Klicken Sie in der Motorsteuerungssoftware auf die Schaltfläche Bedienung aktivieren , um den Motor einzuschalten.
- Schalten Sie das Hochspannungsnetzteil ein und stellen Sie die Spannung für Anode und Kathode ein: Minuspol (Nadel): 18 kV; plus Pol (Kollektor): 1,5 kV.
- Starten Sie die Spritzenpumpe mit einem Durchfluss von 3 ml/h.
- Stellen Sie einen Timer auf 20 min.
- Beobachten Sie die Nadelspitze für die Bildung eines Schneiderkegels. Je nach Form des Kegels an der Nadelspitze stellt man die Spannung an der Kathode in Schritten von ±100 V ein, bis ein stabiler Schneiderkegel aufgebaut ist.
HINWEIS: Wenn der Tropfen hängt, ist die Spannung zu niedrig. Ein instationärer Fluss kann jedoch darauf hinweisen, dass die Spannung zu hoch eingestellt ist. - Warten Sie 20 Minuten, bis die Spitzenschablonen ausreichend mit Fasern bedeckt sind.
- Schalten Sie die Spritzenpumpe aus.
- Schalten Sie das Netzteil aus, indem Sie den Netzschalter umlegen.
- Stoppen Sie den Motor, indem Sie in der Motorsteuerungssoftware auf die Schaltfläche Aktiviert einschalten klicken.
ACHTUNG: Um Verletzungen durch bewegliche Teile im System zu vermeiden, warten Sie, bis der Kollektor vollständig gestoppt wurde, um die Testkammer zu öffnen.
- Zweite Schicht
- Ändern Sie in der Motorsteuerungssoftware das Eingabefeld Zielgeschwindigkeit auf 10 U/min.
- Wiederholen Sie die Schritte 3.2.1.1-3.2.1.9.
- Dritte Schicht
HINWEIS: Bevor die Gerüste vollständig trocken sind, sind sie extrem empfindlich gegenüber mechanischer Beanspruchung. Seien Sie sehr vorsichtig, wenn Sie die Schritte 3.2.3.2-3.2.3.6 ausführen. Vermeiden Sie es, die Gerüste / Fasern während dieser Schritte zu berühren, da das Gerüst möglicherweise unbrauchbar wird.- Öffnen Sie vorsichtig die Schrauben, die die Kollektorflansche mit der Motorachse verbinden, und entfernen Sie den Prospektkollektor (Abbildung 2B) von der Elektrospinnvorrichtung.
- Schneiden Sie die elektrogesponnenen Fasern mit einem Skalpell entlang der äußeren Kontur jeder Packungsbeilagevorlage ab (Abbildung 2C).
- Entfernen Sie den Flansch auf einer Seite des Kollektors.
- Ziehen Sie die 3D-gedruckten Einsätze heraus und trennen Sie die Beipackzettelschablonen von den nicht leitenden dreieckigen Haltern.
- Drehen Sie alle Prospektvorlagen um 90° und setzen Sie den Kollektor wieder zusammen.
- Setzen Sie den Kollektor in die Elektrospinneinrichtung ein und befestigen Sie ihn fest.
- Überprüfen Sie erneut auf Unausgewogenheiten, bevor Sie mit dem Spinnvorgang fortfahren.
- Ändern Sie in der Motorsteuerungssoftware das Eingabefeld Zielgeschwindigkeit auf 2.000 U/min.
- Wiederholen Sie die Schritte 3.2.1.1-3.2.1.9.
HINWEIS: Nach Abschluss des Elektrospinnprozesses wird dringend empfohlen, den Schlauch und die Nadel mit reinem DMF zu spülen, um ein Verstopfen des Schlauches zu vermeiden.
- Fluoreszierend gefärbte Gerüste (optional)
HINWEIS: Fluoreszierende Farbstoffe werden verwendet, um die Fasern unter einem herkömmlichen Fluoreszenzmikroskop sichtbar zu machen. Dies ist nur bei der Implementierung der Methode und für die Qualitätskontrolle nach dem Anwenden neuer Einstellungen erforderlich. Die Verwendung von fluoreszierenden Farbstoffen wird bei der Herstellung von Gerüsten unter Verwendung festgelegter Einstellungen nicht empfohlen.- Teilen Sie die in Schritt 1.2 vorbereitete Spinnlösung in drei gleiche Portionen in separaten Flaschen auf.
- Messen Sie mit einer Waage 1 mg Fluoreszenzfarbstoff für jedes Gramm (0,1 Gew.-%) Polymerlösung. Wiederholen Sie dies für alle drei fluoreszierenden Farbstoffe (z. B. Fluorescein, Texas Red, 4',6-Diamidino-2-phenylindol [DAPI]).
- Fügen Sie den Farbstoff der Spinnlösung hinzu, schließen Sie den Flaschendeckel und rühren Sie für 2-3 h oder bis zur Homogenisierung.
HINWEIS: Um zu verhindern, dass die fluoreszierenden Farbstoffe verblassen, schützen Sie die Spinnlösung so weit wie möglich vor Licht, d.h. indem Sie eine undurchsichtige Abdeckung über den Magnetrührer legen. Das Verfahren für fluoreszierend gefärbte Gerüste ist dem in den Schritten 3.2.1-3.2.3 beschriebenen Standardverfahren sehr ähnlich. - Ersetzen Sie in Schritt 3.2.1 die Standardspritze durch eine Spritze, die mit der Spinnlösung gefüllt ist, die den ersten fluoreszierenden Farbstoff enthält.
- Ersetzen Sie in Schritt 3.2.2 die aktuell verwendeten Schläuche und Nadeln durch neue oder gereinigte. Anschließend legen Sie eine Spritze mit der Spinnlösung, die den zweiten fluoreszierenden Farbstoff enthält, in die Spritzenpumpe.
- Ersetzen Sie in Schritt 3.2.3 erneut den Schlauch und die Nadel durch neue oder gereinigte Schläuche und ersetzen Sie die Spritze durch eine Spritze, die mit Spinnlösung gefüllt ist, die den dritten Fluoreszenzfarbstoff enthält.
HINWEIS: Um Verzögerungen während des Herstellungsprozesses zu vermeiden, ist es von Vorteil, drei Sätze von Schläuchen und Nadeln zu verwenden. Alternativ können Schlauch und Nadel zwischen der Herstellung von Schichten gründlich mit THF und DMF gespült werden, bis keine Spinnlösung mit fluoreszierendem Farbstoff mehr im System verbleibt.
- Erste Schicht
4. Nachbearbeitung und Probenentnahme
- Nachbearbeitung von Gerüsten
- Entfernen Sie den Kollektor aus der Elektrospinnvorrichtung.
- Schneiden Sie mit einem Skalpell jede Vorlage an ihrer Basis frei, wie in Schritt 3.2.3.2 beschrieben.
- Öffnen Sie den Kollektor, wie oben beschrieben, und legen Sie die Vorlagen unten auf ein Fach.
- Stellen Sie das Tablett über Nacht bei 40 °C in einen Trockenschrank.
- Nachdem die Proben vollständig getrocknet sind, verwenden Sie ein Skalpell, um vorsichtig entlang der Ränder der Packungsbeilageschablone zu schneiden, um überschüssige Fasern zu entfernen.
- Danach schälen Sie vorsichtig das Prospektgerüst der Vorlage und legen Sie es zur weiteren Verarbeitung auf ein Tablett.
Ergebnisse
Dieses Protokoll zielt auf die Entwicklung eines dreischichtigen Flugblattgerüsts ab, das für den Einsatz im kardiovaskulären Tissue Engineering von Herzklappen bestimmt ist. Es ahmt die Kollagenkonfiguration der drei Schichten in der einheimischen menschlichen Herzklappe nach. Jede Schicht besteht aus Fasern mit einem Gesamtdurchmesser von 4,1 ± 1,6 μm (Abbildung 1).
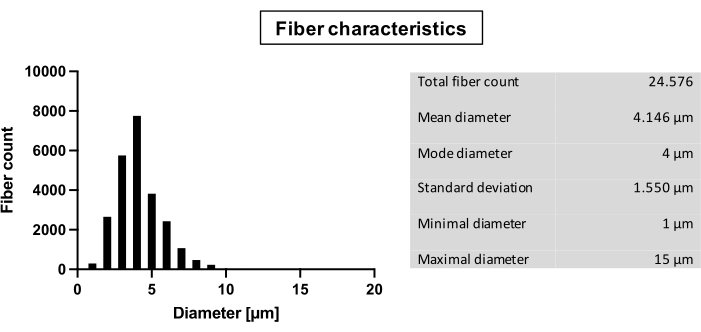
Abbildung 1: Fasereigenschaften. Analyse von Fasern: Gesamtfaserzahl; Durchmesser in μm: Mittelwert, Mode, Standardabweichung, minimaler Durchmesser, maximaler Durchmesser. Bitte klicken Sie hier, um eine größere Version dieser Abbildung zu sehen.
Die Prospektvorlagen sind für eine Aortenklappenprothese mit einem Durchmesser von 24 mm ausgelegt (Abbildung 2C). Nach dem Trocknen behielten die Prospektgerüste ihre Form einer 3D-Herzklappenspitze bei (Abbildung 3A).

Abbildung 2: Elektrospinnaufbau. (A) Zusammengebauter 3D-gedruckter Kollektor in der Dreheinrichtung; (B) CAD-Rendering des 3D-druckbaren Kollektors; (C) CAD-Darstellung der in B negativ dargestellten Herzklappenpackung; Dreieck zeigt vergrößerten Teil an. Abkürzung: CAD = Computer-Aided Design. Bitte klicken Sie hier, um eine größere Version dieser Abbildung zu sehen.
Zur Beurteilung der ausgerichteten und nicht ausgerichteten Schichten wurde die REM-Bildgebung verwendet (TEMP F3512-21). Die Fotos wurden mit 100-facher, 500-facher und 2.000-facher Vergrößerung an drei verschiedenen Stellen auf einem Gerüst aufgenommen. Ausgerichtete Fasergerüste erscheinen mit einer glatten Oberfläche und strenger Ausrichtung in Umfangsrichtung (Abbildung 3B). Die visuelle Analyse des 2.000-fachen Bildes in Bezug auf die Faserorientierung bestätigt die primäre Ausrichtung der Fasern (Abbildung 3C). Nicht ausgerichtete Fasergerüste zeigen eine ähnlich glatte Oberfläche im Vergleich zu den ausgerichteten Fasern. Die Faserorientierung ist ungeordnet, mit vielen markanten Schnittpunkten zwischen den Fasern (Abbildung 3D). Die anschließende visuelle Analyse bestätigt die Unausrichtung von Fasern, ohne dass eine primäre Orientierung sichtbar ist (Abbildung 3E).

Abbildung 3: Elektrogesponnenes Beipackzettel und REM-Bildgebung. (A) Elektrogesponnenes mehrschichtiges Beipackzettel und 3D-gedrucktes Beipackungskollektor; (B) REM-Bild von nicht ausgerichteten Fasern (Vergrößerung 1.000x); (C) Faserorientierungsanalyse von nicht ausgerichteten Fasern; (D) REM-Bild von ausgerichteten Fasern (Vergrößerung 1.000x); (E) Faserorientierungsanalyse von ausgerichteten Fasern. Maßstabsstäbe = 10 mm (A), 100 μm (B, D). Abkürzung: SEM = Rasterelektronenmikroskopie. Bitte klicken Sie hier, um eine größere Version dieser Abbildung zu sehen.
Die Bildgebung von fluoreszierend gefärbten mehrschichtigen Gerüsten ergab drei einzelne Schichten mit unterschiedlichen Faserorientierungen (Abbildung 4D). Die untere Schicht (Abbildung 4A; blau) zeigt ausgerichtete Faserlinien in horizontaler Ausrichtung mit sehr geringem Schnittpunkt zwischen den Fasern. Die mittlere Schicht (Abbildung 4B; grün) zeigt nicht ausgerichtete Fasern ohne primäre Faserorientierung. Die oberste Schicht (Abbildung 4C; rot) zeigt ausgerichtete Fasern in senkrechter Ausrichtung. Die visuelle Analyse der oberen und unteren Schichten zeigt einen durchschnittlichen Winkel zwischen den beiden Schichten von 89°, der der 90°-Drehung des Kollektors während des Spinnvorgangs entspricht (Abbildung 4E).
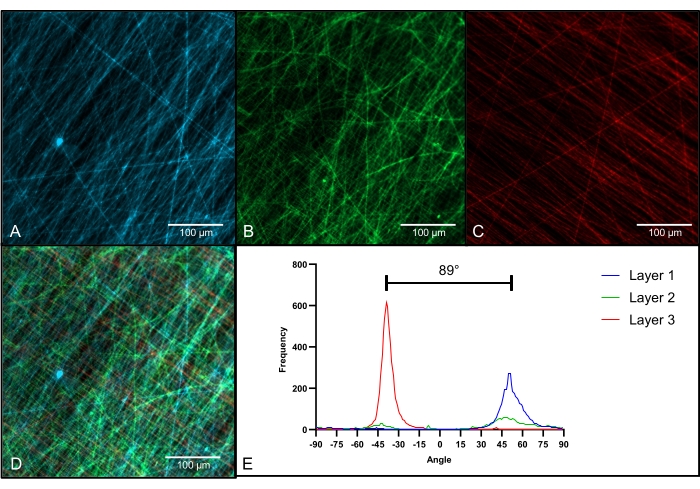
Abbildung 4: Fluoreszenzmikroskopie eines mehrschichtigen Gerüsts. (A) Fluoreszenzbild der ersten Schicht mit primärer Ausrichtung von unten links nach oben rechts; (B) Fluoreszenzbild der zweiten Schicht mit nicht ausgerichteter Faserorientierung; (C) Fluoreszenzbild der dritten Schicht mit primärer Ausrichtung von unten rechts nach oben links; (D) Fluoreszenzbild aller drei Schichten, die in einem Gerüst zusammengefasst sind; (E) Faserorientierungsanalyse für alle drei Schichten (Schicht 1: blau; Schicht 2: grün; Schicht 3: rot); Vergrößerung = 400x (A-D); Maßstabsstäbe = 100 μm (A-D). Bitte klicken Sie hier, um eine größere Version dieser Abbildung zu sehen.
Die Dickenmessung wurde an 21 Proben durchgeführt (Abbildung 5A) (TEMP F3510-21). Alle Beispiele wurden unter Anwendung der gleichen Parameter erstellt. Temperatur und Luftfeuchtigkeit können zwischen 20,3 °C und 26,1 °C bzw. 35 % bzw. 55 % Luftfeuchtigkeit variieren. Die Ergebnisse zeigten eine relativ lineare Zunahme der Dicke um ~2,65 μm pro min.
Ein weiteres Experiment zeigte die Konsistenz der Ergebnisse nach 60 Minuten Spinnen unter übereinstimmenden Parametern (Abbildung 5B). Luftfeuchtigkeit und Temperatur können zwischen 35% und 50% Luftfeuchtigkeit bzw. 20,3 °C bis 26,1 °C variieren. Das Ergebnis waren Gerüste zwischen 126 und 181 μm Dicke. Die durchschnittliche Dicke betrug 151,11 ± 13,17 μm. Die Zunahme der Dicke betrug im Durchschnitt ~ 2,52 μm pro min.
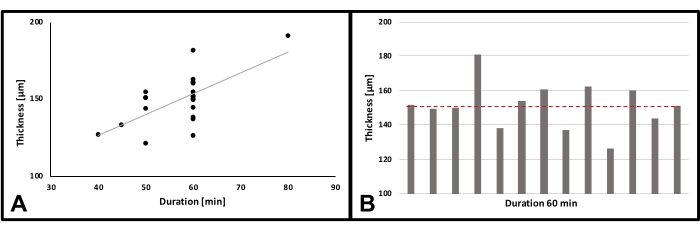
Abbildung 5: Dickenmessung. a) Dicke der Gerüste je gesponnener Zeit; n = 21; Korrelationskoeffizient (r) = 0,653; p** = 0,00132; B) Dicke der Proben nach 60 min; n = 13; rote Linie: Mittelwert. Bitte klicken Sie hier, um eine größere Version dieser Abbildung zu sehen.
Zugversuche für ausgerichtete und nicht ausgerichtete Fasergerüste wurden in zwei Richtungen durchgeführt, entlang der Umfangsrichtung und senkrecht dazu. Jeder Mörtel bestand aus 15 Exemplaren. Aus Flugzeuggerüsten wurden Proben nach DIN 53504:2017-03 entnommen. Die Dicke wurde an drei verschiedenen Stellen auf jeder Probe gemessen und zur Berechnung der maximalen Kraftwerte pro Quadratmillimeter verwendet.
Die Dickenwerte liegen zwischen 0,03 und 0,2 mm. Der Vergleich der Zugfestigkeit ergab einen signifikanten Unterschied (p < 0,001) zwischen den Orientierungen für die ausgerichteten Fasergerüste (Abbildung 6A). Die Gerüste erreichten entlang der umlaufenden Ausrichtung eine maximale Festigkeit von 12,26 ± 2,59 N/mm2. Die Zugfestigkeit wurde auf 3,86 ± 1,08 N/mm2 in senkrechter Richtung reduziert.
Nicht ausgerichtete Fasergerüste zeigen keinen Unterschied in der Zugfestigkeit für die verschiedenen Orientierungen (F1: 7,19 ± 1,75 N/mm 2, F2: 7,54 ± 1,59 N/mm2; p = 0,60). Die vergleichende Analyse der Bruchdehnung für die ausgerichteten Fasergerüste ergab signifikante Unterschiede (p < 0,001) in der Dehnbarkeit zwischen den Richtungen (Abbildung 6B). Die Erweiterbarkeit erreichte 187,01 ± 39,37% in Umfangsrichtung im Vergleich zu 107,16 ± 30,04% in senkrechter Richtung.
Im Gegensatz dazu zeigte die Bruchdehnung für die nicht ausgerichteten Fasermatten eine gleichmäßige Dehnbarkeit in beide Richtungen (F1: 269,74 ± 24,78 % ; F2: 285,01 ± 25,58 %; p = 0,69). Repräsentative Spannungs-Dehnungs-Kurven zeigen große Unterschiede im Verhalten des Materials, abhängig von der Richtung, in der die Zugkraft angewendet wird. Nicht ausgerichtete Fasermatten zeigten lineares elastisches Verhalten, während ausgerichtete Fasermatten Nichtlinearität in axialer Richtung zeigten.
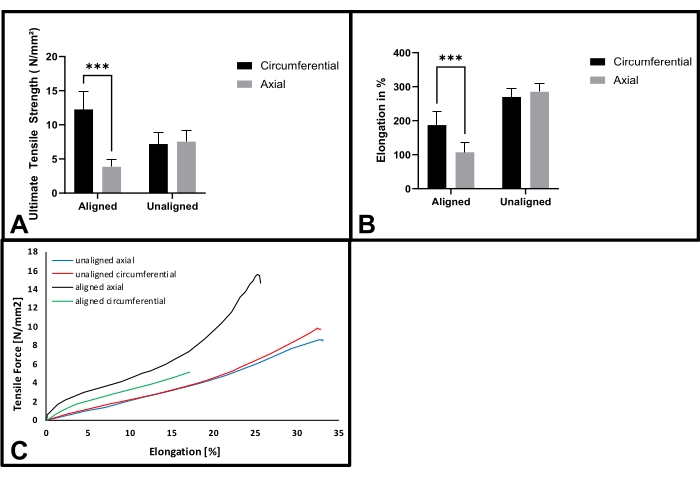
Abbildung 6: Zugversuche von ausgerichteten und nicht ausgerichteten Fasern. (A) Ultimative Zugfestigkeit für ausgerichtete und nicht ausgerichtete Fasermatten in umlaufender und axialer Richtung; n = 15; (B) Bruchdehnung bei ausgerichteten und nicht ausgerichteten Fasermatten in umlaufender und axialer Richtung; n = 15; (C) Repräsentative Spannungs-Dehnungs-Kurven von ausgerichteten und nicht ausgerichteten Gerüsten, die in axialer bzw. umlaufender Richtung gezogen werden. (***p < 0,001). Bitte klicken Sie hier, um eine größere Version dieser Abbildung zu sehen.
| Fertigungsmetriken | |||||||||
| Name | Material | Menge | Gesamtzeit | Gesamtgewicht [g] | Kosten [€ pro kg] | Gesamtkosten | |||
| 1 | Specimen_Mount_A | Reguläre PLA | 2 | 18:19 | 159 | 51,33 € | 8,16 € | ||
| 2 | Specimen_Mount_B | Reguläre PLA | 2 | 19:42 | 161 | 51,33 € | 8,26 € | ||
| 3 | Kollektorflansch | Leitfähige PLA | 2 | 10:40 | 95 | 99,98 € | 9,50 € | ||
| 4 | Leaflet_Inlet | Leitfähige PLA | 9 | 05:32 | 31 | 99,98 € | 3,10 € | ||
| Gesamt | 29,02 € | ||||||||
Tabelle 1: Fertigungsmetriken. Tabelle mit Angabe von Menge, Herstellungszeit, benötigter Materialmenge und Kosten für 3D-gedruckte Teile. Abkürzung: PLA = Polymilchsäure.
Ergänzende Datei 1: Anpassbarer Kollektorflansch. Step-Datei zum Anpassen und Drucken von Kollektorflansch. Bitte klicken Sie hier, um diese Datei herunterzuladen.
Ergänzende Datei 2: Prospektvorlage. STL-Datei zum Drucken der Prospektvorlage. Bitte klicken Sie hier, um diese Datei herunterzuladen.
Ergänzende Datei 3: Probenhalterung A. STL-Datei zum Drucken von Probenhalterung A. Bitte klicken Sie hier, um diese Datei herunterzuladen.
Ergänzende Datei 4: Probenhalterung B. STL-Datei zum Drucken von Probenhalterung B. Bitte klicken Sie hier, um diese Datei herunterzuladen.
Ergänzende Datei 5: Kollektorflansch. STL-Datei zum Drucken des Kollektorflansches. Bitte klicken Sie hier, um diese Datei herunterzuladen.
Ergänzende Datei 6: Verbindende Metallstange. Technische Zeichnung zum Bau von Metallpleuelstangen. Bitte klicken Sie hier, um diese Datei herunterzuladen.
Diskussion
Das beschriebene Protokoll stellt zwei Innovationen im Bereich des (kardiovaskulären) Tissue Engineering vor: die kostengünstige Herstellung von vollständig 3D-gedruckten Phantomen für das Elektrospinnen und die Verwendung eines vielseitigen Kollektors zur Herstellung anpassungsfähiger, mehrschichtiger Herzklappenblätter.
In jüngster Zeit ist der 3D-Druck zu einem wertvollen Werkzeug für die Herstellung von Laborgeräten geworden, z.B. Bioreaktoren oder Fertigungs- und Testaufbauten11,12. Daher war es möglich, den in dieser Studie vorgestellten Elektrospinnaufbau in kurzer Zeit und zu einem erschwinglichen Budget herzustellen (Tabelle 1). Dies steht im Einklang mit früheren Erkenntnissen für die kostengünstige Herstellung von Elektrospinnaufbauten durch den Einsatz von 3D-Druck13.
Darüber hinaus ist dies nach bestem Wissen der Autoren das erste Mal, dass ein leitfähiges 3D-Druckmaterial verwendet wurde, um einen Elektrospinnsammler für Herzklappenbroschüren herzustellen. Bisher wurden 3D-gedruckte Kollektoren entweder durch Metalllasersintern14 oder mittels nichtleitendem Polymerdruck und anschließender Nachbearbeitung mit einer leitfähigenBeschichtung 15 hergestellt. Im Gegensatz zu diesem neuartigen Ansatz sind diese Verfahren erheblich benachteiligt, da sie teurer sind, viel länger dauern oder mehr Handarbeit erfordern.
Das Elektrospinnen hängt von einer Vielzahl von Variablen ab, die die Morphologie der erzeugten Fasern beeinflussen. Obwohl verschiedene kommerzielle Elektrospinn-Setups auf dem Markt erhältlich sind, verwenden viele Forschungsgruppen hochgradig individualisierte Setups, um ihren spezifischen Anforderungen gerecht zu werden16. Unter Berücksichtigung dessen müssen die in diesem Protokoll beschriebenen Werte (Spannung, Entfernung und Drehzahl) möglicherweise für einzelne Setups angepasst werden und sollten als Ausgangspunkt und nicht als feste Werte betrachtet werden. Weiterhin ist bekannt, dass Umweltparameter einen signifikanten Einfluss auf die Elektrospinnergebnisse haben können17,18. Daher wird dringend empfohlen, zumindest die Temperatur und Luftfeuchtigkeit innerhalb des Elektrospinngeräts zu kontrollieren. Optimale Elektrospinnergebnisse wurden zwischen 15-20% relativer Luftfeuchtigkeit bei einer Temperatur zwischen 21 und 24 °C erzielt. Um diesem Protokoll zu folgen, ist die folgende Ausrüstung unerlässlich: ein Motor, der in der Lage ist, einen Kollektor mit einem Gewicht von ca. 300 g auf eine Drehzahl von 2.000 U / min zu beschleunigen, eine Spritzenpumpe, die für kleine Volumenströme von 1-3 ml / h geeignet ist, und ein zweipoliges Netzteil mit ±20 kV Gleichstrom (DC).
In Übereinstimmung mit früheren Studien war es möglich, die faserige Struktur der elektrogesponnenen Gerüste durch Fluoreszenzmikroskopiesichtbar zu machen 19. Die mehrschichtige Struktur des Gerüsts inklusive der unterschiedlichen Faserorientierungen konnte erfolgreich demonstriert werden. Insbesondere bei der Arbeit mit mehreren Schichten oder mehreren Materialien sollte die Einführung von fluoreszierenden Farbstoffen als Standardverfahren für eine strenge Qualitätskontrolle betrachtet werden. Es könnte die visuelle Bewertung der Ergebnisse nach Änderungen der Parameter oder des Workflow-Protokolls verbessern. Die Anwendung von Farbstoff in Gerüsten, die für die In-vivo- oder In-vitro-Beurteilung verwendet werden, kann nicht empfohlen werden. Dies ist wichtig, um Interferenzen mit etablierten Analysemethoden zu vermeiden.
Die Nachahmung der natürlichen Herzklappenmorphologie ist von großer Bedeutung, um ein gewebetechnisch hergestelltes Replikat herzustellen, das als Herzklappenprothese verwendet werden kann (Abbildung 4B). Es hat sich gezeigt, dass die spezifische Ventilgeometrie einen hohen Einfluss auf den In-vivo-Umbau 20 hat. In diesem Zusammenhang ist der 3D-Druck der Prospektgeometrie für das Elektrospinnen von Vorteil, da Iterationen einfach und schnell zu implementieren sind. Auch die Erstellung personalisierter Klappengeometrien ist denkbar und die anschließende Entwicklung individueller und personalisierter 3D-Modelle von Herzklappenanomalien, beispielsweise für Lehrzwecke, ist möglich.
Die weitere Verbesserung der gewebetechnischen Herzklappeneigenschaften steht im Mittelpunkt der aktuellen Forschungsbemühungen, da mehrere Forschungsgruppen an der Entwicklung mehrschichtiger Gerüste mit definierten Faserorientierungen gearbeitet haben. Masoumi et al. stellten Verbundgerüste aus einer geformten Polyglycerin-Sebacate-Schicht und elektrogesponnenen Polycaprolacton (PCL) -Fasermatten21 her. So könnte eine dreifache Schicht aus zwei orientierten, elektrogesponnenen Schichten erzeugt werden, die durch eine Platte aus mikrofabriziertem Polyglycerin-Sebakat getrennt sind. Im Gegensatz zu den vorhandenen Gerüsten waren sie jedoch weder in einer 3D-Form noch ahmten sie die mittlere Schicht (Spongiosa) adäquat nach. Ein weiterer Ansatz zur Herstellung einer bioinspirierten, gewebetechnisch hergestellten Herzklappe wurde von Jana et al.22,23 verfolgt. Sie produzierten erfolgreich dreischichtige Gerüste mit ausgerichteten Fasern unter Verwendung von Aluminiumkollektoren für die PCL-basierte Elektrospinnung. Auch diese Gerüste wiesen morphologische Unvollkommenheiten auf, da sie nur ein 2D-Aussehen haben und das endgültige Gerüst von Speichen durchzogen ist.
Obwohl das Protokoll detaillierte Informationen darüber enthält, wie dreischichtige 3D-Herzklappenbroschüren hergestellt werden, sind mehrere weitere Schritte erforderlich, um eine tatsächliche Herzklappenprothese zu erstellen. Für die hier beschriebenen Prospekte wird ein Stent von 24 mm Durchmesser empfohlen. Ergänzend zum verwendeten Stent können die Beipackzettel mit zusätzlichen Stützstrukturen zum Nähen versehen werden. Um maximale Flexibilität zu ermöglichen, sind die hier gezeigten Merkblätter nicht auf ein bestimmtes Stent-Design individualisiert. Dies kann durch einfaches Ändern der Vorlage mithilfe von CAD-Software erfolgen.
Obwohl die vorgestellte Methode für das Herzklappen-Tissue-Engineering verwendet wird, wird sie für Elektrospinn-Setups in der Orthopädie24, Urologie25, HNO-Heilkunde26 und anderen leicht anwendbar sein. Die Herstellung anspruchsvoller und/oder individualisierter 3D-Konstrukte ist durch den Einsatz anderer 3D-gedruckter Kollektoren möglich. Obwohl sich das Material des Kollektors verändert hat, bleibt das Prinzip des Elektrospinnensintakt 27. Daher ist die Verwendung verschiedener Polymere theoretisch möglich, obwohl eine Anpassung der Elektrospinnparameter erforderlich sein kann.
Insgesamt beschreibt das vorgestellte Protokoll eine einfache und kostengünstige Möglichkeit, mehrschichtige Herzklappenbeilagen herzustellen. Die Anwendung des 3D-Drucks ermöglicht eine schnelle Anpassung und Modifikation des Kollektors und der Einsätze. Dies ermöglicht die Herstellung patientenspezifischer Prothesen ohne einen komplizierten Herstellungsprozess von beispielsweise Metallsammlern. Mehrere Samples können in einem Durchlauf unter identischen Bedingungen erstellt werden. Daher können materialzerstörende Tests an den Proben durchgeführt werden, mit dem Vorteil, dass (fast) identische übrig bleiben, um das eigentliche Ventil zu bauen. Die Einbeziehung der Druckdateien als Supplemental Files in diese Studie soll die Weiterentwicklung von mehrschichtigen Herzklappengerüsten unterstützen. Diese neue Elektrospinntechnik hat auch ein hohes Potenzial für andere Bereiche der regenerativen Medizin, da modifizierte Kollektoren und andere 3D-gedruckte, spinnende Vorlagen einfach zu implementieren sind.
Offenlegungen
Die Autoren erklären keine Interessenkonflikte.
Danksagungen
Unterstützt wurde diese Arbeit durch das Clinician Scientist Program In Vascular Medicine (PRIME), gefördert durch die Deutsche Forschungsgemeinschaft (DFG), Projektnummer MA 2186/14-1.
Materialien
| Name | Company | Catalog Number | Comments |
| BTC-FR2.5TN.D09 | ZwickRoell GmbH & Co. KG | Traction engine (Tensile tests) | |
| C5-E Motor Controller | Nanotec Electronic GmbH & Co. KG | Motor controll unit | |
| CH1: CPN 30 kV | 0.3 mA | iseg Spezialelectronik GmbH | Power Supply Unit Anode | |
| CH1: CPN 30 kV | 0.3 mA | iseg Spezialelektronik GmbH | Power Supply Unit Kathode | |
| Conductive Composite PLA | ProtoPasta | Conductive PLA | |
| Cura 4.7.1 | Ultimaker BV | Slicing Software Ultimaker, step 1.1.2 | |
| DAPI Stock Solution c = 0.1 mg/mL | Sigma-Aldrich Chemie GmbH | DAPI | |
| Disposable Scalpel No. 23 | FEATHER | Scalpel | |
| Fluorescein (C.I. 45350) M 376.28 g/mol | Carl Roth GmbH + Co. KG | Fluorescein | |
| Fume Hood as per DIN 12924 Class 2 | Köttermann GmbH | Fume Hood | |
| Leica Applicatin Suite X 3.5.5.19976 | Leica Microsystems GmbH | Software for Confocal Laser Scanning Microscope | |
| Luerlock Syringe 20 mL | BD Plastipak | Luerlock Syringe | |
| Metal needle plane 2.50/2.00 x 20 mm | Unimed S.A. | Needle with plane tip | |
| Montage-complet-tubes; inner diameter x outer diameter: 1/16" x 1/8", length 1.000 mm | Bohlender GmbH | F740-28 | Solvent resistant tubes |
| N,N-Dimethylformamide ≥99.8% | Sigma-Aldrich Chemie GmbH | Dimethylformamide | |
| Pellethane 2363 80AE | Velox GmbH Hamburg | Polyurethane | |
| PLA | Ultimaker BV | PLA | |
| Plug&Drive Studio (1.0.4) | Nanotec Electronic GmbH & Co. KG | Motor operation software | |
| SEM Evo LS 10 | Zeiss MicroImaging GmbH | Scanning Electron Microscope | |
| SHT 31-D | Adafruit Industries | Temperature and Humidity Sensor | |
| SolidWorks 2020 CAD Software | Dassault Systèmes | Commercial CAD Software | |
| Sulforhodamine 101 50 mg | Sigma - Aldrich | S 7635 | Texas Red |
| Syringe Pump Model: Fusion 100 | Chemyx Inc. | Syringe Pump | |
| TCS SP8 inverted CEL BMi8 | Leica Microsystems GmbH | Confocal Laser Scanning Microscope | |
| testXpert V11.02 | ZwickRoell GmbH & Co. KG | Software Tensile Test | |
| Tetrahydrofuran ≥99.9% | Sigma-Aldrich Chemie GmbH | Tetrahydrofuran | |
| Type 1511530000202 #980361 | Binder Labortechnik GmbH | Heating Cabinet | |
| Ultimaker 3 Extended | Ultimaker BV | 3D Printer |
Referenzen
- Van Camp, G. Cardiovascular disease prevention. Acta Clinica Belgica. 69 (6), 407-411 (2014).
- Iung, B., Vahanian, A. Epidemiology of valvular heart disease in the adult. Nature Reviews Cardiology. 8 (3), 162-172 (2011).
- Fioretta, E. S., et al. Cardiovascular tissue engineering: From basic science to clinical application. Experimental Gerontology. 117 (1), 1-12 (2019).
- Xue, J., Wu, T., Dai, Y., Xia, Y. Electrospinning and electrospun nanofibers: methods, materials, and applications. Chemical Reviews. 119 (8), 5298 (2019).
- Grande, D., Ramier, J., Versace, D. L., Renard, E., Langlois, V. Design of functionalized biodegradable PHA-based electrospun scaffolds meant for tissue engineering applications. New Biotechnology. 37, 129-137 (2017).
- Tara, S., et al. Well-organized neointima of large-pore poly(l-lactic acid) vascular graft coated with poly(l-lactic-co-ε-caprolactone) prevents calcific deposition compared to small-pore electrospun poly(l-lactic acid) graft in a mouse aortic implantation model. Atherosclerosis. 237 (2), 684-691 (2014).
- Voorneveld, J., Oosthuysen, A., Franz, T., Zilla, P., Bezuidenhout, D. Dual electrospinning with sacrificial fibers for engineered porosity and enhancement of tissue ingrowth. Journal of Biomedical Material Research. 105 (6), 1559-1572 (2017).
- Kishan, A. P., Cosgriff-Hernandez, E. M. Recent advancements in electrospinning design for tissue engineering applications: A review. Journal of Biomedical Materials Research. 105 (10), 2892-2905 (2017).
- Sacks, M. S., David Merryman, W., Schmidt, D. E. On the biomechanics of heart valve function. Journal of Biomechanics. 42 (12), 1804-1824 (2009).
- Buchanan, R. M., Sacks, M. S. Interlayer micromechanics of the aortic heart valve leaflet. Biomechanics and Modeling in Mechanobiology. 13 (4), 813-826 (2014).
- Gensler, M., et al. 3D printing of bioreactors in tissue engineering: A generalised approach. PLoS One. 15 (11), 0242615 (2020).
- Grab, M., et al. Customized 3D printed bioreactors for decellularization-High efficiency and quality on a budget. Artificial Organs. 45 (12), 1477-1490 (2021).
- Huang, J., Koutsos, V., Radacsi, N. Low-cost FDM 3D-printed modular electrospray/electrospinning setup for biomedical applications. 3D Printing in Medicine. 6 (1), 8 (2020).
- Fukunishi, T., et al. Preclinical study of patient-specific cell-free nanofiber tissue-engineered vascular grafts using 3-dimensional printing in a sheep model. Journal of Thoracic and Cardiovascular Surgery. 153 (4), 924-932 (2017).
- Jana, S., Lerman, A. In vivo tissue engineering of a trilayered leaflet-shaped tissue construct. Regenerative Medicine. 15 (1), 1177-1192 (2020).
- Hasan, A., et al. Electrospun scaffolds for tissue engineering of vascular grafts. Acta Biomaterialia. 10 (1), 11-25 (2014).
- Wang, X., Ding, B., Yu, J., Yang, J. Large-scale fabrication of two-dimensional spider-web-like gelatin nano-nets via electro-netting. Colloids and Surfaces B: Biointerfaces. 86 (2), 345-352 (2011).
- Yang, G. -. Z., Li, H. -. P., Yang, J. -. H., Wan, J., Yu, D. -. G. Influence of working temperature on the formation of electrospun polymer nanofibers. Nanoscale Research Letters. 12 (1), 55 (2017).
- Ekaputra, A. K., Prestwich, G. D., Cool, S. M., Hutmacher, D. W. Combining electrospun scaffolds with electrosprayed hydrogels leads to three-dimensional cellularization of hybrid constructs. Biomacromolecules. 9 (8), 2097-2103 (2008).
- Motta, S. E., et al. Geometry influences inflammatory host cell response and remodeling in tissue-engineered heart valves in-vivo. Scientific Reports. 10 (1), 19882 (2020).
- Masoumi, N., et al. Tri-layered elastomeric scaffolds for engineering heart valve leaflets. Biomaterials. 35 (27), 7774-7785 (2014).
- Jana, S., Lerman, A. Behavior of valvular interstitial cells on trilayered nanofibrous substrate mimicking morphologies of heart valve leaflet. Acta Biomaterialia. 85, 142-156 (2019).
- Jana, S., Franchi, F., Lerman, A. Trilayered tissue structure with leaflet-like orientations developed through in vivo tissue engineering. Biomedical Materials. 15 (1), 015004 (2019).
- Zhou, Y., Chyu, J., Zumwalt, M. Recent progress of fabrication of cell scaffold by electrospinning technique for articular cartilage tissue engineering. International Journal of Biomaterials. 2018, 1953636 (2018).
- Zamani, M., Shakhssalim, N., Ramakrishna, S., Naji, M. Electrospinning: application and prospects for urologic tissue engineering. Frontiers in Bioengineering and Biotechnology. 8, 579925 (2020).
- Heilingoetter, A., Smith, S., Malhotra, P., Johnson, J., Chiang, T. Applications of Electrospinning for Tissue Engineering in Otolaryngology. Annals of Otology, Rhinology & Laryngology. 130 (4), 395-404 (2020).
- Xue, J., Xie, J., Liu, W., Xia, Y. Electrospun nanofibers: new concepts, materials, and applications. Accounts of Chemical Research. 50 (8), 1976-1987 (2017).
Nachdrucke und Genehmigungen
Genehmigung beantragen, um den Text oder die Abbildungen dieses JoVE-Artikels zu verwenden
Genehmigung beantragenWeitere Artikel entdecken
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Alle Rechte vorbehalten