Se requiere una suscripción a JoVE para ver este contenido. Inicie sesión o comience su prueba gratuita.
Method Article
Detección rápida de patógenos bacterianos que causan infecciones del tracto respiratorio inferior a través de la amplificación isotérmica mediada por bucle basada en chips microfluídicos
* Estos autores han contribuido por igual
En este artículo
Resumen
Varios patógenos bacterianos pueden causar infecciones del tracto respiratorio y provocar graves problemas de salud si no se detectan con precisión y se tratan con prontitud. La detección rápida y precisa de estos patógenos a través de la amplificación isotérmica mediada por bucle proporciona una gestión y un control eficaces de las infecciones del tracto respiratorio en entornos clínicos.
Resumen
Las infecciones del tracto respiratorio (ITR) se encuentran entre los problemas más comunes en los entornos clínicos. La identificación rápida y precisa de los patógenos bacterianos proporcionará directrices prácticas para el manejo y tratamiento de las infecciones respiratorias crónicas. Este estudio describe un método para detectar rápidamente patógenos bacterianos que causan infecciones del tracto respiratorio a través de la amplificación isotérmica mediada por bucle multicanal (LAMP). LAMP es una herramienta diagnóstica sensible y específica que detecta rápidamente los ácidos nucleicos bacterianos con alta precisión y fiabilidad. El método propuesto ofrece una ventaja significativa sobre los métodos tradicionales de cultivo bacteriano, que requieren mucho tiempo y a menudo requieren una mayor sensibilidad para detectar niveles bajos de ácidos nucleicos bacterianos. En este artículo se presentan resultados representativos de la infección por K. pneumoniae y sus múltiples coinfecciones utilizando LAMP para la detección de muestras (esputo, líquido de lavado bronquial y líquido de lavado alveolar) del tracto respiratorio inferior. En resumen, el método LAMP multicanal proporciona un medio rápido y eficiente para identificar patógenos bacterianos únicos y múltiples en muestras clínicas, lo que puede ayudar a prevenir la propagación de patógenos bacterianos y ayudar en el tratamiento adecuado de las ITR.
Introducción
Las infecciones del tracto respiratorio (ITR) causadas por patógenos bacterianos contribuyen principalmente a la morbilidad y mortalidad en todo el mundo1. Se define como cualquier síntoma de las vías respiratorias superiores o inferiores acompañado de fiebre que dura 2-3 días. Si bien la infección de las vías respiratorias superiores es más común que la infección de las vías respiratorias inferiores, las infecciones crónicas y recurrentes de las vías respiratorias también son afecciones clínicas comunes, que plantean grandes riesgos para las personas y suponen una carga significativa para los sistemas de salud2. Los patógenos bacterianos comunes de las RTI incluyen Streptococcus pneumoniae3, Haemophilus influenzae4, Staphylococcus aureus, Escherichia coli, Klebsiella pneumoniae, Stenotrophomonas maltophilia, entre otros. Estas bacterias patógenas suelen colonizar las superficies mucosas de la nasofaringe y el tracto respiratorio superior del huésped, causando síntomas típicos de las infecciones respiratorias agudas, como dolor de garganta y bronquitis. Causan neumonía cuando se propagan desde el tracto respiratorio superior a áreas estériles del tracto respiratorio inferior y pueden propagarse de persona a persona a través del tracto respiratorio5. En casos graves, también pueden provocar enfermedades bacterianas invasivas, especialmente neumonía bacteriémica, meningitis y sepsis, que son las principales causas de morbilidad y mortalidad en personas de todos los grupos de edad en todo el mundo.
Las pruebas tradicionales para las ITR implican el cultivo microbiológico utilizando hisopos faríngeos y muestras respiratorias de esputo6. Además, las pruebas serológicas, como el ensayo de inmunoabsorción enzimática (ELISA), detectan anticuerpos o antígenos en el suero, mientras que las pruebas de aglutinación observan la reacción de aglutinación de anticuerpos y antígenos para detectar la infección7. El cultivo microbiano se considera el estándar de oro para el diagnóstico de las ITR, pero su baja tasa de positividad del cultivo, su escasa fiabilidad y su largo ciclo de detección limitan la eficacia diagnóstica8. En realidad, el diagnóstico rápido y preciso de las infecciones respiratorias agudas es crucial para la erradicación precisa del patógeno bacteriano. Los métodos de detección rápidos y eficaces pueden ayudar a reducir la tasa de transmisión de patógenos, acortar la duración de la infección y disminuir el uso innecesario de antibióticos 9,10. Los métodos basados en la biología molecular aceleran significativamente la detección, como la reacción en cadena de la polimerasa (PCR), que amplifica la secuencia de ADN de un gen objetivo para detectar patógenos. Sin embargo, la PCR tradicional requiere un equipo complejo de ciclo de temperatura, que es engorroso y requiere mucho tiempo. Además, cada amplificación de ADN mediante PCR (excepto la PCR en tiempo real) concluye con la separación electroforética del producto, lo que también lleva tiempo. La visualización del producto requiere tintes, muchos de los cuales son mutagénicos o cancerígenos. Por lo tanto, es imperativo desarrollar continuamente nuevos métodos y tecnologías para diagnosticar patógenos bacterianos RTI.
La amplificación isotérmica mediada por bucle (LAMP) es una tecnología molecular novedosa y emergente desarrollada inicialmente por Notomi et al. en 200011. LAMP puede amplificar el ADN en condiciones isotérmicas estables sin equipos complejos de ciclo de temperatura, lo que lo hace adecuado para la detección rápida y reduce la complejidad y el costo del equipo12. LAMP puede detectar bajas concentraciones de ADN objetivo con alta sensibilidad13. Utiliza múltiples cebadores específicos para mejorar la selectividad de las secuencias diana y reducir la posibilidad de falsos positivos14. Poco a poco, LAMP se está utilizando ampliamente en los laboratorios clínicos debido a su facilidad, rapidez e intuitivo funcionamiento, incluso para detectar RTI. En este estudio, investigamos la efectividad de LAMP en la detección de RTI más bajos en muestras clínicas (esputo, líquido de lavado bronquial y líquido de lavado alveolar), como se muestra en la Figura 1. Es evidente que LAMP ofrece ventajas como la velocidad, la sensibilidad y la facilidad de uso sobre las pruebas tradicionales en la detección de RTI más bajos, lo que lo convierte en una aplicación prometedora.
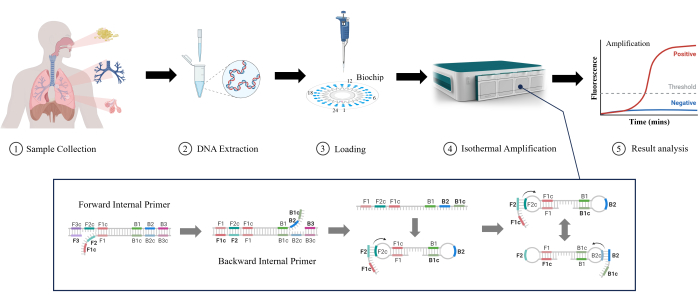
Figura 1: Ilustración esquemática del método de detección LAMP. Haga clic aquí para ver una versión más grande de esta figura.
Protocolo
Todas las muestras para este estudio fueron evaluadas y aprobadas por el Comité de Revisión de Ética del Hospital Popular Provincial de Guangdong (Número de aprobación: KY2023-1114-01). Todos los participantes firmaron un consentimiento informado por escrito antes de los experimentos. Los reactivos y equipos utilizados para el estudio se enumeran en la Tabla de Materiales. Las abreviaturas utilizadas en el protocolo se enumeran en la Tabla Suplementaria 1.
1. Recogida de muestras clínicas de las vías respiratorias inferiores
- Recolección de esputo
- Limpie la cavidad bucal y los dientes con agua limpia, asegurando la extracción de la dentadura postiza si corresponde. Toser enérgicamente para expulsar el esputo respiratorio profundo en un recipiente de esputo (mínimo 0,6 mL).
- Evite la contaminación con saliva o secreción nasal. Si la tos es difícil, administrar la inhalación de una solución de NaCl de 100 g/L a 45 °C para facilitar la expectoración. Transfiera el espécimen a un recipiente estéril y hermético.
NOTA: Asegúrese de que las muestras de esputo se recolecten por la mañana y antes de cualquier uso de medicamentos antibacterianos.
- Líquido de lavado bronquial (BLF)
- Inserte el cabezal colector en la tráquea desde la fosa nasal o el sitio de la traqueostomía (aproximadamente 30 cm de profundidad). Inyecte 5 mL de solución salina, establezca presión negativa, gire el cabezal del colector y retírelo lentamente.
- Recoja la mucosidad extraída y enjuague el colector una vez con una solución de muestreo (solución salina fisiológica o agua estéril para inyección). Alternativamente, conecte un catéter urinario pediátrico a una jeringa de 50 ml como sustituto de la recolección.
- Líquido de lavado alveolar (ALF)
- Identificar la ubicación de la lesión a través de exámenes de imágenes del tórax. Seleccione el área más significativa o de progreso rápido para el lavado.
- Inyectar 1-2 mL de lidocaína al 2% en el segmento bronquial a través del canal de biopsia durante el lavado, proporcionando anestesia local para el segmento pulmonar lavado15. Para los pacientes bajo anestesia general intravenosa que aún exhiben fuertes reacciones en las vías respiratorias, inyecte 1-2 mL de lidocaína al 2%.
- Después de la anestesia local, inserte un broncoscopio de fibra óptica a través de la boca o la nariz, pasando a través de la faringe hasta el bronquio del lóbulo medio derecho o el segmento lingual del pulmón izquierdo. Coloque su punta en la abertura de la rama bronquial e introduzca lentamente solución salina fisiológica estéril.
- Administrar 30-50 mL de solución salina por sesión, con un volumen de 100-250 mL (máx. 300 mL). Recoja la mucosidad extraída en un recipiente estéril sellado.
2. Extracción de ADN
- En función de la viscosidad de las muestras del tracto respiratorio inferior, añada una cantidad adecuada de NaOH al 10%. Para muestras con baja viscosidad, agregue 2-3 veces el volumen de la muestra de solución licuadora. Para muestras con viscosidad moderada, agregue 5-6 veces el volumen de la muestra de solución licuadora. Para muestras con alta viscosidad, agregue de 8 a 10 veces el volumen de la muestra de solución licuadora.
- Ajuste el volumen de NaOH al 10% de acuerdo con la viscosidad de la muestra. Dispersar las muestras de la forma más uniforme posible utilizando un mezclador de vórtice durante 15 s e incubar a 37 °C durante 30 min para la licuefacción.
NOTA: Para muestras más espesas, aumente el volumen de NaOH o extienda el tiempo de licuefacción. La calidad de licuefacción de las muestras influye directamente en la eficiencia de la extracción posterior. Idealmente, las muestras licuadas deben exhibir una consistencia consistente y no pegajosa.
- Ajuste el volumen de NaOH al 10% de acuerdo con la viscosidad de la muestra. Dispersar las muestras de la forma más uniforme posible utilizando un mezclador de vórtice durante 15 s e incubar a 37 °C durante 30 min para la licuefacción.
- Pipetear 1 mL de la muestra licuada en un tubo de centrífuga de 1,5 mL. Centrifugar a una velocidad de 15.777 × g durante 5 min a 2-6 °C, luego use una pipeta para eliminar y desechar el sobrenadante.
NOTA: Al aspirar la muestra, evite extraer impurezas del fondo del tubo; Si hay muchas impurezas, la muestra se puede centrifugar a 1.753-2.739 × g durante 1 minuto antes de la aspiración. - Agregue 1 ml de solución de lavado al tubo de centrífuga y al vórtice para levantar el precipitado desde el fondo del tubo. No es necesario dispersarlo por completo.
- Centrifugar la solución a 15.777 × g durante 5 minutos, desechar el sobrenadante y tratar de no tocar el precipitado.
NOTA: Asegúrese de retirar completamente la solución de lavado para evitar que afecte la amplificación posterior.
- Centrifugar la solución a 15.777 × g durante 5 minutos, desechar el sobrenadante y tratar de no tocar el precipitado.
- Agregue 100 μL de solución de extracción de ácido nucleico al tubo de centrífuga. Utilice una pipeta para aspirar y mezclar bien el precipitado. Transfiera el líquido y el precipitado juntos a un tubo de extracción de ácido nucleico. La composición de la solución de extracción de ácido nucleico se presenta en la Tabla 1.
- Coloque los tubos de extracción de ácido nucleico en un mezclador de vórtice y vórtice a velocidad media durante al menos 5 minutos. Después del vórtice, transfiera los tubos de extracción de ácido nucleico a un baño de metal con una temperatura constante y caliente a 100 °C durante 5 min.
- Centrifugar a 15.777 × g a 2-6 °C durante 5 min y reservar.
NOTA: Si la reacción de amplificación por PCR se realiza dentro de las 24 horas, el ácido nucleico se puede almacenar a 4 °C. Después de la amplificación, almacene el ácido nucleico a -20 °C. Para el almacenamiento a largo plazo (más de 24 h), almacene el ácido nucleico a -20 °C. Cuando esté listo para usar de nuevo, descongele la muestra de forma natural, mezcle el vórtice, caliéntelo en un baño de agua a 95 °C durante 5 minutos, centrifugue a 10.956 × g durante 1 minuto y utilice el sobrenadante para la amplificación por PCR.
| Solución | Componentes | Número | Especificación |
| Solución de lavado | EDTA de 10 mM | 1 botella | 24 mL/frasco |
| Reactivo de extracción de ácidos nucleicos | 10 mM de Tris-HCl, 1 mM de EDTA, conservantes de ácidos nucleicos | 2 tubos | 1,2 mL/frasco |
| Tubo de extracción de ácido nucleico | Cuentas de vidrio | 1 bolsa | 24 botellas/bolsa |
Tabla 1: Composición del reactivo de extracción de ácidos nucleicos.
3. Amplificación isotérmica mediada por bucle y chip de microfluido
- Reactivo y chip microfluídico
- Realizar reacciones de amplificación isotérmica en un chip microfluídico en forma de disco (ver Tabla de Materiales). Realice la amplificación a temperatura constante a 65 °C.
- Realice análisis de fluorescencia en tiempo real utilizando un método de incorporación de colorante fluorescente14 en el analizador de ácido nucleico de chip microfluídico de amplificación a temperatura constante. Observe una curva de amplificación en forma de S para muestras positivas utilizando una polimerasa con funcionalidad de desplazamiento de hebra.
- Amplificación isotérmica mediada por bucle
- Diríjase a seis regiones de secuencia con cuatro cebadores específicos, incluidos dos cebadores internos y dos cebadores externos (proporcionados con el kit LAMP).
NOTA: El ADN se replica y amplifica continuamente a una temperatura constante utilizando una ADN polimerasa con funcionalidad de desplazamiento de hebra. El proceso de reacción involucra la etapa de síntesis de plantilla en forma de mancuerna, la etapa de amplificación cíclica, la elongación y la etapa de reciclaje, formando finalmente una mezcla de fragmentos de ADN con estructuras de bucle de tallo y similares a coliflor. Consulte las instrucciones del kit para obtener información detallada (Archivo complementario 1). - Agregue cebadores de dos bucles al sistema de reacción para mejorar la eficiencia de la reacción, que se une a las estructuras de vástago-bucle, iniciando la síntesis de desplazamiento de hebra y la replicación cíclica. La composición del kit de detección de ácidos nucleicos para patógenos del tracto respiratorio se presenta en la Tabla 2.
NOTA: El kit de reactivos utiliza el método LAMP. El principio se basa en el equilibrio dinámico del ADN a unos 65 °C, donde cualquier cebador que se extienda a través del emparejamiento de bases en el sitio complementario del ADN bicatenario hace que la otra hebra se disocie, formando una sola hebra.
- Diríjase a seis regiones de secuencia con cuatro cebadores específicos, incluidos dos cebadores internos y dos cebadores externos (proporcionados con el kit LAMP).
- Chip microfluídico
NOTA: Cada chip microfluídico (ver Tabla de Materiales) está equipado con 24 pozos de reacción numerados en sentido contrario a las agujas del reloj, con la entrada y salida del pozo 1 correspondiente al pozo de reacción 1 (Figura 2). Un conjunto específico de cebadores para la amplificación y detección de una secuencia diana de ácido nucleico particular está incrustado y fijado en cada pocillo de reacción.- Mezcle la muestra de ADN con el reactivo de amplificación. Inyecte la mezcla en el chip y distribúyala a cada centrífuga del pozo de reacción a 1.000 × g durante 30 s a temperatura ambiente.
NOTA: Las reacciones de amplificación isotérmica independientes y la detección de fluorescencia en tiempo real coexisten en cada pozo de reacción en el chip. Si se detecta una curva de amplificación en forma de S en un pocillo de reacción en particular, el índice de detección correspondiente para ese pocillo es positivo.
- Mezcle la muestra de ADN con el reactivo de amplificación. Inyecte la mezcla en el chip y distribúyala a cada centrífuga del pozo de reacción a 1.000 × g durante 30 s a temperatura ambiente.
| Componentes | Composición | Número |
| Chip | Imprimaciones | 12 plazas |
| Película de sellado | / | 1 hoja |
| Reactivo de amplificación isotérmica | Colorante fluorescente, Enzima | 270 μL/tubo |
| Control positivo | ADN genómico de Escherichia coli | 160 μL/tubo |
Tabla 2: Composición del kit de detección de ácidos nucleicos para patógenos del tracto respiratorio.
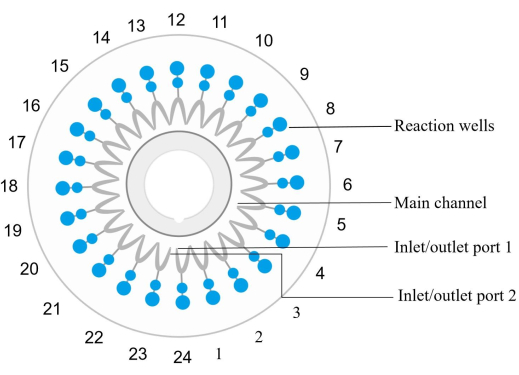
Figura 2: Diagrama de la estructura del chip de disco. Los pozos de reacción se numeran secuencialmente en sentido contrario a las agujas del reloj, donde el puerto de entrada/salida 1 corresponde al pozo de reacción número 1. Los pozos de reacción 1, 4, 7, 10, 13, 16, 19, 22 y 24 son controles negativos. El pozo de reacción 6 es un control positivo (E. coli). El pozo de reacción 12 es un control positivo interno y el pozo de reacción 23 es un control positivo externo. El pozo de reacción 2 detecta spn. El pozo de reacción 3 detecta sau. El pozo de reacción 5 detecta MRSA. El pozo de reacción 8 detecta kpn. El pozo de reacción 9 detecta pae. El pozo de reacción 11 detecta aba. El pozo de reacción 14 detecta sma. El pozo de reacción 15 detecta hin. Consulte la Tabla 5 para obtener detalles de muestra. Haga clic aquí para ver una versión más grande de esta figura.
4. Preparación de muestras y detección de bacterias
- Preparar el sistema de reacción de amplificación isotérmica
- Tome el reactivo de amplificación isotérmica del kit y deje que se descongele completamente a temperatura ambiente. Agite suavemente para mezclar bien y centrifugue brevemente para recoger en el fondo del tubo.
- En el área de almacenamiento y preparación de reactivos, pipetee 20 μL del reactivo de amplificación isotérmica en un tubo de centrífuga preparado de 200 μL. Cubra el tubo y muévalo al área de preparación de muestras con un tubo de centrífuga por muestra.
- En el área de preparación de la muestra, agregue 34,5 μL de la muestra de ácido nucleico objetivo. Agite suavemente para mezclar bien y centrifugue brevemente para recoger en el fondo del tubo. El volumen total de cada sistema de reacción de amplificación de ácido nucleico es de 54,5 μL (Tabla 3).
- Procedimiento de carga de virutas
- En el empaque del chip, etiquete el número de muestra. Abra el chip microfluídico con la etiqueta del embalaje hacia arriba.
- Coloque el chip con los puertos de entrada y salida hacia arriba. Con una pipeta, extraiga 50 μL del sistema de reacción de amplificación preparado y añádalo al canal principal del chip a través del puerto de entrada. Deje de agregar cuando el canal principal esté lleno y limpie rápidamente cualquier exceso de líquido alrededor de los puertos de entrada y salida con un pañuelo sin pelusa.
- Use pinzas para recoger una película de sellado y cubrirla sobre los puertos de entrada y salida. Presione una punta de pipeta limpia sobre la película de sellado en una dirección. Asegúrese de que haya un sello hermético.
- Reacción de qPCR
- Una vez que la fuente de luz del analizador de ácido nucleico haya completado el precalentamiento, haga clic en el botón Abrir bandeja . Coloque la viruta con la parte delantera hacia arriba en la bandeja, asegurándose de que el pequeño cilindro de ubicación emerja del espacio central de la viruta para asegurarla. Alinee el dispositivo de posicionamiento central en la bandeja con el orificio central grande en el chip.
- Haga clic en el botón Cerrar bandeja para insertar el chip en el analizador de ácido nucleico.
- En el área Información de muestra de la interfaz de detección, introduzca la información para analizar la muestra. El número de muestra, el número de chip y el tipo de muestra son obligatorios; otros son opcionales.
- Haga clic en el botón Iniciar detección en el área de operación para iniciar la detección de muestras. El instrumento realizará pruebas de muestra de acuerdo con el programa preestablecido.
NOTA: Una vez completada la detección, el software que acompaña al dispositivo realizará automáticamente el análisis de datos. Al mismo tiempo, el analizador de ácido nucleico iniciará un proceso de enfriamiento automático. Una vez que la temperatura desciende a 37 °C, el instrumento abre automáticamente la bandeja y expulsa el chip para su recuperación. Los resultados serán interpretados automáticamente por el sistema (Tabla 4).
- Normas de control de calidad
- Un control de calidad positivo y nueve controles de calidad negativos están incluidos en cada chip de este kit de reactivos. Asegúrese de que los resultados de detección del control de calidad positivo sean positivos y, al mismo tiempo, los resultados de los nueve controles de calidad negativos sean negativos.
NOTA: Los resultados se muestran en el lado derecho de la imagen indicando "Resultados del control de calidad: Experimento normal (Normal positivo, Normal negativo)", lo que indica que los resultados de la prueba son válidos. Es necesario repetir la prueba si algún resultado es incorrecto y el resultado de la prueba de muestra se considera inválido. En el chip se incluye un control interno positivo que utiliza cebadores específicos para humanos, cuyo resultado es positivo para las pruebas de muestras clínicas, mientras que es negativo si la muestra tiene un bajo contenido de ADN genómico humano, lo que indica un recuento de células más bajo. En tales casos, vuelva a recolectar y volver a analizar las muestras.
- Un control de calidad positivo y nueve controles de calidad negativos están incluidos en cada chip de este kit de reactivos. Asegúrese de que los resultados de detección del control de calidad positivo sean positivos y, al mismo tiempo, los resultados de los nueve controles de calidad negativos sean negativos.
- Análisis de resultados
- Una vez completada la detección, utilice el método de máximo de la segunda derivada combinado con algoritmos protegidos comercialmente en el software para calcular el primer punto de inflexión de la curva de amplificación en forma de S durante la fase de amplificación rápida. Los detalles se describen en la parte de "Principios de la prueba" de las instrucciones del kit de detección de ácido nucleico de patógenos respiratorios (archivo complementario 1).
NOTA: El valor TP es la diferencia de tiempo entre el punto de inflexión y el origen. El resultado se interpreta en función de los valores de TP y juicio positivo. Si el valor TP de un índice de detección es menor o igual que el valor de juicio positivo de ese índice, se interpreta como positivo. Si el valor de TP excede el valor de juicio positivo, se interpreta como negativo, de acuerdo con los criterios de "valor de decisión positivo" en las instrucciones. El área "Área de la curva de fluorescencia" muestra la curva normalizada, y el área "Resultado de la detección" muestra los resultados del control de calidad y la detección para cada parámetro (Tabla 5).
- Una vez completada la detección, utilice el método de máximo de la segunda derivada combinado con algoritmos protegidos comercialmente en el software para calcular el primer punto de inflexión de la curva de amplificación en forma de S durante la fase de amplificación rápida. Los detalles se describen en la parte de "Principios de la prueba" de las instrucciones del kit de detección de ácido nucleico de patógenos respiratorios (archivo complementario 1).
| Reactivo | Volumen (μl) |
| Reactivo de amplificación isotérmica | 20 |
| Plantilla de ADN | 34.5 |
Tabla 3: Sistema de reacción de amplificación isotérmica.
| Paso | Uno | Dos |
| Temperatura (°C) | 37 | 65 |
| Tiempo (min) | 3 | 47 |
Tabla 4: Programa de reacción de amplificación de ácidos nucleicos.
| Nombre del indicador | Valor de control positivo |
| Streptococcus pneumoniae (sp) | 30 |
| Staphylococcus aureus (sau) | 34 |
| Staphylococcus aureus resistente a la meticilina (SARM) | 22 |
| Klebsiella pneumoniae (kpn) | 29 |
| Pseudomonas aeruginosa (pae) | 36 |
| Acinetobacter baumannii (aba) | 36 |
| Stenotrophomonas maltophilia (sma) | 27 |
| Haemophilus influenzae (hin) | 36 |
Tabla 5: Valor de control positivo para el indicador de infección.
Resultados
Este experimento emplea tecnología de amplificación isotérmica, realizando reacciones en un chip de disco microfluídico. La reacción se produce en un analizador de ácido nucleico de chip microfluídico, que emplea un método de inserción de colorante de fluorescencia. La reacción isotérmica se realiza a una temperatura constante de 65 °C y el análisis de fluorescencia en tiempo real se lleva a cabo simultáneamente. Las muestras positivas se amplifican bajo la acción de la polimerasa con funcionalidad de desp...
Discusión
Las infecciones del tracto respiratorio son infecciones prevalentes asociadas al hospital, que imponen graves consecuencias a los pacientes y aumentan las tasas de mortalidad16. La identificación oportuna y precisa de los patógenos potenciales, seguida de antibióticos eficaces, es la clave para el éxito del tratamiento y la mejora del pronóstico, especialmente dadas las limitaciones inherentes a los métodos de cultivo tradicionales17. En este estudio, utilizamos un m?...
Divulgaciones
Los autores declaran no tener conflicto de intereses.
Agradecimientos
Apreciamos enormemente el apoyo financiero brindado por la Fundación de Investigación Básica y Básica Aplicada de Guangdong (Subvención No. 2022A1515220023) y la Fundación de Investigación para Talentos Avanzados del Hospital Popular Provincial de Guandong (Subvención No. KY012023293).
Materiales
| Name | Company | Catalog Number | Comments |
| Bath Incubator(MK2000-2) | ALLSHENG | Provide a constant temperature environment | |
| Bronchial lavage fluid collector head | TIANPINGHUACHANG | SEDA 20172081375 | Collecting bronchoalveolar lavage fluid |
| Fiberoptic bronchoscope | OLYMPUS | SEDA 20153062703 | A flexible bronchoscope equipped with a fiberoptic light source and camera, to visually examine the airways and structures within the lungs. Assist in collecting bronchoalveolar lavage |
HR1500- B2 B2 | Haier | SEDA 20183541642 | Biosafety cabinet |
| NAOH | MACKLIN | S817977 | Liquefy viscous lower respiratory tract sample |
| Nucleic acid detection kit for respiratory tract pathogens | Capitalbio Technology | SEDA 20173401346 | Testing for bacteria infection |
| Nucleic acid extraction reagent | Capitalbio Technology | SEDA 20160034 | For DNA extraction |
| RTisochip-W | Capitalbio Technology | SEDA 20193220539 | Loop-mediated Isothermal Amplification |
| THERMO ST16R | Thermo Fisher Scientific | SEDA 20180585 | Centrifuge the residual liquid off the wall of the tube. |
| Vortex mixer VM-5005 | JOANLAB | For mixing reagent |
Referencias
- GBD 2016 Lower Respiratory Infections Collaborators. Estimates of the global, regional, and national morbidity, mortality, and aetiologies of lower respiratory infections in 195 countries, 1990-2016: A systematic analysis for the global burden of disease study 2016. Lancet Infect Dis. 18 (11), 1191-1210 (2018).
- Niederman, M. S., Torres, A. Respiratory infections. Eur Respir Rev. 31 (166), 220150 (2022).
- Weiser, J. N., Ferreira, D. M., Paton, J. C. Streptococcus pneumoniae: Transmission, colonization and invasion. Nat Rev Microbiol. 16 (6), 355-367 (2018).
- Watt, J. P., et al. Burden of disease caused by Haemophilus influenzae type b in children younger than 5 years_ global estimates. Lancet. 374 (9693), 903-911 (2009).
- Kadioglu, A., Weiser, J. N., Paton, J. C., Andrew, P. W. The role of streptococcus pneumoniae virulence factors in host respiratory colonization and disease. Nat Rev Microbiol. 6 (4), 288-301 (2008).
- Popova, G., Boskovska, K., Arnaudova-Danevska, I., Smilevska-Spasova, O., Jakovska, T. Sputum quality assessment regarding sputum culture for diagnosing lower respiratory tract infections in children. Open Access Maced J Med Sci. 7 (12), 1926-1930 (2019).
- Nuyttens, H., Cyncynatus, C., Renaudin, H., Pereyre, S., Identification Bébéar, C. expression and serological evaluation of the recombinant ATP synthase beta subunit of mycoplasma pneumoniae. BMC Microbiol. 10 (1), 216 (2010).
- Noviello, S., Huang, D. B. The basics and the advancements in diagnosis of bacterial lower respiratory tract infections. Diagnostics (Basel). 9 (2), 37 (2019).
- Hanson, K. E., et al. Molecular testing for acute respiratory tract infections: Clinical and diagnostic recommendations from the IDSA's diagnostics committee. Clin Infect Dis. 71 (10), 2744-2751 (2020).
- Daniel Reynolds, J. P. B., et al. The threat of multidrug-resistant/extensively drug-resistant gram-negative respiratory infections: Another pandemic. Eur Respir Rev. 31 (166), 220068 (2022).
- T Notomi, H. O., et al. Loop-mediated isothermal amplification of DNA. Nucleic Acids Res. 28 (12), 63 (2000).
- Soroka, M., Wasowicz, B., Rymaszewska, A. Loop-mediated isothermal amplification (LAMP): The better sibling of PCR. Cells. 10 (8), 1931 (2021).
- Mori, Y., Kitao, M., Tomita, N., Notomi, T. Real-time turbidimetry of lamp reaction for quantifying template DNA. Biophys J. 59 (2), 145-157 (2004).
- Parida, M., Sannarangaiah, S., Dash, P. K., Rao, P. V., Morita, K. Loop mediated isothermal amplification (LAMP): A new generation of innovative gene amplification technique: Perspectives in clinical diagnosis of infectious diseases. Rev Med Virol. 18 (6), 407-421 (2008).
- Chinese Medical Association Respiratory Branch Critical Care Medicine Group, Working Committee on Critical Care Medicine of the Chinese Physicians Association Respiratory Physicians Branch. Standardization of collection, submission, testing, and interpretation of bronchoalveolar lavage fluid in ICU patients. Chin J Tubere Respir Dis. 43 (9), 744-756 (2020).
- Koch, A. M., Nilsen, R. M., Eriksen, H. M., Cox, R. J., Harthug, S. Mortality related to hospital-associated infections in a tertiary hospital: Repeated cross-sectional studies between 2004-2011. Antimicrob Resist Infect Control. 4 (1), 57 (2015).
- Seymour, C. W. F. G., et al. Time to treatment and mortality during mandated emergency care for sepsis. N Engl J Med. 376 (23), 2235-2244 (2017).
- Choi, C. W., Hyun, J. W., Hwang, R. Y., Powell, C. A. Loop-mediated isothermal amplification assay for detection of candidatus Liberibacter asiaticus: A causal agent of citrus huanglongbing. Plant Pathol. 34 (6), 499-505 (2018).
- Büscher, P., Njiru, Z. K. Loop-mediated isothermal amplification technology: Towards point of care diagnostics. PLoS Negl Trop Dis. 6 (6), e1572 (2012).
- Notomi, T., Mori, Y., Tomita, N., Kanda, H. Loop-mediated isothermal amplification (LAMP): Principle, features, and future prospects. J Microbiol. 53 (1), 1-5 (2015).
- Ajibola, O., Gulumbe, B., Eze, A., Obishakin, E. Tools for detection of schistosomiasis in resource limited settings. Medical Sciences. 6 (2), 39 (2018).
- Kumar, Y. S. B., et al. Loop-mediated isothermal amplification (LAMP): A rapid and sensitive tool for quality assessment of meat products. Compr Rev Food Sci Food SAF. 16 (6), 1359-1378 (2017).
- Hongling Ou, Y. W., et al. Rapid detection of multiple pathogens by the combined loop-mediated isothermal amplification technology and microfluidic chip technology. Ann Palliat Med. 10 (10), 11053-11066 (2021).
- Liang Wang, J. -. X. L., et al. Quantitative polymerase chain reaction (qPCR)-based rapid diagnosis of helicobacter pylori infection and antibiotic resistance. J Vis Exp. (197), e65689 (2023).
- Jing-Wen Lyu, B. X., et al. Rapid prediction of multidrug-resistant klebsiella pneumoniae through deep learning analysis of SERS spectra. Microbiol Spectr. 11 (2), e0412622 (2023).
- Wei Liu, J. -. W. T., et al. Discrimination between carbapenem-resistant and carbapenem-sensitive klebsiella pneumoniae strains through computational analysis of surface-enhanced Raman spectra a pilot study. Microbiol Spectr. 10 (1), e0240921 (2022).
- Zhang, L. Y., et al. Classification and prediction of klebsiella pneumoniae strains with different MLST allelic profiles via SERS spectral analysis. Peer J. 11, e16161 (2023).
- Zhi Liu, Q. Z., et al. Rapid and sensitive detection of salmonella in chickens using loop-mediated isothermal amplification combined with a lateral flow dipstick. J Microbiol Biotechnol. 29 (3), 454-464 (2019).
- Chen, F., et al. Fully Integrated microfluidic platform for multiplexed detection of hunov by a dynamic confined-space-implemented one-pot RPA-LAMP system. Adv Sci (Weinh). 21, e2306612 (2023).
Reimpresiones y Permisos
Solicitar permiso para reutilizar el texto o las figuras de este JoVE artículos
Solicitar permisoThis article has been published
Video Coming Soon
ACERCA DE JoVE
Copyright © 2025 MyJoVE Corporation. Todos los derechos reservados