A subscription to JoVE is required to view this content. Sign in or start your free trial.
Method Article
מדידה של חומצת שומן β-חמצון בהשעיה של הפטוציטים עכברים מבודדים טריים
* These authors contributed equally
In This Article
Summary
חמצון β חומצות שומן הוא מסלול מטבולי חיוני האחראי על הפקת אנרגיה בסוגי תאים רבים ושונים, כולל הפטוציטים. כאן אנו מתארים שיטה למדידת חמצון-β חומצות שומן בהפטוציטים ראשוניים שזה עתה בודדו באמצעות 14חומצה פלמיטית המסומנת כ-C.
Abstract
חמצון β של חומצות שומן הוא מסלול מטבולי מרכזי כדי לענות על דרישות האנרגיה של הכבד ולספק מצעים וקו-פקטורים לתהליכים נוספים, כגון קטוגנזה וגלוקונאוגנזה, החיוניים לשמירה על הומאוסטזיס של גלוקוז בכל הגוף ולתמיכה בתפקוד איברים חוץ-כבדיים במצב של צום. חומצת שומן β-חמצון מתרחשת בתוך המיטוכונדריה והפרוקסיזומים ומווסתת באמצעות מנגנונים מרובים, כולל ספיגה והפעלה של חומצות שומן, רמות ביטוי אנזימים וזמינות של קו-פקטורים כגון קו-אנזים A ו-NAD+. במבחנים המודדים חומצות שומן β-חמצון בהומוגנטים של הכבד, ליזה של תאים והתוספת הנפוצה של רמות סופראפיזיולוגיות של קו-פקטורים מסווים את ההשפעות של מנגנוני ויסות אלה. יתר על כן, שלמות האברונים בהומוגנטים קשה לשליטה ויכולה להשתנות באופן משמעותי בין ההכנות. המדידה של חומצת שומן β חמצון בהפטוציטים ראשוניים שלמים מתגברת על המלכודות הנ"ל. פרוטוקול זה מתאר שיטה למדידת חומצת שומן β-חמצון בתרחיף של הפטוציטים של עכברים ראשוניים שבודדו זה עתה, עם 14חומצה פלמיטית עם תווית C. על ידי הימנעות משעות עד ימים של תרבית, לשיטה זו יש יתרון בכך שהיא משמרת טוב יותר את רמות ביטוי החלבון ואת פעילות המסלולים המטבוליים של הכבד המקורי, כולל הפעלת חומצת שומן β חמצון שנצפתה בהפטוציטים שבודדו מעכברים בצום בהשוואה לעכברים שניזונו.
Introduction
חמצון β של חומצות שומן הוא תהליך חיוני בחילוף החומרים של השומנים, המספק מסלול קטבולי לאיזון סינתזת חומצות השומן וצריכתן מהתזונה. תהליך זה מייצר אנרגיה עבור איברים רבים, כולל שריר הלב, קליפת הכליות והכבד הצום, ומשתמש בחומצות שומן המתקבלות מהתזונה, ליפוליזה של רקמת השומן ומאגריהטריגליצרידים הפנימיים 1,2.
חמצון של חומצת שומן דרך מסלול החמצון β גורם לקיצור רציף של שרשרת האציל השומנית על ידי שני פחמנים בו זמנית, המשתחררים כאצטיל-CoA, ותהליך זה מתרחש הן במיטוכונדריה והן בפרוקסיזומים. בעוד שרוב חומצות השומן עוברות רק חמצון β, חלקן מתחמצנות בפחמנים שונים לפני שהן נכנסות למסלול זה. לדוגמה, חומצות שומן בתחליפי 3-מתיל, כגון חומצה פיטנית, עוברות הסרה של פחמן אחד על ידי חמצון α בפרוקסיזומים לפני שהן נכנסות למסלול החמצון β. באופן דומה, חומצות שומן מסוימות מומרות תחילה לחומצות שומן דיקרבוקסיליות על ידי חמצון של קבוצת המתיל הטרמינלית (ω-חמצון) ברשתית האנדופלסמית לפני שהן עוברות חמצון מועדף בפרוקסיזומים על ידי חמצון β3.
ללא קשר לאברון הספציפי, יש להמיר תחילה חומצת שומן לתיואסטר קו-אנזים A (CoA), או אציל-CoA, כדי להתחמצן דרך מסלול החמצון β. β-חמצון של אציל-CoAs ארוכי שרשרת במטריצה המיטוכונדרית דורש את מעבורת קרניטין לטרנסלוקציה שלהם, כאשר קרניטין פלמיטואיל-טרנספראז 1 (CPT1) מזרז את ההמרה של אציל-CoAs לאציל-קרניטין והוא האנזים המגביל את הקצב בתהליך זה4. לאחר שהם עוברים טרנסלוקציה למטריצה המיטוכונדרית, האציל-CoAs נוצרים מחדש ומשמשים כמצעים למכונות החמצון β המיטוכונדריה. במצב של צום, האצטיל-CoA המיוצר באמצעות חמצון β במיטוכונדריה בכבד מתועל בעיקר לקטוזגנזה. פרוקסיזומים משמשים כאתר העיקרי לחמצון β של חומצות שומן ארוכות מאוד, שרשרת מסועפת ודיקרבוקסיליות. פרוקסיזומים אינם דורשים ממעבורת קרניטין לייבא מצעי חומצות שומן, ובמקום זאת מייבאים את הכתב אציל-CoAs באמצעות פעילותם של מובילי הקלטת הקושרים ATP (ABC) ABCD1-35. בתוך הפרוקסיזומים, אציל-CoAs מתחמצנים לאחר מכן על-ידי קבוצה ייעודית של אנזימים, הנבדלים מחומצת השומן המיטוכונדרית β-חמצון." גם מיטוכונדריה וגם פרוקסיזומים דורשים אספקה של NAD+ ו-CoA חופשי כדי לחמצן שרשראות אציל שומניות. רמות CoA בכבד הוכחו כגוברות בתגובה לצום, מה שתומך בקצב המוגבר של חמצון חומצות שומן המתרחש במצב זה6. יתר על כן, פירוק מוגבר של CoA בפרוקסיזומים גורם לירידה סלקטיבית בחמצון חומצות שומן פרוקסיסומליות7. לכן, התהליך של חמצון חומצות שומן בתוך התא מווסת על ידי רמות הביטוי והפעילויות של אנזימים המעורבים בהפעלה, הובלה וחמצון של חומצות שומן, כמו גם ריכוזים של קו-פקטורים ומטבוליטים אחרים לאורך תאים תת-תאיים מרובים.
פרוצדורות המשתמשות בהומוגנטים של רקמות למדידת חמצון חומצות שומן הורסות את הארכיטקטורה התאית המסדירה ותומכת בתהליך זה, מה שמוביל לאיסוף נתונים שאינם משקפים במדויק את חילוף החומרים in vivo. בעוד שטכניקות המשתמשות בהפטוציטים ראשוניים מצופים משמרות את המערכת הזו, גידול תאים מבודדים לפרקי זמן ממושכים גורם לאובדן פרופיל ביטוי הגנים in vivo שהיה קיים בתאים כאשר הם עדיין חיו בתוך החיה 8,9. הפרוטוקול הבא מתאר שיטה לבודד הפטוציטים ראשוניים ולבחון את יכולתם לחומצת שומן β-חמצון מיד לאחר הבידוד ובתרחיף, באמצעות [1-14C]חומצה פלמיטית. הבדיקה מבוססת על מדידת הרדיואקטיביות הקשורה למטבוליטים המסיסים בחומצה (ASM) או למוצרים, כמו אצטיל-CoA, המיוצרים על ידי חמצון β של [1-14C] חומצה פלמיטית10,11.
Protocol
כל ההליכים הניסיוניים על עכברים (C57BL/6J, זכרים, בני 9-11 שבועות) אושרו על ידי הוועדות המוסדיות לטיפול ושימוש בבעלי חיים (IACUC) של אוניברסיטת מערב וירג'יניה.
1. בידוד הפטוציטים
- הכנה
- בימים שלפני בידוד הפטוציטים, הכינו את המאגרים ואת אמצעי תרביות התאים המפורטים בטבלה 1. הגדר אמבט מים כאשר הטמפרטורה מוגדרת ל -37 מעלות צלזיוס קרוב למקום שבו יבוצע הניתוח.
- ביום הבידוד של הפטוציטים, תחת מכסה מנוע זרימה למינרי, להעביר 35 מ"ל של Buffer 1 לצינור צנטריפוגה סטרילי של 50 מ"ל ו-70 מ"ל של Buffer 2 לכוס סטרילית של 100 מ"ל או לבקבוק.
- מוסיפים אנטיביוטיקה גנטמיצין (50 מיקרוגרם/מ"ל) ופניצילין/סטרפטומיצין (1x) לשני המאגרים.
- מעבירים 20 מ"ל של Buffer 2 כפי שהוכן בשלב 1.1.3 לצלחת תרבית תאים של 100 מ"מ ומניחים על קרח.
- העבר את 50 מ"ל הנותרים של Buffer 2 לצינור צנטריפוגה סטרילי של 50 מ"ל. מניחים את צינורות ה-50 מ"ל המכילים את ה-Buffers 1 ו-2 המכילים תוסף אנטיביוטיקה באמבט מים בטמפרטורה של 37 מעלות צלזיוס ונותנים להם להתחמם למשך 15 דקות לפחות לפני תחילת הזלוף.
הערה: אם מבצעים בידודים מרובים של הפטוציטים בפגישה, הגדל את מספר האליקוטים המשלימים לאנטיביוטיקה של Buffers 1 ו-2 כדי להתכונן בהתאם. - להפשיר תמיסת קולגן ולשמור על קרח.
הערה: אם מאוחסנים כראוי, אין אובדן משמעותי של פעילות האנזימים בתמיסות קולגן שהוקפאו והופשרו עד 3 פעמים ומשמשות תוך 3 שבועות מההכנה. - הכן את המכשירים הכירורגיים ואת המשאבה הפריסטלטית. לעקר את הקווים של המשאבה peristaltic על ידי מחזור 15 מ"ל של 70% אתנול, ואחריו 15 מ"ל של מים סטריליים.
- חברו מחט של 22 גרם לקו היציאה (איור 1A). המסנן החלול של קטטר פועל היטב כמחבר. מלאו את הקווים ב-Buffer 1 ובדקו את הקווים, המחבר והמחט כדי לוודא שלא נלכדו בועות אוויר.
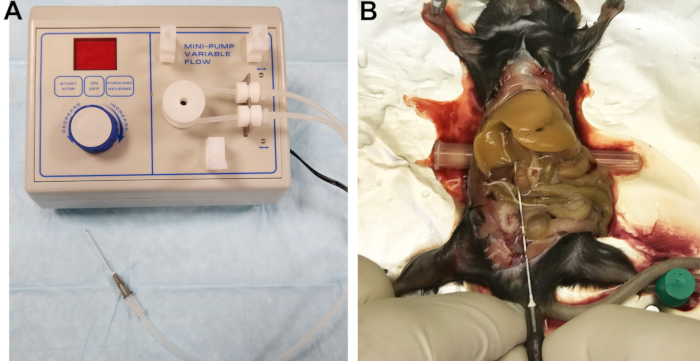
איור 1: מנגנון פרפוזיה וכבד מחורר. (A) משאבה פריסטלטית עם קו יציאה המחובר למחט המשמשת לתחנונים ולתחבולה של הכבד. (B) קנוציה מוצלחת מסומנת על ידי תפיחה מיידית והומוגנית של הכבד. אנא לחץ כאן כדי להציג גרסה גדולה יותר של נתון זה.
- זלוף כבד ודיסוציאציה
- הרדמה עכבר באמצעות שאיפת איזופלורן עם אוויר ברמה רפואית כגז נשא, תוך שימוש ב-4% איזופלורן לאינדוקציה ו-1.5% איזופלורן כדי לשמור על הרדמה. אמת את עומק ההרדמה על ידי הערכת אובדן רפלקס הדוושה.
- כאשר אין תגובה לצביטת הבוהן, הניחו את העכבר בתנוחת שכיבה על לוח ניתוח, הוציאו את הגפיים והצמידו אותן ללוח באמצעות סיכות.
- לרסס באופן חופשי את הבטן והחזה של העכבר עם 70% אתנול.
- באמצעות מלקחיים, למשוך את העור ואת דופן הבטן ליד בסיס הבטן ולחתוך לרוחב, משני צדי קו האמצע ועד הסרעפת, כדי לחשוף את האיברים.
- חשוף את הווריד הנבוב התחתון (IVC) על ידי הזזת המעיים לצד ימין והפיכה עדינה של אונות הכבד כלפי מעלה. הכנס אובייקט גלילי קטן, כגון מכסה מחט, מתחת לחלק האחורי של העכבר כדי להטות מעט את ה-IVC ולהקל על התותח שלו (איור 1B).
- הפעל את המשאבה במהירות הנמוכה ביותר, ועם Buffer 1 זורם, הכנס את המחט ל- IVC.
- חותכים את וריד הפורטל כדי להקל על הלחץ ומאפשרים ניקוז של מאגרי דם וזלוף, ואז מגבירים מיד את קצב הזרימה ל-7 מ"ל/דקה. אם נעשה זאת בצורה נכונה, הכבד יתנפח באופן אחיד תוך מספר שניות (איור 1B).
- לקבלת תוצאות עקביות יותר, החזק את המחט במקומה ביד במשך כל משך הזלוף.
- מכניסים את הכבד למאגר חם 1. כדי להימנע מהכנסת בועות אוויר, ודאו שהקו המוחדר לצינור המכיל את Buffer 1 נשאר שקוע באופן רציף.
- בזמן שהזלוף מתרחש, הוסיפו 130 μL של תמיסת קולגן ל-Buffer 2 וערבבו על ידי צנרת למעלה ולמטה או ערבוב עם פיפטה סרולוגית של 5 מ"ל או 10 מ"ל.
- מכיוון שהנפח בצינור המכיל את Buffer 1 יורד לכ-5 מ"ל, הוסף באיטיות 5 מ"ל של Buffer 2 ל-Buffer 1 על-ידי צנרת בצד הצינור. המטרה היא להימנע מהכנסת בועות אוויר בשורה תוך מעבר מ-Buffer 1 ל-Buffer 2.
- המתן עד שעוצמת הקול תקטן שוב ל- 5 מ"ל ותוסיף לאט לאט עוד 5 מ"ל של Buffer 2. חזור על פעולה אחת נוספת. כאשר Buffer 2 מחליף את Buffer 1 והדיסוציאציה מתחילה, הכבד יתנפח.
- הוסף את Buffer 2 הנותר לצינור המכיל במקור את Buffer 1. עצור את הזלוף כאשר יש בערך 5-10 מ"ל של Buffer 2 שנותרו בצינור.
הערה: בעוד Buffer 2 מחלחל לכבד, ניתן להדק את וריד הפורטל לסירוגין עם מלקחיים במשך 5 שניות. שלב זה הוא אופציונלי, אך העלייה הנובעת מכך בלחץ בכל הכבד יכולה לשפר את הדיסוציאציה שלו, ובכך את תפוקת הפטוציטים הסופית. - יש לכרות בזהירות את הכבד ולהעבירו לתבשיל תרבית 100 מ"מ המכיל את 20 מ"ל של Buffer 2 קר כקרח שהונח בצד בשלב 1.1.4.
- מתחת למכסה המנוע של הזרימה הלמינרית, מפרקים בעדינות את הכבד באמצעות מספריים כירורגיים ופינצטה.
- הוסיפו כ-20 מ"ל של M199 קר כקרח לתרחיף הפטוציטים וסננו אותו דרך מסננת של 100 מיקרומטרים באמצעות הבוכנה של מזרק כדי לקדם בעדינות את שחרורם של הפטוציטים נוספים מחתיכות כבד גדולות יותר.
- יש לשטוף את צלחת התרבית בקוטר 100 מ"מ ואת מסננת התאים בתוספת M199 עד שצינור האיסוף מתמלא.
- צנטריפוגה את המתלים ב 50 x g במשך 2 דקות ב 4 ° C. בזהירות לשאוף את supernatant ולהחיות בעדינות את גלולת hepatocyte ב 30 מ"ל של M199 קר על ידי מערבולת.
- גלולה את hepatocytes כאמור בשלב 1.2.18. חוזרים על הכביסה פעם נוספת.
- בצעו החייאה של הפטוציטים ב-10 מ"ל של M199 חם וקבעו את הכדאיות והתפוקה באמצעות שיטת ההדרה הכחולה של טריפאן והמוציטומטר12.
- דיללו את התאים ב-M199 שחוממו ל-37 מעלות צלזיוס לריכוז סופי של 1.0 x 106 תאים בני קיימא/מ"ל ומיד התחילו את הבדיקה.
2. בדיקת חומצות שומן β-חמצון
הערה: הבדיקה נערכת במשולש, וכל תערובת תגובה מכילה 750,000 תאים, 1.35 מ"ג/מ"ל אלבומין בסרום בקר (BSA), 100 μM חומצה פלמיטית, ו-0.4 μCi [1-14C] חומצה פלמיטית בנפח סופי של 2 מ"ל.
אזהרה: תרכובות רדיואקטיביות מסוכנות. רכישה, טיפול, אחסון וסילוק של חומר רדיואקטיבי בהתאם לתקנות המוסדיות, המדינתיות והפדרליות.
- הכנה
- בימים שלפני הבדיקה, הכינו את החומצה הדקליסטית ואת תמיסות ה-BSA (טבלה 1) ואחסנו אותן בטמפרטורה של -20 מעלות צלזיוס.
- ביום הבדיקה, השלם את השלבים 2.1.3-2.1.9 לפני תחילת זלוף הכבד.
- להפשיר את החומצה הדקלמית ואת תמיסות ה-BSA. הכינו את תערובת המצע לתגובות מרובות בתוספת עודף של 20%-30%, עם הגדרת בדיקה טיפוסית המוצגת בטבלה 2.
- Aliquot 13.5 μL של תמיסת BSA לכל תגובה בצינור microcentrifuge וחם עד 41 °C (41 °C), ואז להוסיף 1 μL של תמיסת חומצה פלמיטית 200 mM (BSA: יחס טוחנת חומצה פלמיטית = 1:5) לכל תגובה.
הערה: עדיף לוותר על תמיסות שהוכנו באמצעות ממסים אורגניים, כגון תמיסות חומצה פלמיטית רדיואקטיבית ולא רדיואקטיבית, עם פיפטת תזוזה חיובית וטיפים מתאימים. - מערבולת נמרצת ודגירה ב 41 °C (64 °F) כדי להקל על היווצרות של חומצה פלמיטית מסיסה: BSA מורכב. מערבולת מדי פעם בתקופת הדגירה.
- התערובת תיראה בתחילה מעוננת אך תבהיר לחלוטין לאחר 20-30 דקות של דגירה בטמפרטורה של 41 מעלות צלזיוס. שמור אותו בטמפרטורה של 41 °C (41 °F) עד שיהיה מוכן להתחיל את התגובות.
- Aliquot 133 μL של 1 M חומצה פרכלורית ב 1.5 מ"ל צינורות microcentrifuge כדי לעצור את התגובות.
אזהרה: חומצה פרכלורית היא חומצה חזקה ומחמצנת חזקה. נדרש ציוד מגן מתאים לטיפול במתחם זה. - Aliquot 485.5 μL של M199 לכל תגובה לתוך צינור ולשמור אותו על 37 °C כדי לדלל את BSA רדיואקטיבי: קומפלקס חומצה פלמיטית מוכן בשלבים 2.1.4-2.1.1.6 לפני תחילת התגובות.
- תחלקו 750 μL של M199 בצינורות עגולים עם תחתית עגולה של 14 מ"ל כמו הדגימות. אם תרצה בכך, יש להוסיף מעכבים של חומצת שומן β-חמצון, כגון אטומוקסיר, רוטנון ואנטימיצין, כולל בקרת רכב (טבלה 2).
- במהלך שלבי שטיפת הפטוציטים, 10-15 דקות לפני תחילת התגובות, העבירו את הצינורות שהוכנו בשלב 2.1.9 לאמבטיית מים רועדת שנקבעה ל-37 מעלות צלזיוס ורעדה ב-180-200 סל"ד.
- התחלה, עצירה וניתוח של חומצות השומן β תגובות חמצון
- אם הכדאיות של הפטוציטים מקובלת (בדרך כלל ≥ 75%, איור 2), עבור כל תגובה, העבירו 0.8 μL של [1-14 C] חומצה פלמיטית (0.5 mCi/mL) לצינור microcentrifuge המכיל את ה-BSA המובהר: תמיסת חומצה פלמיטית (שלבים 2.1.4-2.1.6). מערבולת ולחזור לאמבטיית המים בטמפרטורה של 41 מעלות צלזיוס.
- כדי לאזן את ההפטוציטים ל -37 מעלות צלזיוס ולדגום אותם מראש עם מעכבים (אם קיימים), מיד לאחר החייאת הפטוציטים הסופית (שלב 1.2.21), להעביר 750 μL של תרחיף הפטוציטים עם פיפטה של 1 מ"ל לכל אחד מהצינורות העגולים של 14 מ"ל באמבטיה המים הרועדים (צעדים 2.1.9-2.1.10) ומערבולת לזמן קצר במהירות נמוכה לערבוב.
- תקעו כל תוספת ב-30 שניות ודגרו במשך 15 דקות. כדי לשמור דגימה לקביעת חלבונים, מעבירים אליקוט נוסף של הפטוציטים לצינור מיקרו-סנטריפוג' של 1.5 מ"ל ומסובבים ב-3,000 x גרם למשך 5 דקות.
הערה: בעת חלוקת, יש לסובב או לערבב בעדינות את תרחיף הפטוציטים באופן רציף עם הפיפטה של 1 מ"ל כדי למנוע התיישבות והשתנות גדולה במספר התאים בין דגימות. - הסר את חומר העל ואחסן את הכדור בטמפרטורה של -80 מעלות צלזיוס עד שיהיה מוכן למדוד את כמות החלבון הכוללת בדגימה כדי לנרמל את התוצאות (איור 3).
- בזמן שההפטוציטים נמצאים תחת דגירה מוקדמת ב-37 מעלות צלזיוס, הוסיפו את ה-BSA הרדיואקטיבי: קומפלקס חומצה פלמיטית למדיום החם ב-2.1.8, ושמרו על 37 מעלות צלזיוס עד שהם מוכנים להתחיל את התגובות. זהו תמהיל המצע הסופי.
- כדי להתחיל את התגובות, להסיר את hepatocytes מן האמבטיה מים ולהוסיף 500 μL של תערובת מצע.
- מערבולת במהירות נמוכה במשך 5 שניות כדי להחיות לחלוטין את התאים ולחזור לאמבט המים. חזור עם כל הדגימות, מזעזע ב -30 שניות.
- דגירה למשך 15 דקות. התחל קבוצה של תגובות ועצור מיד (ראה שלבים 2.2.10-2.2.11) כדי לקבוע את הרדיואקטיביות ברקע (טבלה 2).
- מעבירים אליקוטים כפולים (200-250 μL) של שאריות המצע לבקבוקוני חרטום של 6 מ"ל ומניחים בצד לספירה. השתמש בספירות אלה כדי לחשב את הרדיואקטיביות המתאימה לסך הנמולים של חומצה פלמיטית הזמינים לחמצון ב-500 μL של תערובת מצע.
- כדי לעצור את התגובות, להסיר את hepatocytes מן האמבטיה מים, resuspened hepatocytes על ידי מערבולת במהירות מתונה, ולאחר מכן להעביר 400 μL של תרחיף hepatocyte לצינורות microcentrifuge המכילים חומצה perchloric.
- מיד מכסה את הצינורות. חזור על רצף זה עבור כל הדגימות, מזעזע ב- 30 שניות.
- מערבולת נמרצת של צינורות המיקרו-צנטריפוגה בגודל 1.5 מ"ל ומסובבת אותם במורד צינורות המיקרו-צנטריפוגה בגודל 1.5 מ"ל ב-13,000 x גרם למשך 10 דקות.
- מעבירים 300 μL של ה-supernatant לבקבוקון 6 מ"ל, מוסיפים 4 מ"ל של נוזל ציצית, וסופרים את הרדיואקטיביות בדגימות ובתערובת המצע aliquots (שלב 2.2.9) במונה חרציות.
אזהרה: לאחר צנטריפוגה, פתח את הצינורות מתחת למכסה אדים כדי להימנע מנשימה של 14C-CO2 המיוצר על ידי חמצון מלא של 14C-אצטיל-CoA שנוצר על ידי חומצת שומן β-חמצון ומשתחרר על ידי התנאים החומציים.
| מאגרים/רכיבי מדיה | כמות | ריכוז סופי | הוראות |
| פתרון ג' | |||
| KCl | 1.79 גרם | 480 mM | מוסיפים מים ל-50 מ"ל. חנות ב 4 °C (74 °F) |
| MgSO4 הפטהידרט | 1.48 גרם | 120 mM | |
| KH2PO4 | 0.81 גרם | 119 mM | |
| כרית קרבס-הנסלייט (KHB), ללא סידן | |||
| NaCl | 7.0 גרם | 120 mM | הוסיפו מים ל-900 מ"ל, התאימו את ה-pH ל-7.4 והביאו את עוצמת הקול הסופית ל-1 ליטר. |
| NaHCO3 | 2.0 גרם | 24 mM | |
| 1 M HEPES pH 7.45 | 5 מ"ל | 5 מ"מ | |
| גלוקוז | 1 או 2 גרם | 5.6 או 11 mM | |
| פתרון ג' | 10 מ"ל | ||
| חיץ 1 | |||
| ק.ב. | 500 מ"ל | מערבבים רכיבים ומסננים מעקרים. חנות ב 4 °C (74 °F) | |
| 50 mM EGTA | 1.0 מ"ל | 0.1 מ"מ | |
| מאגר 2 | |||
| ק.ב. | 500 מ"ל | מערבבים רכיבים ומסננים מעקרים. חנות ב 4 °C (74 °F) | |
| 1 M CaCl2 דיהידרט | 686 μL | 1.4 מ"מ | |
| תמיסת גנטמיצין | |||
| גנטמיצין סולפט | 0.5 גרם | 50 מ"ג/מ"ל | מוסיפים מים ל-10 מ"ל ומסננים עיקור. Aliquot וחנות ב -20 °C (75 °F) |
| תמיסת קולגן | |||
| תערובת קולגן I ו-II | 10 מ"ג | 7 מ"ג/מ"ל | להמיס את כל התוכן של הבקבוקון ב 1.43 מ"ל של מים. Aliquot וחנות ב -20 °C (75 °F) |
| M199 | |||
| M199 | 1 שקית | מוסיפים מים ל-900 מ"ל ומתאימים את ה-pH ל-7.2-7.4. מביאים את הנפח הסופי ל-1 ליטר ומסננים מעקרים. חנות ב 4 °C (74 °F) | |
| NaHCO3 | 2.2 גרם | 26 מ"מ | |
| 1 M HEPES (ציון תרבית תאים) | 25 מ"ל | 25 mM | |
| תוספת גלוקוז (רק לעכברים שניזונו) | 1 גרם | 11 מ"מ | |
| פתרון BSA | |||
| BSA נטול חומצות שומן | 400 מ"ג | 20% (w/v) | מתמוססים ב-2 מ"ל של מים. Aliquot וחנות ב -20 °C (75 °F) |
| תמיסת חומצה פלמיטית לא רדיואקטיבית | |||
| חומצה פלמיטית | 103 מ"ג | 200 mM | להמיס ב 2 מ"ל של אתנול, לאחסן ב -20 °C (76 °F) |
| 1 M חומצה פרכלורית | |||
| 70% חומצה פרכלורית | 3.5 מ"ל | 1 מ' | דילול ל 40 מ"ל עם מים. יש לאחסן בטמפרטורת החדר |
טבלה 1: מאגרים, מדיה ותמיסות אחרות הדרושות לבידוד הפטוציטים ולחומצת השומן β-חמצון
| מספר תגובה | מעכבי ± M199 | תרחיף הפטוציטים (μL) | תערובת מצע (μL) | ||||
| נפח (μL) | אטומוקסיר | ||||||
| 1 | 750 | - | חימום מראש ב 37 °C (76 °F) | 750 | דגירה מוקדמת בטמפרטורה של 37 מעלות צלזיוס למשך 15 דקות | 500 | דגירה ב 37 °C (66 °F) למשך 15 דקות |
| 2 | |||||||
| 3 | |||||||
| 4 | + | ||||||
| 5 | |||||||
| 6 | |||||||
| 7 | + | עצור מיד | |||||
| 8 | |||||||
| 9 | |||||||
טבלה 2: דוגמה למערך הניסויי של תרחיף הפטוציטים שנבחן במשולש בנוכחות ובהיעדר אטומוקסיר.
תוצאות
זלוף הכבד המתואר כאן מניב בדרך כלל 30-40 מיליון תאים/כבד עם כדאיות ממוצעת של 80%, כפי שהוערך על ידי הרחקה כחולה של טריפאן (איור 2). הריכוז האופייני של גלוקוז במאגר Krebs-Henseleit (KHB), המשמש להכנת מאגרי הזלוף 1 ו -2, הוא 11 mM. כאשר מודדים חומצת שומן β-חמצון בהפטוציטים המבודדים מעכברים בצום, נ?...
Discussion
במהלך זלוף הכבד, חשוב להימנע מהכנסת בועות אוויר, שכן הן חוסמות את המיקרו-קפילרים בכבד, מונעות או מגבילות את זרימת החיץ ומפחיתות באופן כללי את תפוקת הפטוציטים ואת הכדאיות20,21. אמצעי זהירות, כגון בדיקה מדוקדקת של קו הכניסה הממולא במאגר לפני התותח של ה-IVC והימנעו...
Disclosures
למחברים אין ניגודי עניינים לחשוף.
Acknowledgements
עבודה זו נתמכה על ידי מענק המכונים הלאומיים לבריאות R35GM119528 לרוברטה לאונרדי.
Materials
| Name | Company | Catalog Number | Comments |
| (R)-(+)-Etomoxir sodium salt | Tocris Bioscience | 4539/10 | |
| [1-14C]-Palmitic acid, 50–60 mCi/mmol, 0.5 mCi/mL | American Radiolabeled Chemicals | ARC 0172A | |
| 1 M HEPES, sterile | Corning | 25060CI | |
| 10 µL disposable capillaries/pistons for positive displacement pipette | Mettler Toledo | 17008604 | |
| 1000 µL, 200 µL, and 10 µL pipettes and tips | |||
| 5 mL, 10 mL, and 25 mL serological pipettes | |||
| 50 mL sterile centrifuge tubes | CellTreat | 229421 | |
| 70% Perchloric acid | Fisher Scientific | A2296-1LB | |
| BSA, fatty acid-free | Fisher Scientific | BP9704100 | |
| CaCl2 dihydrate | MilliporeSigma | 223506 | |
| D-(+)-Glucose | MilliporeSigma | G7021 | |
| EGTA | Gold Biotechnology | E-217 | |
| Ethanol | Pharmco | 111000200CSPP | |
| Filter System, 0.22 μm PES Filter, 500 mL, Sterile | CellTreat | 229707 | |
| Gentamicin sulphate | Gold Biotechnology | G-400-25 | |
| HDPE, 6.5 mL scintillation vials | Fisher Scientific | 03-342-3 | |
| Hemocytometer | |||
| Hypodermic needles 22 G, 1.5 in | BD Biosciences | 305156 | |
| Isoflurane | VetOne | 502017 | |
| KCl | Fisher Scientific | BP366-1 | |
| KH2PO4 | MilliporeSigma | P5655 | |
| Liberase TM Research Grade | MilliporeSigma | 5401119001 | Defined blend of purified collagenase I and II with a medium concentration of thermolysin |
| M199 medium | MilliporeSigma | M5017 | |
| MgSO4 heptahydrate | MilliporeSigma | M1880 | |
| Microcentrifuge | Fisher Scientific | accuSpin Micro 17 | |
| Microdissecting Scissors | Roboz Surgical Instrument Co | RS-5980 | |
| NaCl | Chem-Impex International | 30070 | |
| NaHCO3 | Acros Organics | 424270010 | |
| Palmitic acid | MilliporeSigma | P0500 | |
| Penicillin/streptomycin (100x) | Gibco | 15140122 | |
| Phosphate buffered saline (PBS) | Cytiva Life Sciences | SH30256.01 | |
| Positive displacement pipette MR-10, 10 µL | Mettler Toledo | 17008575 | |
| Refrigerated centrifuge with inserts for 50 mL conical tubes | Eppendorf | 5810 R | |
| Round-bottom, 14 mL, polypropylene culture test tubes | Fisher Scientific | 14-956-9A | |
| Scintillation counter | Perkin Elmer | TriCarb 4810 TR | |
| ScintiVerse BD cocktail | Fisher Scientific | SX18-4 | |
| Shaking water bath, 30 L capacity | New Brunswick Scientific | Model G76 | |
| Sterile cell strainers, 100 µm | Fisher Scientific | 22363549 | |
| Thumb Dressing Forceps | Roboz Surgical Instrument Co | RS-8120 | |
| Trypan Blue | Corning | 25900CI | |
| Variable-flow peristaltic pump | Fisher Scientific | 138762 | |
| Water baths, 2–2.5 L capacity |
References
- Alves-Bezerra, M., Cohen, D. E. Triglyceride Metabolism in the Liver. Comprehensive Physiology. 8 (1), 1-8 (2017).
- Lopaschuk, G. D., Ussher, J. R., Folmes, C. D., Jaswal, J. S., Stanley, W. C. Myocardial fatty acid metabolism in health and disease. Physiological Reviews. 90 (1), 207-258 (2010).
- Mannaerts, G. P., van Veldhoven, P. P. Functions and organization of peroxisomal beta-oxidation. Annals of the New York Academy of Sciences. 804, 99-115 (1996).
- Kerner, J., Hoppel, C. Fatty acid import into mitochondria. Biochimica et Biophysica Acta (BBA) - Bioenergetics. 1486 (1), 1-17 (2000).
- Baker, A., et al. Peroxisomal ABC transporters: functions and mechanism. Biochemical Society Transactions. 43 (5), 959-965 (2015).
- Leonardi, R., Rehg, J. E., Rock, C. O., Jackowski, S. Pantothenate kinase 1 is required to support the metabolic transition from the fed to the fasted state. PloS One. 5 (6), 11107 (2010).
- Shumar, S. A., Kerr, E. W., Fagone, P., Infante, A. M., Leonardi, R. Overexpression of Nudt7 decreases bile acid levels and peroxisomal fatty acid oxidation in the liver. Journal of Lipid Research. 60 (5), 1005-1019 (2019).
- Richert, L., et al. Gene expression in human hepatocytes in suspension after isolation is similar to the liver of origin, is not affected by hepatocyte cold storage and cryopreservation, but is strongly changed after hepatocyte plating. Drug Metabolism and Disposition: The Biological Fate of Chemicals. 34 (5), 870-879 (2006).
- Colbert, R. A., Amatruda, J. M., Young, D. A. Changes in the expression of hepatocyte protein gene-products associated with adaptation of cells to primary culture. Clinical Chemistry. 30 (12), 2053-2058 (1984).
- Spurway, T. D., Sherratt, H. A., Pogson, C. I., Agius, L. The flux control coefficient of carnitine palmitoyltransferase I on palmitate beta-oxidation in rat hepatocyte cultures. Biochemical Journal. 323, 119-122 (1997).
- Consitt, L. A., et al. Peroxisome proliferator-activated receptor-gamma coactivator-1alpha overexpression increases lipid oxidation in myocytes from extremely obese individuals. Diabetes. 59 (6), 1407-1415 (2010).
- Lee, S. M., Schelcher, C., Demmel, M., Hauner, M., Thasler, W. E. Isolation of human hepatocytes by a two-step collagenase perfusion procedure. Journal of Visualized Experiments: JoVE. (79), e50615 (2013).
- Lilly, K., Chung, C., Kerner, J., VanRenterghem, R., Bieber, L. L. Effect of etomoxiryl-CoA on different carnitine acyltransferases. Biochemical Pharmacology. 43 (2), 353-361 (1992).
- Yu, X. X., Drackley, J. K., Odle, J. Rates of mitochondrial and peroxisomal beta-oxidation of palmitate change during postnatal development and food deprivation in liver, kidney and heart of pigs. Journal of Nutrition. 127 (9), 1814-1821 (1997).
- Yu, X. X., Drackley, J. K., Odle, J., Lin, X. Response of hepatic mitochondrial and peroxisomal beta-oxidation to increasing palmitate concentrations in piglets. Biology of the Neonate. 72 (5), 284-292 (1997).
- Veerkamp, J. H., van Moerkerk, H. T. Peroxisomal fatty acid oxidation in rat and human tissues. Effect of nutritional state, clofibrate treatment and postnatal development in the rat. Biochimica et Biophysica Acta (BBA) - Bioenergetics. 875 (2), 301-310 (1986).
- Hakvoort, T. B., et al. Interorgan coordination of the murine adaptive response to fasting. Journal of Biological Chemistry. 286 (18), 16332-16343 (2011).
- Sokolovic, M., et al. The transcriptomic signature of fasting murine liver. BMC Genomics. 9, 528 (2008).
- Kersten, S., et al. Peroxisome proliferator-activated receptor alpha mediates the adaptive response to fasting. Journal of Clinical Investigation. 103 (11), 1489-1498 (1999).
- Li, W. C., Ralphs, K. L., Tosh, D. Isolation and culture of adult mouse hepatocytes. Methods in Molecular Biology. 633, 185-196 (2010).
- Ng, I. C., et al. Isolation of Primary Rat Hepatocytes with Multiparameter Perfusion Control. Journal of Visualized Experiments: JoVE. (170), e62289 (2021).
- Shen, L., Hillebrand, A., Wang, D. Q., Liu, M. Isolation and primary culture of rat hepatic cells. Journal of Visualized Experiments: JoVE. (64), e3917 (2012).
- Fulgencio, J. P., Kohl, C., Girard, J., Pegorier, J. P. Effect of metformin on fatty acid and glucose metabolism in freshly isolated hepatocytes and on specific gene expression in cultured hepatocytes. Biochemical Pharmacology. 62 (4), 439-446 (2001).
- Leonardi, R., Rock, C. O., Jackowski, S. Pank1 deletion in leptin-deficient mice reduces hyperglycaemia and hyperinsulinaemia and modifies global metabolism without affecting insulin resistance. Diabetologia. 57 (7), 1466-1475 (2014).
- Bougarne, N., et al. PPARalpha blocks glucocorticoid receptor alpha-mediated transactivation but cooperates with the activated glucocorticoid receptor alpha for transrepression on NF-kappaB. Proceedings of the National Academy of Sciences of the United States of America. 106 (18), 7397-7402 (2009).
- Korelova, K., Jirouskova, M., Sarnova, L., Gregor, M. Isolation and 3D collagen sandwich culture of primary mouse hepatocytes to study the role of cytoskeleton in bile canalicular formation in vitro. Journal of Visualized Experiments: JoVE. (154), e60507 (2019).
Reprints and Permissions
Request permission to reuse the text or figures of this JoVE article
Request PermissionExplore More Articles
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. All rights reserved