A subscription to JoVE is required to view this content. Sign in or start your free trial.
Method Article
טיפול חדשני בדליפת מרה מורכבת לאחר השתלת כבד
* These authors contributed equally
In This Article
Summary
דליפת מרה היא סיבוך שכיח לאחר השתלת כבד המשפיע באופן משמעותי על הפרוגנוזה של החולים. הפרוטוקול מציג שיטה חדשה לשילוב כולנגיופנקראטוגרפיה אנדוסקופית רטרוגרדית (ERCP), כולדוקוסקופ ענף וכולנגיוסקופיה טרנסהפטית מלעורית (PTCS) לטיפול בדליפת מרה מורכבת לאחר השתלת כבד.
Abstract
דליפת מרה היא סיבוך שכיח לאחר השתלת כבד שבדרך כלל ניתן לרפא באמצעות כולנגיופנקראטוגרפיה אנדוסקופית רטרוגרדית (ERCP), ניקוז כולנגיאלי דרך הכבד מלעורי (PTCD), כולנגיוסקופיה דרך הכבד מלעורית (PTCS) וניתוח. אנו מדווחים על טיפול חדשני בדליפת מרה שנמשך 9 חודשים לאחר השתלת כבד, במהלכו ERCP, PTCD, PTCS וטיפול כירורגי היו לשווא. השתמשנו בשיטה חדשה של טיפול מולטי-אנדוסקופי. ראשית, ERCP וכולנגיוסקופיה של מפעיל יחיד פרפורלי משמשים להצבת סטנט פלסטיק כסמן בקצה הדיסטלי של אתר דליפת המרה. שנית, PTCS מבוצע דרך צינור ה-PTCD. במהלך הניתוח, הקצה הפרוקסימלי של אתר דליפת המרה ממוקם על ידי סטנט הפלסטיק ואולטרסאונד B, והמשכיות דרכי המרה משוחזרת באופן זמני דרך חוט ההנחיה וצנתר השתן. שלישית, מניחים חוט מנחה דו-ראשי, מסירים את קטטר השתן, מניחים את הסטנטים ומשחזרים את המשכיות המרה. לסיכום, מצאנו שיטה חדשה המשלבת ERCP, כולנגיוסקופיה של מפעיל יחיד ו-PTCS לטיפול בדליפת מרה מורכבת לאחר השתלת כבד.
Introduction
השתלת כבד הפכה לסטנדרט טיפול בחולים עם מחלת כבד סופנית. לאחר השתלת כבד, כ-1/3 מהחולים מושפעים מסיבוכים בדרכי המרה, ואלה גורמים לתחלואה משמעותית ולירידה בהישרדות החולה, מה שנקרא עקב אכילס של השתלת כבד1. דליפת מרה היא הסיבוך השני בשכיחותו לאחר השתלת כבד, עם שכיחות של 2%-21%2,3,4. גישות נפוצות לטיפול בסיבוכי מרה כוללות כולנגיופנקראטוגרפיה אנדוסקופית רטרוגרדית (ERCP), ניקוז כולנגיאלי דרך הכבד מלעורי (PTCD), כולנגיוסקופיה טרנסהפטית מלעורית (PTCS) וניתוח5, אך לא כולן יעילות.
מטרת שיטה זו היא לטפל בדליפת מרה מורכבת לאחר השתלת כבד על ידי שילוב של ERCP, כולנגיוסקופיה של מפעיל יחיד ו-PTCS.
העיקרון הטכני של שיטה זו מחולק לשלושה שלבים. ראשית, באמצעות ERCP וכולנגיוסקופיה של מפעיל יחיד פרפורלי, הקצה הדיסטלי של דליפת המרה מזוהה בראייה ישירה, וסטנט פלסטיק ממוקם כסמן. לאחר מכן, באמצעות PTCS, בהנחיית הסטנט הפלסטי, מחפשים את הקצה הפרוקסימלי של דליפת המרה מצינור הכבד המשותף בראייה ישירה, וצנתר השתן משחזר את המשכיות דרכי המרה. לבסוף, באמצעות ERCP, נעשה שימוש בחוט מנחה דו-ראשי, מסירים את קטטר השתן, ומניחים את הסטנטים של צינור הכבד השמאלי והימני כדי לשחזר את המשכיות המרה.
כולנגיוסקופיה פראורלית (POCS) דווחה לראשונה על ידי יפן בשנת 19766. Chen et al.7 דיווחו לראשונה על הדור הראשון של מערכת כולדוקוסקופ הדמיה של מפעיל יחיד, SpyGlass, בשנת 2007, והדור השני של SpyGlass (SpyGlass DS) הושק על ידי בוסטון בשנת 20158. עם התפתחות המכשירים, הכולנגיוסקופיה של המפעיל היחיד הפרפורלי הפכה דקה יותר ויש לה יותר פונקציות.
היתרון הגדול ביותר בשיטה זו הוא שניתן לבצע אותה בראייה ישירה של כולנגיוסקופיה מפעיל יחיד פרפורלית, מה שמגדיל את אחוזי ההצלחה והבטיחות של הניתוח 9,10,11,12. ריינר9 דיווח על הצבת סטנט מוצלחת באמצעות מערכת ראיית מרה ישירה בחולים לאחר השתלת כבד עם כשל בהשתלת סטנט ERCP, והם הציעו כי הדמיה ישירה של הפתח הזעיר בהיצרות המרה הייתה הדרך היחידה לעבור בהצלחה את החוט המנחה.
שיטה זו מתאימה לחולים עם דליפת מרה מורכבת לאחר השתלת כבד שאינם ניתנים לריפוי על ידי ERCP, PTCD, PTCS וניתוח.
אנו מדווחים על מקרה של גבר בן 38 שהיה לו היסטוריה של מחלת קרוהן וויטיליגו בנוסף לאי ספיקת כבד חריפה על כרונית שנגרמה כתוצאה מהתפרצות נגיף הפטיטיס B. תפקודי הכבד ירדו עם הזמן למרות טיפולים חוזרים ונשנים בכבד מלאכותי. כאשר ילד בן 15 עם מוות מוחי סיפק כבד תורם תואם, דליפת מרה התרחשה 14 יום אחרי השתלת הכבד (איור 1A). צינור הניקוז של חלל הבטן וה-PTCD הותקנו מיד עקב כאבי בטן חריפים והלם ספטי. לאחר הניקוז, בריאותו הכללית של המטופל השתפרה, וכמות התפליט הצפק פחתה מאוד (איור 1B).
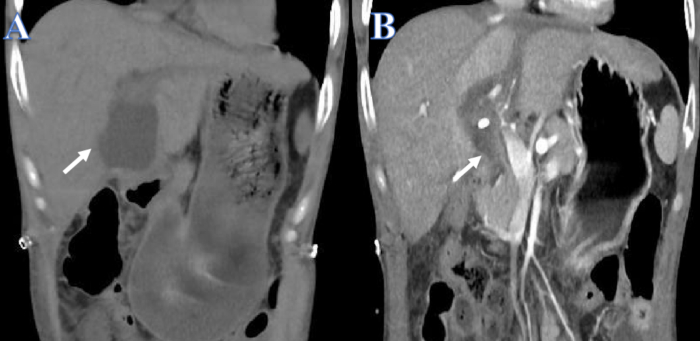
איור 1: לפני ואחרי ניקוז דליפת מרה. (A) החץ הלבן מראה את הנוזל לפני הניקוז. (B) החץ הלבן מראה את הנוזל אחרי הניקוז. אנא לחץ כאן לצפייה בגרסה גדולה יותר של איור זה.
לאחר 3 שבועות, צינור המרה התוך-כבדי לא היה מספיק כדי לתמוך בחוט המנחה, שעבר בקלות דרך צינור המרה התוך-כבדי למקומות אחרים, כך שהניסיון לשחזר את דרכי המרה מלמעלה למטה דרך צינור ה-PTCD בצינורות הכבד השמאלי והימני נכשל שניהם (איור 2). לאחר 4 שבועות, ניסיון לשחזר את דרכי המרה באמצעות ERCP מלמטה למעלה לא הצליח מכיוון שהחוט המנחה לא יכול היה לעבור דרך היצרות לתוך צינור המרה התוך-כבדי (איור 3). לאחר שבועיים, לא ניתן היה לאתר את צינור המרה המשותף, והיו אבנים רבות בצומת צינורות הכבד השמאלי והימני בהילר, מה שלא אפשר היה לשחזר את דרכי המרה מלמעלה למטה עם PTCS. כ-4 שבועות לאחר מכן, ניסיון לשחזר את דרכי המרה על ידי choledochojejunostomy נכשל בגלל הדלקת והבצקת הברורה של הרקמה המקיפה את דליפת המרה, והיסטוריית קרוהן קודמת של המטופל הגדילה מאוד את הסיכון לדליפת מרה לאחר הניתוח עם פיסטולה במעי.
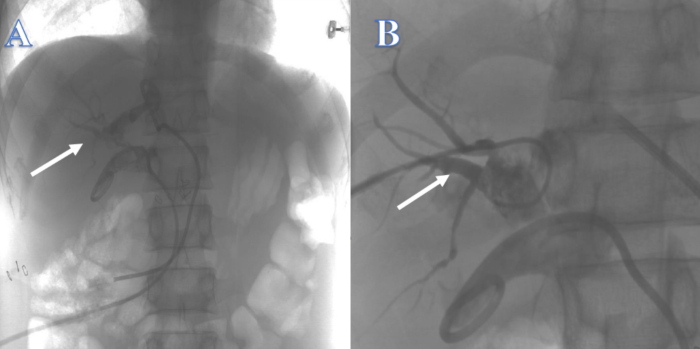
איור 2: המשכיות המרה משוחזרת על ידי PTC. (A) החץ הלבן מציין ניסיון מצינור הכבד השמאלי. (B) החץ הלבן מציין ניסיון מצינור הכבד הימני. אנא לחץ כאן לצפייה בגרסה גדולה יותר של איור זה.

איור 3: המשכיות המרה ששוחזרה על ידי ERCP. חוט ההנחיה לא יכול היה להיכנס לצינור המרה התוך-כבדי. אנא לחץ כאן לצפייה בגרסה גדולה יותר של איור זה.
כאן, מצאנו שיטה חדשה לשילוב ERCP, כולנגיוסקופיה של מפעיל יחיד ו-PTCS לטיפול בדליפת מרה מורכבת לאחר השתלת כבד. תחילה הונח סטנט פלסטיק לאיתור הקצה הדיסטלי של דליפת המרה באמצעות ERCP וכולנגיוסקופיה של מפעיל יחיד פרפורלי. הקצה הפרוקסימלי של דליפת המרה אותר לאחר מכן על ידי אולטרסאונד PTCS ו-B, ולבסוף, ההמשכיות של דרכי המרה שוחזרה על ידי ERCP.
Protocol
המחקר תאם את ההנחיות האתיות של הצהרת הלסינקי משנת 1975 ואושר על ידי ועדת האתיקה של בית החולים המסונף הראשון של אוניברסיטת סון יאט-סן. ההסכמה מדעת התקבלה מהמטופל.
1. הכנה טרום ניתוחית
- הנחו את המטופל לצום במשך 6-8 שעות לפני ERCP. יש לתת פטידין 1 מ"ג/ק"ג, אניסודאמין 20 מ"ג, הזרקת מידזולם 1 מ"ג, פלורביפרופן 100 מ"ג תוך ורידי וטטרקאין הידרוכלוריד דרך הפה. כאשר רפלקס הלוע נעלם, הרדמה מקומית בתוספת טשטוש ושיכוך כאבים נחשבו מוצלחים.
2. מיקום סטנט פלסטיק
- ודא שהמטופל ממוקם במצב שכיבה, וברגע שעומק ההרדמה משביע רצון, התחל בהליך. הכנס את התריסריון לפה, העביר אותו דרך הוושט והקיבה כדי להגיע לתריסריון, ומצא את פפילת התריסריון.
- הכנס את חוט ההנחיה לצינור המרה המשותף.
- מתן הזרקת יופרומיד (ריכוז יוד 300 מ"ג/מ"ל) בקצב של 2 מ"ל לשנייה דרך צינור ERCP או PTCD. התבונן בדרכי המרה התוך-כבדיות והחוץ-כבדיות לכולנגיוגרפיה לאחר ההזרקה, וזהה את ההיצרות של צינור המרה. שימו לב שההיצרות של צינור המרה ממוקמת בצינור הכבד המשותף ולא ניתן לדמיין בו זמנית את צינורות המרה התוך-כבדיים והחוץ-כבדיים (איור 4A).
- הרחב את הפתח התחתון של צינור המרה המשותף עם בלון הרחבה של 6-8 מ"מ ל-7 מ"מ על ידי הזרקת יופרומיד לתוך הבלון.
- הכנס את הכולנגיוסקופיה של המפעיל היחיד כדי להתבונן בצינור המרה, מצא היצרויות שלא ניתן לעבור דרכן, והכנס את חוט ההנחיה דרך היצרות, ואחריו הרחבה עם בוגי מרחיב מרה של 6 מ"מ.
- הרחבת ההיצרות עם בלון הרחבה של 6-8 מ"מ ל-7 מ"מ על ידי הזרקת יופרומיד (איור 4B).
- הכנס שוב את הכולנגיוסקופיה של המפעיל היחיד הפראורלי כדי להתבונן בצינור המרה. שימו לב לצינור המרה העיוור עם אבנים וחומר פלוקולנטי, ללא צינור מרה תוך-כבדי שנצפה גם לאחר הזרקת יופרומיד.
- הכניסו סטנט מרה מפלסטיק בגודל 7F x 7 ס"מ לתוך הצינור העיוור דרך ההיצרות, והקצה השני הוצב מחוץ לפפילה של התריסריון (איור 4C).
- לאורך כל ההליך, ספק חמצן דרך צינורית האף במהירות של 3 ליטר לדקה ועקוב מקרוב אחר הסימנים החיוניים במהלך ERCP. לאחר מכן, ספקו תרופות לעיכוב חומצה (אסומפרזול 40 מ"ג BID), עיכוב אנזים (אוקטראוטיד 0.6 מ"ג Q12H), תזונה פרנטרלית (תחליב שומן, חומצות אמינו (17) וגלוקוז (1%) הזרקה של 1920 מ"ל QD), עיכוב כאב (פלורביפרופן 100 מ"ג QD) ועיכוב זיהומים (Cefoperazone Sodium ו-Sulbactam Sodium להזרקה 1.5 גרם Q8H). בצע בדיקת עמילאז לאחר הניתוח.
- השלם את הניתוח והורו למטופל לצום עד שרמת העמילאז יורדת לנורמה. התבונן מקרוב במטופל לכאבי בטן, מלנה וכו '.
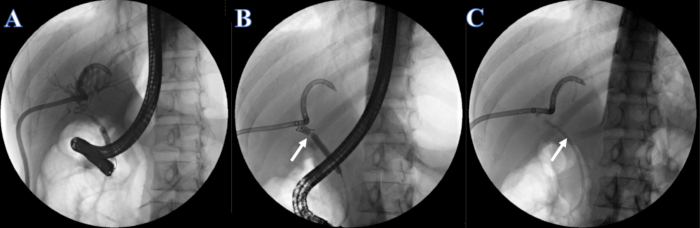
איור 4: סטנט פלסטיק שהוצב על ידי ERCP. (א) כולנגיוגרפיה PTCD. (ב) החץ הלבן מציין את הקטע הצר. (C) החץ הלבן מציין סטנט פלסטיק. אנא לחץ כאן לצפייה בגרסה גדולה יותר של איור זה.
3. הכנסת קטטר שתן
- לאחר שבוע של החלמה, הורה למטופל לשכב בשכיבה ולתת הרדמה. מחטאים את עור האפיגסטריום עם 0.5% יודופור ומכסים במגבות סטריליות.
- לאחר אישור הרדמה נכונה, הכנס את חוט ההנחיה לאורך צינור ה-PTCD, הסר את צינור ה-PTCD והנח צינור נדן מגן 20F לאורך חוט ההנחיה. הסר את חוט ההנחיה והניח כולדוכוסקופ לאורך הנדן.
- שטפו את החומר הפלוקולנטי הצהוב שנצפה בדרכי המרה של אונות הכבד הימנית והשמאלית במי מלח רגילים.
- זהה את צינור הכבד המשותף על ידי מציאת צומת צינורות הכבד השמאלי והימני בהנחיית אולטרסאונד B. שטפו את החומר הפלוקולנטי הצהוב בפתח צינור הכבד המשותף והרחיבו את ההיצרות של צינור הכבד המשותף עם בלונים של 6 מ"מ ו -8 מ"מ.
- זהה את צינור המרה המשותף על ידי סטנט הפלסטיק המוצב בשלב 2 בהנחיית אולטרסאונד B. הכנס את הכולדוקוסקופ לאורך צינור הכבד המשותף, ושטוף והרחיב את הקטע הסטנוטי של צינור הכבד המשותף שוב ושוב. פתח את הקטע הסטנוטי לחלוטין ומצא את הסטנט הפלסטי ממוקם בשלב 2.
- הכנס את חוט ההנחיה לפפילת התריסריון, הסר את הנדן והכנס קטטר שתן 12F לאורך חוט ההנחיה לתריסריון. לאחר שתסיים, הסר את חוט ההנחיה.
- תפר את העור עם מחט מתחדדת ותפר 0-0/T שאינו נספג וקשר את התפר על העור וצנתר השתן.
- להחזיר את המטופל למחלקה ולתת תרופות לעיכוב חומצה (אסומפרזול 40 מ"ג BID), עיכוב אנזים (אוקטראוטיד 0.6 מ"ג Q12H), תזונה פרנטרלית (תחליב שומן, חומצות אמינו (17) וגלוקוז (1%) הזרקה 1920 מ"ל QD), עיכוב כאב (פלורביפרופן 100 מ"ג QD) ועיכוב זיהומים (Cefoperazone Sodium ו-Sulbactam Sodium להזרקה 1.5 גרם Q8H). בצע בדיקת עמילאז לאחר הניתוח.
- הנחו את המטופל לצום עד שרמת העמילאז יורדת לנורמה. התבונן מקרוב במטופל לכאבי בטן, מלנה וכו '.
4. מיקום סטנט מרה
- לאחר שבוע אחד של התאוששות, יש להניח את סטנט המרה. הנחו את המטופל לשכב במצב שכיבה ולתת הרדמה. בדוק שהסטנט הפלסטי וצנתר השתן נמצאים במקומם (איור 5A).
- לאחר הרדמה נכונה, הכנס את התריסריון לפה, העביר אותו דרך הוושט והקיבה, הגיע לתריסריון ומצא את פפילת התריסריון. זהה את קטטר השתן ואת קצוות הסטנט הפלסטי והסר את הסטנט הפלסטי מהפה.
- הכנס את חוט ההנחיה הדו-ראשי לאורך קטטר השתן. ודא כניסה נכונה של חוט מנחה לתריסריון ולאחר מכן clamp עם גוף זר clamp, עובר דרך התריסריון, הקיבה והוושט, ומוסר מהפה.
- חתוך את קו הקיבוע של העור של קטטר השתן והסר את קטטר השתן. תחת פלואורוסקופיה רנטגן, כוונן את הקצה השני של חוט ההנחיה הדו-ראשי לתוך צינור הכבד הימני על ידי משיכת חוט ההנחיה הדו-ראשי מצד הפה (איור 5B).
- הכנס חוט מנחה נוסף לצינור הכבד השמאלי (איור 5B).
- הניחו צינור מרה כפול של צמה בגודל 7F x 7 ס"מ בצינור הכבד השמאלי (איור 5C), וסטנט פלסטיק של צינור מרה בגודל 8.5 F x 12 ס"מ בצינור הכבד הימני, כאשר הקצה השני מוביל מהפפילה של התריסריון (איור 5D).
- לאורך כל ההליך, ספק חמצן דרך צינורית האף במהירות של 3 ליטר לדקה ועקוב מקרוב אחר הסימנים החיוניים במהלך ERCP. לאחר מכן, ספקו תרופות לעיכוב חומצה (אסומפרזול 40 מ"ג BID), עיכוב אנזים (אוקטראוטיד 0.6 מ"ג Q12H), תזונה פרנטרלית (תחליב שומן, חומצות אמינו (17) וגלוקוז (1%) הזרקה של 1920 מ"ל QD), עיכוב כאב (פלורביפרופן 100 מ"ג QD) ועיכוב זיהומים (Cefoperazone Sodium ו-Sulbactam Sodium להזרקה 1.5 גרם Q8H). בצע בדיקת עמילאז לאחר הניתוח.
- השלם את הפעולה. הנחו את המטופל לצום עד שרמת העמילאז יורדת לנורמה. התבונן מקרוב במטופל לכאבי בטן, מלנה וכו '.
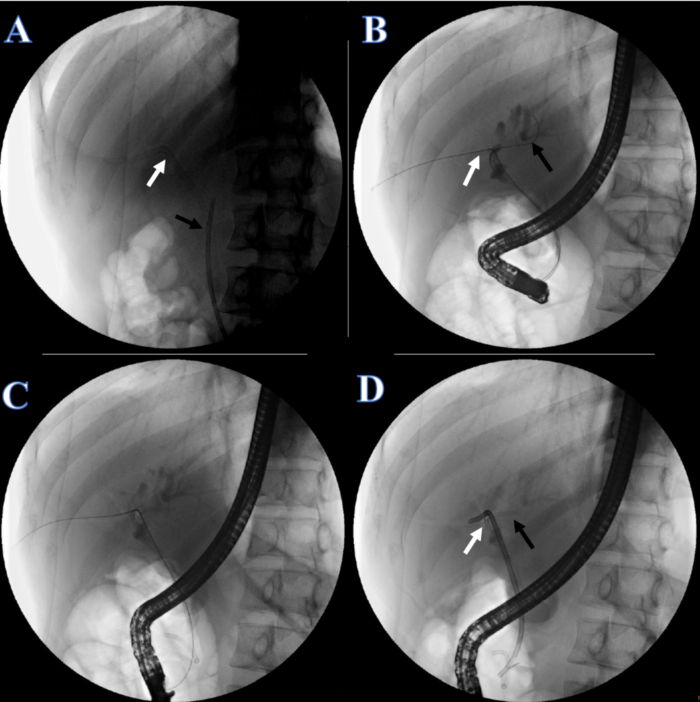
איור 5: המשכיות המרה משוחזרת על ידי ERCP. (A) החץ הלבן מציין את צינור ה-PTCD. החץ השחור מציין את הסטנט הפלסטי. (ב) החץ הלבן מציין את חוט ההנחיה הכפול דרך צינור הכבד הימני. החץ השחור מציין חוט מנחה דרך צינור הכבד השמאלי. (C) סטנט פלסטיק לצינור הכבד השמאלי. (D) החץ הלבן מציין את הסטנט הפלסטי של צינור הכבד הימני. החץ השחור מציין את הסטנט הפלסטי לצינור הכבד השמאלי. אנא לחץ כאן לצפייה בגרסה גדולה יותר של איור זה.
תוצאות
אנו מתארים שיטה חדשה המשלבת ERCP, כולנגיוסקופיה של מפעיל יחיד ו-PTCS לטיפול בדליפת מרה מורכבת לאחר השתלת כבד. כדי לשחזר את המשכיות המרה, מיקמנו צינור מרה כפול בגודל 7F x 7 ס"מ בצינור הכבד השמאלי (איור 5C) וסטנט פלסטיק של צינור מרה בגודל 8.5 F x 12 ס"מ ב...
Discussion
במחקר מצאנו שיטה חדשה לשילוב ERCP, כולנגיוסקופיה פרופורלית של מפעיל יחיד ו-PTCS לטיפול בדליפת מרה מורכבת לאחר השתלת כבד. השלבים העיקריים של שיטה זו היו כדלקמן: ראשית, תחת כולנגיוסקופיה של מפעיל יחיד פרפורלי, זוהה קצה דליפת המרה, והוצב סטנט פלסטיק. שנית, בהנחיית אולטרסאונד B, נ?...
Disclosures
המחברים מצהירים שאין ניגוד עניינים.
Acknowledgements
עבודה זו נתמכה על ידי מענקים מהקרן הלאומית למדעי הטבע של סין (81873591); קרן מדעי הטבע של גואנגדונג (2022A1515011052); פרויקט תכנון המדע והטכנולוגיה של מחוז גואנגדונג (2018A050506030); תוכנית המדע והטכנולוגיה של גואנגג'ואו (201704020073); תחזית בניית מעבדות מפתח במחוז גואנג-דונג על תרומת איברים ואימונולוגיה של השתלות (2013A061401007 ו-2017B030314018); ובסיס שיתוף הפעולה הבינלאומי של מחוז גואנג-דונג למדע וטכנולוגיה (השתלת איברים) (2015B050501002).
Materials
| Name | Company | Catalog Number | Comments |
| Biliary stent | Boston Scientific | M00533560 | 7 F*7 cm |
| Branch choledochoscope | Leinzett | LAN-EP-2612 | |
| Disposable electric snare | Boston Scientific | M00562320 | |
| Disposable sphincterotomy knife | Boston Scientific | M00545170 | |
| Electronic choledochoscope | Olympus | / | |
| Electronic duodenum mirror | Olympus | / | |
| Guidewire | Boston Scientific | M00556140 | |
| Guidewire guided the dilated balloon catheter | Boston Scientific | M00558600 | |
| Integrated biliary stent | Boston Scientific | M00539210 | 7 F*7 cm |
| Integrated biliary stent | Boston Scientific | M00539280 | 8.5 F*12 cm |
References
- Duffy, J. P., et al. Long-term patient outcome and quality of life after liver transplantation: Analysis of 20-year survivors. Ann Surg. 252 (4), 652-661 (2010).
- Riediger, C., et al. T-tube or no t-tube in the reconstruction of the biliary tract during orthotopic liver transplantation: Systematic review and meta-analysis. Liver Transpl. 16 (6), 705-717 (2010).
- Wojcicki, M., Milkiewicz, P., Silva, M. Biliary tract complications after liver transplantation: A review. Dig Surg. 25 (4), 245-257 (2008).
- Thuluvath, P. J., Pfau, P. R., Kimmey, M. B., Ginsberg, G. G. Biliary complications after liver transplantation: The role of endoscopy. Endoscopy. 37 (9), 857-863 (2005).
- Macías-Gómez, C., Dumonceau, J. M. Endoscopic management of biliary complications after liver transplantation: An evidence-based review. World J Gastrointest Endosc. 7 (6), 606-616 (2015).
- Nakajima, M., Akasaka, Y., Fukumoto, K., Mitsuyoshi, Y., Kawai, K. Peroral cholangiopancreatosocopy (pcps) under duodenoscopic guidance. Am J Gastroenterol. 66 (3), 241-247 (1976).
- Chen, Y. K., et al. Single-operator cholangioscopy in patients requiring evaluation of bile duct disease or therapy of biliary stones (with videos). Gastrointest Endosc. 74 (4), 805-814 (2011).
- Kulpatcharapong, S., Pittayanon, R. S. J. K., Rerknimitr, R. Diagnostic performance of different cholangioscopes in patients with biliary strictures: A systematic review. Endoscopy. 52 (3), 174-185 (2020).
- Rainer, F., et al. A novel way to avoid reoperation for biliary strictures after liver transplantation: Cholangioscopy-assisted guidewire placement. Endoscopy. 51 (11), E314-E316 (2019).
- Bokemeyer, A., et al. Digital single-operator cholangioscopy: A useful tool for selective guidewire placements across complex biliary strictures. Surg Endosc. 33 (3), 731-737 (2019).
- Woo, Y. S., et al. Spyglass cholangioscopy-assisted guidewire placement for post-ldlt biliary strictures: A case series. Surg Endosc. 30 (9), 3897-3903 (2016).
- Martins, F. P., Seleti, S. M. R., Contini, M. L., Ga, D. E. P., Ferrari, A. P. Is there a place for cholangioscopic evaluation of biliary anastomotic stricture after deceased donor liver transplant. Arq Gastroenterol. 57 (4), 347-353 (2020).
- Magro, B., Tacelli, M., Mazzola, A., Conti, F., Celsa, C. Biliary complications after liver transplantation: Current perspectives and future strategies. Hepatobiliary Surg Nutr. 10 (1), 76-92 (2021).
- Arain, M. A., Attam, R., Freeman, M. L. Advances in endoscopic management of biliary tract complications after liver transplantation. Liver Transpl. 19 (5), 482-498 (2013).
- Tsujino, T., et al. Endoscopic management of biliary complications after adult living donor liver transplantation. Am J Gastroenterol. 101 (10), 2230-2236 (2006).
- López Álvarez, M., Otero, M., Vázquez Millán, M. A., Suárez López, F., Alonso Aguirre, P. Endoscopic treatment of biliary complications after liver transplantation. Rev Esp Enferm Dig. 112 (8), 605-608 (2020).
- Alves, A. R., Gomes, D., Furtado, E., Tomé, L. Efficacy of endoscopic retrograde cholangiopancreatography in the treatment of biliary complications following liver transplant: 10 years of a single-centre experience. GE Port J Gastroenterol. 25 (1), 10-17 (2018).
- Yasen, A., et al. Efficiency of percutaneous transhepatic cholangioscopy in the treatment of biliary complications after liver transplantation. HPB (Oxford). 25 (4), 463-471 (2023).
- Zimmerman, M. A., et al. resolution of biliary complications after living and deceased donor liver transplantation: A report from the adult-to-adult living donor liver transplantation cohort study consortium. Liver Transpl. 19 (3), 259-267 (2013).
- Moy, B. T., Birk, J. W. A review on the management of biliary complications after orthotopic liver transplantation. J Clin Transl Hepatol. 7 (1), 61-71 (2019).
- Wadhawan, M., Kumar, A. Management issues in post living donor liver transplant biliary strictures. World J Hepatol. 8 (10), 461-470 (2016).
- Enochsson, L., et al. Nationwide, population-based data from 11,074 ercp procedures from the swedish registry for gallstone surgery and ercp. Gastrointest Endosc. 72 (6), 1175-1184 (2010).
- Khan, M. A., et al. Endoscopic ultrasound-guided biliary drainage: A systematic review and meta-analysis. Dig Dis Sci. 61 (3), 684-703 (2016).
- Dhir, V., et al. Endoscopic ultrasonography-guided biliary and pancreatic duct interventions. Dig Endosc. 29 (4), 472-485 (2017).
- Derdeyn, J., Laleman, W. Current role of endoscopic cholangioscopy. Curr Opin Gastroenterol. 34 (5), 301-308 (2018).
- Iwashita, T., Doi, S., Yasuda, I. Endoscopic ultrasound-guided biliary drainage: A review. Clin J Gastroenterol. 7 (2), 94-102 (2014).
Reprints and Permissions
Request permission to reuse the text or figures of this JoVE article
Request PermissionExplore More Articles
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. All rights reserved