JoVE 비디오를 활용하시려면 도서관을 통한 기관 구독이 필요합니다. 전체 비디오를 보시려면 로그인하거나 무료 트라이얼을 시작하세요.
Method Article
간 이식 후 복잡한 담즙 누출에 대한 새로운 치료법
* 이 저자들은 동등하게 기여했습니다
요약
담즙 누출은 간 이식 후 환자의 예후에 큰 영향을 미치는 흔한 합병증입니다. 이 프로토콜은 간 이식 후 복잡한 담즙 누출을 치료하기 위해 내시경 역행성 담췌관 조영술(ERCP), 분지 담췌관 내시경 및 경피적 간담관 내시경(PTCS)을 결합하는 새로운 방법을 제시합니다.
초록
담즙 누출은 간 이식 후 흔히 발생하는 합병증으로, 일반적으로 내시경적 역행성 담췌관 조영술(ERCP), 경피적 경간 담관 배액술(PTCD), 경피적 경간 담관 검사(PTCS) 및 수술로 치료할 수 있습니다. 간 이식 후 9개월 동안 ERCP, PTCD, PTCS 및 수술 요법이 헛수고였던 담즙 누출에 대한 새로운 치료법을 보고합니다. 우리는 다중 내시경 치료의 새로운 방법을 사용했습니다. 먼저, ERCP 및 peroral single operator cholangioscopy를 사용하여 담즙 누출 부위의 원위 끝에 마커로 플라스틱 스텐트를 배치합니다. 둘째, PTCD관을 통해 PTCS를 수행한다. 수술 중 담즙 누출 부위의 근위부 말단은 플라스틱 스텐트와 B 초음파에 의해 위치하며, 담도의 연속성은 가이드 와이어와 요로 카테터를 통해 일시적으로 재건됩니다. 셋째, 양방향 가이드와이어를 배치하고, 요로 카테터를 제거하고, 스텐트를 삽입하고, 담도 연속성을 재건합니다. 결론적으로, 우리는 간 이식 후 복잡한 담즙 누출을 치료하기 위해 ERCP, peroral single operator cholangioscopy 및 PTCS를 결합한 새로운 방법을 발견했습니다.
서문
간 이식은 말기 간 질환 환자에서 표준 치료법이 되었습니다. 간 이식 후환자의 약 1/3이 담도 합병증의 영향을 받으며, 이로 인해 심각한 이환율이 발생하고 환자 생존율이 감소하는데, 이를 간 이식의 아킬레스건 발꿈치1라고 합니다. 담즙 누출은 간 이식 다음으로 두 번째로 흔한 합병증으로, 발생률은 2%-21%2,3,4입니다. 담즙 합병증을 치료하기 위해 일반적으로 사용되는 접근법으로는 내시경적 역행성 담췌관 조영술(ERCP), 경피적 경간 담관 배액술(PTCD), 경피적 경간 담관 검사(PTCS) 및 수술이 있지만, 5 모두 효과적인 것은 아니다.
이 방법의 목표는 ERCP, peroral single operator cholangioscopy 및 PTCS를 결합하여 간 이식 후 복잡한 담즙 누출을 해결하는 것입니다.
이 방법의 기술 원리는 세 단계로 나뉩니다. 먼저, ERCP 및 peroral single operator cholangioscopy를 통해 담즙 누출의 말단을 직접 시력으로 확인하고 플라스틱 스텐트를 마커로 배치합니다. 그런 다음 PTCS를 통해 플라스틱 스텐트의 안내에 따라 담도 누출의 근위부 끝을 직접 시야 하에 총간관에서 검색하고 요로 카테터는 담도의 연속성을 재구성합니다. 마지막으로 ERCP를 통해 양방향 가이드 와이어를 사용하고 요로 카테터를 제거한 다음 좌우 간관 스텐트를 삽입하여 담도 연속성을 재건합니다.
경구담관경검사(POCS)는 1976년 일본에서 처음 보고되었다6. Chen et al.7 은 2007년에 1세대 단일 작업자 시각화 담즙경 시스템인 SpyGlass를 처음 보고했으며, 2015년 보스턴에서 2세대 SpyGlass(SpyGlass DS)를출시했습니다8. 기구의 개발로 비구강 단일 작업자 담관경 검사는 더 얇아지고 더 많은 기능을 갖게 되었습니다.
이 방법의 가장 큰 장점은 비구강 단일 작업자 담관경 검사의 직접적인 시야 하에 수행할 수 있어 수술의 성공률과 안전성을 높일 수 있다는 것입니다 9,10,11,12. Rainer9은 ERCP 스텐트 이식 실패로 간 이식 후 환자를 대상으로 직접 담도 시력 시스템을 사용하여 스텐트를 성공적으로 삽입했다고 보고했으며, 담도 협착의 작은 구멍을 직접 시각화하는 것이 가이드와이어를 성공적으로 통과할 수 있는 유일한 방법이라고 제안했습니다.
이 방법은 간 이식 후 ERCP, PTCD, PTCS 및 수술로 치료할 수 없는 복합 담즙 누출이 있는 환자에게 적합합니다.
우리는 B형 간염 바이러스의 발병으로 인한 급성 및 만성 간 부전 외에도 크론병과 백반증의 병력이 있는 38세 남성의 사례를 보고합니다. 간 기능은 반복적인 인공 간 치료에도 불구하고 시간이 지남에 따라 감소했습니다. 뇌사를 일으킨 15세 아동이 일치하는 기증자 간을 제공했을 때, 간 이식 14일 후에 담즙 누출이 발생했습니다(그림 1A). 복강 배액관과 PTCD는 급성 복통과 패혈성 쇼크로 인해 즉시 설치되었습니다. 배액 후 환자의 전반적인 건강이 개선되고 복막 삼출액이 크게 감소했습니다(그림 1B).
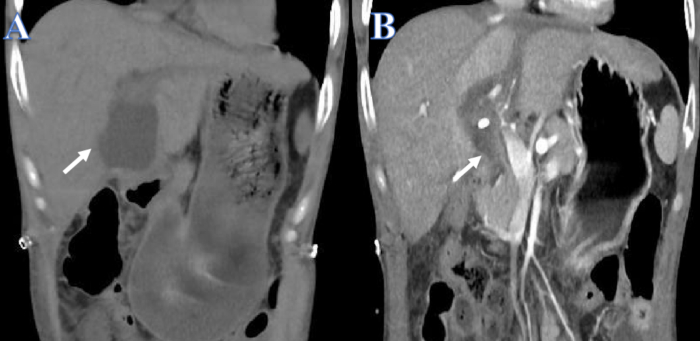
그림 1: 담즙 누출 배액 전과 후. (A) 흰색 화살표는 배수 전의 유체를 나타냅니다. (B) 흰색 화살표는 배수 후의 유체를 나타냅니다. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
3주 후, 간내 담관은 간내 담관을 통해 다른 위치로 쉽게 전달되는 가이드 와이어를 지지하기에 충분하지 않았기 때문에 좌우 간관의 PTCD 튜브를 통해 담도를 위에서 아래로 재건하려는 시도는 모두 실패했습니다(그림 2). 4주 후, ERCP를 사용하여 담도를 아래에서 위로 재건하려는 시도는 가이드와이어가 협착을 통해 간내 담관으로 들어갈 수 없었기 때문에 성공하지 못했습니다(그림 3). 2주가 지나도 총담관을 찾을 수 없었고, 골관의 좌우 간관이 만나는 곳에 수많은 결석이 있어 PTCS로 담도를 위에서 아래로 재건할 수 없었습니다. 약 4주 후, 담즙 누출을 둘러싼 조직의 명백한 염증과 부종으로 인해 담도 절개술로 담도를 재건하려는 시도는 실패했고, 환자의 이전 크론병 병력으로 인해 장 누공을 동반한 수술 후 담도 누출의 위험이 크게 증가했습니다.
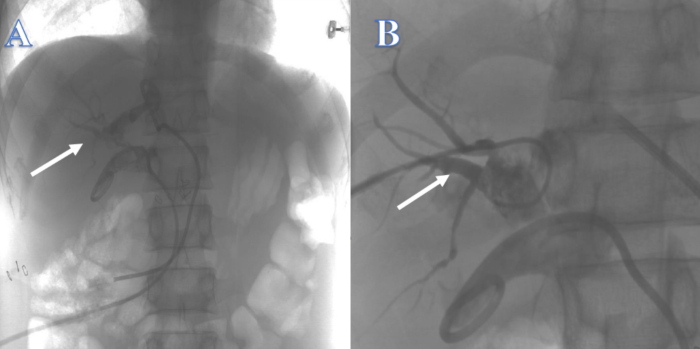
그림 2: PTC에 의해 재구성한 담즙 연속성. (A) 흰색 화살표는 좌측 간관에서 시도를 나타냅니다. (B) 흰색 화살표는 오른쪽 간관에서 시도를 나타냅니다. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.

그림 3: ERCP에 의해 재구성한 담즙 연속성. 가이드와이어가 간내 담관으로 들어갈 수 없습니다. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
여기에서는 간 이식 후 복잡한 담즙 누출을 치료하기 위해 ERCP, peroral single operator cholangioscopy 및 PTCS를 결합하는 새로운 방법을 찾았습니다. ERCP 및 비구강 단일 작업자 담관경을 통해 담즙 누출의 말단을 찾기 위해 먼저 플라스틱 스텐트를 삽입했습니다. 그런 다음 PTCS와 B 초음파로 담즙 누출의 근위부 끝을 찾았고, 마지막으로 ERCP로 담도의 연속성을 재구성했습니다.
프로토콜
이 연구는 1975년 헬싱키 선언의 윤리 지침을 준수했으며 Sun Yat-sen University의 First Affiliated Hospital의 윤리 위원회의 승인을 받았습니다. 환자로부터 사전 동의를 받았습니다.
1. 수술 전 준비
- ERCP 전에 환자에게 6-8시간 동안 금식하도록 지시합니다. 페티딘 1mg/kg, 아니소다민 20mg, 미다졸람 주사 1mg, 플루르비프로펜 100mg을 정맥 주사, 테트라카인 염산염을 경구 투여합니다. 인두 반사가 사라지면 국소 마취와 진정제 및 진통제가 성공적인 것으로 간주되었습니다.
2. 플라스틱 스텐트 삽입
- 환자가 엎드린 자세로 놓였는지 확인하고 마취 깊이가 만족스러우면 절차를 시작합니다. 십이지장 내시경을 입에 삽입하고 식도와 위를 통과시켜 십이지장에 도달하고 십이지장 유두를 찾습니다.
- 가이드와이어를 총담관에 삽입합니다.
- ERCP 또는 PTCD 튜브를 통해 2mL/s의 속도로 요오프로마이드 주사(요오드 농도 300mg/mL)를 투여합니다. 주사 후 담관 조영술을 위해 간내 및 간외 담관을 관찰하고 담관의 협착을 확인합니다. 담관의 협착은 총간관에 위치하며 간내 및 간외 담관은 동시에 시각화할 수 없습니다(그림 4A).
- 6-8mm 확장 풍선이 있는 총담관의 아래쪽 개구부를 풍선에 요오프로마이드를 주입하여 7mm로 확장합니다.
- peroral single operator cholangioscopy를 삽입하여 담관을 관찰하고 통과할 수 없는 협착을 찾은 후 협착을 통해 가이드 와이어를 삽입한 후 6mm 담도 확장 부기로 팽창시킵니다.
- 요오프로마이드 주사를 주입하여 6-8mm 확장 풍선이 있는 협착증을 7mm로 확장합니다(그림 4B).
- 담관을 관찰하기 위해 peroral single operator cholangioscopy를 다시 삽입합니다. 결석과 응집성 물질이 있는 블라인드 담관에 주목하십시오.
- 협착을 통해 7F x 7cm 플라스틱 담도 스텐트를 블라인드 덕트에 삽입하고 다른 쪽 끝을 십이지장 유두 밖으로 배치합니다(그림 4C).
- 시술 전반에 걸쳐 3L/min의 속도로 비강 캐뉼라를 통해 산소를 공급하고 ERCP 중 활력 징후를 면밀히 모니터링합니다. 그런 다음 위산 억제(에소메프라졸 40mg BID), 효소 억제(옥트레오타이드 0.6mg Q12H), 비경구 영양(지방 에멀젼, 아미노산(17) 및 포도당(1%) 주사 1920mL QD), 통증 억제(플루르비프로펜 100mg QD) 및 감염 억제(주사용 Cefoperazone Sodium 및 Sulbactam Sodium 주사용 1.5g Q8H)를 위한 약물을 제공합니다. 수술 후 아밀라아제 검사를 실시합니다.
- 수술을 완료하고 환자에게 아밀라아제 수치가 정상으로 떨어질 때까지 단식하도록 지시합니다. 복통, 멜레나 등이 있는지 환자를 면밀히 관찰합니다.
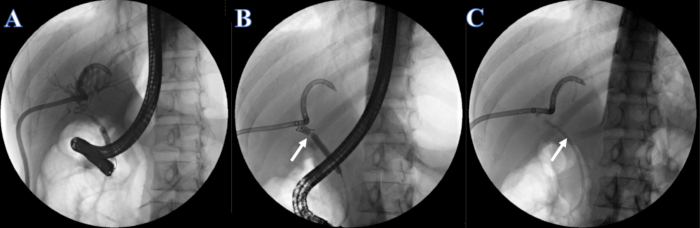
그림 4: ERCP에 의해 삽입된 플라스틱 스텐트. (A) PTCD 담관 조영술. (B) 흰색 화살표는 좁은 부분을 나타냅니다. (C) 흰색 화살표는 플라스틱 스텐트를 나타냅니다. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
3. 요로 카테터 배치
- 회복 1주일 후, 환자에게 누운 자세로 누워 마취를 실시하도록 지시합니다. 0.5% 요오드로 상위부 피부를 소독하고 멸균 수건으로 덮습니다.
- 적절한 마취를 확인한 후 PTCD 튜브를 따라 가이드와이어를 삽입하고 PTCD 튜브를 제거한 후 가이드와이어를 따라 20F 보호 피복 튜브를 놓습니다. 가이드와이어를 제거하고 칼집을 따라 담즙경을 놓습니다.
- 오른쪽 및 왼쪽 간엽의 담관에서 관찰된 노란색 응집성 물질을 정상 식염수로 세척합니다.
- B 초음파의 안내에 따라 좌우 간관의 접합부를 찾아 공통간관을 확인합니다. 총간관 개구부의 노란색 응집성 물질을 씻어내고 6mm 및 8mm 풍선으로 총간관의 협착을 확장시킵니다.
- B-초음파 유도 아래의 2단계에서 삽입한 플라스틱 스텐트로 총담관을 확인합니다. 총간관을 따라 담즙경을 삽입하고 총간관의 협착 부분을 반복적으로 세척 및 확장시킵니다. 협착 분절을 완전히 열고 2단계에서 배치된 플라스틱 스텐트를 찾습니다.
- 가이드와이어를 십이지장 유두에 삽입하고 덮개를 제거한 다음 가이드와이어를 따라 십이지장에 12F 요로 카테터를 삽입합니다. 완료되면 가이드와이어를 제거합니다.
- 테이퍼 바늘과 0-0/T 비흡수성 봉합사로 피부를 꿰매고 피부와 요로 카테터에 봉합사를 매듭지습니다.
- 환자를 병동으로 돌려보내 위산 억제제(에소메프라졸 40mg BID), 효소 억제제(옥트레오타이드 0.6mg Q12H), 비경구 영양제(지방 에멀젼, 아미노산(17) 및 포도당(1%) 주사 1920mL QD), 통증 억제제(플루르비프로펜 100mg QD) 및 감염 억제제(주사용 Cefoperazone Sodium 및 Sulbactam Sodium 주사용 1.5g Q8H)에 대한 약물을 투여합니다. 수술 후 아밀라아제 검사를 실시합니다.
- 아밀라아제 수치가 정상으로 떨어질 때까지 환자에게 단식하도록 지시합니다. 복통, 멜레나 등이 있는지 환자를 면밀히 관찰합니다.
4. 담즙 스텐트 삽입
- 회복 1주일 후, 담도 스텐트를 삽입한다. 환자에게 엎드린 자세로 누워 마취를 시행하도록 지시합니다. 플라스틱 스텐트와 요로 카테터가 제자리에 있는지 확인합니다(그림 5A).
- 적절한 마취 후 십이지장 내시경을 입에 삽입하고 식도와 위를 통과시켜 십이지장에 도달하여 십이지장 유두를 찾습니다. 요로 카테터와 플라스틱 스텐트 끝을 확인하고 입에서 플라스틱 스텐트를 제거합니다.
- 요로 카테터를 따라 양방향 가이드 와이어를 삽입합니다. 가이드와이어가 십이지장에 올바르게 삽입되었는지 확인한 다음 clamp 이물질로amp, 십이지장, 위, 식도를 통과하여 입에서 제거합니다.
- 요로 카테터의 피부 고정 라인을 자르고 요로 카테터를 제거합니다. X선 형광투시법에서 입 쪽에서 양방향 가이드 와이어를 당겨 양방향 가이드 와이어의 다른 쪽 끝을 오른쪽 간관으로 조정합니다(그림 5B).
- 왼쪽 간관에 다른 가이드와이어를 삽입합니다(그림 5B).
- 왼쪽 간관에 7F x 7cm 이중 피그테일 담관을 배치하고(그림 5C), 오른쪽 간관에 8.5F x 12cm 담관 플라스틱 스텐트를 배치하고 다른 쪽 끝은 십이지장 유두에서 이어집니다(그림 5D).
- 시술 전반에 걸쳐 3L/min의 속도로 비강 캐뉼라를 통해 산소를 공급하고 ERCP 중 활력 징후를 면밀히 모니터링합니다. 그런 다음 위산 억제(에소메프라졸 40mg BID), 효소 억제(옥트레오타이드 0.6mg Q12H), 비경구 영양(지방 에멀젼, 아미노산(17) 및 포도당(1%) 주사 1920mL QD), 통증 억제(플루르비프로펜 100mg QD) 및 감염 억제(주사용 Cefoperazone Sodium 및 Sulbactam Sodium 주사용 1.5g Q8H)를 위한 약물을 제공합니다. 수술 후 아밀라아제 검사를 실시합니다.
- 작업을 완료합니다. 아밀라아제 수치가 정상으로 떨어질 때까지 환자에게 단식하도록 지시합니다. 복통, 멜레나 등이 있는지 환자를 면밀히 관찰합니다.
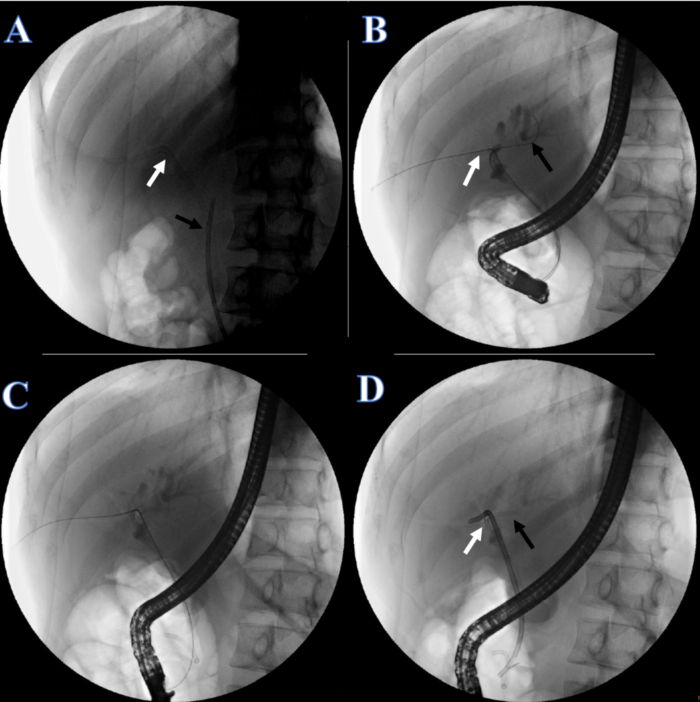
그림 5: ERCP에 의해 재구성한 담즙 연속성. (A) 흰색 화살표는 PTCD 튜브를 나타냅니다. 검은색 화살표는 플라스틱 스텐트를 나타냅니다. (B) 흰색 화살표는 오른쪽 간관을 통과하는 이중 가이드 와이어를 나타냅니다. 검은색 화살표는 왼쪽 간관을 통과하는 가이드 와이어를 나타냅니다. (C) 좌측 간관을 위한 플라스틱 스텐트. (D) 흰색 화살표는 오른쪽 간관에 대한 플라스틱 스텐트를 나타냅니다. 검은색 화살표는 좌측 간관에 삽입된 플라스틱 스텐트를 나타냅니다. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
결과
간 이식 후 복잡한 담즙 누출을 치료하기 위해 ERCP, peroral single operator cholangioscopy 및 PTCS를 결합한 새로운 방법을 설명합니다. 담즙의 연속성을 재구성하기 위해 여러 내시경을 조합하여 좌측 간관에 7F x 7cm 이중 땋은 머리 담관(그림 5C)을 배치하고 오른쪽 간관에 8.5F x 12cm 담관 플라스틱 스텐트(그림 5D)?...
토론
이 연구에서 우리는 간 이식 후 복합 담즙 누출을 치료하기 위해 ERCP, peroral single operator cholangioscopy 및 PTCS를 결합하는 새로운 방법을 발견했습니다. 이 방법의 핵심 단계는 다음과 같습니다: 먼저, peroral single operator cholangioscopy를 통해 담즙 누출 부위를 확인하고 플라스틱 스텐트를 삽입했습니다. 둘째, B-초음파의 안내에 따라 일반적인 간관 협착을 관찰하고 확장시켰으며...
공개
저자는 이해 상충이 없음을 선언합니다.
감사의 말
이 연구는 중국 국립 자연 과학 재단 (81873591)의 보조금으로 지원되었습니다. 광동자연과학재단(2022A1515011052); 광동성 과학기술계획사업(2018A050506030); 광저우 과학 기술 프로그램(201704020073); 장기 기증 및 이식 면역학에 관한 광둥성 핵심 실험실 건설 전망(2013A061401007 및 2017B030314018); 및 광둥성 국제 과학 기술 협력 기지(장기 이식)(2015B050501002).
자료
| Name | Company | Catalog Number | Comments |
| Biliary stent | Boston Scientific | M00533560 | 7 F*7 cm |
| Branch choledochoscope | Leinzett | LAN-EP-2612 | |
| Disposable electric snare | Boston Scientific | M00562320 | |
| Disposable sphincterotomy knife | Boston Scientific | M00545170 | |
| Electronic choledochoscope | Olympus | / | |
| Electronic duodenum mirror | Olympus | / | |
| Guidewire | Boston Scientific | M00556140 | |
| Guidewire guided the dilated balloon catheter | Boston Scientific | M00558600 | |
| Integrated biliary stent | Boston Scientific | M00539210 | 7 F*7 cm |
| Integrated biliary stent | Boston Scientific | M00539280 | 8.5 F*12 cm |
참고문헌
- Duffy, J. P., et al. Long-term patient outcome and quality of life after liver transplantation: Analysis of 20-year survivors. Ann Surg. 252 (4), 652-661 (2010).
- Riediger, C., et al. T-tube or no t-tube in the reconstruction of the biliary tract during orthotopic liver transplantation: Systematic review and meta-analysis. Liver Transpl. 16 (6), 705-717 (2010).
- Wojcicki, M., Milkiewicz, P., Silva, M. Biliary tract complications after liver transplantation: A review. Dig Surg. 25 (4), 245-257 (2008).
- Thuluvath, P. J., Pfau, P. R., Kimmey, M. B., Ginsberg, G. G. Biliary complications after liver transplantation: The role of endoscopy. Endoscopy. 37 (9), 857-863 (2005).
- Macías-Gómez, C., Dumonceau, J. M. Endoscopic management of biliary complications after liver transplantation: An evidence-based review. World J Gastrointest Endosc. 7 (6), 606-616 (2015).
- Nakajima, M., Akasaka, Y., Fukumoto, K., Mitsuyoshi, Y., Kawai, K. Peroral cholangiopancreatosocopy (pcps) under duodenoscopic guidance. Am J Gastroenterol. 66 (3), 241-247 (1976).
- Chen, Y. K., et al. Single-operator cholangioscopy in patients requiring evaluation of bile duct disease or therapy of biliary stones (with videos). Gastrointest Endosc. 74 (4), 805-814 (2011).
- Kulpatcharapong, S., Pittayanon, R. S. J. K., Rerknimitr, R. Diagnostic performance of different cholangioscopes in patients with biliary strictures: A systematic review. Endoscopy. 52 (3), 174-185 (2020).
- Rainer, F., et al. A novel way to avoid reoperation for biliary strictures after liver transplantation: Cholangioscopy-assisted guidewire placement. Endoscopy. 51 (11), E314-E316 (2019).
- Bokemeyer, A., et al. Digital single-operator cholangioscopy: A useful tool for selective guidewire placements across complex biliary strictures. Surg Endosc. 33 (3), 731-737 (2019).
- Woo, Y. S., et al. Spyglass cholangioscopy-assisted guidewire placement for post-ldlt biliary strictures: A case series. Surg Endosc. 30 (9), 3897-3903 (2016).
- Martins, F. P., Seleti, S. M. R., Contini, M. L., Ga, D. E. P., Ferrari, A. P. Is there a place for cholangioscopic evaluation of biliary anastomotic stricture after deceased donor liver transplant. Arq Gastroenterol. 57 (4), 347-353 (2020).
- Magro, B., Tacelli, M., Mazzola, A., Conti, F., Celsa, C. Biliary complications after liver transplantation: Current perspectives and future strategies. Hepatobiliary Surg Nutr. 10 (1), 76-92 (2021).
- Arain, M. A., Attam, R., Freeman, M. L. Advances in endoscopic management of biliary tract complications after liver transplantation. Liver Transpl. 19 (5), 482-498 (2013).
- Tsujino, T., et al. Endoscopic management of biliary complications after adult living donor liver transplantation. Am J Gastroenterol. 101 (10), 2230-2236 (2006).
- López Álvarez, M., Otero, M., Vázquez Millán, M. A., Suárez López, F., Alonso Aguirre, P. Endoscopic treatment of biliary complications after liver transplantation. Rev Esp Enferm Dig. 112 (8), 605-608 (2020).
- Alves, A. R., Gomes, D., Furtado, E., Tomé, L. Efficacy of endoscopic retrograde cholangiopancreatography in the treatment of biliary complications following liver transplant: 10 years of a single-centre experience. GE Port J Gastroenterol. 25 (1), 10-17 (2018).
- Yasen, A., et al. Efficiency of percutaneous transhepatic cholangioscopy in the treatment of biliary complications after liver transplantation. HPB (Oxford). 25 (4), 463-471 (2023).
- Zimmerman, M. A., et al. resolution of biliary complications after living and deceased donor liver transplantation: A report from the adult-to-adult living donor liver transplantation cohort study consortium. Liver Transpl. 19 (3), 259-267 (2013).
- Moy, B. T., Birk, J. W. A review on the management of biliary complications after orthotopic liver transplantation. J Clin Transl Hepatol. 7 (1), 61-71 (2019).
- Wadhawan, M., Kumar, A. Management issues in post living donor liver transplant biliary strictures. World J Hepatol. 8 (10), 461-470 (2016).
- Enochsson, L., et al. Nationwide, population-based data from 11,074 ercp procedures from the swedish registry for gallstone surgery and ercp. Gastrointest Endosc. 72 (6), 1175-1184 (2010).
- Khan, M. A., et al. Endoscopic ultrasound-guided biliary drainage: A systematic review and meta-analysis. Dig Dis Sci. 61 (3), 684-703 (2016).
- Dhir, V., et al. Endoscopic ultrasonography-guided biliary and pancreatic duct interventions. Dig Endosc. 29 (4), 472-485 (2017).
- Derdeyn, J., Laleman, W. Current role of endoscopic cholangioscopy. Curr Opin Gastroenterol. 34 (5), 301-308 (2018).
- Iwashita, T., Doi, S., Yasuda, I. Endoscopic ultrasound-guided biliary drainage: A review. Clin J Gastroenterol. 7 (2), 94-102 (2014).
재인쇄 및 허가
JoVE'article의 텍스트 или 그림을 다시 사용하시려면 허가 살펴보기
허가 살펴보기더 많은 기사 탐색
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. 판권 소유