Method Article
ヒト単球由来M1とM2の分極化と 結核 菌感染時のフローサイトメトリーによる解析
Erratum Notice
要約
このプロトコルは、ヒトM1-またはM2偏光マクロファージにおける 結核 菌感染を、GFP標識型毒性株H37Rvに感染したマクロファージ様細胞への末梢血単球の分化に基づいて研究し、M1/M2マーカーの選択を含む10色のパネルを使用してフローサイトメトリーで分析する方法を提供する。
要約
ヒトマクロファージ は、結核 菌(Mtb)感染の原発宿主細胞であり、結核の免疫制御において中心的な役割を果たしている。我々は、多様なマクロフサブセットジュで緑色蛍光タンパク質(GFP)標識Mtbの可視化と深い特徴付けを可能にする10色のフローサイトメトリーパネルを用いて、M1(古典的に活性化された)またはM2(代替活性化)マクロファージ様細胞への免疫分極化を従う実験的プロトコルを確立した。健康な献血者から得られた単球は、顆粒球マクロファージコロニー刺激因子(GM-CSF)またはマクロファージコロニー刺激因子(M-CSF)と共に分化し、続いてIFN-γおよびリポ多糖(LPS)またはIL-4で分極を行い、M1またはM2細胞に分極した。完全に分極化したM1およびM2細胞は、Mtb感染マクロファージが4時間または24時間感染後にフローサイトメトリーで染色される前に、4時間Mtb-GFPに感染した。サンプル取得をフローサイトメトリーで行い、データをフローサイトメトリー解析ソフトウェアを用いて分析した。均一多様体近似法と投影(UMAP)とフェノグラフ解析による手動格子化と次元縮小が行われた。このプロトコルは、感染していないM1細胞に対するCD64、CD86、TLR2、HLA-DRおよびCCR7のレベルの上昇を特徴とする効果的なM1/M2偏光をもたらし、未感染のM2細胞はCd163、CD200R、CD206およびCD80のM2フェノタイプマーカーの強力なアップレギュレーションを示した。M1偏光細胞は、典型的には、M2偏光細胞に比べて少ない細菌を含んでいた。Mtb感染後にいくつかのM1/M2マーカーがダウンレギュレートされ、Mtbがマクロファージ偏光を調節できることを示唆している。さらに、異なるサイズの24の異なる細胞クラスターは、感染後24時間でM1およびM2未感染細胞およびMtb感染細胞の間で一意に分布することが判明した。Mtbマクロファージ研究のバックボーンとして、さまざまな研究分野での特別なニーズに採用することができるM1/M2フローサイトメトリープロトコル。
概要
マクロファージは、組織恒常性、炎症、疾患病理の調節に大きく寄与する免疫細胞である。自然免疫の必須成分である、細胞の単球マクロファージ系統は、変化した環境キューに応答して異種表現型を発現し、その可塑性および異なる解剖学的および免疫学的位置への適応を反映する1。微小環境に存在する成長因子、サイトカインおよび他のメディエーターに応じて、マクロファージは、細菌制御およびクリアランス2において異なる役割を持つ2つの主要な可逆集団に分類されている:炎症促進、古典的に活性化されたM1偏光マクロファージおよび抗炎症、代わりに活性化されたM2偏光マクロファージこの免疫偏光マクロファージのグループ化は、マクロファージの活性化および分化が線形ではないとして単純と考えられるが、疾患の発症および進行の結果において各集団が異なる特徴および機能的役割を有する連続体としてより正確に示される4、5、6、7。しかし、M1/M2マクロファージモデルには、いくつかの異なる研究分野で使用できる多くの実験的な利点があります。
結核菌(Mtb)は結核の原因物質であり、毎秒1人に感染すると推定されており、世界で最も致死的な単一感染因子と考えられている(グローバルTBレポート2019)。気道はMtb感染の主要経路であるため、肺胞マクロファージはMtbに感染する好ましい宿主細胞であり、肺におけるMtbの主要な障壁および感染性貯留層の両方を表す。異なる刺激に応答したマクロファージ分極は、7年にわたって広範囲に研究されており、出版された作品のほとんどで、 M2分極は、M2偏光刺激因子(M-CSF)およびIL-410,11と γ共に、顆粒球マクロファージコロニー刺激因子(GM-CSF)と共に誘導される。M1マクロファージは、細胞内病原体に対する抗菌反応を媒介し、抗腫瘍免疫12に必須の役割を有する強力なエフェクター細胞である。一方、M2マクロファージは、抗炎症機能、高い貪食能力を有し、寄生虫感染症12と同様に創傷治癒および組織修復に主に関与している。したがって、M1マクロファージは、M2マクロファージ13と比較してMtbの細胞内制御においてより有効であると考えられている。しかし、Mtb細菌は、自然免疫14、15、16、17を破壊するためにマクロファージ分極を調節する可能性も有する。
末梢血18から得られる単球の分化からマクロファージを生成することは一般的であるが、マクロファージは、マウス20,21から誘導多能性幹細胞(iPSC)19または骨髄由来マクロファージからも生成され得る。これらは、成熟したマクロファージ様細胞の均質集団に増殖し、分化する単球/マクロファージ前駆体から得られた一次マクロファージ細胞を研究するための実現可能な技術である。しかし、これらのプロトコルは、得られた細胞の表現型および機能に関する深い知識を提供することはめったになく、また、生体内で得られたマクロファージの間で観察される自然な不均一性を考慮する。Mtbは厳格なヒト病原体であるため、ヒト化モデルシステムでMtbを研究する利点もあります。フローサイトメトリーは、懸濁液22における単一細胞の複数の表現型および機能的特性を評価する可能性を提供する強力な技術であり、自己蛍光23、24としても知られているマクロファージなどの付着細胞でかなり困難になり得るものである。固く付着したマクロファージの化学的剥離に加えて、Mtb感染は、Mtb感染マクロファージのフローサイトメトリック分析において別のレベルの複雑さを追加する細胞に重大なストレス因子をもたらす可能性がある。
本実験プロトコルでは、病原性のMtb株H37Rvに感染した一次末梢血単球由来細胞の免疫分極に基づくヒトマクロファージ感染モデルを用いて、選択したM1およびM2マーカー25の発現を含む10色パネルを用いてフローサイトメトリーで解析した。このプロトコルは、M1またはM2偏光単球由来マクロファージにおけるMtb感染に対する応答を研究するための効率的で再現可能な方法を提供する。また、付着性Mtb感染マクロファージにフローサイトメトリーを用いると、従来のM1およびM2マクロファージに関連する様々な表面マーカーと、Mtb感染に対する縦方向の応答を研究することができます。重要なことに、このプロトコルは、他の病原体との感染症の調査、抗腫瘍研究、炎症状態の研究、薬物スクリーニングなどにも容易に採用することができ、また、ヒト臨床サンプルにおけるM1/M2マクロファージ分極の評価のために利用することができる。
プロトコル
健康な匿名の献血者からのヒト末梢血は、スウェーデンのハディンゲにあるカロリンスカ大学病院の血液バンクから得られた(倫理的承認Dnr 2010/603-31/4)。生きた毒性Mtbを含むすべての実験ステップは、スウェーデン公衆衛生庁(FOHM)、ソルナ、スウェーデンのバイオセーフティレベル3(BSL-3)研究所で行われました。
1. 培地、バッファー、細菌培養物の調製
注: すべての試薬と消耗品の詳細は、 材料表に記載されています。
- RPMI完全培地:1 mMのピルビン酸ナトリウム、2 mM L-グルタミン、10 mM HEPES、および10%の加熱不活性化ウシ血清(FBS)を含むRPMI 1640を補う。Mtb感染を行う場合は、細胞培養培地中の抗生物質を避けてください。
- 無血清RPMI培地:1 mMピルビン酸ナトリウム、2 mM L-グルタミンおよび10 mM HEPESを含むRPMI 1640を補う。
- 洗浄バッファー: 0.05%(v/v) Tween-80 を含むリン酸緩衝塩(PBS)を準備します。
- FACS バッファ: 2.5% (v/v) FBS と 0.5 mM EDTA を含む PBS を準備します。
- 固定バッファー: 4% ホルムアルデヒドを含む PBS を PBS に準備します。使用前に新しく調製し、例えば、37%ホルムアルデヒドのストック溶液から混合してください。
- 透過バッファー: 0.1% クエン酸ナトリウムと 0.1% トリトン X-100 を脱イオン水に加えます。
- 洗浄バッファー(免疫蛍光用):0.1%BSAおよび0.1%Tween-20を含むPBSを調製する。
- ブロッキングバッファー: PBSに0.1%BSAおよび10%正常ヤギ血清(NGS)を含むPBSを調製します。
- 染色緩衝液(免疫蛍光のため):0.1%BSAを含むPBSをPBSに調製する。
- 結核完全培地:サプリメントミドルブルック7H9スープ0.05%(v/v)トゥイーン-80、0.5%(v/v)グリセロール、カナマイシン(20 μg/mL)、10%(v/v)ミドルブルックオレイン酸、アルブミン、デキストロースおよびカタラーゼ濃縮(ミドルブルックOADC濃縮)。
- 細菌培養:標準的な毒性のMtb検査株、H37Rvを使用して、緑色蛍光タンパク質(GFP)を構成的に発現し、単球由来細胞の感染を行う。このMtb株は、GFPをコードする遺伝子と、カナマイシン耐性の遺伝子を含むpFPV2プラスミドを運びます。抗生物質耐性により、カナマイシンを含む培養物中のプラスミド発現菌の連続的な選択が可能となる。細菌を-80°CでTB完全培地および70%グリセロール(1:1希釈)に保存する。
2. 末梢血単核細胞のバフィーコートからの分離
注:クラスIIバイオセーフティキャビネット内の人間の血液(潜在的に伝染性)ですべての作業を行います。廃棄する前に15分間消毒剤を含む残留血液製剤を不活性化する。この場合、健康なボランティアから血液が得られた。このインビトロマクロファージ分化プロトコルは、10 x 106 分離PBMCs/ドナー/ウェルを含むように設定されました。各ドナーから、1つのバフィーコートは、全血から発生する濃縮白血球懸濁液の約50mLを含み、通常は500〜800 x 106 PBMC を提供し、そこから約10%または50〜80 x 106 個の単球を回収することができます。
- 50 mLチューブで調製した密度勾配媒体の15 mLの上に15mLのバフィーコート血液をロードします。管の壁にピペット先端を傾け、密度勾配層の上にゆっくりと血液を重ね合わせ.
- 0加速と0減速で室温(RT)で25分間、600 x g でチューブを回転させます。
注:遠心分離の前に慎重に蓋を閉じ、遠心分離後に潜在的なこぼれのためのチューブホルダーを常にチェックしてください。 - 滅菌パスツールピペットで上のプラズマ層を取り出し、その後、滅菌パスツールピペットを使用して、新しい50 mLチューブに単核細胞層を慎重に収集します。PBMCペレットに無血清RPMI培地を加え、50mLの最終容積を得る。RTで5分間500 x g で遠心分離する前にチューブを数回反転させることによって慎重に混合します。
- 上清を慎重に捨て、指の中でチューブの底を反転させて細胞ペレットを再中断します。
- PBMCsから濃度勾配媒体汚染を除去するために、無血清RPMIで細胞を2~3回洗浄し、50mLの最終体積を得る。500 x g で 5 分間の遠心分離器 RT で 5 分間、細胞上清が透明になるまで洗浄します。
- 上清を捨て、細胞を20mLの無血清RPMI培地で再懸濁する。
- トリパンブルー染色、手動で血球計を使用するか、または自動セルカウンターを使用して細胞を数えます。セルの懸濁液を1:2または1:10希釈で希釈し、セルトリパンブルーサンプルを96ウェルプレート(例えば50μL+ 50 μL(血球計計用)または10μL+10μL(自動細胞数カウント用)に混合し、細胞を数えて生細胞/mLの数を得る。
注意:トリパンブルーは有毒であり、別の化学廃棄物に廃棄する必要があります。
3. 単球由来細胞の分化と分極化
注:単球由来細胞の分化と分極化のために、M0、M1様、M2様細胞、および完全M1およびM2偏光細胞に対して以前に確立したプロトコルが25に続いた。ここでは、分かりやすくするため、完全偏光M1およびM2マクロファージのみを説明します。
- 単球の分離のためにプラスチック付着を使用してください。簡単に言えば、適切な濃度で6ウェル培養プレートに新たに分離したPBMCsを種分し、例えば、2mL無血清RPMI培地で10 x 106 PBMCs/well、37°Cおよび5%CO2でインキュベートする。
- 2~3時間後、非接着性細胞をピペットで取り除き、1mLの無血清培地でウェルを3回洗浄します。この付着した細胞は単球であり、ウェルに加えたPBMCs全体の約10%、すなわち10 x 10 6 PBMCsから10個 の10個 の単球を含む。
- マクロファージ分化のために、M1およびM2マクロファージ分極のための50 ng/mL GM-CSFまたはM-CSFを含む働く溶液を準備し、ウェルあたりRPMI完全培地の2 mLで添加した。5%CO2インキュベーターで細胞を37°Cで3日間培養した。
- 3日目に、各ウェルの最上層から慎重に細胞培養培地1mLを除去し、M-CSFまたはGM-CSFの二重濃度を含む1mLの新鮮なRPMI完全培地で細胞培養液を補い、ウェル内の50ng/mL最終濃度を得る。100 ng/mL/well のあらかじめ作られた作業ソリューションに成長因子を追加します。
- 6日目に、細胞分化の最後の18〜20時間に対して異なる刺激を加え、完全に偏光および成熟したM1(インターフェロンγを得る。IFN-γ、及びリポ多糖;LPS(大腸菌O55:B5))またはM2(インターロイキン4;IL-4)マクロファージ。M1偏光の場合は、RPMI完全培地でIFN-γとLPSを調製し、ウェルあたり50 μLを加えて、細胞培養中の50 ng/mL IFN-γおよび10 ng/mL LPSの最終濃度を得ます。M2偏光の場合、RPMI完全培地でIL-4を調製し、ウェルあたり50 μLを加えて、細胞培養中の20ng/mLの最終濃度を得ます。
- M0偏光マクロファージの分化については、M-CSFのみで細胞を刺激し、サイトカインを追加(M2様表現型を提供する)を一切加えずに25。
- 光顕微鏡で単球由来細胞培養の形態を定期的に確認し、より小さな単球が大きなマクロファージ様細胞に分化されるようにする。また、M1とM2偏光の間の潜在的な形態学的差異、すなわち、より丸みを帯びた形状25を有するM2細胞と比較して、細長いM1細胞および伸伸長M1細胞を監視する。
- 7日目に、単球由来細胞のプレートをBSL-3検査室に移し、有害なMtbを感染させる。
4. Mtb文化の作製
注: BSL-3 ファシリティでは、以下の手順を実行する必要があります。悪質なMtbを使用するすべての作業のために、保護服、呼吸保護、および耐エタノール性手袋を使用してください。
- 細菌アリコートの1 mLでバイアルを解凍し、50 mL濾過キャップチューブに9 mLの完全な培地(1:10希釈)と混合します。37°Cおよび5%CO2でインキュベーター中の懸濁液を培養する。
- 24時間後、細菌の懸濁液を2,300 x g で10分間回転させ、慎重に培地を注ぎます。新しい50 mLろ過キャップ培養チューブに15〜20 mLの新鮮な結核完全培地で細菌ペレットを再懸濁し、37°Cおよび5%CO2でインキュベートする。2~3日ごとにチューブに沈降した細菌を混合して、すべての細菌細胞に均質な栄養補給を維持します。
- 7~10日後、50 mLスクリューキャップチューブに移す前に、上下にピペットを入れて適切に細菌懸濁液を混合します。
- 35~40 mLの無菌洗浄バッファーを50 mLチューブに加え、2,300 x g で10分間、細菌の懸濁液を回転させます。洗浄手順を一度繰り返します。細菌ペレットを1mLの無血清RPMI培地に再懸濁し、マイクロピペットでピペット化する。
- さらに9 mLの無血清RPMI培地を加え、クラスIIバイオセーフティキャビネット内で細菌懸濁液を37°Cで5分間超音波処理し、細菌の塊を破壊します。チューブを水浴超音波処理器に繰り返し(3~4回)浸して、細菌の塊の最大の破壊を確実にします。バイオセーフティキャビネット内に配置された分光光度計を使用して、1mLの細菌懸濁液の光学密度(OD)を600nm波長で測定します。無血清RPMI培地を使用して、基準を設定します。
- (OD+0.155)/0.161 = Y, Y x 107= Y x 106 CFU/mL、例えば、OD値0.32は細菌濃度(0.32 +0.155)/0.161=2.95、2.95 x 10 7=29.5 x 106 CFU/mLを提供する。
5. 単球由来細胞のMtb感染
注: BSL-3 ファシリティでは、以下の手順を実行する必要があります。
- 無血清RPMI培地中の細菌ペレットを新しい無菌50 mLチューブに再懸濁し、最終細菌濃度を約5 x 106 CFU/mLに調整します。
- 単球由来細胞を含む6ウェルプレートから細胞培養培地を取り除く。各ウェルに無血清RPMI培地1mLを加えます。細菌懸濁液を1ウェルあたり1 mL添加して感染多重性(MOI)5:1、すなわち、2mL/wellで106マクロファージあたり5 x 106 CFUを得て、37°Cおよび5%CO2で4時間プレートをインキュベートする。
- 感染後、細胞外細菌を除去するために1mLの無菌洗浄バッファーで細胞を3回洗浄する。プレートを傾け、慎重にコーナーから全体の洗浄バッファーを削除します。抗生物質を使わずに2 mLのRPMI完全培地でMtb感染した単球由来細胞を再懸濁し、細胞をフローサイトメトリーの前にさらに24時間(または他の時点)のために細胞を流動させる。
6. Mtb感染単球由来細胞のフローサイトメトリー染色
注: BSL-3 ファシリティでは、以下の手順を実行する必要があります。フローサイトメトリー染色は、チューブの代わりに96ウェルプレートで行うことができます。
- Mtb感染細胞(および未感染コントロール)を6ウェルプレートのウェルから取り外し、37°Cおよび5%CO2で少なくとも30分間、1ウェル当たり1mLのFACSバッファをインキュベーションします。
- ピペットを数回上下に軽くして、細胞が切り離されていることを確認します。可能であれば、顕微鏡検査で細胞剥離を確認してください。各ウェルからセルサスペンションをねじ込みマイクロ遠心チューブに移し、200 x g で5分間チューブを回転させます。上清をピペットで慎重に捨てます。
- 各チューブ内の細胞ペレットをFACSバッファーで2回洗浄し、200 x g で細胞を5分間回転させます。
- TLR2(AF647)、CD206(APC-Cy7)、CD163(BV605)、CD80(BV65)を含むフルオロクロム共役抗ヒト抗体の約50μLカクテルを有する細胞(約0.5 x 106〜10 6 個/チューブ)を染色する )、CCR7(BV711)、CD86(BV786)、CD200R(PE)、CD64(PE-ダズル594)、HLA-DR(PE-Cy5)(表1)を4°C(冷蔵庫)で30分間生用染料ゾンビ-UVと組み合わせて暗い。
- 400 μL の FACS バッファーで染色した細胞を 2 回洗浄し、200 x g で 5 分間回転させます。
- 暗い場所でRTで30分間、200μLの固定バッファー(新たに調製)で染色した細胞を固定し、マイコバクテリアの完全な不活性化を確実にします。
- 400 μLのFACSバッファーで細胞を2回洗浄し、200 x g で 5 分間回転して余分な固定バッファーを除去します。
- FACSバッファーの400 μLで固定細胞を再懸濁し、新しい1 mLマイクロ遠心分離チューブにサンプルを移してからBSL-2のフローサイトメトリーのためにBSL-3の実験室から取り出します。染色した細胞は、サンプル取得まで+4°Cで保存します。
注:BSL-3の実験室からそれらを取り出す前に70%エタノールでチューブをスプレーしてください。ホルムアルデヒドは有毒(発がん性)であり、クラスIIバイオセーフティキャビネットで取り扱う必要があります。ホルムアルデヒド廃棄物を別の化学廃棄物に廃棄する。
7. Mtb感染単球由来細胞のフローサイトメトリックデータ取得および分析
注: 手順 7.1 ~ 7.2 は、前述のフロー サイトメトリー染色の前に実行する必要があります。細胞固定後のタンデム色素の凝集および解離の問題を回避するために、一次抗体染色後4〜10時間以内にMtb感染細胞と未感染細胞のサンプル取得が行われる。
- 上記のフローサイトメトリー染色の前に、補償ビーズ(陽性および陰性の両方)を用いて、染色パネルに記載されているフルオロクロム共役抗体(表1)ごとに蛍光シグナルを補正する。
- ヒトマクロファージの染色に対する抗体希釈を活性化し、フルオロクロームごとに最適なシグナルを得る。
- 染色されていない細胞を使用して、陰性細胞集団のゲートを設定するために必要なバックグラウンド蛍光のレベルを決定し、染色された細胞を視覚化することができます(マクロファージは高度に自己蛍光です)。
- データ収集に推奨されるソフトウェアを使用して、フローサイトメーターで最低50,000個のセル/サンプルを取得します。
- フローサイトメトリー標準(FCS)形式3.1のフローサイトメーターから取得ファイルをエクスポートします。
- フローサイトメトリー解析ソフトウェアのFCSファイルを解析します。
- 前方および側面散乱(FSCおよびSSC)特性に従ってマクロファージをゲートし、ゾンビ-UV生存率染料を使用して生細胞/死細胞ゲーティングによって死細胞を除外する。
- FITCチャネルでH37Rv-GFP感染マクロファージを可視化します。
- 全マーカーに対して正に染色された細胞および幾何平均蛍光強度(MFI)の頻度を特定する(表1)。
8. Mtb感染単球由来細胞の蛍光染色
注:Mtb感染はBSL-3施設で行う必要があります。
- 免疫染色の場合、無血清RPMI培地の500 μLの種子2 x 105 PBMCs/ウェルを8ウェルチャンバースライドに入れ、2 x 104 の単球/ウェルを得る。単球の分化およびM1/M2分極化後、上述したようにMtb感染を進める。30分間の固定バッファでMtb感染の24時間後にスライドを固定します。固定スライドは、さらなる分析が行なくなるまで-20°Cの冷凍庫に保管されます。
- 200 μLのPBSで、単球由来の細胞をそれぞれ10分間2回洗浄します。
- 200 μL のパーメアビライゼーションバッファーで、RT で 5 分間透過します。
- 200 μLのPBSで細胞を3回洗浄し、それぞれ5分間洗浄します。
- 200 μLの洗浄バッファーをそれぞれ 5 分間洗浄して、細胞を 2 回洗います。
- RTで30分間のブロッキングバッファの200 μLで非特異的な結合をブロックします。
- 一次抗体を染色バッファーで1:100希釈し、非コンジュゲートCD64抗体(クローン:10.1)でM1細胞をインキュベートし、M2細胞を非共役CD163抗体(ポリクローナル)で2時間RTで培養します。
- 次に、200 μLの洗浄バッファーをそれぞれ 10 分間洗浄して、細胞を 3 回洗浄します。
- 蛍光標識二次抗体を染色バッファーで1:1,000希釈し、抗マウスIgG-Alexa Fluor 594でM1細胞をインキュベートし、抗ウサギIgG-アレクサフルーオール594をRTで1時間培養します。
- 200 μLの洗浄バッファーで細胞を3回洗浄し、それぞれ 10 分間洗います。
- チャンバーグリッドを取り外し、各ウェルにDAPI取り付け媒体の約20 μLを追加し、各スライドに1.5 mmのカバースリップを置きます。
- マニキュアの層でカバースリップをシールします。
- GFP(グリーンチャネル)の励起のために486 nmで放出されるレーザーを用いた共焦点顕微鏡を使用して画像を取得し、DAPI(青)の場合は402 nm、2次抗体(赤)の場合は560nmをそれぞれ取得します。
結果
M0、M2様細胞、M1(完全偏光M1細胞)、M2(完全偏光M2細胞)、M2(完全偏光M2細胞)への単球由来細胞の分極化に用いられるサイトカイン刺激の模式図を 図1Aに示し、M0、M1、M2細胞培養の代表的な画像、およびM1培養の代表的な画像を0日目、3、7に 示す図1Bに示す図である。未感染M0細胞は、基本的な格言戦略を実証するために使用された(図2A)。最初は、骨髄細胞(〜85%)は、大きな細胞を含む前方散乱(FSC)および側面散乱(SSC)特性に従ってゲートされ、ドットプロットの左下隅に見られるSSCおよびFSCが低い小型の破片を除いた。第2のプロットでは、ダブレット(すなわち、細胞塊)は、単一細胞と比較して面積が増加したが、高さが似ていると定義し、さらなる分析から除外した。したがって、斜めの形状ゲートの内側には、FSC-AreaとFSC-高さ(単一細胞)の間に比例するセルのみが含まれていました。次に、死細胞内部の細胞質タンパク質を染色するゾンビ-UV生存性色素を、その後の分析から死んだ細胞を除外するために使用した。予想通り、生じき生きとしていないM0細胞は、FITCチャネルで可視化されたMtb-GFP発現に対して陰性であった。
次に、感染していないMtb感染M1およびM2マクロファージと同様に同じ格言戦略を、感染後4時間で適用しました(図2B,C)。感染していないM1偏光マクロファージのFCS/SSCゲートで2つのサブ集団が検出された。1つの集団は小さいサイズ(FCS)と粒度(SSC)が高く、もう一方の集団はより大きなサイズと粒度が低い(図2B)、一方で感染していないM2細胞の正門はより均質に見えた(図2C)。M1およびM2単球由来細胞は共に、Mtb感染時に高い粒度および細胞サイズの減少に垂直シフトを示し、これは細胞内Mtb細菌の取り込みによって引き起こされる細胞内の複雑さの増加を反映している可能性がある(図2B,C)。さらに、生存性染色は、細胞死の増強を明らかにした(17-22%)MOIのMtb感染M1およびM2細胞の中で、未感染M0細胞と比較して(99%)(図2A-C)または感染していないM1およびM2細胞(データは示されていない)。代表的なデータは、Mtb-GFP発現(すなわち、Mtb感染率)が、4時間の感染後のM1(GFP陽性細胞19%GFP陽性細胞)細胞と比較してM2(すなわち、Mtb感染性)において実質的に高かった(図2B,C)。24時間の感染後、Mtb-GFP発現はM1およびM2細胞でそれぞれ43%および85%であったが、Mtb感染後4~24時間から4~24時間でGFP発現が相対的に高く、M2細胞と比較して126%対10.4%の増加がM2細胞およびM2細胞でそれぞれ10.4%増加したことを示唆した。
未感染の単球由来細胞におけるM1/M2偏光の有効性を特徴付けるために、CD64およびCD86(CD64+CD86+)およびCD163およびCD200R(CD163+ CD200R+)の二重陽性であるM1細胞を同定するためにドットプロットを使用した。図 3A,B)。M1/M2マーカーの選択は、主に私たちの前の研究25からの結果に基づいて行われましたが、他の研究26、27、28、29からも行われました。染色された細胞に対する象限を、染色されていないM1/M2細胞に対応するゲートを用いて設定した(図3A)。これらのマーカーはいずれもM1またはM2細胞によって排他的に発現されないが、表面発現の強度と同様に陽性細胞の割合は異なる。これはM1細胞の約95%およびM2細胞の79%がCD64+CD86+であったM1染色から特に明らかであったが、M1サブセットでは染色強度が実質的に高かった(図3A)。M1細胞の27%がM2マーカーCD200Rに陽性であったのに対し、CD163では陽性であったのはわずか1%で、63%のCD163+CD200R+M2細胞と比較して0.5%のCD163+CD200R+M1細胞を提供した(図3A)。 4時間のMtb感染後、Mtb-GFP陽性M1偏光細胞(16%)でCD200R+細胞の頻度の増加が認められ、一方、M2細胞においてCD163発現が減少した(図3B)。ヒートマップは、CD163+CD200R+M2細胞におけるGFP発現の高強度を示すが、CD64+CD86+M2サブセットも対応するM1細胞サブセットと比較した(図3B)。全体として、それぞれのM1およびM2マーカーの発現の変化も図3Cのヒストグラムで視覚化される。さらに、Mtb-GFP細菌はCD64+M1細胞およびCD163+M2細胞においても共焦点顕微鏡で可視化され、M1細胞と比較してM2内部Mtbの細胞内取り込みおよび/または増殖を増強した(図3D)。
手作業の格子の結果を検証するために、均一多様体近似法と投影法(UMAP)を用いて次元縮小を適用しました。UMAP分析の結果、4時間のMtb感染はマクロファージの分極化に影響を及ぼすには不十分であり、24時間の感染とは対照的に、M1およびM2のクラスターが感染していない細胞および感染細胞に明確に分離された(図4A)。未感染のM1マクロファージは、M2マクロファージと比較してCD64、CD86、TLR2、HLA-DRおよびCCR7の発現が高く表示され、未感染のM2細胞はM2フェノタイプマーカーCD163、CD200R、CD206およびCD80の強力なアップレギュレーションを示した(図4B,C)。手動ゲーティングに同意して、24時間後のMtb感染は、M2細胞上のCD163、CD200RおよびCD206の明確なダウンレギュレーションを引き起こし、M1細胞上のCD86およびHLA-DRのアップレギュレーション(図4B,C)は、Mtbがマクロファージ偏光を調節できることを示唆している。その後のフェノグラフ分析(図4D-F)は、UMAPグラフ(図4D)、円グラフ(図4E)およびヒートマップ(図4F)に示すように、M1およびM2未感染細胞およびMtb感染細胞の間で一意に分布した異なるサイズの24の異なるクラスタを同定した。全体として、これらの結果は、Mtb感染によってさらに変調される、このプロトコルの有望な効率を示し、型素で機能的に多様なM1およびM2偏光細胞を生み出す。
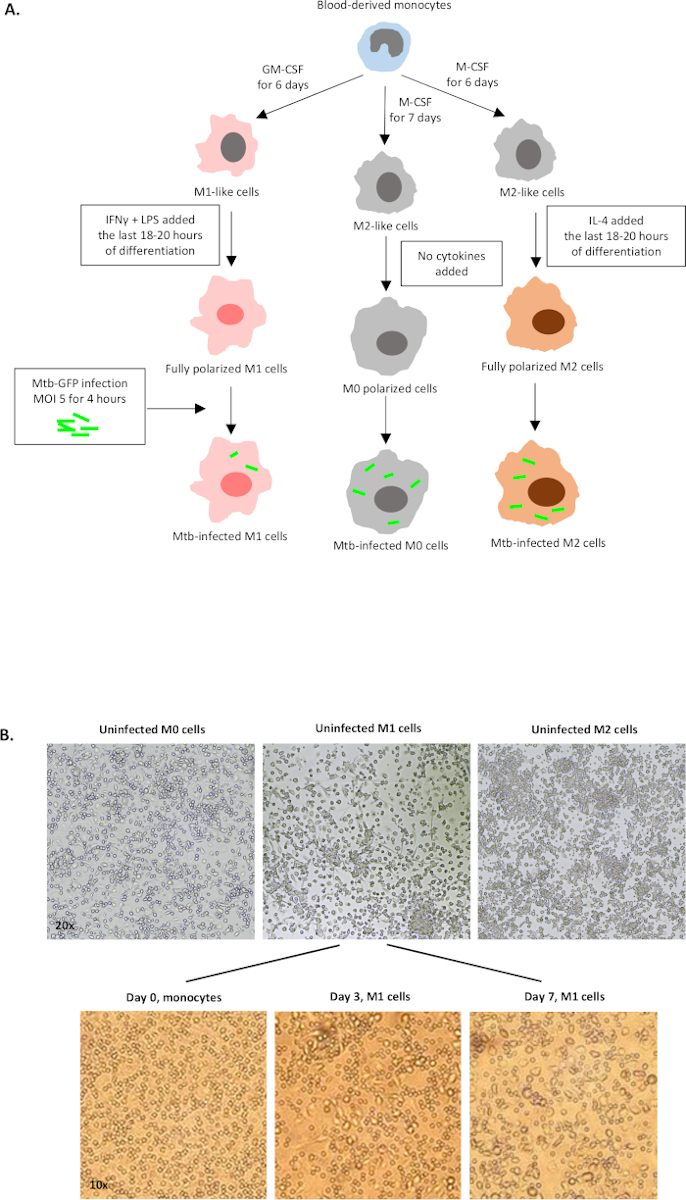
図1:ヒト骨髄由来細胞のインビトロ分化と分極化の模式図。(A)M0(M2様)、M1(古典的に活性化)、M2(代替活性化)細胞が描かれている。健康な献血者から得られた単球は、プロトコルに記載されているように異なるサイトカインで分極し、GFP標識Mtb株H37Rvに感染し、10色フローサイトメトリーで分析する前に4時間であった。M1偏光細胞は、通常、M2偏光細胞に比べて少ない細菌を含む。(B)7日目の6ウェルプレートにおける完全分極化、未感染のM0、M1およびM2細胞の顕微鏡画像、および0日目、3日目、7日目におけるM1細胞分化の代表的な画像。倍率は20倍(上パネル)と10x(下パネル)です。なお、M1細胞は、より丸みを帯びたM0およびM2セル(上部パネル)に比べて、より細長く伸びています。この図の大きなバージョンを表示するには、ここをクリックしてください。
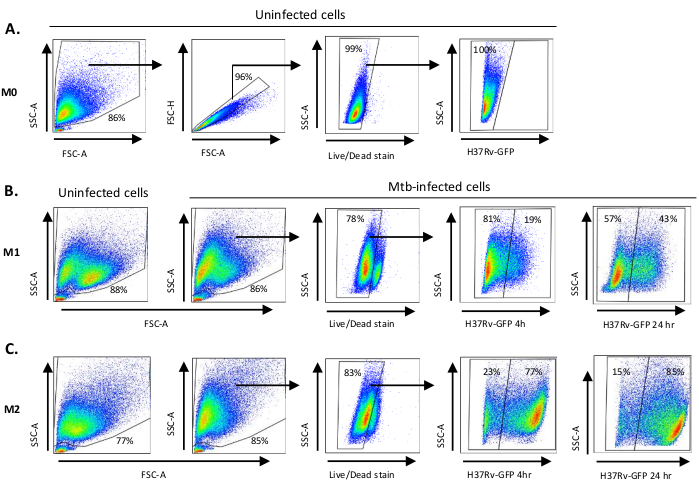
図2:微分偏光骨髄由来細胞の格子化戦略(A)感染していないM0マクロファージの前方散乱(FSC)および側面散乱(SSC)特性を示す代表的なドットプロット。FSC-A/FSC-H プロットは、面積と高さに比例した単一セルの手動格言を示しています。ライブセルゲートは、ゾンビUV(生存性染料)に陽性であった細胞を除外した。細胞内Mtbは、FITCチャネルで観察された生細胞におけるGFP発現によって検出された。(B)M1の接合と(C)M2マクロファージは、感染していない細胞およびMtb感染細胞の両方のFCS/SSCドットプロットを示す4時間および24時間感染後。この図の大きなバージョンを表示するには、ここをクリックしてください。

図3:インビトロM1/M2偏光プロトコルの有効性。代表的なドットプロットおよびM2偏光細胞のサブセット周波数を示すM1-およびM2偏光細胞のサブセット周波数を示す CD64およびCD86(M1)またはCD163およびCD200R(M2)中(A)未感染細胞および(B)Mtb感染した染色された細胞4 h感染後の細胞。(B)のドットプロットは、異なるサブゲートから得られたM1およびM2偏光マクロファージにおけるGFP発現(ヒートマップ)の蛍光強度を示す。(C)蛍光強度の幾何学的平均(MFI)は、Mtb感染の4時間後に1人の代表的ドナーからのヒストグラムで示されている。感染していないM1(水色)およびM2細胞(薄紫色)のMFI値は上部パネルに提示され、Mtb感染したM1(深い青色)およびM2細胞(深い紫色)が下のパネルに提示される。(D)非感染およびMtb感染M1およびM2偏光細胞の代表的な共焦点像が示されている。M1およびM2細胞は、それぞれ免疫蛍光を用いてCD64およびCD163発現のために染色した。正の表面染色は赤で示され、GFP発現細胞内細菌は緑色で示されている。DAPI染色された核は青色で示される。スケール – 10 μm。右の画像の倍率は350倍です。 この図の大きなバージョンを表示するには、ここをクリックしてください。
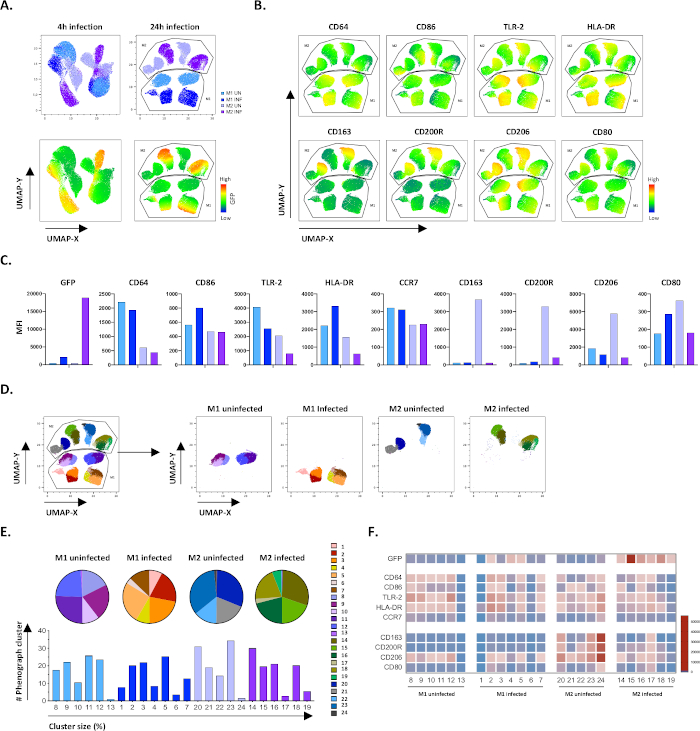
図4:均一多様体近似と投影(UMAP)による次元低減、および未感染およびMtb感染M1およびM2細胞のフェノグラフ分析。(A)UMAPは、感染していないMtb感染したM1およびM2細胞培養物から、2つの代表的な献血者、4時間(左グラフ)または24時間(右グラフ)感染後の細胞培養から11000個の生細胞を連結することによって作成される。GFP発現(下部パネル)のヒートマップは、未感染細胞とMtb感染細胞を示しています。(B-C)感染していないM1およびM2細胞24時間感染後のM2細胞で発現するマーカーのMFIは、(B)ヒートマップまたは(C)棒プロットとして示される。(D-F)フェノグラフ分析では、感染していないM1およびM2培養物の間で、感染していないM1およびM2培養物の間で、微分分布している24のクラスターが同定された。クラスタ 8 ~ 13 は感染していない M1 細胞で一意、クラスタ 1 ~ 7 は Mtb 感染 M1 細胞で一意、クラスタ 20 ~ 24 は感染していない M2 細胞では一意、クラスタ 14~19 は Mtb 感染 M2 細胞では一意です。各フェノグラフクラスター内の各マーカーのMFIは、(F)に示されています。データは、未感染のM1(水色)およびM2細胞(薄紫色)およびMtb感染M1(深い青色)およびM2細胞(深い紫色)として提示される。この図の大きなバージョンを表示するには、ここをクリックしてください。
表1:フローサイトメトリーに使用する抗体のリスト。
| レーザー | フィルター | フルオロクロム | 表現型 | 機能 | クローン | カタログいいえ。 | 会社 |
| 639 | 670/30 | AF647 | TLR2 | 病原体認識受容体 | TL2.1 | 309714 | バイオレジェンド |
| 639 | 780/60 | APC-Cy7 | CD206 | マンノース受容体 | 15-2 | 321120 | バイオレジェンド |
| 405 | 610/20 | BV605 | CD163 | スカベンジャー受容体 | GHI/61 | 333616 | バイオレジェンド |
| 405 | 670/30 | BV650 | CD80 | 共刺激分子 | 2D10 | 305227 | バイオレジェンド |
| 405 | 710/50 | BV711 | CCR7 | ケモカイン受容体 | G043H7 | 353228 | バイオレジェンド |
| 405 | 780/60 | BV785 | CD86 | 共刺激分子 | IT2.2 | 305442 | バイオレジェンド |
| 488 | 530/30 | GFP | Mtb | 細胞内細菌 | |||
| 561 | 586/15 | PE | CD200R | 阻害受容体 | OX-108 | 329306 | バイオレジェンド |
| 561 | 620/14 | PE/ダズル 594 | CD64 | IgGのFcガンマ受容体-I | 10.1 | 305032 | バイオレジェンド |
| 561 | 661/20 | PE-Cy5 (PC5) | HLA-DR | MHCクラスII分子 | L243 | 307608 | バイオレジェンド |
| 355 | 450/50 | BUV395 | 生存性染料 | ライブ/デッドセルマーカー | ゾンビUV | 423108 | インビトロジェン |
ディスカッション
この実験プロトコルは、多様なマクロファージサブセットにおけるGFP標識Mtbの可視化と深い特徴付けを可能にする10色フローサイトメトリーパネルを用いた評価を含むM1またはM2表現型への骨髄由来細胞の有効な偏光を記述する。結核は古代のヒト疾患ですが、現在のところMtbマクロファージ相互作用を研究するための黄金の標準モデルはなく、リンパ球応答の分析と比較してマクロファージの多色フローサイトメトリーが複雑になる可能性があります。マクロファージに対するヒト単球のインビトロ分化のための利用可能なプロトコルはほとんど、生成されたマクロファージの種類に関する深い知識を提示する。マーカーの固体パネルを使用したマクロファージ活性化のマクロファージ偏光およびフローサイトメトリック評価のための基本的なプロトコルは、そのような特性評価を促進し、異なる条件下で処理された偏光細胞の追加の特徴を探求する機会を提供する可能性がある。これには、インビトロで培養された細胞の分析と、臨床サンプルにおける生体内の細胞の分析、すなわち、PBMCおよび体液からの単細胞懸濁液(すなわち、気管支肺胞洗浄)または均質化組織の両方が含まれる。したがって、患者から得られた単球およびマクロファージの分化および/または活性化状態は、疾患の結果に関連する可能性がある。末梢血におけるCD16+CD163+単球の拡大は、肺結核患者30において報告されている。アトピー性皮膚炎患者31の炎症皮膚においてもCD163+細胞の増加頻度が検出された。同様に、CD206+M2様マクロファージは、アミポサイト組織32の微小環境における細胞の増殖および分化を阻害し、急性骨髄性白血病患者(AML)29の患者から骨髄サンプルに富化することが示されている。 変形性関節症患者の全血中のCD163(M2)細胞に対するCD64(M1)の上昇率は、疾患重症度33に関連していることが判明した。別の研究では、CD86(M1)およびCD163(M2)を用いて、悪性脳腫瘍34のサブグループにおいて組織における高いM1発現が悪い結果と相関していることを実証した。
この実験M1/M2フローサイトメトリープロトコルには、いくつかの重要な利点があります。このモデルは、毒性Mtb感染に対する自然免疫応答を研究する機会を提供し、混合リンパ球反応(MDR)でM1またはM2マクロファージと共に自家T細胞を添加することによって適応免疫応答の研究を含む開発が可能である。このプロトコルは、異なる免疫調節化合物および抗菌化合物の薬物スクリーニングおよび試験にも適しています。ここでは、Mtb感染後の骨髄由来細胞に対するビタミンDおよびヒストンデアセチル化酵素阻害剤フェニルブチレートの効果を研究した。M1/M2フローサイトメトリーは、細胞培養上清または患者の血漿によるコンディショニング後のマクロファージ活性化を評価するためにも使用できます。HIVまたは蠕虫または結核糖尿病の併存症との結核共感染のインビボ研究は困難であるかもしれないが、あまり複雑でないM1/M2モデルは、インビトロでの共罹患の研究を容易にするかもしれない。同様に、このプロトコルは、細胞のMtb感染性を調べるか、個々のM1/M2細胞の貪食性および抗原提示能力を調べるために、伝染研究のために利用される可能性がある。M1/M2フローサイトメトリーは、バイオマーカーやワクチン研究、治療中の病気の予後に従う、骨髄由来細胞を標的とした治療法の試験にも魅力的です。重要なのは、 マクロファージ偏光表現型と共焦点顕微鏡を用いた機能的応答の同時評価のために、フローサイトメトリーに並行して多くの異なる方法を適用することができ(図3D)、リアルタイムPCR、ウェスタンブロット、多重アッセイおよびELISAは、GFP-発現を用いた細胞内細菌感染性および増殖の評価と同様に、GFP-発現(フロー細胞質およびコンプロノサイク法およびCFU)を用いた細胞内細菌感染性および増殖の評価を用いた。Mtb-GFP細菌によるM1細胞またはM2細胞の感染により、同じサンプルから感染していない細胞とMtb感染細胞を単一細胞RNAシーケンシング解析のために選別することもできます。
また、記載されたプロトコルには、技術的および科学的な欠点を含むいくつかの制限があります。ヒトの献血者からの単球由来マクロファージを用いた欠点は、ドナーのばらつきが高いことが多く、ヒト組織の生理学的環境において細胞が分極化しないことである。M1/M2偏光効果やドナー間のMtb感染率のばらつきが大きいと、実験間の変動、統計的パワーの低下、信頼性の高い結果を得るために多くのドナーを含める必要がある。さらに、PBMCsからの単球のプラスチック付着は、ドナー依存の数の単球/ウェルをもたらし、最終的にはMtb感染後のマクロファージ分極化および細胞生存率に影響を与える可能性のある任意のMOIを提供する可能性がある。プロトコルの重要なステップは、マクロファージ偏光に影響を与える可能性のある細胞培養を汚染するために他の細胞タイプを防ぐために適切な洗浄を含む。低すぎるMOIは潜在的な結核感染を模倣するかもしれないが、あまりにも高いMOIは細胞を殺し、適切なMOIを使用することの重要性を強調する。さらに、剥離時にしっかりと接着性の細胞を取り出すのは難しい可能性があり、フローサイトメトリー分析に使用される特定のマクロファージサブセットの偏った表現につながる可能性があります。フローサイトメトリー分析の重要なステップは、ビーズ補償マトリックスと、染色されていない細胞やFMO(蛍光マイナス1)コントロールなどの陰性制御を適切に使用して、正しい手動格言を確実に行うことを含みます。
もう一つの制限は、局所組織環境からではなく、血液に由来する単球の分極化を含む。ヒト結核の特徴は、Mtb感染組織における肉芽腫の形成であり、したがって、結核の免疫病理学は局所組織部位で優先的に研究されるべきである。しかし、単球は、炎症/感染時に末梢血から肺にリクルートされ、そこで細胞は、GM−CSF12のような炎症性サイトカインの存在下でマクロファージに分化することができる。重要なことに、生体内の組織の生理的なミリューでは、結核感染の運命に寄与する多様なM1およびM2様マクロファージ集団の混合物および異なる比率を含むマクロファージ偏光の大きな不均一性がある36。我々は、以前に、TB37におけるマクロファージ媒介性肉芽腫形成の3D研究を可能にするヒト組織性肺組織モデルを開発した。現在のM1/M2偏光プロトコルを肺組織モデルと組み合わせて利用して、実験組織における結核肉芽腫形成、エフェクター機能、M1/M2比をさらに研究することは興味深いかもしれません。
このM1/M2流動測定プロトコルは、炎症反応と同様に阻害に関連する特徴の評価に有用な骨髄マーカーの拡張パネルを含むように容易に適応することができる。PD-1、SIRP-α、IDOおよびアルギナーゼなどの阻害免疫チェックポイント分子に大きな研究関心があり、マクロファージ応答38を調節することができる。この文脈において、骨髄細胞の分極化はまた、結核38を含むいくつかの疾患に関与することが示されている免疫調節マクロファージ(Mreg)または骨髄由来サプレッサー細胞(MDSC)を促進する他の刺激を伴う可能性がある。M1/M2/Mregマクロファージサブセットのより高度なフローサイトメトリーパネルには、サイトカイン/ケモカインIL-1β、TNF-α、IL-10およびMCP-1または誘導性一酸化窒素(iNOS)および抗菌ペプチドなどの他の可溶性因子またはエフェクター分子の細胞内染色も含まれる。これは、T細胞39について広く説明されているものと同様に、多機能マクロファージ応答を研究する可能性を高めることができる。
現在、フローサイトメトリー染色パネルには最大30〜40色を含めることができ、これは複数の細胞サブセットおよび分子を同時に免疫表現する能力を提供する。このM1/M2フローサイトメトリープロトコルの基本的な実験的なセットアップは、ほとんどの古い、また新しいフローサイトメーターと互換性があり、BSL-3環境で悪質なMtbの仕事によってもたらされる課題を含む個々のニーズに基づいて構築され、調整することができるバックボーンとして使用することができる。今日では、UMAPのような次元低減技術は、フローサイトメトリーソフトウェアの新しいバージョンで利用可能であり、高次元データ40の可視化と解釈を改善するために不可欠な単一細胞研究で生成された多数のパラメータの分析を可能にする。フローサイトメトリーの絶え間ない技術改善は、マルチパラメトリック表現型と現代の細胞選別機能の組み合わせを含め、今後数年間続く可能性が高く、このプロトコルはいくつかのマクロファージベースのMtb感染アッセイに有用であることが証明される可能性があります。
開示事項
著者らは開示するものは何もない。
謝辞
スウェーデンの公衆衛生庁、マチルダ・スヴェンソン、ソロモン・ゲブレマイケルの同僚に、BSL-3研究所での支援に感謝します。
この研究は、スウェーデン心臓肺財団(HLF)(2019-0299、2019-0302からSB)、スウェーデン研究評議会(VR)(2014-02592)からの助成金によって支えられました。 2019-01744とSBに2019-04720)、抗生物質耐性を防ぐための財団(レジスト)、カロリンスカ研究所とSB(マルコ・ロレティのための博士教育の部分的な資金調達)のKID(マルコ・ロレティのための博士教育の部分的な資金調達) から。MLはスウェーデン小児がん財団(TJ2018-0128およびPR2019-0100)から支援されました。
資料
| Name | Company | Catalog Number | Comments |
| 8-well chamber slides | Lab-Tek | 154534 | |
| BD Comp bead plus | BD | 560497 | |
| Bovine Serum Albumin | Sigma-Aldrich | A7906 | |
| DAPI Mounting media | Vector Laboratories | H-1200-10 | |
| EDTA (0.5 M) | Karolinska University hospital, Huddinge | N/A | |
| Falcon 6-well Flat Bottom plates | Corning Life Sciences | 353046 | |
| Fetal bovine serum (FBS) | Sigma-Aldrich | F7524 | |
| Formaldehyde | Sigma-Aldrich | F8775 | |
| Glycerol (70%) | Karolinska University hospital, Huddinge | N/A | |
| GM-CSF | Peprotech | 300-03 | |
| Goat anti-mouse IgG Alexa Fluor 594 secondary antibody | Invitrogen | R37121 | Secondary antibody for CD64 |
| Goat anti-Rabbit IgG Alexa Fluor 594 secondary antibody | Invitrogen | A-11037 | Secondary antibody for CD163 |
| HEPES | GE Healthcare Life Sciences | SH30237.01 | |
| IFN-γ | Peprotech | 300-02 | |
| IL-4 | Peprotech | 200-04 | |
| L-Glutamine | GE Healthcare Life Sciences | SH30034.01 | |
| LPS (Escherichia coli O55:B5) | Sigma-Aldrich | L6529 | |
| Lymphoprep | Alere Technologies AS | 11508545 | |
| M-CSF | Peprotech | 300-25 | |
| Middle Brook 7H10 agar plates | Karolinska University hospital, Huddinge | N/A | |
| Middle Brook 7H9 media | Karolinska University hospital, Huddinge | N/A | |
| Mouse anti-human CD64 primary antibody | Bio-Rad | MCA756G | Clone: 10.1 |
| Na-pyruvate | GE Healthcare Life Sciences | SH300239.01 | |
| Normal goat serum | Jackson ImmunoResearch | 005-000-121 | |
| Rabbit anti-human CD163 primary antibody | GeneTex | GTX81526 | Polyclonal |
| RPMI 1640 | Life Technologies Corporation | SH30096.01 | |
| Triton X-100 | Sigma-Aldrich | X-100 | |
| TubeSpin bioreactor tubes | TPP Techno Plastic Products AG | 87050 | |
| Tween-20 | Sigma-Aldrich | P9416 | |
| Tween-80 | Sigma-Aldrich | P4780 |
参考文献
- Sica, A., Mantovani, A. Macrophage plasticity and polarization: in vivo veritas. Journal of Clinical Investigation. 122 (3), 787-795 (2012).
- Cassetta, L., Cassol, E., Poli, G. Macrophage polarization in health and disease. Scientific World Journal. 11, 2391-2402 (2011).
- Mills, C. D., Kincaid, K., Alt, J. M., Heilman, M. J., Hill, A. M. M-1/M-2 macrophages and the Th1/Th2 paradigm. Journal of Immunology. 164 (12), 6166-6173 (2000).
- Martinez, F. O., Gordon, S. The M1 and M2 paradigm of macrophage activation: time for reassessment. F1000 Prime Reports. 6, 13 (2014).
- Atri, C., Guerfali, F. Z., Laouini, D. Role of human macrophage polarization in inflammation during infectious diseases. International Journal of Molecular Sciences. 19 (6), (2018).
- Flynn, J. L., Gideon, H. P., Mattila, J. T., Lin, P. L. Immunology studies in non-human primate models of tuberculosis. Immunological Reviews. 264 (1), 60-73 (2015).
- Mosser, D. M., Edwards, J. P. Exploring the full spectrum of macrophage activation. Nature Reviews Immunology. 8 (12), 958-969 (2008).
- Fleetwood, A. J., Lawrence, T., Hamilton, J. A., Cook, A. D. Granulocyte-macrophage colony-stimulating factor (CSF) and macrophage CSF-dependent macrophage phenotypes display differences in cytokine profiles and transcription factor activities: implications for CSF blockade in inflammation. Journal of Immunology. 178 (8), 5245-5252 (2007).
- Nathan, C. F., Murray, H. W., Wiebe, M. E., Rubin, B. Y. Identification of interferon-gamma as the lymphokine that activates human macrophage oxidative metabolism and antimicrobial activity. Journal of Experimental Medicine. 158 (3), 670-689 (1983).
- Leidi, M., et al. M2 macrophages phagocytose rituximab-opsonized leukemic targets more efficiently than m1 cells in vitro. Journal of Immunology. 182 (7), 4415-4422 (2009).
- Stein, M., Keshav, S., Harris, N., Gordon, S. Interleukin 4 potently enhances murine macrophage mannose receptor activity: a marker of alternative immunologic macrophage activation. Journal of Experimental Medicine. 176 (1), 287-292 (1992).
- Italiani, P., Boraschi, D. From Monocytes to M1/M2 macrophages: Phenotypical vs. functional differentiation. Frontiers in Immunology. 5, 514 (2014).
- Verreck, F. A., et al. Human IL-23-producing type 1 macrophages promote but IL-10-producing type 2 macrophages subvert immunity to (myco)bacteria. Proceedings of the National Academy of Sciences. 101 (13), 4560-4565 (2004).
- Redente, E. F., et al. Differential polarization of alveolar macrophages and bone marrow-derived monocytes following chemically and pathogen-induced chronic lung inflammation. Journal of Leukocyte Biology. 88 (1), 159-168 (2010).
- Refai, A., Gritli, S., Barbouche, M. R., Essafi, M. Mycobacterium tuberculosis virulent factor ESAT-6 drives macrophage differentiation toward the pro-inflammatory M1 phenotype and subsequently switches it to the anti-inflammatory M2 phenotype. Frontiers in Cellular and Infection Microbiology. 8, 327 (2018).
- Kahnert, A., et al. Alternative activation deprives macrophages of a coordinated defense program to Mycobacterium tuberculosis. European Journal of Immunology. 36 (3), 631-647 (2006).
- Marino, S., et al. Macrophage polarization drives granuloma outcome during Mycobacterium tuberculosis infection. Infection and Immunity. 83 (1), 324-338 (2015).
- Erbel, C., et al. An in vitro model to study heterogeneity of human macrophage differentiation and polarization. Journal of Visualized Experiments. (76), e50332 (2013).
- Lee, C. Z. W., Kozaki, T., Ginhoux, F. Publisher Correction: Studying tissue macrophages in vitro: are iPSC-derived cells the answer. Nature Reviews Immunology. 18 (11), 726 (2018).
- Ying, W., Cheruku, P. S., Bazer, F. W., Safe, S. H., Zhou, B. Investigation of macrophage polarization using bone marrow derived macrophages. Journal of Visualized Experiments. (76), e50323 (2013).
- Van den Bossche, J., Baardman, J., de Winther, M. P. Metabolic characterization of polarized M1 and M2 bone marrow-derived macrophages using real-time extracellular flux analysis. Journal of Visualized Experiments. (105), e53424 (2015).
- McKinnon, K. M. Flow Cytometry: An Overview. Current Protocols in Immunology. 120, 1-11 (2018).
- Njoroge, J. M., et al. Characterization of viable autofluorescent macrophages among cultured peripheral blood mononuclear cells. Cytometry. 44 (1), 38-44 (2001).
- Li, F., et al. Autofluorescence contributes to false-positive intracellular Foxp3 staining in macrophages: a lesson learned from flow cytometry. Journal of Immunological Methods. 386 (1-2), 101-107 (2012).
- Rao Muvva, J., Parasa, V. R., Lerm, M., Svensson, M., Brighenti, S. Polarization of human monocyte-derived cells with vitamin D promotes control of Mycobacterium tuberculosis infection. Frontiers in Immunology. 10, 3157 (2019).
- Tarique, A. A., et al. functional, and plasticity features of classical and alternatively activated human macrophages. American Journal of Respiratory Cell and Molecular Biology. 53 (5), 676-688 (2015).
- Hristodorov, D., et al. Targeting CD64 mediates elimination of M1 but not M2 macrophages in vitro and in cutaneous inflammation in mice and patient biopsies. MAbs. 7 (5), 853-862 (2015).
- Jaguin, M., Houlbert, N., Fardel, O., Lecureur, V. Polarization profiles of human M-CSF-generated macrophages and comparison of M1-markers in classically activated macrophages from GM-CSF and M-CSF origin. Cellular Immunology. 281 (1), 51-61 (2013).
- Xu, Z. J., et al. The M2 macrophage marker CD206: a novel prognostic indicator for acute myeloid leukemia. Oncoimmunology. 9 (1), 1683347 (2020).
- Liu, Q., et al. Differential expression and predictive value of monocyte scavenger receptor CD163 in populations with different tuberculosis infection statuses. BMC Infectious Diseases. 19 (1), 1006 (2019).
- Sugaya, M., et al. Association of the numbers of CD163(+) cells in lesional skin and serum levels of soluble CD163 with disease progression of cutaneous T cell lymphoma. Journal of Dermatological Science. 68 (1), 45-51 (2012).
- Nawaz, A., et al. CD206(+) M2-like macrophages regulate systemic glucose metabolism by inhibiting proliferation of adipocyte progenitors. Nature Communications. 8 (1), 286 (2017).
- Liu, B., Zhang, M., Zhao, J., Zheng, M., Yang, H. Imbalance of M1/M2 macrophages is linked to severity level of knee osteoarthritis. Experimental and Therapeutic Medicine. 16 (6), 5009-5014 (2018).
- Lee, C., et al. M1 macrophage recruitment correlates with worse outcome in SHH Medulloblastomas. BMC Cancer. 18 (1), 535 (2018).
- Rekha, R. S., et al. Phenylbutyrate induces LL-37-dependent autophagy and intracellular killing of Mycobacterium tuberculosis in human macrophages. Autophagy. 11 (9), 1688-1699 (2015).
- Mattila, J. T., et al. Microenvironments in tuberculous granulomas are delineated by distinct populations of macrophage subsets and expression of nitric oxide synthase and arginase isoforms. Journal of Immunology. 191 (2), 773-784 (2013).
- Braian, C., Svensson, M., Brighenti, S., Lerm, M., Parasa, V. R. A 3D Human Lung Tissue Model for Functional Studies on Mycobacterium tuberculosis Infection. Journal of Visualized Experiments. (104), e53084 (2015).
- Brighenti, S., Joosten, S. A. Friends and foes of tuberculosis: modulation of protective immunity. Journal of Internal Medicine. , 12778 (2018).
- Chattopadhyay, P. K., Roederer, M. Good cell, bad cell: flow cytometry reveals T-cell subsets important in HIV disease. Cytometry Part A. 77 (7), 614-622 (2010).
- Becht, E., et al. Dimensionality reduction for visualizing single-cell data using UMAP. Nature Biotechnology. 37, 38-44 (2019).
Erratum
Formal Correction: Erratum: Polarization of M1 and M2 Human Monocyte-Derived Cells and Analysis with Flow Cytometry upon Mycobacterium tuberculosis Infection
Posted by JoVE Editors on 10/14/2020. Citeable Link.
An erratum was issued for: Polarization of M1 and M2 Human Monocyte-Derived Cells and Analysis with Flow Cytometry upon Mycobacterium tuberculosis Infection. Author and affiliation information was updated.
The author and affiliation information was updated from:
Akhirunnesa Mily1, Sadaf Kalsum1, Marco Giulio Loreti1, Rokeya Sultana Rekha2, Jagadeeswara Rao Muvva1, Magda Lourda1,3, Susanna Brighenti1
1Center for Infectious Medicine (CIM), Department of Medicine Huddinge, ANA Futura, Karolinska Institutet
2Clinical Microbiology, Department of Laboratory Medicine (Labmed), ANA Futura, Karolinska Institutet
3Childhood Cancer Research Unit, Department of Women's and Children's Health, Karolinska Institutet
to:
Akhirunnesa Mily1,2, Sadaf Kalsum1, Marco Giulio Loreti1, Rokeya Sultana Rekha3, Jagadeeswara Rao Muvva1, Magda Lourda1,4, Susanna Brighenti1
1Center for Infectious Medicine (CIM), Department of Medicine Huddinge, ANA Futura, Karolinska Institutet
2Infectious Diseases Division, International Centre for Diarrhoeal Disease Research, Bangladesh
3Clinical Microbiology, Department of Laboratory Medicine (Labmed), ANA Futura, Karolinska Institutet
4Childhood Cancer Research Unit, Department of Women's and Children's Health, Karolinska Institutet
転載および許可
このJoVE論文のテキスト又は図を再利用するための許可を申請します
許可を申請This article has been published
Video Coming Soon
Copyright © 2023 MyJoVE Corporation. All rights reserved