Method Article
神経細胞移植のヒト大脳オルガノイドモデル
要約
ここでは、標識された神経細胞をヒト大脳オルガノイドに移植および追跡するためのプロトコルについて説明します。
要約
細胞移植アプローチの進歩には、移植された細胞の機能的効力を正確に評価できるモデルシステムが必要です。中枢神経系では、異種移植は依然として最先端ですが、そのようなモデルは技術的に困難であり、スループットに限界があり、高価です。さらに、存在する環境シグナルは、ヒト細胞と完全に交差反応するわけではありません。この論文では、ヒト神経細胞をヒト大脳オルガノイドに移植および追跡するための、安価でアクセスしやすく、ハイスループット互換のモデルを提示します。これらのオルガノイドは、市販のキットを使用してヒト人工多能性幹細胞から容易に作製でき、大脳の主要な細胞タイプを含んでいます。
まず、EGFP標識ヒトiPS細胞由来の神経前駆細胞(NPC)をこれらのオルガノイドに注入することで、この移植プロトコルを実証します。次に、生細胞蛍光顕微鏡法によるオルガノイドにおけるこれらの細胞の増殖を追跡するための考慮事項について説明し、オルガノイドに移植されたEGFP標識NPCの4か月間の追跡を示します。最後に、移植された細胞の局所的な状況での切片化、周期的免疫蛍光染色、およびイメージングのプロトコルを提示します。ここで紹介するオルガノイド移植モデルでは、安価で実施が簡単なプロトコルにより、移植されたヒト細胞をヒト微小環境で直接(少なくとも4か月)追跡することができます。したがって、これは、神経細胞治療(移植)と、中枢神経系(CNS)腫瘍をより微小環境的に正確な方法でモデル化するための有用なモデルである可能性が高い。
概要
ヒトの脳は、神経系とグリア系の複数の細胞型で構成される複雑な器官です。これらが一緒になって、認知を生じさせる洗練されたネットワークを形成します。外傷性脳損傷(TBI)1,2、神経変性疾患3,4,5,6,7、脳卒中8など、さまざまな神経疾患の治療薬として、このシステムへの細胞移植に大きな関心が寄せられています.しかし、このような戦略の進歩における大きな限界の1つは、予想される移植結果を決定するために利用可能な前臨床モデルが相対的に不足していることです。現在最も使用されているモデルは、細胞電位を決定するためのin vitro培養法とマウスへの異種移植です。細胞培養法は分化と自己複製能を評価できますが9、これらは移植の文脈で細胞が遭遇する微小環境を模倣しない最適な増殖条件下で行われます。さらに、細胞の増殖の仕方も、細胞の挙動に影響を与える可能性がある10。
マウスの脳は微小環境のすべての細胞を含んでおり、移植のための非常に強力なモデルシステムである11。しかし、マウスとヒト皮質の間には重要な違いがあり12,13、すべての成長因子が種間で交差反応するわけではありません。霊長類モデルは、人間のシステムをよりよく模倣し、重要な前臨床結果ももたらした、より緊密な代替手段です14。しかし、これらのより近縁な近縁種でさえ、細胞構成に重要な違いを保持している15。これらのモデルシステムはどちらも、移植中の細胞挙動に関する貴重な洞察を提供し、最終的な治療の外科的要素を組み込んでいますが、不完全なままです。また、コストがかかり、技術的にも困難であるため(つまり、動物に脳外科手術を行わなければならない)、可能なスループットが制限されます。さらに、ヒトの脳細胞を動物に移植することに関連する倫理的問題は山ほどある16。脳スライス培養では、1つの脳を切断して複数の治療に使用することができるため、動物移植の制限の一部が取り除かれます。しかし、これらは寿命(数週間)が限られており、依然として動物由来であり、(薄切りであるため)細胞の注入を模倣するのに十分な体積/表面の完全性を有していない17。したがって、厳密な細胞培養/ポテンシャルモデルとin vivo移植の間には重要なギャップが残っています。
脳オルガノイドは、脳内に存在する主要な神経細胞タイプを含むin vitroモデルであり、ヒト人工多能性幹細胞(iPS細胞)から大量に生成することができます18,19。したがって、このようなオルガノイドは、移植環境における目的の試験細胞の機能的能力の評価を可能にする細胞状況を提供する。実際、最近の研究では、ヒト大脳オルガノイドに移植された神経前駆細胞(NPC)は、肥満の糖尿病患者であるエベレ複合免疫不全gアンマ(NSG)マウスの脳に移植されたNPCと同様に生存、増殖、分化することが実証されました20。したがって、脳オルガノイドは、ヒトの脳の細胞型を捕捉する、虐待がなく、長寿命(>6ヶ月)で費用対効果の高いシステムです。そのため、神経細胞の再生能力を早期に試験するための理想的な移植レシピエントとなる可能性があります。
この論文では、標識されたヒトNPCをヒト脳オルガノイドに移植し、その後追跡するためのプロトコルを提示します(図1)。これは、GFP標識NPCを成熟した(生後2〜4か月の)脳オルガノイドに注射することから始まります18。その後、移植された細胞に続いて、生細胞蛍光顕微鏡を4ヶ月間にわたって行います。この間、注射部位での細胞の持続性だけでなく、オルガノイドの遠位領域への遊走も示しています。エンドポイントでは、以前の研究に基づいて、既存のAlexaFluorベースの色素を消光して追加の染色およびイメージングラウンドを可能にするプロトコルを含む、これらのオルガノイドに由来する組織学的切片の抗原賦活化、染色、およびイメージングを実証します21。従ってこのプロトコルは移植の設定のセルの微分容量の測定で有用、接木の耐久性、 その場のセル拡張および移植の場所からのセル移動で有用であることができる。これは、再生医療/細胞治療への応用だけでなく、腫瘍細胞を関連する領域特異的なオルガノイドに生着させることによる腫瘍モデリングにも役立つと期待されています。
プロトコル
注:このプロトコルで使用されるすべての材料、試薬、および機器の詳細については、 材料表 を参照してください。
1. レンチウイルス形質導入による細胞の蛍光色素標識
- 選択した可溶化基底膜マトリックスのアリコートを氷上で解凍します。
- アリコートが解凍されている間に、滅菌水を加えて、24ウェルプレートのウェル間の隙間を埋め、外側のすべてのウェルも埋めます。
注:これにより、中央に8つのウェルが開いて使用することができ、セルが高湿度に保たれるため、蒸発による変動が最小限に抑えられます。 - 可溶化した基底膜マトリックスを氷冷DMEM/F12培地で1:100に希釈します(ここで使用したロットで最終濃度0.089 mg/mLが得られました)。
- 希釈した可溶化基底膜マトリックス300μLを、実施する感染ごとに調製した24ウェルプレートの中間(オープン)ウェルの1つに加えます。ウェルの底全体を均等に覆い、必要に応じてさらに追加して、均一なコーティングを確保してください。
- プレートを37°Cで30分間インキュベートし、ウェル底に沿って層を固化させます。このインキュベーションの最後に、液体がまだウェルの底を完全に覆っており、中央で蒸発していないことを確認します。蒸発は湿度が低すぎることを示しています。このような場合は、コーティングを繰り返してください。
注:プレートは前日の夜にコーティングし、希釈した可溶化基底膜マトリックスに放置しても、明らかな悪影響はありません。ただし、蒸発の危険性が大幅に高まるため、使用前に慎重に検査する必要があります。 - ウェルプレート内で増殖するコンフルエントiPS細胞由来NPCの1つのウェルから培地を除去します。
注:この論文では、継代3と継代10の間のメーカーの指示に従って市販キットを使用して作製されたiPS細胞由来の神経前駆細胞を使用しました。 - ウェルの側面に1 mLのPBSを静かに加え、プレートを揺り動かして均一に洗浄します。
- PBSを除去し、300 μLのタンパク質分解-コラーゲン分解酵素混合物と交換し、再びプレートを揺動させてウェル底部を完全にコーティングします。37°Cで5分間インキュベートします。 細胞がプレート表面から剥離していることを光学顕微鏡で確認します。
- P1,000ピペットで、700 μLのDMEM/F12を加え、この混合物をプレート底面のすべての表面にスプレーして細胞を剥離します。ピペットを上下に動かして、細胞凝集体が均一な単一細胞懸濁液に分解されるようにします。細胞を採取し、15 mLの円錐形チューブに9 mLのDMEM/F12培地を加えます。
- 300 × g で5分間遠心分離します。
- この間に、10 μM Y-27632 を添加した培地を、1ウェルあたり500 μL分プレーティング用に十分な量と、再懸濁用に 1 mL を調製します。
注:Y-27632は、単細胞として継代した後のNPCの高い生存率を確保するために必要です。 - 上清を除去し、細胞をY-27632を添加した培地1 mLに再懸濁し、ピペッティングを数回静かに上下させて細胞凝集体を分解します。
- 数マイクロリットルの細胞を取り出し、トリパンブルーで希釈します(1:5〜1:10)。
- 血球計算盤で生細胞(トリパンブルー陰性)を数えます。トリパンブルーの希釈率を調整して、血球計算盤の象限ごとに少なくとも50個の生細胞が得られるようにし、カウントが正確であることを確認します。各ウェルに 100,000 個の細胞が存在するのに必要な細胞懸濁液の量を計算します。
- ピペッティングで細胞を穏やかに上下に混合し、計算された容量(ウェルあたり100,000細胞の場合)を取ります。これをY-27632を添加した培地(ステップ1.11から)に添加し、最終容量がプレートングするウェルあたり500 μLになるようにします。
- 希釈した可溶化基底膜マトリックスを、以前にコーティングしたウェルから除去します(30分以上のインキュベーションが完了していると仮定します)。
- ピペッティングで細胞を穏やかに混合し、各ウェルに500 μLの細胞懸濁液を加えます。
- 細胞を均等に分散させるには、細胞培養インキュベーターに入れる直前に、プレートを穏やかな直線的なスイープ(前後、停止、前後)で大きな「+」記号の動きで動かします。
- 37°C、5%CO2で一晩(16〜24時間)インキュベートします。
- 培地を取り除き、滴定レンチウイルスを加えます。単一の統合イベントが必要な場合は、細胞あたり0.3感染単位の感染の多様性を目指し(理想的には目的の細胞で滴定)、培地(Y-27632なし)に最大500 μLを補充します。
注:関心のあるレンチウイルスは、以前に行われたように、事前に滴定して購入するか、社内で製造することができます22。ここでは、ピューロマイシン耐性を有する自社製GFPレンチウイルスを用いて、EGFPを発現するNPCを作製し、選抜した。レンチウイルスが目的の細胞で滴定されておらず、コピー数が重要な場合は、いくつかのウェルに数容量を追加し、~30%のEGFP+ 細胞を含むウェルを48〜72時間後に使用することをお勧めします。コピー数が重要でない場合は、過剰なウイルスを追加することができますが、挿入突然変異誘発により、一部のクローンで異常な挙動を引き起こす可能性があるという警告があります。注意:レンチウイルスベクターは、レベル2〜3の生物学的危険です(内容によって異なります)。レンチウイルスの取り扱い、表面やプラスチック製品の除染、液体廃棄物については、地域のバイオセーフティ規制に従ってください。 - 細胞をインキュベーターに戻し、37°C、5%CO2で24時間インキュベートします。
- インキュベーターから細胞を取り出し、上清を取り除きます。
注意:この時点では、細胞からの上清にレンチウイルス粒子がまだ含まれているため、その取り扱いと廃棄については、引き続き地域のバイオセーフティ規制に従ってください。 - ウェルの壁にPBSを静かに添加し、2 x 500 μLのPBSで細胞をすすぎます。次に、ウェルの隅から取り出して、残っているレンチウイルスを洗い流します。
注意:この時点では、細胞からの上清にレンチウイルス粒子がまだ含まれているため、その取り扱いと廃棄については、引き続き地域のバイオセーフティ規制に従ってください。 - 500 μLの新鮮な培地(Y-27632なし)に変更し、37°C、5%CO2 で一晩増殖させ続けます。
- 生細胞蛍光顕微鏡を使用して、EGFPを発現する細胞の割合を検証し、進行するウェルを選択します。
- 選択したレンチウイルスベクターに選択カセット(ピューロマイシン耐性などの抗生物質耐性遺伝子)が含まれている場合は、選択剤(ここでは1 μg/mLのピューロマイシン)を、感受性はあるが耐性のない細胞を死滅させる、以前に検証された用量で培地に添加します。そうでない場合は、蛍光活性化セルソーティングを使用して、最初の分割時にEGFP+ 細胞を単離します。
- 今後は、コンフルエントを毎日モニタリングしながら細胞を維持し、毎日完全な培地交換を行ってください。
- コンフルエントに達したら、新しい6ウェルコーティングプレート(希釈した可溶化基底膜マトリックス1 mL;ステップ1.3〜1.5を参照)のウェルを1つ以上調製し、ステップ1.6〜1.15の説明に従って細胞を回収します。
注:選択剤が含まれていない場合は、この段階でフローサイトメトリーで細胞をソーティングします。細胞がストレスを最小限に抑えるために十分に広いノズルと低圧で選別されていること、および選別プロセスのすべてのステップに 10 μM Y-27632 が含まれていることを確認してください。 - 最終密度が200,000細胞/cm2になるように細胞を播種します。
- 毎日の監視を維持し、毎日メディアの変更を完了します。
注:セルが再びコンフルエントに達すると、使用する準備が整います。または、次のようにして、将来の使用のために在庫を凍結できるようになりました。 - 手順1.6-1.15の説明に従って、セルを分割し、収集し、カウントします。
- クライオバイアルのセットに関連情報(継代、EGFP%、ラインなど)を事前にラベル付けします。
- 400,000細胞/mLの培地+10%DMSOで再懸濁します。
注:DMSOは凍結していないと細胞に毒性があるため、DMSOの存在下で室温で過ごす時間は最小限に抑えてください。 - クライオバイアルごとにステップ1.33の混合物1 mL(400,000細胞)を加え、細胞凍結容器に入れます。
- 容器を-80°Cの冷凍庫に一晩移します。
- 翌日、細胞を液体窒素に移して長期保存します。
2. 脳オルガノイドへの標識細胞注入
注:この論文では、脳オルガノイドは、メーカーの指示に従って市販のキットを使用して製造されました。これは、目的の大脳オルガノイドに置き換えることができます。プロトコルのこの部分で使用される材料は、4°C以上で可溶化された基底膜マトリックスのゲル化を避けるために、事前に冷却する必要があります。
- 可溶化した基底膜マトリックスと接触させるインスリンシリンシリンジ、チップ、チューブを-20°Cに置き、冷まします。
- 実施する注入回数に応じて、氷上で可溶化した基底膜マトリックスの適切なサイズのアリコートを融解します(~2 μL/注入)。所要時間は約30分です。
- アリコートが解凍されている間に、ステップ1.6-1.15の説明に従って細胞を分割、収穫、およびカウントします。
- 注入ごとに必要な容量を計算します。複数回注入する場合は、細胞の総量を1.5 mLのチューブに入れ、最大1 mLのDMEM/F12を加えます。
注:数回の追加注入が可能な容量は、損失/ピペッティングエラーを考慮するために使用する必要があります。 - 次のステップを準備している間、細胞を氷に入れます。
- 融解後、可溶化した基底膜マトリックスを氷冷DMEM/F12で最終濃度3 mg/mLに希釈します。
- 氷からシングルセル懸濁液を取り出し、300 × g 、4°Cで5分間スピンダウンします。
注:冷蔵遠心分離機が利用できない場合、室温での回転は一般的に許容されるようです。 - 細胞ペレットを乱すことなく、培地を完全に静かに取り除きます。希釈した可溶化基底膜マトリックス(3 mg/mL)に穏やかにピペッティングして細胞ペレットを再懸濁し、実施する注入あたりの最終容量が2 μLになるようにし、使用するまで直ちに氷上に戻します。
注:細胞の再懸濁は、気泡の形成やゲル化を避けるために、予冷したチップでゆっくりと行う必要があります。 - 冷やしたシリンジを-20°Cの冷凍庫からアイスバケットに移します。使用するまで保管してください。
- 脳オルガノイドの入ったプレートをインキュベーターから取り出します。ワイドボアチップを使用して、注入するオルガノイドを35 mmディッシュに移します。オルガノイドを安定させ、注入を容易にするために、オルガノイドを傷つけることなく、可能な限りすべての培地を除去します。
注:オルガノイドを破壊しないように、ワイドボアチップを使用することが重要です。それらが利用できない場合は、滅菌ハサミで通常のP1,000チップの端を切ります。 - オルガノイドが入った35 mmのディッシュを解剖顕微鏡の下に置き、注入をガイドし、促進します。
注:無菌領域に解剖顕微鏡がない場合は、制御が多少低下しますが、顕微鏡なしで注入を行うことができます。別の代替手段は、拡大ループまたはメガネの使用です。 - オルガノイドを注入する準備ができたら、冷やしたP20ピペットチップで細胞を静かに再懸濁し、2 μL(注入する細胞数を含む)を予冷滅滅菌スライドに移します。
注:複数回の注入の場合は、スライドガラス全体に2 μLの容量を追加することができます。氷の上に置き、蒸発しないように注意してください。 - 氷から冷やしたインスリン注射器を取り出し、針の面取りを下に向けて2 μLの細胞懸濁液をゆっくりと吸い上げ、すべての細胞/培地を吸収します。
注意: 空気を引き込まないように、極端にゆっくりと進んでください。 - オルガノイドが入った皿の蓋を開け、顕微鏡の焦点を合わせます。片手で皿を持ちます。針の斜角を上に置き、もう一方の手で細胞をオルガノイド表面にゆっくりと注入します。
注:組織を傷つけないように、ゆっくりと注入することが重要です。 - 注射後、蓋を皿に戻し、注入したオルガノイドを1〜2分間放置します。
注:これにより、希釈された可溶化基底膜マトリックスがゲル化し、細胞を所定の位置に保持できます。培地の添加が早すぎると、表面に付着した細胞が洗い流されてしまう可能性があります。 - 500 μLのオルガノイド培地を静かに添加し、ワイドボアチップのオルガノイドを24ウェルプレートのウェルに移します。オルガノイドを37°C、5%CO2 で一晩インキュベートします。2日おきに完全な培地交換を行います。
注:画像調整に使用されるネガティブコントロールオルガノイド(モック注入)を含めることが重要です。これを行うには、前述のオルガノイドに希釈可溶化基底膜マトリックス(3 mg/mL)を注入し、細胞なしで最終容量の 2 μL を得ます。
3. 生細胞蛍光イメージングによる移植片トラッキング
注:目的の蛍光色素を励起でき、その蛍光を検出するために必要なフィルターセットを備えた蛍光顕微鏡を使用してください。前述したように、ここで使用したNPCはEGFP+で、励起ピークは488 nm、発光ピークは~510 nmでした。
- ネガティブコントロールオルガノイド(非注入またはモック注入)をロードし、自家蛍光が最小になるように照明強度と露光時間を設定します。ここで使用した機器では、照明強度を1〜2、露光時間を80ms〜100msに設定しました。
注:多くの励起波長(特に低波長)は細胞に毒性を持つ可能性があるため、オルガノイドの損傷を防ぐために、強度を低く保ち、長時間探すことは避けることをお勧めします。 - ポジティブコントロールオルガノイドをロードし、必要に応じて曝露時間を増やして、標識細胞がはっきりと見えるようにします。オルガノイドをワイドボアピペットチップで再配置し、注入部位(EGFP+ 領域)を見つけます。
- 培地をネガティブコントロールオルガノイドから完全に除去します。ネガティブコントロールオルガノイドをロードし、選択した設定でイメージングします(ここで使用した装置では、照明強度を1〜2、露光時間を80ms〜100msに設定しました)。イメージングが完了したら、オルガノイドが乾燥しないように、すぐに新しい培地を加えます。
注:培地除去は、浮遊して常に動いているオルガノイドの高さと向きを固定し、高品質のイメージングを妨げるため、良好な画像を得るために重要です。 - 各試験オルガノイドで培地の除去/イメージングを繰り返します。
- オルガノイドを通常のインキュベーション/培地交換(ステップ2.16と同様)に戻し、必要な間隔でイメージングを繰り返します。ここでは、注入後1週目、9週目、16週目にオルガノイドを画像化し、注入したEGFP+ NPCの生存、増殖、分化、および遊走を追跡してテストしました。
4. 組織学および免疫蛍光法
- エンドポイントで、オルガノイドを、オルガノイドのIDとその他の必要な識別子で標識された組織学カセットに移します。
- カセットに10%ホルマリンを入れ、閉じます。室温で24時間保管してください。
- オルガノイドの入ったクローズドカセットを組織プロセスに移し、次のプロトコルを設定します:エタノール70%10分、エタノール80%20分、エタノール95%30分、エタノール100%30分、エタノール100%40分、エタノール100%50分、トルエン30分、トルエン40分、トルエン50分、パラフィン59°Cで25分、パラフィン59°Cで35分、 パラフィンは59°Cで40分、パラフィンは59°Cで50分。
注意: 上記の手順は、特に指定がない限り、室温の真空下で行われます。このプロトコルは、水を最大100%のアルコールグラジエントに置き換えます。トルエンとの中間工程は、アルコールとパラフィンの両方が可溶であるため、アルコールとパラフィンの間の遷移です。 注意: トルエンとパラフィンは可燃性の高い液体であり、吸入したり、皮膚や目に触れたりして損傷を引き起こす可能性があるため、危険物と見なされます。必ずしっかりと密閉して安全な場所に保管してください。取り扱いの際は、適切な個人用保護具を着用してください。地域の化学物質危険規制に従って廃棄物を処分してください。 - オルガノイドの入ったクローズドカセットを包埋ステーションのパラフィン浴に移します。
- カセットを浴槽から取り出して開き、オルガノイドをスチール製のベース型に移します。型をパラフィンディスペンサーの下に置き、パラフィンで完全に覆います。
- 空のカセットをスチールベース金型の上に置きます。ここで、カセットの上にさらにパラフィンを追加します。
- カセットを上にしたスチールベースモールドを氷に移し、5分間冷まします。スチールモールドを取り外し、オルガノイドをパラフィンブロックに埋め込んだカセットを保管します。
- カセットをミクロトームに移し、切片を切断します。必要に応じてセクションをカットします。
注:ここでは、オルガノイド全体に15μmの厚さの切片を作製しました。 - 各切片を45°Cに設定したウォーターバスの表面に滴下し、ガラス顕微鏡スライドで拾います。
- スライドを42°Cのインキュベーターで一晩乾燥させます。
注:スライドは、染色時まで室温で保存できるようになりました。 - トルエンを充填したCoplinスライド染色ジャーにスライドを2分間入れます。この手順をもう一度繰り返します。
注意: トルエンは可燃性の高い液体であり、吸入したり、皮膚や目に触れたりすることで損傷を引き起こす可能性があるため、危険物と見なされます。必ずしっかりと密閉して安全な場所に保管してください。取り扱いの際は、適切な個人用保護具を着用してください。地域の化学物質危険規制に従って廃棄物を処分してください。 - EtOH 100%で満たされたガラス製のCoplinスライド染色ジャーに2分間移します。この手順をもう一度繰り返します。
- 蒸留水で満たされたガラス製のCoplinスライド染色ジャーに2分間移します。この手順をもう一度繰り返します。
- 抗原賦活化のために、クエン酸緩衝液(10 mM クエン酸、0.05% Tween 20、pH 6.0)を調製します。
注:クエン酸緩衝液は、室温で最大3か月間保存することも、4°Cで長期間保存することもできます。 - ウォーターバスを95°Cから100°Cの間に設定します。
注意: このウォーターバスは、注意しないと火傷を引き起こす可能性があります。浴槽やその部品に直接触れないように、必要なすべての予防措置を講じてください。 - ウォーターバスに、スライドを中に入れることができるプラスチック容器を浮かべます。溶けないように、プラスチックが浴槽の底に触れないようにしてください(底部加熱浴の場合)。プラスチック容器内にクエン酸緩衝液を注ぎ、95〜100°Cに達します。
- 緩衝液が希望の温度に達したら、スライドを緩衝液の中に置き、容器を蓋でゆるく覆います。スライドを容器内のウォーターバスに30〜40分間放置します。
- プラスチック容器をウォーターバスから取り出し、室温でさらに20分間冷まします。
- スライドをPBSで3 x 2分間洗浄します。PBSは、サンプルに触れたり、過度に乾燥させたりすることなく、ペーパーティッシュで除去します。
- 透過処理バッファー(90 mLのPBS + 0.1% Tween-20)を調製し、スライドガラス染色ジャーに充填します。スライドを透過処理バッファーに浸し、10分間インキュベートします。
- スライドをPBSで3 x 2分間洗浄します。
- 各サンプルを覆うのに十分な染色ミックス(~25 μL)を調製します。
注:ここで使用した抗体および最終濃度については、 表1 を参照してください。 - 25 μLの染色ミックスを添加して、各オルガノイドスライスを覆います。室温で1時間、または暗所で4°Cで一晩インキュベートします。
注:染色ミックスの蒸発を防ぐために、サンプルを高湿度に保ってください。スライドを湿気に保つための容器が利用できない場合は、隅にウェットティッシュを入れた箱に入れてください。 - スライドをPBSで3 x 2分間洗浄します。
- スライドガラス染色瓶の中の蒸留水で一度すすぎ、塩分を取り除きます。
- 各サンプルに10 μLの液体封入液+ 4',6-ジアミジノ-2-フェニルインドール(DAPI)を加えます。
注:2回目の染色を行わない場合は、スライドを密封することができます。ここでは、カバーガラスの除去が組織を損傷する可能性があるため、急冷/再染色のためにスライドを覆っていませんでした。 - 選択した蛍光顕微鏡を使用してスライドを画像化します。
注:強度と露光時間を適切に設定できるように、各抗体のポジティブコントロールとネガティブコントロールを用意してください(ここで使用する装置では、照明強度は5〜6、露光時間は2,000〜3,000msに設定されています)。さらに、使用する各チャンネルに適切な検出器が顕微鏡にあることを確認してください。サンプルは覆われていないため、イメージング中は表向きに配置する必要があることに注意してください。 - イメージング後、新しい2倍クエンチングバッファー(PBS中9%H2O2+50mMNaOH)を調製します。
注意: 焼入れ液は、使用する直前に新たに調製する必要があります。反応はH2O2の活性に敏感であり、これは時間の経過とともに減少する。注意:H2O 2は刺激物であり、NaOHは苛性です。これらは適切な安全装置で処理する必要があり、皮膚への接触は避けてください。.地域の化学物質安全ポリシーに従って廃棄されていることを確認してください。 - ガラス製のCoplinスライド染色ジャーに2xクエンチングバッファー(45 mL)を半分まで充填し、45 mLのPBSを加えて、スライドを中に入れます。4°Cで一晩インキュベートします。
- 蛍光顕微鏡で、蛍光色素が効果的に消光されたことを確認します。
- 上記のように染色とイメージングを繰り返します。
注:焼入れと再染色は、必要に応じて追加のラウンドで繰り返すことができますが、追加のラウンドごとに損傷のリスクが増加します。
5. イメージの登録
- フィジーを開きます。
- ラウンド 1 とラウンド 2 の DAPI 画像を含むフォルダーを作成します。必要に応じて、どちらがどれであるかを明確にするために名前を変更します。
- 画像登録の出力用に空のフォルダを作成します。
- [ プラグイン] |参加登録 |仮想スタックスライスを登録します。
- [ソース ディレクトリ] で、各ラウンドの DAPI 画像を含むフォルダーを選択します。
- [ 出力ディレクトリ] で、登録出力用に作成したフォルダーを選択します。
- [ 特徴抽出モデル ] を [リジッド ] に設定し、[ レジストレーション モデル] ドロップダウン メニューを [リジッド - 移動 + 回転 ] に設定してレジストレーションを修正し、変形ではなく、位置合わせのために画像を移動および回転のみできるようにします。
注: 変形が予想される場合は、 特徴抽出モデル と レジストレーション モデル を必要に応じて アフィン または他のモデルに調整できますが、これにより望ましくない変換が発生する可能性があります。時折、ラウンド間でスライスが損傷し、レジストレーションが成功しないことがあります。 - Save transforms(トランスフォームを保存 )チェックボックスをオンにしてトランスフォームパラメータを保存し、他のチャンネルに適用できるようにします。
- [ OK]をクリックします。
- 変換ファイルを保存する場所(デフォルトは入力ディレクトリ)を選択し、[開く]をクリックします。
- 変換の参照として使用する DAPI 画像を選択します。他の各ラウンドのDAPI画像は、このラウンドにアライメントされます。
注:完了すると、登録された画像がスタックとして(および出力フォルダーに)表示されます。 - 下部のスライドバーを使用して画像を前後に切り替え、画像のレジストレーションが成功したことを確認します(少なくとも重なり合う領域では、核は両方の画像で同じ場所にあります)。
- 入力画像のラウンドごとに.xmlファイルが作成されていることを確認します。
注: これらには、そのラウンドのファイルに必要な変換パラメータが含まれています。 - 登録するすべての画像(各ラウンドの各チャンネル)を含むフォルダーを作成します。ファイルの順序に注意してください。
- トランスフォームパラメータ用のフォルダを作成し、登録するチャンネルごとにラウンドごとに.xmlファイルのコピーを1つ作成します。次の手順では、変換パラメーター ファイルの順序で各画像を調べて変換するため、登録する画像と変換パラメーターのコピーの間でファイルの順序 (名前) が同じであることを再確認します。
- [ プラグイン] |トランスフォーム |仮想スタックスライスを変換します。
- [ソースディレクトリ]で、登録する画像が格納されているフォルダーを選択します。
- [ 出力ディレクトリ] で、登録出力用に作成したフォルダーを選択します。
- [変換ディレクトリ] で、変換するイメージ ファイルごとに 1 つのコピーを含む.xmlファイルを含むフォルダーを選択します。繰り返しになりますが、順序がファイルと一致していることを確認します(つまり、ラウンド1チャンネルごとにラウンド1.xmlのコピー1つ、ラウンド2チャンネルごとにラウンド2.xmlのコピー1つなど)。
- [ OK]をクリックします。
注:完了すると、そのラウンドから登録された画像がスタックとして(および出力フォルダーに)表示されます。 - 下部のスライドバーを使用して、チャンネル間を前後に切り替えます。すべてのチャネルが同じ方法で変換されたことを確認します。そうでない場合は、 transforms ディレクトリ内の .xml ファイルが間違っていることが原因である可能性があります。この場合、ファイルを修正して繰り返します。
注意: 表示される輝度範囲は1つのチャンネルに基づいていますが、これは実際に保存された画像には影響せず、ディスプレイにのみ影響します。 - レジストレーションされた画像がすべてラウンド間で正常に位置合わせされ、オーバーレイ/ダウンストリーム分析の準備ができていることを確認します。
注: 大きなバッチの登録を行うには、より効率的なプログラム方法があります。ここで紹介する方法は、プログラミングを必要としない簡単な方法です。
結果
大脳オルガノイドの同一性の検証として、成熟した(生後2ヶ月の)大脳オルガノイドの組織学的切片をPAX6(背側NPCのマーカー23)およびSATB2(成熟した有糸分裂後の上層ニューロンのマーカー24)について染色した。予想通り、PAX6+ 細胞はオルガノイドの内部に存在し、SATB2+ 細胞は上層に存在していました(図2)。これらの結果は、使用された大脳オルガノイドが、分化キットで指定されているように、実際に背側前脳であったことを裏付けています。脳オルガノイド移植系の用量依存性を確立するために、生後2か月の脳オルガノイドにEGFP+ iPS細胞由来NPCの数を増やして注入しました。インプット細胞数に対するGFP蛍光の明確な用量依存性が存在し、10,000細胞以上で一貫したEGFP+ 細胞パッチ検出が見られました(図3)。次に、移植されたNPCの持続性と移動性を、移植されたオルガノイドを経時的に追跡することによって評価しました。このために、50,000個のiPS細胞由来EGFP+ NPCを、同じiPS細胞株から作製した生後2〜3か月の脳オルガノイドに移植しました。注入されたオルガノイドとコントロールは、次の3〜4か月間、指定された時点でEGFP陽性の画像化されました。この移植シリーズでは、4か月の追跡期間を通じて注射部位の持続性を観察しました(図4A)。追加のEGFP+ 細胞パッチは移植後9日までに現れ、研究エンドポイント(オルガノイドに応じて3〜4か月)まで持続し、細胞の移動と新しい部位への統合を示しています(図4A)。より高い倍率では、オルガノイドへの長い突起で明確な神経形態が観察され(図4B)、注入された細胞の統合が確認されました。
注入後遅くに注入した細胞の分化状態を決定するために、4ヶ月間追跡されたオルガノイドとそのコントロールを固定し、パラフィン包埋し、厚さ15 μmのスライスに切断し、スライドガラスに取り付けました。次に、スライスを処理し、1回の蛍光染色(EGFP、TUJ1、NESTIN)または2回の連続した染色サイクルでマーカーを添加(MAP2、GFAP)しました。最初の1ラウンド染色では、NPC状態を保持する細胞(NESTIN+TUJ1−)と神経運命に分化した細胞(NESTIN−TUJ1+)の混合物を含むEGFP+細胞が注射部位に存在することが確認されました(図5)。対照オルガノイドと注入オルガノイドの両方で、NESTIN+ NPCはごくわずかしか観察されず(すべてではありませんが、ほとんどが注射部位にEGFP+移植されたNPCでした)、TUJ1+の未熟成熟ニューロンの大部分が観察されました(図5)。2ラウンド染色により、オルガノイドの外側領域の大部分に成熟したニューロン(NESTIN-TUJ1+MAP2+GFAP-)が見られ、中央に向かって未熟なニューロン(NESTIN-TUJ1+MAP2-GFAP−)の領域が明らかになりました(図6A、B)。アストロサイト(NESTIN−TUJ1−MAP2−GFAP+)は、注入されたオルガノイドとコントロールオルガノイドの両方に存在し、外縁の周囲に散在していました(図6A、B)。注入したオルガノイドで2ラウンド染色を行ったスライスは、成熟ニューロンの表現型を採用したEGFP+細胞の小さなサテライトコロニーを注入部位から遠く離れたところに示しました(図6B、C)。これらのいくつかは、アストロサイトに近接しているように見えました。しかし、GFAP染色と完全に重複するEGFP+細胞は存在せず、アストロサイト自体を生成するのではなく、隣接していることを示唆しています(図6B、C)。
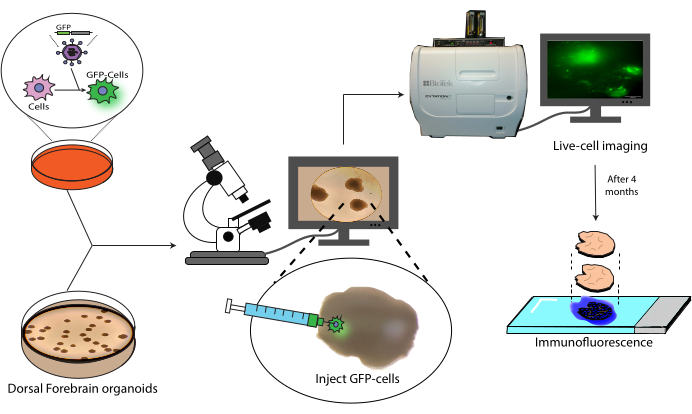
図1:標識細胞の脳オルガノイドへの移植モデル。 レンチウイルス形質導入による標識細胞の作製、脳オルガノイドへの移植、生細胞イメージングと免疫蛍光法による追跡の概略図。略語:GFP = green fluorescent protein。 この図の拡大版をご覧になるには、ここをクリックしてください。
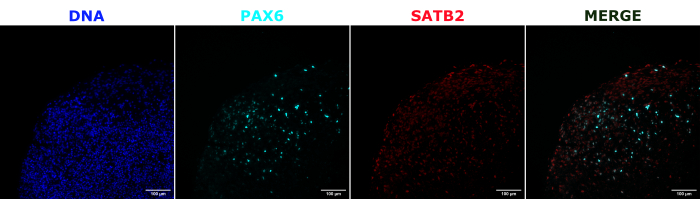
図2:初期および後期オルガノイドの構造を示す組織学的切片の免疫蛍光法。 生後2ヶ月の脳オルガノイドを固定し、パラフィン包埋し、スライスし、PAX6、SATB2、およびDAPIで染色しました。未染色の切片を使用して、自家蛍光による偽陽性シグナルを回避するための曝露時間と積分時間を設定しました。PAX6+細胞はオルガノイドの内部に存在し、SATB2+細胞は上層に存在した。Zスタック画像は、15μmの組織切片全体にわたって4.2μmごとに撮影されました。光学セクションは、Gen5ソフトウェアのフォーカススタッキングオプションとデフォルトオプションを使用して結合されました。スケールバー = 100 μm。略語: PAX6 = ペアボックス6タンパク質;SATB2 = 特殊なATリッチ配列結合タンパク質2;DAPI = 4',6-ジアミジノ-2-フェニルインドール。 この図の拡大版をご覧になるには、ここをクリックしてください。
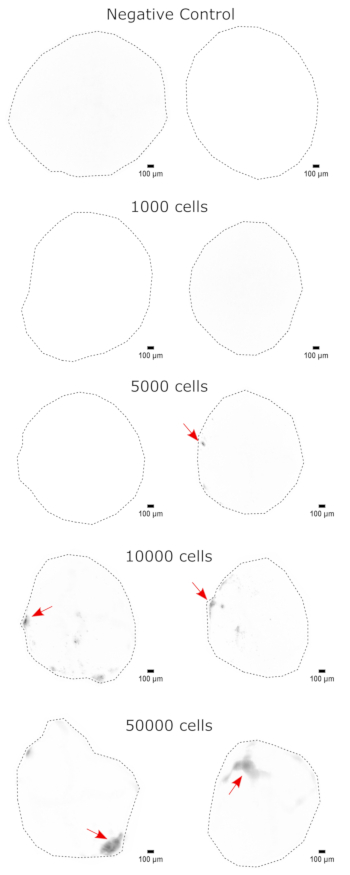
図3:NPCの脳オルガノイドへの用量依存的な生着。 オルガノイドには、0個(ネガティブコントロール)、1,000個、5,000個、10,000個、または50,000個のGFP+ iPS細胞由来NPCを移植しました。移植後1週間で、オルガノイドをGFPフィルターキューブでCytation 5にイメージングしました。ネガティブコントロールを使用して、自家蛍光を最小限に抑えるための曝露時間と積分時間を設定しました。色が濃いほど、ネガティブコントロールよりもEGFP蛍光が多いことを示します。スケールバー = 100 μm。これらはオルガノイド全体の4倍画像です。イメージング後、オルガノイド全体のバックグラウンド強度の変動を補正するために、表示前にピクセル半径50のローリングボールバックグラウンド減算を行いました。生着が最も高い領域として特定された注射部位は、生着が存在した場所に赤い矢印で示されます。略語:NPC =神経前駆細胞;GFP = 緑色蛍光タンパク質;EGFP = 増強GFP;iPS細胞=人工多能性幹細胞。 この図の拡大版をご覧になるには、ここをクリックしてください。
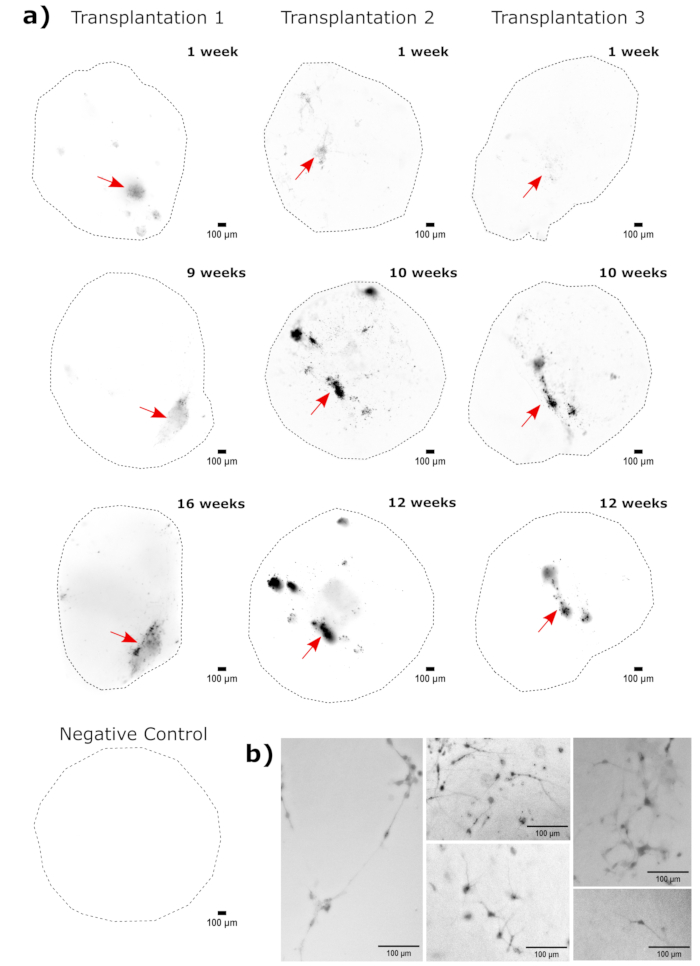
図4:蛍光生細胞イメージングによる移植細胞の増殖、遊走、および持続性の追跡。 (A)コントロールオルガノイドと移植オルガノイド(50,000 GFP+ iPS細胞由来NPC)に続いて、2つの独立した移植セットから2〜4か月にわたって蛍光生細胞イメージングを行いました。ネガティブコントロールオルガノイドを使用して、各時点での自家蛍光を最小限に抑えるための曝露時間と積分時間を設定しました。EGFP画像は、移植後の指示された時間にCytation 5のGFPフィルターキューブを使用してキャプチャされました。色が濃いほど、その時点のネガティブコントロールと比較してEGFP蛍光が多いことを示します。オルガノイド全体の変動するバックグラウンド強度を補正するために、表示前にピクセル半径50のローリングボールバックグラウンド減算を行いました。オルガノイドを各時点でほぼ同じ向きに配置し、表示の一貫性を確保し、移植された細胞増殖を明確に示すために画像を回転させました。最も早い時点で生着が最も高い領域として特定された注入部位は、赤い矢印で示されています。ネガティブコントロールオルガノイドの例を図の下部に示します。(B)移植後1週目および15週目に生着したオルガノイドからの例20x画像を示す。局所的なコントラストは、神経突起の視認性を確保するためにFIJIを使用して表示する前に強化されました。スケールバー = 100 μm。略語:NPC =神経前駆細胞;GFP = 緑色蛍光タンパク質;EGFP = 増強GFP;iPS細胞=人工多能性幹細胞。 この図の拡大版をご覧になるには、ここをクリックしてください。
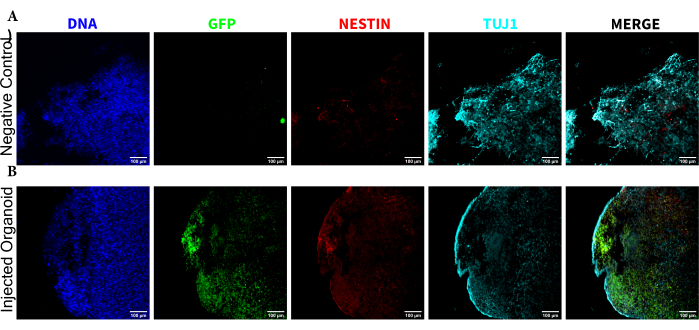
図5:組織学的切片の免疫蛍光法により、注射部位に移植されたNPCの持続性、遊走および神経分化が明らかになりました。 (A)非注入オルガノイドおよび(B)移植オルガノイドからのシングルチャンネル蛍光画像。右のオーバーレイ画像は、対象となる3つのチャンネル(NESTIN、TUJ1、EGFP)を示していますが、DAPIは含まれていません。表示の最小値は、ネガティブセルからのシグナルのみを除外するように設定しました(非注入コントロールからの EGFP と、既知のマーカーの組み合わせに基づいて他のチャネルについて決定)。表示の最大値は、任意の細胞でその抗体について観察された最高のシグナルに基づいていました。直接比較できるように、非注射オルガノイドと移植オルガノイドの間で表示範囲を一定に保ちました。スケールバー = 100 μm。略語:NPC =神経前駆細胞;DAPI = 4',6-ジアミジノ-2-フェニルインドール;TUJ1 = β-IIIチューブリン;EGFP = 増強された緑色蛍光タンパク質。 この図の拡大版をご覧になるには、ここをクリックしてください。
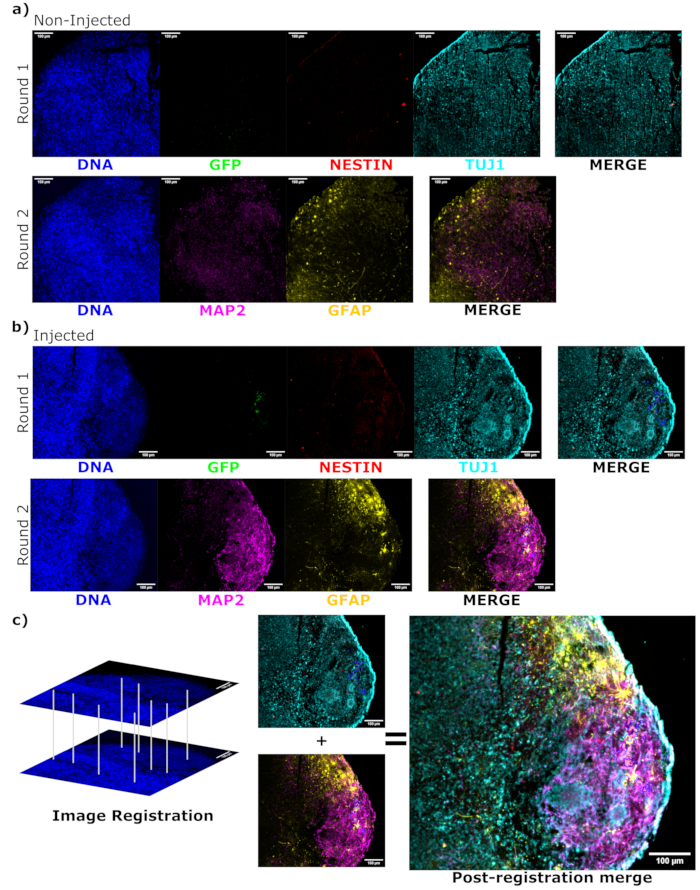
図6:組織切片の周期的免疫蛍光法を用いた生着細胞の分化状態と局在化の評価。 非注入オルガノイド、(A)年齢一致オルガノイド、および(B)移植オルガノイドからのシングルチャンネル蛍光画像が、示されているように、1回目と2回目の染色に示されています。表示の最小値は、ネガティブセルからのシグナルのみを除外するように設定しました(非注入コントロールからの EGFP と、既知のマーカーの組み合わせに基づいて他のチャネルについて決定)。表示の最大値は、任意の細胞でその抗体について観察された最高のシグナルに基づいていました。表示範囲(およびもちろんイメージングパラメータ)は、直接比較できるように、コントロールオルガノイドと注入オルガノイドの間で一定に保たれました。スケールバー = 100 μm。各オルガノイドの染色ラウンドごとに重ね合わせた画像(DAPIを除く)を右側に示します。(B)画像レジストレーションを行った注入オルガノイドについては、すべての画像を両方の染色ラウンドで観察された領域にトリミングします。(B、C)注入されたオルガノイドの場合、EGFP+ 細胞領域は青色の輪郭で囲まれています。(C)は、画像登録時にDAPIを使用して特徴を照合する方法の図を示し、その後に登録された画像の全体的なマージを示します。略語:DAPI = 4',6-ジアミジノ-2-フェニルインドール;TUJ1 = β-IIIチューブリン;EGFP = 増強緑色蛍光タンパク質;MAP2 = 微小管関連タンパク質 2;GFAP = グリア線維性酸性タンパク質。 この図の拡大版をご覧になるには、ここをクリックしてください。
| クローン | 蛍光色素 | 濃度 | |
| 抗NESTIN | セッションID: 10C2 | アレクサフルオッ... 594 | 1で2,000 |
| アンチTUBB3 | TUJ1 | AlexaFluor 647(アレクサフローア647) | 1で2,000 |
| 抗GFP | FM264Gの | アレクサフローア488 | 1で200 |
| アンチGFAP | SMIの25 | アレクサフルオッ... 594 | 1で500 |
| アンチMAP2 | SMIの52 | アレクサフローア488 | 1人に1,000人 |
| アンチPAX6 | O18-1330 | AlexaFluor 647(アレクサフローア647) | 1で100 |
| アンチSATB2 | EPNCIR130A | アレクサフルオッ... 594 | 1で500 |
表1:染色用の抗体濃度。 略語:TUBB3 =ベータチューブリンIII;GFP = 緑色蛍光タンパク質;GFAP =グリア線維性酸性タンパク質;MAP2 = 微小管関連タンパク質 2;PAX6 = ペアボックス6タンパク質;SATB2 = 特殊なATリッチ配列結合タンパク質2。
ディスカッション
中枢神経系損傷/神経変性疾患の治療のための細胞治療アプローチへの大きな関心を考えると1,2,3,4,5,6,7,8、移植環境における細胞機能のモデルの重要性が高まっています。この論文では、標識されたヒトNPCをヒト大脳オルガノイドに移植する方法と、その生細胞追跡、組織学および免疫蛍光染色によるエンドポイント評価について紹介します。重要なことは、移植された細胞がオルガノイド設定で遊走、分化、および長期(4か月)の持続が可能であることを示したことです。このような長期持続性は、脳スライス培養の保守性よりも顕著に向上する17。したがって、このシステムは、生存、増殖、分化など、潜在的な治療環境で評価する必要がある多くの行動を調べるのに適しています。実際、最近の直交研究では、移植されたNPCは、NSGマウスの脳に移植されたNPCと比較して、大脳オルガノイドで同様の挙動を示すことが示され20、移植レシピエントとしてのオルガノイドの有用性が確認されました。これはin vitroシステムであるため、サイトカインや目的の薬物を添加することも簡単です。これは、炎症や免疫抑制剤などの特定の環境が移植細胞に及ぼす影響をよりよく理解し、治療環境で遭遇する可能性のあるものをさらに模倣するために使用できます。私たちが実証したサイクリック免疫蛍光プロトコール(以前の研究21に基づく)は、このアプローチの力をさらに拡張し、幅広い系統マーカーと潜在的に疾患特異的マーカーを単一のセクションで同時に評価することを可能にし、したがって、移植された細胞と組織への影響を正確に追跡することができます。もちろん、分析の目的に応じて、代わりに他のエンドポイント評価方法を使用することもできます。例えば、細胞の形態が主な関心事である場合は、3D再構成による組織透明化を、特定の細胞タイプの定量化が最終目標である場合は、解離とそれに続くフローサイトメトリーを使用することができます。この方法は、中枢神経系腫瘍などの他の細胞タイプに容易に拡張でき、微小環境に関連する状況での研究が可能になる可能性があると期待しています。同様に、レシピエントとして使用されるオルガノイドは、疾患モデルオルガノイドと交換される可能性があり25、26、27、これらの疾患の移植アプローチのモデル化が可能になる可能性がある。
すべてのモデルと同様に、ここで紹介するモデルにも独自の制限があります。一つには、iPS細胞由来のオルガノイドは発生的に未熟であり19、したがって、多くの神経変性疾患が現れる老化した脳と比較して重要な違いがあります。また、大脳オルガノイドは発生において不均一であり19、したがって、まったく同じ生理学的ニッチへの一貫した注入を妨げている。さらに、それらは関連する脳領域の細胞型を含んでいるが18,19、それらは内皮、ミクログリア、および免疫成分を欠いており、これらはin vivoの設定でも重要である14。これにより、宿主が細胞移植にどのように反応するかの研究が制限されます。現在、血管28細胞とミクログリア29細胞を追加し、オルガノイドの一貫性と局所化18を増加させ、オルガノイド移植システムのモデリング能力を向上させる技術がオンライン化されています。ただし、ここで紹介する以上のテストと最適化が必要になります。このプロトコルは安価で特殊な機器を必要としませんが、注入深さなど、多くの重要な技術的考慮事項が残っています。これは、オルガノイドが灌流されていないため、オルガノイドが大きくなりすぎると壊死中心を持つことが多く19、生細胞追跡のために光がオルガノイドコアを透過できないという事実によるものです。そのため、深く注入しすぎた細胞や、内部で遊走したコロニーを見逃す可能性があります。これは、組織浸透度30のより優れた長波長蛍光色素を使用することで改善できるが、オルガノイドのサイズおよび検出装置によっては、これは引き続き検討事項となる可能性が高い。最後に、脳オルガノイドは発生段階にあるため、注入するオルガノイドの発生段階によって環境が異なる可能性があるため、移植のタイミングも重要な考慮事項です。これは、注射時のオルガノイド年齢を一定にすることである程度制御できますが、考慮が必要な要因であることは間違いありません。
このプロトコルは安価で、シンプルで、動物を使わず、特殊な機器を必要としないため、移植モデリングをさまざまなラボで利用することができます。神経細胞治療とオルガノイドモデルシステムの両方における急速な進歩により、ここで紹介するオルガノイド移植プロトコルは、さまざまな疾患や治療アプローチの有用なモデルとなることが期待されます。
開示事項
著者は何も開示していません。
謝辞
資料
| Name | Company | Catalog Number | Comments |
| Accutase | StemCell Technologies | 7920 | proteolytic-collagenolytic enzyme mix |
| Alexa Fluor 488 anti-GFP Antibody | BioLegend | 338008 | |
| Alexa Fluor 488 anti-MAP2 (clone SMI 52) | BioLegend | 801804 | |
| Alexa Fluor 594 anti-GFAP Antibody (clone SMI 25) | BioLegend | 837510 | |
| Alexa Fluor 594 anti-Nestin (clone 10C2) | BioLegend | 656804 | |
| Alexa Fluor 647 anti-Tubulin β 3 (TUBB3) (clone TUJ1) | BioLegend | 801209 | |
| Citric Acid Monohydrate | Fisher Chemical | A104-500 | |
| Cytation 5 Cell Imaging Multimode Reader | Biotek | - | |
| Denaturated Ethyl Alcohol (Anhydrous) | ChapTec | - | |
| DMEM F12/Glutamax | Thermo | 10565018 | |
| Dymethil Sulfoxide (DMSO), Sterile | BioShop | DMS666.100 | |
| FIJI 1.53c | - | - | |
| Formalin solution, neutral buffered, 10% | Sigma | HT501128-4L | |
| Gen5 | - | - | |
| HistoCore Arcadia H | Leica Biosystems | - | |
| Matrigel Growth Factor Reduced (GFR) | Corning | 356231 | Phenol Red-free, LDEV-free |
| MX35 microtome blade | Epredia | 3053835 | |
| NaOH | Sigma | 655104 | |
| PBS (-Ca -Mg) | Sigma | D8537 | |
| Puromycin Dihydrochloride | Thermo | A1113803 | |
| ROCK inhibitor Y-27632 | Abcam | ab120129 | |
| Simport Scientific Stainless-Steel Base Molds | Fisher Scientific | 22-038-209 | |
| Simport Scientific UNISETTE Biopsy Processing/Embedding Cassette | Fisher Scientific | 36-101-9255 | |
| STEMdiff Forebrain Neuron Differentiation Kit | StemCell Technologies | 8600 | |
| STEMdiff Neural Progenitor Medium | StemCell Technologies | 5833 | |
| STEMdiff SMADi Neural Induction Kit | StemCell Technologies | 8581 | |
| Thermo Scientific Shandon Finesse ME Microtome | Thermo Scientific | - | |
| Tissue Prep | Fisher Scientific | T555 | |
| Tissue-Tek VIP 6 AI Tissue Processor | Sakura Finetek | - | |
| Toluene (histological) | ChapTec | - | |
| Trypan blue; 0.4% (wt/vol) | Thermo | 15250061 | |
| Tween 20 | BioShop | TWN510.100 |
参考文献
- Spurlock, M. S., et al. Amelioration of penetrating ballistic-like brain injury induced cognitive deficits after neuronal differentiation of transplanted human neural stem cells. Journal of Neurotrauma. 34 (11), 1981 (2017).
- Zhou, Y., Shao, A., Xu, W., Wu, H., Deng, Y. Advance of stem cell treatment for traumatic brain injury. Frontiers in Cellular Neuroscience. 13, 301 (2019).
- Hayashi, Y., Lin, H. -. T., Lee, C. -. C., Tsai, K. -. J. Effects of neural stem cell transplantation in Alzheimer's disease models. Journal of Biomedical Science. 27 (1), 29 (2020).
- Kefalopoulou, Z., et al. Long-term clinical outcome of fetal cell transplantation for Parkinson disease: Two case reports. JAMA Neurology. 71 (1), 83-87 (2014).
- Li, W., et al. Extensive graft-derived dopaminergic innervation is maintained 24 years after transplantation in the degenerating parkinsonian brain. Proceedings of the National Academy of Sciences of the United States of America. 113 (23), 6544-6549 (2016).
- Parmar, M., Grealish, S., Henchcliffe, C. The future of stem cell therapies for Parkinson disease. Nature Reviews Neuroscience. 21 (2), 103-115 (2020).
- Takahashi, J. iPS cell-based therapy for Parkinson's disease: A Kyoto trial. Regenerative Therapy. 13, 18-22 (2020).
- Krause, M., Phan, T. G., Ma, H., Sobey, C. G., Lim, R. Cell-based therapies for stroke: Are we there yet. Frontiers in Neurology. 10, 656 (2019).
- Coles-Takabe, B. L. K., et al. Don't look: Growing clonal versus nonclonal neural stem cell colonies. Stem Cells. 26 (11), 2938-2944 (2008).
- Duval, K., et al. Modeling physiological events in 2D vs. 3D cell culture. Physiology. 32 (4), 266-277 (2017).
- Jakel, R. J., Schneider, B. L., Svendsen, C. N. Using human neural stem cells to model neurological disease. Nature Reviews Genetics. 5 (2), 136-144 (2004).
- Hodge, R. D., et al. Conserved cell types with divergent features in human versus mouse cortex. Nature. 573 (7772), 61-68 (2019).
- Li, J., et al. Conservation and divergence of vulnerability and responses to stressors between human and mouse astrocytes. Nature Communications. 12 (1), 3958 (2021).
- Morizane, A., et al. MHC matching improves engraftment of iPSC-derived neurons in non-human primates. Nature Communications. 8 (1), 385 (2017).
- Khrameeva, E., et al. Single-cell-resolution transcriptome map of human, chimpanzee, bonobo, and macaque brains. Genome Research. 30 (5), 776-789 (2020).
- Powell, K. Hybrid brains: The ethics of transplanting human neurons into animals. Nature. 608 (7921), 22-25 (2022).
- Humpel, C. Organotypic brain slice cultures: A review. Neuroscience. 305, 86-98 (2015).
- Birey, F., et al. Assembly of functionally integrated human forebrain spheroids. Nature. 545 (7652), 54-59 (2017).
- Lancaster, M. A., et al. Cerebral organoids model human brain development and microcephaly. Nature. 501 (7467), 373-379 (2013).
- García-Delgado, A. B., et al. Brain organoids to evaluate cellular therapies. Animals. 12 (22), (2022).
- Lin, J. -. R., Fallahi-Sichani, M., Sorger, P. K. Highly multiplexed imaging of single cells using a high-throughput cyclic immunofluorescence method. Nature Communications. 6 (1), 8390 (2015).
- Knapp, D. J. H. F., et al. Single-cell analysis identifies a CD33+ subset of human cord blood cells with high regenerative potential. Nature Cell Biology. 20 (6), 710-720 (2018).
- Georgala, P. A., Carr, C. B., Price, D. J. The role of Pax6 in forebrain development. Developmental Neurobiology. 71 (8), 690-709 (2011).
- Britanova, O., et al. Satb2 is a postmitotic determinant for upper-layer neuron specification in the neocortex. Neuron. 57 (3), 378-392 (2008).
- Kim, H., et al. Modeling G2019S-LRRK2 sporadic Parkinson's disease in 3D midbrain organoids. Stem Cell Reports. 12 (3), 518-531 (2019).
- Smits, L. M., et al. Modeling Parkinson's disease in midbrain-like organoids. NPJ Parkinson's Disease. 5, 5 (2019).
- Jin, M., et al. Type-I-interferon signaling drives microglial dysfunction and senescence in human iPSC models of Down syndrome and Alzheimer's disease. Cell Stem Cell. 29 (7), 1135.e8-1153.e8 (2022).
- Sun, X. -. Y., et al. Generation of vascularized brain organoids to study neurovascular interactions. eLife. 11, e76707 (2022).
- Popova, G., et al. Human microglia states are conserved across experimental models and regulate neural stem cell responses in chimeric organoids. Cell Stem Cell. 28 (12), 2153.e6-2166.e6 (2021).
- Wang, S., Li, B., Zhang, F. Molecular fluorophores for deep-tissue bioimaging. ACS Central Science. 6 (8), 1302-1316 (2020).
転載および許可
このJoVE論文のテキスト又は図を再利用するための許可を申請します
許可を申請さらに記事を探す
This article has been published
Video Coming Soon
Copyright © 2023 MyJoVE Corporation. All rights reserved