このコンテンツを視聴するには、JoVE 購読が必要です。 サインイン又は無料トライアルを申し込む。
Method Article
横隔膜運動ニューロンの変性と補償の定量的バイオマーカーとしてのラット横隔膜運動ユニット接続性結果測定の評価
* これらの著者は同等に貢献しました
要約
この研究では、ラットのダイヤフラム運動ユニットの接続性を定量化するために、運動ユニットの数とサイズを推定するための in vivo 法を紹介します。これらの手法に対する段階的なアプローチについて説明します。
要約
人工呼吸器筋機能の喪失は、運動ニューロンの損傷と神経変性の結果です(例:.、頸髄損傷と筋萎縮性側索硬化症)。横隔膜運動ニューロンは、中枢神経系と筋肉との間の最終的なリンクであり、それぞれの運動単位(単一の運動ニューロンによって神経支配される筋線維のグループ)は、神経筋換気システムの最小の機能単位を表しています。複合筋活動電位 (CMAP)、単一運動単位電位 (SMUP)、および運動単位数推定 (MUNE) は、動物モデルの運動単位の完全性を経時的に評価できるようにする確立された電気生理学的アプローチですが、主に四肢の筋肉に適用されています。したがって、この研究の目的は、横隔膜 MUNE、運動単位サイズ (SMUP として表される)、および CMAP を定量化するために縦断的に使用できる前臨床げっ歯類研究のアプローチを説明し、運動ニューロン損失モデルでこれらのアプローチの有用性を実証することです。運動ニューロンの損傷や疾患におけるニューロンの損傷、変性、再生に関する高感度で客観的、かつ翻訳的に関連性のあるバイオマーカーは、実験的研究の発見から臨床試験までを大幅に支援し、加速させることができます。
概要
C3からC6筋節レベルまで伸びる横隔膜運動ニューロン(MN)は、中枢神経系(CNS)から横隔膜筋1への最終的なリンクを形成します。横隔膜運動単位 (MU) は、単一の脊髄 MN とその神経支配された横隔膜筋線維で構成され、呼吸器系の最小の機能単位を形成します。換気機能には、横隔膜MUプールの協調的な活性化によって達成される横隔膜筋の適切な収縮が必要です2,3。筋萎縮性側索硬化症(ALS)を含む多くの神経疾患は、重度の換気障害を引き起こし、最終的には死因の一因となります4。
いくつかの電気生理学的アプローチを使用して、in vivoでの運動ユニット(MU)プールの完全性を評価および監視できます。複合筋活動電位(CMAP)は、末梢神経刺激後の特定の筋肉または筋肉群のすべての筋線維の合計脱分極を反映しており、ALS 5,6および脊髄性筋萎縮症(SMA)7,8,9を含むさまざまな神経筋状態に敏感です。CMAP評価の限界は、付随的なスプラウティングが、MU損失10の存在下でもCMAPの振幅と面積の維持につながる可能性があることである。この制限を克服するために、運動ユニット番号とサイズ11 の両方を評価するために CMAP 手法に変更が加えられました。さらに、電気生理学的システムによるダイヤフラムCMAPの機能評価を調査したin vivo研究は、記載されたダイアフラムCMAP記録技術を運動単位数推定12に利用することも可能である可能性があることを示唆した。
漸進運動単位数推定(MUNE)技術は、1970年代初頭にMcComasらによって、ヒトの指伸筋に対して最初に導入されました13。インクリメンタルMUNEアプローチは、従来のCMAP記録技術の修正であり、その間に徐々に増加する刺激が送達され、単一の運動単位応答の指標として定量的な、オールオアゼロのサブマックスインクリメントが記録されました。合計された増分と平均化された増分は、単一モーター単位電位 (SMUP) のサイズの推定値を計算するために使用されました。次に、この計算されたサイズをCMAP振幅に分割して、検査対象の筋肉を神経支配するMUの数を推定しました11。MUNEは、運動単位損失の検出と監視において高い感度を示し、CMAP振幅や面積14,15などの測定値で観察可能な変化の前に運動単位機能障害を特定することができます。ALS患者では、MUNEは非常に感度が高いことが証明されており、疾患の発症、進行、および予後の著名なバイオマーカーとして機能しています16,17。
MUNEの多数の適応が開発され、神経変性、神経損傷、および自然な老化プロセス18,19,20,21などの条件でMU機能を評価するために広く使用されています。最初の説明以来、電気生理学的応答とインクリメンタルフォース(機械的)測定の両方を利用したさまざまな適応が、人間の研究と動物モデルの両方で採用されてきました22。MUNEは、運動ニューロンと筋肉との接続性を非侵襲的に機能評価します。MUNEを縦断的に適用することで、疾患や誘発された表現型の進行を理解し、臨床および前臨床の場での治療介入の保護効果または再生効果を評価することができます。MUNE測定の再現性の有効性と、人体の大部分にわたるMUプールの技術の臨床的関連性に関係なく、努力は主にげっ歯類の筋肉の四肢筋に焦点を当ててきました10,23,24,25。
したがって、この研究の目的は、化合物筋活動電位 (CMAP)、SMUP、および横隔膜運動単位数 (MUNE) を in vivo 評価として取得するためのアプローチを説明することでした。これは、前臨床げっ歯類研究で縦断的に使用して、MUNE、運動単位サイズ (SMUP として表される)、および CMAP を定量化できます。さらに、横隔膜 MN 変性剤であるサポリンに結合したコレラ毒素 B フラグメント (CTB-SAP) の胸腔内投与後の横隔膜 MU 数の喪失を強調する代表的なデータを示します。
プロトコル
すべての手順は、ミズーリ大学の動物管理および使用委員会によって確立されたガイドラインに従って承認および実施されました。実験は、11〜15週齢の成体の雄Sprague-Dawleyラットで行われました。これらのラットはペアで飼育され、12:12の明暗サイクル下に置かれ、標準的な市販のペレット食品とHCl処理水が常に利用可能でした。
1.動物の準備と麻酔の分娩
- ネズミを取り扱うときは、適切な個人用保護具を着用してください。
- 吸入麻酔薬に3〜5%イソフルランを投与し、適切な導入を確保します。ラットが適切に麻酔されたら、仰臥位に置き、1〜3%の吸入イソフルランで麻酔を維持します。.鉗子を使用して後肢の足パッドに優しく圧力をかけ、離脱反応がないことを確認して、麻酔の深さの十分性を確認します。
注:ラットのサイズと体重に基づいて、麻酔の深さを監視し、それに応じてイソフルラン濃度を調整します。 - サーモスタット加温プレートを使用して温度を37°Cに維持し、CMAPの振幅と遅延に影響を与える可能性のある温度の変動を防ぎます。
- 乾燥を防ぐために、獣医用石油ベースの軟膏を目に塗ります。呼吸数を観察し、鉗子でフットパッドに圧力をかけたときの離脱反応を確認することにより、麻酔の深さを監視します。
- バリカンを使用して研究する胸と首の下3分の1から毛を取り除きます。実験全体を通してラットの呼吸を監視します。
注:CMAPとMUNEの記録と麻酔の中止に続いて、ラットが十分な意識を取り戻すまで放置しないでください。.完全に回復するまで、動物をホームケージに戻さないでください。
2. 電極の配置とセットアップ
- 図1に示すように、28Gモノポーラ針電極のペアを配置して、CMAP、SMUP、およびMUNEを記録します。
- アクティブ (E1) 針電極を鎖骨中央線上 (最後の肋骨境界より下) に皮下に配置し、参照 (E2) 針電極をキシフス プロセスと最後の胸骨軟骨との間の角度に皮下に配置します。
注:針電極は横隔膜の筋肉に挿入しないでください。代わりに、それらは皮下領域に配置する必要があります。
- アクティブ (E1) 針電極を鎖骨中央線上 (最後の肋骨境界より下) に皮下に配置し、参照 (E2) 針電極をキシフス プロセスと最後の胸骨軟骨との間の角度に皮下に配置します。
- 頸動脈シートでの横隔神経の刺激には、神経刺激の陰極および陽極として一対の 28 G 単極針電極を使用し、前斜筋と中斜筋の間の外側頸部に皮下に配置され、約 1 cm 離れて配置されます。刺激針の配置が4番目の頸椎(C4)の下のレベルにあることを確認してください。
注意: 横隔神経やその他の構造の損傷を避けるために、刺激電極を深く挿入しすぎないでください。 図1 は電極の配置を示しています。 - 接地電極は、テールに使い捨ての表面電極を配置します。
3. データ取得
- フレニックCMAP
- 横隔神経を刺激するために、持続時間が0.1ミリ秒、強度が60〜100mAの範囲の単相陰極方形波パルスを適用することにより、横隔膜CMAP応答を記録します。
- 刺激強度を徐々に増加させながら、応答の振幅がそれ以上の増加を示さなくなるまで、CMAP応答を取得します。超最大刺激を確保するには、刺激強度を最大限引き出すために使用したレベルの約120%まで上げ、追加の応答を記録します。CMAP サイズが増えなくなった場合は、この応答を最大 CMAP と見なします。
注:呼気中に刺激を与えることは、CMAP記録中の同時筋活動ノイズを最小限に抑えるために望ましいです。 - CMAPのピークツーピーク振幅をミリボルト(mV)単位で測定し、文書化します(図2)。
注:CMAP振幅は、塩基間およびピーク間およびピークtoピークで評価できます。臨床電気診断システムは、多くの場合、等電基基から最初の負のピークまで計算される塩基間評価がデフォルトになります。
- 平均シングルモーターユニット電位(SMUP)サイズとMUNE計算
- インクリメンタル刺激技術を使用して平均SMUPサイズを計算します。
- 漸進的な応答を引き出すには、1 Hzの周波数で0.1 msの持続時間で最大以下の刺激を投与し、最小限のオールオアナッシング応答が達成されるまで0.03 mA刻みで強度を徐々に増加させます。2mA〜10mAの範囲の刺激強度で初期応答を取得します。
- 刺激強度が2mAから10mAの間で初期応答が起こらない場合は、刺激カソードの位置を変更し、首の横隔神経から近づけるか遠ざけるかして、必要な刺激強度をそれぞれ減らしたり増やしたりします。
- 最初の増分応答が 2 mA から 10 mA の範囲の刺激強度で達成された場合は、最初の応答を保存し、0.03 mA の増分で調整して、段階的に高い刺激強度で追加の増分を取得し、ステップ 3.2.2 の次の基準を満たす合計 9 つの追加増分を達成します。
注: 各 SMUP は、前の増分から各増分を差し引くことによって定量化されます。
- 増分応答を測定する際には、各増分が次の基準を満たしていることを確認してください。
- 増分応答の最初の負のピークが、最大CMAP応答の負のピークと時間的に整列していることを確認します。
注:呼吸周期からのバックグラウンドノイズによって観察されるわずかな動きは、実験の性質に固有のものです。しかし、ライブ観測中にSMUPが一貫して存在することで、その特定のCMAPに対するSMUPのアイデンティティが確認されます。 - 横隔膜は呼吸に関与する動的な筋肉であるため、各呼吸サイクルがベースライン運動を誘発する可能性があります。したがって、3つの重複する応答間で一貫性を確認することにより、各増分応答の安定性と分画の欠如を確認します。
注:低振幅の誘発電位、特に最初のSMUPを呼吸活動によるバックグラウンドノイズと区別するには、警戒を怠らず、3〜4回の呼吸サイクルを観察することが重要です。また、精度のために、ピークがCMAPのピークと整列していることを確認してください。 - 各増分が明確で、前の増分よりも大きいことを確認します。したがって、増分応答をリアルタイムで視覚的に区別し、以前に記録された増分に重なる応答を観察します。
注:各振幅での刺激の複数回の反復は、増分の一貫性と事前定義された基準への準拠を確保するために実施される場合があります。 - 前述の基準で各インクリメントを目視で確認した後、インクリメント振幅が少なくとも25μVであることを確認してください。増分が25 μV未満の場合は、測定値を破棄し、応答を再評価します。
- 10 個のインクリメンタル応答を記録した後、各インクリメント応答の振幅が 10 個すべてのインクリメントの合計振幅の 3 分の 1 を超えないことを確認します。これは、最終応答の合計振幅を表します。この基準が満たされない場合は、10の増分応答の測定を繰り返します。
注:3分の1のしきい値は、各増分応答が単一のモーターユニットの活性化を表すという仮定に基づいています。任意の増分応答の振幅が、10個の増分すべての合計振幅の3分の1を超える場合、その応答が単一の運動ユニットの活性化のみに起因するものではない可能性があることを示唆しています。それどころか、それは、追加の運動ユニットの動員や、電気ノイズや人工物22,26のような非特異的な活動の存在によって影響を受ける可能性がある。 - SMUP の平均振幅を推定するには、10 個の増分の値を平均化します。平均SMUP振幅を測定する別の方法は、最終インクリメンタル応答の全振幅をインクリメント11の総数で割ることである。
- 増分応答の最初の負のピークが、最大CMAP応答の負のピークと時間的に整列していることを確認します。
- 最大 CMAP 振幅 (ピークツーピーク) を平均 SMUP 振幅 (ピークツーピーク) で割って MUNE を求めます。特定の電気生理学的システムでは、SMUPはマイクロボルト(μV)で記録されますが、CMAPは通常ミリボルト(mV)で表されます。必要に応じて、MONE を計算する前に、CMAP と SMUP の測定値を同じ単位に変換します。
注:ピークツーピークCMAP、平均SMUP、およびMUNEは、通常、クリニックの筋電図システムによって自動的に計算されます。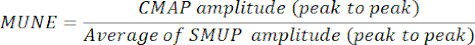
CMAP = 複合筋活動電位
SMUP = 単一モーターユニット電位
MUNE = Motor Unit Number Estimation
- インクリメンタル刺激技術を使用して平均SMUPサイズを計算します。
結果
このレポートで概説されているCMAP、SMUP、およびMUNE技術は、低侵襲電極配置を使用して横隔膜筋の神経筋機能の記録を可能にします(図1)。振幅と面積のパラメータを使用して、最大CMAPサイズを特徴付け、筋肉群の出力の全体的な尺度を提供できます(図2)。しかし、現在の方法では、CMAPとSMUPの両方のサイズを定量化するた...
ディスカッション
ALSなどのMN変性疾患では、換気に関与するMUを評価することが重要である28。ALS患者における呼吸器性MN変性の発生にもかかわらず、MN死の特異的な発症と進行は未だに完全には理解されていない29,30,31。この側面の重要性を認識して、遺伝的ベース(SOD1 2,32
開示事項
WDAは、NMD Pharma、Avidity Biosciencesから研究資金を受けており、NMD Pharma、Avidity Biosciences、Dyne Therapeutics、Novartis、Design Therapeutics、Catalyst Pharmaceuticals、Novartisからコンサルティング料を受けています。
謝辞
この研究は、ミズーリ州脊髄損傷/疾患研究プログラム(NLNおよびWDA)からの脊髄損傷/疾患研究プログラム助成金によって資金提供されました。
資料
| Name | Company | Catalog Number | Comments |
| 2 mL Glass Syringe | Kent Scientific Corporation | SOMNO-2ML | |
| 50 mL, Model 705 RN syringe | Hamilton Company | 7637-01 | Utilized to conduct intrapleural injection |
| 5008 - Formulab Diet | LabDiet | 0001325 | |
| Autoclavable 26 G needles (26S RN 9.52 mm 40°) | Hamilton Company | 7804-04 | Utilized to conduct intrapleural injection |
| Cholera toxin B-subunit (CTB) | MilliporeSigma | C9903 | Utilized for intrapleural injection to label surviving motor neurons |
| Cholera toxin B-subunit conjugated to saporin (CTB-SAP) | Advanced Targeting Systems | IT-14 | Utilized for intrapleural injection to cause motor neuron death |
| Detachable Cable | Technomed | 202845-0000 | to connect the recorder electrode to the electrodiagnostic machine |
| Disposable 2" x 2" disc electrode with leads | Cadwell | 302290-000 | ground electrode |
| disposable monopolar needles 28 G | Technomed | 202270-000 | cathode and anode stimulating electrodes- recording electrodes |
| EMG needle cable (Amp/stim switch box) | Cadwell | 190266-200 | to connect monopolar electrodes to electrodiagnostic stimulator |
| Helping Hands alligator clip with iron base | Radio Shack | 64-079 | Maintaining recording electrode placement |
| Isoflurane (250 mL bottle) | Piramal Healthcare | ||
| monoject curved tip irrigating syringe | Covidien | 81412012 | utilized for application of electrode gel |
| PhysioSuite Physiological Monitoring System with RightTemp Homeothermic Warming | Kent Scientific Corporation | PS-RT | Includes infrared warming pad, rectal probe, and pad temperature probe |
| Pro trimmer Pet Grooming Kit | Oster | 078577-010-003 | clippers for hair removal |
| Saporin (SAP) | Advanced Targeting Systems | PR-01 | Utilized for intrapleural injection (control agent when injected by itself) |
| Sierra Summit EMG system | Cadwell Industries, Inc., Kennewick, WA | portable electrodiagnostic system | |
| SomnoSuite Low-Flow Digital Anesthesia System | Kent Scientific Corporation | SOMNO | Includes anti-spill, anti-vapor bottle top adapter; Y adapter tubing; charcoal scavenging filter |
| Sprague-Dawley rat | Envigo colony 208a, Indianapolis, IN | ||
| Veterinarian petroleum-based ophthalmic ointment | Puralube | 26870 | applied during anesthesia to avoid corneal injury |
参考文献
- Mantilla, C. B., Zhan, W. -. Z., Sieck, G. C. Retrograde labeling of phrenic motoneurons by intrapleural injection. J Neurosci Methods. 182 (2), 244-249 (2009).
- Nichols, N. L., Satriotomo, I., Harrigan, D. J., Mitchell, G. S. Acute intermittent hypoxia induced phrenic long-term facilitation despite increased sod1 expression in a rat model of als. Exp Neurol. 273, 138-150 (2015).
- Nichols, N. L., Craig, T. A., Tanner, M. A. Phrenic long-term facilitation following intrapleural ctb-sap-induced respiratory motor neuron death. Respir Physiol Neurobiol. 256, 43-49 (2018).
- Kiernan, M. C., et al. Amyotrophic lateral sclerosis. Lancet. 377 (9769), 942-955 (2011).
- Boërio, D., Kalmar, B., Greensmith, L., Bostock, H. Excitability properties of mouse motor axons in the mutant sod1g93a model of amyotrophic lateral sclerosis. Muscle Nerve. 41 (6), 774-784 (2010).
- Shibuya, K., et al. Motor cortical function determines prognosis in sporadic als. Neurology. 87 (5), 513-520 (2016).
- Lewelt, A., et al. Compound muscle action potential and motor function in children with spinal muscular atrophy. Muscle Nerve. 42 (5), 703-708 (2010).
- Mcgovern, V. L., et al. Smn expression is required in motor neurons to rescue electrophysiological deficits in the smnδ7 mouse model of sma. Hum Mol Genet. 24 (19), 5524-5541 (2015).
- Arnold, W. D., et al. Electrophysiological biomarkers in spinal muscular atrophy: Preclinical proof of concept. Ann Clin Transl Neurol. 1 (1), 34-44 (2014).
- Harrigan, M. E., et al. Assessing rat forelimb and hindlimb motor unit connectivity as objective and robust biomarkers of spinal motor neuron function. Sci Rep. 9 (1), 16699 (2019).
- Arnold, W. D., et al. Electrophysiological motor unit number estimation (mune) measuring compound muscle action potential (cmap) in mouse hindlimb muscles. J. Vis. Exp: JoVE. (103), e52899 (2015).
- Martin, M., Li, K., Wright, M. C., Lepore, A. C. Functional and morphological assessment of diaphragm innervation by phrenic motor neurons. J. Vis. Exp: JoVE. (99), e52605 (2015).
- Mccomas, A., Fawcett, P. R. W., Campbell, M., Sica, R. Electrophysiological estimation of the number of motor units within a human muscle. J Neurol Neurosurg Psychiatry. 34 (2), 121-131 (1971).
- Felice, K. J. A longitudinal study comparing thenar motor unit number estimates to other quantitative tests in patients with amyotrophic lateral sclerosis. Muscle Nerve. 20 (2), 179-185 (1997).
- Vucic, S., Rutkove, S. B. Neurophysiological biomarkers in amyotrophic lateral sclerosis. Curr Opin Neurol. 31 (5), 640-647 (2018).
- Carleton, S., Brown, W. Changes in motor unit populations in motor neurone disease. J Neurol Neurosurg Psychiatry. 42 (1), 42-51 (1979).
- Yuen, E. C., Olney, R. K. Longitudinal study of fiber density and motor unit number estimate in patients with amyotrophic lateral sclerosis. Neurology. 49 (2), 573-578 (1997).
- Gooch, C. L., et al. Motor unit number estimation: A technology and literature review. Muscle Nerve. 50 (6), 884-893 (2014).
- Henderson, R. D., Ridall, P. G., Hutchinson, N. M., Pettitt, A. N., Mccombe, P. A. Bayesian statistical mune method. Muscle Nerve. 36 (2), 206-213 (2007).
- Shefner, J., et al. Multipoint incremental motor unit number estimation as an outcome measure in als. Neurology. 77 (3), 235-241 (2011).
- Stein, R. B., Yang, J. F. Methods for estimating the number of motor units in human muscles. Ann Neurol. 28 (4), 487-495 (1990).
- Shefner, J. M. Motor unit number estimation in human neurological diseases and animal models. Clin Neurophysiol. 112 (6), 955-964 (2001).
- Ahad, M., Rutkove, S. Correlation between muscle electrical impedance data and standard neurophysiologic parameters after experimental neurogenic injury. Physiol Meas. 31 (11), 1437 (2010).
- Kasselman, L. J., Shefner, J. M., Rutkove, S. B. Motor unit number estimation in the rat tail using a modified multipoint stimulation technique. Muscle Nerve. 40 (1), 115-121 (2009).
- Ngo, S., et al. The relationship between bayesian motor unit number estimation and histological measurements of motor neurons in wild-type and sod1g93a mice. Clin Neurophysiol. 123 (10), 2080-2091 (2012).
- Feasby, T., Brown, W. Variation of motor unit size in the human extensor digitorum brevis and thenar muscles. J Neurol Neurosurg Psychiatry. 37 (8), 916-926 (1974).
- Nichols, N. L., Vinit, S., Bauernschmidt, L., Mitchell, G. S. Respiratory function after selective respiratory motor neuron death from intrapleural ctb-saporin injections. Exp Neurol. 267, 18-29 (2015).
- Nichols, N. L., et al. Ventilatory control in als. Respir Physiol Neurobiol. 189 (2), 429-437 (2013).
- Cifra, A., Nani, F., Nistri, A. Respiratory motoneurons and pathological conditions: Lessons from hypoglossal motoneurons challenged by excitotoxic or oxidative stress. Respir Physiol Neurobiol. 179 (1), 89-96 (2011).
- Kobayashi, Z., et al. Fals with gly72ser mutation in sod1 gene: Report of a family including the first autopsy case. J Neurol Sci. 300 (1), 9-13 (2011).
- Su, M., Wakabayashi, K., Tanno, Y., Inuzuka, T., Takahashi, H. An autopsy case of amyotrophic lateral sclerosis with concomitant alzheimer's and incidental lewy body diseases. No to shinkei= Brain and nerve. 48 (10), 931-936 (1996).
- Lladó, J., et al. Degeneration of respiratory motor neurons in the sod1 g93a transgenic rat model of als. Neurobiol Dis. 21 (1), 110-118 (2006).
- Borkowski, L. F., Smith, C. L., Keilholz, A. N., Nichols, N. L. Divergent receptor utilization is necessary for phrenic long-term facilitation over the course of motor neuron loss following ctb-sap intrapleural injections. J Neurophysiol. 126 (3), 709-722 (2021).
- Nicolopoulos-Stournaras, S., Iles, J. F. Motor neuron columns in the lumbar spinal cord of the rat. J Comp Neurol. 217 (1), 75-85 (1983).
- Tosolini, A. P., Morris, R. Targeting motor end plates for delivery of adenoviruses: An approach to maximize uptake and transduction of spinal cord motor neurons. Sci Rep. 6 (1), 33058 (2016).
- Mchanwell, S., Biscoe, T. The localization of motoneurons supplying the hindlimb muscles of the mouse. Phil. Trans. R. , 477-508 (1981).
- Nair, J., et al. Histological identification of phrenic afferent projections to the spinal cord. Respir Physiol Neurobiol. 236, 57-68 (2017).
- Courtine, G., et al. Can experiments in nonhuman primates expedite the translation of treatments for spinal cord injury in humans. Nat Med. 13 (5), 561-566 (2007).
- Friedli, L., et al. Pronounced species divergence in corticospinal tract reorganization and functional recovery after lateralized spinal cord injury favors primates. Sci Transl Med. 7 (302), 134 (2015).
- Arnold, R., et al. Nerve excitability in the rat forelimb: A technique to improve translational utility. J Neurosci Methods. 275, 19-24 (2017).
- Boriek, A., Rodarte, J., Reid, M. Shape and tension distribution of the passive rat diaphragm. Am J Physiol Regul Integr Comp Physiol. 280, R33-R41 (2001).
転載および許可
このJoVE論文のテキスト又は図を再利用するための許可を申請します
許可を申請This article has been published
Video Coming Soon
Copyright © 2023 MyJoVE Corporation. All rights reserved