Method Article
형광 현미경을 사용 키네신 -1-화물 식별
요약
여기에서, 프로토콜은 키네신 -1-화물을 식별하기 위해 제시된다. 키네신-1 중쇄 (KIF5B)의 모터리스 돌연변이는 세포질에 집계 및화물의 응집을 유도한다. 모두 집계는 형광 현미경에서 검출된다. 유사한 전략이 다른 모터 단백질화물을 식별하기 위해 사용될 수있다.
초록
Fluorescence microscopy is employed to identify Kinesin-1 cargos. Recently, the heavy chain of Kinesin-1 (KIF5B) was shown to transport the nuclear transcription factor c-MYC for proteosomal degradation in the cytoplasm. The method described here involves the study of a motorless KIF5B mutant for fluorescence microscopy. The wild-type and motorless KIF5B proteins are tagged with the fluorescent protein tdTomato. The wild-type tdTomato-KIF5B appears homogenously in the cytoplasm, while the motorless tdTomato-KIF5B mutant forms aggregates in the cytoplasm. Aggregation of the motorless KIF5B mutant induces aggregation of its cargo c-MYC in the cytoplasm. Hence, this method provides a visual means to identify the cargos of Kinesin-1. A similar strategy can be utilized to identify cargos of other motor proteins.
서문
키네신-1은 선행 성 1,2화물 수송을 매개 모터 단백질이다. 그것은 키네신 빛 체인 1 (KLC1) 및 키네신 무거운 체인의 두 서브 유닛 (KHCs)의 두 개의 서브 유닛의 heterotetramer이다. KIF5B 1, KHC는 자사의 N 말단, ATP를 가수 분해 및 미세 소관을 따라 이동을 위해 기계적 에너지를 화학 에너지로 변환에서 모터 도메인이 포함되어 있습니다. 그것의 C- 말단 지역은화물과 연관 KLC1와 상호 작용 이합체 도메인이 포함되어 있습니다. 키네신-1은 소포, 세포 기관과의 mRNA 3,4 등의화물을 수송한다. 최근 KIF5B는 세포질 5 proteosomal 저하에 대한 핵 전사 인자 C-MYC 수송을 보였다. 세 가지 방법 (화학적 억제제의 siRNA / shRNA를 지배적 네거티브 체)은 키네신 - 1 기능을 억제하기 위해 사용 하였다. 그들 모두는 세포질에서 C-MYC의 응집을 유도. 마지막 방법의 경우, C-MYC은 지배적 인 negat에 의해 영향을 받았다돌연변이는 일반적으로 (미세 소관 중단 등) 세포 내 구성 요소에 대한 영향이나 단백질 응집에를주지 않는 것을 건의, 다른 관련 KIF5A 모터 단백질의에 의해 KIF5B의 돌연변이를 필자는 아니지만. KIF5B 지배적 네거티브 체는 또한 전사 인자에 대한 일반적인 영향을주지 않는다는 것을 시사 다른 전사 인자에 영향을 미치지 않았다. 오히려 우성 네거티브 체는화물에 대한 특정 효과를 발휘하는 것을 시사한다.
우성 네거티브 변이체의 사용은 모터 단백질의 분야에서 일반적이다. 키네신과 myosins의 유사 모터리스 돌연변이는 이전에 사용되었다. 이들은 주로 자신의화물의 세포 내 지역화 또는 세포 기능에 6-12 돌연변이의 효과를 입증하기 위해 사용되었다. 덜 강조 돌연변이와 그들에 의해 영향을받는화물 사이의 공간 관계에 넣었다. 그러나, 어떤 빈도로, 돌연변이는 CA와 공동 지역화 관찰rgos 6,10.
KIF5B 및 관련 단백질 간의 상호 작용은 이전에 생체 효모 두 하이브리드 분석법 및 면역 침전과 같은 공동 체외 풀다운 분석 생화학 13-16에서 풀다운 검정에 의해 확인 하였다. 이 기사에서는 추가로 시각적 방법을 사용하여 형광 현미경은 KIF5B화물 단백질을 식별하기 위해 설명되어 있습니다. 방법 우성 네거티브 체로서 작용하는 모터리스 KIF5B 변이체를 사용한다. 그것은 세포질에 집계 및화물의 응집을 유도한다.
17 tdTomato 형광 단백질 야생 형 및 모터리스 KIF5B 돌연변이의 태그는 형광 현미경으로 자신의 시각화를 가능하게한다. 태그 KIF5B 단백질 적절 KIF5B 태그로부터 분리 된 스펙트럼 특성을 갖는 다른 형광 단백질을 융합 단백질 후보와 공동 발현 될 수있다. 태그 단백질 생균 직접 관찰형광 현미경 하에서. 모터리스 KIF5B 돌연변이에 의해 후보 단백질 응집 유도 후보 단백질 KIF5B의 생체화물인지 확인한다. 또한 tdTomato 태깅 KIF5B 단백질은 내인성화물 단백질에 미치는 영향을 연구하는 세포만을 표현할 수있다. 나중에, 면역 형광 현미경이 형광 염료와 접합 적절한 이차 항체이어서 형질 감염된 세포를 고정 후보 내인성 단백질에 대한 특이 항체로 염색 된 행한다. 이 경우, 생리 학적 수준에서 내인성 후보 단백질 연구된다. 다른 모터 단백질 유사 모터리스 돌연변이들은화물을 식별하기 위해 제조 될 수있다.
프로토콜
tdTomato-태그 야생 형 및 모터리스 KIF5B 단백질 1. 복제
- 표 1의 프라이머를 사용하여 인간 야생형 및 모터리스 KIF5B의 단백질의 cDNA를 증폭의 Taq DNA 중합 효소 (100 ㎕를 5 대)의 dNTP 혼합물 (각 옥시 뉴클레오티드 2 mM)을 30 사이클의 10X 버퍼. 각 사이클은 변성 단계 (30 초 동안 95 ° C), 어닐링 단계 (30 초 동안 45 ° C) 및 확장 단계 (3 분 동안 72 ° C)로 구성된다.
- 페놀 / 클로로포름을 동량 증폭 된 DNA 생성물을 추출물 (1 : 1).
주 : 페놀은 가연성이며 화상을 입을 수 있습니다. 클로로포름은 위험합니다. 그들과의 직접적인 접촉을 피하고 화학 흄 후드를 사용합니다. 대안으로, PCR 생성물은 다양한 장비에 의해 정제 할 수있다.- 1 분 동안 실온에서 마이크로 원심 18,000 XG 스핀. 새로운 튜브에 수용액을 옮기고 클로로포름 동일 부피로 추출한다.
- 회전0.5 분 동안 실온에서 마이크로 원심 18,000 XG에. 새로운 튜브를 수용액을 전송합니다.
- 3 M 나트륨 아세테이트의 10 볼륨과 무수 에탄올의 두 볼륨이있는 수용액을 섞는다.
- 5 분 동안 실온에서 마이크로 원심 18,000 XG 스핀. 수용액을 폐기하십시오.
- 75 % 에탄올의 두 볼륨 DNA 펠렛을 씻으십시오. 수용액을 버리고 공기를 실온에서 5 분간 DNA 펠렛을 건조. 34 μl의 물에서 DNA 펠렛을 재현 탁.
- 제한 40 μL의 최종 부피에서 증폭 된 제품을 소화하는 것은 SalI로 (10 대)과의 BamHI (10 대)와 두 시간 동안 37 ° C에서 자신의 10X 버퍼의 4 μl를 효소. 에티 디움 브로마이드 (0.2 μg의 / ㎖)을 함유하는 아가로 오스 겔에서 분해 제품 (100 V에서 1.0 %)을 해결.
주 : 에티 디움 브로마이드 강력한 돌연변이이며 피부를 통해 흡수 될 수있다. 따라서 w 직접 또는 간접 접촉을 방지하는 것이 중요i 번째 에티 디움 브로마이드. - 열에 의해 정화에 대한 올바른 밴드를 잘라. DNA 절편을 함유하는 아가로 오스 겔을 단다. 이어서 약 20 분 동안 37 ℃에서 용해 완충액 (0.1 g, 300 μL)에 용해.
- 5 초 동안 실온에서의 microcentrifuge의 열 스핀에 생성 된 솔루션을 추가합니다. 흐름을 통해 폐기하십시오.
- 단계 1.5를 반복하여 0.5 ㎖의 가용화 버퍼와 컬럼을 씻으십시오. 단계 1.5를 반복하여 0.75 ml의 세척 버퍼 다시 열을 씻으십시오. 2 분 나머지 세척 버퍼를 제거하기위한 열을 스핀.
- 150 단계를 반복하여 50 ㎕의 물과 DNA 단편을 용리시킨다. 에티 디움 브로마이드 (0.2 μg의 / ㎖)을 함유하는 아가로 오스 겔 (100 V에서 1.0 %)의 DNA 사이즈 래더 대조의 분취 량을 실행하여 DNA 단편의 농도를 추정한다.
- 이전 번째로 분해 ptdTomato-C1 벡터 (17) (100 NG)로 정제 된 제품 (약 100 NG)를 결찰즉 동일한 제한이 16 시간 동안 실온에서 T4 DNA 리가 제 (000 단위) 및 1 ㎕의 10X 결찰 완충액을 사용하여 10 ㎕의 효소.
참고 : 야생 형 및 모터리스 돌연변이가 각각 2에서 963에 963과 584에 아미노산이 포함되어 있습니다. 이전에, 더 큰 모터리스 KIF5B 변이체는 그 기능 (9)를 식별하는 데 사용 하였다. 작은 모터리스 KIF5B 돌연변이는 발현 수준을 증가시키기 위해, 본 연구에 사용 하였다.
2. 면역 형광 현미경
- 살아있는 세포 또는 또는 40 배 이하의 배율 간접 형광 이미징, 1 ml의 완전 배지에서 0.2-0300000 HeLa 세포를 시드의 각 웰에 [둘 베코 변형 이글 중간 10 % 소 태아 혈청 (DMEM) (FBS)] 여섯 잘 플레이트. 5 % CO 2와 37 ° C에서 성장.
- 40X 이상 배율 간접 면역 형광 연구, 커버 유리를 세척를 들어, 무수 에탄올 짧게과의 (18mm X 18mm 1.5 두께)에서 그들을 공기 건조바이오 안전성 캐비닛 내부 여섯 웰 플레이트의 우물은 오염을 방지 할 수 있습니다.
- 1 종 0.2-0300000 셀은 6 웰 플레이트의 각 웰에 DMEM 배지를 완료 ㎖로.
- 형질 단지의 제조
- 다음날, 바이오 캐비닛 내부화물 후보 단백질 발현 플라스미드의 존재 또는 부재 tdTomato 태깅 야생형 또는 모터리스 KIF5B위한 발현 플라스미드 0.6 μg의 (총) 희석 (pTagCFP-C-MYC 5 ) 1.6 ml의 마이크로 원심 튜브에 0.1 ㎖의 트랜 스펙 션 배지.
참고 : 벡터 pTagCFP-C-MYC는 TagCFP - 태그 C-MYC을 표현한다. - 또 다른 1.6 ml의 microcentrifuge 관에 0.1 ml의 형질 매체에 형질 전환 시약 1.8 μl를 추가합니다. 일반적으로 12 샘플 충분히 희석 형질 전환 시약의 마스터 믹스를 준비합니다.
- 실온에서 5 분 동안 인큐베이션.
- 희석 된 0.1 ml의 DNA를로 희석하여 0.1 ml의 형질 전환 시약을 추가합니다. 미튜브 반전 내용 X. 마이크로 원심 5 초 동안 튜브를 스핀.
- 실온에서 45 분 동안 인큐베이션.
- 다음날, 바이오 캐비닛 내부화물 후보 단백질 발현 플라스미드의 존재 또는 부재 tdTomato 태깅 야생형 또는 모터리스 KIF5B위한 발현 플라스미드 0.6 μg의 (총) 희석 (pTagCFP-C-MYC 5 ) 1.6 ml의 마이크로 원심 튜브에 0.1 ㎖의 트랜 스펙 션 배지.
- 세포의 세척
- 형질 감염 복합체의 형성을위한 배양 기간 동안 세포를 시딩 인산염 완충 식염수 (PBS)로 3 번 씻는다.
- 각 시드의 세포 배지를 교체 아니라 0.8 ml의 예열 형질 매체. 37 ° C에서 인큐베이터에 접시를 돌려줍니다.
- 세포의 형질
- 45 분의 인큐베이션 후, 플레이트의 각 웰에 DNA / 형질 전환 시약 (단계 2.3에서 제조) 착체 0.2 mL를 적하 추가.
- 그들은 37 ° C에서 인큐베이터에 반환되기 전에 5 초 동안 부드럽게 6 잘 판 바위.
- 6-8 시간 후, 전체 DMEM 배지로 배지를 교체한다.
- 라이브 셀 형광 이미징 (18)
- 배양의 부가 16 시간 후t는 37 ° C, 1 μM의 최종 농도로 배지에 DNA에 인터 훽스트 33342 염색을 추가한다.
참고 훽스트 33342이 세포 핵 얼룩 세포 투과성 DNA의 삽입 성 염료이다. - 40X 대물 렌즈를 이용하여 형광 현미경으로 형광 단백질의 발현을 조사하기 전에 37 ° C의 배양기에서 10 분 동안 형질 감염된 세포를 인큐베이션. DAPI, CFP, FITC와 Cy3에 대한 필터 설정은 각각 (Ex350에 ㎚ / Em460에 ㎚) (Ex436에 ㎚ / Em480에 ㎚) (Ex470에 ㎚ / Em525 수 (NM)) 및 (Ex545에 ㎚ / Em605에 ㎚)이다.
주 : 배경 인해 완전 DMEM 배지 자동 형광으로 높으면 페놀 레드없는 배지가 사용된다.
- 배양의 부가 16 시간 후t는 37 ° C, 1 μM의 최종 농도로 배지에 DNA에 인터 훽스트 33342 염색을 추가한다.
간접 면역 형광 연구 3.
- 파라 포름 알데히드 용액의 조제
- 파라 포름 알데히드 분말 (100 ml의 PBS 당 4 g)을 달아 PBS에 추가합니다.
참고 : 파라 포름 알데히드는 가연성 고체 및 잠재적 인 암 해저드입니다디. 그것은 눈, 호흡계 및 피부를 자극. 따라서, 파라 포름 알데히드와의 접촉 또는 흡입을 방지하는 것이 중요하다. - 용액 (150 ㎕를 10 N의 NaOH / 100 ㎖)에 NaOH를 추가합니다.
- 가끔 흔들어 2-3 시간 동안 42 ° C에 37에서 솔루션을 유지합니다.
- 용해 후, 파라 포름 알데히드 분말 용액 (75 μL / 100 ㎖)에 빙초산을 첨가하여 pH를 7.0으로 조정합니다.
- 파라 포름 알데히드 분말 (100 ml의 PBS 당 4 g)을 달아 PBS에 추가합니다.
- 대상 단백질 염색
- 37 ° C에서 16 시간 동안 더 배양 한 후, 5 초 동안 6 웰 플레이트 소용돌이하여 PBS로 한번 실온에서 형질 감염된 세포를 씻는다.
- 웰당 갓 제조 한 4 % 파라 포름 알데히드 용액을 1 ㎖로 세포를 고정한다. 실온에서 30 분 동안 인큐베이션.
- 한 번에 5 초 6 웰 플레이트에 대해 소용돌이에 의해 PBS로 세포를 씻으십시오. 솔루션을 폐기하십시오.
- 30 분 동안 실온에서 0.1 % (PBS)에서 트리톤 X-100 1 ㎖로 세포를 인큐베이션. DET이들 세포 표적에 대한 항체의 접근을 허용하는 세포막 Permeabilize 하시려면 것이다 트리톤 X-100 ergent.
- 5 초 때마다 6 웰 플레이트 소용돌이하여 PBS로 4 회 세포를 씻으십시오. 각 세척 후 솔루션을 폐기하십시오.
- 4 시간 동안 흔들어 실온에서 PBS 용액에 10 %의 FBS (0.1 μg의 / ㎖ C-MYC 토끼 항체 또는 p53의 마우스 항체) 일차 항체 1 ㎖로 세포를 인큐베이션.
- 5 초 때마다 6 웰 플레이트 소용돌이하여 PBS로 4 회를 씻으십시오. 각 세척 후 솔루션을 폐기하십시오.
- 2 시간 동안 흔들어 어둠 속에서 실온에서 PBS에 10 % FBS에서, (0.5 μg의 / ㎖ 알렉사 형석 488 - 공액 안티 - 토끼 또는 항 - 마우스 IgG 항체) 형광 염료 접합 이차 항체에 1 ㎖의 인큐베이션.
- 5 초 때마다 6 웰 플레이트 소용돌이하여 PBS로 4 회를 씻으십시오. 각 세척 후 솔루션을 폐기하십시오.
- 핵 염색 및 장착
- DNA에 인터 염료 4 ', 6-diamidino -2- 페닐 인돌의 1ml를 가진 세포를 인큐베이션. 더 커버 유리가 사용되지 않은 경우 3.4 단계로 진행합니다.
- 각 현미경 슬라이드에 장착 용액 10 μl를 적용합니다. 현미경 슬라이드에 장착 솔루션을 통해 각각의 커버 유리를 탑재합니다.
- 어두운 밤새 실온에서 인큐베이션.
- 매니큐어와 커버 유리의 가장자리를 밀봉합니다. 밤새 매니큐어 가스를 제거하기 위해 연기 후드 내부의 어둠 속에서 놓습니다.
주의 : DAPI는 세포핵 얼룩 DNA에 인터 염료이다. - 형광 현미경 (19)
- 다음 날, 40X 목표를 사용하여 형광 현미경으로 세포를 검사합니다. DAPI, CFP, FITC와 Cy3에 대한 필터 설정은 각각 (Ex350에 ㎚ / Em460에 ㎚) (Ex436에 ㎚ / Em480에 ㎚) (Ex470에 ㎚ / Em525 수 (NM)) 및 (Ex545에 ㎚ / Em605에 ㎚)이다.
결과
외인성는 C-MYC는 핵 (도 1A)를 중심으로 나타난 반면 야생형 KIF5B은 세포질에서 발현 균일 나타났다. 그러나, 모터리스 KIF5B 돌연변이 세포질 (도 1a)의 응집체를 형성했다. 모터리스 KIF5B의 집계는 C-MYC의 응집을 유도. 세포의 비율이 낮았다 야생형 KIF5B 발현 세포 TagCFP 태그가 C-MYC 집계를 발현. 그러나, 모터리스 KIF5B는 (도 1a)을 공동 발현 될 때 상당히 높았다. C-MYC와 돌연변이 KIF5B의 관찰 공동 현지화 (그림 1) KIF5B는 C-MYC의 세포 내 현지화를 조절하고 C-MYC는 키네신-1의화물 있음을 시사한다. 구조가 단독으로 표현 된에 음성 대조군은 그림 1A의 하부 패널에 포함되어 있습니다. 결과는 형광 emissio의 유의 블리드 - 스루가 없다고 표시엔. 모터리스 KIF5B 또한 내인성 C-MYC (도 1b) 및 전사 인자 p53의 (도 2)의 응집을 유도 나타내는 C-MYC 및 p53이 모두 키네신-1화물이며 KIF5B 두 내인성 단백질의 세포 내 위치 파악을 조절한다. 함께 키네신-1 억제제는 C-MYC 및 p53이 모두 5 벵골 락톤 (RBL) 고 분자량 종 (20)이 유도 형성 상승한 결과, p53의 가능성 키네신-1화물이다. C-MYC 같은 핵 전사 인자 p53의는, 또한 프로 테아 좀 저하 (21, 22)의 세포질에 핵에서 내 보낸 것을주의하는 것이 재미있다. 모터리스 KIF5B 변이체의 발현이 세포 내 지역화 C-에 Fos 영향을하거나 응집 (도 3)이 발생하지 않았기 때문에 KIF5B하여 전사 인자의 이동이 상세하게 보인다. 전술 한 데이터는 운전 방식이 있음을 입증이 책에서 사용 d를 키네신-1화물의 높은 특이성 식별 할 수 있습니다. 유사한 전략은 다른 모터 단백질에 적용될 수있다.
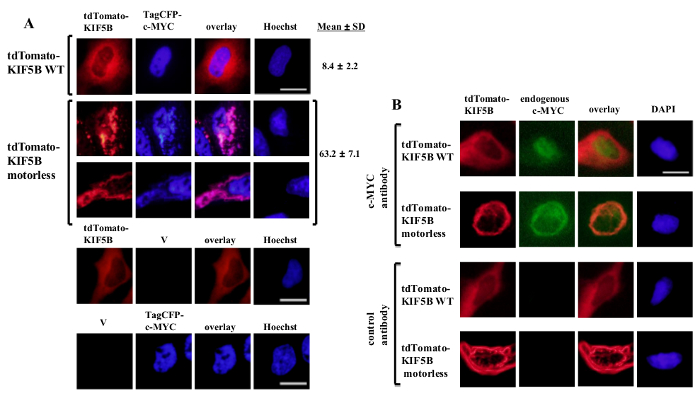
그림 1 : 모터리스 KIF5B 돌연변이 체의 발현은 세포질에서 C-MYC 응집을 유도 (A) 헬라 세포는 tdTomato-태그 야생형 (WT) KIF5B (적색)과 TagCFP - 태그 C-MYC (파란색)으로 형질 감염시켰다.. MYC는 C-핵에 주로 등장 TagCFP-태그 동안 tdTomato-태그 WT KIF5B는 세포질에 주로 나타났다. 그러나, tdTomato-태그 모터리스 KIF5B 돌연변이 (빨간색)은 세포질에서 사상 또는 반점 집계를 형성했다. 모터리스 KIF5B의 발현은 C-MYC의 응집을 유도. 돌연변이 KIF5B 및 C-MYC의 함께 (핑크) 공동는 지역화. CFP-C-MYC (%)의 집계를 나타내는 세포 (%)의 비율이 표시됩니다. 결과로서 도시SD (N = 3) ± 의미한다. tdTomato-태그 KIF5B 단백질 또는 빈 벡터 (V)와 함께 TagCFP - 태그 C-MYC의 발현과 음성 대조군은 하단 패널에 표시됩니다. (B) 유사한 결과 tdTomato 태깅 WT 또는 모터리스 KIF5B 단백질 (적색)을 나타냈다 내인성 C-MYC (녹색)로 수득 하였다. tdTomato-태그 모터리스 KIF5B 돌연변이는 세포질에 집계를 형성하고, 내생 C-MYC의 응집을 유도. 집계의 두 종류의 세포질 (오렌지)에서 함께 지역화 공동. 핵은 염료의 Hoechst 33342 또는 DAPI로 염색 하였다. 스케일 바; 20 μm의. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.

그림 2 : 모터리스 KIF5B 돌연변이 체의 발현은 t에서 내인성 p53의 응집을 유도내인성 p53의 (녹색)이 핵을 중심으로 등장하면서 그 HeLa 세포이다. 세포질 외인성 tdTomato 태깅 된 야생형 (WT) KIF5B (적색), 세포질 주로 나타났다. 반면, 태그가 tdTomato 모터리스 KIF5B 돌연변이 (적색) 세포질 응집체 형성. 모터리스 KIF5B의 발현은 세포질 (노란색)의 KIF5B의 공동 현지화 및 p53의 결과, p53의의 응집을 유도. 실험을 3 회 실시 하였다. 핵은 DAPI 염색으로 염색 하였다. 스케일 바; 20 μm의. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
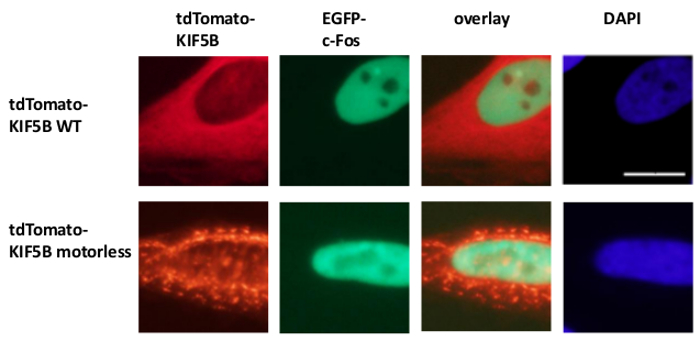
그림 3 :. 모터리스 KIF5B 돌연변이 체의 발현은 세포질에서 C-FOS를 응집을 유도하지 않습니다 야생형을 tdTomato가-태그 (WT) KIF5B (적색) 등장주로 EGFP-C-에 Fos (녹색)이 핵을 중심으로 등장 동안 HeLa 세포의 세포질에서. 반대로 tdTomato 태깅 KIF5B 모터리스 돌연변이 (적색) 세포질 응집체 형성. 모터리스 KIF5B의 발현은 C-FOS를 응집을 유도하지 않았다. 실험 4 번 수행 하였다. 세포의 핵은 DAPI 염색으로 염색 하였다. 스케일 바; 20 μm의. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
| 공통의 역방향 프라이머 | 5'-AGAGGATCCTTACACTTGTTTGCCTCCTC-3 ' |
| 야생형 KIF5B 정방향 프라이머 | AGAGTCGACGCGGACCTGGCCGAGTGCAACATCAAAGT 5'-3 ' |
| 모터리스 KIF5B 정방향 프라이머 | AGAGTCGACGATGAAGAGTTCACTGTTGC 5'-3 ' |
표 1 : 야생 형 및 모터리스 KIF5B 단백질을 복제하기위한 프라이머 시퀀스.
토론
기재된 방법은 미세 소관을 따라 이동할 수있는 능력이 결여 모터리스 KIF5B 변이체의 특성을 이용하지만 동일한화물 단백질과 상호 작용하는 테트라 머 단백질을 야생형 KIF5B와 다이머를 형성하고, 이에 따라, 허용 할 수있는 능력을 보유 야생형 KIF5B있다. 모터리스 KIF5B 따라서, 그화물로 집계 mislocalized 지배적 인 부정적인 돌연변이 및 양식 역할을합니다. 이 방법은 (그림 1) 5에게 키네신-1화물 C-MYC를 식별하기 위해 입증된다. 이 기사에서는 동일한 모터리스 KIF5B 돌연변이는 키네신-1의 또 다른 잠재적 인화물 (그림 2)로 p53의를 식별하는 데 사용되었다. 이 방법론은 키네신 -1- 다른화물을 식별 가능한 것을 나타낸다. 또한, 돌연변이의 특성은 대조군 단백질에 Fos-C (도 3)에 대한 돌연변이의 효과의 부족에 의해 제공된다.
이 프로토콜에서는 야생 타이를 tdTomato-태그퍼가기 또는 모터리스 KIF5B 단백질은 다른 형광 단백질 태그 후보화물 단백질과 동시 발현된다. 이 경우에, 살아있는 세포의 형광 현미경 및 이미징이 수행된다. 응집체의 형성은 저속 촬상으로 추적 될 수있다. 이와 달리, 태깅 tdTomato 단백질 단독 발현 및 생리적 수준에서 후보화물 단백질 특이 적 항체를 이용하여 간접 면역 형광 현미경 검사에 의해 가시화된다. 형광 단백질 tdTomato는 밝기와 광 안정성 (17)에 대해 선택된다. 배경 완전한 DMEM 배지 자동 형광에 의한 높으면 페놀 레드없는 배지가 사용된다.
모터리스 KIF5B 돌연변이 화학량 야생형 KIF5B와 이합체를 형성한다. 따라서, 그 기능을 억제하고, 응집체를 형성하도록 야생형 카운터 파트와 이합체를 형성하도록 모터리스 KIF5B 변이체의 충분한 양을 표현하는 것이 중요하다. , EXPR의 최적화를이 문제를 해결하려면모터리스 돌연변이의 ession이 필수적이다. 이는 이량 체화 도메인을 포함하는 소형 모터리스 돌연변이를 사용하여 달성된다. 또한, 적절한 형질 전환 시약 및 프로토콜의 최적화도 필요하다. DNA / 형질 전환 시약과 HeLa 세포의 배양 기간은 외래 단백질 및 세포 생존의 발현 HeLa 세포에서 최적화되었다. 배양 시간은 기타 세포주에 대해 최적화 될 필요가있다.
40X에 4 배 사이의 배율의 경우, 커버 안경이 필요하지 않습니다. 세포를 직접 웰에서 검사 될 수있다. 따라서,이 경우, 프로토콜은 저렴하고 편리하다. 40X 이상 배율의 경우, 세포를 염색 한 후, 오일 침지 목표 아래 검사에 대한 현미경 슬라이드에 장착되어, 우물에 커버 유리에 성장하고있다.
모터리스 KIF5B 단백질 응집체의 관찰 세포질의 크기에 의해 제한된다. 을 감지하기 쉽습니다많은 포유 동물 세포의 집합체. 그러나, 세포질 부피의 핵 주위의 신경 돌기 작은 경우 신경 세포의 응집체를 관찰 비교적 어렵다.
프로토콜은 생체 효모 두 하이브리드 생화학 풀다운 분석 13-16 이외에 KIF5B화물과의 연관성을 표시하기 위해 사용된다. 이러한 모든 분석은 서로 다른 물리적 조건 관계를 결정하고 그 결과를 서로 보완 할 수있다. 또 다른 분석을 통해이 형광 분석의 장점은 KIF5B 의해화물의 세포 내 편재 규제를 표시 할 수 있다는 점이다 (도 1 및도 2).
프로토콜 KIF5B에 한정되지 않고, 다른 키네신 모터 (3) 및 (3)의 세포 내화물 운송에 사용 미오신 모터 (23, 24)의 일부로서 다른 모터 단백질의화물을 식별하는데 사용될 수있다. 이 모터 단백질은 또한 올리고머에 대한 키네신 모터와 마이 오신 모터 용 미세 섬유 및 코일 코일 세그먼트에 대한 미세 소관을 따라 이동을 위해 모터 도메인이 포함되어 있습니다. 그들 대부분은 동종이 량체 3,23를 형성한다. 따라서, 유사한 전략은화물을 식별하기 위해 자신의 모터리스 우성 네거티브 돌연변이를 생성하여 이들에인가 될 수있다.
공개
이 문서의 무료 액세스 출판 및 생산 로슈에 의해 지급됩니다.
감사의 말
Roche's Publication Grant covered the Free Access publication and production of this article. The author also thanks E. Premkumar Reddy, Richard V. Mettus, Stephen C. Cosenza, Sau Ying Yip and Sol D. Gloria for their support and critical reading of the manuscript.
자료
| Name | Company | Catalog Number | Comments |
| absolute ethanol (200 proof) | Fisher Scientific | BP2818 | |
| DAPI | Sigma-Aldrich | D9542 | |
| Hoechst 33342 | Sigma-Aldrich | B2261 | |
| Opti-MEM-I (transfection medium) | Life Technologies | 51985 | |
| ProLong Diamond Antifade Mountant | Life Technologies | P36961 | |
| formaldehyde, para | Fisher Scientific | O4042-500 | |
| Triton-X100 | Fisher Scientific | BP151-500 | |
| X-tremeGENE 9 DNA Transfection Reagent | Roche | 6365787001 | |
| Taq DNA polymerase | Life Technologies | 10342020 | |
| PCR Grade Nucleotide Mix (dNTP Mix) | Roche | 12111424 | |
| Microscope cover glass | Fisher Scientific | 12-541A | |
| GeneRuler 1 kb Plus DNA ladder | Life Technologies | SM1333 | |
| PureLink Quick Gel Extraction kit | Life Technologies | K210012 | |
| BamHI | New England Biolab | R0136 | |
| SalI | New England Biolab | R0138 | |
| T4 DNA ligase | New England Biolab | M0202T | |
| Ethidium bromide | Thermo Scientific | 17898 | |
| DMEM | Life Technologies | 11995-065 | |
| c-MYC rabbit antibody | Cell Signaling | 5606 | |
| p53 mouse antibody | Santa Cruz | sc-126 | |
| Alexa Fluor 488-conjugated anti-rabbit IgG antibody | Life Technologies | A11008 | |
| Alexa Fluor 488-conjugated anti-mouse IgG antibody | Life Technologies | A11059 | |
| fluorescent microscope | Olympus IX71_Fluoview | ||
| computer software for imaging | cellSens |
참고문헌
- Hirokawa, N., Niwa, S., Tanaka, Y. Molecular motors in neurons: transport mechanisms and roles in brain function, development, and disease. Neuron. 68, 610-638 (2010).
- Yu, Y., Feng, Y. M. The role of kinesin family proteins in tumorigenesis and progression: potential biomarkers and molecular targets for cancer therapy. Cancer. 116, 5150-5160 (2010).
- Verhey, K. J., Hammond, J. W. Traffic control: regulation of kinesin motors. Nat Rev Mol Cell Biol. 10, 765-777 (2009).
- Hirokawa, N., Noda, Y., Tanaka, Y., Niwa, S. Kinesin superfamily motor proteins and intracellular transport. Nat Rev Mol Cell Biol. 10, 682-696 (2009).
- Lee, C. M. Transport of c-MYC by Kinesin-1 for proteasomal degradation in the cytoplasm. Biochim Biophys Acta. 1843, 2027-2036 (2014).
- Bittins, C. M., Eichler, T. W., Hammer, J. A., Gerdes, H. H. Dominant-negative myosin Va impairs retrograde but not anterograde axonal transport of large dense core vesicles. Cell Mol Neurobiol. 30, 369-379 (2010).
- Kimura, T., Watanabe, H., Iwamatsu, A., Kaibuchi, K. Tubulin and CRMP-2 complex is transported via Kinesin-1. J Neurochem. 93, 1371-1382 (2005).
- Lindsay, A. J., McCaffrey, M. W. Myosin Va is required for the transport of fragile X mental retardation protein (FMRP) granules. Biol Cell. 106, 57-71 (2014).
- Rivera, J., Chu, P. J., Lewis, T. L., Arnold, D. B. The role of Kif5B in axonal localization of Kv1 K(+) channels. Eur J Neurosci. 25, 136-146 (2007).
- Roland, J. T., Kenworthy, A. K., Peranen, J., Caplan, S., Goldenring, J. R. Myosin Vb interacts with Rab8a on a tubular network containing EHD1 and EHD3. Mol Biol Cell. 18, 2828-2837 (2007).
- Uchida, A., Alami, N. H., Brown, A. Tight functional coupling of kinesin-1A and dynein motors in the bidirectional transport of neurofilaments. Mol Biol Cell. 20, 4997-5006 (2009).
- Zadeh, A. D., et al. Kif5b is an essential forward trafficking motor for the Kv1.5 cardiac potassium channel. J Physiol. 587, 4565-4574 (2009).
- Su, Y. Y., et al. KIF5B promotes the forward transport and axonal function of the voltage-gated sodium channel Nav1.8. J Neurosci. 33, 17884-17896 (2013).
- Lalioti, V. S., Vergarajauregui, S., Tsuchiya, Y., Hernandez-Tiedra, S., Sandoval, I. V. Daxx functions as a scaffold of a protein assembly constituted by GLUT4, JNK1 and KIF5B. . J Cell Physiol. 218, 416-426 (2009).
- Cho, K. I., et al. Association of the kinesin-binding domain of RanBP2 to KIF5B and KIF5C determines mitochondria localization and function. Traffic. 8, 1722-1735 (2007).
- Diefenbach, R. J., Diefenbach, E., Douglas, M. W., Cunningham, A. L. The ribosome receptor, p180, interacts with kinesin heavy chain, KIF5B. Biochem Biophys Res Commun. 319, 987-992 (2004).
- Shaner, N. C., et al. Improved monomeric red, orange and yellow fluorescent proteins derived from Discosoma sp. red fluorescent protein. Nat Biotechnol. 22, 1567-1572 (2004).
- Waters, J. C. Live-cell fluorescence imaging. Methods Cell Biol. 114, 125-150 (2013).
- Sanderson, M. J., Smith, I., Parker, I., Bootman, M. D. Fluorescence microscopy. Cold Spring Harb Protoc. 2014, (2014).
- Hopkins, S. C., Vale, R. D., Kuntz, I. D. Inhibitors of kinesin activity from structure-based computer screening. Biochemistry. 39, 2805-2814 (2000).
- Zhang, Y., Xiong, Y. Control of p53 ubiquitination and nuclear export by MDM2 and ARF. Cell Growth Differ. 12, 175-186 (2001).
- Michael, D., Oren, M. The p53-Mdm2 module and the ubiquitin system. Semin Cancer Biol. 13, 49-58 (2003).
- Kneussel, M., Wagner, W. Myosin motors at neuronal synapses: drivers of membrane transport and actin dynamics. Nat Rev Neurosci. 14, 233-247 (2013).
- Maravillas-Montero, J. L., Santos-Argumedo, L. The myosin family: unconventional roles of actin-dependent molecular motors in immune cells. J Leukoc Biol. 91, 35-46 (2012).
재인쇄 및 허가
JoVE'article의 텍스트 или 그림을 다시 사용하시려면 허가 살펴보기
허가 살펴보기This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. 판권 소유