Method Article
동시 간섭 반사 및 전체 내부 반사 형광 현미경 검사 이미징 동적 미세 소관 및 관련 단백질
요약
우리는 동적 미세 소관 및 형광 표지 된 미세 소관 관련 단백질의 동시 이미징을 위해 간섭 반사 현미경 검사 및 전체-내부-반사-형광 현미경을 구현하기위한 프로토콜을 제시합니다.
초록
세포골격 필라멘트 및 이들의 관련 단백질의 직접적인 시각화를 위해 몇몇 기술이 채택되었다. 전체-내부-반사-형광(TIRF) 현미경은 신호 대 배경 비율이 높지만 형광 단백질의 광표백 및 광손상을 겪습니다. 간섭 반사 현미경 (IRM) 및 간섭 산란 현미경 (iSCAT)과 같은 라벨이없는 기술은 광표백 문제를 우회하지만 단일 분자를 쉽게 시각화 할 수는 없습니다. 이 논문은 IRM을 시험관 내에서 미세소관 관련 단백질(MAPs) 및 동적 미세소관의 동시 이미징을 위한 상업용 TIRF 현미경과 결합하기 위한 프로토콜을 제시합니다. 이 프로토콜은 동적 미세 소관과 상호 작용하는 MAP의 고속 관찰을 허용합니다. 이는 미세 소관 라벨링의 필요성과 두 번째 여기 레이저와 같은 몇 가지 추가 광학 부품의 필요성을 제거함으로써 기존의 두 가지 색상 TIRF 설정을 개선합니다. 두 채널 모두 이미지 등록 및 프레임 동기화 문제를 피하기 위해 동일한 카메라 칩에서 이미지화됩니다. 이 설정은 동적 미세 소관 위를 걷는 단일 키네신 분자를 시각화하여 입증됩니다.
서문
전체-내부-반사-형광(TIRF) 현미경은 일반적으로 단일 형광 분자의 시각화를 위해 사용된다. TIRF는 후피형광 이미징과 비교하여 우수한 배경 억제를 달성하여 단일 형광단의 고해상도 국소화 및 추적을 허용합니다. 이러한 이유로, TIRF는 형광 표지된 미세소관-관련 단백질을 시각화하기 위한 바람직한 방법이며, 미세소관 1,2를 이미지화하는데 자주 사용된다.
MAP에 의한 미세 소관 역학의 조절을 조사하기 위해서는 종종 미세 소관과 MAP를 동시에 이미지화해야합니다. 이러한 목적을위한 대부분의 기존 방법은 비용이 많이 들거나 기술적 인 단점을 겪습니다. 예를 들어, 동시 두 가지 색상 TIRF에는 두 개의 여기 레이저와 두 개의 카메라가 필요합니다. 높은 비용 외에도 별도의 카메라의 필요성으로 인해 프레임 동기화 및 이미지 등록 문제가 발생합니다. 회전 필터 큐브가 연속 프레임(3)에서 여기 레이저 사이를 물리적으로 전환하는 데 사용되는 경우 이러한 필요성은 회피될 수 있다. 이러한 설정에서는 단일 카메라 칩을 사용할 수 있으며 프레임은 미세 소관과 MAP의 이미지를 번갈아 가며 사용할 수 있습니다. 그러나, 이 기술은 필터 변화의 속도에 의해 제한되며, 이는 전형적으로 프레임 레이트를 초당 0.5프레임(fps) 미만으로 제한한다. 이러한 프레임 속도는 최대 500nm/s의 속도로 발생하는 미세소관의 수축, 800nm/s 정도의 속도로 키네신을 걷는 것, 또는 0.3μm2/s4를 초과하는 확산 계수로 발생하는 MAP의 확산과 같은 빠른 동적 프로세스를 해결하기에 충분하지 않습니다. 이는 움직이는 미세소관 팁(5)의 위치에 대한 MAP의 위치와 같이 각 채널에서 두 개의 이동 표적의 상대적 위치를 추적할 때 특히 문제가 된다.
이러한 광학적 제약 외에도 두 가지 색상 TIRF 현미경 검사에서는 MAP와 미세 소관을 방출 스펙트럼이 충분히 분리 된 다른 형광단으로 표지해야합니다. 튜불린의 형광 표지는 미세 소관 역학6을 변화시킬 수 있고, 형광단의 광표백은 이미징 속도(7)를 제한한다. 이러한 문제로 인해 미세 소관을 시각화하기 위해 라벨이없는 이미징 기술이 개발되었습니다. 여기에는 간섭 산란 현미경 (iSCAT) 8,9, 회전 일관성 산란 현미경 (ROCS)10, 공간 광 간섭 현미경 (SLIM)11 및 간섭 반사 현미경 (IRM) 12,13이 포함됩니다. 이러한 기술은 형광 이미징의 단점 없이 미세소관의 빠른 라벨 없는 이미징을 허용하지만 단일 MAP를 시각화하는 데 사용할 수는 없습니다.
이러한 라벨이 없는 기술 중에서 IRM은 저렴한 비용과 계측에 대한 겸손한 요구로 두드러집니다. 우리는 최근에 IRM을 상업용 TIRF 현미경과 결합하기위한 프로토콜을 제시하여 미세 소관 및 형광 MAP를 교대로 프레임3,13으로 이미징 할 수 있습니다. 이 백서에서는 단일 카메라 칩에서 TIRF 및 IRM 이미지를 동시에 캡처하도록 이 설정을 수정하는 프로토콜을 제시합니다. 여기에는 TIRF 레이저 및 IRM LED 광원으로 샘플을 동시에 비추기 위해 여기 경로에 저렴한 빔 스플리터를 추가하는 작업이 포함됩니다. 수정된 상용 이미지 스플리터는 TIRF 및 IRM 신호를 분광적으로 분리하여 동일한 카메라 칩의 개별 반쪽에 투사하는 데 사용됩니다. 우리는 또한 이미징 중에 시약을 신속하게 교환 할 수있는 미세 유체 시스템을 사용합니다. 이 프로토콜은 이 설정을 사용하여 동적 미세소관 및 MAP를 이미지화하는 방법을 설명합니다. 이 장치의 능력은 10 s-1의 프레임 속도로 포획되는 축소 미세 소관에서 걷는 키네신-1 단백질의 첫 번째 시각화를 제시함으로써 입증됩니다.
프로토콜
1. 유동 챔버의 제조
참고: 미세유체 유동 챔버는 폴리디메틸실록산(PDMS) 마이크로채널을 세척 및 기능화된 커버 글라스에 부착하여 제작됩니다. 마이크로채널은 마스터 몰드에서 주조될 것이다.
-
PDMS 채널의 제조
- 이미징되는 특정 분석에 적합한 표면 화학으로 세척 및 / 또는 기능화 된 커버 글라스를 준비하십시오.
참고: 키네신 운동성 분석의 경우, 피라냐 세척 실란화 커버 글라스가 사용됩니다. 이들은 Gell et에 기재된 바와 같이 제조된다. al.1 대안으로, 더 간단한 절차는 이소프로판올에서 커버 글라스를 초음파 처리 한 다음 메탄올을 3x 20 분 사이클 동안 초음파 처리하는 것입니다. - 마스터 몰드를 준비하려면 단면 고정 테이프의 스트립을 원하는 흐름 채널 크기로 자릅니다. 스트립을 10cm 페트리 접시의 바닥에 부착하고 스트립 사이에 최소 1cm 간격으로 좌우로 배치하십시오.
참고: 정밀한 채널 치수가 필요한 경우, 금형은 포토리소그래피(14)를 사용하여 실리콘 웨이퍼에 제작될 수 있습니다. - PDMS 중합체를 제조하기 위하여는, 경화제와 염기 엘라스토머를 1:10 질량비로 결합하십시오. 2 분 동안 혼합하십시오.
참고: 이 혼합 비율은 중합체의 강성을 조정하기 위해 변화될 수 있다. 경화제에 대한 염기의 비율이 높을수록 더 부드러운 중합체가 생깁니다. - 모든 기포가 사라질 때까지 진공 챔버에서 혼합물을 탈기하십시오.
- 혼합물을 ~ 0.5cm 두께의 층으로 마스터 몰드에 붓고 거품이 생기지 않도록주의하십시오.
- 혼합물을 70°C의 예열된 오븐에서 40분 동안 굽는다.
참고: PDMS 블록이 두꺼운(>1cm) 경우 더 긴 경화 시간이 필요할 수 있습니다. 완전히 경화 될 때까지 5 분 단위로 가열을 계속하십시오. - 중합체의 구조화된 영역을 잘라낸다. PDMS 펀처를 사용하여 채널의 각 끝에 구멍을 펀치합니다.
참고: 이 프로토콜에서 구멍 직경은 0.75mm로 설정되며 필요한 유량에 따라 조정할 수 있습니다. PDMS 채널은 건조한 환경에 장기간 보관할 수 있지만 사용하기 전에 청소해야 합니다. - PDMS 블록의 구조화된 측면을 청소합니다. 고정 테이프를 사용하여 큰 입자를 제거하십시오. 이소프로판올로 헹구고 메탄올로 헹구십시오. 이 헹굼을 3 배 반복하고, 초순수로 헹구고, 표면을 불어 말리십시오.
- 플라즈마는 산소 또는 공기 플라즈마를 사용하여 PDMS를 청소합니다.
참고: 이 프로토콜에서는 18W 공기 플라즈마가 사용됩니다. - 플라즈마 세척된 PDMS를 적절하게 세척된 커버 글라스 위에 놓고 80°C에서 15분 동안 핫플레이트 상에 가열한다.
참고: 에폭시 수지는 PDMS 블록의 측면에 적용하여 커버 글라스에 더 잘 부착할 수 있습니다. - 적절한 크기의 저밀도 폴리에틸렌(LDPE) 튜브를 구멍에 삽입합니다. 출구 튜빙을 0.5 mL 주사기에 연결하십시오.
참고: 이 프로토콜에서 내경이 0.023in인 튜브는 외경 금속 어댑터의 0.025를 통해 PDMS에 연결됩니다. - 유입 튜브를 용액에 침지하고 주사기로 필요한 부피를 인출함으로써 용액을 마이크로채널 내로 유동시킨다.
- 이미징되는 특정 분석에 적합한 표면 화학으로 세척 및 / 또는 기능화 된 커버 글라스를 준비하십시오.
2. 광학 설정
-
현미경의 변형(그림 1)
- IRM 이미징13을 사용하도록 TIRF 현미경을 수정합니다. 현미경의 필터 휠에 사용되는 50/50(반사율(R)/투과(T)) 빔 스플리터를 10/90(R/T) 빔 스플리터로 교체합니다.
- 카메라와 현미경 사이에 이미지 분할기를 삽입합니다.
- 이미지 스플리터의 필터 큐브에 10/90(R/T) 빔 스플리터를 삽입합니다. 반사 빔의 전면에 600 nm 장투과 필터를 배치하고 투과된 빔 앞에 적절한 형광 방출 필터를 배치한다.
참고: R/T 비율이 다른 빔 스플리터를 사용하여 수집되는 IRM 및 TIRF 방출광의 분율을 조정할 수 있습니다. - 제조업체의 사양에 따라 이미지 스플리터를 정렬하여 카메라 칩의 TIRF 및 IRM 신호를 공간적으로 분리합니다.
참고: 일반적인 형광단의 TIRF 신호가 미세소관의 IRM 신호보다 훨씬 약하고 두 신호가 오버레이된 경우 감지할 수 없기 때문에 신호의 공간적 분리가 필요합니다.
3. 이미징 동적 미세 소관 및 단일 키네신 분자
- 표면 기능화 및 패시베이션
- BRB80 완충액 (80 mM Na-PIPES, 1 mM EGTA, 1 mMMgCl2, NaOH로 pH 7.8로 적정)을 반응 챔버 내로 유동시켰다.
- BRB80에서 0.025 mg/mL로 희석된 항생제 용액을 유동시키고 실온에서 10분 동안 인큐베이션한다.
- BRB80으로 채널을 세척하십시오.
- F-127 용액 (하룻밤 사이에 BRB80에 용해된 1% 플루로닉 F-127 (w/v))을 유동시키고, 표면 패시베이션을 위해 적어도 20분 동안 인큐베이션한다.
참고: 실란화된 커버 글라스 대신 쉽게 청소할 수 있는 커버 글라스를 사용하는 경우, BRB80에서 2mg/mL 카제인을 실온에서 >20분 동안 사용하여 패시베이트합니다. - BRB80으로 채널을 세척하십시오.
- 이미징 준비
- 온도 제어가 필요한 경우 대물 히터를 사용하여 올바른 온도로 설정하십시오.
참고: 이 프로토콜에서는 모든 실험이 28°C에서 수행됩니다. - 샘플을 현미경 스테이지에 놓고 IRM 이미징을 위해 에피조명 광원(>600nm)을 켭니다.
참고: 이 프로토콜에서는 백색 LED 광원이 600nm 장역 필터와 함께 사용됩니다. - 현미경을 시료 표면에 집중시킵니다. PDMS-솔루션 인터페이스 근처에서 올바른 초점면을 찾습니다.
참고: IRM에서 채널의 수성 내부는 PDMS 폴리머보다 훨씬 밝게 나타나야 합니다. - 채널 중심 근처의 시야를 선택합니다.
- BRB80에 0.1 μm 형광 마이크로비드의 용액을 준비한다(밀도: 109 비드/mL, 이 프로토콜에 사용된 비드에 대한 200배 희석에 해당).
- 마이크로비드 용액의 적어도 하나의 채널 부피로 유동한다.
- IRM을 통해 반응을 모니터링합니다. 마이크로 비드가 점차적으로 표면에 "착륙"할 때까지 기다리십시오. 마이크로비드의 원하는 밀도가 달성되면, 과량의 BRB80을 세척한다.
- 온도 제어가 필요한 경우 대물 히터를 사용하여 올바른 온도로 설정하십시오.
- 성장 비오티닐화 구아닐 5'-α,β-메틸렌디포스포네이트 (GMPCPP)-안정화된 미세소관 종자
- 0.6 mL 원심분리 튜브에서, BRB80 중의 1 mM GMPCPP, 1 mMMgCl2, 및 2 μM 비오티닐화 튜불린(5-10% 표지 화학량론)을 함유하는 용액 50 μL를 제조하였다.
참고 : 올바른 라벨링 화학량론은 고밀도 비오티닐화 튜불린과 라벨링되지 않은 소 튜불린을 올바른 비율로 결합하여 달성 할 수 있습니다. - 용액을 얼음 상에서 5분 동안 인큐베이션한 다음, 37°C에서 12.5분 동안 인큐베이션한다.
참고 : 종자의 길이는 중합 시간을 조정하여 제어 할 수 있습니다. - 100 μL의 실온 BRB80을 첨가하여 중합을 중단시킨다.
- 용액을 실온에서 초원심분리기에서 회전시킨다(126,000 x g, 5분). 상층액을 피펫을 이용하여 폐기하여 중합되지 않은 튜불린을 제거한다.
참고: 이 프로토콜에서는 공기 구동 초원심분리기가 사용됩니다. - 200 μL의 실온 BRB80을 펠렛에 첨가한다. 부드럽게 그러나 철저하게 피펫팅하여 펠렛을 재현탁하십시오. 절단 팁이있는 200 μL 피펫을 사용하여 미세 소관의 전단을 줄입니다.
- 0.6 mL 원심분리 튜브에서, BRB80 중의 1 mM GMPCPP, 1 mMMgCl2, 및 2 μM 비오티닐화 튜불린(5-10% 표지 화학량론)을 함유하는 용액 50 μL를 제조하였다.
- 성장 동적 구아노신 디포스페이트 (GDP) - 튜불린 "확장"
참고 : 씨앗은 유동 채널의 항생제 표면에 고정됩니다. 동적 GTP / GDP "확장"은 고정 된 씨앗의 끝에서 자랄 것입니다.- BRB80에 씨앗을 20x로 희석하십시오. 희석된 종자를 반응 챔버 내로 유동시킨다.
- IRM을 통해 반응을 모니터링합니다. 씨앗이 점차적으로 표면에 "착륙"하고 그것에 결합 될 때까지 기다리십시오. 원하는 종자 밀도가 달성되면 BRB80으로 과잉을 씻어 내십시오.
- 미세소관 연장 혼합물을 제조하였다: BRB80 완충액 중의 12 μM 비표지된 튜불린, 1 mM GTP, 5 mM 디티오트레이톨 (DTT).
- 연장 혼합물의 적어도 하나의 채널 부피로 유동한다. 반응 온도가 28°C인지 확인하십시오.
- 미세 소관 확장이 시간이 지남에 따라 씨앗에서 자랄 때까지 기다리십시오.
참고: 정상 상태 길이는 일반적으로 20분 이내에 달성됩니다. - 이미징을 위해 동적 미세 소관을 사용하십시오. 키네신-1에 대한 단계 3.5에 기재된 바와 같이 미세소관 상의 형광 MAP를 추가하고 시각화한다.
참고: 미세소관은 표면 결합되어 있기 때문에 TIRF에서 쉽게 볼 수 있습니다.
- 키네신 운동성 분석
참고: 이 단계는 축소된 미세소관에 대한 모타일 녹색 형광 단백질(GFP) 표지된 키네신-1을 시각화하기 위한 프로토콜을 설명합니다. eGFP (rKin430-eGFP)에 융합된 절단된 래트 키네신-1 구축물을 앞서15,16에 기재된 바와 같이 발현시키고 정제하였다.- 운동성 완충액을 준비하십시오 : BRB80에서 1 mM ATP 및 0.2 mg / mL 카제인.
- 키네신-eGFP를 운동성 완충액으로 10 nM로 희석한다.
- 2 mM ATP로 보충된 산화적 광표백(80 mM 글루코스, 80 mg/mL 글루코스 옥시다제, 32 mg/mL 카탈라아제, 0.2 mg/mL 카제인, 20 mM DTT)을 상쇄하기 위해 2x 산소 스캐빈저 용액을 준비하십시오.
- 0.5 nM의 최종 키네신 농도를 위해 산소 제거제 10부, BRB80 9부, 및 10 nM 키네신-eGFP의 1부를 결합한다.
참고: 총 볼륨은 채널 볼륨보다 1.5배 이상 커야 합니다. - 현미경 소프트웨어에서 이미징 설정을 설정합니다.
참고: 이 프로토콜에서 비디오는 100ms 노출 시간으로 10fps로 녹화됩니다. 레이저 강도는 ~ 0.05kW /cm2입니다. - 이미징을 시작하고 키네신 용액을 챔버로 흐르게하십시오.
- 측정이 완료되면 스테이지가 원형 또는 횡방향 동작으로 천천히 변환되는 짧은(~5초) 비디오를 녹화합니다. 이 비디오의 중앙값 투영을 배경 이미지로 사용하고 원시 측정에서 뺍니다.
4. 이미지 처리 및 분석
참고: 이미지 처리는 NIH ImageJ2 (imagej.nih.gov/ij/)를 사용하여 수행되었다. TIRF 및 IRM 채널의 분할 및 정렬을 자동화하기 위해 매크로가 개발되었습니다. 이 매크로를 사용하려면 GaussFit_OnSpot 플러그인을 설치해야 합니다(ImageJ 플러그인 리포지토리에서 사용 가능).
- 배경 녹화에서 이미지 |을 클릭하여 ImageJ에서 중간 투영을 만듭니다 . 스택 | Z 프로젝트.
- | 처리를 클릭하여 원시 이미지 데이터에서 중앙값 배경 투영을 빼십시오 . 이미지 계산기.
참고: "32비트(부동 소수점) 결과" 옵션을 확인하십시오. - 이미지 등록을 위해 관심 있는 미세소관 근처에 있는 마이크로비드 컬렉션을 선택하고 이를 사용하여 TIRF 및 IRM 이미지를 정렬합니다.
- 이 컬렉션의 각 비드에 대해 다중 점 선택 도구를 사용하여 TIRF 채널의 대략적인 위치를 표시한 다음 IRM 채널에서 해당 위치를 표시합니다.
참고: 예를 들어, 두 개의 비드(1과 2)가 있는 경우 멀티포인트 선택은 다음과 같은 순서로 4개의 점을 갖습니다. (1) TIRF에서 비드 1, (2) IRM에서 비드 1, (3) TIRF의 비드 2, IRM의 비드 2. - 제공된 ImageJ 매크로(ImageSplitterRegistration.ijm)를 실행합니다.
참고: 이것은 다음 단계를 자동화한다: i) 가우시안에 피팅하여 각 비드의 중심 위치를 추정하는 단계; ii) 각각의 비드에 대해, IRM 채널 내의 중심으로부터 TIRF 채널 내의 중심을 분리하는 변위 벡터를 계산하는 단계; iii) 모든 비드에 걸쳐이 변위 벡터를 평균화하는 단계; iv) TIRF 및 IRM 채널을 별도의 이미지로 분할하는 단계; v) iii)에서 계산된 평균 변위 벡터에 의해 TIRF 이미지를 번역하는 단계; vi) TIRF 및 IRM 이미지를 다중 채널 .tiff 파일에 오버레이합니다.
결과
광학 설정은 그림 1에서 개략적으로 설명되어 있습니다. IRM 조명과 TIRF 여기 라이트는 모두 10/90(R/T) 빔 스플리터(BS1)를 통해 목표물의 후면 조리개(100x, NA: 1.49)로 향합니다. 방출된 신호는 동일한 빔 스플리터(BS1)를 통과하고 미러(M1)를 통해 이미지 스플리터에 반사된다. 이미지 스플리터의 구성 요소( 그림 1에서 파선으로 묶음)는 적절한 스펙트럼 필터와 함께 90/10(R/T) 빔 스플리터(BS2)를 통해 IRM 및 TIRF 신호를 분리합니다. 마지막으로 분할 이미지는 시각화를 위해 카메라 칩에 투영됩니다. 이미지 스플리터의 정렬은 TIRF 및 IRM 신호가 칩의 개별 반쪽에 투영되도록 하는 것입니다.
잘 정렬된 현미경에서 카메라 이미지는 그림 2와 같이 중간 분할 이미지를 표시해야 합니다. 표면 결합된 미세소관은 IRM 채널(13)에서 쉽게 볼 수 있어야 하고, 형광 키네신은 TIRF 채널에서 볼 수 있어야 한다.
두 채널을 정렬하고 등록하는 데 사용되는 마이크로비드는 TIRF 이미지에는 밝은 점으로, IRM 이미지에는 어두운 점으로 나타납니다. 원시 데이터에서 구슬이 표시되지만 배경 뺄셈은 대비를 크게 향상시킵니다(그림 2). 빼기에 사용되는 배경 이미지는 움직이는 스테이지로 녹화된 비디오의 시간 중앙값입니다. 프로토콜에 설명된 바와 같이, 이미지 정렬은 관심 영역 근처의 비드 콜렉션을 선택하고 제공된 매크로(imageSplitterRegistration.ijm)를 실행함으로써 수행되었다. 매크로는 점을 가우시안에 맞추고 각 채널에서 적합의 중심점 사이의 평균 거리를 최소화하여 이미지를 정렬합니다. 이 과정은 형광 마이크로비드의 양호한 정렬을 보여주는 도 2에 나타내어진다(TIRF 채널에서는 녹색, IRM 채널에서는 검은색).
마지막으로,이 동시 이미징 설정의 기능은 미세 소관의 수축 끝을 향해 걷는 단일 키네신 분자를 관찰함으로써 입증됩니다. 도 3은 수축하는 미세소관(회색) 위를 걷는 eGFP 표지된 키네신 분자(녹색)의 키모그래프를 도시한다. 또한 키모그래프가 생성된 기록의 일련의 스냅샷도 제시됩니다.
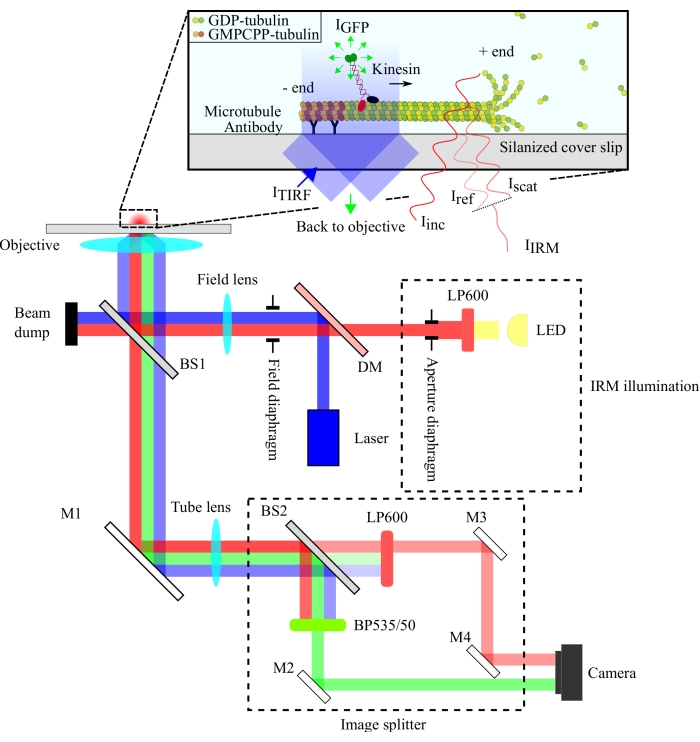
그림 1: 키네신 운동성의 IRM 및 TIRF 동시 이미징을 위한 광학 설정의 개략적인 표현. LED 광원의 에피조명은 조리개 다이어프램을 통과하여 10/90(R/T) 빔 스플리터(BS1)에 도달합니다. 빔 스플리터는 샘플을 비추는 목표까지 적색 IRM 조명광과 488nm TIRF 여기광을 부분적으로 반사합니다. 샘플의 신호는 동일한 목표에 의해 수집되고 IRM 및 TIRF 이미지가 90/10(R/T) 빔 스플리터(BS2)에 의해 공간적으로 분리되는 이미지 분할 어셈블리로 전달됩니다. 그런 다음 신호는 카메라 칩에 도달하기 전에 분광으로 필터링됩니다. 약어: IRM = 간섭 반사 현미경; TIRF = 전체-내부-반사-형광; LED = 발광 다이오드; I TIRF =TIRF 조명; I GFP =GFP 형광; Iinc = IRM 조명; Iref = 유리 / 물 계면에서 산란 된 빛; Iscat = 미세 소관에서 산란 된 빛; I IRM =IRM 신호 (Iref 및 Iscat의 간섭); R/T = 반사/전송됨; LP600: 롱 패스 필터 (600 nm); DM = 이색성 거울; BS1 및 BS2 = 빔 스플리터 1 및 2; M1, M2, M3, M4 = 미러; BP535/50 = 대역 통과(535/50 nm); GFP = 녹색 형광 단백질; GMPCPP = 구아닐릴 5'-α,β-메틸렌디포스포네이트; GDP = 구아노신 디포스페이트. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
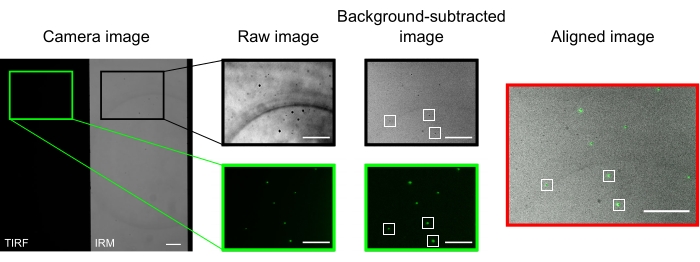
그림 2: 배경 빼기 및 이미지 정렬. TIRF(왼쪽 절반) 및 IRM(오른쪽 절반) 이미지는 동일한 카메라 칩(카메라 이미지)의 두 절반에 동시에 나타납니다. 시간 중앙값 배경 빼기는 IRM에서는 어둡고 TIRF 이미지에서는 밝게 나타나는 구슬(배경에서 뺀 이미지)의 대비를 증가시킵니다. IRM 및 TIRF 이미지는 선택한 구슬(흰색 사각형)의 지역화에 따라 변환(오른쪽)에 의해 정렬됩니다. 스케일 바 = 10 μm. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.

그림 3: 미세소관 수축 중 Kinesins의 움직임에 대한 키모그래프 및 스냅샷. 키모그래프(왼쪽)는 eGFP-kinesin-1(녹색)이 미세소관의 플러스 끝(진한 회색)을 향해 걷는 것을 보여준다. 해당 시계열의 스냅숏이 표시됩니다(오른쪽). 흰색 화살표는 단일 키네신-1 분자를 보여줍니다. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
ImageSplitterRegistration 파일: 이 파일을 다운로드하려면 여기를 클릭하십시오.
토론
미세 소관 관련 단백질 (MAPs)에 의한 미세 소관 역학의 조절을 연구하려면 종종 미세 소관과 MAP의 동시 이미징이 필요합니다. TIRF와 같은 형광 현미경 기술은 전형적으로 이러한 목적을 위해 사용된다. 그러나, 이들은 형광 이미징의 단점에 의해 제한되며, 여기에는 광표백, 광손상 및 형광단 표지의 필요성이 포함된다. IRM과 같은 라벨이 없는 방법은 미세소관을 시각화하는 데 적합하지만 단일 형광단을 이미징할 수는 없습니다. 이 프로토콜은 라벨이 없는 IRM 이미징과 TIRF 현미경을 결합하여 동적 미세소관과 MAP를 동시에 이미징합니다.
IRM 설정은 >600nm로 필터링된 LED 조명원을 사용하는 반면, TIRF 설정은 488nm 레이저를 사용합니다. 우리는 저렴한 플레이트 빔 스플리터를 사용하여 조명 빛을 샘플에 반사하고 수집 된 신호를 검출기로 전송했습니다 (그림 1). 단일 분자 신호의 손실을 최소화하기 위해 10% 반사율 및 90% 투과율을 갖는 빔 스플리터가 선택되었다. 조명 광도의 90 % 손실은 조명 레이저 및 LED의 전력을 증가시켜 보상됩니다.
신호의 스펙트럼 분리는 90/10(R/T) 빔 스플리터와 두 개의 스펙트럼 필터(IRM의 경우 롱 패스 600nm, TIRF의 경우 대역 통과 535/50nm)를 사용하여 달성되었습니다. 스펙트럼으로 분리된 IRM 및 TIRF 신호는 이미지 스플리터 어셈블리를 사용하여 단일 카메라 칩의 두 절반에 프로젝션됩니다. 90/10 빔 스플리터를 사용하면 IRM 신호의 90%가 희생되지만 이는 LED 조명원의 강도를 높여 보상됩니다. 이색성 미러를 사용하여 IRM 및 TIRF 신호를 보다 효율적으로 분리할 수도 있습니다. 분석에 포함된 형광 마이크로비드는 TIRF 및 IRM 이미지의 정확한 정렬을 가능하게 하고 목표를 집중시키기 위한 기준 역할을 합니다.
이 프로토콜에서 가장 중요한 광학 요소는 높은 수치 조리개 (NA) 목표입니다. 이는 전체 내부 반사를 달성 할뿐만 아니라 수집 효율과 이미지 대비를 극대화하는 데에도 필수적입니다. 획득 된 이미지의 품질은 또한 유리 표면의 청결도와 불균일 한 조명을 수정하고 정적 인 특징을 제거하기 위해 명확한 배경 이미지의 획득에 달려 있습니다. IRM 이미징의 경우 장파장 조명(>600nm)을 사용하여 미세소관과 단백질의 광손상을 최소화하는 것이 좋습니다. 이는 백색 LED 광원을 사용하는 경우 특히 중요하며, 이 경우 자외선을 제거하기 위해 장거리 통과 필터가 포함되어야 합니다.
이 프로토콜은 동적 미세 소관의 라벨 없는 고속 이미징과 형광 MAP(17)의 동시 고해상도 시각화를 가능하게 합니다. 미세 소관과 MAP의 이미지를 캡처하는 필터 큐브 스위칭 기술과 비교할 때, 이 설정은 필터 큐브의 물리적 회전에 의존하지 않기 때문에 훨씬 더 높은 프레임 속도를 낼 수 있습니다. 두 가지 색상의 TIRF 이미징 기술과 비교할 때,이 기술은 덜 까다로운 광학 설정을 사용하고 미세 소관의 형광단 표지의 필요성을 회피합니다. 이 설정의 주요 제한 사항은 MAP의 TIRF 이미징 때문입니다. 프레임 속도는 형광단의 노출 시간에 의해 제한되며, 형광단의 광표백은 여전히 가능성으로 남아 있습니다. 그럼에도 불구하고, 이 프로토콜은 필요한 경우에만 TIRF를 사용하고(즉, MAP를 시각화하지만 미세소관은 시각화하기 위해) TIRF의 한계 내에서 가능한 최고 속도를 달성하기 때문에 기존 기술을 개선합니다. 미세 소관과 MAP가 모두 간섭 기술을 통해 시각화 된 경우에만 추가 개선이 가능하지만 한계와 실험적 과제가있는 금속 나노 입자로 MAP를 라벨링해야합니다.
이 기술의 기능을 입증하기 위해 우리는 IRM과 TIRF를 통해 두 가지 빠른 동적 과정, 즉 미세 소관의 수축과 형광 키네신 분자의 보행을 동시에 시각화했습니다. 이 기술은 이전에 축소 미세 소관5에 대한 스파스틴의 빠른 확산을 시각화하기 위해 사용되었습니다. MAP 및 미세소관에 대한 이러한 적용 외에도, 이 프로토콜은 세포막 또는 액틴 필라멘트와 같은 IRM을 통해 시각화될 수 있을 만큼 방대한 거대 분자 구조와 동시에 단일 형광 분자를 시각화하는 데 사용될 수 있습니다.
공개
저자는 공개 할 이해 상충이 없습니다.
감사의 말
클린룸 장비를 공유해 주신 Thierry Emonet의 연구실에 감사드립니다. 이 연구에 사용된 정제된 eGFP-키네신을 준비해 주신 Yin-Wei Kuo에게 감사드립니다. Y.T.는 Feodor Lynen Research Fellowship을 통해 Alexander von Humboldt Foundation의 지원을 인정합니다. 이 작업은 NIH Grant R01 GM139337 (J.H.)에 의해 지원되었습니다.
자료
| Name | Company | Catalog Number | Comments |
| 10/90 (R/T) beam splitter | Thorlabs | BSN10R | Plane beam splitter used in the excitation beam path |
| 90/10 (R/T) beam splitter | Thorlabs | BSX10R | Plane beam splitter used in the image splitter |
| Anti-biotin antibody | Sigma-Aldrich | B3640 | Used to functionalize surface for bonding biotinylated microtubules |
| ATP | Sigma-Aldrich | FLAAS | Used for preparing the motility buffer |
| Band-pass filter | Newport | HPM535-50 | Hard-coated band-pas filter is used in image splitter to image GFP signal |
| Biotinylated tubulin | Cytoskeleton, Inc. | T333P-A | Used to bind microtubule seeds to the surface of the flow channel |
| Casein | Sigma-Aldrich | C8654 | Casein is used to block nonspesific interactions |
| Catalase | Sigma-Aldrich | C9322 | Used for preparing the oxygen scavenger solution |
| Desiccator chamber | Southern Labware | 55207 | Desiccator is used for degasing the resin |
| DTT | Sigma-Aldrich | D0632 | Used for preparing the oxygen scavenger solution |
| EGTA | Sigma-Aldrich | E4378 | Used for preparing the BRB80 buffer |
| Glucose | Sigma-Aldrich | G7528 | Used for preparing the oxygen scavenger solution |
| Glucose oxidase | Sigma-Aldrich | G7016 | Used for preparing the oxygen scavenger solution |
| GMPCPP nucleotides | Jena Bioscience | NU-405L | Used for the polymerization of stabilized microtubules |
| Image splitter | Teledyne-Photometrics Imaging | OptoSplit II | An image splitter is used to split the images spatially. When buying, make sure about the compatibility with the microscope |
| ImajeJ2 | NIH | ImageJ2 is used for image analysis | |
| Kinesin | prepared in house (see references in text) | ||
| LDPE tubing | Thomas Scientific | 9565S22 | Non-toxic, lower density polyethylene micro bore tubing is used for fluid transfers |
| LED light source | Lumencor | Lumencor sola light engine | Used for IRM imaging |
| Long-pass filters | Thorlabs | FELH0600 | Hard-coated long pass filters. One is used as an excitation filter, other is used in image splitter to image IRM signal |
| Magnesium chloride | Sigma-Aldrich | 63068 | Used for preparing the BRB80 buffer |
| Micoscope objective heater | okolab | H401-T-DUAL-BL | Used to keep sample temperature constant via heating the objective |
| Microscope | Nikon | Ti-Eclipse | An inverted microscope that is used in the experiments |
| Na-PIPES | Sigma-Aldrich | P2949 | Used for preparing the BRB80 buffer |
| Nikon CFI Apochromat TIRF 100XC Oil objective | Nikon | MRD01991 | The imaging objective has 1.49 numerical aperture |
| PDMS and curing agent | Electron Microscopy Sciences | Sylgard 184 (24236-10) | Used for contructing the flow channels |
| PDMS puncher | World Precision Instruments LLC | 504529 | Used to punch hole into the PDMS |
| Plasma cleaner | Harrick Plasma | DPC-32G | The air plasma is used to remove organic contamination from the PDMS surface |
| Poloxamer 407 (commercial name Pluronic F-127) | Sigma-aldrich | P2443 | Used for channel surface passivation to minimize nonspecific binding |
| Sodium hydroxide | Sigma-Aldrich | 567530 | Used for preparing the BRB80 buffer |
| Stabilized microtubules | prepared in house (see references in text) | ||
| Table-top ultracentrifuge | Beckman Coulter | 340400 | Used to spin down microtubule seeds |
| TetraSpeck beads | ThermoFisher Scientific | T7279 | Used as a reference for aligning images |
| Zyla 4.2 camera | Andor | Zyla 4.2 | Scientific CMOS camera with spesifications: 2048 x 2048 pixels (6.5 μm pixel size) with quantum efficiency of 72% and 16 bit dynamic range |
참고문헌
- Gell, C., et al. Microtubule dynamics reconstituted in vitro and imaged by single-molecule fluorescence microscopy. Methods in Cell Biology. 95, 221-245 (2010).
- Axelrod, D. Chapter 7: Total internal reflection fluorescence microscopy. Methods in Cell Biology. 89, 169-221 (2008).
- Kuo, Y. -. W., Trottier, O., Mahamdeh, M., Howard, J. Spastin is a dual-function enzyme that severs microtubules and promotes their regrowth to increase the number and mass of microtubules. Proceedings of the National Academy of Sciences of the United States of America. 116 (12), 5533-5541 (2019).
- Hinrichs, M. H., et al. Tau protein diffuses along the microtubule lattice. The Journal of Biological Chemistry. 287 (46), 38559-38568 (2012).
- Al-Hiyasat, A., Tuna, Y., Kuo, Y. -. W., Howard, J. Herding of proteins by the ends of shrinking polymers. arXiv:. , (2021).
- Guo, H., et al. Mechanism and dynamics of breakage of fluorescent microtubules. Biophysical Journal. 90 (6), 2093-2098 (2006).
- Moerner, W. E., Fromm, D. P. Methods of single-molecule fluorescence spectroscopy and microscopy. Review of Scientific Instruments. 74 (8), 3597-3619 (2003).
- Taylor, R. W., Sandoghdar, V., Astratov, V. . Interferometric scattering (iSCAT) microscopy and related techniques. in Label-free super-resolution microscopy. , 25-65 (2019).
- Young, G., Kukura, P. Interferometric scattering microscopy). Annual Review of Physical Chemistry. 70 (1), 301-322 (2019).
- Koch, M. D., Rohrbach, A. Label-free imaging and bending analysis of microtubules by ROCS microscopy and optical trapping. Biophysical Journal. 114 (1), 168-177 (2018).
- Kandel, M. E., Teng, K. W., Selvin, P. R., Popescu, G. Label-free imaging of single microtubule dynamics using spatial light interference microscopy. ACS Nano. 11 (1), 647-655 (2017).
- Mahamdeh, M., Simmert, S., Luchniak, A., Schäffer, E., Howard, J. Label-free high-speed wide-field imaging of single microtubules using interference reflection microscopy. Journal of Microscopy. 272 (1), 60-66 (2018).
- Mahamdeh, M., Howard, J. Implementation of interference reflection microscopy for label-free, high-speed imaging of microtubules. Journal of Visualized Experiments: JoVE. (150), e59520 (2019).
- Voldman, J., Gray, M. L., Schmidt, M. A. Microfabrication in biology and medicine. Annual Review of Biomedical Engineering. 1, 401-425 (1999).
- Rogers, K. R., et al. KIF1D is a fast non-processive kinesin that demonstrates novel K-loop-dependent mechanochemistry. The EMBO Journal. 20 (18), 5101-5113 (2001).
- Leduc, C., Ruhnow, F., Howard, J., Diez, S. Detection of fractional steps in cargo movement by the collective operation of kinesin-1 motors. Proceedings of the National Academy of Sciences of the United States of America. 104 (26), 10847-10852 (2007).
- Tuna, Y., Al-Hiyasat, A., Howard, J. Imaging dynamic microtubules and associated proteins by Simultaneous Interference-Reflection and Total-Internal-Reflection-Fluorescence Microscopy. arXiv. , (2022).
재인쇄 및 허가
JoVE'article의 텍스트 или 그림을 다시 사용하시려면 허가 살펴보기
허가 살펴보기더 많은 기사 탐색
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. 판권 소유