É necessária uma assinatura da JoVE para visualizar este conteúdo. Faça login ou comece sua avaliação gratuita.
Method Article
Medindo Cepas de Tecido Local em Tendões via Correlação de Imagem Digital de Código Aberto
Neste Artigo
Resumo
Este artigo descreve um algoritmo de correlação de imagem digital de código aberto para medir cepas de tecido 2D locais dentro de explantes de tendões. A precisão da técnica foi validada usando várias técnicas e está disponível para uso público.
Resumo
Há um interesse científico considerável em entender as cepas que as células tendinosas experimentam in situ e como essas cepas influenciam a remodelação tecidual. Com base nesse interesse, várias técnicas analíticas foram desenvolvidas para medir cepas teciduais locais dentro de explantes tendinosos durante a carga. No entanto, em vários casos, a precisão e a sensibilidade dessas técnicas não foram relatadas, e nenhum dos algoritmos está disponível publicamente. Isso dificultou a medição mais difundida de cepas teciduais locais em explantes tendinos. Portanto, o objetivo deste trabalho foi criar uma ferramenta de análise validada para medir cepas teciduais locais em explantes tendinosos que esteja prontamente disponível e seja fácil de usar. Especificamente, um algoritmo de correlação de imagem digital de Lagrangian aumentada (ALDIC) disponível publicamente foi adaptado para medir cepas 2D, rastreando os deslocamentos dos núcleos celulares dentro dos tendões de Aquiles de camundongos sob tensão uniaxial. Além disso, a acurácia das deformações calculadas foi validada pela análise de imagens transformadas digitalmente, bem como pela comparação das deformações com valores determinados a partir de uma técnica independente (ou seja, linhas fotobranqueadas). Finalmente, uma técnica foi incorporada ao algoritmo para reconstruir a imagem de referência usando o campo de deslocamento calculado, que pode ser usado para avaliar a precisão do algoritmo na ausência de valores de deformação conhecidos ou uma técnica de medição secundária. O algoritmo é capaz de medir deformações de até 0,1 com uma precisão de 0,00015. A técnica de comparação de uma imagem de referência reconstruída com a imagem de referência real identificou com sucesso amostras que apresentavam dados errôneos e indicou que, em amostras com bons dados, aproximadamente 85% do campo de deslocamento era preciso. Finalmente, as cepas medidas nos tendões de Aquiles de camundongos foram consistentes com a literatura anterior. Portanto, este algoritmo é uma ferramenta altamente útil e adaptável para medir com precisão as cepas de tecido locais nos tendões.
Introdução
Os tendões são tecidos mecanossensíveis que se adaptam e degeneram em resposta à carga mecânica 1,2,3,4. Devido ao papel que os estímulos mecânicos desempenham na biologia celular do tendão, há um grande interesse em entender as cepas que as células tendinosas experimentam no ambiente do tecido nativo durante a carga. Várias técnicas experimentais e analíticas foram desenvolvidas para medir cepas teciduais locais em tendões. Estes incluem análises de correlação digital de imagem (CIVD) 2D/3D de deformações superficiais usando padrões de manchas ou linhas fotobranqueadas (PBLs)5,6,7,8, medição das mudanças na distância centróide-centróide de núcleos individuais dentro do tecido 9,10 e um recente método DIC 3D de campo completo que considera o movimento fora do plano e as deformações 3D 11 . No entanto, a precisão e a sensibilidade dessas técnicas foram relatadas em apenas alguns casos, e nenhuma dessas técnicas foi disponibilizada publicamente, o que dificulta a adoção e utilização generalizadas dessas técnicas.
O objetivo deste trabalho foi criar uma ferramenta de análise validada para medir cepas teciduais locais em explantes tendinosos que esteja prontamente disponível e seja de fácil utilização. O método escolhido baseia-se em um algoritmo de correlação de imagem digital de Lagrangian aumentada (ALDIC) publicamente disponível escrito em MATLAB que foi desenvolvido por Yang e Bhattacharya12. Este algoritmo foi adaptado para análise de amostras de tendões e validado aplicando-o a imagens transformadas digitalmente e comparando as cepas medidas em amostras de tendões reais com os resultados obtidos a partir de linhas fotobranqueadas. Além disso, funcionalidades adicionais foram implementadas no algoritmo para confirmar a precisão do campo de deslocamento calculado, mesmo na ausência de valores de deformação conhecidos ou uma técnica de medição secundária. Portanto, este algoritmo é uma ferramenta altamente útil e adaptável para medir com precisão as cepas de tecido 2D locais nos tendões.
Protocolo
Este estudo foi aprovado pelo Comitê Institucional de Cuidados e Uso de Animais da Universidade Estadual da Pensilvânia.
1. Preparação de tecidos
- Para este protocolo, colher os tendões de Aquiles de camundongos machos C57BL/6 de 2-4 meses de idade.
NOTA: Diferentes tendões ou ligamentos de camundongos ou outros pequenos animais também podem ser usados.- Faça uma incisão na pele superficial ao tendão de Aquiles para expor o tendão plantar e o tecido conjuntivo circundante. Em seguida, remova-os usando uma lâmina cirúrgica.
- Separe os músculos sóleo e gastrocnêmio expostos do membro posterior e raspe-os cuidadosamente do tendão de Aquiles com a lâmina cirúrgica
- Separe o calcâneo do resto do pé com um acessório de roda de corte em uma ferramenta rotativa.
- Coloração do tecido em 1,5 mL de uma solução de 5 μg/mL de 5-(4,6-diclorotriazinol) aminofluoresceína (DTAF) e tampão de bicarbonato de sódio 0,1 M por 20 min em um misturador rotativo à temperatura ambiente. Esta solução cora proteínas (por exemplo, matriz extracelular) no tecido.
Observação : durante esse período de 20 minutos, a etapa 1.3 deve ser concluída. - Prepare uma solução 1:1.000 de DRAQ5 em solução salina tamponada com fosfato (PBS) para manchar os núcleos. Use um misturador de vórtice para homogeneizar a solução.
- Após o período de incubação de 20 minutos na etapa 1.2, transferir o tecido da solução DTAF para a solução DRAQ5 e incubar em um espaço escuro por 10 minutos à temperatura ambiente.
2. Carregamento do tendão e aquisição de imagens
NOTA: Este protocolo requer um dispositivo de tração que pode ser montado em cima de um microscópio confocal. Para este estudo, foi utilizado o dispositivo de microtração descrito por Peterson e Szczesny13 .
- Coloque o tendão nas alças do dispositivo de carga de tração. Antes de montar as alças no dispositivo de carregamento, use pinças digitais para medir a distância entre o acessório calcâneo e a empunhadura oposta. Esta distância é o comprimento do medidor do tendão.
- Como alternativa, monte as alças no dispositivo de carregamento antes de inserir o tendão e empurre para o contato para definir a posição do motor de deslocamento zero. O deslocamento dos motores após a inserção do tendão poderia fornecer um comprimento de medidor de aderência a aderência potencialmente mais preciso.
- Monte as alças no dispositivo de carregamento, que contém PBS para manter a hidratação do tecido. Alinhe o tendão da melhor forma possível com o eixo x ou o eixo y das imagens do microscópio para que as saídas de tensão x e tensão y do algoritmo correspondam aos eixos tendinosos.
NOTA: Neste estudo, os tendões foram alinhados com o eixo x. Se não for possível alinhar perfeitamente o tendão com os eixos da imagem, então as saídas de deformação x e tensão y do algoritmo podem ser transformadas para se alinharem com os eixos longitudinais/perpendiculares do tendão usando equações de transformação de deformação padrão14. - Pré-carregue o tendão com 1 g de tensão e, se desejar, aplique carga cíclica para pré-condicionar a amostra. Neste protocolo, não foi utilizado nenhum pré-condicionamento, uma vez que o objetivo do estudo foi validar as cepas teciduais locais medidas em vez de medir as propriedades do material tecidual. Se houver interesse em medir as propriedades do material em macroescala, que dependem do histórico de carga, recomenda-se o pré-condicionamento. Após o pré-condicionamento e recuperação, reaplique uma pré-carga de 1 g.
- Se desejar, fotobranquear um conjunto de quatro linhas espaçadas a 80 μm de distância na região central do tecido (ver Peterson e Szczesny13 para mais detalhes).
NOTA: As linhas fotobranqueadas foram utilizadas para validar as medidas do algoritmo ALDIC e não são necessárias para a realização do ALDIC em si. O número e o espaçamento das linhas podem ser ajustados, e a localização das linhas deve ser escolhida para evitar quaisquer artefatos na amostra que diminuam a clareza da linha. - Repita o procedimento de fotobranqueamento nos extremos esquerdo e direito do tecido perto das alças.
- Usando o microscópio confocal, adquira imagens volumétricas (x,y: 1,25 μm/pixel, z: 2,5 μm/pixel) da fluorescência DTAF e DRAQ5 a 1 g de pré-carga.
- Realize uma rampa de deformação de 0,5%/s a 2% de deformação. Observe que a taxa de deformação e a magnitude da deformação incremental podem ser ajustadas.
- Deixe o tecido estressar relaxar por 10 min.
NOTA: A duração do relaxamento da tensão deve ser escolhida de modo que a amostra esteja sob uma carga aproximadamente quasiestática durante a aquisição da imagem. Para determinar se a duração do relaxamento da tensão é aceitável, determine a inclinação da curva força-tempo durante o minuto final do relaxamento da tensão (Figura 1 Suplementar) e multiplique essa inclinação pela duração total da imagem. Neste estudo, a força aplicada no maior incremento de deformação nunca se alterou em mais de 5%. - Tire outra imagem volumétrica do tecido após a deformação.
- Repita os passos 2.7-2.9 até que a tensão final desejada seja atingida. Neste trabalho, optou-se por um valor final de deformação de 12%.
3. Processamento de imagens
- Use ImageJ ou Fiji para criar projeções z máximas de cada imagem volumétrica do canal DRAQ5 (nuclear). Isso servirá como as imagens salpicadas 2D para o ALDIC.
- Salve as projeções z de intensidade máxima como arquivos .tiff e nomeie-as de acordo com a seguinte convenção de nomenclatura.
- Use um número como o primeiro caractere do nome da imagem.
- Faça com que o número corresponda à ordem em que as imagens serão consideradas durante a análise de deformação. Por exemplo, a primeira imagem deve começar com uma, e a segunda imagem deve começar com duas. Números diferentes podem ser escolhidos, mas eles devem aumentar sequencialmente. Um exemplo de convenção de nomenclatura é o seguinte: "0_Experiment1_MaxZProjection".
- Salve todas as projeções z de intensidade máxima renomeadas em uma pasta.
4. Instalação e aplicação do código de análise de linha fotobranqueada
NOTA: Essas etapas só são necessárias se for desejado confirmar a precisão do algoritmo ALDIC usando linhas fotobranqueadas. O código calcula a deformação de tecido local como a mudança normalizada média na distância entre cada linha fotobranqueada dentro do conjunto de linhas fotobranqueadas. Neste estudo, os valores locais médios foram então calculados em todos os conjuntos de linhas fotobranqueadas (ou seja, no centro e nas extremidades esquerda/direita) para determinar um único valor médio de deformação tecidual local para cada amostra. Este valor foi então utilizado para estimar a acurácia do algoritmo ALDIC.
- Baixe a pasta "PBL Code" do GitHub (https://github.com/Szczesnytendon/TendonStrainCalc) e mova todo o conteúdo para o diretório de trabalho no MATLAB.
- Abra o script MATLAB "Micro_Mech_Template.m".
- Pressione Executar e selecione um dos arquivos de imagem que contêm as imagens volumétricas. As imagens volumétricas podem ser qualquer um dos seguintes tipos de arquivo: .lsm, .tiff, .nd2.
- O software carregará automaticamente todas as imagens na pasta e exibirá uma imagem projetada da imagem volumétrica de referência. Quando solicitado, clique com o botão esquerdo do mouse para criar linhas de vários pontos que rastreiam as extremidades esquerda e direita do exemplo. Clique com o botão direito do mouse para encerrar uma linha. Depois que a entrada for processada, se as bordas estiverem corretas, pressione Ok para aceitar o resultado.
- Desenhe uma linha diagonal aleatória na amostra como uma linha de referência quando solicitado.
- Insira o número de linhas fotobranqueadas criadas e trace as linhas fotobranqueadas com linhas de vários pontos.
- Se o resultado for aceitável, aceite-o. Se o resultado estiver errado, ajuste-o e reprocesse-o.
- Repita a etapa 4.2 para todas as imagens e mova todas as imagens de linhas rastreadas para uma única pasta.
- Abra o script "Micro_Mech_Strain.m".
- Pressione Executar para executar o código e selecione uma das imagens salvas onde as linhas fotobranqueadas são rastreadas.
- Confirme se as imagens selecionadas que acompanham estão corretas assim que a imagem for selecionada pressionando Ok.
5. Criando imagens transformadas digitalmente
NOTA: Essas etapas só são necessárias se for desejado confirmar a precisão do algoritmo ALDIC usando imagens transformadas digitalmente. Essas imagens simulam campos de deformação 2D homogêneos de magnitude conhecida, transformando artificialmente a imagem de referência.
- Baixe o código "Digital_strain.m" do GitHub (https://github.com/Szczesnytendon/TendonStrainCalc).
- Abra e execute o código.
- Quando solicitado, insira os valores desejados para a deformação máxima aplicada, o incremento de deformação aplicada e a razão de Poisson. Pressione Ok.
NOTA: Para este experimento, a deformação máxima aplicada foi de 0,1 (10%), o incremento de deformação aplicado foi de 0,02 (2%), e foi utilizada uma razão de Poisson de 1, o que é consistente com os dados experimentais do teste de tração tendínea15,16. O código usa o imwarp da função MATLAB incorporado e os valores de entrada (por exemplo, incrementos de deformação, proporção de Poisson) para criar as imagens transformadas digitalmente. - Quando solicitado, selecione a imagem de referência não deformada.
- Para cada incremento de deformação, uma sobreposição da imagem de referência e da imagem transformada é exibida. A imagem transformada será salva no diretório sob o título "DigitallyTransformedX%Strain", onde X é o incremento de deformação.
6. Instalação e aplicação do código de cálculo e validação de tensão
- Baixe a pasta "Código de Cálculo e Validação de Deformação" do GitHub (https://github.com/Szczesnytendon/TendonStrainCalc) e mova todo o conteúdo para o diretório de trabalho do MATLAB
- Instale um compilador mex C/C++ de acordo com Yang e Bhattacharya12. As etapas estão resumidas abaixo.
- Verifique o MATLAB para ver se um compilador mex C/C++ foi instalado digitando "mex -setup" na janela de comando do MATLAB e pressionando Enter.
- Se aparecer um erro indicando que um compilador não é suportado ou presente, avance para os passos 6.3 e 6.4.
- Se não houver nenhum erro, avance para o passo 6.5
- Para baixar um compilador mex C/C++, vá para "https:/tdm-gcc.tdragon.net/" e escolha o compilador TDM-gcc.
- Instale o compilador baixado em um local conhecido.
- Retorne à janela de comando do MATLAB e digite: "setenv("MW_MINGW64_LOC","[Digite seu caminho de instalação aqui]")". Por exemplo, isso poderia ser "setenv("MW_MINGW64_LOC","C:\TDM-GCC-64")". Se este comando for executado com êxito, o compilador mex está instalado corretamente.
- Digite o script de função "main_aldic.m" e altere a linha 22 para corresponder ao comando executado na etapa 6.5.
- Abra o script "Strain_calc_and_validate.m".
- Pressione Executar para iniciar a análise da imagem.
- Quando solicitado, altere os valores para os parâmetros ALDIC conforme desejado.
Observação : O tamanho da janela deve ser de 0,25 a 1 vezes o tamanho do subconjunto. Para obter mais informações sobre as opções de parâmetros, consulte o manual do usuário on-line: (https://www.researchgate.net/publication/344796296_Augmented_Lagrangian_Digital
_Image_Correlation_AL-DIC_Code_Manual).- Os seguintes valores foram utilizados neste estudo:
Tamanho do subconjunto (pixels): 20
Tamanho da janela (pixels): 10
Método para resolver ALDIC: Diferença Finita (1)
A computação paralela não foi utilizada (1)
Método para calcular a adivinhação inicial: Pesquisa multigrid com base na pirâmide de imagem (0)
- Os seguintes valores foram utilizados neste estudo:
- Quando solicitado, marque a caixa de seleção "Sim" para que o algoritmo salve automaticamente o valor médio, o desvio padrão e os mapas 2D para a coleção desejada de variáveis (por exemplo, deformação x, deformação y, deformação de cisalhamento, regiões defeituosas, etc.). Selecione quais variáveis devem ser salvas e pressione Ok.
- Quando solicitado, altere os parâmetros conforme desejado.
- Os seguintes valores foram utilizados neste experimento:
Pontos circundantes para calcular a deformação (numP): 12
Coeficiente de correlação para identificação de região ruim (corr_threshold): 0,5
Tamanho da sub-região (pixels) para análise de região incorreta (Subtamanho): 32
- Os seguintes valores foram utilizados neste experimento:
- Quando solicitado, selecione a pasta que contém as projeções z de intensidade máxima renomeadas. Observe que o software executa automaticamente ALDIC incremental para determinar os campos de deformação das imagens deformadas. Ou seja, cada imagem deformada serve como a nova imagem de "referência" para a próxima imagem deformada. Isso melhora a precisão dos resultados (Figura 2 Suplementar) em comparação com a realização de ALDIC cumulativo, onde cada imagem deformada é comparada com a imagem de referência original (0% de deformação). Para executar uma análise cumulativa, carregue as imagens, mas selecione apenas a imagem de referência original e a imagem deformada de interesse.
NOTA: A deformação normal é calculada como λ - 1, onde λ é o estiramento do tecido. O estiramento do tecido é calculado de acordo com , onde N = [1 0]T ou [0 1]T para a direção x e direção y, respectivamente, e C = F T F, onde F é o gradiente de deformação calculado usando pontos "numP" em torno de cada saída de ponto de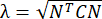 dados pelo algoritmo ALDIC. A deformação de cisalhamento é calculada como
dados pelo algoritmo ALDIC. A deformação de cisalhamento é calculada como 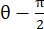 , onde
, onde 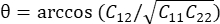 .
. - Quando solicitado, clique com o botão esquerdo do mouse para criar um polígono de quatro pontos para definir a região de interesse para medir as deformação. Comece com o ponto no canto superior esquerdo e atribua os pontos subsequentes no sentido horário.
NOTA: A variável "Armazenamento" salva no espaço de trabalho do MATLAB contém todos os valores para a deformação x média, o desvio padrão da deformação x, a deformação y média, o desvio padrão da deformação y, a deformação média do cisalhamento, o desvio padrão da deformação de cisalhamento e a porcentagem de regiões defeituosas. As regiões ruins são definidas de acordo com a análise do coeficiente de correlação dentro da região de interesse selecionada na etapa 6.13. A pasta "NuclearTrackingResults" (que pode ser renomeada ajustando as linhas 555 e 556) armazena todos os gráficos especificados na etapa 6.10. Esta pasta também contém um arquivo de planilha com o nome "Resultados", que armazena todas as médias e desvios padrão especificados na etapa 6.10.
Resultados
Antes de analisar os campos de deformação em amostras de tecido reais, o protocolo ALDIC foi validado pela primeira vez usando imagens digitalmente tensas / transformadas de núcleos dentro dos tendões de Aquiles de camundongos. Especificamente, as imagens foram transformadas para produzir digitalmente cepas uniformes na direção x de 2%, 4%, 6%, 8% e 10% de deformação com uma razão de Poisson simulada de 115,16. A acurácia do algoritmo ALDIC foi então a...
Discussão
O objetivo deste trabalho foi fornecer um método validado de código aberto para medir os campos de deformação 2D em tendões sob carga de tração. A fundação do software foi baseada em um algoritmo ALDIC disponível publicamente12. Esse algoritmo foi incorporado em um código MATLAB maior com a funcionalidade adicional de análise de deformação incremental (versus cumulativa). Este algoritmo adaptado foi então aplicado ao teste de tração de tendões, e sua precisão foi avaliada por du...
Divulgações
Todos os autores não têm conflitos de interesse para divulgar.
Agradecimentos
Este trabalho foi financiado pelos Institutos Nacionais de Saúde (R21 AR079095) e pela National Science Foundation (2142627).
Materiais
| Name | Company | Catalog Number | Comments |
| 5-DTAF (5-(4,6-Dichlorotriazinyl) Aminofluorescein), single isomer | ThermoFisher | D16 | |
| Calipers | Mitutoyo | 500-196-30 | |
| Confocal Microscope | Nikon | A1R HD | |
| Corning LSE Vortex Mixer | Coning | 6775 | |
| DRAQ5 Fluorescent Probe Solution (5 mM) | ThermoFisher | 62554 | |
| MATLAB | MathWorks | R2022b | |
| Tensile Loading Device | N/A | N/A | Tensile loading device described in Peterson et al, 2020. (ref 13) |
| Tube Revolver Rotator | ThermoFisher | 88881001 |
Referências
- Devkota, A. C. Distributing a fixed amount of cyclic loading to tendon explants over longer periods induces greater cellular and mechanical responses. Journal of Orthopaedic Research. 11 (4), 1609-1612 (2007).
- Sun, H. B., et al. Cycle-dependent matrix remodeling gene expression response in fatigue-loaded rat patellar tendons. Journal of Orthopaedic Research. 28 (10), 1380-1386 (2010).
- Shepherd, J. H., Screen, H. R. C. Fatigue loading of tendon. International Journal of Experimental Pathology. 94 (4), 260-270 (2013).
- Paschall, L., Pedaprolu, K., Carrozzi, S., Dhawan, A., Szczesny, S. Mechanical stimulation as both the cause and the cure of tendon and ligament injuries. Regenerative Rehabilitation: From Basic Science to the Clinic. , 359-386 (2022).
- Andarawis-Puri, N., Ricchetti, E. T., Soslowsky, L. J. Rotator cuff tendon strain correlates with tear propagation. Journal of Biomechanics. 42 (2), 158-163 (2009).
- Cheng, V. W. T., Screen, H. R. C. The micro-structural strain response of tendon. Journal of Materials Science. 42 (21), 8957-8965 (2007).
- Luyckx, T., et al. Digital image correlation as a tool for three-dimensional strain analysis in human tendon tissue. Journal of Experimental Orthopaedics. 1 (1), 7 (2014).
- Duncan, N. A., Bruehlmann, S. B., Hunter, C. J., Shao, X., Kelly, E. J. In situ cell-matrix mechanics in tendon fascicles and seeded collagen gels: Implications for the multiscale design of biomaterials. Computer Methods in Biomechanics and Biomedical Engineering. 17 (1), 39-47 (2014).
- Arnoczky, S. P., Lavagnino, M., Whallon, J. H., Hoonjan, A. In situ cell nucleus deformation in tendons under tensile load; A morphological analysis using confocal laser microscopy. Journal of Orthopaedic Research. 20 (1), 29-35 (2002).
- Screen, H. R. C., Bader, D. L., Lee, D. A., Shelton, J. C. Local strain measurement within tendon. Strain. 40 (4), 157-163 (2004).
- Fung, A. K., Paredes, J. J., Andarawis-Puri, N. Novel image analysis methods for quantification of in situ 3-D tendon cell and matrix strain. Journal of Biomechanics. 67, 184-189 (2018).
- Yang, J., Bhattacharya, K. Augmented Lagrangian digital image correlation. Experimental Mechanics. 59 (2), 187-205 (2019).
- Peterson, B. E., Szczesny, S. E. Dependence of tendon multiscale mechanics on sample gauge length is consistent with discontinuous collagen fibrils. Acta Biomaterialia. 117, 302-309 (2020).
- Humphrey, J. D., O'Rourke, S. L. . An Introduction to Biomechanics. , (2015).
- Reese, S. P., Weiss, J. A. Tendon fascicles exhibit a linear correlation between Poisson's ratio and force during uniaxial stress relaxation. Journal of Biomechanical Engineering. 135 (3), 34501 (2013).
- Ahmadzadeh, H., Freedman, B. R., Connizzo, B. K., Soslowsky, L. J., Shenoy, V. B. Micromechanical poroelastic finite element and shear-lag models of tendon predict large strain dependent Poisson's ratios and fluid expulsion under tensile loading. Acta Biomaterialia. 22, 83-91 (2015).
- Szczesny, S. E., Elliott, D. M. Interfibrillar shear stress is the loading mechanism of collagen fibrils in tendon. Acta Biomaterialia. 10 (6), 2582-2590 (2014).
- Han, W. M., et al. Macro- to microscale strain transfer in fibrous tissues is heterogeneous and tissue-specific. Biophysical Journal. 105 (3), 807-817 (2013).
- Pedaprolu, K., Szczesny, S. E. A novel, open-source, low-cost bioreactor for load-controlled cyclic loading of tendon explants. Journal of Biomechanical Engineering. 144 (8), 084505 (2022).
- Gatt, R., et al. Negative Poisson's ratios in tendons: An unexpected mechanical response. Acta Biomaterialia. 24, 201-208 (2015).
Reimpressões e Permissões
Solicitar permissão para reutilizar o texto ou figuras deste artigo JoVE
Solicitar PermissãoExplore Mais Artigos
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Todos os direitos reservados