Для просмотра этого контента требуется подписка на Jove Войдите в систему или начните бесплатную пробную версию.
Method Article
Свойств поверхности синтезированных нанопористого углерода и кремния матрицы
В этой статье
Резюме
Здесь мы приводим синтеза и характеристика приказал нанопористого углерода (с размером пор 4.6 Нм) и SBA-15 (с размером пор 5,3 Нм). Работа описывает поверхность и текстурные свойства нанопористого молекулярного сита, их смачиваемости и плавления поведение D2O, замкнутые в материалах.
Аннотация
В этой работе, мы сообщаем, синтез и характеристика приказал нанопористого углеродного материала (также называемые приказал мезопористых углеродного материала [ОМС]) с 4.6 Нм поры и приказал кремнезема пористой матрицы, SBA-15, с размером пор 5,3 Нм. Эта работа описывает свойства поверхности нанопористого молекулярного сита, их смачиваемости и плавления поведение D2O помещены в по-разному приказал пористых материалов с аналогичными размерами пор. Для этой цели ОМС и SBA-15 с весьма упорядоченный нанопористого, что структуры являются синтезированных через пропиткой кремний матрицы, применяя предвестником углерода и золь гель методом, соответственно. Пористая структура исследуемых систем характеризуется анализ адсорбции десорбции N2 в 77 K. Чтобы определить электрохимический характер поверхности синтезированных материалов, проводятся измерения потенциометрического титрования; полученные результаты для ОМС показывает значительное рНpzc сдвиг в сторону более высокие значения рН, по отношению к SBA-15. Это предполагает, что расследование ОМС поверхностные свойства, относящиеся к кислородосодержащие функциональных групп. Для описания свойств поверхности материалов, также определяются контактные углы жидкостей, проникая изучал пористых кровати. Метод капиллярного поднятия подтвердили увеличение смачиваемости кремнезема стены относительно стены углерода и влияние шероховатостью поровое на взаимодействие жидкости/стены, которая гораздо более выраженным для кремнезема чем для углерода мезопор. Мы также изучили плавления поведение D2O, помещены в ОМС и SBA-15, применяя метод диэлектрика. Результаты показывают, что депрессия температуры плавления D2O в порах ОМС около 15 K выше относительно депрессии температуры плавления в СБА-15 поры с сопоставимого размера 5 Нм. Это вызвано влиянием адсорбата/адсорбента взаимодействий изученных матрицах.
Введение
В 1992 году приказал нанопористого кремнеземные материалы были получены в первый раз, используя органические шаблон; с тех пор большое количество публикаций, связанных с различными аспектами этих структур, методов синтеза, исследование их свойств, их модификации, и различных приложений появились в литературе1,2 ,3. Интерес к SBA-15 нанопористого кремния матрица4 объясняется их уникальные качества: большую площадь поверхности, широкие поры с распределения размеров Единообразного поровое и хорошие химических и механических свойств. Нанопористого кремнеземные материалы с цилиндрическим поры, например SBA-155, часто используются в качестве пористой матрицы для катализаторов, как они эффективные катализаторы в органических реакций6,7. Материал может быть синтезировано с широкий спектр методов, которые могут повлиять на их характеристики8,9,10. Таким образом, важно оптимизировать эти методы для потенциального применения во многих областях: электрохимических устройствах, нанотехнологии, биологии и медицины, систем доставки, наркотиков или адгезии и трибологии. В настоящем исследовании, представлены два различных типов нанопористого структур, а именно кремния и углерода пористых матриц. Для сравнения их свойства, SBA-15 матрица синтезируется с использованием золь гель методом, и приказал нанопористого углеродного материала готовится путем пропитки результирующей матрицы кремния с предвестником углерода.
Пористый углерод материалы важны для многих приборов из-за их высокой поверхности и их уникальные и четко определенные физико-химических свойств6,,1112. Типичные подготовка приводит в материалах со случайно распределенными пористости и неупорядоченной структурой; Существует также ограниченные возможности для изменения параметров общего поры, и полученные таким образом, структуры с распределением размера относительно широкие поры13. Эта возможность расширена для нанопористого углеродных материалов с высокой площади поверхности и приказал систем Нанопоры. Более предсказуемое, геометрии и больше контроля физико-химических процессов внутри порового пространства имеют важное значение во многих приложениях: как катализаторов, системы разделения СМИ, передовых электронных материалов и nanoreactors в многих научных областях14 , 15.
Чтобы получить Пористый углерод реплик, приказал силикатов может выступать в качестве твердых матрицы, которому непосредственно вводятся углерода прекурсоров. Этот метод можно разделить на несколько этапов: выбор приказал кремнезема материала; осаждение углерода прекурсоров в матрице кремния; Цементация; затем удаление матрицы кремнезема. Много различных типов углеродистых материалов могут быть получены этим методом, но не все непористых материалов имеют упорядоченную структуру. Важным элементом этого процесса является выбор подходящих матрицы, чьи Нанопоры должны образовывать стабильное, трехмерные структуры16.
В этой работе исследовано влияние типа стен поры на поверхности свойств синтезированных нанопористого матриц. Свойств поверхности материала ОМС отражаются свойства поверхности кремнезема аналоговый (SBA-15) по ОМС. Текстурные и структурные свойства обоих типов материалов (ОМС и SBA-15) характеризуются низкой температуры N2 Адсорбция/десорбция измерений (на 77 K), просвечивающей электронной микроскопии (ТЕА) и энергии энергодисперсионный рентгеновский анализ ( EDX).
Адсорбция/десорбция измерение низкотемпературных газов является одним из самых важных методов при характеристике пористых материалов. Газ азот используется как адсорбата из-за его высокой чистоты и возможность для создания сильного взаимодействия с твердые адсорбенты. Важные преимущества этой техники являются удобный склад и относительно легко процедур обработки данных. Определение изотермы адсорбции/десорбции азота основан на накопление молекул адсорбата на поверхности твердого адсорбента на 77 K в широком диапазоне давления (0P/P). Барретт, Джойнер и Halenda (BJH) порядок расчета распределением пор по размерам от экспериментальной изотермы адсорбции и десорбции применяется. Наиболее важные предположения метода BJH включают в себя плоскую поверхность и равномерное распределение адсорбата на исследуемой поверхности. Однако эта теория основана на уравнении Кельвин, и он остается наиболее широко используемым способом расчета распределением пор по размерам в диапазоне мезопористых.
Чтобы оценить электрохимический характер образцов, применяется метод потенциометрического титрования. Химии поверхности материала зависит от поверхности заряда, связанных с наличием гетероатомами или функциональных групп на поверхности. Свойств поверхности также исследуются путем анализа угол контакта. Смачиваемости внутри поры, обеспечивает сведения о взаимодействии адсорбата адсорбент. С помощью метода диэлектрической релаксационной спектроскопии (DRS) изучается влияние неровностей стены на температуру плавления воды в обоих образцах. Измерения диэлектрической постоянной позволяют расследования плавления явления как поляризуемость жидкости и твердых фаз отличаются друг от друга. Изменение наклона температурная зависимость емкости показывает, что таяние происходит в системе.
протокол
1. Подготовка материалов ОМС
-
Синтез кремнезема матрицы как прекурсор ОМС
- Подготовить 360 mL 1.6 М HCl, добавляя 50 мл HCl (36-38%) в раунд нижней колбе 500 мл и, затем, добавляя 310 мл ультрачистая вода (резистивность 18.2 MΩ·cm).
- К этому, добавить 10 g PE 10500 полимер (6.500 г/моль).
- Место колбу в ультразвуковой ванне. Нагрейте раствор до 35 ° C и перемешать до тех пор, пока полностью растворяется твердого полимера, делая однородной смеси.
- Добавьте 10 g 1,3,5-trimethylbenzene в колбу и перемешать содержимое (перемешивания скоростью 220 об/мин), поддерживая его на 35 ° C в водяной бане.
- После перемешивания в течение 30 мин, добавьте 34 g orthosilicate тетраэтилсвинца (Теос) в колбу. Добавьте Теос медленно и каплям при постоянном перемешивании. Убедитесь, что она занимает 10 минут, чтобы добавить 34 g Теос.
- Перемешайте смесь решение снова для 20 h при той же температуре (35 ° C).
- Передавать содержимое колбы в картридж политетрафторэтилена и поместите его в автоклаве. Оставьте раствор для 24 h на 90 ° C.
- Фильтровать результирующий осадок, используя воронка Бюхнера и мыть его с дистиллированной водой, используя по меньшей мере 1 л.
- Полученные твердых при комнатной температуре в сухом и применить термической обработки образца на 500 ° C, с использованием муфельные печи в атмосфере воздуха на 6 ч.
-
Пропитка результирующей матрицы кремнезема, используя предвестником углерода
- Подготовить пропитки решения (IS1 и IS2) с соответствующей пропорции воды, 3 M серной кислоты (VI) и сахара (глюкозы), где глюкозы играет роль углерода прекурсоров и серная кислота выступает в качестве катализатора.
Предупреждение: Серная кислота является высокотоксичным, он вызывает серьезные ожоги кожи и повреждение глаз.- Подготовьте IS1. Для каждого грамма кремния смесь 5 g воды, 0,14 g 3 M серной кислоты (VI) и 1,25 г сахара.
- Подготовьте IS2. Для каждого грамма кремния смесь 5 g воды, 0,08 г 3 M серной кислоты (VI) и 0,75 г сахара.
- Место материала кремния (1 g) и приготовленный раствор IS1 углерода прекурсоров и катализатора в 500 мл флакон. Нагрейте смесь в вакуумной сушкой при 100 ° C на 6 ч.
Примечание: В этом шаге, используйте только IS1. IS2 должны применяться в следующем шаге. - Добавьте IS2 в смеси в вакууме, сушка (для раствора с прекурсорами частично обугленный углерода). Нагрейте смесь снова в вакуумной сушкой при 160 ° C в течение 12 ч.
- Подготовить пропитки решения (IS1 и IS2) с соответствующей пропорции воды, 3 M серной кислоты (VI) и сахара (глюкозы), где глюкозы играет роль углерода прекурсоров и серная кислота выступает в качестве катализатора.
-
Цементация и закалка
- Передать полученный композита раствор для дробления крупных частиц и однородности материала.
- Разместите полученный продукт в топку потока и нагреть ее до 700 ° C (со скоростью нагревания 2,5 ° C/мин) и тепла для 6 ч при этой температуре. Нагрейте материал в атмосфере азота.
- Дайте раствору остыть перед открытием печи.
-
Удаление матрицы путем травления кремния
- Подготовка 100 мл травления решение (ES). Смешайте 50 мл 95% спирта этилового и 50 мл воды. Добавление 7 g гидроксида калия и перемешать до тех пор, пока она растворяется.
- Все полученные обугленный материала (по крайней мере 1 g) в 250 мл раунд нижней колбе и добавить 100 мл ES.
- Поставки системы с Дефлегматоры и магнитную мешалку и тепла до кипения, постоянно помешивая. Кипятите смесь на 1 ч.
- Передать полученный материал воронка Бюхнера, мыть с по крайней мере 4 Л дистиллированной воды и высушите его.
2. подготовка матрицы SBA-15 кремнезема
- Синтезировать матрицу кремнезема.
- Подготовка 150 мл 1,6 М HCl.
- Растворите 4 g PE 6400 полимера (EO13PO70EO13) в 150 мл раствора кислоты в раунд нижней колбе.
- Место колбу в ультразвуковой ванне. Нагрейте раствор до 40 ° C и размешать так что полимера может распустить (по крайней мере за 30 минут).
- Медленно добавьте 8.5 g Теос в колбу, каплям, при постоянном перемешивании. Перемешайте смесь раствора для 24 ч при той же температуре (40 ° C).
- Передавать содержимое колбы политетрафторэтилена картриджа. Оставьте раствор для 24 h в 120 ° C духовке.
- Фильтровать результирующий осадок, используя воронка Бюхнера и мыть его с дистиллированной водой (по крайней мере 1 Л).
- Сухие полученные твердых при комнатной температуре и огарка за 6 ч при температуре 600 ° C, с использованием муфельные печи в атмосфере воздуха.
3. методы характеризации
- Азота низкотемпературная Адсорбция/десорбция измерения
- Используйте анализатор автоматический сорбции для получения N2 изотермы адсорбции/десорбции в 77 K.
- Используйте соответствующие стеклянная трубка для азота сорбции измерений. Перед добавлением пористый образец в стеклянной трубки, очистить трубу в ультразвуковую моечную машину и промойте его первый дистиллированной водой и, далее, с безводного этилового спирта.
- Нагрейте стеклянную трубку при 150 ° C 3 h и заполнить трубу с сжатым азотом. Вес пустой стеклотрубки в условиях азота до измерения для минимизации веса ошибка.
- Поместите образец в стеклянную трубку и весят общая масса (масса образца с стеклянной трубки).
- До измерения Дега образца. Место стеклянную трубку с образцом в дегазации порт анализатор сорбции. Применяются следующие условия процесса: давление менее 0,01 мм рт.ст., 423 K, температура и продолжительность 24 ч. В дегазации порту Подключите образец в вакууме и тепло его до заданной температуры (423 K). После дегазации, заполните образца с азотом и передача его в порт анализа.
- Просвечивающей электронной микроскопии
- Используйте ТЕА микроскоп с 120 кв (для SBA-15) и 200 кв (для материала ОМС) ускоряющего напряжения для сбора ТЕА изображения хорошего качества.
- Для подготовки монодисперсных фильм образца, разогнать образца (1 мг) в этаноле (1 мл). Выполните процедуру дисперсии в пробки microcentrifuge, поместив его в ультразвуковой ванне на 3 мин.
- Место два капли дисперсии на ТЕА медной сетки с использованием микропипеткой. Сетке ТЕА передать Микроскоп ТЕА и начать изображений ТЕА.
- Энергии дисперсионных рентгеновская спектроскопия
- Используйте сканирующий электронный микроскоп оснащен детектор рентгеновского излучения для получения энергии энергодисперсионный рентгеновский спектр образцов.
- Применить ускорение напряжения 15 кв урожай спектра. Выберите кремния как элемент оптимизации для SBA-15 и углерода для образца ОМС.
- Потенциометрическое титрование измерение
- Используйте автоматическое бюретки для выполнения эксперимента потенциометрического титрования. Добавьте титранта в малых и контролируемых порций (по словам титрования программного обеспечения и процедуры). Обеспечивают наименьший прирост, по крайней мере 1 мкл, путем автоматического дозирования активизирована.
- Разогнать 0,1 г образца в 30 мл раствора электролита (водный раствор 0,1 М NaCl). Используйте магнитную мешалку и изотермических условиях (293 ± 0,1 K) во время процедуры дисперсии.
- Добавьте 1-2 мл титранта (0,1 М раствор NaOH) подвеска.
Примечание: Выполнение добавления в небольших аликвоты (каждый, чтобы быть около 0,05 мл). Автоматическое бюретки процедура должна обеспечить по меньшей мере десяток экспериментальных точек в диапазоне pH от 1 до 14. - Вычислите поверхностная плотность заряда Qs, с помощью следующей формулы.
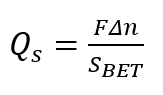 (1)
(1)
Здесь,
Δn = изменение в балансе H+/OH– , сокращены на массы образца;
S-ставка = Brunauer-Эмметт-кассир (BET) площадь поверхности пористой твердом состоянии;
F = число Фарадея.
- Капиллярный подъем метод для измерения смачиваемость
- Для определения угла контакта внутри поры, исследованных образцов, используйте метод капиллярного поднятия.
Примечание: Этот метод основан на измерении массового подъема жидкости, которая проникает пористых кровать, как функция времени. Основные этого метода предполагается, основывается на факте, что проникающая жидкость продвигается в столбце пористых и что эта колонна состоит из межзерновой капилляров с определенным средний радиус. Таким образом каждый отношение производных для одного капиллярные действителен для слоя пористого порошка. В одной вертикальной капилляр смачивающая жидкость плывет против гравитационных сил вследствие разности давления жидкости и пара в поры (капиллярное давление). В этом смысле, проникновение жидкости в пористых кровать позволяет определить динамический продвижении угол контакта внутри поры. - Примените изменение Уошберн уравнение17,18, выражено следующим образом.
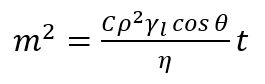 (2)
(2)
Здесь,
m = масса измеряемой жидкости;
C = геометрических параметров зависит от распределения, форма и размер поры;
Ρ = плотность;
Γl= поверхностное натяжение;
Η = вязкость проникающей жидкости;
Θ = угол контакта;
t = время. - Используя уравнение (2), оцените значения выдвигаясь контактных углов внутри поры, изучал.
- Подготовьте Тензиометр силы. Для порошков используйте стеклянную трубку с диаметром 3 мм и керамические агломерата; для жидкости используйте судно с диаметром 22 мм и максимальный объём 10 мл.
- Мера 0,017 г образца.
- Запустите программу компьютера, подключенных к Тензиометр. Поставьте сосуд с жидкостью на сцене, двигателем и приостановить стеклянную трубку с образцом на электронные весы.
- Запустите двигатель и начать приближается к жидкости в сосуде с образца с постоянной низкой скоростью 10 мм/мин; Установите глубину погружения образец трубки в жидкости равен 1 мм.
- С этого момента, зависимость m2 = f(t) регистры в компьютерной программе.
- Остановить эксперимент когда зависимость m2 = f(t) начинает показать характерные плато.
- Проверка на точность, повторив эту процедуру 3 x - 5 x.
- Для определения угла контакта внутри поры, исследованных образцов, используйте метод капиллярного поднятия.
- Диэлектрической релаксационной спектроскопии
- Чтобы описать плавления поведение замкнутые воды внутри изучал пористых матриц, выполните измерения температуры электрической емкости C образца в параллельной пластине конденсатор изготовлен из нержавеющей стали19, 20 , 21. чтобы измерить емкость C как функция температуры и частоты прикладной циклических электрического поля, используйте импеданс анализатора.
Примечание: Комплекс электрическая проницаемость определяется как ε * = ε' + iε'', где ε' = C/C0 является реальной и ε'' = tgδ·ε' является мнимой частью диэлектрическая проницаемость, где C0 емкость пустая конденсатор и tgδ являются диэлектрических потерь. - Положите измеряемых образца в конденсаторе пластины.
- Выберите диапазон частот от 100 Гц до 1 МГц и температуре от 140 K до 305 K. управления уровень температуры изменения с контроллером температуры; Установите уровень температуры как равным 0,8 K/мин во время охлаждения и 0,6 K/мин во время нагрева.
- Чтобы описать плавления поведение замкнутые воды внутри изучал пористых матриц, выполните измерения температуры электрической емкости C образца в параллельной пластине конденсатор изготовлен из нержавеющей стали19, 20 , 21. чтобы измерить емкость C как функция температуры и частоты прикладной циклических электрического поля, используйте импеданс анализатора.
Результаты
Чтобы охарактеризовать пористая структура исследуемых образцов ОМС и SBA-15, N2 адсорбции десорбции изотермы были записаны в 77 K. Экспериментальный N2 газ адсорбции десорбции изотермы, характеризующие исследуемых систем, а также распределением размера поры (PSD...
Обсуждение
Важнейшие шаги в ходе подготовки заказанных мезопористых углеродных материалов включают в себя подготовку приказал мезопористых кремнеземные материалы как шаблон с четко определенных структурных свойств, которые влияют на свойства окончательного материалов и закалки/карбонизации ...
Раскрытие информации
Авторы не имеют ничего сообщать.
Благодарности
Авторы хотели бы поблагодарить Национальный центр науки для оказания финансовой поддержки с Грант не. ДЕК-2013/09/B/ST4/03711 и УМО-2016/22/ST4/00092. Авторы также признательны за частичную поддержку Польши оперативной программы Человеческого капитала PO KL 4.1.1, а также начиная с национального центра исследований и развития, под исследовательский грант нет. PBS1/A9/13/2012. Авторы особенно признательны за профессор L. Hołysz из отдела отличные явления, химический факультет, Университет Марии Кюри-Склодовской, Люблин, Польша, за ее доброту и позволяя измерения смачиваемости в СБА-15 Нанопоры.
Материалы
| Name | Company | Catalog Number | Comments |
| 1,3,5-trimethylbenzene | Sigma-Aldrich, Poland | M7200 Sigma-Aldrich | Mesitylene, also known as 1,3,5-trimethylbenzene, reagent grade, assay: 98%. |
| anhydrous ethanol | POCH, Avantor Performance Materials Poland S.A. | 396480111 | Assay, min. 99.8 %, analysis-pur (a.p.) |
| ASAP 2020. Accelerated Surface Area and Porosimetry System | Micromeritics Instrument Corporation, Norcross, GA, USA | Samples were outgassed before analysis at 120 oC for 24 hours in degas port of analyzer. The dead space volume was measured for calibration on experimental measurement using helium as a adsorbate. | |
| Automatic burette Dosimat 665 | Metrohm, Switzerland | The surface charge properties were experimentally determined by potentiometric titration of the suspension at constant temperature 20°C maintained by the thermostatic device. Prior to potentiometric titration measurements, the solid samples were dried by 24 hours at 120 oC. The initial pH was established by addition of 0.3 cm3 of 0.2 mol/L HCl. T The 0.1 mol/L NaOH solution was used as a titrant, added gradually by using automatic burette. | |
| Digital pH-meter pHm-240 | Radiometer, Copenhagen | Device coupled with automatic burette | |
| ethyl alcohol | POCH, Avantor Performance Materials Poland S.A. | 396420420 | Assay, min. 96 %.analysis-pur (a.p.) |
| glucose | POCH, Avantor Performance Materials Poland S.A. | 459560448 | assay 99.5% |
| Hydrochloric acid | POCH, Avantor Performance Materials Poland S.A. | 575283115 | Hydrochloric acid, 35 - 38% analysis-pur (a.p.) |
| HOPG graphite substrate | Spi Supplies | LOT#1170906 | HOPG SPI-2 Grade, 20x20x1 mm |
| Impedance analyzer Solartron 1260 | Solartron | ||
| Pluronic PE 6400 polymer | BASF (Polska) | (EO13PO70EO13) | |
| Pluronic PE10500 | BASF Canada Inc. | Molar mass 6500 g/mol | |
| potassium hydroxide | Sigma-Aldrich, Poland | P5958 Sigma-Aldrich | BioXtra, ≥85% KOH basis |
| SEM microscope | JEOL JSM-7001F | Scanning Electron Microscope with EDS detector | |
| Sigma Force Tensiometer 701 | KSV, Sigma701, Biolin Scientific | force tensiometer | |
| Sulfuric acid (VI) | POCH, Avantor Performance Materials Poland S.A. | 575000115 | |
| surface glass type KS 324 Kavalier | Megan Poland | 80 % of SiO2 , 11% of Na2O and 9% of CaO | |
| Tecnai G2 T20 X-TWIN | FEI, USA | Transmission Electron Microscope with EDX detector. | |
| TEM microscope | JEOL JEM-1400 | ||
| temperature controller ITC503 | Oxford Instruments | ||
| Tetraethylorthosilicate | Sigma-Aldrich, Poland | 131903 | Tetraethyl silicate, TEOS, reagent grade, assay 98% |
| Ultrapure water | Millipore, Merck KGaA, Darmstadt, Germany | SIMSV0001 | Simplicity Water Purification SystemUltrapure Water: 18.2 MegOhm·cm, TOC: <5 ppb |
Ссылки
- Tao, Y., Kanoh, H., Abrams, L., Kaneko, K. Mesopore-Modified Zeolites: Preparation, Characterization, and Applications. Chemical Reviews. , 896-910 (2006).
- Wan, Y., Zhao, D. On the Controllable Soft-Templating Approach to Mesoporous Silicates. Chemical Reviews. 107, 2821-2860 (2007).
- Khder, A. E. S., Hassan, H. M. A., El-Shall, M. S. Acid catalyzed organic transformations by heteropolytungstophosphoric acid supported on MCM-41. Applied Catalysis A. 411, 77-86 (2012).
- Zhao, D. D., et al. Triblock Copolymer Syntheses of Mesoporous Silica with Periodic 50 to 300 Angstrom Pores. Science. 279, 548-552 (1998).
- Linssen, T., Cassiers, K., Cool, P., Vansant, E. Mesoporous templated silicates: an overview of their synthesis, catalytic activation and evaluation of the stability. Advances in Colloid and Interface Science. 103, 121-147 (2003).
- Eftekhari, A., Fan, Z. Ordered mesoporous carbon and its applications for electrochemical energy storage and conversion. Materials Chemistry Frontiers. 1, 1001-1027 (2017).
- Sing, K. Characterization of porous materials: past, present and future. Colloids and Surfaces A. 241, 3-7 (2004).
- Huo, Q., Margolese, D. I. Generalized synthesis of periodic surfactant/inorganic composite materials. Nature. 368, 317-321 (1994).
- Selvaraj, M., Kawi, S., Park, D. W., Ha, C. S. Synthesis and characterization of GaSBA-15: Effect of synthesis parameters and hydrothermal stability. Microporous and Mesoporous Materials. , 586-595 (2009).
- Leonard, A., et al. Toward a better control of internal structure and external morphology of mesoporous silicas synthesized using a nonionic surfactant. Langmuir. 19, 5484-5490 (2003).
- Liang, C., Li, Z., Dai, S. Mesoporous Carbon Materials: Synthesis and Modification. Angewandte Chemie International Edition. 47, 3696-3717 (2008).
- Babić, B., et al. New mesoporous carbon materials synthesized by a templating procedure. Ceramics International. 39 (4), 4035-4043 (2013).
- Allen, S. J., Whitten, L., Mckay, G. The Production and Characterization of Activated Carbons: A Review. Developments in Chemical Engineering and Mineral Processing. 6, 231-261 (1998).
- Kwak, G., et al. Preparation Method of Co3O4 Nanoparticles Using Ordered Mesoporous Carbons as a Template and Their Application for Fischer-Tropsch Synthesis. The Journal of Physical Chemistry C. 117 (4), 1773-1779 (2013).
- Koo, H. M., et al. Effect of the ordered meso-macroporous structure of Co/SiO2 on the enhanced activity of hydrogenation of CO to hydrocarbons. Catalysis Science and Technology. 6, 4221-4231 (2016).
- Jun, S., Joo, S. H., Ryoo, R., Kruk, M., Jaroniec, M. Synthesis of New, Nanoporous Carbon with Hexagonally Ordered Mesostructure. Journal of the American Chemical Society. 122 (43), 10712-10713 (2000).
- Washburn, E. W. The dynamics of capillary flow. Physical Review Series2. 17, 273 (1921).
- Śliwińska-Bartkowiak, M., Sterczyńska, A., Long, Y., Gubbins, K. E. Influence of Microroughness on the Wetting Properties of Nano-Porous Silica Matrices. Molecular Physics. 112, 2365-2371 (2014).
- Śliwińska-Bartkowiak, M., et al. Melting/freezing behavior of a fluid confined in porous glasses and MCM-41: dielectric spectroscopy and molecular simulation. Journal of Chemical Physics. 114, 950-962 (2001).
- Coasne, B., Czwartos, J., Śliwińska-Bartkowiak, M., Gubbins, K. E. Freezing of mixtures confined in silica nanopores: experiment and molecular simulation. Journal of Chemical Physics. 133, 084701-084709 (2010).
- Chełkowski, A. . Dielectric Physics. , (1990).
- Radhakrishnan, R., Gubbins, K. E., Śliwińska-Bartkowiak, M. Global phase diagrams for freezing in porous media. Journal of Chemical Physics. 116, 1147-1155 (2002).
- Gubbins, K. E., Long, Y., Śliwińska-Bartkowiak, M. Thermodynamics of confined nano-phases. Journal of Chemical Thermodynamics. 74, 169-183 (2014).
- Radhakrishnan, R., Gubbins, K. E., Śliwińska-Bartkowiak, M. Effect of the fluid-wall interaction on freezing of confined fluids: Toward the development of a global phase diagram. Journal of Chemical Physics. 112, 11048 (2000).
- Cassie, A. B. D., Baxter, S. Wettability of porous surfaces. Transactions of the Faraday Society. 40, 546 (1944).
- Sing, K. Adsorption methods for the characterization of porous materials. Advances in Colloid and Interface Science. 76, 3-11 (1998).
- Sing, K. The use of nitrogen adsorption for the characterisation of porous materials. Colloids and Surfaces A. 187, 3-9 (2001).
- Yu, C., Fan, J., Tian, B., Zhao, D. Morphology Development of Mesoporous Materials: a Colloidal Phase Separation Mechanism. Chemistry of Materials. 16 (5), 889-898 (2004).
- Liu, D., et al. Enhancement of Electrochemical Hydrogen Insertion in N-Doped Highly Ordered Mesoporous Carbon. The Journal of Physical Chemistry C. 118 (5), 2370-2374 (2014).
- Choi, W. C., et al. Platinum Nanoclusters Studded in the Microporous Nanowalls of Ordered Mesoporous Carbon. Advanced Materials. 17, 446-451 (2005).
- Rouquerol, F., Rouquerol, J., Sing, K. . Adsorption by Powders and Porous Solids: Principles, Methodology and Application. , (1999).
- Gregg, S. J., Sing, K. S. W. . Adsorption, Surface Area and Porosity. , (1982).
- Llewellyn, P. L., Rouquerol, F., Rouquerol, J., Sing, K. S. W., Unger, K. K., Kreysa, G., Baselt, J. P. Critical appraisal of the use of nitrogen adsorption for the characterization of porous carbons. Characterization of Porous Solids V. , 421-427 (2000).
- Sing, K. S. W. The use of gas adsorption for the characterization of porous solids. Colloids and Surfaces. 38, 113-124 (1989).
- Rouquerol, J. Recommendations for the characterization of porous solids. Pure & Applied Chemistry. 66, 1739-1758 (1994).
- Marega, C. A direct SAXS approach for the determination of specific surface area of clay in polymer-layered silicate nanocomposites. The Journal of Physical Chemistry B. 116, 7596-7602 (2012).
- Tsao, C. S., et al. Neutron Scattering Methodology for Absolute Measurement of Room-Temperature Hydrogen Storage Capacity and Evidence for Spillover Effect in a Pt-Doped Activated Carbon. The Journal of Physical Chemistry Letters. 1, 1569-1573 (2010).
- Mattson, J. S., Mark, H. B. . Activated Carbon: Surface Chemistry and Adsorption from Solution. , (1971).
- László, K., Szucs, A. Surface characterization of polyethyleneterephthalate (PET) based activated carbon and the effect of pH on its adsorption capacity from aqueous phenol and 2,3,4-trichlorophenol solutions. Carbon. 39, 1945-1953 (2001).
- Garten, V. A., Weiss, D. E., Willis, J. B. A new interpretation of the acidic and basic structures in carbons. Australian Journal of Chemistry. 10, 309-328 (1957).
- Boehm, H. P. Surface oxides on carbon and their analysis: A critical assessment. Carbon. 40, 145-149 (2002).
- Menendez, J. A., Phillips, J., Xia, B., Radovic, L. R. On the modification and characterization of chemical surface properties of activated carbon: In the search of carbons with stable basic properties. Langmuir. 12, 4404-4410 (1996).
Перепечатки и разрешения
Запросить разрешение на использование текста или рисунков этого JoVE статьи
Запросить разрешениеThis article has been published
Video Coming Soon
Авторские права © 2025 MyJoVE Corporation. Все права защищены