JoVE 비디오를 활용하시려면 도서관을 통한 기관 구독이 필요합니다. 전체 비디오를 보시려면 로그인하거나 무료 트라이얼을 시작하세요.
Method Article
합성된 성공 탄소 그리고 실리 카 매트릭스의 표면 특성
요약
여기 우리 합성 및 주문된 성공 (4.6 nm 기 공 크기)와 탄소와 SBA-15 (5.3 nm 기 공 크기)의 특성을 보고합니다. 작업 표면 및 성공 분자 체의 텍스처 속성, 그들의 습윤 D2O 자료에 국한의 녹는 동작에 설명 합니다.
초록
이 작품에서는, 우리는 합성 및 특성의 주문 성공 4.6 nm 기 공 크기와 정렬 된 실리 카 다공성 매트릭스, 탄소 재료 (정렬된 mesoporous 탄소 소재 [OMC] 라고도 함) 보고 5.3 nm 기 공 크기와 SBA-15. 이 작품 성공 분자 체, 그들의 습윤의 표면 특성을 설명 하 고 D2O의 녹는 동작 비슷한 기 공 크기와 다르게 정렬 된 다공성 물질에 국한. 이 위해 OMC와 구조는 고도로 정렬 된 성공으로 SBA 15 합성 실리 카 매트릭스의 임신을 통해 탄소 전 구체를 적용 하 여 고 졸-겔 방법에 의해 각각. 조사 시스템의 다공성 구조는 N2 흡착-탈 착 분석 77 공화국에 의해 특징입니다. 합성된 재료의 표면의 전기 화학적 특성을 확인 하려면 potentiometric 적정 측정 실시 하는; OMC에 대 한 취득된 결과 pH, SBA 15 기준의 더 높은 값으로 중요 한 pHpzc 변화를 보여줍니다. 이 조사 OMC 속성이 표면 산소 기반 기능 그룹에 관련 된 제안 합니다. 설명 하기 위해 재료의 표면 특성, 공부 다공성 침대를 관통 하는 액체의 접촉 각도 또한 결정 됩니다. 모 세관 상승 방법 탄소 벽을 기준으로 실리 카 벽의 증가 습윤 및 탄소 mesopores에 대 한 보다 실리 카에 대 한 발음 훨씬 더는 액체/벽 상호 작용에 기 공 거칠기의 영향을 확인 했습니다. 우리 또한 D2O 유 전체 메서드를 적용 하 여 OMC와 SBA 15에 국한의 녹는 동작을 공부 했다. 결과 D2O OMC의 숨 구멍에서의 용융 온도의 우울증 약 15 K SBA 15에 녹는 온도의 우울증에 상대적으로 높은 비교 5 nm 크기 숨 구멍은 보여준다. 이것은 공부 매트릭스의 흡착/흡착 제 상호 작용의 영향에 의해 발생 합니다.
서문
1992 년에, 주문된 성공 실리 카 재료 했다 처음으로 사용 하 여 얻은 유기 템플릿; 그 이후, 이러한 구조, 합성 방법, 그들의 속성을 수정의 조사의 다양 한 측면에 관련 된 많은 간행물 및 다른 응용 프로그램은 문학1,2에 등장 ,3. SBA 15 성공 실리 카 매트릭스4 에 대 한 관심은 그들의 독특한 품질: 균일 한 기 공 크기 분포와 좋은 화학 및 기계적 특성 모 공 넓은 높은 표면 영역. SBA 155, 같은 원통형 숨 구멍을가지고 성공 실리 카 재료는 자주 사용 다공성 매트릭스로 촉매에 대 한 그들은 효율적인 촉매 유기 반응6,7. 자료는 그들의 특성8,,910에 영향을 미칠 수 있는 방법의 다양 한 합성 수 있습니다. 따라서, 그것은 많은 분야에서 잠재적인 응용 프로그램에 대 한 이러한 메서드를 최적화 하기 위해 중요 한: 전기 화학 장치, 나노기술, 생물 및 의학, 약물 전달 시스템, 또는 접착에 원상. 현재의에서 연구, 두 개의 서로 다른 유형의 성공 구조, 즉 실리 카와 탄소 다공성 행렬 표시 됩니다. 그들의 속성을 비교 SBA 15 행렬 합성 솔-젤 메서드를 사용 하 고 주문된 성공 탄소 재료는 탄소 전 구체와 결과 실리 카 매트릭스의 임신에 의해 준비.
다공성 탄소 재료는 그들의 높은 표면적과 그들의 고유 하 고 잘 정의 된 물리 화학적 특성6,,1112많은 기기에서 중요 합니다. 일반적인 준비 결과 자료 무작위로 분산된 다공성 및 무질서 구조; 또한 일반 공 매개 변수 변경에 대 한 제한 가능성 고 따라서 상대적으로 광범위 한 기 공 크기 분포와 구조13얻을 수 있습니다. 이 가능성 높은 표면 영역 성공 탄소 재료에 대 한 확대 이며 nanopores의 시스템을 주문 합니다. 더 형상과 기 공 공간 안에 물리 화학 프로세스의 제어는 많은 응용 프로그램에서 중요 한 예측: 촉매, 분리 미디어 시스템, 전자 재료, 그리고 많은 과학 분야14 nanoreactors 고급 , 15.
다공성 탄소 복제본을 얻으려면 정렬 된 규 산 염 단단한 매트릭스는 탄소 선구자 직접 소개로 작동할 수 있다. 메서드를 여러 단계로 분할 될 수 있다: 정렬 된 실리 카 재료;의 선택 실리 카 매트릭스; 탄소 전조의 증 착 탄 화; 그런 다음, 실리 카 매트릭스의 제거입니다. 이 방법에 의해 탄소 재료의 다양 한 종류를 얻을 수 있습니다 하지만 모든 nonporous 물자 명령된 구조. 과정의 중요 한 요소는 누구의 nanopores163 차원 구조 형성 해야 합니다 적당 한 매트릭스의 선택 이다.
이 작품에서는, 합성된 성공 매트릭스의 표면 특성에 기 공 벽의 종류의 영향을 조사. OMC 재료의 표면 특성은 실리 카의 아날로그 (SBA-15) OMC의 표면 특성에 의해 반영 됩니다. 재료 (OMC 및 SBA 15)의 두 종류의 텍스처와 구조 속성 (77 K)에서 낮은 온도 N2 흡착/탈 착 측정, 전송 전자 현미경 (TEM), 에너지 분산 x-선 분석 (에 의해 특징 EDX)입니다.
낮은-온도 가스 흡착/탈 착 측정 다공성 재료의 특성 중 가장 중요 한 기술 중 하나입니다. 질소 가스는 고체 adsorbents 강한 상호 작용을 만들는 높은 순도 가능성으로 인해 흡착으로 사용 됩니다. 이 기술의 중요 한 장점은 사용자 친화적인 상용 장비와 상대적으로 쉬운 데이터 처리 절차입니다. 질소 흡착/탈 착 등온선의 결정은 다양 한 압력 (P/P0)에 77 K에서 고체 흡착 제 표면에 흡착 분자의 축적을 기반으로 합니다. 기 공 크기 분포 실험 흡착 또는 탈 착 등온선에서 계산에 대 한 배 럿, 조 이너, 및 Halenda (BJH) 절차 적용 됩니다. BJH 방법의 가장 중요 한 가정 평면 표면 및 조사 표면에 흡착의 동등한 배급을 포함 한다. 그러나,이 이론은 켈빈 방정식에 근거 하 고 mesoporous 범위의 기 공 크기 분포를 계산 하기 위한 가장 널리 사용 되는 방식으로 남아 있다.
샘플의 전기 화학적 특성을 평가 하는 potentiometric 적정 방법은 적용 됩니다. 재료의 표면 화학 heteroatoms 또는 표면에 기능적인 그룹의 존재와 관련 된 표면 충전에 따라 달라 집니다. 표면 특성은 또한 접촉 각 분석에 의해 조사 됩니다. 모 공 안에 습윤 흡착 흡착 제 상호 작용에 대 한 정보를 제공합니다. 두 샘플에 물 녹는 온도에 벽 거칠기의 영향이 유전 휴식 분광학 (DRS) 기법으로 공부 된다. 유 전체 상수의 측정 액체의 polarizability로 현상 녹는의 조사를 허용 하 고 단단한 단계는 서로 다릅니다. 커패시턴스의 온도 의존의 경사에 있는 변화는 용융 시스템에서 발생 합니다 보여 줍니다.
프로토콜
1입니다. OMC 자료의 준비
-
OMC 전조로 실리 카 매트릭스의 합성
- 1.6 M HCl의 360 mL 50 mL HCl (36%-38%)를 추가 하 여 준비 500 mL 둥근 바닥 플라스 크와, 초순 (18.2 ㏁ 저항력)의 다음, 추가 310 mL.
- PE 10500 10 g 추가, 폴리머 (6.500 g/mol).
- 초음파 목욕에 플라스 크를 놓습니다. 35 ° C에 솔루션을 열 고 고체 폴리머 완전히 녹아 균질 혼합물을 만들기까지 그것을 저 어.
- 플라스 크에 1.3.5-trimethylbenzene의 10 g를 추가 하 고 35 ° c 물 목욕에서 그것을 유지 하 여 (220 rpm의 교 반 속도)에서 콘텐츠를 저 어.
- 30 분 동안 교 반 후 플라스 크를 tetraethyl orthosilicate (TEOS)의 34 g을 추가 합니다. 추가 TEOS 천천히 그리고 dropwise 지속적인 교 반. TEOS의 34 g 추가 10 분 걸리는 것을 확인 하십시오.
- 동일한 온도 (35 ° C)에서 다시 20 h에 대 한 솔루션 혼합물을 저 어.
- 소계 카트리지에 플라스 크의 내용을 전송 하 고 압력솥에 넣습니다. 90 ° c.에 24 h에 대 한 솔루션을 두고
- Büchner 퍼 널을 사용 하 여 결과 침전을 필터링 하 고 적어도 1 l.를 사용 하 여 증류수로 씻어
- 실 온에서 얻은 고체 건조 하 고 6 h에 대 한 공기 분위기에 휩 싸이 다 용광로 사용 하 여 500 ° C에서 샘플을 열 처리를 적용.
-
탄소 전 구체를 사용 하 여 결과 실리 카 매트릭스의 임신
- 임신 솔루션 (IS1, IS2) 물, 3 M 황산 (VI)의 적절 한 비율을 준비 하 고 탄소 선구자의 역할을 담당 하는 포도 당 및 황산 촉매 역할 (포도 당), 설탕.
주의: 황산은 매우 독성, 그것은 원인 심각한 피부 화상과 눈 손상을.- IS1 준비. 실리 카의 각 그램, 물 5 g, 3 M 황산 (VI)의 0.14 g, 설탕의 1.25 g 섞는다.
- IS2 준비. 실리 카의 각 그램, 물 5 g, 3m 황산 (VI)의 0.08 g, 설탕의 0.75 g 섞는다.
- 실리 카 재료 (1 g)와 탄소 전 구체와 촉매의 준비 된 솔루션 IS1 500 mL 플라스 크에 배치 합니다. 100 ° C 6 h에서 진공 건조 기에서 혼합 열.
참고:이 단계에서 IS1만 사용 합니다. IS2 다음 단계에서 적용 되어야 한다. - IS2 진공 (부분적으로 탄 화 탄소 전 구체와 솔루션)를 건조 기에 혼합물에 추가 합니다. 160 ° C 12 h에서 진공 건조 기에서 다시 혼합물이 열.
- 임신 솔루션 (IS1, IS2) 물, 3 M 황산 (VI)의 적절 한 비율을 준비 하 고 탄소 선구자의 역할을 담당 하는 포도 당 및 황산 촉매 역할 (포도 당), 설탕.
-
템 퍼/탄 화
- 더 큰 입자의 조각화 및 재료의 균질에 대 한 박격포를 얻은 합성을 전송 합니다.
- 흐름으로 얻은 제품을 놓고 (2.5 ° C/min의 승 온 속도)에서 700 ° C 고 열이이 온도에 6 h에 대 한 열. 질소 분위기에서 자료 열.
- 수로 열기 전에 냉각 솔루션.
-
에칭에 의해 실리 카 매트릭스의 제거
- 100 mL의 에칭 해결책 (ES)를 준비 합니다. 95% 에틸 알코올 및 물 50 mL 50 mL를 혼합. 7 g의 수산화 칼륨을 추가 하 고 그것은 녹아 때까지 저 어.
- 장소 모든 250 mL 둥근 바닥 플라스 크에 탄 화 물질 (1g 이상)을 취득 하 고 ES의 100 mL를 추가 합니다.
- 지속적으로 교 반 하면서 환류 콘덴서 및 자력과 종 기에 열 시스템을 제공 합니다. 1 시간에 대 한 혼합물을 끓인 다.
- Büchner 퍼 널을 얻은 자료를 전송, 증류수, 적어도 4 l 세척 하 고 건조.
2. 실리 카 SBA 15 매트릭스의 준비
- 음성 합성 실리 카 매트릭스.
- 1.6 M HCl의 150 mL를 준비 합니다.
- 150 mL 둥근 바닥 플라스 크에 산 성 솔루션에에서 PE 6400 폴리머 (EO13포70EO13)의 4 g 용 해.
- 초음파 목욕에 플라스 크를 놓습니다. 40 ° C에 솔루션을 열 고 중합체를 해산 할 수 있도록 그것을 저 어 (적어도 30 분).
- 천천히 추가 TEOS의 8.5 g는 플라스 크에 dropwise, 지속적인 교 반. 동일한 온도 (40 ℃)에서 24 h에 대 한 솔루션 혼합물을 저 어.
- 소계 카트리지를 플라스 크의 내용을 전송 합니다. 120 ° C 오븐에서 24 h에 대 한 솔루션을 둡니다.
- Büchner 퍼 널을 사용 하 여 결과 침전 필터 및 증류수 (1 리터 이상)와 그것을 씻어.
- 건조 한 실내 온도 공기 분위기에 휩 싸이 다 용광로 사용 하 여 600 ℃에서 6 h calcine에서 얻은 고체.
3입니다. 특성화의 방법
- 낮은-온도 질소 흡착/탈 착 측정
- 자동 수 착 분석기 77 공화국에서 흡착/탈 착 등온선 N2 를 사용 하 여
- 적절 한 유리 튜브를 사용 하 여 질소 수 착 측정. 유리 튜브를 다공성 샘플을 추가 하기 전에 초음파 세척기에 튜브를 청소 하 고 증류수와 함께 첫 번째 고, 무수 에탄올과 다음 그것을 씻어.
- 유리 튜브 3 h 150 ° C에서가 열 하 고 압축 된 질소로 튜브를 입력 합니다. 무게 무게 오류를 최소화 하기 위해 측정 전에 질소 조건 하에서 빈 유리 튜브.
- 유리 튜브에 샘플을 놓고 총 질량 (유리 튜브 샘플의 질량) 무게.
- 측정을 하기 전에 샘플을 드. 수 착 분석기의 생성 포트에 샘플 유리 튜브를 놓습니다. 다음 프로세스 조건 적용: 423 K의 온도 0.01 mmHg의 압력 그리고 24 h의 기간. 생성 포트에서 진공에 샘플을 연결 하 고 설정된 온도 (423 K) 열. 기체 제거, 후 샘플 질소를 분석 포트에 전송.
- 전송 전자 현미경 검사 법
- 120 편 현미경을 사용 하 여 좋은 품질의 TEM 이미지를 수집 하는 kV (SBA-15)에 대 한 및 200 kV (OMC 자료)에 대 한 가속 전압.
- 샘플의 단 분산 영화 준비에 대 한 샘플 (1 mg) 에탄올 (1 mL)에 분산. Microcentrifuge 튜브에 3 분 동안 초음파 목욕에서 그것을 배치 하 여 분산 절차를 수행 합니다.
- 가장 구리 격자는 micropipette를 사용 하 여 분산의 두 방울을 놓습니다. TEM 현미경을 가장 그리드를 전송 하 고 가장 이미징 시작 합니다.
- 에너지 흩어진 엑스레이 분광학
- X 선 검출기를 장착 하는 스캐닝 전자 현미경을 사용 하 여 샘플의 에너지 분산 x-선 스펙트럼을 취득.
- 15의 가속 전압을 적용 스펙트럼 수확 kV. SBA 15, OMC 샘플에 대 한 탄소에 대 한 최적화 요소로 실리콘을 선택 합니다.
- Potentiometric 적정 측정
- Potentiometric 적정 실험을 수행 하는 자동 뷰 렛을 사용 합니다. (에 따르면 적정 소프트웨어 및 절차) 작고 제어 부분에는 titrant를 추가 합니다. 자동 투약 intrument에 의해 가장 작은 증가, 1 μ를 제공 합니다.
- 0.1 g의 전해질 용액 (0.1 M NaCl의 물 솔루션) 30 mL에 샘플의 분산. 자력 및 등온 조건 (293 ± 0.1 K)를 사용 하 여 분산 과정.
- 정지에 titrant (0.1 M NaOH 솔루션)의 1-2 mL를 추가 합니다.
참고: 작은 aliquots (약 0.05 mL 수를 각각)에 추가 수행 합니다. 자동 뷰 렛 절차 1에서 14의 pH 범위에서 적어도 12 실험 포인트를 제공 해야 합니다. - Qs, 다음 수식을 사용 하 여 충전의 표면 밀도 계산 합니다.
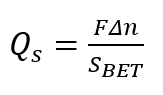 (1)
(1)
여기,
Δn = 샘플;의 질량 당 감소 H+/OH- 균형에 변화
S내기 = Brunauer-모트-텔러 (내기) 면적 다공성 고체;
F = 패러데이 수.
- 습윤 측정용 모 세관 상승 방법
- 공부 샘플의 숨 구멍 안에 접촉 각을 결정, 모 세관 상승 메서드를 사용 합니다.
참고:이 메서드는 시간의 기능으로 다공성 침대를 관통 하는 액체의 질량 상승의 측정에 기반. 이 방법의 주요 가정은 사실에 근거한 관통 액체 다공성 열으로 발전 하 고이 열 특정 평균 반경 입자 모세 혈관으로 구성 된. 따라서, 단일 모 세관 파생 된 모든 관계는 다공성 파우더의 계층에 대 한 유효 합니다. 단일 세로 모 세관에서 일로 액체 숨 구멍 (모 세관 압력)에 액체와 증기 압력의 차이 결과로 중력에 대 한 수레. 이 의미에서 다공성 침대에 액체의 침투는 모 공 내부 동적 전진 접촉 각의 결정을 수 있습니다. - 적용 수정된 워시의 방정식17,18, 다음과 같이 표현 됩니다.
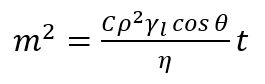 (2)
(2)
여기,
m = 질량 측정 액체;
C = 기하학적 매개 변수 의존 배포, 모양 및 크기의 숨 구멍;
Ρ = 밀도;
Γl= 표면 장력.
Η =; 관통 하는 액체의 점도
Θ = 연락처 각도;
t = 시간. - 방정식 (2), using 공부 숨 구멍 안에 전진 접촉 각의 값 예상.
- 힘 뿐만 준비 합니다. 파우더를 함께 사용 하 여 유리 튜브 직경 3 m m와 세라믹 화; 액체, 직경 22 mm와 최대 볼륨 10 mL의 그릇을 사용 합니다.
- 측정 샘플의 0.017 g.
- 뿐만에 연결 된 컴퓨터 프로그램을 시작 합니다. 모터 구동 단계에 액체 용기를 넣고 전자 저울에 샘플 유리 튜브를 일시 중단.
- 모터를 시작 하 고 일정 한 속도로 낮은 10 mm/min; 샘플 용기에 액체 접근 시작 1 m m 액체 동등으로 샘플 튜브의 침수 깊이 설정 합니다.
- 이 순간, 의존 m2 에서 컴퓨터 프로그램에서 f(t) 레지스터 =.
- 실험을 중지 때 의존 m2 = f(t) 시작 표시 특성 고원.
- X-5 x 3이이 절차를 반복 하 여 정확도를 확인 합니다.
- 공부 샘플의 숨 구멍 안에 접촉 각을 결정, 모 세관 상승 메서드를 사용 합니다.
- 유 전체 휴식 분광학
- 공부 다공성 행렬 안에 갇혀 물 녹는 동작을 설명 하기 위해 스테인리스19, 의 평행 판 축전기에 있는 샘플의 전기 용량 C 의 온도 측정을 수행 20 , 21. 커패시턴스 C 온도의 기능 및 적용 된 순환 전기 분야의 주파수를 측정 하는 임피던스 분석기 사용 하 여.
참고: 복잡 한 전기 유전율 ε *로 정의 됩니다 ε =' + iε ', 어디 ε' = C/C0 은 진짜, 및 ε ' tgδ·ε =' C0 가 빈의 커패시턴스는 유전율의 허수부는 커패시터와 tgδ는 유 전체 손실. - 측정된 샘플을 격판덮개 축전기에 넣습니다.
- 1 MHz와 K. 제어 온도의 속도 변화 온도 컨트롤러; 305에 140 K에서 온도 100 Hz에서 주파수 범위 선택 냉각 하는 동안 0.8 K/min와 난방 과정 동안 0.6 K/min로 온도 속도 설정 합니다.
- 공부 다공성 행렬 안에 갇혀 물 녹는 동작을 설명 하기 위해 스테인리스19, 의 평행 판 축전기에 있는 샘플의 전기 용량 C 의 온도 측정을 수행 20 , 21. 커패시턴스 C 온도의 기능 및 적용 된 순환 전기 분야의 주파수를 측정 하는 임피던스 분석기 사용 하 여.
결과
OMC와 SBA-15, N2 흡착-탈 착의 조사 샘플의 다공성 구조를 특성화 하기 위해 등온선 77 공화국에서 기록 되었다 실험 N2 가스 흡착-탈 착 등온선 조사 시스템 뿐만 아니라 흡착 및 탈 착 데이터에서 얻은 기 공 크기 분포 (PSD) 특성화 그림 1A-D에 표시 됩니다. 수 착 등온선 (그림 1A, C)에 굴절 ?...
토론
정렬된 mesoporous 탄소 재료의 준비 하는 동안 중요 한 단계는 잘 정의 된 구조 속성 최종 재료의 특성에 영향을 주는 서식 파일로 정렬된 mesoporous 실리 카 재료의 준비와 질소 분위기에서 부드럽게/탄 화 단계입니다. mesoporous의 준비의 일반적인 방법의 수정 지시 원통형 모28 우려 규는 untypical 구조 감독 에이전트는 구조 개선에 대 한 PE10500 고분자의 응용 재료의 속성입니다. 서식 ?...
공개
저자는 공개 없다.
감사의 말
저자 국립 과학 센터를 부여와 재정 지원을 제공 하기 위한 감사 하 고 싶습니다 없습니다. 12 월-2013/09/B/ST4/03711와 UMO-2016/22/ST4/00092. 저자는 또한 연구를 위한 국가 센터에서는 폴란드 운영 프로그램 인적 자본 포 KL에서 4.1.1, 또한 부분 지원에 감사 하 고 개발, 연구에서 부여 없음. PBS1/A 9/13/2012입니다. 저자는 특히 계 현상, 화학의 교수, 마리아 퀴리 Skłodowska 대학, 루블 린, 폴란드에서 교수 L. Hołysz, 그녀의 친절 및 SBA 15 nanopores에 습윤의 측정을 사용에 대 한 감사.
자료
| Name | Company | Catalog Number | Comments |
| 1,3,5-trimethylbenzene | Sigma-Aldrich, Poland | M7200 Sigma-Aldrich | Mesitylene, also known as 1,3,5-trimethylbenzene, reagent grade, assay: 98%. |
| anhydrous ethanol | POCH, Avantor Performance Materials Poland S.A. | 396480111 | Assay, min. 99.8 %, analysis-pur (a.p.) |
| ASAP 2020. Accelerated Surface Area and Porosimetry System | Micromeritics Instrument Corporation, Norcross, GA, USA | Samples were outgassed before analysis at 120 oC for 24 hours in degas port of analyzer. The dead space volume was measured for calibration on experimental measurement using helium as a adsorbate. | |
| Automatic burette Dosimat 665 | Metrohm, Switzerland | The surface charge properties were experimentally determined by potentiometric titration of the suspension at constant temperature 20°C maintained by the thermostatic device. Prior to potentiometric titration measurements, the solid samples were dried by 24 hours at 120 oC. The initial pH was established by addition of 0.3 cm3 of 0.2 mol/L HCl. T The 0.1 mol/L NaOH solution was used as a titrant, added gradually by using automatic burette. | |
| Digital pH-meter pHm-240 | Radiometer, Copenhagen | Device coupled with automatic burette | |
| ethyl alcohol | POCH, Avantor Performance Materials Poland S.A. | 396420420 | Assay, min. 96 %.analysis-pur (a.p.) |
| glucose | POCH, Avantor Performance Materials Poland S.A. | 459560448 | assay 99.5% |
| Hydrochloric acid | POCH, Avantor Performance Materials Poland S.A. | 575283115 | Hydrochloric acid, 35 - 38% analysis-pur (a.p.) |
| HOPG graphite substrate | Spi Supplies | LOT#1170906 | HOPG SPI-2 Grade, 20x20x1 mm |
| Impedance analyzer Solartron 1260 | Solartron | ||
| Pluronic PE 6400 polymer | BASF (Polska) | (EO13PO70EO13) | |
| Pluronic PE10500 | BASF Canada Inc. | Molar mass 6500 g/mol | |
| potassium hydroxide | Sigma-Aldrich, Poland | P5958 Sigma-Aldrich | BioXtra, ≥85% KOH basis |
| SEM microscope | JEOL JSM-7001F | Scanning Electron Microscope with EDS detector | |
| Sigma Force Tensiometer 701 | KSV, Sigma701, Biolin Scientific | force tensiometer | |
| Sulfuric acid (VI) | POCH, Avantor Performance Materials Poland S.A. | 575000115 | |
| surface glass type KS 324 Kavalier | Megan Poland | 80 % of SiO2 , 11% of Na2O and 9% of CaO | |
| Tecnai G2 T20 X-TWIN | FEI, USA | Transmission Electron Microscope with EDX detector. | |
| TEM microscope | JEOL JEM-1400 | ||
| temperature controller ITC503 | Oxford Instruments | ||
| Tetraethylorthosilicate | Sigma-Aldrich, Poland | 131903 | Tetraethyl silicate, TEOS, reagent grade, assay 98% |
| Ultrapure water | Millipore, Merck KGaA, Darmstadt, Germany | SIMSV0001 | Simplicity Water Purification SystemUltrapure Water: 18.2 MegOhm·cm, TOC: <5 ppb |
참고문헌
- Tao, Y., Kanoh, H., Abrams, L., Kaneko, K. Mesopore-Modified Zeolites: Preparation, Characterization, and Applications. Chemical Reviews. , 896-910 (2006).
- Wan, Y., Zhao, D. On the Controllable Soft-Templating Approach to Mesoporous Silicates. Chemical Reviews. 107, 2821-2860 (2007).
- Khder, A. E. S., Hassan, H. M. A., El-Shall, M. S. Acid catalyzed organic transformations by heteropolytungstophosphoric acid supported on MCM-41. Applied Catalysis A. 411, 77-86 (2012).
- Zhao, D. D., et al. Triblock Copolymer Syntheses of Mesoporous Silica with Periodic 50 to 300 Angstrom Pores. Science. 279, 548-552 (1998).
- Linssen, T., Cassiers, K., Cool, P., Vansant, E. Mesoporous templated silicates: an overview of their synthesis, catalytic activation and evaluation of the stability. Advances in Colloid and Interface Science. 103, 121-147 (2003).
- Eftekhari, A., Fan, Z. Ordered mesoporous carbon and its applications for electrochemical energy storage and conversion. Materials Chemistry Frontiers. 1, 1001-1027 (2017).
- Sing, K. Characterization of porous materials: past, present and future. Colloids and Surfaces A. 241, 3-7 (2004).
- Huo, Q., Margolese, D. I. Generalized synthesis of periodic surfactant/inorganic composite materials. Nature. 368, 317-321 (1994).
- Selvaraj, M., Kawi, S., Park, D. W., Ha, C. S. Synthesis and characterization of GaSBA-15: Effect of synthesis parameters and hydrothermal stability. Microporous and Mesoporous Materials. , 586-595 (2009).
- Leonard, A., et al. Toward a better control of internal structure and external morphology of mesoporous silicas synthesized using a nonionic surfactant. Langmuir. 19, 5484-5490 (2003).
- Liang, C., Li, Z., Dai, S. Mesoporous Carbon Materials: Synthesis and Modification. Angewandte Chemie International Edition. 47, 3696-3717 (2008).
- Babić, B., et al. New mesoporous carbon materials synthesized by a templating procedure. Ceramics International. 39 (4), 4035-4043 (2013).
- Allen, S. J., Whitten, L., Mckay, G. The Production and Characterization of Activated Carbons: A Review. Developments in Chemical Engineering and Mineral Processing. 6, 231-261 (1998).
- Kwak, G., et al. Preparation Method of Co3O4 Nanoparticles Using Ordered Mesoporous Carbons as a Template and Their Application for Fischer-Tropsch Synthesis. The Journal of Physical Chemistry C. 117 (4), 1773-1779 (2013).
- Koo, H. M., et al. Effect of the ordered meso-macroporous structure of Co/SiO2 on the enhanced activity of hydrogenation of CO to hydrocarbons. Catalysis Science and Technology. 6, 4221-4231 (2016).
- Jun, S., Joo, S. H., Ryoo, R., Kruk, M., Jaroniec, M. Synthesis of New, Nanoporous Carbon with Hexagonally Ordered Mesostructure. Journal of the American Chemical Society. 122 (43), 10712-10713 (2000).
- Washburn, E. W. The dynamics of capillary flow. Physical Review Series2. 17, 273 (1921).
- Śliwińska-Bartkowiak, M., Sterczyńska, A., Long, Y., Gubbins, K. E. Influence of Microroughness on the Wetting Properties of Nano-Porous Silica Matrices. Molecular Physics. 112, 2365-2371 (2014).
- Śliwińska-Bartkowiak, M., et al. Melting/freezing behavior of a fluid confined in porous glasses and MCM-41: dielectric spectroscopy and molecular simulation. Journal of Chemical Physics. 114, 950-962 (2001).
- Coasne, B., Czwartos, J., Śliwińska-Bartkowiak, M., Gubbins, K. E. Freezing of mixtures confined in silica nanopores: experiment and molecular simulation. Journal of Chemical Physics. 133, 084701-084709 (2010).
- Chełkowski, A. . Dielectric Physics. , (1990).
- Radhakrishnan, R., Gubbins, K. E., Śliwińska-Bartkowiak, M. Global phase diagrams for freezing in porous media. Journal of Chemical Physics. 116, 1147-1155 (2002).
- Gubbins, K. E., Long, Y., Śliwińska-Bartkowiak, M. Thermodynamics of confined nano-phases. Journal of Chemical Thermodynamics. 74, 169-183 (2014).
- Radhakrishnan, R., Gubbins, K. E., Śliwińska-Bartkowiak, M. Effect of the fluid-wall interaction on freezing of confined fluids: Toward the development of a global phase diagram. Journal of Chemical Physics. 112, 11048 (2000).
- Cassie, A. B. D., Baxter, S. Wettability of porous surfaces. Transactions of the Faraday Society. 40, 546 (1944).
- Sing, K. Adsorption methods for the characterization of porous materials. Advances in Colloid and Interface Science. 76, 3-11 (1998).
- Sing, K. The use of nitrogen adsorption for the characterisation of porous materials. Colloids and Surfaces A. 187, 3-9 (2001).
- Yu, C., Fan, J., Tian, B., Zhao, D. Morphology Development of Mesoporous Materials: a Colloidal Phase Separation Mechanism. Chemistry of Materials. 16 (5), 889-898 (2004).
- Liu, D., et al. Enhancement of Electrochemical Hydrogen Insertion in N-Doped Highly Ordered Mesoporous Carbon. The Journal of Physical Chemistry C. 118 (5), 2370-2374 (2014).
- Choi, W. C., et al. Platinum Nanoclusters Studded in the Microporous Nanowalls of Ordered Mesoporous Carbon. Advanced Materials. 17, 446-451 (2005).
- Rouquerol, F., Rouquerol, J., Sing, K. . Adsorption by Powders and Porous Solids: Principles, Methodology and Application. , (1999).
- Gregg, S. J., Sing, K. S. W. . Adsorption, Surface Area and Porosity. , (1982).
- Llewellyn, P. L., Rouquerol, F., Rouquerol, J., Sing, K. S. W., Unger, K. K., Kreysa, G., Baselt, J. P. Critical appraisal of the use of nitrogen adsorption for the characterization of porous carbons. Characterization of Porous Solids V. , 421-427 (2000).
- Sing, K. S. W. The use of gas adsorption for the characterization of porous solids. Colloids and Surfaces. 38, 113-124 (1989).
- Rouquerol, J. Recommendations for the characterization of porous solids. Pure & Applied Chemistry. 66, 1739-1758 (1994).
- Marega, C. A direct SAXS approach for the determination of specific surface area of clay in polymer-layered silicate nanocomposites. The Journal of Physical Chemistry B. 116, 7596-7602 (2012).
- Tsao, C. S., et al. Neutron Scattering Methodology for Absolute Measurement of Room-Temperature Hydrogen Storage Capacity and Evidence for Spillover Effect in a Pt-Doped Activated Carbon. The Journal of Physical Chemistry Letters. 1, 1569-1573 (2010).
- Mattson, J. S., Mark, H. B. . Activated Carbon: Surface Chemistry and Adsorption from Solution. , (1971).
- László, K., Szucs, A. Surface characterization of polyethyleneterephthalate (PET) based activated carbon and the effect of pH on its adsorption capacity from aqueous phenol and 2,3,4-trichlorophenol solutions. Carbon. 39, 1945-1953 (2001).
- Garten, V. A., Weiss, D. E., Willis, J. B. A new interpretation of the acidic and basic structures in carbons. Australian Journal of Chemistry. 10, 309-328 (1957).
- Boehm, H. P. Surface oxides on carbon and their analysis: A critical assessment. Carbon. 40, 145-149 (2002).
- Menendez, J. A., Phillips, J., Xia, B., Radovic, L. R. On the modification and characterization of chemical surface properties of activated carbon: In the search of carbons with stable basic properties. Langmuir. 12, 4404-4410 (1996).
재인쇄 및 허가
JoVE'article의 텍스트 или 그림을 다시 사용하시려면 허가 살펴보기
허가 살펴보기더 많은 기사 탐색
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. 판권 소유