このコンテンツを視聴するには、JoVE 購読が必要です。 サインイン又は無料トライアルを申し込む。
Method Article
イン・ビトロBis-3-クロロピペリジンによるG-四重鎖DNA構造のケミカルマッピング
要約
Bis-3-クロロピペリジン(B-CeP)は、 in vitroでDNAテンプレート中のG-四重鎖構造を同定および特性評価するための有用な化学プローブです。このプロトコルはB-CePsの調査の反作用を行い、高リゾリューションのポリアクリルアミドのゲルの電気泳動によって反作用生成物を解決するプロシージャを詳述する。
要約
G-四重鎖(G4)は、遺伝子発現や疾患において重要な役割を果たす生物学的に関連性のある非標準的なDNA構造であり、重要な治療標的となります。潜在的なG四重鎖形成配列(PQS)内のDNAの in vitro 特性評価には、アクセス可能な方法が必要です。B-CePは、核酸の高次構造を調べるための有用な化学プローブであることが証明されているアルキル化剤の一種です。この論文では、B-CePとグアニンの N7との特異的な反応性を利用した新しいケミカルマッピングアッセイと、それに続くアルキル化Gsでの直接鎖切断について説明します。
すなわち、G4フォールドとアンフォールドDNAの形態を区別するために、B-CeP 1を用いて、G4配列を仮定できる15-merのDNAであるトロンビン結合アプタマー(TBA)をプローブします。B-CeP応答グアニンとB-CeP1の反応により、高分解能ポリアクリルアミドゲル電気泳動(PAGE)により、アルキル化グアニンの個々のアルキル化付加物およびDNA鎖切断の位置を特定することにより、一塩基レベルで分離できる生成物が得られます。B-CePを用いたマッピングは、G-四重鎖形成DNA配列の in vitro 特性評価のためのシンプルで強力なツールであり、G-テトラッドの形成に関与するグアニンの正確な位置を特定することができます。
概要
核酸は、典型的なワトソン・クリック二重らせんに加えて、グアニンに富む配列により、代替のG-四重鎖(G4)型など、さまざまな二次構造を採用することができます。G4構造は、4つのグアニンがフーグステン水素結合を介して相互作用するG-テトラッドと呼ばれる平面四量体の形成に基づいています。G-テトラッドは、グアニンコアの中心に配位した一価の陽イオンによって積み重ねられ、さらに安定化されます(図1)1。
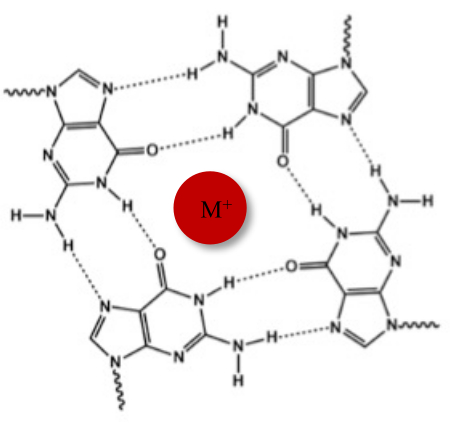
図1:G-四重構造の模式図 。 (A)G-テトラッドの模式図。平面アレイは、フーグスティーン塩基対形成と中心陽イオン(M+)によって安定化されます。この図の拡大版をご覧になるには、ここをクリックしてください。
少なくとも2つの連続したグアニンヌクレオチドが4回以上ランされた配列は、G-四重鎖構造で折りたたまれる可能性のあるG-四重鎖形成配列(PQS)です。PQSは、テロメア、遺伝子プロモーター、リボソームDNA、組換え部位など、さまざまな細胞環境にあり、多くの生物学的プロセスの制御に関与しています2。したがって、ヒトゲノム中のG4の同定と実験的検証は、現在、主に計算ツールによって行われており、生物学的に重要な問題です3。計算による予測をサポートしたり、予測不可能なG4構造を検出したりするために、DNAテンプレート中のG4形成を同定するためのケミカルマッピングに基づくアクセス可能な方法がここに示されており、G-tetrad構造を形成するグアニンの正確な同定が可能です。
報告されたケミカルマッピングアッセイは、G4構造の形成に続くビス-3-クロロピペリジン(B-CeP)とグアニンとの異なる反応性を利用しています。B-CePは求核剤4,5,6,7,8,9との反応性が高いため、グアニンヌクレオチドのN7位と非常に効率的に反応する能力を持つ核酸アルキル化剤である10。アルキル化に続いて、一本鎖および二本鎖DNAコンストラクトの脱品と鎖切断が行われます。それどころか、G4配列におけるG-テトラッドの形成に関与するグアニンは、グアニンのN7位がフーグスティーン水素結合に関与しているため、B-CePアルキル化の影響を受けません。このB-CePの特異的な反応性により、G4構造の検出だけでなく、一本鎖および二本鎖DNA中のグアニンと比較してアルキル化からの相対的な保護から推定できるため、テトラドを形成するグアニンの同定も可能になります。
ここでは、カリウム陽イオンの存在下でG4配列を仮定できる15-mer DNAであるトロンビン結合アプタマー(TBA)の特性評価のプローブとして、B-CeP 1(図2A)を用いてケミカルマッピングプロトコルを報告しています11,12。TBA(G4-TBA)のG4配列は、2つのコントロール、すなわち一本鎖型のTBA(ssTBA)と、その相補的な配列にアニーリングされて二本鎖コンストラクト(dsTBA)を形成するTBAと直接比較されます(表1)。プロービング反応の生成物は、高分解能ポリアクリルアミドゲル電気泳動(PAGE)によって、アルキル化グアニンの個々のアルキル化付加物とDNA鎖切断の位置を特定することにより、一塩基レベルで分離されます。ゲル上での可視化は、TBAオリゴヌクレオチドと3'末端に蛍光色素を結合させることで可能になります(表1)。このプロトコルは異なった構造(G4および対照)のTBAを折る方法、およびB-CePsとそれに続くPAGEの探る反作用を行う方法を示す。
プロトコル
1. 核酸および化学プローブの調製
- 核酸
注:「TBA」と名付けられたオリゴヌクレオチドは、15 mer の DNA 配列 5'-GGT-TGG-TGT-GGT-TGG-3' で、3' 末端に蛍光色素の 5-カルボキシフルオレセイン(FAM)で標識され、ゲル上での可視化を可能にします。非標識オリゴヌクレオチド「cTBA」は、そのDNA相補的配列5'-CCA-ACC-ACA-CCA-ACC-3'です。 表1に示すように、TBAおよびcTBAは、3つの異なる構造を得るために採用される。- オートクレーブチップと0.5mLチューブは、滅菌済みの使い捨て製品を入手し、汚染を防ぎます。
- 各オリゴヌクレオチドを超純水に可溶化して最終濃度100μMになるようにストック溶液を調製します。 メーカーが提供する260 nmの吸光係数を使用して、紫外可視(UV-Vis)分光光度計で正確なオリゴヌクレオチド濃度を決定します。
注:消光係数:TBAとcTBAには、それぞれ164,300 M-1 cm-1と138,600 M-1 cm-1を使用しました。 - TBAおよびcTBAストック溶液は-20°Cで保管してください(これらの条件で数ヶ月間)。
- 化合物B-CeP1
注:化合物B-CeP1は、以前に報告されたように合成されます6。- B-CeP 1 原液を ~10 mM で調製します。ヒュームフード内の分析天びんを使用して凍結乾燥化合物~1 mgを秤量し、100%ジメチルスルホキシド(DMSO)に可溶化します。
- 実際の化合物量とDMSO(d = 1.1 g/cm3)に基づいて、正確な化合物濃度を計算します。
注:コンパウンドは常に手袋を着用して取り扱ってください(凍結乾燥時とDMSOに溶解時の両方)13,14。
表1:このプロトコルで使用されるオリゴヌクレオチド構造。この表をダウンロードするには、ここをクリックしてください。
2. 核酸コンストラクトのフォールディング
- 緩衝液の調製
- BPE緩衝液(重リン酸-エチレンジアミン四酢酸[EDTA]、5x:2mMNaH2PO 4、6 mM Na 2 HPO 4、1 mMNa2EDTA、pH7.4)および超純水中の500 mM KClの溶液を調製する。孔径0.22μmのフィルターで溶液をろ過します。
注意: 最良の結果を得るには、新しく調製した溶液を使用してください。BPEバッファーは、4°Cで最大15日間保存できます。
- BPE緩衝液(重リン酸-エチレンジアミン四酢酸[EDTA]、5x:2mMNaH2PO 4、6 mM Na 2 HPO 4、1 mMNa2EDTA、pH7.4)および超純水中の500 mM KClの溶液を調製する。孔径0.22μmのフィルターで溶液をろ過します。
- 熱リフォールディング法によるG4-TBA、ssTBA、dsTBA試料のフォールディング
注:カリウムカチオンは、G4構造(G4-TBA)を折りたたむために必要です。コントロールssTBAおよびdsTBAの折り畳み溶液にカリウムカチオンを添加しないでください。- 1x BPEおよび100 mM KClに4 μMのG4-TBA溶液を調製し、チューブを95°Cで5分間加熱してオリゴヌクレオチドG4-TBA溶液を変性させ、ゆっくりと室温(RT)まで冷却してTBAをG-四重鎖に折りたたむようにします。
- 4 μM の ssTBA 溶液 40 μL を 1x BPE で調製します。ステップ2.2.1で説明したように、熱再折り手順を実行して、TBAを一本鎖の形で折ります。
- 等モル量のTBAとcTBAを1x BPEで混合して、40 μLのdsTBA溶液を調製します。TBAが相補的配列cTBAにアニーリングし、TBAの二本鎖形態を形成するために、上記のように熱リフォールディング手順(ステップ2.2.1)を実行します。
注:各フォールディング溶液の最終容量は、各サンプルに 5 μL の 4 μM 溶液が必要であることを考慮して、プロービング反応のサンプル数に基づいています。ピペッティングエラーを避けるために、各溶液を少し多めに準備します。
3. プロービング反応
注:プロービング反応は、熱リフォールディング手順の直後に行う必要があります。
- G4-TBA、ssTBA、dsTBAのフォールディング溶液がRTまで冷却されたら、ショートスピン遠心分離(7,000 × g 、室温で5-8秒)を行い、プロービング反応を開始します。
- 21本の空の0.5 mLオートクレーブチューブを準備します。 表 2 に報告されているように、ラボサンプル用にそれぞれ 7 本のチューブを 3 セットラックにまとめます。
注:各列セットは、G4-TBA、ssTBA、およびdsTBAの3つの異なるTBA折り畳み条件に対応しています。各行は、3つの異なるインキュベーション時間に対応しています。カラム内の各細胞は、最終的なB-CeP 1プローブ濃度に対応します(表2)。チューブにはっきりとラベルを付けてください。 - 各チューブに3μLの超純水を加えます。
- 折りたたんだG4-TBAを5μL、1セット目の各チューブに加えます(ステップ3.2)。2セット目の各チューブに5μLの折りたたんだssTBAを加えます。3セット目の各チューブに折りたたんだdsTBAを5μL加えます。
- B-CeP 1原液を超純水で250 μMおよび25 μMに希釈します。
注:B-CeP 1ケミカルプローブの希釈液は、水との競合反応を避けるために、新たに調製し、直ちにDNA基質と反応させる必要があります。 - 適切な B-CeP 1 希釈液 2 μL(25 μM および 250 μM)をサンプルに加えます。3 つのコントロールサンプル (C) 中の化合物を超純水に置き換えて、化合物の非存在下で異なる折り畳みの TBA を分析します。すべてのサンプルを37°Cでインキュベートします。
- 1時間、4時間、15時間のインキュベーション後、次のステップまでチューブを-20°Cに置いて反応を停止します。
注:サンプルはこれらの条件で数日間保管できます。 - サンプルを真空遠心分離機で乾燥させます。
注:乾燥したサンプルは、PAGE分析に進む前に、-20°Cで数週間保存できます。
表2:プロービング反応のサンプル(構造、プローブ濃度、インキュベーション時間)。 各列セットは、3つの異なるTBAフォールディング条件(G4-TBA、ssTBA、およびdsTBA)に対応しています。各行は、3つの異なるインキュベーション時間(1、4、15時間)に対応しています。カラム内の各細胞は、最終的なB-CeP 1プローブ濃度(5または50μM)に対応します。各セットのコントロール(C)は、化合物の非存在下でより長い時間(15時間)インキュベートした、異なる折り畳みのTBAのサンプルに対応する。 この表をダウンロードするには、ここをクリックしてください。
4. 高解像度PAGE
- 変性ポリアクリルアミド溶液の調製
注:事前に500 mLの20%変性ポリアクリルアミドゲル溶液を調製してください。この溶液の約 80 mL を各実験に使用します。琥珀色のガラス瓶を使用するか、ガラス瓶をアルミホイルで覆って、溶液をRTで保存します。
注意:ポリアクリルアミドは神経毒性があります。ゲルの準備と注入のすべての段階で、手袋と白衣を着用してください。重合したアクリルアミドは、汚染された物質に適した箱に廃棄してください。- 1Lビーカーに尿素210gを計量します。250 mL の 40% アクリルアミド/ビスアクリルアミド(19/1)溶液と 50 mL の 10x TBE(890 mM Tris-HCl、890 mM ホウ酸塩、20 mM EDTA、pH 8)を加えます。
- ビーカーを攪拌プレートに置き、攪拌棒で溶液を混合します。ミキシング中は、飛沫や汚染を防ぐために、ビーカーをアルミホイルで覆ってください。
- 尿素が完全に溶解し、溶液が透明になるまで溶液を混合します。
注: この手順には何時間もかかる場合があります。尿素の溶解を促進するために、所望の最終容量を超えずに少量の水を加えます。 - 攪拌棒を取り外します。溶液をシリンダーに注ぎ、500 mLの正確な最終容量まで水を加えます。
- ゲル装置の設置
- 2枚のプレート(1枚はノッチ付き、もう1枚はノッチなし)を70%エタノールで洗浄し、乾燥させてから、プレートをジメチルジクロロシラン溶液で処理します。
注:シラン化はスキップできますが、ゲルサンドイッチを分解するときにプレートの1つからゲルを放出するのに役立ちます。
注意:シラン化溶液は手袋で取り扱い、ドラフト内でこの溶液でプレート処理を行ってください。 - 0.4mmのスペーサーを長い方のプレートの長い方の端に沿って置き、短いプレートをもう片方のプレートの上に置き、2つのプレートを下部に合わせます。
- 紙テープを上面以外のすべての端に沿って何層にも重ねます。
- 鋳造中の漏れを防ぐために、ゲルの底にテープの層を追加します。
- サプライヤーの指示に従って、ガラスサンドイッチの側面を清潔なクランプでクリップします(サプライヤーによって、使用する装置、サンドイッチクランプ、およびガスケットがわずかに異なります)。
- 2枚のプレート(1枚はノッチ付き、もう1枚はノッチなし)を70%エタノールで洗浄し、乾燥させてから、プレートをジメチルジクロロシラン溶液で処理します。
- ゲルを注ぐ
注:ポリアクリルアミド重合は温度に敏感であるため、ゲルを室温(25°C)で注いでください。- 使用直前に、ビーカーに、あらかじめ調製した変性ポリアクリルアミド溶液80 mL(ステップ4.1)、10% m/V過硫酸アンモニウム(APS)溶液450 μL、テトラメチルエチレンジアミン(TEMED)45 μLを注ぎます。
- 溶液を混合し、50 mLのシリンジを使用してガラスプレートの間にすばやく注ぎます。気泡を避けながら、ガラス板の間に必要な数のウェルで櫛を導入します。必要に応じて、ゲル溶液を加えてサンドイッチを完全に満たします。コームに4つのクランプを配置して押し下げ、ウェルを均等に分配できるようにします。
- ゲルを少なくとも45分間重合させます。
- ゲルのランニング
- 重合後、クランプと紙テープの層をすべて取り除きます。櫛をゆっくりと取り外し、蒸留水で井戸を徹底的にすすいでください。
- 特定のサプライヤーの指示に従って、ゲルサンドイッチを垂直ゲル電気泳動装置に正しく配置します。
- TBEランニングバッファー(1x:89 mM Tris-HCl、89 mM ホウ酸塩、2 mM EDTA、pH 8)を脱イオン水で調製し、上部と下部の両方のリザーバーにバッファーを充填します。
- 50 Wで少なくとも30分間、ゲル電気泳動のプレランを実行して、プレートをウォームアップします。
- 超純水に変性ゲルローディングバッファー(DGLB:1 M Tris-HCl、80%ホルムアミド、50%グリセロール、0.05%ブロモフェノールブルー)を調製します。
注:GLBは、オリゴヌクレオチドサンプルのゲルシステムへの移動を追跡し、サンプルをゲルのウェルにロードすることができます。変性剤ホルムアミドの存在により、非変性PAGEでも、サイズに応じてDNA種を分離することができます。 - 乾燥したサンプル(ステップ 3.8 のサンプル)を 5 μL の DGLB に再懸濁します。
- サンプルをロードする前に、上部バッファーチャンバー内の小型シリンジとTBEバッファーを使用してウェルを洗浄し、ウェルから尿素を除去します。
注意: この手順を数回繰り返してウェルを正確に洗浄し、解釈が困難なバンドを回避します。 - サンプルをクリーンウェルにロードし、ロードの順序をメモします。
- ゲル電気泳動を 50 W で 2 時間、または少なくともブロモフェノールブルー色素がゲルの 2/3 まで実行します。
- ゲルのイメージング
- 電気泳動後、電源を切り、ガラスサンドイッチを取り外し、ガラスを清掃します。
- FAM標識オリゴヌクレオチドバンドの蛍光をゲルイメージャーでスキャンして検出します。
結果
図 2 は、3 つの異なる構造に折りたたまれた TBA オリゴヌクレオチドの B-CeP 1 を使用したプロトコルに記載されているように、実施されたケミカルマッピングアッセイの代表的な結果を示しています。TBA(G4-TBA)のG-四重鎖配列は、オリゴヌクレオチドをBPE中でK+カチオンの存在下で折りたたむことによって得られたが、同じTBA配列の一本鎖型(ssTBA)はカリウム非存在...
ディスカッション
G-四重鎖は、通常、グアニンに富むDNA配列内で折りたたまれる核酸二次構造であり、遺伝的制御や疾患との関連から重要な研究対象となっています。B-CePによるケミカルマッピングは、DNA G4の特性評価に有用なプロトコルであり、生理学的塩条件下でのG-テトラッドの形成に関与するグアニン塩基を同定するために使用できます。
このプロトコルで使用される化学プロー?...
開示事項
著者には開示すべき利益相反はありません。
謝辞
この研究は、パドヴァ大学薬理科学部(PRIDJ-BIRD2019)の支援を受けました。
資料
| Name | Company | Catalog Number | Comments |
| Acrylamide/bis-acrylamide solution 40% | Applichem | A3658 | R45-46-20/21-25-36/38-43-48/23/ 24/25-62 |
| Ammonium per-sulfate (APS) | Sigma Aldrich | A7460 | |
| Analytical balance | Mettler Toledo | ||
| Autoclave | pbi international | ||
| Boric acid | Sigma Aldrich | B0252 | |
| Bromophenol blue Brilliant blue R | Sigma Aldrich | B0149 | |
| di-Sodium hydrogen phosphate dodecahydrate | Fluka | 71649 | |
| DMSO | Sigma Aldrich | 276855 | |
| DNA oligonucleotides | Integrated DNA Technologies | synthesis of custom sequences | |
| EDTA disodium | Sigma Aldrich | E5134 | |
| Formamide | Fluka | 40248 | H351-360D-373 |
| Gel imager | GE Healtcare | STORM B40 | |
| Glycerol | Sigma Aldrich | G5516 | |
| Micro tubes 0.5 mL | Sarstedt | 72.704 | |
| Potassium Chloride | Sigma Aldrich | P9541 | |
| Sequencing apparatus | Biometra | Model S2 | |
| Silanization solution I | Fluka | 85126 | H225, 314, 318, 336, 304, 400, 410 |
| Sodium phosphate monobasic | Carlo Erba | 480086 | |
| Speedvac concentrator | Thermo Scientific | Savant DNA 120 | |
| TEMED | Fluka | 87689 | R11-21/22-23-34 |
| Tris-HCl | MERCK | 1.08387.2500 | |
| Urea | Sigma Aldrich | 51456 | |
| UV-Vis spectrophotometer | Thermo Scientific | Nanodrop 1000 |
参考文献
- Davis, J. T. G-quartets 40 years later: from 5'-GMP to molecular biology and supramolecular chemistry. Angewandte Chemie. 43 (6), 668-698 (2004).
- Varshney, D., Spiegel, J., Zyner, K., Tannahill, D., Balasubramanian, S. The regulation and functions of DNA and RNA G-quadruplexes. Nature Reviews Molecular Cell Biology. 21 (8), 459-474 (2020).
- Chambers, V. S., et al. High-throughput sequencing of DNA G-quadruplex structures in the human genome. Nature Biotechnology. 33 (8), 877-881 (2015).
- Zuravka, I., Sosic, A., Gatto, B., Gottlich, R. Synthesis and evaluation of a bis-3-chloropiperidine derivative incorporating an anthraquinone pharmacophore. Bioorganic & Medicinal Chemistry Letters. 25 (20), 4606-4609 (2015).
- Zuravka, I., Roesmann, R., Sosic, A., Gottlich, R., Gatto, B. Bis-3-chloropiperidines containing bridging lysine linkers: Influence of side chain structure on DNA alkylating activity. Bioorganic & Medicinal Chemistry. 23 (6), 1241-1250 (2015).
- Zuravka, I., et al. Synthesis and DNA cleavage activity of bis-3-chloropiperidines as alkylating agents. ChemMedChem. 9 (9), 2178-2185 (2014).
- Sosic, A., Gottlich, R., Fabris, D., Gatto, B. B-CePs as cross-linking probes for the investigation of RNA higher-order structure. Nucleic Acids Research. 49 (12), 6660-6672 (2021).
- Sosic, A., et al. Bis-3-chloropiperidines targeting TAR RNA as a novel strategy to impair the HIV-1 nucleocapsid protein. Molecules. 26 (7), 1874 (2021).
- Sosic, A., et al. In vitro evaluation of bis-3-chloropiperidines as RNA modulators targeting TAR and TAR-protein interaction. International Journal of Molecular Sciences. 23 (2), 582 (2022).
- Sosic, A., et al. Direct and topoisomerase II mediated DNA damage by bis-3-chloropiperidines: The importance of being an earnest G. ChemMedChem. 12 (17), 1471-1479 (2017).
- Bock, L. C., Griffin, L. C., Latham, J. A., Vermaas, E. H., Toole, J. J. Selection of single-stranded DNA molecules that bind and inhibit human thrombin. Nature. 355 (6360), 564-566 (1992).
- Paborsky, L. R., McCurdy, S. N., Griffin, L. C., Toole, J. J., Leung, L. L. The single-stranded DNA aptamer-binding site of human thrombin. The Journal of Biological Chemistry. 268 (28), 20808-20811 (1993).
- Carraro, C., et al. Behind the mirror: chirality tunes the reactivity and cytotoxicity of chloropiperidines as potential anticancer agents. ACS Medicinal Chemistry Letters. 10 (4), 552-557 (2019).
- Carraro, C., et al. Appended aromatic moieties in flexible bis-3-chloropiperidines confer tropism against pancreatic cancer cells. ChemMedChem. 16 (5), 860-868 (2021).
- Kypr, J., Kejnovska, I., Renciuk, D., Vorlickova, M. Circular dichroism and conformational polymorphism of DNA. Nucleic Acids Research. 37 (6), 1713-1725 (2009).
- Onel, B., Wu, G., Sun, D., Lin, C., Yang, D. Electrophoretic mobility shift assay and dimethyl sulfate footprinting for characterization of G-quadruplexes and G-quadruplex-protein complexes. Methods in Molecular Biology. 2035, 201-222 (2019).
転載および許可
このJoVE論文のテキスト又は図を再利用するための許可を申請します
許可を申請さらに記事を探す
This article has been published
Video Coming Soon
Copyright © 2023 MyJoVE Corporation. All rights reserved