Bu içeriği görüntülemek için JoVE aboneliği gereklidir. Oturum açın veya ücretsiz deneme sürümünü başlatın.
Method Article
Prodrug-Boya Nanoassment'lerinin Kolay Hazırlanması ve Fotoaktivasyonu
Bu Makalede
Özet
Bu protokol, ışığa duyarlı bir ön ilaç-boya nanomontajının imalatını ve karakterizasyonunu açıklar. Işık ışınlama kurulumu da dahil olmak üzere, ışıkla tetiklenen sökme yoluyla nanopartiküllerden ilaç salınımı metodolojisi açıkça tanımlanmıştır. Işık ışınlamasını takiben nanopartiküllerden salınan ilaçlar, insan kolorektal tümör hücreleri üzerinde mükemmel anti-proliferasyon etkileri göstermiştir.
Özet
Kendi kendine montaj, nano ölçekli ilaç dağıtım sistemleri oluşturmak için basit ama güvenilir bir yöntemdir. Fotoaktivatable ön ilaçlar, ışık ışınlaması ile modüle edilen hedef bölgelerdeki nanotaşıyıcılardan kontrol edilebilir ilaç salınımını sağlar. Bu protokolde, fotoaktivatable ön ilaç-boya nanopartiküllerinin moleküler kendi kendine montaj yoluyla üretilmesi için kolay bir yöntem sunulmaktadır. Ön ilaç sentezi, nanopartikül üretimi, nanomontajın fiziksel karakterizasyonu, fotobölünme gösterimi ve in vitro sitotoksisite doğrulaması için prosedürler ayrıntılı olarak açıklanmaktadır. İlk olarak fotobölünebilir bir bor-dipyrromethene-chlorambucil (BC) ön ilacı sentezlendi. BC ve yakın kızılötesi bir boya olan IR-783, optimize edilmiş bir oranda, nanopartiküllere (IR783 / BC NP'ler) kendiliğinden monte edilebilir. Sentezlenen nanopartiküller ortalama 87.22 nm boyuta ve -29.8 mV'luk bir yüzey yüküne sahipti. Nanopartiküller, iletim elektronik mikroskobu ile gözlemlenebilen ışık ışınlaması üzerine demonte edildi. BC'nin fotobölünmesi 10 dakika içinde tamamlandı ve klorambusil için% 22'lik bir geri kazanım verimliliği elde edildi. Nanopartiküller, ışınlanmamış nanopartiküller ve ışınlanmış serbest BC ön ilacı ile karşılaştırıldığında, 530 nm'de ışık ışınlaması altında gelişmiş sitotoksisite göstermiştir. Bu protokol, ışığa duyarlı ilaç taşıyıcı sistemlerin inşası ve değerlendirilmesi için bir referans sağlar.
Giriş
Kemoterapi, kanser hücrelerini öldürmek için sitotoksik ajanlar kullanan ve böylece tümör büyümesini inhibe eden yaygın bir kanser tedavisidir1. Bununla birlikte, hastalar kemoterapi ilaçlarının hedef dışı emilimine bağlı olarak kardiyotoksisite ve hepatotoksisite gibi yan etkilerden muzdarip olabilirler 2,3,4. Bu nedenle, tümörlerde ilaç salınımının/aktivasyonunun mekansal zamansal kontrolü yoluyla lokalize ilaç verilmesi, normal dokularda ilaç maruziyetini en aza indirmek için gereklidir.
Ön ilaçlar, normal dokularda azalmış toksisite sergileyen, ancak aktivasyon üzerine hastalıklı lezyonlarda etkilerini koruyan kimyasal olarak modifiye edilmiş ilaçlardır 5,6. Ön ilaçlar, pH7,8, enzimler 9,10, ultrason 11,12, ısı 13 ve ışık14,15,1 6 gibi çeşitli uyaranlara yanıt verebilir ve ebeveyn ilaçlarını özellikle lezyonlarda serbest bırakabilir. Bununla birlikte, birçok ön ilaç, zayıf çözünürlük, yanlış emilim oranı ve erken metabolik yıkım gibi gelişimlerini sınırlayabilecek doğal dezavantajlar sergiler17. Bu bağlamda, ön ilaç nanomontajlarının oluşumu, yan etkilerin azalması, yerinde ilaç salınımı, daha iyi retansiyon ve tedavi ve görüntüleme kombinasyonu gibi avantajlar sunarak, bu nanomontajlar için büyük uygulama potansiyeline işaret etmektedir. Doksorubisin ön ilaç nanosferleri, kurkumin prodrug miselleri ve camptothecin prodrug nanofiberleri18 dahil olmak üzere hastalık tedavisi için birçok prodrug nanoassemblies geliştirilmiştir.
Bu protokolde, yüksek ön ilaç içeriği, iyi su dağılabilirliği, uzun süreli stabilite ve hassas yanıt verme kabiliyeti sergileyen ön ilaç-boya nanomontajlarının hazırlanması için basit bir yöntem sunuyoruz. IR783, nanomontajların stabilizatörü olarak hizmet edebilen suda çözünür bir yakın kızılötesi boyadır19. Nanomontajın diğer bileşeni, iki ana nedenden dolayı tasarlanmış bir ön ilaç olan bor-dipyrromethene-chlorambucil'dir (BODIPY-Cb, BC). Klorambucil (Cb) in vivo sistemik toksisite gösterdiğinden, ön ilaç formu toksisitesini azaltabilir20. BC ön ilacı, hastalık lezyonlarına yönelik 530 nm ışık ışınlaması kullanılarak fotoparçalanabilir ve Cb'nin lokal salınımını sağlar. Öte yandan, Cb sulu ortamlarda hidrolize eğilimlidir ve bir ön ilaç formu21'e dönüştürülerek korunabilir. Bu nedenle, BC ön ilacı ve IR-783 boyasının birlikte montajının istikrarlı ve etkili bir ilaç dağıtım nanosistemi oluşturması bekleniyordu (Şekil 1A). Bu ön ilaç boyası nanomontajı, ön ilaç moleküllerinin dağılabilirliğini ve stabilitesini arttırır, bu da ışıkla kontrol edilebilir ilaç dağıtımında uygulama potansiyelini düşündürmektedir. BC ön ilacının fotobölünmesi, nanopartiküllerin sökülmesini ve lezyonlarda Cb'nin ışık kontrollü salınımını sağlar (Ek Şekil 1).
Protokol
1. Bor-dipirometen-klorambucil (BC) ön ilacının sentezi (Şekil 2)22
- BODIPY-OAc sentezi
- 1.903 g 2,4-dimetil pirrol tartın ve azot atmosferi altında yuvarlak tabanlı bir şişede 20 mL susuz diklorometan (DCM) içinde çözün. 1.638 g asetoksi asetil klorür tartın ve çözeltiye damla damla ekleyin. Oda sıcaklığında 10 dakika karıştırmaya devam edin ve ardından çözeltiyi 40 ° C'de 1 saat geri çekin.
- Karışımı oda sıcaklığına soğutun. 5.170 g N,N-diizopropiletilamin (DIPEA) tartın ve karıştırarak karışıma damla damla ekleyin. 30 dakika sonra, 5.677 g bor triflorür dietil eterat (BF3· OEt2), çözeltiye damla damla ekleyin ve 30 dakika daha karıştırmaya devam edin.
- Karışıma 10 g silika jel (200-400 ağ) ekleyin ve çözücüyü 45 ° C'de döner buharlaştırma ile çıkarın. Silika jel kuru toza döndüğünde buharlaşmayı durdurun.
- Kartuşun altına bir frit ekleyin (bkz. Silika jeli (adım 1.1.3'ten itibaren) kartuşa doldurun ve ardından doldurulmuş jelin üstündeki kartuşa başka bir frit ekleyin.
- Kartuşu flaş kromatografi sistemine bağlı tasmaya sabitleyin (bkz. Malzeme Tablosu) ve kilitlemek için çevirin. Kartuşu flaş kromatografi sistemindeki altı valfin üzerine takın ve valfin altına bir flaş sütunu (bkz.
- Kromatografi cihazını çalıştırın ve algılama dalga boyları olarak 515 nm ve 365 nm'yi ayarlayın. 4/3 (v/v) hekzan/DCM ile elüzyon gerçekleştirin. 515 nm sinyal göründüğünde elüent fraksiyonları toplayın.
- Solvent toplama şişesinde daha fazla çözücü toplanmayana kadar 40 °C'de döner buharlaştırma ile çözücüyü toplanan fraksiyonlardan uzaklaştırın. Solventin geri kalanını çıkarmak için katı ürünü gece boyunca vakumlu bir kurutma odasına yerleştirin.
- BODIPY-OH sentezi
- 1.120 g BODIPY-OAc (adım 1.1'de sentezlenmiş) tartın ve oda sıcaklığında 70 mL tetrahidrofuran (THF) içinde tamamen folyo ile kaplanmış olarak çözün. BODIPY-OAc çözeltisine damla damla 70 mL 0,1 M LiOH sulu çözelti ekleyin.
- Karışımı 30 dakika karıştırın ve çözücü toplama şişesinde daha fazla çözücü toplanmayana kadar çözücüyü 40 ° C'de döner buharlaştırma ile çıkarın. Suyu gidermek için kalıntıyı gece boyunca vakumlu bir kurutma odasına yerleştirin.
- Kuru kalıntıyı 30 mL DCM içinde çözün ve çözeltiye 10 g silika jel ekleyin. Çözücüyü 40 °C'de döner buharlaştırma ile çıkarın. Silika jel kuru toza döndüğünde buharlaşmayı durdurun.
- BODIPY-OH ürününü kolon kromatografisi ile saflaştırın, 1.1.4 ila 1.1.6 arasındaki adımları izleyin, yalnızca DCM elüent olarak.
- Farklı elüsyon zaman noktalarında toplanan kesirleri, ince tabaka kromatografisi (TLC) üzerinde BODIPY-OAc'nin THF çözeltisi ile karşılaştırın ve ürünü tanımlayın23.
- Salınan fraksiyonun 3-4 μL'sini ve BODIPY-OAc çözeltisini TLC plakasının bir kenarında aynı yükseklikte ayrı ayrı tespit edin. TLC plakasını 1 mL DCM içeren bir cam odaya yerleştirin, lekeli kenarı DCM çözücüsüne batırın, ancak iki nokta çözücünün dışında tutun.
- DCM çözücü plakanın yüksekliğinin yarısından fazlasına ulaştığında TLC plakasını çıkarın. BODIPY-OAc noktasından farklı bir yükseklikte bir TLC noktasına sahip elütlenmiş fraksiyonu seçin.
- BODIPY-OH ürününü elde etmek için çözücüyü 40 °C'de (adım 1.1.7) döner buharlaştırma ile çıkarın.
- BODIPY-(Me)2-OH Sentezi
- 313 mg BODIPY-OH tartın ve bir azot atmosferi altında karanlıkta 35 mL susuz dietil eter içinde çözün. Çözeltiye damla damla 3.75 mL metil magnezyum iyodür (dietil eter içinde 3 M) ekleyin ve oda sıcaklığında 3 saat boyunca karıştırmaya devam edin.
- Damla damla 3,5 mL su ekleyerek reaksiyonu söndürün.
- Karışımı DCM ve su ile çıkarın.
- Karışımı 125 mL'lik bir ayırıcı huniye aktarın. Karışıma 20 mL DCM ekleyin.
- Ayırıcı hunisinin kapağını kapatın. Huni yaklaşık 45° eğin ve huniyi hafifçe sallayın. Söndürmek için kapağı açın. Bu adımı 3 kez tekrarlayın ve 3 dakika bekletin.
- Alt valfi açın ve alt organik fazı bir beherde toplayın.
- Sulu faza 30 mL DCM ekleyin. Ekstraksiyonu (adım 1.3.3.2 ve 1.3.3.3) her seferinde 30 mL DCM ile 3 kez tekrarlayın.
- Organik fazı gece boyunca kurutmak için toplanan organik faza 10 g katı Na2SO4 ekleyin.
- Bir filtreleme şişesini kauçuk tüplü bir vakum pompasına bağlayın. Büchner hunisine bir parça filtre kağıdı yerleştirin ve huniyi şişenin üstüne yerleştirin. Filtre kağıdını 1 mL DCM ile ıslatın, karışımı huniye aktarın ve vakum pompasını açın. Organik çözeltiyi şişede toplayın.
- Organik çözeltiye 10 g silika jel ekleyin. Silika jel kuru toza dönene kadar organik çözücüyü 40 ° C'de döner buharlaştırma ile uzaklaştırın. BODIPY-(Me)2-OH ürününü kolon kromatografisi ile (adım 1.1.4 ila 1.1.6) elüent olarak hekzan/DCM = 1/1 (v/v) ile saflaştırın.
- Adım 1.2.5'te (BODIPY-OH'den farklı bir yükseklikte TLC noktası) açıklandığı gibi TLC analizini kullanarak ürünü içeren salınımlı fraksiyonları seçin. Ürünü adım 1.1.7'de açıklandığı gibi elde etmek için çözücüyü 40 °C'de döner buharlaştırma ile çıkarın.
- BODIPY-(Me)2-I 2-OH Sentezi
- 41 mg BODIPY-(Me)2-OH tartın ve bir azot atmosferi altında karanlıkta 2.5 mL susuz THF içinde çözün. 74 mg N-iyodosüksinamid tartın ve 1 mL susuz THF içinde çözün.
- N-iyodosüksinamid çözeltisini BODIPY-(Me)2-OH çözeltisine damla damla ekleyin. Oda sıcaklığında 3,5 saat karıştırdıktan sonra, döner evaporatör üzerindeki çözücü toplama şişesinde daha fazla çözücü toplanmayana kadar çözücüyü 40 °C'de döner buharlaştırma ile çıkarın.
- Kalıntıyı 10 mL DCM içinde çözün ve adım 1.3.3'te açıklandığı gibi her seferinde 30 mL su ile 3 kez yıkayın. Organik fazı Na2SO 4 ile kurutun (adım 1.3.4 ve 1.3.5). BODIPY-(Me)2-I 2-OH ürününü elde etmek için çözücüyü 40 °C'de (adım 1.1.7) döner buharlaştırma ile çıkarın.
- BODIPY-Cb sentezi
- 85 mg klorambucil tartın ve bir azot atmosferi altında karanlıkta 2 mL susuz DCM içinde çözün. 69 mg N , N'-dicyclohexylcarbodiimide tartın ve 1 mL susuz DCM içinde çözün. 10 dakika karıştırarak klorambucil çözeltisine damla damla ekleyin.
- 1.7 mg 4-dimetilaminopiridin 0.5 mL susuz DCM içinde çözülür. Bu çözeltiyi karışıma ekleyin ve oda sıcaklığında 10 dakika karıştırmaya devam edin. Daha sonra 2 mL susuz DCM içinde çözülmüş 73 mg BODIPY-(Me)2-I 2-OH ekleyin ve2 saat boyunca karıştırmaya devam edin.
- Karışıma 10 g silika jel ekleyin ve çözücüyü 40 ° C'de döner buharlaştırma ile çıkarın. Silika jel kuru toza döndüğünde buharlaşmayı durdurun. BODIPY-Cb ürününü kolon kromatografisi (adım 1.1.4 ila 1.1.6, 540 nm ve 365 nm sinyal dalga boyu) ile hekzan/DCM = 7/3 (v/v) ile elüent olarak saflaştırın.
- TLC analizini kullanarak BODIPY-(Me)2-I 2-OH'den farklı ürünü içeren salınımlı fraksiyonları seçin (adım 1.2.5). BODIPY-Cb ürününü elde etmek için çözücüyü 40 °C'de (adım 1.1.7) döner buharlaştırma ile uzaklaştırın.
2. IR783 / BC NP'lerin flaş çökeltme yöntemi ile hazırlanması
- BC ön ilacının (BODIPY-Cb) 10 mg'ını tartın ve 10 mg / mL'lik bir stok çözeltisi elde etmek için 1.5 mL'lik bir mikrotüp içinde 1 mL DMSO içinde çözün. BC çözeltisini folyo ile örtün.
- 300 μL 0.4 mg / mL IR-783'ü filtrelenmiş deiyonize suda 1.5 mL'lik bir mikrotüp içinde hazırlayın. Bu mikrotüpü 1.500 rpm'de bir vorteks karıştırıcıya yerleştirin.
- DMSO'daki BC çözeltisinden 20 μL'sini, 20 μL pipet kullanarak sabit bir hızda 10 sn üzerinde IR-783 çözeltisine ekleyin. Pipet ucunun ucu mikrotüpün iç duvarına temas etmelidir (Şekil 1B).
- IR783/BC NP çözeltisini elde etmek için mikrotüpü vorteks karıştırıcıda 30 saniye daha tutun. Ardından, nanopartikül çözeltisini tamamen folyo ile kaplı bir rafa yerleştirin.
- Agregaları gidermek için elde edilen IR783/BC NP çözeltisini 2.000 x g ve 4 °C'de 10 dakika boyunca santrifüj edin. Peletin rahatsız edilmemesi için tüpün içinde ~ 20 μL bırakarak süpernatanı toplayın. Pelet atın.
- Süpernatantı 30.000 x g ve 4 ° C'de 30 dakika boyunca iki kez santrifüj edin ve nanopartikül çökeltisini her iki santrifüjden toplayın. Nanopartikülleri 300 μL 1x PBS'de yeniden askıya alın.
NOT: DMSO'daki hidrofobik BC ön ilacı, vorteksleme ile suda dağıldığında, DMSO su ile çözülür ve ön ilaç molekülleri, yerel aşırı doygunluk durumu24 altında kendilerini sabit tutmak için nano ölçekli düzenekler oluşturma eğilimindedir. - IR-783 ve BC içeriğini, Tablo 1'de gösterilen elüsyon yöntemini kullanarak yüksek performanslı sıvı kromatografisi (HPLC) ile ölçün.
NOT: HPLC numunesi, eşit hacimde nanopartikül çözeltisi ve asetonitrilin karıştırılmasıyla hazırlanır. Enjeksiyon hacmi 20 μL'dir. Klorambucil ve BC ön ilacı için algılama dalga boyu 260 nm'dir ve IR783 için algılama dalga boyu 783 nm'dir. HPLC kolonu, 2,7 μm partikül boyutuna ve 120 şgözenek boyutuna sahip analitik 4,6 mm (iç çap) x 100 mm (uzunluk) C18 sütundur. - İlaç kapsülleme verimliliğini (EE%) ve yükleme kapasitesini (LC%) aşağıdaki denklemlere göre hesaplayın:

| Süre (min) | Asetonitril (%) | Su (%) |
| 0 | 20 | 80 |
| 5 | 20 | 80 |
| 30 | 95 | 5 |
| 35 | 95 | 5 |
Tablo 1: BC ön ilacının kalitatif ve kantitatif analizi için HPLC yöntemi ve fotobölünmesi . İzin alınarak çoğaltılmıştır25. Telif Hakkı 2022, Wiley.
3. IR783/BC NP'lerin karakterizasyonu
- IR783/BC NP'lerin ortalama boyutunu dinamik ışık saçılımı (DLS) cihazıyla ölçün (bkz. Bir küvete 200 μL IR783/BC NP çözeltisi ekleyin ve küveti ölçüm için tutucuya yerleştirin. Ölçüm türünü 'boyut' ve ölçüm sıcaklığını 25 °C olarak ayarlayın. Her ölçüm için 20 s süreli üç ölçüm gerçekleştirin.
- IR783/BC NP'lerin yüzey yükünü, zeta potansiyeli test küveti kullanarak DLS cihazıyla ölçün.
- 25 μL IR783/BC NP çözeltisini 1,5 mL'lik bir mikrotüp içinde 725 μL deiyonize su ile seyreltin ve çözeltiyi zeta potansiyeli olan bir test küvetine ekleyin. Küveti numune oluğuna yerleştirin. Numune oluğunu kapatın.
- Ölçüm türünü 'zeta potansiyeli' ve ölçüm sıcaklığını 25 °C olarak ayarlayın. 10 ölçüm yapın.
- İletim elektron mikroskobu (TEM) görüntülemesi için numuneleri hazırlayın. Bir bakır ızgara (300 ağ) üzerindeki bir delikli karbon film parçasına 10 μL IR783 / BC NP çözeltisi ekleyin ve 7 μL'yi çıkarın. otomatik buharlaşma için gece boyunca film üzerinde 3 μL çözelti bırakın.
NOT: NP çözeltisinin 10 μL'sinin eklenmesi ve ardından 7 μL'nin çıkarılması, damlacığın film üzerinde daha geniş bir alanı kaplamasını sağlar.
4. IR783 / BC NP'lerin Fotoaktivasyonu
- Demir ayaklı bir LED lamba (530 nm; bakınız Malzeme Tablosu) kurun, böylece ışık doğrudan çalışma zeminine bakacaktır. Doğrudan LED lambanın altına entegre bir küre fotodiyot fotometresi (bkz. Malzeme Tablosu) yerleştirin.
NOT: Çevresel ışığın etkisini önlemek için, tüm ışık ışınlama deneyleri karanlık bir odada gerçekleştirilir. - LED lambasını açın ve fotometrenin kapağını açın. Işınlamayı kaydedin ve ilgili yazılımı kullanarak lamba parametrelerini ayarlayın (bkz. Işınımı 50 mW/cm2 olarak ayarlamak için giriş akımını (mA) ayarlayın.
NOT: Işın, LED lamba ile fotometre arasındaki mesafeden de etkilenir. Burada kullanılan kurulumda (Şekil 3A,B) mesafe 5 cm'de sabitlenmiştir. - IR783/BC NP çözeltisini deiyonize su ile BC konsantrasyonuna göre 50 μM'ye seyreltin. 1,5 mL'lik bir mikrotüpe 200 μL IR783/BC NP çözeltisi ekleyin. Tüpü, mikrotüpün oluk bağlantı boyutuna ve adım 4.1'deki fotometre ile aynı yüksekliğe sahip bir köpük blok üzerine yerleştirin (Şekil 3C, D).
- Tüpün kapağını açın. LED lambayı açın ve nanopartikül çözeltisini 1, 2, 3, 5, 7 ve 10 dakika boyunca ışınlayın.
- Işık ışınlamasından sonra HPLC ile BC tüketimini ve Cb salınımını sayısallaştırın. Aşağıdaki denklemleri kullanarak kalan BC ve Cb salınımının yüzdesini hesaplayın:

5. IR783 / BC NP'lerin ışık ışınlaması ile ve ışık ışınlaması olmadan sitotoksisitesinin test edilmesi
- RPMI 1640 ortamında, 37 ° C'de% 5 CO 2 atmosferinde% 10 fetal sığır serumu ve% 1 Penisilin-Streptomisin (tam ortam) içeren kültür HCT116 hücreleri (insan kolorektal tümör hücre hattı) (90 mm'lik bir hücre kültürü kabında çanak başına ~2 x 106 hücre). Rutin olarak hücreleri her 2-3 günde bir alt kültüre alın.
NOT: HCT116 bir insan kolon hücre hattıdır. HeLa, MCF7 ve A549 hücreleri gibi diğer kanser hücreleriyle karşılaştırıldığında, HCT-116 hücreleri, IR783 tarafından hedeflenebilen ve IR783 / BC NP'lerin hücresel alımını artırabilen daha yüksek bir kaveolin-125 seviyesini eksprese eder. - HCT116 hücrelerini 96 delikli plakalarda RPMI 1640 tam ortam ile kuyu başına 104 hücre yoğunluğunda plakalayın.
- Hücre akıcılığı% 50'yi aştığında ortamı kültür kabından aspire edin. Hücreleri 1x PBS ile yıkayın ve PBS'yi çıkarın. 1 mL% 0.25 tripsin çözeltisi ekleyin ve% 5 CO2 inkübatörde 37 ° C'de inkübe edin.
- 3 dakika sonra, tripsin sindirimini söndürmek için 2 mL tam ortam ekleyin. Hücreleri yeniden askıya alın, hücre süspansiyonunu 15 mL'lik bir santrifüjleme tüpüne aktarın ve 3 dakika boyunca 300 x g'de santrifüjleyin. Süpernatantı atın ve hücre peletini 1 mL tam ortamda yeniden askıya alın.
- Hücre süspansiyonunun 10 μL'sini tam ortamla 200 μL'ye seyreltin. Bir hemositometreye 10 μL yerleştirin ve bir kapak kayması ile kapatın.
- Hemositometreyi mikroskop altında gözlemleyin (göz merceği: 10x; objektif lens: 4x). Dört köşe karesindeki ve merkezdeki hücre numaralarını sayın ve kaydedin. Formülü kullanarak hücre konsantrasyonunu hesaplayın:
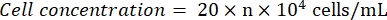
Burada n = beş karenin hücre sayılarının ortalaması. - Hücre süspansiyonunu 1 x 105 hücre/mL'ye seyreltin. Hücreleri tohumlamak için 96 delikli bir plakaya kuyucuk başına 100 μL hücre süspansiyonu ekleyin. Tohumlanmamış kuyucuklara kuyucuk başına 100 μL PBS ekleyin.
- Hücreleri (1) 0.1-150 μM serbest BC, (2) 0.1-150 μM IR783/BC NP'ler (BC konsantrasyonuna göre), (3) 0.1-150 μM serbest BC ışık ışınlaması veya (4) 0.1-150 μM IR783/BC NP'ler (BC konsantrasyonuna göre) ışık ışınlaması ile tedavi edin. Hücreleri 37 ° C'de% 5 CO2 inkübatörde 6 saat boyunca inkübe edin.
NOT: Serbest BC ve IR783/BC NP çözümleri, ilgili stok çözümlerinden komple ortamla seyreltilir. - 6 saatlik inkübasyondan sonra, ön ilaç / nanopartikül içeren ortamı taze tam ortamla değiştirin. Işınlanmayan Grup 1 ve 2'yi karanlıkta 24 saat boyunca inkübe edin. Grup 3 ve 4 için, hücreleri 5 dakika boyunca 530 nm LED lamba (50 mW /cm2) ile ışınlayın ve 24 saat boyunca inkübe edin.
NOT: Adım 4.1'deki fotometre ile aynı yüksekliği sağlamak için hücre plakaları bir köpük blok üzerine yerleştirilir. - 3-(4,5-dimetiltiazol-2-yl)-2,5-difenil tetrazolium bromür (MTT) testi ile hücre canlılığını belirleyin.
- BC veya nanopartikül işleminden sonra, her bir oyuğa 10 μL MTT (PBS'de 10 mg / mL) ekleyin ve plakaları 3 saat boyunca 37 ° C'de inkübe edin. Ardından, ortamı çıkarın ve her bir kuyucuğa 100 μL DMSO ekleyin. Absorbansı 490 nm, 570 nm ve 630 nm'de bir mikroplaka okuyucu ile okuyun.
- Aşağıdaki denklemi kullanarak hücre canlılığını hesaplayın:

NOT: Analiz için her grubun dört bağımsız deneyi (n = 4) yapılır. OD490 , hücre canlılığının hesaplanmasında OD570-OD 630 ile değiştirilebilir.
Sonuçlar
IR783 / BC NP'ler bu çalışmada bir flaş çökeltme yöntemi kullanılarak başarıyla üretildi. Sentezlenen IR783/BC NP'ler mor bir çözelti olarak sunulurken, IR783'ün sulu çözeltisi maviydi (Şekil 4A). Şekil 4B'de gösterildiği gibi, IR783 / BC NP'ler, 0.089'luk bir polidispersite indeksi (PDI) ile yaklaşık 87.22 nm'lik bir ortalama boyut sergiledi ve dar bir boyut dağılımı gösterdi. IR783 / NP'lerin yüzey yükü yaklaşık -29.8 mV idi (
Tartışmalar
Bu protokol, nanopartikül oluşumu için basit ve kullanışlı bir yaklaşım sunan ön ilaç-boya nanopartiküllerinin üretimi için basit bir flaş çökeltme yöntemini özetlemektedir. Bu yöntemde birkaç kritik adım vardır. İlk olarak, sentez, imalat ve karakterizasyonun tüm adımları için, BC ön ilacının çevresel ışıkla gereksiz fotobölünmesinden kaçınmak için mikrotüpler gibi kaplar folyo ile kaplanmalıdır. Ayrıca, flaş çökeltme adımında, IR-783 çözeltisini içeren mikrotüp, BC ö...
Açıklamalar
No.PCT/CN2021/081262 ile bir PCT başvurusu yapılmıştır.
Teşekkürler
Hong Kong Üniversitesi Li Ka Shing Tıp Fakültesi Çekirdek Tesisi'nin yardımını kabul ediyoruz. Hong Kong Üniversitesi'nden Profesör Chi-Ming Che'ye insan HCT116 hücre hattını sağladığı için teşekkür ederiz. Bu çalışma, Ming Wai Lau Onarıcı Tıp Merkezi Ortak Üye Programı ve Hong Kong Araştırma Hibeleri Konseyi (Erken Kariyer Programı, No. 27115220) tarafından desteklenmiştir.
Malzemeler
| Name | Company | Catalog Number | Comments |
| 1260 Infinity II HPLC | Agilent Technologies | ||
| 2,4-Dimethyl pyrrole | J&K Scientific | 315305 | |
| 3-(4,5-dimethylthiazol-2-yl)-2,5-diphenyl tetrazolium bromide(MTT) | Gibco | M6494 | |
| 4-Dimethylaminopyridine (4-DMAP) | J&K Scientific | 212279 | |
| 90 mm Petri Dish Clear Treated Sterile | SPL | 11090 | |
| 96-well Tissue Culture Plate Clear Treated Sterile | SPL | 30096 | |
| Acetoxyacetyl chloride | J&K Scientific | 192001 | |
| Boron trifluoride diethyl etherate | J&K Scientific | 921076 | |
| Büchner funnel | AS ONE | 3-6466-01 | |
| Chlorambucil | J&K Scientific | 321407-1G | |
| CM100 Transmission Electron Microscope | Philips | ||
| CombiFlash RF chromatography system | Teledyne ISCO | ||
| Dichloromethane | DUKSAN Pure Chemicals | JT9315-88 | |
| Dimethyl sulfoxide | DUKSAN Pure Chemicals | 2762 | |
| Disposable cuvette | Malvern Panalytical | DTS1070 | Zeta potential measurement |
| Disposable cuvette | Malvern Panalytical | ZEN0040 | |
| Empty Disposable Sample Load Cartridges | Teledyne ISCO | 693873225 | can hold up to 65 g |
| Fetal bovine serum | Gibco | 10270106 | |
| Filtering flask | AS ONE | 3-7089-03 | |
| Hexane | DUKSAN Pure Chemicals | 4198 | |
| Holey carbon film on copper grid | Beijing Zhongjingkeyi Technology Co.,Ltd | BZ10023a | |
| HPLC column (InfinityLab Poroshell 120) | Agilent Technologies | 695975-902T | |
| Integrating sphere photodiode power sensor | Thorlabs | S142C | |
| IR783 | Tokyo Chemical Industry (TCI) Co., Ltd | I1031 | |
| LED | Mightex | LCS-0530-15-11 | |
| LED Driver Control Panel V3.2.0 (Software) | Mightex | ||
| Lithium Hydroxide Anhydrous | TCI | L0225 | |
| Methylmagnesium iodide, 3M solution in diethyl ether | Aladdin | M140783 | |
| N,N-Diisopropyl ethyl amine (DIPEA) | J&K Scientific | 203402 | |
| N,N'-Dicyclohexylcarbodiimide (DCC) | J&K Scientific | 275928 | |
| penicillin–streptomycin | Gibco | 15140122 | |
| Phosphate-buffered saline (10×) | Sigma-Aldrich | P5493 | |
| Power and energy meter | Thorlabs | PM100 USB | |
| Rotavapor | BUCHI Rotavapor R300 | ||
| RMPI 1640 | Gibco | 21870076 | |
| Separatory funnel (125 mL) | Synthware | F474125L | |
| Silver Silica Gel Disposable Flash Columns, 40 g | Teledyne ISCO | 692203340 | |
| Sodium sulfate, anhydrous | Alfa Aesar | A19890 | |
| SpectraMax M4 | Molecular Devices LLC | ||
| Tetrahydrofuran (THF), anhydrous | J&K Scientific | 943616 | |
| Trypsin-EDTA (0.25%), phenol red | Gibco | 25200056 | |
| Vortex | DLAB Scientific Co., Ltd | MX-S | |
| Zetasizer Nano ZS90 | Malvern Instrument |
Referanslar
- Chabner, B. A., Roberts, T. G. Chemotherapy and the war on cancer. Nature Reviews Cancer. 5 (1), 65-72 (2005).
- Monsuez, J. -. J., Charniot, J. -. C., Vignat, N., Artigou, J. -. Y. Cardiac side-effects of cancer chemotherapy. International Journal of Cardiology. 144 (1), 3-15 (2010).
- Floyd, J., Mirza, I., Sachs, B., Perry, M. C. Hepatotoxicity of chemotherapy. Seminars in Oncology. 33 (1), 50-67 (2006).
- Bar-Joseph, H., Stemmer, S. M., Tsarfaty, I., Shalgi, R., Ben-Aharon, I. Chemotherapy-induced vascular toxicity-real-time in vivo imaging of vessel impairment. Journal of Visualized Experiments. (95), e51650 (2015).
- Denny, W. A. Prodrug strategies in cancer therapy. European Journal of Medicinal Chemistry. 36 (7-8), 577-595 (2001).
- Kastrati, I., Delgado-Rivera, L., Georgieva, G., Thatcher, G. R. J., Frasor, J. Synthesis and characterization of an aspirin-fumarate prodrug that inhibits NFκB activity and breast cancer stem cells. Journal of Visualized Experiments. (119), e54798 (2017).
- Mao, J., et al. A simple dual-pH responsive prodrug-based polymeric micelles for drug delivery. ACS Applied Materials & Interfaces. 8 (27), 17109-17117 (2016).
- Li, S. -. Y., et al. A pH-responsive prodrug for real-time drug release monitoring and targeted cancer therapy. Chemical Communications. 50 (80), 11852-11855 (2014).
- Andresen, T. L., Thompson, D. H., Kaasgaard, T. Enzyme-triggered nanomedicine: Drug release strategies in cancer therapy (Invited Review). Molecular Membrane Biology. 27 (7), 353-363 (2010).
- Xu, G., McLeod, H. L. Strategies for enzyme/prodrug cancer therapy. Clinical Cancer Research. 7 (11), 3314-3324 (2001).
- Luo, W., et al. Dual-targeted and pH-sensitive doxorubicin prodrug-microbubble complex with ultrasound for tumor treatment. Theranostics. 7 (2), 452 (2017).
- Gao, J., et al. Ultrasound triggered phase-change nanodroplets for doxorubicin prodrug delivery and ultrasound diagnosis: An in vitro study. Colloids and Surfaces B: Biointerfaces. 174, 416-425 (2019).
- Brade, A. M., Szmitko, P., Ngo, D., Liu, F. -. F., Klamut, H. J. Heat-directed suicide gene therapy for breast cancer. Cancer Gene Therapy. 10 (4), 294-301 (2003).
- Long, K., et al. One-photon red light-triggered disassembly of small-molecule nanoparticles for drug delivery. Journal of Nanobiotechnology. 19 (1), 357 (2021).
- Liu, Y., Long, K., Kang, W., Wang, T., Wang, W. Optochemical control of immune checkpoint blockade via light-triggered PD-L1 dimerization. Advanced NanoBiomed Research. 2 (6), 2200017 (2022).
- Wang, T., et al. Optochemical control of mTOR signaling and mTOR-dependent autophagy. ACS Pharmacology & Translational Science. 5 (3), 149-155 (2022).
- Abet, V., Filace, F., Recio, J., Alvarez-Builla, J., Burgos, C. Prodrug approach: An overview of recent cases. European Journal of Medicinal Chemistry. 127, 810-827 (2017).
- Li, G., et al. Small-molecule prodrug nanoassemblies: an emerging nanoplatform for anticancer drug delivery. Small. 17 (52), 2101460 (2021).
- Shamay, Y., et al. Quantitative self-assembly prediction yields targeted nanomedicines. Nature Materials. 17 (4), 361-368 (2018).
- Sinoway, P. A., Callen, J. P. Chlorambucil. Arthritis & Rheumatism. 36 (3), 319-324 (1993).
- Owen, W. R., Stewart, P. J. Kinetics and mechanism of chlorambucil hydrolysis. Journal of Pharmaceutical Sciences. 68 (8), 992-996 (1979).
- Lv, W., et al. Upconversion-like photolysis of BODIPY-based prodrugs via a one-photon process. Journal of the American Chemical Society. 141 (44), 17482-17486 (2019).
- Silver, J. Let us teach proper thin layer chromatography technique. Journal of Chemical Education. 97 (12), 4217-4219 (2020).
- Saad, W. S., Prud'homme, R. K. Principles of nanoparticle formation by flash nanoprecipitation. Nano Today. 11 (2), 212-227 (2016).
- Long, K., et al. Photoresponsive prodrug-dye nanoassembly for in-situ monitorable cancer therapy. Bioengineering & Translational Medicine. 7 (3), 10311 (2022).
- Zhong, T., et al. A self-assembling nanomedicine of conjugated linoleic acid-paclitaxel conjugate (CLA-PTX) with higher drug loading and carrier-free characteristic. Scientific Reports. 6 (1), 36614 (2016).
- Long, K., et al. Green light-triggered intraocular drug release for intravenous chemotherapy of retinoblastoma. Advanced Science. 8 (20), 2101754 (2021).
- Lv, W., Wang, W. One-photon upconversion-like photolysis: a new strategy to achieve long-wavelength light-excitable photolysis. Synlett. 31 (12), 1129-1134 (2020).
- Rwei, A. Y., Wang, W., Kohane, D. S. Photoresponsive nanoparticles for drug delivery. Nano Today. 10 (4), 451-467 (2015).
- Grzelczak, M., Vermant, J., Furst, E. M., Liz-Marzán, L. M. Directed self-assembly of nanoparticles. ACS Nano. 4 (7), 3591-3605 (2010).
- Gnanasammandhan, M. K., Idris, N. M., Bansal, A., Huang, K., Zhang, Y. Near-IR photoactivation using mesoporous silica-coated NaYF4:Yb,Er/Tm upconversion nanoparticles. Nature Protocols. 11 (4), 688-713 (2016).
Yeniden Basımlar ve İzinler
Bu JoVE makalesinin metnini veya resimlerini yeniden kullanma izni talebi
Izin talebiThis article has been published
Video Coming Soon
JoVE Hakkında
Telif Hakkı © 2020 MyJove Corporation. Tüm hakları saklıdır