Bu içeriği görüntülemek için JoVE aboneliği gereklidir. Oturum açın veya ücretsiz deneme sürümünü başlatın.
Method Article
İnsan Kalçasındaki Mikroyapısal Başarısızlık Mekanizmasının Görüntülenmesi
Bu Makalede
Özet
Protokol, büyük hacimli mikro-BT taraması, özel yapım bir sıkıştırma aşaması ve gelişmiş görüntü işleme araçlarını birleştirerek tüm proksimal insan femurundaki kemik mikro yapısının deformasyonunun ve tokluğunun ölçülmesini sağlar.
Özet
Giderek artan yükler altında kemik mikroyapısının görüntülenmesi, kemiğin mikroyapısal bozulma davranışının gözlemlenmesini sağlar. Burada, femur boynunun klinik olarak anlamlı kırıklarına neden olan, giderek artan deformasyon altında tüm proksimal femurun üç boyutlu mikroyapısal görüntülerinin bir dizisini elde etmek için bir protokol açıklıyoruz. Protokol, popülasyondaki kemik mineral yoğunluğunun alt ucunda 66-80 yaş arası kadın donörlerden alınan dört femora kullanılarak gösterilmiştir (T-skoru aralığı = −2.09 ila −4.75). Mikro-bilgisayarlı tomografi (mikro-BT) görüntüleme sırasında uygulanan yükü kaydederken, tek bacaklı bir duruşu taklit eden örneklerin yüklenmesi için radyo-şeffaf bir sıkıştırma aşaması tasarlanmıştır. Görüş alanı 146 mm genişliğinde ve 132 mm yüksekliğindeydi ve izotropik piksel boyutu 0,03 mm idi. Kuvvet artışı, kırılma yükünün sonlu eleman tahminlerine dayanıyordu. Sıkıştırma aşaması, yer değiştirmeyi numuneye uygulamak ve öngörülen kuvvet artışlarını yürürlüğe koymak için kullanıldı. Femur boynunun açılması ve kesilmesine bağlı alt sermaye kırıkları dört ila beş yük artışından sonra meydana geldi. Mikro-BT görüntüleri ve reaksiyon kuvveti ölçümleri, kemik gerilmesini ve enerji absorpsiyon kapasitesini incelemek için işlendi. Erken yükleme adımlarında korteksin kararsızlığı ortaya çıktı. Femur başındaki subkondral kemik, kırık öncesi% 16'ya ulaşan büyük deformasyonlar ve kırık kadar destek kapasitesinde ilerleyici bir artış gösterdi. Deformasyon enerjisi, kırılmaya kadar yer değiştirme ile doğrusal olarak artarken, rijitlik kırılmadan hemen önce sıfıra yakın değerlere düşmüştür. Kırılma enerjisinin dörtte üçü, son %25'lik kuvvet artışı sırasında numune tarafından alındı. Sonuç olarak, geliştirilen protokol, ileri bir donör yaşında kayda değer bir enerji emme kapasitesi veya hasar toleransı ve kortikal ve trabeküler kemik arasında sinerjik bir etkileşim ortaya çıkardı.
Giriş
Femur boynu kırıkları yaşlanan nüfus için büyük bir yüktür. Mikro-bilgisayarlı tomografi (mikro-BT) görüntüleme ve eşlik eden mekanik testler, kemik mikro yapısının gözlemlenmesine ve kemik gücü, yaşa bağlı değişiklikler ve yük altındaki yer değiştirmelerle ilişkisinin incelenmesine olanak tanır 1,2. Bununla birlikte, yakın zamana kadar, yük altındaki kemiğin mikro-BT çalışmaları, eksize edilmiş kemik çekirdekleri3, küçük hayvanlar4 ve insan omurga üniteleri5 ile sınırlıydı. Mevcut protokol, tüm proksimal insan femurunun mikroyapısının yük altında ve bir kırıktan sonra yer değiştirmesini ölçebilir.
İnsan uyluk kemiğinin başarısızlığını araştırmak için çeşitli çalışmalar yapılmıştır ve bunlar zaman zaman zıt sonuçlara ulaşmıştır. Örneğin, kortikal ve trabeküler yapıların yaşa bağlı incelmesinin, kemiğin elastik instabilitesine neden olarak yaşa bağlı kırılmaya yatkınlığı belirlediği düşünülmektedir6,7, bu da elastik instabilite olmadığı varsayılarak kortikal gerilme ve femoral kuvvet tahminlerinin yüksek katsayısı ile bariz bir tezat oluşturmaktadır (R2 = 0.80-0.97)8,9. Bununla birlikte, bu tür çalışmalar femur kuvvetini sistematik olarak hafife almıştır (%21-29 oranında), bu nedenle modellerde uygulanan kırılgan ve yarı kırılgan kemik tepkilerini sorgulamaktadır 8,10. Görünüşte zıt olan bu bulgular için olası bir açıklama, izole kemik çekirdeklerine kıyasla tüm kemiklerin farklı bir kırılma davranışında bulunabilir. Bu nedenle, tüm proksimal femurlarda kemik mikroyapısının deformasyon ve kırık yanıtlarını gözlemlemek, kalça kırığı mekaniği ve ilgili uygulamalar hakkında bilgi sahibi olmayı ilerletebilir.
Tüm insan kemiklerini mikrometrik çözünürlükte görüntülemek için mevcut yöntemler sınırlıdır. Portal ve dedektör boyutu, insan proksimal uyluk kemiğini barındırmak için uygun bir çalışma hacmi (yaklaşık 13 cm x 10 cm, genişlik x uzunluk) ve ilgili mikro mimari özelliklerin yakalanabilmesini sağlamak için muhtemelen 0,02-0,03 mm mertebesinde bir piksel boyutu sağlamalıdır11. Bu spesifikasyonlar şu anda bazı senkrotron tesisleri1 ve ticari olarak temin edilebilen bazı büyük hacimli mikro-BT tarayıcıları12,13 tarafından karşılanabilir. Sıkıştırma aşaması, insan uyluk kemiğinde bir kırılmaya neden olmak için yeterli bir kuvvet üretirken X-ışını zayıflamasını en aza indirmek için radyo-şeffaf olmalıdır (örneğin, yaşlı beyaz kadınlar için 0,9 kN ile 14,3 kN arasında)14. Bu büyük kırılma yükü değişimi, kırılmaya yönelik yük adımlarının sayısının, genel deney süresinin ve üretilen karşılık gelen veri miktarının planlanmasını zorlaştırır. Bu sorunu çözmek için, kırık yükü ve yeri, klinik bilgisayarlı tomografi (BT) görüntülerinden alınan numunenin kemik yoğunluğu dağılımı kullanılarak sonlu elemanlar modellemesi yoluyla tahmin edilebilir 1,2. Son olarak, deneyden sonra, tüm insan uyluk kemiğindeki başarısızlık mekanizmalarını ve enerji yayma kapasitesini incelemek için üretilen büyük miktarda verinin işlenmesi gerekir.
Burada, femur boynunun klinik olarak anlamlı kırıklarına neden olan, giderek artan deformasyon altında tüm proksimal femurun üç boyutlu mikroyapısal görüntülerinin bir dizisini elde etmek için bir protokol açıklıyoruz2. Protokol, numune sıkıştırmanın kademeli olarak artırılmasının planlanmasını, özel bir radyo-şeffaf sıkıştırma aşaması aracılığıyla yüklenmeyi, büyük hacimli bir mikro-CT tarayıcı aracılığıyla görüntülemeyi ve görüntülerin ve yük profillerinin işlenmesini içerir.
Protokol
Protokol, bir vücut bağış programından alınan 12 femur örneği ile geliştirildi ve test edildi. Örnekler taze olarak elde edildi ve Flinders Üniversitesi Biyomekanik ve İmplant Laboratuvarı'nda (Tonsley, Güney Avustralya, Avustralya) -20 °C'de saklandı. Deney boyunca kemik nemi korundu. Bağışçılar Kafkasyalı kadınlardı (66-80 yaş). Flinders Üniversitesi Sosyal ve Davranışsal Araştırma Etik Kurulu'ndan (SBREC) etik izni alınmıştır (Proje # 6380).
1. Numuneye özel bir yük adımı artışının planlanması
- Femur örneğini, bir dilim kalınlığını ve yaklaşık 0,5-0,7 mm'lik bir düzlem içi piksel boyutunu hedefleyen bir klinik BT tarayıcı kullanarak tarayın. Bu adım, kemik görselleştirme için önceden kaydedilmiş standart görüntüleme protokolleri kullanılarak herhangi bir kamu görüntüleme tesisinde uzman bir radyograf tarafından tamamlanabilir.
- Numune ile birlikte, bilinen beş dipotasyum hidrojen fosfat konsantrasyonuna sahip bir CT dansitometri kalibrasyon fantomunu tarayın (K2HPO4, eşdeğer yoğunluk aralığı yaklaşık 59 mg∙cm−3 ile 375 mg∙cm−3 arasında).
- Klinik BT görüntülerinden15 kemik geometrisini segmentlere ayırın, kemiğin segmentli geometrisini birbirine bağlayın ve Schileo ve ark.8 tarafından bildirilen yoğunluk-elastik modül ilişkisini kullanarak izotropik malzeme özelliklerini eleman eleman kalibre edilmiş kemik yoğunluğu değerlerine eşleyin. Sonlu elemanlar yazılımında daha fazla analiz için ağı kaydedin. Segmentasyon ve sonlu elemanlar yazılımıyla birlikte verilen ilgili yönergeleri izleyerek her adımı tamamlayın.
- Ağı sonlu elemanlar yazılımına aktarın. Modelin 3-6 mm distal ucunu tamamen kısıtlayın. Koronal düzlemde femur şaft ekseninden 1,000° eklenen ve femur başının merkezinden geçen 8 N'luk bir nominal kuvvet uygulayın. Bu yükleme koşulu, statik tek bacaklı duruş görevini (orthoload.com) taklit eder.
- Yerleşik PCG çözücüyü kullanarak sonlu elemanlar modelini çözün (yakınsama toleransı: 1 x 10−7).
NOT: Burada sonlu elemanlar yazılımı ANSYS kullanılmıştır.- Aşağıdaki komutları yürüterek element merkezinde birinci ve üçüncü ana gerinim bileşenlerini içeren bir eleman tablosu oluşturun:
/POST1
ETABLE,, EPTO1,1
ETABLE,, EPTO3,3 - Aşağıdaki komutları yürüterek modeldeki birinci ve üçüncü ana gerinim bileşenleri ile gerilim (%0,73 gerinim) ve sıkıştırmada (%1,04 gerinim)8 (Şekil 1) kemik verim gerinim arasındaki gerinim oranını hesaplayın:
SMULT, RFT, EPTO1, , 1 / 0.0074,1,
SMULT, RFT, EPTO3, ,1/0.0104,1,
- Aşağıdaki komutları yürüterek element merkezinde birinci ve üçüncü ana gerinim bileşenlerini içeren bir eleman tablosu oluşturun:
- Nominal kuvveti hem gerilim hem de sıkıştırmadaki tepe gerinim oranına göre ölçeklendirin ve kırılma yükünün bir tahminini elde etmek için ikisinin en büyüğünü atın. Yük artışını, hesaplanan kırılma yükünün 1/4'ü olarak belirleyin1.
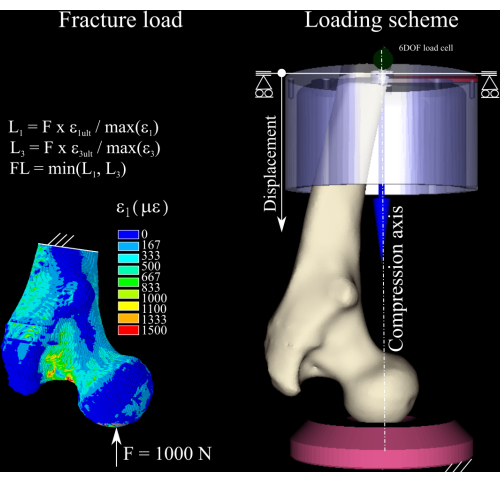
Şekil 1: Kırılma yükünün hesaplanması. Sonlu elemanlar gerinim haritası, nominal kuvveti kırılma yüküne dönüştürmek için kullanılan denklemler (solda) ve uyluk kemiğini (sağ orta), distal alüminyum (sağ üst) kabı ve polietilen basınç soketini (sağ alt) gösteren yükleme şeması. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.
2. Femur numune düzeneğinin hazırlanması (Şekil 2)
- Numuneyi dondurucudan çıkarın (−20 °C).
- Kemik nemini korumak için numuneyi fizyolojik bir çözeltiye batırılmış emici malzemeye sarılmış su geçirmez bir plastik torbada tutarken 24 saat oda sıcaklığında (RT) çözdürün.
- Femoral diyafizi proksimal femur başından 180 mm'de kesin.
- İçbükey şekilli polietilen basınç soketini (Şekil 2D) ve femur başını hizalayarak femur başını hizalama donanımının dikey ekseni üzerinde ortalayın.
- Femur boynunu ve diyafiz eksenini içeren düzlemi frontal düzlemle hizalayın (Şekil 2).
- Dikey eksen, statik tek bacak duruşu sırasında kalça reaksiyon kuvvetinin yönünü temsil edecek şekilde diyafiz eksenini 8° addüksiyona döndürün (Şekil 2).
- Üreticinin talimatlarını izleyerek diş çimentosunu hazırlayın.
- Numunenin distal ucunu 55 mm derinliğinde alüminyum bir saksı kabına koyun ve alüminyum kabı diş çimentosu ile doldurun. Çimentonun sertleşmesini tamamlaması için en az 30 dakika bekleyin.
- Numune düzeneğini −20 °C'de saklayın.
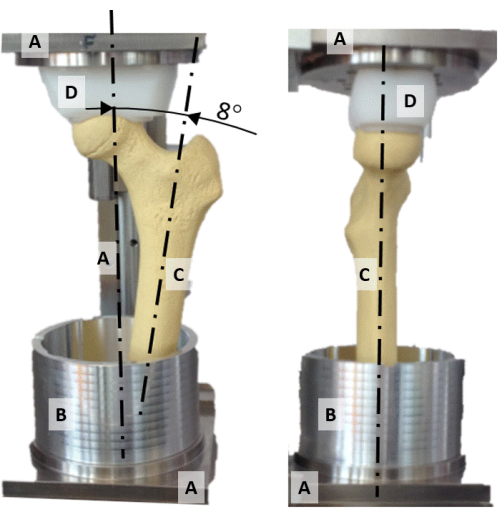
Şekil 2: Hizalama donanımı. (A) çerçeveyi, (B) alüminyum saksı kabını, (C) sentetik bir uyluk kemiği modelini ve (D) küresel şekilli basınç soketini gösteren hizalama donanımının önden (solda) ve yanda (sağda) fotoğrafı. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.
3. Sıkıştırma aşaması montajı
NOT: Sıkıştırma aşamasının dış boyutları, numune hariç 245 mm çap, 576 mm yükseklik ve 14 kg ağırlıktır. Sıkıştırma aşaması iki ana bölümden oluşur: sıkıştırma odası ve aktüatör, aşağıdaki gibi monte edilir:
- Sıkıştırma odası
- Polietilen basınç soketini (104 mm çap, 60 mm yükseklik), bir ucunda (altta) kaynaklı bir alüminyum levha ile kapatılan alüminyum silindirin (203 mm çap, 3 mm et kalınlığı) altına monte edin.
- Aktüatör
- Disk, üç çubuk, üçgen plaka ve dikey rayı kullanarak üst yapıyı birleştirin (Şekil 3).
- Vidalı kriko mekanizmasını (strok: 150 mm, maksimum yük: 10.000 N, dişli oranı: 27:1, devir başına deplasman: 0,148 mm) üçgen plakaya monte edin.
- Açısal adaptörü lineer raya monte edin.
- Düşük sürtünmeli xy tablasını açısal adaptöre monte edin.
- Altı serbestlik dereceli yük hücresini (maksimum ölçüm hatası: %0,005; maksimum kuvvet: 10.000 N; maksimum tork: 500 Nm) yük hücresinin x-z düzlemini üst yapının ön düzlemiyle hizalayarak düşük sürtünmeli tablaya monte edin.
- Aktüatör vidasını açısal adaptöre bağlayın.

Şekil 3: Özel yapım radyosaydam sıkıştırma aşaması düzeneği. Sıkıştırma aşamasının bir fotoğrafı (solda) ve bir modeli (sağda). (A) Altta kapalı 3 mm kalınlığında bir alüminyum silindir olan sıkıştırma odası; (B) üst yapıya sahip aktüatör tertibatı; (C) vidalı kriko mekanizması; (D) düşük sürtünmeli xy tablosu; ve (E) altı eksenli yük hücresi modelde görüntülenir ve gösterilir. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.
4. Denemeyi ayarlama
- Kemik nemini korumak için fizyolojik bir çözeltiye batırılmış emici malzemeye sarılmış su geçirmez bir plastik torbada tutarken numuneyi 24 saat RT'de çözün.
- Alüminyum kap numune düzeneğini, numune düzeneğinin ön düzlemini aktüatörünkiyle hizalayarak yük hücresine monte edin.
- Numune de dahil olmak üzere üst yapıyı sıkıştırma odasına monte edin. Femur başını polietilen basınç soketindeki küresel içbükeylik ile hizalamaya dikkat edin. Femur başının yerine oturduğundan, ancak basınç soketinin küresel boşluğu içinde gevşek olduğundan emin olun.
- Sıkıştırma aşamasını Görüntüleme ve Tıbbi Işın Hattı'ndaki (IMBL) mikro-CT tarayıcının dönüş aşamasına yerleştirin.
- Yük hücresini (hata < %0,005; maksimum kuvvet: 10.000 N; maksimum tork: 500 Nm) gerilim yükselticiye bağlayın.
- Gerinim yükselticiyi USB üzerinden , yük hücresiyle birlikte verilen uygulama yazılımıyla donatılmış bir dizüstü bilgisayara bağlayın.
- Dizüstü bilgisayardaki yük hücresi tarafından ölçülen reaksiyon kuvvetini izlerken, numuneyi basınç soketine doğru aşağı doğru hareket ettirerek sıkıştırma aşamasında vida mekanizmasını çalıştırın. 100 N'ye eşit bir sıkıştırma kuvveti elde edildiğinde vida mekanizmasını durdurun. Numuneyi 50 N ön yüke boşaltın.
- Tek pco.edge sensörlü merceğe bağlı sintilatör "Ruby"yi (http://archive.synchrotron.org.au/31-australian-synchrotron/imbl/811-preparation-for-imaging-experiments) seçin.
- Görüş alanını 76,31 mm x 64,39 mm olarak ayarlayın, bu da 2.560 piksel x 2.160 piksel dizi boyutu için 29,81 μm piksel boyutu sağlar.
- Görüş alanını 29,81 μm piksel boyutunda 145,71 mm x 64,39 mm'ye genişletmek için dönen tablanın eksenini görüş alanı ekseninden 8 mm'ye (yatay olarak) ayarlayın (ofset tarama modu).
- Tarama parametrelerini 60 keV'lik bir ışın enerjisine, 0,1°'lik bir dönüş artışına, iki parti 180° dönüşe (ofset tarama), 50 μs'lik bir pozlama süresine ve dönme konumu başına iki kare ortalamasına ayarlayın.
- Taramayı her biri 26 mm dikey kaydırma ile art arda beş dikey yığılmış tarama elde edecek şekilde ayarlayın, böylece taranan birimin toplam yüksekliği toplam 30 dakikalık tarama süresi için 132,2 mm olur.
5. Eşzamanlı mikroyapısal görüntüleme ile mekanik test
- Mikro-CT (piksel boyutu: 0,03 mm) görüntülemeyi referans koşulunda iki kez gerçekleştirin (sıfır gerinim koşulu olarak alınır).
- Vidalı kriko mekanizmasını tur başına yaklaşık 1 s (0.1-0.2 mm/s) sabit bir hızda manuel olarak çalıştırarak kuvvet artışını uygulayın.
- Mikro-CT görüntüleme yapın.
- Reaksiyon kuvvetinde ani bir düşüşle gösterildiği gibi, numunenin kırılmasına neden olana kadar adım 5.2 ve adım 5.3'ü tekrarlayın.
- Kırık numunenin mikro-BT görüntülemesini gerçekleştirin.
- 1.800 projeksiyon görüntüsünü (2.560 piksel x 896 piksel boyutunda, 76,8 mm x 26,88 mm, genişlik x yükseklik, 32 bit kayan nokta görüntüleri) birleştirin. İşlem, iki projeksiyon görüntüsünü (yatay ofset tarama modunda çekilmiş) ve dikey olarak kaydırılmış beş görüntüyü birleştirir, böylece tek bir projeksiyon görüntüsü üretir.
- Kesit görüntülerinin hacmini yeniden oluşturun (4.407 görüntü, her görüntü 4.888 x 4.888 piksel boyutunda) ve bunları 32 bit, kayan nokta dosyaları olarak kaydedin. TIFF formatı (392 GB disk alanı kaplar).
- Gürültüyü azaltmak için 3 x 3 Gauss filtresi uygulayın. Görüntüleri 8 bit'e dönüştürün (256 gri düzeyli görüntü, bitmap biçiminde kaydedilir ve birim başına yaklaşık 100 GB yer kaplar).
NOT: Bu çalışmada, görüntülerin işlenmesi, IMBL operatörünün rehberliğinde Avustralya Synchrotron'da bulunan yazılım kullanılarak gerçekleştirilmiştir.
6. Yer değiştirme ve gerinim alanının hesaplanması
- Hesaplama süresini azaltmak için kesit görüntülerini dört (120 μm/piksel) alt örnekleyin.
- Yük altındaki numunenin görüntülerini, yüksüz referans durumundaki numunenin görüntülerine uzayda sağlam bir şekilde birlikte kaydedin. Ortak kaydın hedefi olarak distal diyafizi kullanın (Ek Dosya 1 ve Ek Dosya 2).
- Yüzey üç boyutlu modeller oluşturun (. STL dosyaları) mikro-CT görüntülerini ikilileştirdikten sonra görselleştirme için11.
- Izgaranın düğümlerindeki yer değiştirmeleri belirlemek için 50 piksele eşit bir ızgara boyutu (SDER = %0,076 gerinim hatası, BoneDVC, https://bonedvc.insigneo.org/dvc/) kullanarak görüntü hacmini referans hacmine elastik olarak kaydedin.
- Izgarayı sonlu eleman modeline dönüştürün. BoneDVC tarafından hesaplanan düğüm yer değiştirmesini modele uygulayın. Tüm kemik hacmi üzerindeki gerilme tensörünü belirlemek için modeli çözün.
- Tam çözünürlüklü görüntüleri kullanarak en yüksek gerinim seviyelerini gösteren bölgedeki analizi tekrarlayın.
- DVC gerinim haritalarını, interp3 işlevi (Matlab)2 ile kübik enterpolasyon kullanarak tam çözünürlüklü görüntülerle eşleyin.
- Büyük hacimli görselleştirme ve animasyon (Matlab) için yer değiştirmeleri, gerinimleri ve mikroyapısal görüntüleri görselleştirin2.
7. Analiz
- Yüksüz koşullarda ve kırık sonrası elde edilen görüntüleri üst üste bindirerek kemikteki kalıcı deformasyonu (hasarı) görüntüleyin2.
- Yüküz koşullarda, artan yük seviyelerinde ve kırılma sonrası üç boyutlu modelleri üst üste bindirerek kemiğin ilerleyici mikroyapısal deformasyonunu görüntüleyin2.
- Kırık yerindeki kemiğin gerginliğini görüntüleyin2.
- Tanımlayıcı istatistik ve regresyon yöntemlerini kullanarak deformasyon enerjisini, rijitliği ve yer değiştirmeyi analiz edin2.
Sonuçlar
Görüntüler tüm proksimal femuru, basınç soketini, diş çimentosunu, alüminyum kabı ve sarma dokusunu gösterir. Kırık öncesi ve kırık sonrası yük arttıkça kemik mikro mimarisinin giderek deforme olduğu görülebilir (Şekil 4).

Şekil 4: Dizüstü bilgisayara bağlı sıkıştırma<...
Tartışmalar
Mevcut protokol, kalça kırıklarının zaman geçen mikromekaniğinin ex vivo olarak üç boyutlu olarak incelenmesine izin vermektedir. İnsan uyluk kemiğinin proksimal yarısına ilerleyici bir deformasyon uygulayabilen ve reaksiyon kuvvetini ölçebilen bir radyosaydam (alüminyum) sıkıştırma aşaması özel olarak tasarlanmış, üretilmiş ve test edilmiştir. Bu protokolde, mikrometrik çözünürlükte progresif yükleme ile tüm proksimal femuru görüntüleyen geçici bir görüntü hacimleri diz...
Açıklamalar
Tüm yazarlar herhangi bir çıkar çatışması beyan etmez.
Teşekkürler
Avustralya Araştırma Konseyi'nden (FT180100338; IC190100020) minnetle kabul edilir.
Malzemeler
| Name | Company | Catalog Number | Comments |
| Absorbent tissue | N/A | Maintain the bone moisture throughout the experiment | |
| Alignment rig | Custom-made | Rig for positioning the specimen in the potting cup | |
| Aluminium potting cup | Custom-made | Potting cup | |
| Bone saw | N/A | Cut the specimen to size | |
| Calibration phantom QCT Pro | Mindways Software, Inc., Austin, USA | CT Calibration 13002 | Calibrate grey levels in the images into equivalent bone mineral (ash) density levels |
| Clinical Computed-Tmography scanner | General Electric Medical Systems Co., Wisconsin, USA | Optima CT660 | Preliminary imaging for the prediction of the load step to fracture |
| Compressive stage | Custom-made | A 10 kg, radiotransparent compressive stage for applying and maintaining throught imaging a prescribed deformation to the specimen. | |
| Dental cement | Soesterberg, The Netherlands | Vertex RS | |
| Femur specimen | Science Care, Phoenix, USA | ||
| Finite-element analysis software | ANSYS Inc., Canonsburg, USA | ANSYS Mechanical APDL | Finite-element software package |
| Freezer | N/A | Store specimens at -20 °C | |
| Hard Drive | Dell | Disk space: 500 GB per volume | |
| Image bnarization and segmentation software | Skyscan-Bruker, Kontich, Belgium | CT analyzer | Image processing software |
| Image elastic segmentation | The University of Sheffield | Bone DVC | https://bonedvc.insigneo.org/dvc/ |
| Image processing and automation software | The MathWork Inc. | Matlab | Image processing software |
| Image registration software | Skyscan-Bruker, Kontich, Belgium | DataViewer | Image processing software |
| Image segmentation and FE modelling software | Simpleware, Exeter, UK | Scan IP | Bone egmentation software |
| Image stiching script | Australian syncrotron, Clayton, VIC, AU | The script is available at IMBL | |
| Image visualization | Kitware, Clifton Park, NY, USA | Paraview | Image visualization |
| Image visualization | Australian National University | Dristhi | Image visualization: doi:10.1117/12.935640 |
| Imaging and Medical beamline | Australian syncrotron, Clayton, VIC, AU | Large object micro-CT beamline at the Australian Synchrotron | |
| Laptop | Dell Inc., USA | ||
| Low-friction x-y table | THK Co., Tokyo, Japan | ||
| NI signal acquisition software | National Instruments, Austin, TX | NI-DAQmx | |
| Phosphate-buffered saline solution | Custom-made | Maintain the bone moisture throughout the experiment | |
| Plastic bag | N/A | Maintain the bone moisture throughout the experiment | |
| Rail | SKF Inc., Lansdale, PA, USA | ||
| Screw-jack mechanism | Benzlers, Örebro, Sweden | Serie BD (warm gear unit) | stroke: 150 mm, maximal load: 10,000 N, gear ratio: 27:1, a displacement per revolution: 0.148 mm |
| Single pco.edge sensor, lens coupled scintillator | Australian syncrotron, Clayton, VIC, AU | Detector Ruby FOV: 141 x 119 mm; 2560 x 2160 px; 55 µm/px; 50 fps | |
| Six axis load cell | ME-Meßsysteme GmbH, Hennigsdorf, GE | K6D6 | Maximal measurement error: 0.005%; maximal force: 10000 N; maximal torque: 500 Nm |
| Strain amplifier | ME-Meßsysteme GmbH, Hennigsdorf, GE | GSV-1A8USB K6D/M16 |
Referanslar
- Martelli, S., Perilli, E. Time-elapsed synchrotron-light microstructural imaging of femoral neck fracture. Journal of the Mechanical Behavior of Biomedical Materials. 84, 265-272 (2018).
- Martelli, S., Giorgi, M., Dall' Ara, E., Perilli, E. Damage tolerance and toughness of elderly human femora. Acta Biomaterialia. 123, 167-177 (2021).
- Perilli, E., et al. Dependence of mechanical compressive strength on local variations in microarchitecture in cancellous bone of proximal human femur. Journal of Biomechanics. 41 (2), 438-446 (2008).
- Thurner, P. J., et al. Time-lapsed investigation of three-dimensional failure and damage accumulation in trabecular bone using synchrotron light. Bone. 39 (2), 289-299 (2006).
- Jackman, T. M. Quantitative, 3D visualization of the initiation and progression of vertebral fractures under compression and anterior flexion. Journal of Bone and Mineral Research. 31 (4), 777-788 (2016).
- Mayhew, P. M., et al. Relation between age, femoral neck cortical stability, and hip fracture risk. Lancet. 366 (9480), 129-135 (2005).
- Nazarian, A., Stauber, M., Zurakowski, D., Snyder, B. D., Müller, R. The interaction of microstructure and volume fraction in predicting failure in cancellous bone. Bone. 39 (6), 1196-1202 (2006).
- Schileo, E., et al. To what extent can linear finite element models of human femora predict failure under stance and fall loading configurations. Journal of Biomechanics. 47 (14), 3531-3538 (2014).
- Schileo, E., et al. An accurate estimation of bone density improves the accuracy of subject-specific finite element models. Journal of Biomechanics. 41 (11), 2483-2491 (2008).
- Dall'ara, E., et al. A nonlinear QCT-based finite element model validation study for the human femur tested in two configurations in vitro. Bone. 52 (1), 27-38 (2013).
- Perilli, E., Parkinson, I. H., Reynolds, K. J. Micro-CT examination of human bone: from biopsies towards the entire organ. Annali dell'Istituto Superiore di Sanità. 48 (1), 75-82 (2012).
- Wearne, L. S., Rapagna, S., Taylor, M., Perilli, E. Micro-CT scan optimisation for mechanical loading of tibia with titanium tibial tray: A digital volume correlation zero strain error analysis. Journal of the Mechanical Behavior of Biomedical Materials. 134, 105336 (2022).
- Bennett, K. J., et al. Ex vivo assessment of surgically repaired tibial plateau fracture displacement under axial load using large-volume micro-CT. Journal of Biomechanics. 144, 111275 (2022).
- Falcinelli, C., et al. Multiple loading conditions analysis can improve the association between finite element bone strength estimates and proximal femur fractures: A preliminary study in elderly women. Bone. 67, 71-80 (2014).
- Orthopedic Image Segmentation. Synopsys Available from: https://www.synopsys.com/simpleware/news-and-events/ortho-medical-image-segmentation.html (2020)
Yeniden Basımlar ve İzinler
Bu JoVE makalesinin metnini veya resimlerini yeniden kullanma izni talebi
Izin talebiDaha Fazla Makale Keşfet
This article has been published
Video Coming Soon
JoVE Hakkında
Telif Hakkı © 2020 MyJove Corporation. Tüm hakları saklıdır