Method Article
Serumda Döteryumla Zenginleştirilen Retinolün GC-MS Analizi ve Vitamin A Toplam Vücut Depolarının Tahmini
Bu Makalede
Özet
Bu yöntem, retinolün serumdan ekstrakte edilmesini, HPLC kullanılarak ayrılmasını ve GC-MS kullanılarak etiketli ve etiketsiz retinol izotoplarının belirlenmesini içerir. Etiketli retinolün etiketsiz retinolün oranı, A vitamininin toplam vücut depolarını tahmin etmek için kullanılır.
Özet
Bu yöntem, serumdaki retinolün döteryumdan zenginleştirilmesinin belirlenmesini ve vücuttaki A vitamini depolarının tahminini açıklar. İşlem, 0.5 mL %0.85 tuzlu su çözeltisi, 100 μL dahili standart çözelti ve 5 mL kloroform-metanol (2: 1 v / v) çözeltisi kullanılarak 0.4 mL serumdan retinolün ekstrakte edilmesini içerir. Santrifüjleme ve alt kloroform tabakasının çıkarılmasından sonra, karışım nitrojen altında kurutulur ve 0.1 mL etanol içinde yeniden süspanse edilir ve retinol fraksiyonu, bir PE C18 kolonu ile donatılmış bir HPLC sistemi kullanılarak diğer bileşenlerden ayrılır. Retinol fraksiyonu manuel olarak veya bir fraksiyon toplayıcı ile toplanabilir. Daha sonra, retinol fraksiyonu nitrojen altında kurutulur ve %10 trimetilklorosilan içeren O-bis (trimetilsilil) trifloroasetamid (BSTFA) ile türetilir. Son olarak, etiketli ve etiketsiz retinol izotopları, taşıyıcı gaz olarak helyum ve iyonizasyon maddesi olarak metan ile elektron yakalama negatif kimyasal iyonizasyonunu kullanan bir 19091z-431 HP-1 metil siloksan kılcal kolonu ile donatılmış bir GC-MS sistemi kullanılarak nicelleştirilir. Etiketli retinolün etiketsiz retinolün oranı daha sonra A vitamini depolarını tahmin etmek için Olson, Green veya kütle dengesi denklemlerinde kullanılır.
Giriş
A vitamini, büyüme, epitel bütünlüğü, kırmızı kan hücresi üretimi, bağışıklık ve üreme için görme sistemi ve hücre fonksiyonunun sürdürülmesi için gerekli olan temel bir besindir1. A vitamini eksikliği, dünya çapında 100'den fazla ülkeyi etkileyen ciddi bir halk sağlığı sorunudur. Düşük gelirli ülkelerdeki küçük çocukları ve hamile kadınları orantısız bir şekilde etkilemektedir. Dünya genelinde yaklaşık 190 milyon çocuk A vitamini eksikliğinden muzdariptir ve bu da onu halk sağlığı ve çocuk gelişimi için kritik bir konu haline getirmektedir2.
Bu duruma yanıt olarak, 5 yaşın altındaki çocuklara iki yılda bir yüksek dozda A vitamini dağıtımı ile A vitamini takviyesi ve belirli gıda maddelerinin A vitamini takviyesi de dahil olmak üzere çeşitli programlar, birçok düşük gelirli ülkede onlarca yıldır uygulanmaktadır. Bununla birlikte, bu müdahaleler sıklıkla örtüşür ve bazı popülasyonları yanlışlıkla kronik aşırı A vitamini alımına maruz bırakır 3,4. Bu ikili eksiklik ve fazlalık riski, program değerlendirmesine rehberlik etmek için eksiklikten toksisiteye kadar tüm spektrumda A vitamini durumunu doğru bir şekilde değerlendirebilen bir biyobelirteç ihtiyacını vurgulamaktadır.
A vitamini biyobelirteçleri beslenme durumunu değerlendirmek için çok önemlidir. En sık kullanılan biyobelirteçler serum retinol konsantrasyonları ve retinol bağlayıcı proteindir (RBP). Bununla birlikte, bu biyobelirteçlerin enfeksiyonlar ve iltihaplanma tarafından geçici olarak baskılanabileceğini ve bunun da belirli popülasyonlarda A vitamini değerlendirmelerinin özgüllüğünü azaltabileceğini not etmek önemlidir 5,6,7.
Karaciğer biyopsisi veya otopsi örnekleri A vitamini durumunu değerlendirmek için altın standart olarak kabul edilirken, toplam karaciğer A vitamini rezervlerinin en hassas dolaylı göstergesi retinol izotop seyreltme (RID) yöntemidir8. RID, eksikten aşırı depolara kadar tüm spektrumda A vitamini durumunun kantitatif bir tahminini sağlar9. Çoğu araştırma uygulamasında, RID yöntemi, daha sonra 14 ila 21 günlük bir süre boyunca vücut depoları ile karışan oral bir dozda döteryum (2H) veya 13C etiketli retinil asetatın uygulanmasını içerir. Bu süreden sonra bir kan örneği alınır ve serum -80 ° C'de saklanır. Etiketli retinolün toplam retinole oranı daha sonra Olson denklemi11, kütle dengesi denklemi12 veya Yeşil denklem13 kullanılarak A vitamini depolarını10 tahmin etmek için kütle spektrometresi kullanılarak analiz edilir. Bu yazıda sunulan protokol, döteryum (2H) veya 13C etiketli retinil asetatın uygulanması için geçerlidir ve Tang ve ark.14'ün çalışmalarına dayanmaktadır. Bu yöntemin genel amacı, vücuttaki A vitamini durumunu doğru bir şekilde değerlendirmek ve izlemektir11. Eksiklikten fazlalığa kadar geniş bir durum yelpazesinde A vitamini konsantrasyonlarının kantitatif bir tahminini sağlayan güçlü bir yöntemdir15. Genellikle dolaylı önlemlere dayanan diğer yöntemlerden daha doğru ve kesindir9.
Protokol
Protokol, Halk Sağlığı Bakanlığı Etik Kurulu (No. 2015/02/550/CE/CNERSH/SP) tarafından onaylandı ve veli/velilerden bilgilendirilmiş onam alındı.
NOT: A vitamini ışığa duyarlı olduğundan, tüm işlemlerin loş ışıkta veya altın floresan aydınlatma altında yapılması çok önemlidir16. Kullanılan malzemeler Malzeme Tablosunda detaylandırılmıştır.
1. Reaktiflerin hazırlanması
- Sodyum klorür (% 0.85 w / h): 0.85 g NaCl'yi 100 mL hacimsel bir şişede damıtılmış suda çözün. Mezuniyet işaretine kadar damıtılmış su ile doldurun ve karıştırın.
- Kloroform-metanol (2:1 v/v): 300 mL kloroformu bir ölçüm silindiri ile 500 mL hacimsel bir şişeye aktarın. 150 mL metanol ekleyin ve karıştırın.
- HPLC için mobil faz A: Asetonitril/Tetrahidrofuran/ultra saf su (50/20/30, v/v/v): 500 mL asetonitril'i 1000 mL'lik hacimsel bir şişeye aktarın. 200 mL tetrahidrofuran ve 300 mL su ekleyin. Çözeltiyi karıştırın, gözenek boyutu 0.45 μm olan bir membran filtre kullanarak filtreleyin ve sonikat (genlik% 100, frekans 40 kHz ve süre 15 dakika).
- HPLC için mobil faz B: Asetonitril/Tetrahidrofuran/ ultra saf su (50/44/6, h/v/v): 500 mL asetonitril'i 1000 mL'lik hacimsel bir şişeye aktarın. 440 mL Tetrahidrofuran ve 60 mL su ekleyin. Çözeltiyi karıştırın, gözenek boyutu 0.45 μm olan bir membran filtre kullanarak filtreleyin ve sonikat yapın.
2. Standart çözeltilerin hazırlanması
- Tablo 1'de gösterildiği gibi, standardın 40 mg'ını 100 mL'lik bir hacimsel şişede etanol içinde çözerek stok çözeltisini hazırlayın. Çözücü ile mezuniyet işaretine kadar doldurun ve iyice karıştırın.
- Seyreltilmiş stok çözeltileri: Tablo 2'de gösterildiği gibi, 1 mL stok çözeltisini 50 mL'lik bir hacimsel şişeye aktararak seyreltilmiş stok çözeltisini hazırlayın. Mezuniyet işaretine kadar uygun çözücü ile doldurun ve iyice karıştırın.
- Seyreltilmiş stok çözeltilerinin konsantrasyonunun belirlenmesi: Seyreltilmiş çözeltinin bir alikotunu (1 mL) bir kuvars tüpe yerleştirin ve boşluk olarak etanol kullanarak belirtilen dalga boyunda (Tablo 3) spektrofotometredeki emilimini ölçün. Lambert-Beer Yasası17'yi kullanarak hesaplayın. Cihazı 15-30 dakika ısıtarak, istenen dalga boyunu seçerek ve boşluğu numune tutucuya yerleştirerek cihazı sıfırlayarak analizden önce spektrofotometrenin kalibre edildiğinden emin olun. Aşağıdaki formülü kullanarak konsantrasyonu hesaplayın:
Konsantrasyon = (absorbans/absorpsiyon katsayısı) x 106 (μg/dL)
NOT: Değerleri geleneksel birimlerden (μg/dL) SI birimlerine (μmol/L) dönüştürmek için, geleneksel değeri aşağıdaki dönüştürme faktörleriyle çarpın: Retinil asetat için 0.0304 ve Retinol 0.0349 için18. - Çalışma standartlarının hazırlanması: Hacimsel bir pipet kullanarak, seyreltilmiş stok çözeltilerinin 2 mL'sini 100 mL'lik bir erlene aktarın. Şişeyi mezuniyet işaretine kadar etanol ile doldurun, iyice karıştırın ve bir tıpa ile kapatın.
- Her bir çözeltinin tam konsantrasyonunu belirlemek için, bir C18 sütunu ve 340 nm'ye ayarlanmış bir diyot dizisi dedektörü ile donatılmış HPLC kullanarak her bir bileşenin saflığını değerlendirin. Pompayı, Tablo 4'te gösterilen programa göre Mobil Faz A ve Mobil Faz B'yi kullanacak şekilde programlayın. Pompa, dedektör, otomatik numune alma cihazı gibi çeşitli bileşenleri ve tüm sistemin performansını doğrulayarak analizden önce HPLC sisteminin kalibre edildiğinden emin olun.
- Seyreltilmiş stok çözeltilerinin 1 mL'sini kıvrımlı şişelere aktarın ve numuneleri normal prosedüre göre HPLC sistemine enjekte edin. Aşağıdaki denklemi kullanarak saflığı belirleyin:
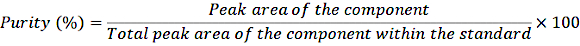
DENKLEM 1
Bu saflık düzeltmesiyle, standart çözeltideki farklı bileşenlerin tam konsantrasyonunu hesaplayın.
- Dahili standardın hazırlanması (retinil asetat OD ~ 0.2): Hacimsel bir pipet kullanarak, 30 mL Retinil asetat çalışma standardını 100 mL'lik bir erlene aktarın. Şişeyi mezuniyet işaretine kadar etanol ile doldurun, iyice karıştırın ve bir tıpa ile kapatın.
- Çalışma çözeltilerinin hazırlanması: 0.500, 0.167, 0.050, 0.0167 ve 0.00 Etiketli ve Etiketsiz retinol oranlarını sağlamak için 10.00, 3.33, 1.00, 0.33 ve 0.00 μg Etiketli Retinol'e 20 μg Etiketsiz Retinol ekleyin.
3. Numune analizi
NOT: Bu çalışmada kullanılan serum örnekleri, Kamerun'daki çocukların A vitamini durumunu izlemek ve değerlendirmek için tasarlanmış bir çalışmanın parçası olarak oral dozda (2 mg retinol eşdeğeri) D8-retinol alan çocuklardan 14. günde toplanmıştır.
- Serumda retinoidlerin ekstraksiyonu: Bu ekstraksiyon, Tang ve ark.14 tarafından modifiye edildiği şekliyle Folch ve ark.19'un çalışmasına dayanmaktadır. Aşağıda açıklanan adımları izleyin.
- Analizden önce donmuş serum örneklerinin oda sıcaklığında (20-25 ° C) hafifçe çözülmesine izin verin. 400 μL serumu 16 x 100 mm'lik tek kullanımlık bir kültür tüpüne alın. 500 μL %0.85 salin artı 100 μL Dahili Standart ve 5 mL kloroform-metanol (2:1 v/h) çözeltisi ekleyin.
- 30 saniye boyunca girdap ve 4 ° C'de 10 dakika boyunca 1157 x g'de santrifüjleyin. Bir cam Pasteur pipeti kullanarak, kloroform alt tabakasını dikkatlice 13 x 100 mm'lik tek kullanımlık bir kültür tüpüne çıkarın. Bir su banyosunda (40 °C) nitrojen gazı altında kurutun ve kalıntıyı 100 μL etanol içinde yeniden süspanse edin. 30 saniye boyunca girdap ve sonikat. Numuneyi bir ek ile kıvrımlı bir şişeye aktarın, kuyuyu kapatın ve etiketleyin. Numune, HPLC retinol toplanması için hazırdır.
- HPLC retinol toplama işlemini aşağıda açıklandığı gibi gerçekleştirin.
- Her serum örneğinden 70 μL'yi, bir C18 kolonu ve 340 nm'ye ayarlanmış bir diyot dizisi dedektörü ile donatılmış bir HPLC sistemine enjekte edin. Pompayı, Tablo 1'te gösterilen programı izleyerek Mobil Faz A ve B'yi 4 mL/dk'lık sabit bir akış hızında verecek şekilde programlayın.
- Serum örneklerini enjekte etmeden önce, 70 μL retinol çalışma solüsyonunu HPLC sistemine enjekte edin ve retinol zirvesinin tutma süresini kaydedin. Ardından, ayrıştırılmış retinol fraksiyonunu buzlu cam tıpa ile 5 mL'lik bir tüpte belirli bir aralıkta toplamak için fraksiyon toplayıcıyı ayarlayın. Bu durumda, retinol fraksiyonu 7.5-10.5 dakika arasında 3 dakikalık bir aralıkta toplandı.
NOT: Retinol konsantrasyonu, bu adımda, retinol standartlarının bir kalibrasyon eğrisi ve dahili standarttan elde edilen geri kazanım oranı kullanılarak da hesaplanabilir.
- Retinolün türetilmesini aşağıda açıklandığı gibi gerçekleştirin.
- HPLC'den toplanan retinol fraksiyonunu azot gazı altında 40 °C'de bir su banyosunda en az 3 saat kurutun. Kurutma sırasında nemin buharlaşmasını kolaylaştırmak için etanol ekleyin (türevlendirme neme duyarlı olduğundan numuneler tamamen kuru olmalıdır). Tüpe %10 TMCS içeren 20 μL BSTFA ekleyin.
- Tüpü 70 °C'ye ayarlanmış kuru bir blok ısıtıcıya yerleştirin ve 30 dakika inkübe edin. Bir cam Pasteur pipeti kullanarak, reaksiyon karışımını bir ek parçalı bir kıvrımlı şişeye aktarın, bir kapak kıvırıcı kullanarak kıvrımlı kapakla sıkıca kapatın ve etiketleyin. Numune artık GC/MS analizi için hazırdır ve analize kadar 4 °C'de bir desikatörde saklanabilir.
- Ek olarak, 100 μL'lik bir çalışma standardı solüsyon setini kurutun ve GC/MS'yi kalibre etmek için yukarıda açıklandığı gibi türevlendirin.
NOT: Retinolün BSTFA kullanılarak türetilmesi, retinolün hidroksil grubunun (-OH) trimetilsilil grubu (-Si(CH3)3) ile değiştirildiği ve retinil trimetilsilil eter oluşturduğu bir kimyasal reaksiyonu içerir. Bu işlem, retinolün uçuculuğunu ve stabilitesini artırarak GC / MS analizi20 için daha uygun hale getirir.
- GC/MS analizi: GC/MS analizi, Tang ve ark.14 tarafından açıklanan prosedür kullanılarak gerçekleştirilir. Aşağıda açıklanan adımları izleyin.
- 3 μL'lik türetilmiş retinol numunesini, bir otomatik numune alma cihazı kullanarak, sıfır ölü hacim konektörü aracılığıyla 15 m x 0.25 mm iç çaplı erimiş silika kılcal kolona bağlı soğuk bir kolon üstü enjektör ile GC'ye enjekte edin. 0.25 μm film kalınlığında bir DB-1 sabit fazı ile kaplanmıştır.
- Kolonlu fırın ve kolon üstü enjektör sıcaklıklarını 15 °C/dk hızında 50 °C'den 285 °C'ye yükselecek şekilde programlayın ve GC/MS arayüz sıcaklığını 285 °C'ye ayarlayın. Retinolün trimetilsilil türevini yaklaşık 12 dakika boyunca elüte etmek için taşıyıcı gaz olarak helyum kullanın.
- İyon kaynağı sıcaklığı 150 °C'ye ayarlanmışken, 0,5 torr metan negatif iyon kimyasal iyonizasyonu kullanan dört kutuplu kütle spektrometresi ile GC elüatını tespit edin. Kütle spektrometresini 260 ile 280 dalton arasında taramaya ayarlayın.
4. Veri analizi
- GC/MS veri analizi yazılımını kullanın.
- İstenen tüm iyonları kütle-yük (m/z) oranlarına göre çıkarın, tepe noktasını entegre edin (tepe noktasının başlangıç ve bitiş noktalarını ayarlamak için manuel entegrasyonu kullanın) ve sonuçları bir elektronik tablo dosyasına aktarın.
NOT: Kullanılan izotopa bağlı olarak, istenen iyonlar aşağıdaki gibi olacaktır: Doğal retinol için 268-270 m/z; [2 H4] -retinol için 271-274 m / z; [13C] -retinol için 278-280 m / z; ve [2 H8]-retinol için 276-280 m/z. - m / z 274, 275, 276, 277 ve 278'de tepe alanı ekleyerek etiketli retinol (ΣD) için tepe noktalarının toplamını hesaplayın. m / z 268, 269 ve 270'te tepe alanı ekleyerek etiketlenmemiş retinol (ΣH) için tepe noktalarının toplamını hesaplayın.
- Aşağıdaki denklemi kullanarak etiketli retinolün (D) zenginleşmesini hesaplayın: D = ΣD/(ΣH + ΣD). Aşağıdaki denklemi kullanarak etiketlenmemiş retinol (H) miktarını hesaplayın: H = 1 - D.
NOT: Gaz Kromatografisi Elektron Yakalama Negatif Kimyasal İyonizasyon Retinil trimetilsilil eterin kütle spektrometresi, moleküler iyon vermez, ancak etiketlenmemiş retinol için m / z 268 ila 271'de, D4-retinol için m / z 272 ila 275'te ve D8-retinol14 için m / z 276 ila 280'de büyük bir fragman iyonu verir. - Sistemi kontrol etmek için, kalibrasyon standartlarının ağırlık oranları ile etiketli retinol ve etiketsiz retinol için entegre alanlar arasında doğrusal bir regresyon denklemi hesaplayın.
5. A vitamini depolarının tahmini
NOT: Bu adım, bir bireyin A vitamini durumunun değerlendirilmesine izin verir.
- Olson denklemi11'i kullanarak A vitamini toplam karaciğer depolarını hesaplayın
A Vitamini Toplam Karaciğer Depoları = F x Doz x [S x a x (H / D - 1)]
F, oral yoldan uygulanan dozun emilim ve saklanma etkinliği için bir faktördür (F = 0.50), Doz, oral yoldan uygulanan etiketli A vitamini miktarıdır (μmol), S, plazmanın karaciğere eşitsizliğini düzelten bir faktördür etiketli retinolün etiketsiz retinole oranı (S = 0.65), a, karıştırma süresi boyunca etiketli A vitamininin geri dönüşü olmayan kaybını düzelten bir faktördür; Spesifik olarak, A = E-kt, burada K tahmini sistem fraksiyonel katabolik hızıdır (K = Ln çocuklar için 2/32 gün) ve T, dozdan bu yana geçen gün olarak ifade edilen zamandır; D / H, etiketli retinolün etiketsiz retinole serum izotopik oranıdır, -1, etiketli A vitamini dozunun toplam vücut A vitamini havuzuna katkısını düzeltir. - A vitamini toplam vücut depolarını (TBS) hesaplamak için Yeşil denklem13'ü kullanın
TBS = Fa × S × (1/SAp)
burada Fa, t zamanında emilen ve vücudun değiştirilebilir depolama havuzlarında bulunan oral olarak etiketlenmiş VA dozunun fraksiyonudur ve S, serumdaki retinol spesifik aktivitenin t zamanındaki depolardakine oranıdır (çocuklar için, Fa × S = 14 günde 0.642)21. SAp, μmol dozu başına serumdaki dozun fraksiyonudur (ör., [etiketli retinol] / (serumda [etiketsiz + etiketli retinol]) / etiketli retinolün (μmol)) oral dozu).
Sonuçlar
Yaklaşık 50 pM/μL kalibrant (retinol ve D 8-retinol) içeren kurutulmuş bir çözeltinin türetilmiş bir numunesinin 3 μL'lik GC/MS'ye enjeksiyonu moleküler iyon göstermedi, ancak retinol için m/z 268'de ana fragman iyonu sergiledi (Şekil 1) ve D8-retinol için m/z 278 (Şekil 2). Bu, retinol ve D 8-retinolün türevlendirilmesi sırasında oluşan retinil trimetilsilil eterin moleküler iyonlarının, GC/MS'de kullanılan iyonizasyon koşulları altında stabil olmadığını gösterir. Öncelikle alfa bölünmesi yoluyla daha küçük parçalara ayrılırlar. Bu yaygın parçalanma modeli, trimetilsilil eter grubuna bitişik bağın kopmasını içerir. Alfa bölünmesi, trimetilsilil grubunun (kütlesi 73 Da'ya sahip olan TMS) ve bir hidrojen atomunun kaybına neden olur, bu da retinol için 268 Da ve D 8-retinol22 için 278 Da kütleli bir fragman iyonuna yol açar. Bu mekanizma, kütle spektrometresi sırasında üretilen spesifik parça iyonlarını analiz ederek numunedeki retinol ve türevlerinin varlığının belirlenmesine ve doğrulanmasına yardımcı olur. Retinol ve D8-retinol karışımlarının enjeksiyonu, retinol için m/z 268'de ve D8-retinol için m/z 276'da iki ana fragman iyonu gösterdi (Şekil 3), bu da numunede bu bileşiklerin varlığını gösterir. Kalibrasyon eğrisi, yüksek bir korelasyon katsayısı ile gösterildiği gibi mükemmel bir doğrusallık sergiledi (Şekil 4), bu da tepe oranı ile ağırlık oranı arasındaki ilişkinin çok düz ve öngörülebilir bir modele sahip olduğunu gösteriyor.
Serum örneklerinin enjeksiyonlarından elde edilen GC / MS yanıtı (oral dozda 2 mg retinol eşdeğeri D8-retinol alan çocuklardan alınan serum; Şekil 5) retinol ve D8-retinolün varlığını gösterir, iki ana fragman iyonu m/z 268 ve m/z 274'te gözlenir. İyonların ekstraksiyonu ve D8-retinol için m/z 274, 275, 276, 277 ve 278'de ve etiketlenmemiş retinol için m/z 268, 269 ve 270'te tepe alanlarının entegrasyonundan sonra elde edilen sonuçlar Tablo 5'te sunulmuştur. Bu sonuçlar, vücuttaki A vitamini depolarını hesaplamak için Olson denklemi11 veya Yeşil denklem13'e entegre edilecektir.
Kararlı izotop seyreltme tekniği, diğer yöntemlerle elde edilemeyen A vitamini seviyelerinin ölçümlerini sağlayarak A vitamini durumunun doğru bir şekilde değerlendirilmesini sağlar. Bu yöntem beslenme çalışmaları, klinik teşhisler ve epidemiyolojik araştırmalar için değerlidir.
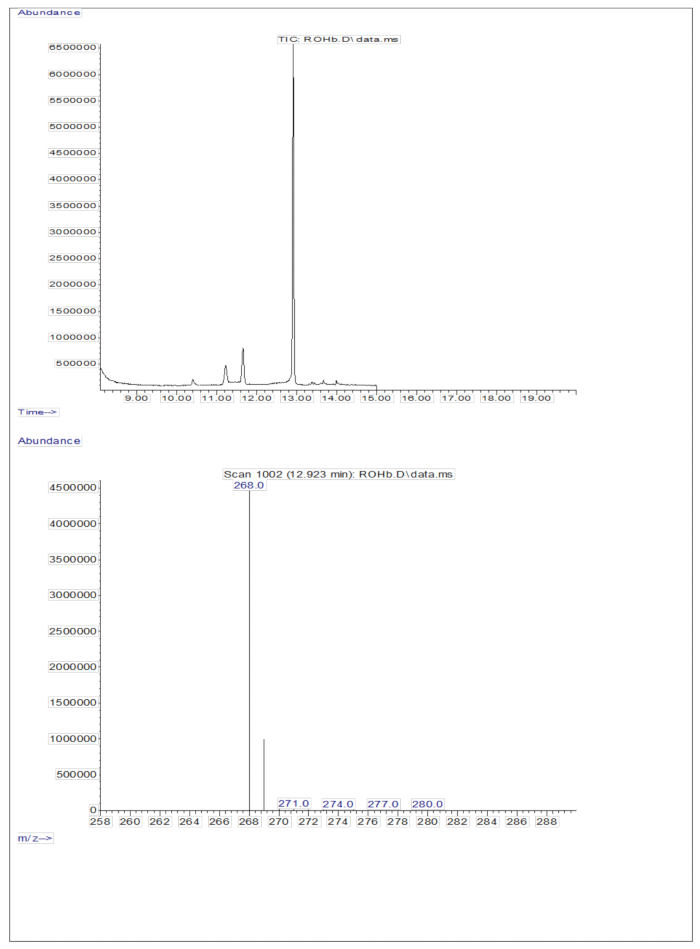
Şekil 1: Retinolün kromatogramı ve kütle spektrumu. Şekil, türetilmiş retinol standardının analizinden elde edilen gaz kromatografisi/metan elektron yakalama negatif kimyasal iyonizasyon-kütle spektrometresi kromatogramını (üst panel) göstermektedir. Alt panel, retinol için m / z 268'i gösteren bir kütle spektrumudur. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.

Şekil 2: D8-retinolün kromatogramı ve kütle spektrumu. Şekil, türetilmiş D8-retinol standardının analizinden elde edilen gaz kromatografisi/metan elektron yakalama negatif kimyasal iyonizasyon-kütle spektrometresi kromatogramını (üst panel) göstermektedir. Alt panel, D8-retinol için m/z 278'i gösteren bir kütle spektrumudur. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.

Şekil 3: Bir retinol ve D8-retinol karışımının kromatogramı ve kütle spektrumu. Şekil, retinol ve D8-retinol standartlarının türetilmiş bir karışımının analizinden elde edilen gaz kromatografisi/metan elektron yakalama negatif kimyasal iyonizasyon-kütle spektrometresi kromatogramını (üst panel) göstermektedir. Alt panel, retinol için m/z 268 ve D8-retinol için m/z 276 gösteren bir kütle spektrumudur. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.
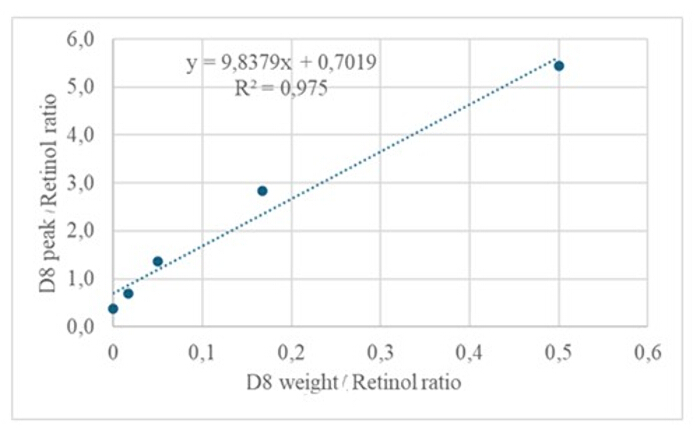
Şekil 4: Kalibrasyon eğrisi. Bu şekil, GC / MS yanıtı ile etiketlenmemiş ve etiketli retinol konsantrasyonu arasındaki ilişkiyi göstermektedir. y = 9.8379x + 0.7019 denklemi ile tanımlanır, burada y (alan oranları) cihaz yanıtını, 9.8379 duyarlılığı, x (ağırlık oranları) analit konsantrasyonunu ve 0.7019 arka plan sinyalini temsil eder. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.
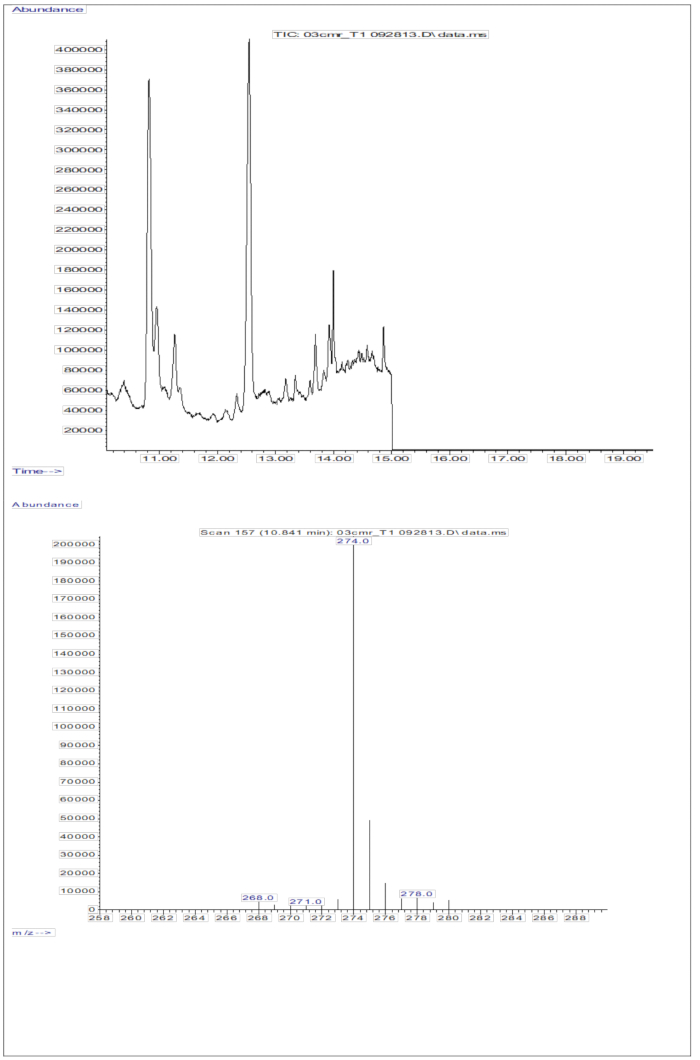
Şekil 5: Serum örneğinin kromatogramı ve kütle spektrumu. Bu şekil, serumun türetilmiş retinol fraksiyonunun analizinden elde edilen gaz kromatografisi/metan elektron yakalama negatif kimyasal iyonizasyon-kütle spektrometresi kromatogramını (üst panel) göstermektedir. Alt panel, D8-retinol için m/z 274'ü gösteren bir kütle spektrumudur. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.
| Standart | Ağırlık (mg) | Hacimsel şişe (mL) | Çözücü |
| A vitamini | 40 | 100 | Etanol |
| Retinil asetat | 40 | 100 | Etanol |
| Döteryum etiketli retinil asetat | 40 | 100 | Etanol |
Tablo 1: Stok çözeltisinin hazırlanması. Bu tablo, daha sonra gelecekteki deneyler için daha düşük konsantrasyonlara seyreltilebilen konsantre retinol ve döteryum etiketli retinil asetat çözeltilerinin nasıl hazırlanacağını göstermektedir.
| Standart | Stok çözeltisi (mL) | Hacimsel şişe (mL) | Çözücü |
| A vitamini | 1 | 50 | Etanol |
| Retinil asetat | 1 | 50 | Etanol |
| Döteryum etiketli retinil asetat | 1 | 50 | Etanol |
Tablo 2: Seyreltilmiş stok çözeltilerinin hazırlanması. Bu tablo, retinol ve döteryum etiketli retinil asetatın kullanıma hazır çözeltilerinin nasıl hazırlanacağını göstermektedir.
| Standart | Dalga boyu (nm) | E1%1 cm |
| A vitamini | 325 | 1850 |
| Retinil asetat | 326 | 1550 |
Tablo 3: Dalga boyu ve E1% 1 cm (Absorpsiyon katsayısı).
| Zaman (dk) | Akış (mL/dk) | Mobil Faz A (%) | Mobil Faz B (%) |
| 0 – 6 | 1 | 100 | 0 |
| 6 – 13 | 1 | 100 → 50 | 0 → 50 |
| 13 - 18 | 1 | 50 | 50 |
| 18 - 20 | 1 | 50 → 0 | 50 → 100 |
| 20 - 28 | 1 | 0 | 100 |
| 28 - 29 | 1 | 0 → 100 | 100 → 0 |
Tablo 4: HPLC mobil aşamaları için zaman çizelgesi. Bu tablo, HPLC kromatografik çalışması sırasında farklı fazların planlanan sırasını ve süresini göstermektedir.
| ŞŞ | SD | D | H | |
| Konu 1 | 64030809 | 566089.7 | 0.008763 | 0.991237 |
| Konu 2 | 194354 | 43861.39 | 0.184125 | 0.815875 |
| Konu 3 | 793490 | 80179.28 | 0.091773 | 0.908227 |
| Konu 4 | 2002063 | 45286.7 | 0.02212 | 0.97788 |
| Konu 5 | 80999193 | 355980.7 | 0.004376 | 0.995624 |
| Konu 6 | 32196717.7 | 216152.7 | 0.006669 | 0.993331 |
| Konu 7 | 40905724.5 | 334818.1 | 0.008119 | 0.991881 |
| Konu 8 | 28336711.5 | 218924.1 | 0.007667 | 0.992333 |
| Konu 9 | 8695135.5 | 542077 | 0.058684 | 0.941316 |
| Konu 10 | 103260212 | 1717728 | 0.016363 | 0.983637 |
| SH: m/z 268, 269 ve 270'teki tepe alanlarının toplamı | ||||
| SD: m/z 274, 275, 276, 277 ve 278'deki tepe alanlarının toplamı | ||||
| D: etiketli retinolün zenginleştirilmesi | ||||
| H: etiketlenmemiş retinol seviyesi |
Tablo 5: Serumun türetilmiş retinol fraksiyonunun GC / MS sonuçları. Bu tablo, A vitamini toplam vücut deposunun hesaplanması için gereken GC/MS çıktılarını bildirmektedir. H, m/z 268, 269 ve 270'teki tepe alanının toplamıdır; D, m/z 274, 275, 276, 277 ve 278'deki tepe alanının toplamıdır; D, etiketli retinolün zenginleştirilmesidir; H, etiketlenmemiş retinol seviyesidir; TBS, A vitamini Tüm Vücut Deposudur.
Tartışmalar
Bu protokolün başarılı bir şekilde uygulanması, her adımın etkin bir şekilde yürütülmesine bağlıdır. Toplanan verilerin doğru ve güvenilir olmasını sağlamak için çözümlerin ve standartların uygun şekilde hazırlanması çok önemlidir. Protokolde açıklanan prosedürler çeşitli ortamlarda test edilmiştir ve numune analizinin amaçlarını karşılayan çözümler ve standartlar elde etmek için uygundur.
Numunelerin analizi, serumdaki retinolün ekstraksiyonu ve ayrılması ile başlar. Serum örneklerinin -80 °C'de saklanması, A vitamininin bozulmasını önlemek için analiz şarttır. Ek olarak, loş ışıkta çalışmak gereklidir16. Retinol fraksiyonunu toplamak için kullanılan HPLC prosedürü, türevlendirme işlemine müdahaleyi önlemek için retinol'ü diğer yağda çözünen bileşenlerden ayırmak için tasarlanmıştır. Ayrıca kolonu yıkamadan yüzlerce numunenin çalıştırılmasına izin verir.
HPLC'den toplanan retinol fraksiyonu, 70 °C'de 30 dakika boyunca BSTFA ile türetilir. Türevlendirme adımı, retinolün uçuculuğunu ve GC-MS'de tespit edilebilirliğini geliştirmek için kritik öneme sahiptir. Suya karşı hassas olduğu için, türevlendirmeden önce numunenin tamamen kurutulması ve GC-MS analizinden önce türevlendirme reaksiyonunun gerçekleşmesi için yeterli zamanın tanınması çok önemlidir. BSTFA ile türevlendirme işleminin, N-metil-N-(tert-butildimetilsilil) trifloroasetamid (MTBSTFA)23,24 kullanılana kıyasla çok hafif ve verimli olduğu ve türetilmiş retinol için çok keskin bir tepe sağladığı fark edildi, taranan kütle aralığında kuyruk veya arka plan tepe noktaları olmadan14. Kapalı bir şişede türetilmiş retinol, bozulmadan 1 ay boyunca 4 ° C'de bir desikatörde tutulabilir14.
GC-MS analizi için, kolonun uygun kalibrasyonunu ve bakımını sağlamak ve enjeksiyon hacmini, sıcaklığını ve akış hızlarını optimize etmek çok önemlidir. Burada kolon üzerine enjeksiyon ile kullanılan koşullar iyi ve güvenilir sonuçlar göstermiştir14. Döteryumlu ve etiketlenmemiş retinolün GC-MS analizi sırasında, Tang ve ark.14 , döteryumlu retinol zirvelerinin hem uygulanan dozda hem de dozu alan deneklerin serumunda ortaya çıktığını gözlemledi. Bu model etiketlenmemiş retinol ile görülmedi. Bu nedenle, döteryumlu retinolün piklerinin dozda önceden oluşturulduğu ve kütle spektrometresindeki parçalanmanın bir sonucu olmadığı sonucuna varmışlardır, bu da döteryumlu retinolün metabolik süreç boyunca yapısını koruduğunu ve biyolojik çalışmalarda retinolün izlenmesi için güvenilir bir belirteç sağladığını düşündürmektedir. Okul öncesi çağındaki çocuklarda 2 mg D8-retinol uygulandıktan sonra serumda döteryumlu retinolün zenginleşmesi 7 saatte artmaya başladı ve 14 günde zirveye ulaştı, bu da daha kısa optimal örnekleme süresi25. 200 μL insan serumunda, retinolün minimum saptanabilir zenginleştirme yüzdesi %0.01'dir, bu da yöntemin çok çeşitli A vitamini durumlarına sahip deneklerden toplanan serum örneklerini analiz edecek kadar hassas olduğunu gösterir14.
Burada sunulan kararlı izotop seyreltme tekniği, A vitamini durumunu değerlendirmek için önemli avantajlar sunarken, bu yöntemin sofistike ekipman ve teknik uzmanlık gerektirdiği, bu da onu birçok ortamda rutin kullanım için pahalı ve daha az erişilebilir hale getirdiği unutulmamalıdır26. Bu nedenle, bu tekniği kullanmayı planlarken bu sınırlamayı göz önünde bulundurmak önemlidir.
Açıklamalar
Bu makale, IAEA tarafından desteklenen A Vitamini Vücut Depolarını ve Karaciğer A Vitamini Konsantrasyonunu Değerlendirmek için Retinol İzotop Seyreltme Yönteminin Kullanılması başlıklı bir serinin parçasıdır.
Teşekkürler
Bu protokolü, Guangwen Tang'ın gözetiminde ve Uluslararası Atom Enerjisi Ajansı'nın (IAEA) mali desteğiyle Jean Mayer USDA Yaşlanma İnsan Beslenmesi Araştırma Merkezi, Tufts Üniversitesi, Boston, ABD'deki Karotenoidler ve Sağlık Laboratuvarı'nda bir burs sırasında öğrendik.
Malzemeler
| Name | Company | Catalog Number | Comments |
| 13x100 mm disposable culture tubes | 99445-13 | PYREX Disposable Rimless Culture Tubes | |
| 16x100 mm disposable culture tubes | 99445-16 | PYREX Disposable Rimless Culture Tubes | |
| 24 Position N-EVAP Nitrogen Evaporator | Organomation Associates, Inc | 11250 | N-EVAP 112, Nitrogen Evaporator, with OA-SYS heating system |
| Acetonitrile | Sigma-Aldrich | 00687 | Acetonitrile, suitable for HPLC, gradient grade, ≥99.9% |
| Amber colored Crimp vials, 2 mL, | SU860033 | Short thread autosampler vial, amber vial 11.6 x 32 mm | |
| Analytical Balance | Mettler Toledo | 30133525 | Precision Balance MS303TS/00 |
| C18 column | Perkin-Elmer Inc | 2580195 | Brownlee Pecosphere RA C18 Cartridge Column - 33 mm x 4.6 mm I.D., Pkg. 5 |
| cap crimper | MilliporeSigma | Z114243 | Hand-operated aluminum cap crimper O.D. 20 mm |
| Capillary column | J & W Scientific | 122-1011 | 15 m × 0.25 mm i.d. fused silica capillary column coated with a DB-1 stationary phase of 0.25 mm film thickness |
| Centrifuge | Sigma 3-18KS | ||
| Chloroform | Sigma-Aldrich | 528730 | Chloroforme, HPLC grade, ≥ 99.9% |
| Conical Flasks: 100 mL, | 4980016 | Borosil Erlenmeyer Flasks Graduated Conical NM Borosilicate | |
| Crimp caps with PTFE seal | Supelco | 27455-U | Crimp seals with PTFE/silicone septa |
| D8-Retinyl acetate | Cambridge Isotope Laboratories Inc. | DLM-2244-PK | Vitamin A acetate 3-4% cis (10, 14, 19, 19, 19, 20, 20, 20-D8, 90%) |
| Dispenser for 1-10 mL | Gilson | F110103 | DISPENSMAN Bottle-top Dispenser |
| Dry Block Heater | Grant | Grant QBH2 High Performance Digital Dry Block Heater | |
| Ethanol | Sigma-Aldrich | 459844 | Ethyl alcohol, Pure, ≥ 99.5%, ACS reagent, 200 proof |
| GC-MS | Agilent | Agilent 7890 A Series Gas Chromatography with 5975C Mass Spectrometer System equipped with a 5975C inert XL EI/CI MSD/DS Turbo CI System, a 7693A Auto?injector Includes transfer turret and a 7693 sample Tray | |
| Glass stoppered volumetric Flasks: 2000 mL | 956854 | BRAND BLAUBRAND volumetric flask, glass stopper, clear glass | |
| Glass stoppered volumetric Flasks: 100 mL | 956849 | BRAND BLAUBRAND volumetric flask, glass stopper, clear glass | |
| Glass stoppered volumetric Flasks: 1000 mL | 956853 | BRAND BLAUBRAND volumetric flask, glass stopper, clear glass | |
| Glass stoppered volumetric Flasks: 25 mL | 956841 | BRAND BLAUBRAND volumetric flask, glass stopper, clear glass | |
| Glass stoppered volumetric Flasks: 50 mL | 956847 | BRAND BLAUBRAND volumetric flask, glass stopper, clear glass | |
| Glass stoppered volumetric Flasks: 500 mL | 956852 | BRAND BLAUBRAND volumetric flask, glass stopper, clear glass | |
| Helium (highest purity) | Air Liquide | UN 1046 Helium compressed, Class 2.2 | |
| HPLC | Varian | Varian 940LC HPLC with fraction collector | |
| Inserts for crimp vials, 5 mm, 175 μL, | AR0-4521-12 | Verex insert, 5 mm Dia, 175 µl, clear, conical bottom, w/bottom spring | |
| Measuring Cylinders: 100 mL | 213902402 | DURAN Measuring Cylinder, with Hexagonal Base, Class A | |
| Measuring Cylinders: 250 mL | 213903604 | DURAN Measuring Cylinder, with Hexagonal Base, Class A | |
| Methane (highest purity) | Air Liquide | UN1971 Methane compressed, Class 2.1 | |
| Methanol | Sigma-Aldrich | 34860 | Methanol, suitable for HPLC, ≥ 99.9% |
| N, O-bis(trmethylsilyi)trifluoroacetamide (BSTFA) with 10% Trimethylchlorosilane (TMCS) | Thermo Scientific | 043939.22 | |
| Nitrogen | Produced by Parker Balston NitroVap Generator | ||
| Pasteur Pipettes, glass, | 13-678-20A | Fisherbrand Disposable Borosilicate Glass Pasteur Pipets | |
| Quartz glass Cuvettes | EW-83301-12 | Cole-Parmer Standard Single Quartz Cuvettes | |
| Retinol | Sigma-Aldrich | 17772 | ≥95.0% (HPLC), ~2700 U/mg |
| Retinyl acetate | Sigma-Aldrich | R0635 | analytical standard grade |
| Sodium chloride | Sigma-Aldrich | S9888 | Chlorure de sodium, ACS reagent, ≥ 99.0% |
| Spectrophotometer | Shimadzu | Uvmini-1240 UV-Vis Spectrophotometer | |
| Tetrahydrofuran | Sigma-Aldrich | 439215 | Tetrahydrofurane, HPLC grade, ≥ 99.9%, inhibitor-free |
| Ultrasonic cleaner | Bransonic | CPX-952-339R | Branson CPX Bransonic Ultrasonic Bath |
| Volumetric Pipettes: 100-1000 µL | 3123000063 | Eppendorf 1-canal micropipette with T.I.P.S. Box 2.1 | |
| Volumetric Pipettes: 20-200 µL | 3123000055 | Eppendorf 1-canal micropipette with T.I.P.S. Box 2.0 | |
| Vortex mixer | Ika | Vortx Genius 3 |
Referanslar
- D'Ambrosio, D., Clugston, R., Blaner, W. Vitamin A metabolism: an update. Nutrients. 3 (1), 63-103 (2011).
- WHO. Global prevalence of vitamin A deficiency in populations at risk 1995-2005. WHO Global Database on Vitamin A Deficiency. , (2009).
- Kraemer, K., et al. Are low tolerable upper intake levels vitamin A undermining effective food fortification efforts. Nutr Rev. 66 (9), 517-525 (2008).
- Allen, L. H., Haskell, M. Estimating the potential for vitamin A toxicity in women and young children. J Nutr. 132 (9 Suppl), 2907S-2919S (2002).
- Filteau, S. M., et al. Influence of morbidity on serum retinol of children in a community-based study in northern Ghana. Am J Clin Nutr. 58 (2), 192-197 (1993).
- Rubin, L. P., Ross, A. C., Stephensen, C. B., Bohn, T., Tanumihardjo, S. A. Metabolic effects of inflammation on vitamin A and carotenoids in humans and animal models. Adv Nutr. 8 (2), 197-212 (2017).
- Suri, D. J., et al. Inflammation adjustments to serum retinol and retinol-binding protein improve specificity but reduce sensitivity when estimating vitamin A deficiency compared with the modified relative dose-response test in Ghanaian children. Curr Dev Nutr. 5 (8), nzab098 (2021).
- Tanumihardjo, S. A. Vitamin A: biomarkers of nutrition for development. Am J Clin Nutr. 94 (2), 658S-665S (2011).
- Furr, H. C., et al. Stable isotope dilution techniques for assessing vitamin A status and bioefficacy of provitamin A carotenoids in humans. Public Health Nutr. 8 (6), 596-607 (2005).
- Haskell, M. J., Ribaya-Mercado, J. D. the Vitamin A Tracer Task Force. Handbook on Vitamin A Tracer Dilution Methods to Assess Status and Evaluate Intervention Programs. Technical Monograph 5. , (2005).
- Furr, H. C., Amedee-Manesme, O., Bergen, H. R., Anderson, D. P., Olson, J. A. Vitamin A concentrations in liver determined by isotope dilution assay with tetradeuterated vitamin A and by biopsy in generally healthy adult humans. Am J Clin Nutr. 49 (4), 713-716 (1989).
- Gannon, B. M., Tanumihardjo, S. A. Comparisons among equations used for retinol isotope dilution in the assessment of total body stores and total liver reserves. J Nutr. 145 (5), 847-854 (2015).
- Green, M. H. Evaluation of the "Olson equation", an isotope dilution method for estimating vitamin A stores. Int J Vitam Nutr Res. 84 (Suppl 1), 9-15 (2014).
- Tang, G., Qin, J., Gregory, G., Dolnikowski, G. G. Deuterium enrichment of retinol in humans determined by gas chromatography electron capture negative chemical ionization mass spectrometry. J Nutr Biochem. 9 (7), 408-414 (1998).
- Tanumihardjo, S., et al. . Appropriate uses of vitamin A tracer (stable isotope) methodology. Vitamin A tracer task force. , (2004).
- Barua, A. B., Furr, H. C. Properties of retinoids: structure, handling, and preparation. Mol Biotechnol. 2 (2), 167-182 (1998).
- Swinehart, D. F. The Beer-Lambert Law. J Chem Edu. 39, 333-335 (1962).
- Barua, A. B., Furr, H. C. Properties of retinoids. Structure, handling, and preparation. Methods Mol Biol. 89, 3-28 (1998).
- Folch, J., Lees, M., Stanley, S. G. H. A simple method for the isolation and purification of total lipides from animal tissues. J Biol Chem. 226 (1), 497-509 (1957).
- Knapp, D. R. . Handbook of analytical derivatization reactions. , (1979).
- Green, M. H., Green, J. B. Use of model-based compartmental analysis and theoretical data to further explore choice of sampling time for assessing vitamin A status in groups and individual human subjects by the retinol isotope dilution method. J Nutr. 157 (7), 2068-2074 (2021).
- Todd, J. F. J. Recommendations for nomenclature and symbolism for mass spectroscopy (including an appendix of terms used in vacuum technology). (Recommendations 1991). Pure and Appl Chem. 63 (10), 1541-1566 (1991).
- Handelman, G. J., Haskell, M. J., Jones, A. D., Clifford, A. J. An improved protocol for determining ratios of retinol-d4 to retinol isolated from human plasma. Anal Chem. 65 (15), 2024-2028 (1993).
- Tang, G., Andrien, B. A., Dolnikowski, G., Russell, R. M. . Methods in Enzymology, Vitamins and Coenzymes. Part L. 282, 140-154 (1997).
- Haskell, M. J., et al. Population-based plasma kinetics of an oral dose of [2H4]retinyl acetate among preschool-age Peruvian children. Am J Clin Nutr. 77 (3), 681-686 (2003).
- Lopez-Teros, V., et al. International experiences in assessing vitamin A status and applying the vitamin A-labeled isotope dilution method. Int J Vitam Nutr Res. 84 (Suppl 1), 40-51 (2014).
Yeniden Basımlar ve İzinler
Bu JoVE makalesinin metnini veya resimlerini yeniden kullanma izni talebi
Izin talebiThis article has been published
Video Coming Soon
JoVE Hakkında
Telif Hakkı © 2020 MyJove Corporation. Tüm hakları saklıdır