Method Article
التصوير بالرنين المغناطيسي الوظيفي للرئة الذي تم حله على طور لتقييم التهوية الرئوية والتروية (V / Q)
In This Article
Summary
هنا ، نصف تنفيذ التصوير بالرنين المغناطيسي الوظيفي للرئة الذي تم حله على الطور كتقنية MR للبروتون الخالية من عامل التباين لتقييم التهوية الرئوية وديناميكيات التروية. تم التحقق من صحته وتطبيقه عبر نقاط القوة الميدانية والفئات العمرية المختلفة ، ويمكن أن يعزز عملية صنع القرار السريري في المستقبل من خلال المساعدة في تحديد كمية المرض ومراقبة العلاج.
Abstract
تحلل فورييه هو طريقة التصوير بالرنين المغناطيسي 1H الخالية من عامل التباين لتقييم نضح الرئة (Q) والتهوية (V). بعد تسجيل الصورة ، يتم تحليل السلسلة الزمنية لكل فوكسيل فيما يتعلق بمكونات تردد القلب والتنفس.
باستخدام تسلسل صدى التدرج الفاسد ثنائي الأبعاد القياسي بدقة زمنية ~ 300 مللي ثانية ، تم تطوير خوارزمية فرز الصور لإنتاج تصوير الرئة الوظيفي الذي تم حله على طور (PREFUL) بدقة زمنية متزايدة. وبالتالي ، من الممكن تقييم حلقات حجم التدفق الإقليمي (FVL) أثناء تنفس حجم المد والجزر وتصوير انتشار موجة النبض أثناء الدورة القلبية. يمكن تطبيق هذه الطريقة عند 1.5T أو 3T مع أجهزة MR القياسية دون الحاجة إلى برمجة التسلسل ، حيث يمكن تنفيذ البروتوكول الموصوف مع تسلسل SPGRE الافتراضي على معظم الأنظمة.
تم التحقق من صحة التصوير بالرنين المغناطيسي للتهوية PREFUL باستخدام تصوير غاز 129Xe و 19F مع اتفاق إقليمي جيد. تم التحقق من صحة التصوير بالرنين المغناطيسي PREFUL المرجح بالتروية باستخدام SPECT بالإضافة إلى التصوير بالرنين المغناطيسي المحسن للتباين الديناميكي (DCE). تم اختبار PREFUL في إعداد بائع مزدوج المركز ويتم تطبيقه حاليا في العديد من التجارب المستمرة متعددة المراكز. علاوة على ذلك ، من الممكن عبر مجموعة من نقاط القوة الميدانية (0.55T-3T) والفئات العمرية المختلفة ، بما في ذلك الأطفال حديثي الولادة.
تم استخدام التصوير بالرنين المغناطيسي الكمي V / Q PREFUL في المرضى الذين يعانون من التليف الكيسي ، ومرض الانسداد الرئوي المزمن ، وارتفاع ضغط الدم الرئوي الخثاري المزمن ، ومرض فيروس كورونا 2019 لتحديد المرض ومراقبة تغير العلاج بعد العلاج. علاوة على ذلك ، ثبت أن تصوير PREFUL V / Q يتنبأ بفقدان الزرع بسبب الخلل الوظيفي المزمن في الطعم الخيفي في الرئة لدى المرضى بعد زراعة الرئة. باختصار ، التصوير بالرنين المغناطيسي PREFUL هو تقنية تم التحقق من صحتها للتهوية الكمية وتصوير الموجات / التروية النبضية الرئوية للكشف عن أمراض الرئة الإقليمية ، والقياس الكمي ، ومراقبة العلاج مع قيمة مضافة محتملة للروتين السريري الحالي.
Introduction
الجهاز التنفسي ، بآلياته المعقدة ، عرضة للأمراض المختلفة. بشكل بارز ، تقلل أمراض الجهاز التنفسي المزمنة مثل مرض الانسداد الرئوي المزمن (COPD) والتليف الكيسي (CF) وارتفاع ضغط الدم الرئوي الخثاري المزمن (CTEPH) بشكل كبير من متوسط العمرالمتوقع 1. نتيجة لذلك ، أصبح التشخيص المبكر والمراقبة وتقييم الاستجابة العلاجية أمرا بالغ الأهمية.
يمكن أن تشتق اختبارات وظائف الرئة (PFTs) معلمات وظائف الرئة العالمية مثل مؤشر Tiffeneau-Pinelli ، الذي يعرف بأنه نسبة حجم الزفير القسري في ثانية واحدة (FEV1) والقدرة الحيوية القسرية (FVC) 2. هذه المعايير راسخة في الروتين السريري ولكنها تفتقر إلى المعلومات الإقليمية وتتطلب مستوى عال من امتثال المرضى. في هذا الصدد ، يمكن أن يوفر التصوير رؤى وإمكانيات إضافية لمعلمات أكثر حساسية. يوفر التصوير المقطعي المحوسب (CT) تصويرا عالي الدقة للتشكل المتني ، كما أن التقنيات الحديثة مثل رسم خرائط الاستجابة البارامترية تسترجع أيضا المعلوماتالوظيفية 3. ومع ذلك ، يظل التصوير المقطعي المحوسب بإصدار فوتون واحد (SPECT) هو المعيار الذهبي الحالي لتصوير التهوية والتروية (V / Q) في الرئة4. وتتطلب طرائق التصوير المذكورة التعرض للإشعاع المؤين الذي يحتاج إلى اهتمام خاص في حالات الرصد والفئات الضعيفة. وبالتالي ، هناك جهد مستمر لتعزيز التصوير بالرنين المغناطيسي كطريقة بديلة.
بطبيعتها ، تعتبر الرئة عضوا صعبا للتصوير بالرنين المغناطيسي نظرا لانخفاض كثافة البروتون واضمحلال الإشارة السريع5. من بين العديد من الأساليب ، تشمل الحلول الأكثر انتشارا استخدام الغاز مفرط الاستقطاب (على سبيل المثال ، 129Xe MRI) للتهوية6 وتطبيق عامل التباين القائم على الجادولينيوم في الوريد لتصوير التروية7. توفر هذه الطرق نسبة إشارة إلى ضوضاء عالية (SNR) وتعتبر على نطاق واسع طرقا قياسية ذهبية في مجتمع التصوير بالرنين المغناطيسي. يتجنب النهج الأحدث تطبيق أي عامل تباين وهو ممكن مع البروتون التقليدي MR في التنفس الحر مع إجمالي وقت اكتساب ~ 1 دقيقة / شريحة. وبالتالي ، يتم تجنب الأحداث الضارة المحتملة والآثار طويلة المدى التي نوقشت مؤخرا لعوامل التباين وتسهيل نشرها دون الحاجة إلى زيادة الاستقطاب والأجهزة متعددة النواة. بالإضافة إلى ذلك ، يتم تجنب مشكلة العثور على حالة تضخم مناسبة ، والتي يمكن أن تؤثر على قيم عيب التهوية المشتقة8 من خلال اكتساب التنفس الحر.
تم تقديم هذا النهج غير المباشر القائم على إشارة MR لأول مرة بواسطة Zapke et al. الذين استخدموا العلاقة المتبادلة للإشارة المرجحة بالبروتون S وحجم الرئة V: S ~ 1 / V.9 يعتمد على عملية تحويل الصور المكتسبة في التنفس الحر إلى حالة تضخم واحدة شائعة (عادة في وضع وسيط بين انتهاء الصلاحية والإلهام النهائي) ، وبالتالي تعويض الحركة والسماح بتحليل السلسلة الزمنية للإشارة في كل فوكسل. بعد ذلك ، يمكن اشتقاق قياس التهوية من هذه الصور المسجلة المزعومة باستخدام المعادلة (1) بواسطة Klimeš et al.10:
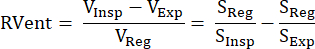 (1)
(1)
مع وحدات التخزين / الإشارات في الإلهام (Insp) ، وانتهاء الصلاحية (Exp) ، والحالة المسجلة (Reg). بعد ذلك ، تم توسيع الطريقة عن طريق إدخال تحلل فورييه للتمييز بين تعديلات الإشارة المرتبطة بتردد التنفس (التهوية) وتردد النبض (التروية) ، وبالتالي ، اشتقاق خريطة V / Q متطابقة مكانيا تماما من عملية استحواذواحدة 11. أصبح هذا ممكنا من خلال الفجوة النموذجية بين ترددات التنفس والقلب ، بحيث يتم تمييز كلا المكونين اللذين يقعان فوق بعضهما البعض في المجال الزمني بشكل فعال في مجال التردد عن طريق تحليل فورييه. بعد الانتقال من المجال المنخفض (0.35T) إلى 1.5T مع تسلسل السبق الحر المتوازن المتوازن للحالة المستقرة (bSSFP) 12 ، بدأت هذه الطريقة في اكتساب المزيد من الاهتمام مع العديد من دراسات المتابعة13،14،15.
نظرا لأن التنفس والنبض يخضعان للتباين ويمكن أن يؤدي تصوير bSSFP (تعويض التدرج) المتاح تجاريا عند 1.5T إلى قطع أثرية كبيرة للنطاقات (خطوط واضحة من فراغ الإشارة) ، فقد تم اقتراح طريقة ذات صلة مع تسلسل صدى التدرج الفاسد (SPGRE) بالاقتران مع ترشيح التمرير المنخفض والتمرير العاليالواسع 16،17. يلتقط هذا الطيف الأكثر تعقيدا من التعديلات الحقيقية المتعلقة بالتنفس والنبض. يتجنب الحساب التالي للسعة في المجال الزمني ضرورة اختيار ذروة تردد واحدة محددة. تم تحقيق مزيد من التحسين من خلال تقسيم التسجيل النموذجي المكون من خطوة واحدة نحو حالة مرجعية واحدة إلى خطوتين منفصلتين. وبالتالي يتم استخدام حقيقة أنه أثناء التنفس الحر يتم الحصول على مجموعة من مراحل التنفس المختلفة بين الإلهام النهائي والانتهاء النهائي بدرجات متفاوتة من التشوه المطلوب نحو حالة ثابتة. بعد اختيار عدة مجموعات وتحديد مجموعة الصور الفردية ، يتم تنفيذ الإجراء التالي: 1) التسجيل داخل مجموعة حالة التنفس المعنية ، 2) التسجيل بين المجموعات خطوة بخطوة من مجموعة متجاورة إلى أخرى (على سبيل المثال ، 1->2 ، 2->3,...) إلى المجموعة التي تمثل المجموعة المرجعية. تم توسيع هذا النهج بشكل أكبر من خلال تقدير الطور لكل صورة لإنشاء دقة زمنية ظاهرة أعلى لتسهيل تحليل ديناميكيات التهوية والتروية ، مما يؤدي إلى مصطلحات MR للرئة الوظيفية التي تم حلها بشكل مرحلي (PREFUL) لتمييز هذا الفرع عن التقنيات الأخرى ذات الصلة18. استفادت دراسات المتابعة من المعلومات الإضافية التي توفرها دورات التنفس والقلب الكاملة وأظهرت زيادة محتملة في حساسية هذهالمعلمات 19 ، 20 ، 21.
كشف التحقق باستخدام المعيار الذهبي SPECT عن معامل نرد بنسبة ≥67٪ لمناطق العيوب22 ، وأظهر قياس التهوية المباشرة مع 129Xe ارتباط نسب عيوب التهوية ≥62٪ في مجموعة مختلطة من مرض الانسداد الرئوي المزمن / التليف الكيسي / الأترابية الصحية23 و 84٪ في مجموعة متعددة المراكز ومتعددة البائعين من التليف الكيسي24 ، والتي أظهرت أيضا ارتباطا مشابها بمؤشر إزالة الرئة ل PREFUL و 129Xe (ص = 0.82 و ص = 0.91). أظهر تحليل التروية لنفس الدراسة أنه لا توجد فروق ذات دلالة إحصائية في التداخل المكاني مع DCE بين المراكز التي تمتقييمها 25. كما تم الإبلاغ عن التوافق مع DCE والاتفاق على نتائج PREFUL بين المراكز لدراسة فرعية مستقبلية بما في ذلك تسعة مراكز26. نتج عن تحليل التكاثر في مرضى الانسداد الرئوي المزمن معامل تباين أقل من 15٪ لجميع المعلمات27. تشير الدراسات الحالية إلى أن معلمة FVL تتمتع بقوة تنبؤية وحساسية أعلى للكشف عن تغيرات العلاج مقارنة بمعلمة التهوية "الثابتة" ، والتي تأخذ فقط مرحلتي الشهيق النهائي والزفير النهائي في الاعتبار. تم إثبات الاستجابة للعلاج بقياسات حلقة حجم التدفق الإقليمية (FVL) بعد العلاج بجهاز الاستنشاق بالإنداكاتيرول-جليكوبيرونيوم (IND / GLY) في مرض الانسداد الرئويالمزمن 28. بالتوافق ، تنبأت معلمة FVL بفقدان الكسب غير المشروع في مرضى زراعة الرئة المزدوجة ، في حين أن قياس التنفس لم يستطع (P = .02 مقابل P = 0.33) 29. تظهر دراسات الجدوى الأولى أنه يمكن تحقيق التصوير الرئوي الوظيفي باستخدام PREFUL عند الرضع وحديثي الولادة الذين يتنفسون بحرية باستخدام أجهزة التصوير بالرنين المغناطيسي السريريةالقياسية 30،31. قارن Glandorf et al. معلمات PREFUL عند 1.5T و 3T (تسلسل SPGRE) ولم يجد فروقا ذات دلالة إحصائية لمعظم المعلمات ، والتي كانت قابلة للتكرار بدرجة كبيرة على الرغم من الاختلاف في شدة المجال32. قد تكون هذه ميزة مهمة ، حيث لا يمكن لكل موقع الوصول إلى ماسحات ضوئية 1.5T أو أقل شدة مجال. في الآونة الأخيرة ، تم إثبات جدوى واكتشاف الأعراض المستمرة بعد الإصابة ب COVID-19 عند 0.55T من خلال تقييم بيانات bSSFP باستخدام PREFUL33.
باختصار ، على الرغم من كونها تقنية جديدة نسبيا ، فقد تمت دراسة PREFUL على نطاق واسع. تم تقييم معايير مهمة مثل التحقق من الصحة بقياسات أكثر مباشرة وراسخة ، وقابلية التكاثر ، والحساسية لعلم الأمراض ، والاستجابة للعلاج وتغييرات التقدم. ومع ذلك ، لا يزال هناك عدد قليل فقط من المراكز المتخصصة التي تستخدم هذه التقنية على الرغم من المتطلبات التكنولوجية المنخفضة. لذلك ، فإن الهدف من هذا العمل هو تلخيص أحدث منهجية PREFUL MR في شكل مكتوب ومرئي. يمكن استخدام هذه المعلومات لإنشاء هذه التقنية في المزيد من المراكز ، وبالتالي ، على المدى الطويل ، تؤدي إلى تقنية أكثر نضجا.
Protocol
حصلت هذه الدراسة على موافقة لجنة الأخلاقيات في كلية الطب في هانوفر ، مما يضمن التزامها بالمعايير الأخلاقية الصارمة طوال عملية البحث. اتبع التحقيق بدقة المبادئ التوجيهية الموضحة في إعلان هلسنكي ، مع التركيز على السلوك الأخلاقي للبحث الطبي. بالإضافة إلى ذلك ، تم الحصول على الموافقة المستنيرة بجد من جميع المشاركين في الدراسة (أو والديهم أو الوصي القانوني) قبل مشاركتهم في فحص التصوير بالرنين المغناطيسي. انظر الشكل 1 للحصول على نظرة عامة مبسطة على خطوات البروتوكول الأساسية ، والتي تتكون من الاستحواذ والتسجيل والتصفية والفرز ، وأخيرا تخليق دورة القلب والجهاز التنفسي. في الأقسام التالية ، يتم وصف جميع الخطوات المعنية بالتفصيل الكامل.
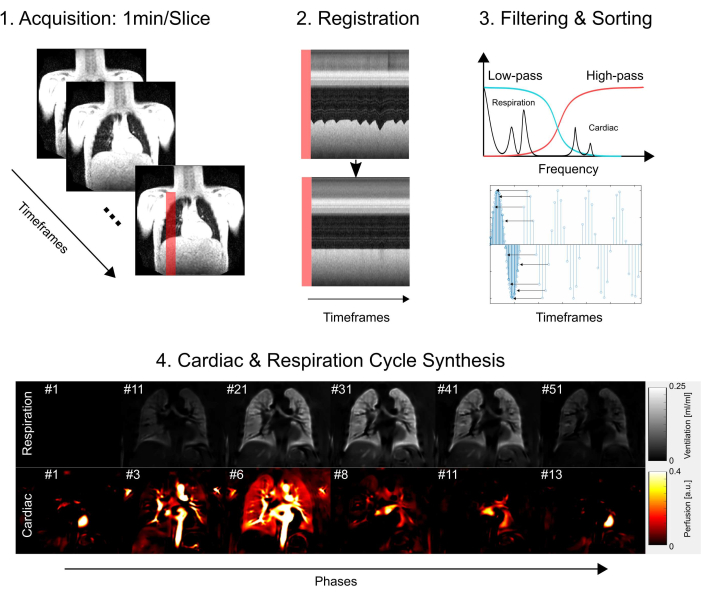
الشكل 1: نظرة عامة تخطيطية على المكونات الأساسية ل PREFUL. 1) الاستحواذ في التنفس الحر ، مما يستلزم 2) تعويض الحركة عن طريق التسجيل كما هو موضح في مخططات الملف الشخصي ويتيح تحليل voxel-by-voxel لمكونات فورييه كما هو موضح في الخطوة 3) التصفية والفرز. بعد التمرير المنخفض (التهوية) والترشيح العالي (التروية) ، 4) يتم استخدام المرحلة المقدرة لفرز الصور إلى دقة زمنية ظاهرة أعلى وتوليف دورة قلبية وتنفسية كاملة. لاحظ أن هذا مخطط مبسط وأن التفاصيل الكاملة موصوفة في المخطوطة. تشمل الخطوات الأخرى ، التي تم حذفها من هذا الشكل ، القياس الكمي للمعلمات وإنشاء التقارير. اختصار: PREFUL = الرئة الوظيفية التي تم حلها على الطور. الرجاء النقر هنا لعرض نسخة أكبر من هذا الرقم.
1. التوظيف
- تجنيد المرضى البالغين أو القاصرينفي تجربة التصوير بالرنين المغناطيسي PREFUL للمرضى والضوابط الصحية بناء على تشخيصهم لاضطراب رئوي بناء على فحص قياس التنفس و / أو التصوير السابق (على سبيل المثال ، الأشعة السينية أو التصوير المقطعي المحوسب) ؛ القدرة على إعطاء الموافقة المستنيرة. القدرة على الاستلقاء بشكل مسطح والبقاء ثابتا طوال مدة فحص التصوير بالرنين المغناطيسي ؛ ولا موانع معروفة للتصوير بالرنين المغناطيسي (على سبيل المثال ، الغرسات المعدنية ، رهاب الأماكن المغلقة).
- استبعاد المرضى إذا كانوا حوامل ، أو خضعوا لجراحة رئوية سابقة خلال الأشهر الستة الماضية ، أو يعانون من ضائقة تنفسية شديدة أو الحاجة إلى مكملات الأكسجين المستمرة ، أو لديهم ردود فعل سلبية سابقة لعوامل التباين القائمة على الجادولينيوم إذا تم استخدام التصوير بالرنين المغناطيسي المعزز بالتباين بالإضافة إلى PREFUL.
- تجنيد الضوابط الصحية إذا لم يكن هناكتاريخ معروف لأمراض الرئة بناء على الفحص السريري والتقرير الذاتي ؛ اختبارات وظائف الرئة طبيعية ؛ أنهم قادرون على إعطاء موافقة مستنيرة ؛ كانوا قادرين على الاستلقاء والبقاء ثابتين طوال مدة فحص التصوير بالرنين المغناطيسي ؛ وليس لديهم موانع معروفة للتصوير بالرنين المغناطيسي.
- استبعاد الأفراد كعناصر تحكم صحية وفقا لتاريخ التدخين الحالي أو السابق ، والتعرض لسموم الرئة المعروفة أو المخاطر المهنية ، والتاريخ العائلي لأمراض الرئة الوراثية ، وأي مرض مزمن معروف قد يؤثر على وظائف الرئة ، والحمل.
- الحصول على نماذج الموافقة. استمر في البروتوكول إذا تم الحصول على نموذج موافقة خطية مستنيرة من المشارك يحتوي على الغرض من البحث وإجراءاته ، وأي مخاطر وفوائد محتملة ، وتأكيدات السرية ، ومدة الدراسة ، والحق في الانسحاب دون عواقب.
- تطبيق الخطوات الإضافية التالية عندما يشمل التوظيف القاصرين.
- الحصول على موافقة خطية مستنيرة من أحد الوالدين أو الوصي على الأقل بالإضافة إلى موافقة القاصر.
- اعرض العملية برمتها بطريقة مناسبة للعمر ومفهومة للقاصر.
- بالنسبة للقصر الأصغر سنا ، استخدم الوسائل المرئية أو كتب القصص أو التفسيرات المبسطة.
- التأكد من أن الدراسة ذات صلة بالفئة العمرية وعدم إدراج القاصرين دون داع.
- السماح للقاصرين بأن يكونوا برفقة شخص بالغ موثوق به (على سبيل المثال، الوالد أو الوصي) أثناء جميع الإجراءات المتعلقة بالمحاكمة ما لم يتعارض ذلك مع نزاهة المحاكمة.
ملاحظة: تفترض الخطوات الموصوفة أن التجربة قد تمت مراجعتها والموافقة عليها من قبل لجنة الأخلاقيات.
- تطبيق الخطوات الإضافية التالية عندما يشمل التوظيف القاصرين.
2. الاستحواذ
- إجراء إجراءات السلامة المسبذولة.
- قبل التصوير بالرنين المغناطيسي ، قم بإجراء فحص مسبق مفصل للمرضى لتحديد موانع الاستعمال المحتملة مثل العمليات الجراحية السابقة أو الأجهزة المزروعة أو الوشم أو التعرض لشظايا معدنية.
- عند الوصول ، قم بتثقيف المرضى حول الخصائص المغناطيسية للإجراء ومخاطره.
- توجيه المرضى لإزالة جميع العناصر المعدنية الشخصية ، بما في ذلك المجوهرات والساعات وبعض مكونات الملابس ، وتزويدهم بثوب إذا لزم الأمر.
- اطلب من أخصائي مدرب فحص المرضى بصريا بحثا عن الأجسام المعدنية التي يتم التغاضي عنها.
- فحص جميع الأجهزة الطبية أو الغرسات للتأكد من توافقها مع التصوير بالرنين المغناطيسي.
- تأكد من وجود بروتوكولات الطوارئ لكل من الموظفين وسلامة المرضى.
- وضع المشارك والمسح الضوئي
- قم بتوجيه المريض رأسه أولا وضعه في وضع ضعيف على نظام 0.55T أو 1.5T أو 3T.
- توفير حماية السمع وجرس الطوارئ والحشو والبطانية للسلامة والراحة.
- ضع ملفا مرنا متعدد القنوات أسفل الذقن مباشرة لضمان حساسية الملف المثلى عبر جميع مناطق الرئة.
- قم بتأمين موضع الملف للحفاظ على الثبات دون إعاقة تنفس المريض.
- اطلب من المريض أن يغمض عينيه ، ثم حدد مركز الرئة باستخدام ليزر التصوير بالرنين المغناطيسي.
- قم بمحاذاة مركز الرئة عند المركز المتساوي واسمح للمريض بفتح عينيه مرة أخرى.
- امسح المترجمات الأولية لتحديد اتجاه عام ، متبوعا بمسح مورفولوجي عرضي لتحديد تشعب القصبة الهوائية.
- قم بتثبيت الشريحة الإكليلية الأولى عند تشعب القصبة الهوائية كمعلم ثابت لتعزيز قابلية التكاثر.
- اعتمادا على بروتوكول المسح ، إما التقاط ثلاث شرائح متباعدة بمسافة شريحة إلى شريحة (تقاس من الحافة إلى الحافة) بنسبة 100٪ (من سمك الشريحة) أو الحصول على شرائح متعددة تمتد عبر الرئة بأكملها بمسافة 20٪ أو 33٪.
- احصل على كل شريحة بشكل منفصل تماما وليست متشابكة.
- قم بتحميل الصور المعاد بناؤها إلى نظام أرشفة الصور والاتصال (PACS) للوصول إليها وتحليلها لاحقا. بدلا من ذلك، للالتزام بمعايير الخصوصية وحماية البيانات، قم بتصدير الصور يدويا إلى محرك أقراص شبكة معين أو حل تخزين مشابه.
ملاحظة: للحصول على معلومات مفصلة عن بروتوكول التسلسل والمعلمات، يرجى الرجوع إلى الجدول 1 والجدول 2. للحصول على تمثيل مرئي لموضع الشريحة ، انظر الشكل 2.
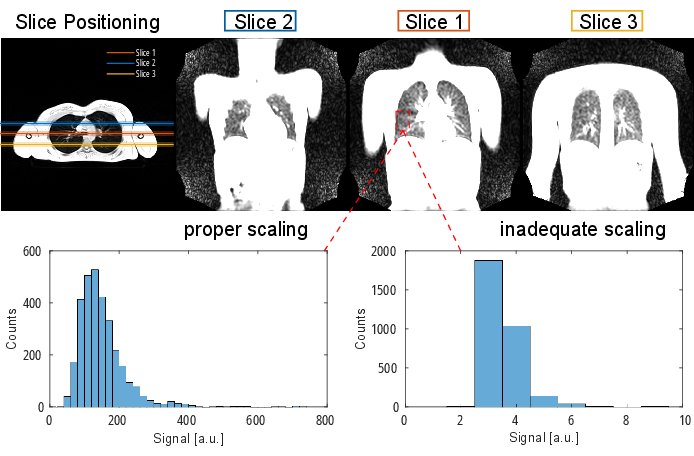
الشكل 2: وضع شريحة نموذجي لتجربة PREFUL تم تصورها باستخدام صدى تدرج ثلاثي الأبعاد في اتجاه عرضي. لاحظ أن الشريحة الأولى موضوعة عند تشعب القصبة الهوائية كمعلم قابل للتكرار. يتم وضع الشرائح2 و 3 مع فجوة شريحة بنسبة 100٪ في الاتجاهين الأمامي والخلفي. تظهر الرسوم البيانية النموذجية توزيعات القيمة مع القياس المناسب وغير الكافي (المنخفض). هذا الأخير يؤدي إلى نطاق ديناميكي منخفض وفقدان الدقة. يجب أيضا تجنب القياس العالي غير الكافي ، والذي يؤدي إلى القص (غير موضح هنا). اختصار: PREFUL = الرئة الوظيفية التي تم حلها على الطور. الرجاء النقر هنا لعرض نسخة أكبر من هذا الرقم.
الجدول 1: مخطط نموذجي لبروتوكول PREFUL. بعد المترجم ، يتم الحصول على حجم ثلاثي الأبعاد من الرئة في اتجاه عرضي. يستخدم هذا الاستحواذ لتخطيط عمليات الاستحواذ PREFUL التالية (انظر أيضا الجدول 2 لإعدادات التسلسل والشكل 2 لتحديد مواقع الشرائح). يمكن إضافة تسلسلات أخرى حسب الدراسة. اختصار: PREFUL = الرئة الوظيفية التي تم حلها على الطور. الرجاء النقر هنا لتنزيل هذا الجدول.
الجدول 2: ملخص معلمات التسلسل لاكتساب PREFUL مع تسلسل صدى التدرج الفاسد. الاختصارات: PREFUL = الرئة الوظيفية التي تم حلها على الطور ؛ SPGRE = تسلسل صدى التدرج المدلل. الرجاء النقر هنا لتنزيل هذا الجدول.
3. المعالجة اللاحقة
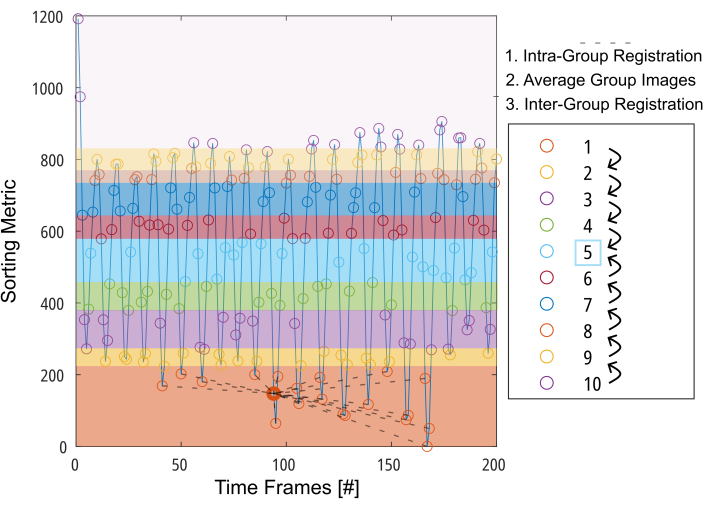
الشكل 3: عرض تخطيطي للتسجيل الموجه للمجموعة لتقليل التشوه المطلوب لتعويض الحركة. بعد تقسيم الصور (ممثلة بالدوائر) إلى 10 مجموعات بناء على مقياس الفرز (على سبيل المثال ، منطقة الرئة المجزأة) ، يتم تسجيل الصور داخل كل مجموعة في موضع وسيط (موضح بخطوط متقطعة للمجموعة 1). بعد ذلك ، يتم حساب متوسط الصور المسجلة واستخدامها في الخطوة الأخيرة من التسجيل بين المجموعات بطريقة خطوة بخطوة نحو المجموعة الوسيطة. الاختصار: GOREG = التسجيل الموجه نحو المجموعة. الرجاء النقر هنا لعرض نسخة أكبر من هذا الرقم.
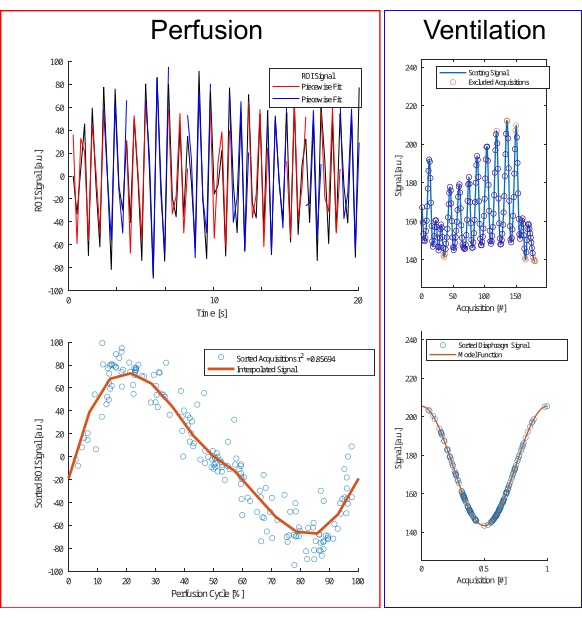
الشكل 4: رسم توضيحي لخوارزمية الفرز للتروية والتهوية. بالنسبة للتروية (على اليسار) ، يتم إجراء تركيب بالقطعة (الصف العلوي) لتقدير المرحلة واللجوء إلى عمليات الاستحواذ (الصف السفلي). بالنسبة للتهوية (على اليمين) ، يتم استبعاد القيم المتطرفة (الصف العلوي) وفرزها وفقا لنموذج جيب التمام (الصف السفلي) بناء على فرق السعة والسعة للتمييز بين مرحلتي الزفير والإلهام. الرجاء النقر هنا لعرض نسخة أكبر من هذا الرقم.
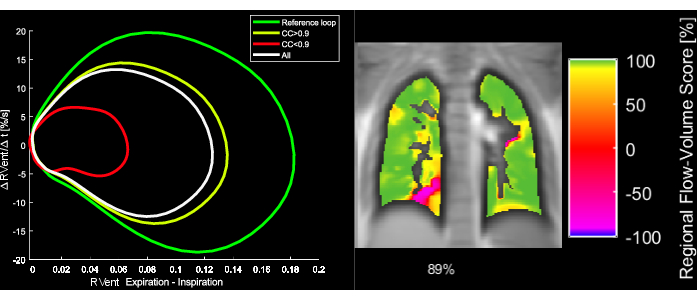
الشكل 5: حلقات حجم التدفق النموذجية ومقياس ارتباط FVL المقابل لمريضة تبلغ من العمر 43 عاما مصابة بمرض الانسداد الرئوي المزمن. لاحظ أنه مع تغيير FVL ، ينخفض FVL-CM. الاختصارات: FVL = حلقة حجم التدفق ؛ FVL-CM = مقياس ارتباط FVL ؛ مرض الانسداد الرئوي المزمن = مرض الانسداد الرئوي المزمن. الرجاء النقر هنا لعرض نسخة أكبر من هذا الرقم.
الجدول 3: تطبيق العتبات على خرائط المعلمات ومجموعة من خرائط العيوب. الرجاء النقر هنا لتنزيل هذا الجدول.
- تسجيل
ملاحظة: في القسم التالي ، يتم وصف إجراء التسجيل غير الصلب إلى حجم مرجعي (يفضل مستوى التنفس متوسط المستوى) باستخدام مخطط موجه نحو المجموعة (GOREG) لتعويض التنفس وحركة القلب.- استرجع الصور.
- في البداية ، قم بإجراء تجزئة الرئة على جميع الصور غير المسجلة ، باستخدام U-Net مدربة وقم بتطبيق مرشح تمرير منخفض مع قطع 0.7 هرتز للحصول على تقدير لمراحل التنفس.
ملاحظة: سيؤدي هذا إلى بدء مسار المعالجة المؤتمتة بالكامل، والذي سيقوم بتنفيذ الخطوات اللاحقة في الخلفية. لا تقتصر خطوات المعالجة الموضحة والموضحة على تطبيق أو لغة معينة ، وبالتالي ، يمكن تنفيذها في تطبيق مخصص به العديد من لغات البرمجة. - صنف كمية كبيرة من الفوكسل المجزأة على أنها مصدر إلهام وكمية منخفضة على أنها انتهاء صلاحية.
- قم بتجميع الصور عن طريق تقسيمها إلى 10 بالمائة ، مع التأكد من أن كل مجموعة من المجموعات العشر الناتجة تحتوي على عدد متساو من الصور.
- حدد ANTs34 (BSplineSyN مع مقياس الارتباط المتبادل) أو Forsberg35،36 (تمدد متعدد الحدود مع تنظيم المرونة والسوائل) كخوارزمية التسجيل.
- إجراء التسجيل الداخلي لكل مجموعة نحو وضع الرئة المتوسط للمجموعة المعنية.
- متوسط نتائج المجموعة للحصول على صورة واحدة لكل مجموعة.
- قم بإجراء التسجيل البيني من كل صورة مجموعة باتجاه الجار التالي فياتجاه المجموعة الخامسة.
- قم بتطبيق سلسلة التشوهات على الصور الأصلية ، حسب الضرورة للوصول إلى موضع الجهاز التنفسي الذي يمثله متوسط الصورة في المجموعة 5. على سبيل المثال ، بالنسبة للصورة 36 ، التي تنتمي إلى المجموعة 3 ، يتم تطبيق حقول التشوه التالية: 36->الصورة 57 (~ وضع الرئة المتوسط في المجموعة 3) -> الخطوة 3->4 -> الخطوة 4->5.
ملاحظة: للحصول على وصف تفصيلي لإجراء GOREG، يرجى الرجوع إلى الشكل 3. قم بإجراء التسجيل باستخدام الحوسبة المتوازية لتقليل وقت المعالجة. يتم إجراء تسجيل GOREG لتقليل مقدار التشوه المطلوب لكل خطوة تسجيل وبالتالي ضمان تقارب الخوارزمية المستقر. ومع ذلك ، يمكن أيضا إجراء التسجيل بخطوة تشوه واحدة فقط نحو وضع الرئة المتوسط. في حين أن جميع دراسات 2D PREFUL المنشورة استخدمت ANTs ، فإن Forsberg ينتج عنه نتائج تصل إلى 6 مرات أسرع مع نتائج ذات جودة مماثلة كما ذكرت في دراسة 3D PREFUL37. تم إنشاء نتائج نموذجية في هذا التقرير من خلال تسجيل Forsberg. راجع الشكل 1 لرؤية رسم توضيحي لتأثير التسجيل على حركة الحجاب الحاجز.
- التصفية العامة
- قم بإزالة التشويش من الصور المسجلة باستخدام التصفية الموجهةبالصور 38 ، باستخدام الصورة المسجلة في المتوسط الزمني كصورة إرشادية. قم بتطبيق الإعدادات التالية: NeighborhoodSize = [10، 10]، DegreeOfSmoothing = 1.
- لتحليل التهوية والتروية ، استخدم مرشح التمرير المنخفض أو العالي مع قطع عند 0.7 هرتز لقمع المكون الآخر المعني. استبعاد أول 20 صورة من جميع خطوات المعالجة الإضافية ، باستثناء حساب التروية الكمي ، لضمان حالة ثابتة في السلسلة الزمنية المضمنة.
ملاحظة: قد يكون من الضروري تغيير الحد إذا كان معدل التنفس أعلى من ~ 40 نفسا / دقيقة.
- تجزئه
ملاحظة: يتم إجراء التجزئة النهائية باستخدام الصور المسجلة في وضع الرئة المتوسط في إجراء من خطوتين كما هو موضح في ما يلي.- قم بإجراء تجزئة حدود الرئة (عائد الاستثمار للرئة) على الصور المسجلة المتوسطية مؤقتا باستخدام U-Net مدربة أو يدويا.
- بعد ذلك ، استبعد الأوعية المركزية الكبيرة لتحسين تجزئة حدود الرئة والحصول على منطقة ذات أهمية أو عائد استثمار لحمة الرئة.
- التروية
ملاحظة: الخطوات التالية مطلوبة لتقدير المرحلة القلبية بدقة لكل صورة في السلسلة المكتسبة ، والتي يتم أخذ عينات منها بتردد منخفض نسبيا (~ 3-5 صور / ثانية) ، خاصة بالمقارنة مع معدل ضربات القلب (عادة 40-90 نبضة في الدقيقة). يتم استخدام إعادة ترتيب البيانات وفقا لمراحل القلب المحددة للحصول على دورة القلب الكاملة مع دقة زمنية محسنة ، متجاوزة معدل أخذ العينات للحصول على البيانات18 (راجع الشكل 4 للحصول على توضيح لإجراء الفرز). لتقدير الطور ، يلزم عائد استثمار بحث بإشارة قوية مرجحة بالنضح. استخدم خوارزمية بحث تكرارية على النحو التالي22.- قم بتوصيل عائد الاستثمار لحدود الرئة لتضمين المنصف في عائد الاستثمار للبحث.
- قم بإنشاء خريطة بسيطة مرجحة بالتروية عن طريق حساب الانحراف المعياري عبر تسلسل الصورة.
- حدد المناطق المقابلة للنسبة المئوية 98 من هذه الخريطة ضمن عائد الاستثمار للبحث كعائد استثمار أولي للخطوات اللاحقة.
- قم بإجراء التركيب الحكيم للقطعة ، وزيادة حجم نقاط البذور طالما تحسن أداء التركيب.
- رتب عائد الاستثمار الموسع للبذور وفقا لأدائها المناسب.
- اجمع بشكل متكرر بين عائد الاستثمار للبذور الأفضل موسعا مع ثاني أفضل ، وثالث أفضل ، وما إلى ذلك ، حتى لا يحسن المزيج المقياس أو يتم النظر في جميع عائد الاستثمار للبذور. ضع في اعتبارك أن عائد الاستثمار النهائي هو عائد الاستثمار للوعاء المستخدم لتقدير مرحلة القلب.
- متوسط الإشارة مكانيا داخل تقدير الطور الأمثل لإنتاج سلسلة زمنية إشارة واحدة لتقدير الطور.
- قم بإجراء التقدير بالقطعة عن طريق تقسيم الإشارة إلى أجزاء أصغر باستخدام الحد الأقصى المحلي للإشارة ، متبوعا بملاءمة جيبية مجزأة مع مراعاة معلمات مثل السعة وإزاحة الطور والتردد (الشكل 4).
- قم بفرز الصور على طور لتمثيل دورة قلبية واحدة.
- استخدم انحدار نواة Nadaraya-Watson مع نواة Gaussian (سيجما = 0.1) لاستعفاء 15 مرحلة على شبكة زمنية متباعدة بشكل موحد تشمل دورة قلبية واحدة.
ملاحظة: ارجع إلى الشكل 1 للحصول على مجموعة فرعية من دورة قلبية كاملة نموذجية مركبة لمتطوع سليم ، بدءا من الانبساط ، والانتقال إلى الانقباض ، والعودة إلى الانبساط.
- التهوية
ملاحظة: لتحليل التروية ، لاحظ أن تردد القلب يظل مستقرا نسبيا مع اختلافات ضئيلة في السعة. في المقابل ، تميل التهوية إلى تجربة المزيد من الاختلافات في حجم المد والجزر وتواترها ، مما يؤدي إلى حالات تنفسية مختلفة مع مراحل تنفسية متطابقة لا يكون لها دائما نفس السعة. مستوحى من نهج Fischer et al. للبوابة الذاتية ، من الضروري تصنيف التهوية بناء على سعة الإشارة.- استبعاد القيم المتطرفة المتطرفة باستخدام القواعد التجريبية (البيانات الأقل من النسبة المئوية الخامسة أو أعلى من النسبة المئوية 97).
- اشتقاق مدى الاتساع R والعزاحة C من سلسلة الإشارة الزمنية التي تم إنشاؤها لتجميع التسجيل.
- حدد دالة نموذج A (t) بتردد محدد بشكل تعسفي fالتنفس (هنا 0.3 هرتز):
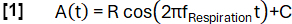
- تصنيف البيانات إلى حالات الإلهام والانتهاء بناء على المنحدر.
- تحقيق تحديد طور أكثر دقة وفقا لوظيفة النموذج:
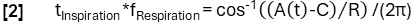
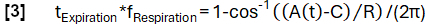
- بعد ذلك ، قم بمحاذاة العينات بناء على مرحلتها وقم بتطبيق انحدار نواة Nadaraya-Watson لحساب التهوية على فترات متباعدة بشكل موحد أثناء الدورة التنفسية.
- احسب التهوية الإقليمية (RVent) لكل مرحلة قياسا على المعادلة 1 ، واستبدل مرحلة الإلهام بالمرحلة المعنية.
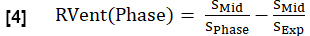
ملاحظة: راجع الشكل 1 لرؤية مجموعة فرعية من دورة تنفسية كاملة نموذجية مركبة لمتطوع سليم ، بدءا من انتهاء الصلاحية ، والانتقال إلى الإلهام ، ثم العودة إلى انتهاء الصلاحية. للحصول على توضيح لخوارزمية الفرز ، انظر الشكل 4.
- حساب المعلمة
ملاحظة: باستخدام دورات التنفس والقلب الكاملة المركبة ، يمكن للمرء اشتقاق المزيد من المعلمات. يتم وصف مجموعة مختارة من أهم المعلمات في ما يلي. - التهوية الإقليمية (RVent)
- باستخدام طور الشهيق ، اشتقاق RVent وفقا لما يلي:
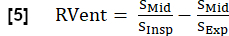
- باستخدام طور الشهيق ، اشتقاق RVent وفقا لما يلي:
- مقياس ارتباط حلقة حجم التدفق (FVL-CM)
ملاحظة: لتقييم جميع مراحل التنفس ، يتم تنفيذ سلسلة من الخطوات لإنشاء التصوير بالرنين المغناطيسي المكافئ لتحليل FVL قياسا على اختبار وظائف الرئة.- احسب منحدر التهوية الإقليمية (RVent) كبديل للتدفق باستخدام مشتق المرة الأولى من RVent. استخدم حاصل فرق متماثل بطول الخطوة h:
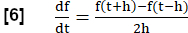
- اختياريا ، اعرض منحدرات RVent الإقليمية أو المتوسطة كدالة ل RVent المعنية ، وبالتالي إنشاء مكافئ PREFUL لتحليل FVL.
- حدد عائد الاستثمار المرجعي من خلال تحديد أكبر منطقة متصلة بقيم RVent في النطاق المئوي من 80 إلى 90 في عائد الاستثمار لحمة الرئة.
- متوسط حلقات حجم التدفق داخل عائد الاستثمار المرجعي المحدد.
- لتحديد تشابه كل FVC للرئة مع المرجع ، قم بالربط المتبادل بين كل FVC في عائد الاستثمار لحمة الرئة بالمرجع بدون تأخير:
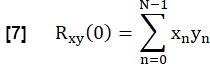
- قم بتطبيعها وفقا لما يلي:
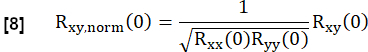
هنا ، يمثل x و y المرجع ومنحنى تدفق RVent المعني.
ملاحظة: لاحظ أنه يتم استخدام عدم التأخير بحيث يؤدي تأخير التهوية إلى ارتباط أقل.
ملاحظة: ارجع إلى الشكل 5 للحصول على توضيح لحساب FVL ومقياس FVL-CM المشتق.
- احسب منحدر التهوية الإقليمية (RVent) كبديل للتدفق باستخدام مشتق المرة الأولى من RVent. استخدم حاصل فرق متماثل بطول الخطوة h:
- التروية الكمية
ملاحظة: يتم إجراء القياس الكمي وفقا ل Glandorf et al. باستخدام الصور الأولى التي تم الحصول عليها خلال الحالة العابرة36.- تطبيع الصور الأربع الأولى المسجلة إلى مستوى منتصف الإلهام باستخدام كمية فوكسل الرئة A كما تم حسابها في الخطوة 3.1.2. يتم التعبير عن هذا الانخفاض في التعديل الناجم عن تغير كثافة البروتون على النحو التالي:
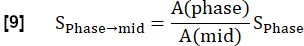
- قم بإجراء ملاءمة أسية لتقدير الإشارة المرتبطة بأقصى قدر من المغنطة باستخدام النموذج:
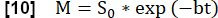
- تحديد خريطة Q المتعلقة بالتروية المتني باستخدام مرحلة الدورة القلبية التي تظهر الإشارات القصوى في عائد الاستثمار لحمة الرئة.
- لتقدير جزء الدم الإقليمي (BF) ، قم بتطبيع قيمة S0 عن طريق حساب متوسط القيم فوق 99.99 بالمائة في عائد الاستثمار للبحث (فوكسل الدم الكامل):
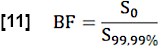
- قم بتقدير كسر التبادل (EF) أثناء الدورة القلبية من خلال النظر في نسبة الحد الأقصى لفرق الإشارة المتوسط بين الحالة المستقرة (SS) والحالة الأولية كما هو محدد بواسطة S0 وفرق الإشارة المرتبط بالتدفق Q:
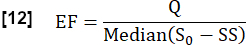
- تحديد تردد القلب fالقلب في 1 / ثانية من عائد الاستثمار للوعاء باستخدام تحليل فورييه (التردد المقابل لأكبر ذروة).
- احسب التروية الكمومية النهائية (QQ) بالملل∙min-1∙100 mL-1 على النحو التالي:
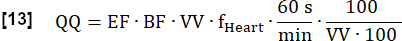
ملاحظة: هنا ، يتم إلغاء حجم فوكسل (VV) [مل / مل] ، ويتم استخدام عامل التحويل 60 ثانية / دقيقة وعامل الاتفاقية 100/100 لعرض النتيجة النهائية في [مل ∙ دقيقة -1∙ 100 مل -1]. EF و BF هي نسب بلا أبعاد.
- تطبيع الصور الأربع الأولى المسجلة إلى مستوى منتصف الإلهام باستخدام كمية فوكسل الرئة A كما تم حسابها في الخطوة 3.1.2. يتم التعبير عن هذا الانخفاض في التعديل الناجم عن تغير كثافة البروتون على النحو التالي:
- العتبة والإحصاءات
- وصف إحصائيا المعلمات المذكورة أعلاه للشريحة الوسطى وجميع الشرائح ذات القيمة المتوسطة (جميع القيم / قيم الشريحة الوسطى) والانحراف المعياري (جميع القيم / قيم الشريحة الوسطى فقط).
- بالإضافة إلى ذلك ، قم بتطبيع الانحراف المعياري لمعامل التباين للحصول على حساب نسبي للتشتت. حدد متوسط القيمة ومعامل التباين كمخرجات إحصائية نهائية.
- تطبيق العتبات على خرائط المعلمات لإنشاء خرائط العيوب واستخلاص قيم النسبة المئوية للعيب (انظر الجدول 3).
- تصنيف القيم التي تقل عن العتبات على أنها عيب في التهوية أو التروية (VD / QD). اجمع بين هذه الخرائط بشكل أكبر لتحديد تداخل العيوب والمناطق العادية (فئات V / Q) ، بما في ذلك المجموعات التالية كما هو موضح في الجدول الرباعي في الجدول 3:
- احسب النسبة المئوية للعيب في فئات عيب التهوية (VD) وعيب التروية (QD) والتهوية / التروية (V / Q) كعدد فوكسل مع الفئة المعنية فيما يتعلق بإجمالي فوكسيل حمة الرئة:
نسبة العيب = #DefectVoxels / #LungParenchyma - احسب نسبة الخلل هذه لكل شريحة والشرائح الإكليلية المركبة. في هذه الدراسة ، اختر النهج المشترك ، حيث يتم تحديد عيب التهوية عن طريق عملية OR: VD = VD (RVent) أو VD (FVL-CM).
ملاحظة: تم إجراء التحليل الموصوف باستخدام تطبيق برمجيات تجاري (انظر جدول المواد) باستخدام صندوق أدوات تسجيل Forsberg.
| البارامتر | عتبة | التعليق |
| RVent | 90النسبة المئوية * 0.4 | العتبة التكيفية |
| FVL-سم | 90% | عتبة ثابتة |
| Q | 90النسبة المئوية * 0.15 | العتبة التكيفية |
| V / Q | لا دينار قطري | دينار قطري |
| لا VD | عادي | عدم تطابق VQ (QD حصري) |
| في دي | عدم تطابق VQ (VD حصري) | VQ عيب المباراة |
النتائج
يوضح الجزء السفلي من الشكل 2 نتيجة القياس المناسب وغير الكافي مع تأثير مماثل على النطاق الديناميكي. يوضح الشكل 6 توزيع الإشارة غير المتجانس ، والذي يمثل عمليات المسح بدون ومعها تطبيع الملف. يوصى بتجنب النطاق الديناميكي المنخفض والصور بدون تطبيع الملف.
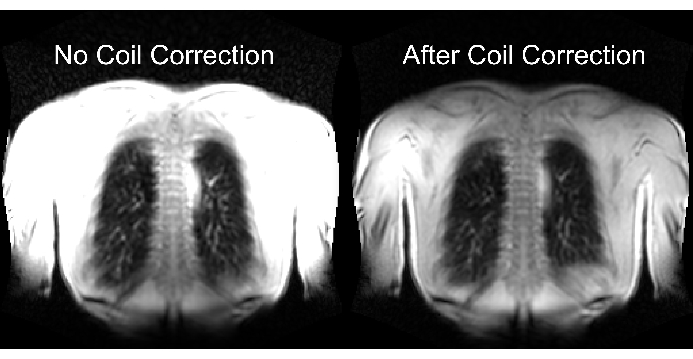
الشكل 6: صور نموذجية بعد الاستحواذ بدون تصحيح الملف (غير صحيح) ومع تصحيح الملف (صحيح). لاحظ تحسين الإشارة الاصطناعية عند حدود الجسم بالقرب من عناصر الملف. الرجاء النقر هنا لعرض نسخة أكبر من هذا الرقم.
يوضح الشكل 7 التجزئة التلقائية الناجحة والفاشلة. لاحظ أن التجزئة الفاشلة لا تشمل جميع فوكسيل الرئة ، مما سيؤدي إلى تزوير المزيد من التحليلات والإحصائيات. مطلوب عناية خاصة للحالات التي تحتوي على تسلل حيث يمكن تصنيف هذه الفوكسل بشكل خاطئ على أنها سفن بسبب إشارتها العالية بواسطة نماذج الذكاء الاصطناعي أو عدم تجزئتها على الإطلاق.
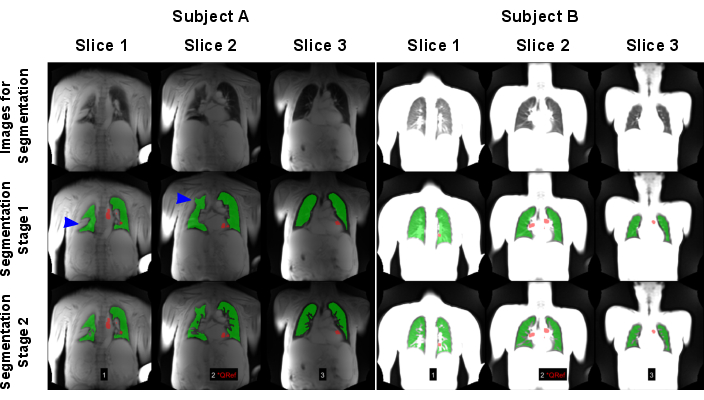
الشكل 7: مثال على التجزئة الآلية التي أدت إلى فشل (الموضوع أ: رجل يبلغ من العمر 83 عاما مصاب بمرض الانسداد الرئوي المزمن) ونتيجة ناجحة (الموضوع ب: أنثى تبلغ من العمر 30 عاما تحكم صحي). يعرض الصف الأول الصور التي تم استخدامها كمدخلات لنماذج الذكاء الاصطناعي. يوضح الصف الثاني نتائج مرحلة التجزئة الأولى التي تتكون من إيجاد حدود الرئة. يوضح الصف الثالث النتيجة النهائية بعد استبعاد السفن. كما هو موضح في الأسهم الزرقاء ، تم تحدي الخوارزمية من خلال اختلافات الرئة عالية الإشارة التي تسببت في اكتشاف حدود الرئة بشكل خاطئ. لاحظ أنه تم تطبيع الصور بواسطة الإشارة القصوى ، مما أدى إلى نتائج مختلفة بسبب فقدان تطبيع الملف للمسح الذي تم إجراؤه على الموضوع A. تظهر المناطق الحمراء عائد الاستثمار ، والذي تم اكتشافه تلقائيا لفرز مرحلة التروية. الاختصارات: مرض الانسداد الرئوي المزمن = مرض الانسداد الرئوي المزمن. عائد الاستثمار = مناطق الاهتمام. الرجاء النقر هنا لعرض نسخة أكبر من هذا الرقم.
يوضح الشكل 8 والشكل 9 خرائط معلمات تمثيلية للتحكم الصحي (30 عاما ، أنثى) ومريض مرض الانسداد الرئوي المزمن (60 عاما ، ذكر). لاحظ أن التحكم الصحي يظهر تهوية ونضح أكثر تجانسا ، وبالتالي ، عدد أقل من فوكسل المعيب. ويمكن الاطلاع على التقارير المقابلة لإحصاءات عائد الاستثمار في الجدول 4 والجدول 5.
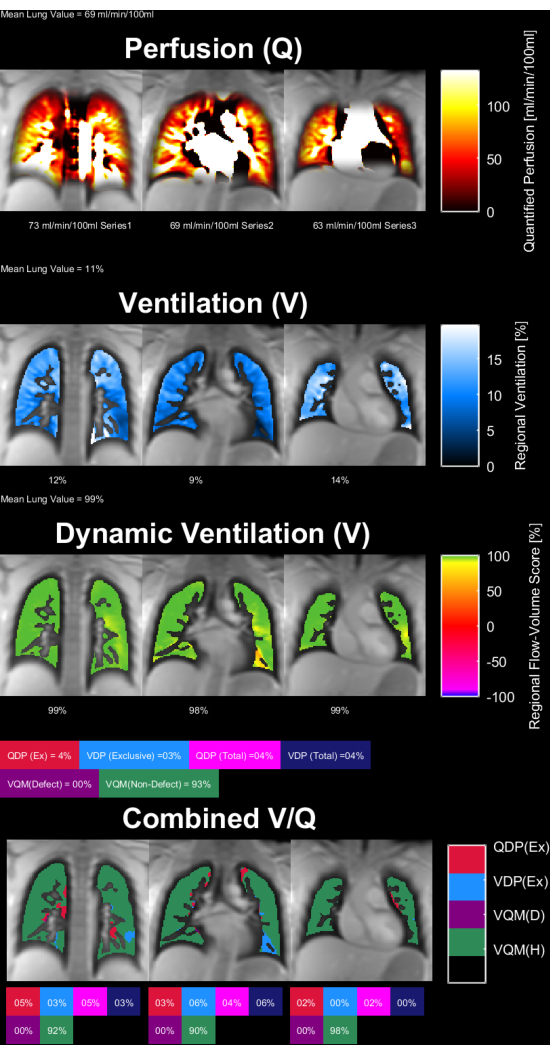
الشكل 8: خرائط معلمات PREFUL لأنثى تبلغ من العمر 30 عاما تتحكم بصحة جيدة. التروية(الصف 1 ) ، والتهوية الإقليمية(الصف الثاني ) ، ومقياس ارتباط حلقة حجم التدفق(الصف 3 ) ، وخرائط V / Q العتبة(الصف الرابع). لاحظ التوزيع المتجانس للقيم المتني والنسب المنخفضة للعيب. الاختصارات: PREFUL = الرئة الوظيفية التي تم حلها على الطور ؛ V = التهوية ؛ س = التروية. الرجاء النقر هنا لعرض نسخة أكبر من هذا الرقم.
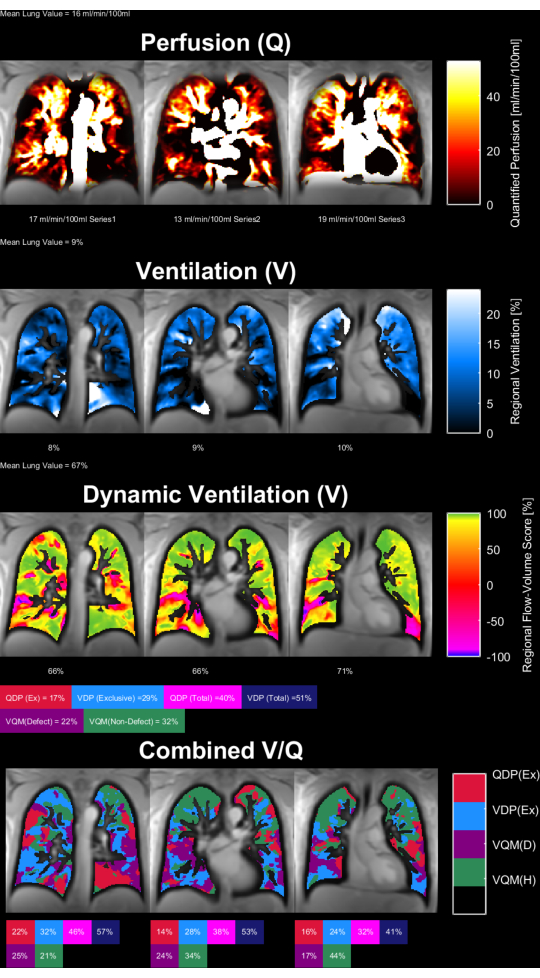
الشكل 9: خرائط معلمات PREFUL لمريض مرض الانسداد الرئوي المزمن يبلغ من العمر 60 عاما. التروية(الصف 1 ) ، والتهوية الإقليمية(الصف الثاني ) ، ومقياس ارتباط حلقة حجم التدفق(الصف 3 ) ، وخرائط V / Q العتبة(الصف الرابع). لاحظ التوزيع غير المتجانس للقيم المتني والنسب المئوية العالية للعيب. الاختصارات: مرض الانسداد الرئوي المزمن = مرض الانسداد الرئوي المزمن. PREFUL = الرئة الوظيفية التي تم حلها على الطور ؛ V = التهوية ؛ س = التروية. الرجاء النقر هنا لعرض نسخة أكبر من هذا الرقم.
الجدول 4: تقرير نموذجي لمعلمات PREFUL التي تم الحصول عليها لتحكم صحي (أنثى تبلغ من العمر 30 عاما). لاحظ قيم معامل التباين والعيب المنخفضة ، والتي تتماشى مع خرائط المعلمات المعروضة في الشكل 8 لنفس الموضوع. انظر أيضا الجدول 5 والشكل 9. اختصار: PREFUL = الرئة الوظيفية التي تم حلها على الطور. الرجاء النقر هنا لتنزيل هذا الجدول.
الجدول 5: تقرير نموذجي لمعلمات PREFUL التي تم الحصول عليها لمريض مرض الانسداد الرئوي المزمن (ذكر يبلغ من العمر 60 عاما). لاحظ قيم معامل التباين والعيب العالية ، والتي تتماشى مع خرائط المعلمات المعروضة في الشكل 9 لنفس الموضوع. انظر أيضا الجدول 4 والشكل 8. الرجاء النقر هنا لتنزيل هذا الجدول.
المواد التكميلية: شرح متحرك لخوارزمية PREFUL. الرجاء النقر هنا لتنزيل هذا الملف.
Discussion
الخطوات الحاسمة
أحد أكثر المزالق شيوعا أثناء الاستحواذ هو عدم كفاية قياس الإشارة ، مما يتسبب في فقدان المعلومات أثناء تحويل DICOM بسبب انخفاض دقة تمثيل البيانات الرقمية. وبالتالي ، يمكن أن يؤدي هذا إلى مشاكل أثناء مرحلة ما بعد المعالجة. مأزق آخر أكثر أهمية هو الحصول على شرائح متعددة بطريقة متشابكة. وبالتالي ، يتم تقليل الدقة الزمنية الفعالة للشرائح الفردية بشكل خطير. بالإضافة إلى ذلك ، اعتمادا على مسافة الشرائح ، يمكن أن يكون لذلك تأثير على تباين التروية وتقديرها الكمي لأن التدفق يعتمد على دورات جديدة بدون تاريخ مغنطة. مطلوب عناية خاصة أثناء إعداد البروتوكول ، خاصة فيما يتعلق بقوة التدرج والصدى غير المتماثل وعرض النطاق الترددي والتصوير المتوازي. يمكن أن تؤدي الانحرافات عن الإعدادات المقترحة حتى لواحد فقط من هذه المعلمات إلى عدم كفاية TE والدقة الزمنية.
تتكون المعالجة اللاحقة من خطوات متعددة ، والتي يجب اتباعها بالترتيب الموصوف. على سبيل المثال ، التسجيل بعد تصفية التمرير المنخفض ليس ذا معنى. وبالتالي ، يؤدي الفشل في خطوة واحدة إلى انهيار خلال الخطوات التالية. هذا يجعل مرحلة التسجيل مهمة بشكل خاص. نظرا لعدم وجود خوارزمية تسجيل واحدة ، اعتمادا على التنفيذ المعني ، يجب تعيين المعلمات تجريبيا. بدون ضبط هذه المعلمات ، سيمنع التسجيل الخاطئ توليد أي نتيجة ذات مغزى. خطوة أخرى قد تستغرق وقتا طويلا وحاسمة أثناء المعالجة اللاحقة هي التجزئة. يمكن أن تؤدي التجزئة الخاطئة إلى حسابات معلمات خاطئة تماما (على سبيل المثال ، عن طريق تضمين المناطق غير الرئوية) في التقرير النهائي. من المرجح أن تحدث مثل هذه التجزئة الخاطئة مع خوارزميات التعلم العميق ، والتي اعتادت على ظهور صور معينة ويتم تطبيقها على صور من بائع / آلة أخرى ذات مظهر مختلف قليلا. وبالتالي ، فإن فحص الجودة المرئية لدقة التجزئة ، مع التصحيح اليدوي المحتمل ، إلزامي.
استكشاف الاخطاء
يتمثل الإجراء النموذجي لاستكشاف الأخطاء وإصلاحها في اتباع جميع الخطوات واحدة تلو الأخرى والتحقق من معقولية النتائج الوسيطة. الإجراء الخاص بالخطوات الرئيسية هو كما يلي: تحقق من الحصول على الصور في التنفس الحر بالتسلسل والإعدادات الصحيحة. بعد ذلك ، تحقق من أن النطاق الديناميكي للإشارات مناسب (~ 50 وحدة فلكية في حمة الرئة). إذا كانت البيانات الأولية لا تزال متوفرة ، كرر إعادة بناء الصور باستخدام عامل قياس مناسب لتجنب الحاجة إلى الحصول على بيانات جديدة. تأكد من أن التسجيل قد تم إجراؤه بدون قطع أثرية رئيسية وحركة متبقية. بعد ذلك ، تحقق مما إذا كانت عائد الاستثمار الصغير يظهر سلسلة زمنية مع تعديلات متوقعة متعلقة بالتهوية والتروية. بعد ذلك ، تحقق مما إذا كانت المرشحات المطبقة تغير الصور بالطريقة المتوقعة (على سبيل المثال ، لا توجد تعديلات عالية التردد في البيانات التي تمت تصفيتها منخفضة التردد). تحقق مما إذا كانت دورات الجهاز التنفسي والقلب المركبة فسيولوجية ولا تظهر قفزات مفاجئة. تحقق من دقة التجزئة. لاحظ أن البحث على مستوى دقة أدق قد يكون ضروريا بمجرد تحديد الخطوة الرئيسية التي تحدث خلالها المشكلة.
القيود
على الرغم من أنه من المعروف أن البروتوكول المقدم ينتج عنه نتائج قابلة للتكرار وحساسة ، إلا أن عدد الخطوات والمعلمات المعنية أثناء الاستحواذ والمعالجة اللاحقة تسمح بتحسين لا نهاية له تقريبا وتتشابك. لذلك ، يجب اتباع نهج من أسفل إلى أعلى من خلال معالجة تحسينات بروتوكول التسلسل أولا (على سبيل المثال ، فيما يتعلق ب SNR ونسبة التباين إلى الضوضاء الوظيفية). بالنسبة لتحسينات ما بعد المعالجة التالية ، قد تكون الحقيقة الأرضية المحددة مسبقا في شكل نموذج رئة رقمي مفيدة40. كما هو معروض ، يحاكي هذا النموذج اكتساب التنفس الحر ويتضمن عدة فئات لمحاكاة عيوب التهوية / التروية. بما في ذلك التشوه المعروف بسبب الحركة ، يمكن أيضا اختبار خوارزميات التسجيل مباشرة. على الرغم من هذه المزايا ، فإن كل نموذج محدود بطبيعته بدقة رسم خرائط الواقع المعقد إلى نموذج محدود ومبسط.
تم العثور على العتبات المقدمة في هذا البروتوكول لإظهار نتائج معقولة للمتطوعين الأصحاء وعبر مجموعات المرضى المختلفة من خلال التحليل التجريبي. ومع ذلك، وكما هو موضح من قبل، من المحتمل أن يكون التعديل مطلوبا اعتمادا على التسلسل وشدة المجال والمجموعة.
يتمثل أحد القيود العامة ل PREFUL في المعالجة اللاحقة الشاملة ، والتي لا تتوفر بسهولة كمنتج طبي حتى الآن ، على الرغم من أن الإصدارات الأولى قيد التنفيذ من Siemens Healthineers و BioVisioneers متاحة للأغراض العلمية في بيئة تعاون علمي / تجارية. تتضمن العمليات الحسابية عادة معالجة متوازية ، مما يطرح متطلبات عالية بشكل خاص على وحدة المعالجة المركزية وذاكرة الوصول العشوائي وقد يتطلب محطات عمل حديثة أو حلول خادم لمعالجة كميات كبيرة من البيانات بشكل فعال. علاوة على ذلك ، فإن خطوات المعالجة اللاحقة التي تستغرق وقتا طويلا تعيق حاليا العرض الفوري للنتائج ، وهو أمر مرغوب فيه لسير العمل السريري.
مقارنة بالطرق الأخرى
هناك العديد من الأساليب المماثلة مثل PREFUL ، بما في ذلك سلف Fourier Desolution ومشتقاته الأخرى مثل Matrix Pencil Desolution41 والنهج المختلف قليلا ذاتية البوابات غير المعززة بالرنين المغناطيسي الوظيفي للرئة (التصوير بالرنين المغناطيسي الحسي) 42. بينما يعمل تحلل فورييه والطرق المماثلة في مجال التردد ، يستخدم PREFUL تصفية فورييه أقل صرامة وحسابا لاحقا للاتساع في المجال الزمني. لذلك ، لا توجد حاجة لتحديد قمم محددة تتوافق مع التهوية / التروية. يمكن أن يؤدي هذا إلى تقليل القابلية لتقلبات التنفس ، والتي من المعروف أنها تحدث في البشر.
بينما تقوم PREFUL بفرز الصور ، تستخدم SENCEFUL فرز خطوط k-space ، مما يؤدي إلى مزيد من المرونة. ومع ذلك ، تتطلب SENCEFUL تسلسلات ذات قدرات بوابات ذاتية ، بينما يمكن إجراء PREFUL باستخدام تسلسل صدى التدرج التدرج التقليدي. وبالمثل ، فإن bSSFP المستخدم بشكل شائع في الأساليب القائمة على تحلل فورييه معروف بتحسين SNR وتباين تدفق الدم ولكنه يتطلب عادة مزيدا من التحسين لاكتساب الرئة خاصة في 3T43. ومع ذلك ، بخلاف ذلك ، لا يوجد سبب لعدم الجمع بين PREFUL والاستحواذ على bSSFP44.
تفترض كل هذه الأساليب القائمة على الإشارات أن بعض تأثيرات الإشارة غير المرغوب فيها ، بما في ذلك T1 و T2 / T2 * والانتشار والحركة عبر المستوى والفوكسلات غير المتعامدة ، لا تكاد تذكر. في حين أن التحقق المتقدم من PREFUL يشير بشكل غير مباشر إلى أن مثل هذه التأثيرات ليست حاسمة بالفعل ، أظهر Triphan et al. أن هناك اعتمادا على T1 و TE الفعالين ، وهو ما يفسره الترجيح المختلف للدم والمكونات المتني اعتمادا على TE45. في ضوء ذلك ، قد تشكل الميزة الأولية ل bSSFP لتصور الدم بسبب تباين T2 / T1 تحديا إضافيا لإنشاء تقدير كمي دقيق مقارنة بميكانيكا التباين الأبسط ل SPGRE. ومع ذلك ، فإن المزيد من الدراسات التي تتناول بشكل مباشر تأثير متغيرات MR المختلفة ، على سبيل المثال ، كما أجراها Glandorf et al. لوسائط التباين46،47 ، من المستحسن لأنها يمكن أن تحدد بشكل مباشر التأثير على PREFUL.
اهميه
نظرا لكونها طريقة خالية من وسائط التباين ، تشترك PREFUL في العديد من المزايا مع الطرق ذات الصلة المذكورة سابقا: 1) لا يوجد تطبيق للإشعاع المؤين وعامل التباين ، 2) لا توجد حاجة لأجهزة أو موظفين إضافيين ، 3) الاستحواذ ، والذي يعتمد فقط على الحد الأدنى من امتثال المريض. هذه المزايا تجعل PREFUL أداة مراقبة ملائمة ، خاصة للفئات الضعيفة مثل الأطفال المصابين بأمراض رئوية مزمنة. على الرغم من أن SNR منخفض مع تسلسل SPGRE ، فإن التوافر والافتقار إلى الحاجة إلى برمجة / تقاسم التسلسل الإضافي يعزز نشر هذا النهج.
كما تمت مناقشته في قسم المقدمة ، فإن عدد الدراسات التي تظهر التحقق الجيد ، وقابلية التكرار ، ونتائج الحساسية ، وقدرات المراقبة تظهر أن أهمية هذه التقنية والمعلمات الديناميكية المقابلة لها تسير في مسار تصاعدي وسيتم دعمها بشكل أكبر من خلال النشر الواسع.
Disclosures
فيليب كليميش وأندرياس فوسكريبنزيف وجينس فوغل كلاوسن هم مساهمون في شركة BioVisioneers GmbH ، وهي شركة لها مصلحة في طرق التصوير بالرنين المغناطيسي الرئوي.
Acknowledgements
تم تمويل هذا العمل من قبل المركز الألماني لأبحاث الرئة (DZL). يود المؤلفون أن يعربوا عن امتنانهم العميق للجميع الذين ساهموا ودعموا في مواصلة تطوير PREFUL ، ولا سيما: مارسيل جوتبيرليت ، تيل ف. كايريت ، ليا بيرندت ، جوليان غلاندورف ، سونيا لوديغر ، توفيق موهير السادي ، كاتارينا بونمان ، ماريوس ويرنز ، روبن مولر ، ماكسيميليان زوبكي ، جيسا بولر ، أجيلو كيرن ، كريستيان كريسوستو ، ميلان سبيث ، أرند أوبرت ، جوليان شيلر ، جيم وايلد ، إدوين فان بيك ، هيلين مارشال ، جينس جوتليب ، مارثا دوهنا ، ديان رينز ، آنا ماريا ديتريتش ، توبياس ويلت ، جينس هولفيلد ، باتريك زاردو ، جايلز سانتير ، فرانز وولفغانغ هيرش ، روبرت جريم ، باستيان بير ، باسم إسماعيل ، أندريه فيشر ، بيرتولد كيفر ، جريجور ثورمر وريبيكا رامب. علاوة على ذلك ، يود المؤلفون أيضا أن يشكروا مصوري الأشعة والمشاركين في الدراسة. على وجه الخصوص ، نشكر فرانك شرودر وسفين ثيل من قسم الأشعة (كلية الطب في هانوفر) على المساعدة الفنية المتميزة في إجراء فحوصات التصوير بالرنين المغناطيسي.
Materials
| Name | Company | Catalog Number | Comments |
| Advanced Normalization Tools (ANTs) | - | Image registration toolbox (https://stnava.github.io/ANTs/; https://github.com/fordanic/image-registration) | |
| Forsberg | - | Image registration toolbox | |
| MRI | Siemens Healthineers AG, Munich, Germany | 0.55T / 1.5T / 3T Scanner | |
| PREFUL App | BioVisioneers GmbH, Laatzen, Germany | PREFUL analysis, Figures and reports |
References
- Vogelmeier, C. F., et al. Global strategy for the diagnosis, management, and prevention of chronic obstructive lung disease 2017 Report: GOLD Executive Summary. Eur Respir J. 49 (3), 1700214 (2017).
- Ranu, H., Wilde, M., Madden, B. Pulmonary function tests. Ulster Med J. 80 (2), 84-90 (2011).
- Galbán, C. J., et al. Computed tomography-based biomarker provides unique signature for diagnosis of COPD phenotypes and disease progression. Nat Med. 18 (11), 1711-1715 (2012).
- Roach, P. J., Schembri, G. P., Bailey, D. L. V/Q Scanning using SPECT and SPECT/CT. J Nucl Med. 54 (9), 1588-1596 (2013).
- Wild, J. M., et al. MRI of the lung (1/3): methods. Insights Imaging. 3 (4), 345-353 (2012).
- Albert, M. S., et al. Biological magnetic resonance imaging using laser-polarized 129Xe. Nature. 370 (6486), 199-201 (1994).
- Berthezène, Y., et al. Contrast-enhanced MR imaging of the lung: assessments of ventilation and perfusion. Radiology. 183 (3), 667-672 (1992).
- Hughes, P. J. C., et al. Assessment of the influence of lung inflation state on the quantitative parameters derived from hyperpolarized gas lung ventilation MRI in healthy volunteers. J Appl Physiol. 126 (1), 183-192 (2019).
- Zapke, M., et al. Magnetic resonance lung function - a breakthrough for lung imaging and functional assessment? A phantom study and clinical trial. Respir Res. 7 (1), 106 (2006).
- Klimeš, F., et al. Free-breathing quantification of regional ventilation derived by phase-resolved functional lung (PREFUL) MRI. NMR Biomed. 32 (6), e4088 (2019).
- Deimling, M., Jellus, V., Geiger, B., Chefd'hotel, C. Time resolved lung ventilation imaging by Fourier decomposition. Proc. Intl. Soc. Mag. Reson. Med. 16, 2639 (2008).
- Bauman, G., et al. Non-contrast-enhanced perfusion and ventilation assessment of the human lung by means of fourier decomposition in proton MRI. Magn Reson Med. 62 (3), 656-664 (2009).
- Bauman, G., et al. Lung ventilation- and perfusion-weighted Fourier decomposition magnetic resonance imaging: In vivo validation with hyperpolarized 3He and dynamic contrast-enhanced MRI. Magn Reson Med. 69 (1), 229-237 (2013).
- Bauman, G., et al. Validation of Fourier decomposition MRI with dynamic contrast-enhanced MRI using visual and automated scoring of pulmonary perfusion in young cystic fibrosis patients. Eur J Radiol. 82 (12), 2371-2377 (2013).
- Sommer, G., et al. Non-contrast-enhanced preoperative assessment of lung perfusion in patients with non-small-cell lung cancer using Fourier decomposition magnetic resonance imaging. Eur J Radiol. 82 (12), e879-e887 (2013).
- Voskrebenzev, A., Gutberlet, M., Becker, L., Wacker, F., Vogel-Claussen, J. Reproducibility of fractional ventilation derived by Fourier decomposition after adjusting for tidal volume with and without an MRI compatible spirometer. Magn Reson Med. 76 (5), 1542-1550 (2016).
- Voskrebenzev, A., Gutberlet, M., Kaireit, T. F., Wacker, F., Vogel-Claussen, J. Low-pass imaging of dynamic acquisitions (LIDA) with a group-oriented registration (GOREG) for proton MR imaging of lung ventilation. Magn Reson Med. 78 (4), 1496-1505 (2017).
- Voskrebenzev, A., et al. Feasibility of quantitative regional ventilation and perfusion mapping with phase-resolved functional lung (PREFUL) MRI in healthy volunteers and COPD, CTEPH, and CF patients. Magn Reson Med. 79 (4), 2306-2314 (2018).
- Voskrebenzev, A., et al. Imaging-based spirometry in chronic obstructive pulmonary disease (COPD) patients using phase resolved functional lung imaging (PREFUL). Proc. Intl. Soc. Mag. Reson. Med. 26, 1079 (2018).
- Alsady, T. M., et al. MRI-derived regional flow-volume loop parameters detect early-stage chronic lung allograft dysfunction. J Magn Reson Imaging. 50 (6), 1873-1882 (2019).
- Pöhler, G. H., et al. Chronic thromboembolic pulmonary hypertension perioperative monitoring using phase-resolved functional lung (PREFUL)-MRI. J Magn Reson Imaging JMRI. 52 (2), 610-619 (2020).
- Behrendt, L., et al. Validation of automated perfusion-weighted phase-resolved functional lung (PREFUL)-MRI in patients with pulmonary diseases. J Magn Reson Imaging. 52 (1), 103-114 (2020).
- Kaireit, T. F., et al. Flow volume loop and regional ventilation assessment using phase-resolved functional lung (PREFUL) MRI: comparison with 129 xenon ventilation MRI and lung function testing. J Magn Reson Imaging JMRI. 53 (4), 1092-1105 (2021).
- Marshall, H., et al. 129Xe and free-breathing 1H ventilation MRI in patients with cystic fibrosis: a dual-center study. J Magn Reson Imaging. 57 (6), 1908-1921 (2023).
- Behrendt, L., et al. A dual center and dual vendor comparison study of automated perfusion-weighted phase-resolved functional lung magnetic resonance imaging with dynamic contrast-enhanced magnetic resonance imaging in patients with cystic fibrosis. Pulm Circ. 12 (2), e12054 (2022).
- Moher Alsady, T., et al. Multicenter standardization of phase-resolved functional lung MRI in patients with suspected chronic thromboembolic pulmonary hypertension. J Magn Reson Imaging. , (2023).
- Pöhler, G. H., et al. Repeatability of phase-resolved functional lung (PREFUL)-MRI ventilation and perfusion parameters in healthy subjects and COPD patients. J Magn Reson Imaging. 53 (3), 915-927 (2021).
- Voskrebenzev, A., et al. PREFUL MRI depicts dual bronchodilator changes in COPD: a retrospective analysis of a randomized controlled trial. Radiol Cardiothorac Imaging. 4 (2), e210147 (2022).
- Vogel-Claussen, J., et al. Phase-resolved functional lung (PREFUL) MRI-derived ventilation and perfusion parameters predict future lung transplant loss. Radiology. 307 (4), e221958 (2023).
- Zanette, B., et al. Clinical feasibility of structural and functional MRI in free-breathing neonates and infants. J Magn Reson Imaging. 55 (6), 1696-1707 (2022).
- Dyke, J. P., et al. Assessment of lung ventilation of premature infants with bronchopulmonary dysplasia at 1.5 Tesla using phase-resolved functional lung magnetic resonance imaging. Pediatr Radiol. 53 (6), 1076-1084 (2023).
- Glandorf, J., et al. Comparison of phase-resolved functional lung (PREFUL) MRI derived perfusion and ventilation parameters at 1.5T and 3T in healthy volunteers. PLOS ONE. 15 (12), e0244638 (2020).
- Lévy, S., et al. Free-breathing low-field MRI of the lungs detects functional alterations associated with persistent symptoms after COVID-19 infection. Invest Radiol. 57 (11), 742-751 (2022).
- Avants, B. B., et al. A reproducible evaluation of ANTs similarity metric performance in brain image registration. NeuroImage. 54 (3), 2033-2044 (2011).
- Forsberg, D., Andersson, M., Knutsson, H. Extending image registration using polynomial expansion to diffeomorphic deformations. SSBA Symposium on Image Analysis. , (2012).
- . fordanic/image-registration Available from: https://github.com/fordanic/image-registration (2022)
- Klimeš, F., et al. Evaluation of image registration algorithms for 3D phase-resolved functional lung ventilation magnetic resonance imaging in healthy volunteers and chronic obstructive pulmonary disease patients. NMR Biomed. 36 (3), e4860 (2023).
- He, K., Sun, J., Tang, X. Guided image filtering. IEEE Trans Pattern Anal Mach Intell. 35 (6), 1397-1409 (2013).
- Glandorf, J., et al. Perfusion quantification using voxel-wise proton density and median signal decay in PREFUL MRI. Magn Reson Med. 86 (3), 1482-1493 (2021).
- Voskrebenzev, A., Gutberlet, M., Klimeš, F., Wacker, F., Vogel-Claussen, J. Introduction of a Digital Lung Model for Validation and Refinement of Functional Lung Imaging Methods. Proc. Intl. Soc. Mag. Reson. Med. 31, 4820 (2023).
- Bauman, G., Bieri, O. Matrix pencil decomposition of time-resolved proton MRI for robust and improved assessment of pulmonary ventilation and perfusion. Magn Reson Med. 77 (1), 336-342 (2017).
- Fischer, A., et al. SElf-gated Non-Contrast-Enhanced FUnctional Lung imaging (SENCEFUL) using a quasi-random fast low-angle shot (FLASH) sequence and proton MRI. NMR Biomed. 27 (8), 907-917 (2014).
- Bauman, G., Pusterla, O., Bieri, O. Functional lung imaging with transient spoiled gradient echo. Magn Reson Med. 81 (3), 1915-1923 (2019).
- Rotärmel, A., et al. GRE bSSFP vs. FLASH based Fourier decomposition lung MRI at 1.5T: evaluation of image quality, fractional ventilation and lung perfusion in healthy volunteers. Prog Intl Soc Mag Reson. 26, 2-4 (2018).
- Triphan, S. M. F., et al. Echo time-dependent observed lung T1 in patients with chronic obstructive pulmonary disease in correlation with quantitative imaging and clinical indices. J Magn Reson Imaging. 54 (5), 1562-1571 (2021).
- Glandorf, J., et al. Effect of intravenously injected gadolinium-based contrast agents on functional lung parameters derived by PREFUL MRI. Magnetic Resonance in Medicine. 83 (3), 1045-1054 (2020).
- Glandorf, J., et al. Influence of gadolinium, field-strength and sequence type on quantified perfusion values in phase-resolved functional lung MRI. PloS One. 18 (8), e0288744 (2023).
Reprints and Permissions
Request permission to reuse the text or figures of this JoVE article
Request PermissionExplore More Articles
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. All rights reserved