Zum Anzeigen dieser Inhalte ist ein JoVE-Abonnement erforderlich. Melden Sie sich an oder starten Sie Ihre kostenlose Testversion.
Method Article
Extraktion von flüchtigen Sexualpheromonen und Chemoattraction-Assay bei Caenorhabditis elegans
In diesem Artikel
Zusammenfassung
Dieses Protokoll etabliert Methoden zur Extraktion und Quantifizierung von Reaktionen auf das flüchtige Sexualpheromon in C. elegans und stellt Werkzeuge zur Untersuchung der chemischen Kommunikation und Navigationsbahn zur Verfügung.
Zusammenfassung
Chemische Kommunikation ist für die Gesundheit, die Fortpflanzung und das allgemeine Wohlbefinden des Organismus von entscheidender Bedeutung. Das Verständnis der molekularen Signalwege, neuronalen Prozesse und Berechnungen, die diese Signale steuern, ist nach wie vor ein aktives Forschungsgebiet. Der Fadenwurm Caenorhabditis elegans bietet ein leistungsfähiges Modell für die Untersuchung dieser Prozesse, da er ein flüchtiges Sexualpheromon produziert. Dieses Pheromon wird von jungfräulichen Weibchen oder spermienarmen Hermaphroditen synthetisiert und dient als Lockstoff für Männchen.
Dieses Protokoll beschreibt eine detaillierte Methode zur Isolierung des flüchtigen Sexualpheromons aus mehreren C. elegans-Stämmen (WT-Stamm N2, daf-22 und fog-2) und C. remanei. Wir stellen auch ein Protokoll zur Quantifizierung der männlichen Chemotaxis-Reaktion auf das flüchtige Sexualpheromon zur Verfügung. Unsere Analyse verwendet Messungen wie den Chemotaxis-Index (C.I.), die Ankunftszeit (A.T.) und ein Trajektoriendiagramm, um die Reaktionen der Männchen unter verschiedenen Bedingungen genau zu vergleichen. Diese Methode ermöglicht robuste Vergleiche zwischen Männchen mit unterschiedlichem genetischen Hintergrund oder Entwicklungsstadien. Darüber hinaus ist der hier skizzierte Versuchsaufbau anpassbar, um andere Chemikalien der Chemoattraktion zu untersuchen.
Einleitung
Das Zusammenspiel zwischen chemischer Kommunikation und Fortpflanzungserfolg ist ein grundlegendes Prinzip im gesamten Tierreich 1,2,3,4,5,6,7,8,9,10. Sexualpheromone lösen eine Vielzahl von sexuell dimorphen Verhaltensweisen aus, die für die Suche nach Partnern, die Koordination der Schritte bei der Suche und Anziehung eines Partners und letztendlich die Förderung der Fortpflanzung einer Spezies unerlässlichsind 11,12,13,14,15,16,17 . Beim Verständnis der Pheromonsignalisierung wurden erhebliche Fortschritte erzielt, aber die molekularen Mechanismen, neuronalen Schaltkreise und Rechenprozesse, die diese Wechselwirkungen steuern, sind oft unvollständig definiert 18,19,20,21,22,23,24,25,26.
Der Fadenwurm Caenorhabditis elegans bietet ein leistungsfähiges Modell, um diese Fragen zu untersuchen. Bemerkenswert ist, dass C. elegans eine ungewöhnliche Fortpflanzungsstrategie aufweist - Hermaphroditen können sich selbst befruchten, aber auch mit Männchen auskreuzen 27,28,29,30,31,32,33. Diese Flexibilität erfordert ein robustes Kommunikationssystem, um den Fortpflanzungsstatus zu signalisieren. C. elegans ist bekannt für seine gut charakterisierten wasserlöslichen Pheromone, die Ascaroside, die eine vielfältige Rolle bei der Entwicklung, dem Verhalten und den sozialen Interaktionen spielen. Jüngste Entdeckungen haben eine eigene Klasse von flüchtigen Sexualpheromonen enthüllt, die von Nematoden verwendet werden. Diese Pheromone werden spezifisch von geschlechtsreifen C. elegans und C. remanei jungfräulichen Weibchen und spermienarmen Hermaphroditen produziert und dienen als Lockstoff für erwachsene Männchen 29,34,35. Dieser Lockstoff weist einen bemerkenswerten Sexualdimorphismus in seiner Herstellung und Wahrnehmung auf. Die weibliche somatische Gonade steuert die Synthese dieses flüchtigen Sexualpheromons, und die Produktion spiegelt dynamisch den Fortpflanzungsstatus wider, indem sie bei der Paarung aufhört und einige Stunden später wieder aufgenommen wird29,34.
Das Verständnis der Nematoden-Sexualpheromonkommunikation bietet Einblicke in die Evolution chemischer Kommunikationssysteme, das Zusammenspiel zwischen Fortpflanzungszustand und Verhalten sowie die Mechanismen, die der sexuell dimorphen neuronalen Verarbeitung zugrunde liegen 24,26,36,37,38,39. Studien deuten darauf hin, dass das amphidische Neuron AWA bei Männern entscheidend für die Pheromonerkennung ist, wobei der G-Protein-gekoppelte Rezeptor SRD-1 eine Schlüsselrolle bei der Pheromonerkennung bei Männern spielt24. C. elegans eignet sich gut für die Untersuchung der chemischen Kommunikation von Tieren, insbesondere der Sexualpheromonsignalisierung, da es bei der Partnersuche auf das olfaktorische System angewiesen ist. Während viel über die Ascarosid-Signalgebung bekannt ist, bietet das flüchtige Sexualpheromonsystem einzigartige Vergleichsmöglichkeiten 25,26,36,40,41,42,43,44,45,46,47,48,49,50,
51,52,53,54,55,56,57. Darüber hinaus ist C. elegans aufgrund seines vollständig sequenzierten Genoms, seiner klar definierten zellulären Abstammung und seiner gut charakterisierten Geruchsmutanten ein leistungsfähiger genetischer Modellorganismus.
Die vollständigen neuronalen Schaltkreise, die an der Verarbeitung dieses Pheromons beteiligt sind, die Berechnungen, die seine Wahrnehmung in gezieltes Partnersuchverhalten umsetzen, und seine Biosyntheseregulation müssen jedoch noch vollständig geklärt werden. Weitere Untersuchungen dieser Prozesse sind entscheidend für das Verständnis der vielfältigen Mechanismen, die die Kommunikation und das Fortpflanzungsverhalten von Tieren steuern. Die Identifizierung von Schlüsselgenen, die an der Synthese, Sekretion und Wahrnehmung von Pheromonen beteiligt sind, verspricht die Enthüllung neuer molekularer Akteure in der Tierkommunikation. Die hier beschriebenen Untersuchungsergebnisse bieten eine Grundlage, um diese Fragen zu beantworten.
Protokoll
1. Rohe Extraktion von Sexualpheromonen aus Weibchen und Hermaphroditen
- Protokoll für die Synchronisation von C. elegans
- Vorbereitung von adulten Weibchen oder Hermaphroditen
- Überwachen Sie die Kulturplatten täglich, bis eine große Population adulter Weibchen/Hermaphroditen vorhanden ist und die OP50-Nahrungsquelle erschöpft ist. Unter Verwendung von fog-2 C. elegans und WT C. remanei Weibchen für die Extraktion von rohem Sexualpheromon bereiten Sie synchronisierte Eier von den verpaarten Weibchen her.
HINWEIS: In diesem Protokoll werden C . elegans fog-2 mutierte XX-Tiere, die keine Selbstspermien produzieren, als weibliche C. elegans-Tiere bezeichnet.
- Überwachen Sie die Kulturplatten täglich, bis eine große Population adulter Weibchen/Hermaphroditen vorhanden ist und die OP50-Nahrungsquelle erschöpft ist. Unter Verwendung von fog-2 C. elegans und WT C. remanei Weibchen für die Extraktion von rohem Sexualpheromon bereiten Sie synchronisierte Eier von den verpaarten Weibchen her.
- Waschen und Pelletieren von Schnecken
- Waschen Sie adulte Würmer von einer gemischten Populationsplatte mit M9-Puffer ab. Sammeln Sie die Wurmsuspension in einem 1,5-ml-Mikrozentrifugenröhrchen. Zentrifugieren Sie bei 1.500 × g für 0,5-1 min, um die Würmer zu pelletieren.
HINWEIS: Vorreinigung bei starker Verschmutzung (optional): Lassen Sie die Würmer bei starker Verschmutzung im Rohr absetzen. Pipettieren Sie den Überstand heraus, um Bakterien zu entfernen, und wiederholen Sie den Vorgang, bis der Überstand klar ist.
- Waschen Sie adulte Würmer von einer gemischten Populationsplatte mit M9-Puffer ab. Sammeln Sie die Wurmsuspension in einem 1,5-ml-Mikrozentrifugenröhrchen. Zentrifugieren Sie bei 1.500 × g für 0,5-1 min, um die Würmer zu pelletieren.
- Bleiche
- Geben Sie 200 μl M9-Puffer zum Wurmpellet. Bereiten Sie den Lysepuffer vor, indem Sie Haushaltsbleiche und 1 M NaOH im Verhältnis 1:1 mischen. Geben Sie 500 μl dieses Lysepuffers in die Mischung, wirbeln Sie 10 s lang vor und machen Sie dann eine Pause, um den Lysezustand unter einem Präpariermikroskop zu überwachen. Wiederholen Sie diesen Vorgang von 10 s Wirbeln, gefolgt von einer Beobachtung, bis die adulten Würmer vollständig lysiert sind.
- Stoppen des Bleichens und Pelletierens der Embryonen
- Wenn adulte Würmer in kleine Fragmente lysiert (aber nicht vollständig aufgelöst) werden, fügen Sie sofort 500 μl M9-Puffer hinzu, um die Reaktion zu verlangsamen. Zentrifugieren Sie bei 15.000 × g für 30-60 s, um die Embryonen zu pelletieren.
HINWEIS: Eine Überlyse kann die Embryonen schädigen. Stoppen Sie die Reaktion, wenn die erwachsenen Wurmkörper in kleine Fragmente zerfallen sind. Die Lyse wird während der Zentrifugen- und Waschschritte fortgesetzt, bis der gesamte Lysepuffer entfernt ist.
- Wenn adulte Würmer in kleine Fragmente lysiert (aber nicht vollständig aufgelöst) werden, fügen Sie sofort 500 μl M9-Puffer hinzu, um die Reaktion zu verlangsamen. Zentrifugieren Sie bei 15.000 × g für 30-60 s, um die Embryonen zu pelletieren.
- Waschen Sie die Embryonen 5x mit 1 mL M9-Puffer und zentrifugieren Sie sie nach jedem Waschen 30-60 s lang bei 15.000 × g . Entfernen Sie den Überstand nach der Zentrifugation.
- Synchronisation
- Resuspendieren Sie die Embryonen in 800 μl M9-Puffer in einem 1,5-ml-Mikrozentrifugenröhrchen. Drehen Sie das Röhrchen 12-15 Stunden lang bei 20 °C, um das Schlüpfen von L1 und den Wurmstopp im L1-Stadium aufgrund fehlender Nahrungszufuhr zu gewährleisten. Lassen Sie die Würmer frei und kultivieren Sie sie 3 Tage lang bei 20° C, bis sie das L4-Stadium erreichen.
- Vorbereitung von adulten Weibchen oder Hermaphroditen
2. Rohe Extraktion von Sexualpheromonen aus einem Tag alten jungfräulichen Weibchen (Abbildung 1A)
HINWEIS: Wir wenden ein zuvor etabliertes Protokoll24 an, um Sexualpheromone aus einem Tag alten jungfräulichen Fog-2 (Feminisierung der Keimbahn) mutierten Weibchen von C. elegans und WT-Weibchen von C. remanei zu extrahieren.
- Vorbereitung adulter Weibchen
- Selektieren und isolieren Sie ca. 200 Weibchen im L4-Stadium fog-2 1 Tag vor der Pheromonextraktion. Um sicherzustellen, dass nur jungfräuliche Weibchen gesammelt werden, trennen Sie diese L4 fog-2 Weibchen vorsichtig nach Geschlecht und verteilen Sie sie auf drei separate 6 cm OP50 NGM-Platten. Geben Sie eine kleine Menge OP50-Bakterien in die Mitte jeder Platte.
HINWEIS: Verteilen Sie 200 weibliche L4-Würmer auf drei separate Platten, um das Risiko zu vermeiden, versehentlich einen männlichen Wurm auf die Platte zu bringen. Wenn ein Männchen gepflückt wird, paart es sich wahrscheinlich mit vielen Weibchen, was dazu führt, dass die meisten Weibchen am nächsten Tag, wenn sie erwachsen werden, befruchtet sind. Befruchtete Weibchen geben keine flüchtigen Sexualpheromone ab, bis die Spermien erschöpft sind, was sich auf die Extraktionsergebnisse auswirkt. Die begrenzte Nahrungsquelle beschränkt die Hermaphroditen auf einen kleineren Bereich in der Mitte des Tellers, wodurch die Wahrscheinlichkeit, dass sie während der Isolationszeit aus dem Teller entkommen, minimiert wird.
- Selektieren und isolieren Sie ca. 200 Weibchen im L4-Stadium fog-2 1 Tag vor der Pheromonextraktion. Um sicherzustellen, dass nur jungfräuliche Weibchen gesammelt werden, trennen Sie diese L4 fog-2 Weibchen vorsichtig nach Geschlecht und verteilen Sie sie auf drei separate 6 cm OP50 NGM-Platten. Geben Sie eine kleine Menge OP50-Bakterien in die Mitte jeder Platte.
- Extraktionsprozess
- Am Tag der Extraktion (Tag 1 der Fortpflanzungsreife, 3 Tage nach der Freisetzung der Würmer aus dem L1-Arrest) werden 100 jungfräuliche, 1 Tag alte Fog-2-Weibchen entnommen und in ein Mikrozentrifugenröhrchen mit 1 ml M9-Puffer isoliert. Waschen Sie die Weibchen 5x mit M9-Puffer, um die bakterielle Kontamination zu minimieren, und inkubieren Sie sie 6 Stunden lang bei 20 °C in 100 μl M9-Puffer, um die Pheromonproduktion und -akkumulation im Medium zu ermöglichen.
- Führen Sie einen ähnlichen Extraktionsprozess für C . remanei-Weibchen durch, indem Sie nur 15-20 Weibchen im L4-Stadium verwenden, die am Tag vor der Extraktion auf drei Platten isoliert wurden, und inkubieren Sie am nächsten Tag fünf jungfräuliche Weibchen in 100 μl M9-Puffer für 6 Stunden bei 25 °C (optimale Wachstumstemperatur für C. remanei)58.
HINWEIS: C . remanei-Weibchen produzieren im Vergleich zu C . elegans-Weibchen eine höhere Menge an flüchtigen Sexualpheromonen. Daher reichen nur fünf Weibchen aus, um 100 μl rohes flüchtiges Sexualpheromon zu extrahieren.
- Lagerung
- Zentrifugieren Sie die Proben bei 15.000 × g für 30-60 s, um die Würmer zu pelletieren. Übertragen Sie den Überstand (mit den Pheromonen) vorsichtig in ein sauberes Röhrchen und entsorgen Sie das Röhrchen mit dem Wurmpellet. Lagern Sie den isolierten Überstand für nachfolgende Chemoattraktions-Assays.
HINWEIS: Der rohe flüchtige Sexualpheromonextrakt kann mindestens 1 Jahr bei -80 °C in einem Mikrozentrifugenröhrchen gelagert werden, das mit Parafilm umwickelt ist, um die Verdunstung zu minimieren.
- Zentrifugieren Sie die Proben bei 15.000 × g für 30-60 s, um die Würmer zu pelletieren. Übertragen Sie den Überstand (mit den Pheromonen) vorsichtig in ein sauberes Röhrchen und entsorgen Sie das Röhrchen mit dem Wurmpellet. Lagern Sie den isolierten Überstand für nachfolgende Chemoattraktions-Assays.
- Qualitätskontrolle
- Vor der Verwendung des Extrakts ist eine Qualitätskontrolle mit N2-Männern oder Him-5-Männern durchzuführen, um seine Chemoattraktivität zu überprüfen (siehe Abschnitt 4).
3. Eine große Menge roher Sexualpheromonextraktion aus 6 Tage alten jungfräulichen Hermaphroditen (Abbildung 1A)
- Wurm-Kultur
- Um etwa 20 ml rohes C. elegans-Sexualpheromon zu erhalten, synchronisieren Sie zwanzig 10 cm große NGM-Platten mit gesunden adulten C. elegans-Würmern (entweder N2- oder daf-22-Mutante) unter Verwendung des oben genannten Bleichprotokolls und waschen Sie sie dann 5x mit M9-Puffer.
HINWEIS: Dieser Prozess bereitet genügend Embryonen für die Pheromonextraktion vor. N2: Der Standardstamm von WT C. elegans , der sowohl wasserlösliche Ascarosid-Pheromone als auch nicht-Ascarosid-flüchtige Sexualpheromone produziert. DAF-22-Mutante : Eine Mutante, der die Fähigkeit fehlt, viele Ascarosid-Pheromone zu produzieren, was sie bei der isolierten Untersuchung von nicht-Ascarosiden flüchtigen Sexualpheromonen hilfreich macht. - Um Würmer im L1-Stadium zu synchronisieren, drehen Sie die Embryonen im M9-Puffer für 12-15 Stunden, um die Entwicklung zu stoppen. Übertragen Sie die festgehaltenen L1-Würmer auf 10 cm große NGM-Kulturplatten, die mit OP50-Bakterien besiedelt sind, um Wachstum und Entwicklung zu ermöglichen.
- Um das Vorhandensein von Männchen auf hermaphroditischen Platten zu minimieren, überprüfen Sie die Platten 2 Tage nach der Wurmfreisetzung im L4-Stadium und entfernen Sie alle beobachteten Männchen (sehr selten).
- Achten Sie nach drei Tagen der Entwicklung auf das Aussehen von Embryonen, die darauf hinweisen, dass die Würmer zu fortpflanzungsreifen Erwachsenen geworden sind.
HINWEIS:Fog-2-mutierte Weibchen von C. elegans und WT-Weibchen von C. remanei sind für die Extraktion von flüchtigem Sexualpheromon in großen Mengen ungeeignet. Die fog-2-mutierten C. elegans und C. remanei haben einen hohen Anteil an Männchen in ihren Populationen, und Männchen paaren sich kontinuierlich mit Weibchen. Befruchtete Weibchen produzieren keine flüchtigen Sexualpheromone. Die Anwesenheit von Männern erschwert die Extraktion dieser Verbindungen.
- Um etwa 20 ml rohes C. elegans-Sexualpheromon zu erhalten, synchronisieren Sie zwanzig 10 cm große NGM-Platten mit gesunden adulten C. elegans-Würmern (entweder N2- oder daf-22-Mutante) unter Verwendung des oben genannten Bleichprotokolls und waschen Sie sie dann 5x mit M9-Puffer.
- Wurmwäsche und Embryonentrennung
- Waschen Sie die Embryonen wiederholt mit M9-Puffer und lassen Sie sie sich absetzen (1 g Sedimentation), bis sich die meisten Erwachsenen am Boden des Röhrchens befinden. 5-7x wiederholen. Lassen Sie die Mikrozentrifugenröhrchen einige Minuten lang ungestört in einem Gestell absetzen, um die Sedimentation der adulten Würmer zu erleichtern und die Trennung der adulten Wurmpopulation von den Embryonen zu ermöglichen, die im Überstand schweben.
- Pipettieren Sie die getrennten adulten Tiere und überführen Sie sie auf neue, mit OP50-Samen angereicherte NGM-Platten.
- Wiederholen Sie diesen Waschvorgang für 5-6 Tage, um die Selbstspermien zu erschöpfen.
HINWEIS: Verwenden Sie für die Extraktion flüchtiger Sexualpheromone Hermaphroditen, die 5-6 Tage alt sind. Dieser Zeitpunkt stellt sicher, dass ihre Selbstspermien wahrscheinlich erschöpft sind, da Hermaphroditen mit verfügbaren Selbstspermien keine flüchtigen Sexualpheromone produzieren. Zahlreiche tote oder noch nicht geschlüpfte Embryonen auf der Platte am 5. oder 6. Tag deuten auf einen geeigneten Zeitpunkt für den Beginn der Pheromonextraktion hin.
- Extraktion von Sexualpheromonen
- Extrahieren Sie das Sexualpheromon, wie in Abschnitt 1 beschrieben, mit Modifikationen.
- Anstatt 100 weibliche C. elegans pro 100 μl hinzuzufügen, fügen Sie M9-Puffer hinzu, der auf dem endgültigen Volumen des Wurmpellets basiert. Fügen Sie 1 ml M9-Puffer pro 50 μl gepackter Würmer hinzu.
- Qualitätskontrolle und Homogenisierung
- Qualitätskontrolle von Testchargen von extrahiertem Pheromon unter Verwendung des Chemoattraktionsassays mit N2-Männchen oder Him-5-Männchen (siehe Abschnitt 4).
- Mischen Sie alle Chargen, um ein homogenes, rohes, flüchtiges Sexualpheromon für Experimente zu erhalten, die eine große Menge an Pheromon benötigen, wie z. B. Screening- oder mikrofluidische Experimente. Lagern Sie den rohen Sexualpheromonextrakt mindestens 1 Jahr bei -80 °C in 50-ml-Röhrchen, die mit Parafilm umwickelt sind, um die Verdunstung zu minimieren.
- Chemoattraction-Assay-basierte Titrationsmethode zur Standardisierung von rohem Sexualpheromonextrakt
- Führen Sie einen Titrationsassay durch, indem Sie serielle Verdünnungen jedes Pheromonextrakts sowohl an WT N2 als auch an him-5 männlichen C. elegans testen. Bestimmen Sie die höchste Verdünnung (niedrigste Konzentration), die bei Kontrollstämmen konsistent eine robuste und reproduzierbare Chemotaxisreaktion hervorruft.
- Bereiten Sie eine Reihe von Verdünnungen aus jedem Rohextrakt (z. B. 1:2, 1:4, 1:8 usw.) in M9-Puffer vor.
- Chemotaxis-Assays
- Standardisierte Chemotaxis-Assays (siehe Abschnitt 4) mit jeder Verdünnung am Referenzstamm der Männchen durchführen. Führen Sie drei Replikate durch, um die Reproduzierbarkeit zu gewährleisten. Vergleichen Sie die optimalen Verdünnungen über verschiedene Extraktionschargen hinweg, um die Konsistenz der Pheromonkonzentration zu beurteilen.
HINWEIS: Dies legt einen Referenzpunkt für die Bewertung der Bioaktivität jedes Extrakts fest. Im Standard-Chemoattraktionstest für Sexualpheromonen werden die ursprünglichen unverdünnten Extrakte für nachfolgende Experimente verwendet, wobei die Titration als Qualitätskontrollschritt dient, um eine konsistente Pheromonaktivität zwischen den Chargen zu gewährleisten. Die Verdünnungsreihe kann je nach experimentellem Bedarf angepasst werden. Angesichts der Tatsache, dass das Standardextraktionsprotokoll durchweg gesättigte Rohpheromonextrakte liefert, ist ein Titrationstest zur Standardisierung des Extrakts für die meisten Experimente möglicherweise nicht erforderlich. Es wird empfohlen, die gleiche Charge rohen Sexualpheromons in einer Reihe verwandter Experimente zu verwenden, um die Konsistenz zu erhalten und die Variabilität der Pheromonaktivität zu minimieren.
- Standardisierte Chemotaxis-Assays (siehe Abschnitt 4) mit jeder Verdünnung am Referenzstamm der Männchen durchführen. Führen Sie drei Replikate durch, um die Reproduzierbarkeit zu gewährleisten. Vergleichen Sie die optimalen Verdünnungen über verschiedene Extraktionschargen hinweg, um die Konsistenz der Pheromonkonzentration zu beurteilen.
4. Flüchtiger Sexualpheromon-Chemoattraktions-Assay
HINWEIS: Der flüchtige Sexualpheromon-Chemoattraction-Assay wurde von zuvor etablierten Methoden adaptiert, die in anderen Chemoattraction-Studien verwendet wurden 24,29,59,60,61. Diese Modifikationen wurden implementiert, um die Sensitivität und Spezifität des Assays für den Nachweis von Reaktionen auf flüchtige Sexualpheromone zu optimieren. Dieser maßgeschneiderte Ansatz verbessert die Anwendbarkeit des Assays für spezifische Forschungsanforderungen.
- Beobachten Sie die Kulturplatten täglich, bis adulte Weibchen/Hermaphroditen reichlich vorhanden sind. Die Gesundheit der Würmer beeinflusst ihre Reaktion auf das Sexualpheromon.
- Vorbereitung von ihm-5 Rüden
- Verwenden Sie das Standard-Bleichprotokoll, um him-5 Würmer zu synchronisieren. Waschen Sie die Würmer nach der Synchronisation 5x mit M9-Puffer. Isolierung von L4-Männchen am Tag vor dem Assay; Übertragen Sie dann einen Tag alte adulte männliche Würmer aus ihren ausgesäten Platten und spülen Sie sie vor dem Assay in M9-Puffer ab. Legen Sie sie vor dem Assay auf unbesäte NGM-Platten, um Bakterienreste zu beseitigen und Interferenzen durch Lebensmittel während des Assays zu verhindern.
HINWEIS: Lassen Sie die Würmer nicht länger als eine Stunde vor dem Assay hungern, da dies ihren inneren Zustand verändern und die Ergebnisse des Sexualpheromon-Chemoattraction-Assays beeinflussen kann. Wenn Sie also beabsichtigen, mehr als 10 Assays an einem einzigen Tag durchzuführen, tauschen Sie die Wurmproben stündlich aus. Wechseln Sie außerdem wiederholt zwischen einem experimentellen Assay und einem Kontrollassay.
- Verwenden Sie das Standard-Bleichprotokoll, um him-5 Würmer zu synchronisieren. Waschen Sie die Würmer nach der Synchronisation 5x mit M9-Puffer. Isolierung von L4-Männchen am Tag vor dem Assay; Übertragen Sie dann einen Tag alte adulte männliche Würmer aus ihren ausgesäten Platten und spülen Sie sie vor dem Assay in M9-Puffer ab. Legen Sie sie vor dem Assay auf unbesäte NGM-Platten, um Bakterienreste zu beseitigen und Interferenzen durch Lebensmittel während des Assays zu verhindern.
- Vorbereitung von Chemoattraction-Agar-Assay-Platten
- Bereiten Sie Chemoattraktions-Assayplatten mit 1,5 % Agar, 25 mM NaCl, 1,5 mM Tris-Base und 3,5 mM Tris-Cl vor, wie in der einschlägigen Literaturbeschrieben 24.
- Erhitzen Sie den Agar in der Chemoattraktionslösung mit einer Mikrowelle, bis er sich vollständig aufgelöst hat. Lassen Sie die Lösung 5 min bei Raumtemperatur abkühlen.
- Verwenden Sie eine Pipettenhilfe, um die Chemoattraction-Agar-Lösung gleichmäßig in den Petrischalen zu verteilen: Gießen Sie 30 mL in jede 10-cm-Schale und 20 mL in jede 6-cm-Schale.
- Nachdem Sie die Chemoattraction-Agar-Lösung in die Petrischalen gegossen haben, lassen Sie die Deckel an einem sauberen Ort mindestens 40 Minuten lang offen, damit die Oberfläche des Agars etwas trocknen kann. Sobald die Oberfläche richtig getrocknet ist, schließen Sie die Deckel.
HINWEIS: Diese Trocknungszeit kann je nach Luftfeuchtigkeit und Temperatur der Laborumgebung variieren.
- Plattenlagerung und Vorbereitung vor dem Assay
- Verpacken Sie die vorbereiteten Assay-Platten und lagern Sie sie bis zu 1 Woche in einem Kühlraum. Nehmen Sie die Platten vor dem Gebrauch aus dem Kühlhaus und lassen Sie sie über eine Stunde lang auf Raumtemperatur akklimatisieren. Öffnen Sie die Deckel, um die Restfeuchtigkeit 20 Minuten vor dem Assay an einem sauberen Ort aus dem Agar verdunsten zu lassen, und stellen Sie sicher, dass sich vor dem Assay kein offensichtliches Wasser auf der Oberfläche befindet.
- Versuchsdesign und Chemoattraction-Assay
- Um den Chemoattraktions-Assay durchzuführen, markieren Sie drei verschiedene Flecken auf dem Deckel und der Unterseite der Petrischale oder verwenden Sie eine auf transparentes Plastikpapier gedruckte Schablone, die unter die Schale gelegt oder am Präpariermikroskop befestigt wird. Zu diesen Markierungen gehören ein mittlerer Punkt (•) als Ausgangspunkt für die Würmer, ein Pluszeichen (+) für den experimentellen Spot (2 μl Sexualpheromon auf dem Deckel und 2 μl 1 M Natriumazid auf der Platte) und ein Minuszeichen (-) für den Kontrollspot (2 μl M9-Puffer auf dem Deckel und 2 μl 1 M Natriumazid) (Abbildung 2A). Passen Sie den Abstand zwischen diesen Markierungen entsprechend der Schalengröße und den spezifischen experimentellen Anforderungen an. In der Regel wird für 6 cm große Petrischalen ein fester Abstand von 1,5 cm vom Startpunkt zu jeder Testsubstanz für die Positivkontrolltests festgelegt.
- Detaillierte Schritte zur Durchführung des Assays (Abbildung 2)
- Tragen Sie 2 μl 1 M Natriumazid auf jeden Versuchs- und Kontrollpunkt auf der Platte auf.
- Pflücke 20 gesunde und frei bewegliche männliche Würmer mit einem Wurmsammler. Setzen Sie gleichzeitig 20 männliche Würmer am Startpunkt unter einem Präpariermikroskop frei.
- Geben Sie schnell 2 μl Sexualpheromon und 2 μl M9-Puffer auf die Versuchs- bzw. Kontrollpunkte auf dem Deckel.
- Schließen Sie vorsichtig den Deckel und platzieren Sie die Assay-Platte an einem ruhigen, temperaturstabilen Ort neben dem Mikroskop.
- Nach 30 Minuten bewerten Sie den Assay, indem Sie die Anzahl der Würmer an jeder Stelle zählen.
HINWEIS: Das Pflücken von 20 Würmern sollte 1-2 Minuten nicht überschreiten, um zu verhindern, dass die früh gepflückten Würmer austrocknen und ungesund werden, was die Ergebnisse beeinträchtigen könnte. Der gesamte Vorgang von der Ernte der Männchen bis zum Schließen des Deckels sollte zwischen 2 und 5 Minuten dauern.
- Positivkontroll-Screening
- Testen Sie die männlichen Würmer mit einer 1.000-fach verdünnten Diacetyllösung (gelöst in 10 % Ethanol und 90 % M9-Puffer), um ihre Reaktionsfähigkeit auf die Chemotaxis zu bestätigen. Bewerten Sie die Ergebnisse des Chemoattraction-Assays 30 Minuten nach Beginn des Tests. Bewerten Sie Würmer, die an den angegebenen Stellen gelähmt sind, basierend auf ihrer Position: "C" für diejenigen auf dem Kontrollpunkt und "E" für diejenigen auf dem Versuchspunkt. Bewerten Sie die Würmer an keiner Stelle mit "N" (Abbildung 2C).
- Um den Chemoattraction Index (C.I.) zu berechnen, verwenden Sie die folgende Formel:
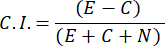
- Es werden nur männliche Proben mit einem Chemotaxis-Index ≥ 0,4 (CI, siehe Abbildung 2C) ausgewählt. Verwenden Sie das Männchen aus der gleichen Charge für den anschließenden Sexualpheromontest.
HINWEIS: Es werden drei separate Assays mit jeweils 20 Würmern durchgeführt, um die Konsistenz und Zuverlässigkeit der Versuchsergebnisse zu gewährleisten. Drei Assays sind in der Regel ausreichend, um auf Konsistenz zu schließen.
5. Richtlinien für den Zeitplan und die Bewertung des Chemoattraktions-Assays
- Bewerten Sie die Chemoattraktionsreaktion der Würmer anhand ihrer endgültigen Positionen. Bewerten Sie die Anzahl der Würmer an jeder Stelle am Ende des Assays, normalerweise 30 Minuten nach dessen Beginn.
HINWEIS: Die Verwendung von Natriumazid an Versuchs- und Kontrollpunkten lähmt ankommende Würmer und erleichtert so eine genaue Bewertung. Die meisten WT N2 und him-5 Männchen sind in der Lage, die Pheromonquelle innerhalb von 6-8 min in einer 6 cm Platte mit einem Abstand von 1,5 cm zu lokalisieren. - Um Defekte in der Chemotaxis-Effizienz zu erfassen, insbesondere um subtile Defekte zu erkennen, sollten Sie den Assay in regelmäßigen Abständen von 3-5 Minuten überwachen.
HINWEIS: Diese häufige Beobachtung ermöglicht die Dokumentation der Zeitpunkte, zu denen die Würmer an den Teststellen eintreffen. Eine solche detaillierte Nachverfolgung kann Fälle aufdecken, in denen Würmer eine verminderte Chemotaxis-Effizienz aufweisen und es dennoch schaffen, den Testpunkt innerhalb des Untersuchungsfensters zu erreichen.
6. Optionale Modifikationen
- Für eine verbesserte Beurteilung der Chemotaxis verwenden Sie eine Kamera, die über der Platte positioniert ist, um die Trajektorien der Würmer während des gesamten Assays aufzuzeichnen.
HINWEIS: Diese Modifikation ermöglicht eine umfassende Analyse ihrer Bewegungsmuster und bietet einen tieferen Einblick in das Verhalten und die Trajektorie der Chemoattraktion (Abbildung 3).
7. Datenanalyse
- Bewertung und Berechnung des Chemoattraction Index (C.I.)
- Führen Sie die Schritte 4.7.1 und 4.7.2 aus.
- Diagramm der Ankunftszeit
- Für eine umfassendere Analyse von Chemoattraktions-Assays sollten Sie den Assay in Abständen von 3-5 Minuten überwachen oder eine Kamera über der Platte einsetzen, um die Flugbahnen der Würmer während des gesamten Assays aufzuzeichnen.
HINWEIS: Diese Ansätze ermöglichen es nicht nur, die Ankunftszeiten der Würmer an den Design-Spots zu bewerten, sondern auch die durchschnittlichen Ankunftszeiten zu vergleichen und die Verteilung dieser Zeiten zu analysieren.
- Für eine umfassendere Analyse von Chemoattraktions-Assays sollten Sie den Assay in Abständen von 3-5 Minuten überwachen oder eine Kamera über der Platte einsetzen, um die Flugbahnen der Würmer während des gesamten Assays aufzuzeichnen.
- Videobasierte Trajektorienanalyse und Datenvisualisierung
HINWEIS: Um die Bewegungsmuster von C. elegans Aufzeichnen und Extrahieren von Trajektorien während der Chemoattraction-Assays (siehe Tabelle der Materialien) und weitere Analysen (Abbildung 3).- Richten Sie das Aufzeichnungssystem ein.
- Starten Sie eine neue Aufnahme und greifen Sie auf das Fenster mit den Aufnahmeeinstellungen zu.
- Definieren Sie die gewünschten Aufnahmeparameter:
- Dateipräfix: Wählen Sie einen aussagekräftigen Namen für die Videodateien (z. B. "experiment1_").
- Bildrate (FPS): Wählen Sie die entsprechenden Bilder pro Sekunde aus, um die Bewegung des Wurms einzufangen (z. B. 7,5 FPS für Würmer auf der Agarplatte und 30 FPS für schwimmende Würmer).
- Dauer: Legen Sie die Länge der Aufzeichnung in Sekunden fest (z. B. 1.800 s [30 min] für einen Bulk-Chemoattraction-Assay).
- Optimieren Sie die Bildqualität: Passen Sie die Beleuchtungsintensität an, um sicherzustellen, dass die Würmer deutlich vor dem Hintergrund sichtbar sind, und stimmen Sie den Fokus feinab, um ein scharfes Bild der Würmer zu erhalten.
- Um die Assay-Platte vorzubereiten, geben Sie zunächst die Kontrolllösung auf die dafür vorgesehene Kontrollstelle. Nimm dann vorsichtig den/die Wurm(e) auf und lass sie vorsichtig in die Mitte der Platte fallen. Sobald sich der/die Wurm(e) eingenistet haben, tragen Sie die Sexualpheromonlösung auf die dafür vorgesehene Versuchsstelle auf.
- Platte positionieren: Platzieren Sie die Platte mit den Würmern vorsichtig in der Mitte des Aufnahmefelds, um den Aufnahmebereich zu maximieren.
- Um die Belastung der Würmer während der Chemotaxis-Assays zu reduzieren, sollten Sie die folgenden zwei Ansätze in Betracht ziehen.
- Legen Sie den Wurm für den Einzelwurm-Assay auf die Testplatte und lassen Sie ihn 5 Minuten lang akklimatisieren, bevor Sie die Sexualpheromonlösung in dem angegebenen Abstand (die Position basierend auf der aktuellen Position des Wurms) einführen.
HINWEIS: Dies minimiert die Handhabung und gibt dem Wurm Zeit, sich an seine neue Umgebung anzupassen. - Bulk Chemoattraction Assay: Lassen Sie die Würmer sich 5 Minuten lang auf der Platte absetzen und dispergieren. Nach dieser Eingewöhnungsphase führen Sie die Pheromonlösung an der vorgesehenen festen Position ein. Messen Sie während der Post-Video-Analyse den Startabstand jedes Wurms vom Pheromon und gruppieren Sie sie entsprechend für die weitere Analyse.
- Legen Sie den Wurm für den Einzelwurm-Assay auf die Testplatte und lassen Sie ihn 5 Minuten lang akklimatisieren, bevor Sie die Sexualpheromonlösung in dem angegebenen Abstand (die Position basierend auf der aktuellen Position des Wurms) einführen.
- Ablauf der Videoanalyse
- Import und Einrichtung: Importieren Sie das aufgenommene Video in die Software. Konfigurieren Sie die Sequenzinformationen (z. B. Bildrate); Geben Sie den Abbildungsmaßstab an (Pixel pro Maßeinheit).
- Bildanpassung: Um die Wurmerkennung zu optimieren, passen Sie den Erkennungsschwellenwert an, bis das grüne Etikett die Würmer eng umrandet, ohne Hintergrundgeräusche oder Artefakte zu erfassen. Wenden Sie außerdem Algorithmen zur Hintergrundglättung an, um Rauschen und Unebenheiten im Bild zu reduzieren und den Kontrast zwischen den Würmern und dem Hintergrund zu verbessern. Experimentieren Sie mit verschiedenen Glättungsstufen, um die optimale Balance zwischen Rauschunterdrückung und Beibehaltung von Wurmdetails zu finden.
HINWEIS: Der ideale Schwellenwert sollte den größten Teil des Körpers jedes Wurms abdecken und Fremdelemente ausschließen. - Optimierung der Erkennungsparameter: Wählen Sie einen repräsentativen Wurm aus, um die Erkennungsparameter automatisch zu generieren. Überprüfen Sie die Erkennungsgenauigkeit durch visuelle Inspektion von 5-10 zufälligen Frames. Wenn die Erkennung nicht zufriedenstellend ist, verfeinern Sie die Erkennungsparameter manuell, überprüfen Sie bei Bedarf die Bildanpassungseinstellungen und fahren Sie mit der Verfolgung fort, sobald die Erkennung zuverlässig ist.
- Korrekturlesen und Reparieren von Tracking-Trajektorien: Nachdem der automatisierte Tracking-Prozess abgeschlossen ist, führen Sie ein manuelles Korrekturlesen der generierten Trajektorien durch. Wenn beim Korrekturlesen Inkonsistenzen festgestellt werden, verwenden Sie die Reparaturfunktion, um die Trajektorie zu korrigieren, und führen Sie die folgenden Vorgänge aus: Verbinden: Verbinden Sie Trajektoriensegmente, denen fälschlicherweise unterschiedliche Identifikatoren zugewiesen wurden, die aber zur gleichen Person gehören. Teilen: Separate Trajektoriensegmente, denen fälschlicherweise dieselbe Kennung zugewiesen wurde, die aber zu unterschiedlichen Personen gehören.
HINWEIS: Ziel ist es, sicherzustellen, dass jede eindeutige Kennung (Nummer) während des gesamten Tracking-Zeitraums konsistent derselben Person zugewiesen wird.
Beispiel: Wenn ein Wurm für einen Zeitraum als "3" gekennzeichnet ist und dann für einen nachfolgenden Zeitraum fälschlicherweise als "7" gekennzeichnet ist, würde die Reparaturfunktion diese beiden Segmente unter dem Bezeichner "3" verbinden. Umgekehrt, wenn zwei Würmer beide für einen Zeitraum als "12" gekennzeichnet sind, würde die Reparaturfunktion dieses Segment in zwei separate Trajektorien aufteilen, die jeweils mit einer eindeutigen Kennung versehen sind. Durch sorgfältiges Korrekturlesen und Durchführen notwendiger Reparaturen kann die Genauigkeit und Zuverlässigkeit der Tracking-Daten erheblich verbessert werden. - Ergebnisvisualisierung und -export: Nutzen Sie Software für die Visualisierung und grundlegende Analyse. Exportieren Sie Daten als CSV-Dateien zur weiteren Analyse mit den bevorzugten Tools oder dem bevorzugten Code. Diese Methode bietet einen grundlegenden Code (siehe https://github.com/edmondztt/pheromone-traj-analysis.git), um die Bewegungsbahn der Schnecke basierend auf fünf Schlüsselparametern zu visualisieren (Abbildung 3). Zeit: Der Verlauf der Trajektorie, farbcodiert, um den Zeitverlauf seit Beginn des Experiments anzuzeigen. Entfernung zum Pheromon: Die Entfernung zwischen dem Wurm und der Pheromonquelle zu jedem Zeitpunkt. Geschwindigkeit: Die Geschwindigkeit der Schnecke an jedem Punkt, die auch die Dreh- und Stoppereignisse anzeigt. Geradlinigkeit: Wie gerade der Weg des Wurms ist. Richtungskorrektheit: Wie ausgerichtet ist die Bewegung des Wurms mit der Richtung des Pheromonziels? Dieser Code bietet eine grundlegende Visualisierung zum Verständnis des Wurmverhaltens und kann für eine tiefere Analyse angepasst und erweitert werden.
HINWEIS: Dieser fortschrittliche Ansatz bietet eine umfassende Alternative zum traditionellen Chemoattraktionsindex, indem er die Navigationsbahn von Würmern als Reaktion auf Sexualpheromone detailliert beschreibt. Es ermöglicht das Verständnis von Bewegungsmustern, ohne sich auf willkürliche Endpunkte der Navigation und Zeitfensterbestimmung verlassen zu müssen, und bietet tiefere Einblicke in die Verhaltensdynamik des Assays. Die Daten wurden über 20 Frames gemittelt, die je nach experimentellem Bedarf angepasst werden können, um Bewegungen, die durch Körperverdrehungen verursacht werden, herauszufiltern.
Ergebnisse
Trajektorienanalyse der flüchtigen Sexualpheromonwahrnehmung defekter Stamm im Chemoattraktionsassay
Dieser Chemoattraction-Assay unterscheidet zuverlässig zwischen Wildtyp- und mutierten Stämmen von C. elegans in ihrer Reaktion auf flüchtige Sexualpheromone. Erfolgreiche Experimente mit him-5-Männchen zeigen durchweg eine robuste Chemotaxis gegenüber der Pheromonquelle. Dies spiegelt sich in einem hohen Chemotaxis-Index (C.I.) (
Diskussion
Dieses Protokoll bietet eine robuste Methodik für die Extraktion flüchtiger Sexualpheromone aus C. elegans sowie die Etablierung eines robusten Chemoattraktionsassays zur Messung männlicher Chemoattraktionsreaktionen. Weitere Informationen finden Sie im WormLab-Benutzerhandbuch (siehe Materialtabelle); Einen grundlegenden Code zur Visualisierung der Bewegungsbahn der Schnecke finden Sie in Protokollabschnitt 7.3.8.5. Mehrere entscheidende Schritte im Protokol...
Offenlegungen
Die Autoren haben keine Interessenkonflikte offenzulegen.
Danksagungen
Wir danken Dr. Tingtao Zhou für das Entwerfen und Schreiben des Codes für die Trajektorienvisualisierungen, die in unserer Analyse verwendet werden. Diese Arbeit wurde unterstützt durch Finanzierung: R01 NS113119 (PWS), Chen Senior Postdoc Fellowship und das Tianqiao and Chrissy Chen Institute for Neuroscience.
Materialien
| Name | Company | Catalog Number | Comments |
| 10 cm Petri dishes | Falcon | 25373-100 | Falcon bacteriological Petri dish 100 x 15 mm |
| 6 cm Petri dishes | Falcon | 25373-085 | Falcon bacteriological Petri dish 60 x 15 mm |
| C. remanei (EM464) | CGC | ||
| Centrifuge | Eppendorf | centrifuge 5418 | Any brand should work. |
| Chemoattraction assay plates | Homemade solution | N/A | 1.5% agar, 25 mM NaCl, 1.5 mM Tris-base, and 3.5 mM Tris-Cl |
| Cholesterol | Alfa Aesar | 57-88-5 | |
| Dissecting Microscope | Leica | LeicaMZ75 | Any brand should work. |
| E. Coli OP50 | CGC | ||
| Ethanol | Koptec | 64-17-5 | |
| fog-2(q71) (JK574) | CGC | ||
| him-5(e1490)(CB4088) | CGC | ||
| Household bleach | Clorox Germicidal bleach concentrated | Bleach | |
| M9 buffer | Homemade solution | N/A | 3 g KH2PO4, 11.3 g Na2HPO4.7H2O, 5 g NaCl, H2O to 1 L. Sterilize by autoclaving. Add 1 mL 1 M MgSO4 after cool down to room temperature. |
| Magnesium Sulfate, Anhydrous, Powder | Macron | M1063-500GM-EA | |
| Microwave | TOSHIBA | N/A | Any brand should work. |
| N2 | CGC | ||
| NaOH | Sigma-aldrich | S318-3 | 1 M |
| NGM plates solution | Homemade solution | N/A | 2.5 g Peptone, 18 g agar, 3 g NaCl, H2O to 1 L.Sterilize by autoclaving. Once the autoclave is done (2 h), wait until the temperature of the medium drops to 65 °C. Put on a hotplate at 65 °C and stir. Then add the following, waiting 5 min between each to avoid crystallization: 1 mL CaCl2 (1 M), 1 mL MgSO4 (1 M), 25 mL K3PO4 (1 M, pH=6), 1 mL Cholesterol ( 5 mg/mL in ethanol). |
| Parafilm | Bemis | 13-374-10 | Bemis Parafilm M Laboratory Wrapping Film |
| Peptone | VWR | 97063-324 | |
| Pipet- aid | Drummond Scientific | 4-000-100 | Any brand should work. |
| Plastic paper | Octago | Waterproof Screen Printing Inkjet Transparency Film | https://www.amazon.com/Octago-Waterproof-Transparency-Printing-Printers/dp/B08HJQWFGD |
| Potassium chloride | Sigma-aldrich | SLBP2366V | |
| Potassium phosphate | Spectrum | 7778-77-0 | |
| Pipette | Eppendorf | SKU: EPPR4331; MFG#: 2231300006 | 20 - 200 µL, 100 - 1000 µL, any brand should work. |
| Rotator | Labnet | SKU: LI-H5500 | Labnet H5500 Mini LabRoller with Dual Direction Rotator. Any brand should work. |
| Sodium chloride | VWR | 7647-14-5 | |
| sodium phosphate dibasic | Sigma-aldrich | SLCG3888 | |
| Tris-base | Sigma-aldrich | 77-86-1 | |
| Tris-Cl | Roche | 1185-53-1 | |
| Tryptone | VWR | 97063-390 | |
| Vortex | Scientific industries | Vortex-Genie 2 | Any brand should work. |
| WormLab system | MBF Bioscience | N/A | https://www.mbfbioscience.com/help/WormLab/Content/home.htm; https://www.mbfbioscience.com/products/wormlab/ |
| Wormpicker | Homemade | N/A | made with platinum and glass pipet tips |
Referenzen
- Audesirk, T. E. Chemoreception in Alphysia californica. Iii. Evidence for pheromones influencing reproductive behavior. Behav Biol. 20 (2), 235-243 (1977).
- Traynor, K. S., Le Conte, Y., Page, R. E. Queen and young larval pheromones impact nursing and reproductive physiology of honey bee (Apis mellifera) workers. Behav Ecol Sociobiol. 68 (12), 2059-2073 (2014).
- Cowley, J. J., Wise, D. R. Pheromones, growth and behaviour. Ciba Found Study Group. 35, 144-170 (1970).
- Epple, G. Pheromones in primate reproduction and social behavior. Adv Behav Biol. 11, 131-155 (1974).
- Levinson, H. Z. Possibilities of using insectistatics and pheromones in pest control. Naturwissenschaften. 62 (6), 272-282 (1975).
- Roelofs, W. Manipulating sex pheromones for insect suppression. Environ Lett. 8 (1), 41-59 (1975).
- Marchlewska-Koj, A. Pheromones and mammalian reproduction. Oxf Rev Reprod Biol. 6, 266-302 (1984).
- Keverne, E. B. Neuroendocrinology briefings 11: Pheromones and reproduction. J Neuroendocrinol. 12 (11), 1045-1046 (2000).
- Rekwot, P. I., Ogwu, D., Oyedipe, E. O., Sekoni, V. O. The role of pheromones and biostimulation in animal reproduction. Anim Reprod Sci. 65 (3-4), 157-170 (2001).
- Gomez-Diaz, C., Benton, R. The joy of sex pheromones. EMBO reports. 14 (10), 874-883 (2013).
- Shorey, H. H., Gaston, L. K., Jefferson, R. N. Insect sex pheromones. Adv Pest Control Res. 8, 57-126 (1968).
- Bruce, H. M. Pheromones and behavior in mice. Acta Neurol Psychiatr Belg. 69 (7), 529-538 (1969).
- Shorey, H. H., Bartell, R. J. Role of a volatile female sex pheromone in stimulating male courtship behaviour in Drosophila melanogaster. Anim Behav. 18 (1), 159-164 (1970).
- Bobadoye, B., et al. Evidence of aggregation-sex pheromone use by longhorned beetles (coleoptera: Cerambycidae) species native to Africa. Environ Entomol. 48 (1), 189-192 (2019).
- Saunders, J. R. Sex pheromones in bacteria. Nature. 275 (5682), 692-694 (1978).
- Schulz, S., Toft, S. Identification of a sex pheromone from a spider. Science. 260 (5114), 1635-1637 (1993).
- Finnegan, D. E., Chambers, J. Identification of the sex pheromone of the guernsey carpet beetle, Anthrenussarnicus mroczkowski (coleoptera: Dermestidae). J Chem Ecol. 19 (5), 971-983 (1993).
- Vaillancourt, L. J., Raudaskoski, M., Specht, C. A., Raper, C. A. Multiple genes encoding pheromones and a pheromone receptor define the b beta 1 mating-type specificity in Schizophyllum commune. Genetics. 146 (2), 541-551 (1997).
- Ludewig, A. H., Schroeder, F. C. Ascaroside signaling in C. elegans. WormBook : the online review of C. elegans biology. , 1-22 (2013).
- Sakai, N., et al. A sexually conditioned switch of chemosensory behavior in C. elegans. PLoS One. 8 (7), e68676 (2013).
- Sengupta, S., Smith, D. P., Mucignat-Caretta, C. How Drosophila detect volatile pheromones: signaling, circuits, and behavior. Neurobiology of chemical communication. , (2014).
- Zhang, Y. K., Reilly, D. K., Yu, J., Srinivasan, J., Schroeder, F. C. Photoaffinity probes for nematode pheromone receptor identification. Org Biomol Chem. 18 (1), 36-40 (2019).
- Aprison, E. Z., Ruvinsky, I. Dynamic regulation of adult-specific functions of the nervous system by signaling from the reproductive system. Curr Biol. 29 (23), 4116-4123.e3 (2019).
- Wan, X., et al. SRD-1 in AWA neurons is the receptor for female volatile sex pheromones in C. elegans males. EMBO Rep. 20 (3), e46288 (2019).
- Peckol, E. L., Troemel, E. R., Bargmann, C. I. Sensory experience and sensory activity regulate chemosensory receptor gene expression in Caenorhabditis elegans. Proc Natl Acad Sci U S A. 98 (20), 11032-11038 (2001).
- Jang, H., et al. Neuromodulatory state and sex specify alternative behaviors through antagonistic synaptic pathways in. C. elegans. Neuron. 75 (4), 585-592 (2012).
- Liu, K. S., Sternberg, P. W. Sensory regulation of male mating behavior in Caenorhabditis elegans. Neuron. 14 (1), 79-89 (1995).
- Chasnov, J. R., Chow, K. L. Why are there males in the hermaphroditic species Caenorhabditis elegans. Genetics. 160 (3), 983-994 (2002).
- Chasnov, J. R., So, W. K., Chan, C. M., Chow, K. L. The species, sex, and stage specificity of a Caenorhabditis sex pheromone. Proc Natl Acad Sci U S A. 104 (16), 6730-6735 (2007).
- Susoy, V., et al. Natural sensory context drives diverse brain-wide activity during C. elegans mating. Cell. 184 (20), 5122-5137.e17 (2021).
- Barriere, A., Felix, M. A. High local genetic diversity and low outcrossing rate in Caenorhabditis elegans natural populations. Curr Biol. 15 (13), 1176-1184 (2005).
- Click, A., Savaliya, C. H., Kienle, S., Herrmann, M., Pires-Dasilva, A. Natural variation of outcrossing in the hermaphroditic nematode Pristionchus pacificus. BMC Evol Biol. 9, 75 (2009).
- Anderson, J. L., Morran, L. T., Phillips, P. C. Outcrossing and the maintenance of males within C. elegans populations. J Hered. 101 (suppl_1), S62-S74 (2010).
- Leighton, D. H., Choe, A., Wu, S. Y., Sternberg, P. W. Communication between oocytes and somatic cells regulates volatile pheromone production in Caenorhabditis elegans. Proc Natl Acad Sci U S A. 111 (50), 17905-17910 (2014).
- White, J. Q., et al. The sensory circuitry for sexual attraction in C. elegans males. Curr Biol. 17 (21), 1847-1857 (2007).
- Fagan, K. A., et al. A single-neuron chemosensory switch determines the valence of a sexually dimorphic sensory behavior. Curr Biol. 28 (6), 902-914.e5 (2018).
- Lipton, J., Kleemann, G., Ghosh, R., Lints, R., Emmons, S. W. Mate searching in Caenorhabditis elegans: A genetic model for sex drive in a simple invertebrate. J Neurosci. 24 (34), 7427-7434 (2004).
- Frady, E. P., Palmer, C. R., Kristan, W. B. Sexual attraction: Sex-specific wiring of neural circuitry. Curr Biol. 22 (22), R953-R956 (2012).
- Liu, Q., et al. Two preputial gland-secreted pheromones evoke sexually dimorphic neural pathways in the mouse vomeronasal system. Front Cell Neurosci. 13, 455 (2019).
- Ludewig, A. H., et al. Pheromone sensing regulates Caenorhabditis elegans lifespan and stress resistance via the deacetylase sir-2.1. Proc Natl Acad Sci U S A. 110 (14), 5522-5527 (2013).
- Golden, J. W., Riddle, D. L. A pheromone influences larval development in the nematode Caenorhabditis elegans. Science. 218 (4572), 578-580 (1982).
- Butcher, R. A., Fujita, M., Schroeder, F. C., Clardy, J. Small-molecule pheromones that control dauer development in Caenorhabditis elegans. Nat Chem Biol. 3 (7), 420-422 (2007).
- Jeong, P. Y., et al. Chemical structure and biological activity of the Caenorhabditis elegans dauer-inducing pheromone. Nature. 433 (7025), 541-545 (2005).
- Butcher, R. A., Ragains, J. R., Kim, E., Clardy, J. A potent dauer pheromone component in Caenorhabditis elegans that acts synergistically with other components. Proc Natl Acad Sci U S A. 105 (38), 14288-14292 (2008).
- Aprison, E. Z., Ruvinsky, I. Counteracting ascarosides act through distinct neurons to determine the sexual identity of C. elegans pheromones. Curr Biol. 27 (17), 2589-2599.e3 (2017).
- Aprison, E. Z., Ruvinsky, I. Sex pheromones of C. elegans males prime the female reproductive system and ameliorate the effects of heat stress. PLoS Genet. 11 (12), e1005729 (2015).
- Izrayelit, Y., et al. Targeted metabolomics reveals a male pheromone and sex-specific ascaroside biosynthesis in Caenorhabditis elegans. ACS Chem Biol. 7 (8), 1321-1325 (2012).
- Kaplan, F., et al. Ascaroside expression in Caenorhabditis elegans is strongly dependent on diet and developmental stage. PLoS One. 6 (3), e17804 (2011).
- Pungaliya, C., et al. A shortcut to identifying small molecule signals that regulate behavior and development in Caenorhabditis elegans. Proc Natl Acad Sci U S A. 106 (19), 7708-7713 (2009).
- Srinivasan, J., et al. A modular library of small molecule signals regulates social behaviors in Caenorhabditis elegans. PLoS Biol. 10 (1), e1001237 (2012).
- Srinivasan, J., et al. A blend of small molecules regulates both mating and development in Caenorhabditis elegans. Nature. 454 (7208), 1115-1118 (2008).
- Choe, A., et al. Ascaroside signaling is widely conserved among nematodes. Curr Biol. 22 (9), 772-780 (2012).
- Von Reuss, S. H., et al. Comparative metabolomics reveals biogenesis of ascarosides, a modular library of small-molecule signals in C. elegans. J Am Chem Soc. 134 (3), 1817-1824 (2012).
- Choe, A., et al. Sex-specific mating pheromones in the nematode panagrellus redivivus. Proc Natl Acad Sci U S A. 109 (51), 20949-20954 (2012).
- Hsueh, Y. P., Mahanti, P., Schroeder, F. C., Sternberg, P. W. Nematode-trapping fungi eavesdrop on nematode pheromones. Curr Biol. 23 (1), 83-86 (2013).
- Hong, M., et al. Early pheromone experience modifies a synaptic activity to influence adult pheromone responses of C. elegans. Curr Biol. 27 (20), 3168-3177.e3 (2017).
- Ryu, L., et al. Feeding state regulates pheromone-mediated avoidance behavior via the insulin signaling pathway in Caenorhabditis elegans. EMBO J. 37 (15), e98402 (2018).
- Diaz, S. A., Lindström, J., Haydon, D. T. Basic demography of Caenorhabditis remanei cultured under standard laboratory conditions. J Nematol. 40 (3), 167 (2008).
- Bargmann, C. I. Chemosensation in C. elegans. WormBook : the online review of C.elegans biology. , 1-29 (2006).
- Margie, O., Palmer, C., Chin-Sang, I. C. elegans chemotaxis assay. JoVE: J Vis Exp. (74), e50069 (2013).
- Bargmann, C. I., Hartwieg, E., Horvitz, H. R. Odorant-selective genes and neurons mediate olfaction in C. elegans. Cell. 74 (3), 515-527 (1993).
Nachdrucke und Genehmigungen
Genehmigung beantragen, um den Text oder die Abbildungen dieses JoVE-Artikels zu verwenden
Genehmigung beantragenThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Alle Rechte vorbehalten