Se requiere una suscripción a JoVE para ver este contenido. Inicie sesión o comience su prueba gratuita.
Method Article
Cromatografía de gases-Espectrometría de masas basada en metabolómica dirigida de muestras de coral duro
En este artículo
Resumen
Aquí, presentamos la extracción y preparación de metabolitos polares y semipolares de un holobionte de coral, así como tejido huésped de coral separado y fracciones celulares de Symbiodiniaceae, para el análisis de cromatografía de gases-espectrometría de masas.
Resumen
Los enfoques basados en cromatografía de gases-espectrometría de masas (GC-MS) han demostrado ser poderosos para dilucidar la base metabólica de la simbiosis cnidario-dinoflagelada y cómo responde el coral al estrés (es decir, durante el blanqueamiento inducido por la temperatura). El perfil de metabolitos en estado estacionario del holobionte de coral, que comprende el huésped cnidario y sus microbios asociados (Symbiodiniaceae y otros protistas, bacterias, arqueas, hongos y virus), se ha aplicado con éxito en condiciones ambientales y de estrés para caracterizar el estado metabólico holístico del coral.
Sin embargo, para responder a las preguntas que rodean las interacciones simbióticas, es necesario analizar los perfiles de metabolitos del coral huésped y sus simbiontes de algas de forma independiente, lo que solo puede lograrse mediante la separación física y el aislamiento de los tejidos, seguidos de una extracción y análisis independientes. Si bien la aplicación de la metabolómica es relativamente nueva en el campo de los corales, los esfuerzos sostenidos de los grupos de investigación han dado como resultado el desarrollo de métodos robustos para analizar los metabolitos en los corales, incluida la separación del tejido huésped de coral y los simbiontes de algas.
Este artículo presenta una guía paso a paso para la separación de holobiontes y la extracción de metabolitos para el análisis de GC-MS, incluidos los pasos clave de optimización para su consideración. Demostramos cómo, una vez analizado de forma independiente, el perfil de metabolitos combinados de las dos fracciones (coral y Symbiodiniaceae) es similar al perfil del conjunto (holobionte), pero al separar los tejidos, también podemos obtener información clave sobre el metabolismo y las interacciones entre los dos socios que no se puede obtener del todo por sí solo.
Introducción
Los metabolitos representan los productos finales de los procesos celulares, y la metabolómica -el estudio del conjunto de metabolitos producidos por un organismo o ecosistema determinado- puede proporcionar una medida directa del funcionamiento del organismo. Esto es particularmente crítico para explorar los ecosistemas, las interacciones simbióticas y las herramientas de restauración, ya que el objetivo de la mayoría de las estrategias de manejo es preservar (o restaurar) funciones específicas de los servicios ecosistémicos2. Los arrecifes de coral son un ecosistema acuático que demuestra el valor potencial de la metabolómica para dilucidar las interacciones simbióticas y vincular las respuestas fisiológicas de los corales con los impactos a nivel de la comunidad y del ecosistema3. La aplicación de la cromatografía de gases-espectrometría de masas de alto rendimiento (GC-MS) es especialmente valorada debido a su capacidad para analizar rápidamente una amplia gama de clases de metabolitos simultáneamente con alta selectividad y sensibilidad, proporcionar una rápida identificación de compuestos cuando se dispone de bibliotecas espectrales y proporcionar un alto nivel de reproducibilidad y precisión, con un coste por muestra relativamente bajo.
Los corales son holobiontes formados por el animal coralino, endosimbiontes dinoflagelados fotosintéticos (familia: Symbiodiniaceae4) y un microbioma complejo 5,6. En general, la aptitud del holobionte se mantiene principalmente a través del intercambio de pequeñas moléculas y elementos para apoyar el funcionamiento metabólico de cada miembro 7,8,9,10. Los enfoques metabolómicos han demostrado ser especialmente poderosos para dilucidar la base metabólica de la especificidad de la simbiosis 9,11, la respuesta de blanqueamiento al estrés térmico 7,8,12,13, las respuestas a enfermedades 14, las respuestas a la exposición a la contaminación 15, la fotoaclimatación 16 y la señalización química 17 en corales, así como para ayudar en el descubrimiento de biomarcadores 18,19. Además, la metabolómica puede proporcionar una valiosa confirmación de las conclusiones inferidas a partir de técnicas basadas en ADN y ARN 9,20. Por lo tanto, existe un potencial considerable para el uso de la metabolómica para evaluar la salud de los arrecifes y desarrollar herramientas para la conservación de los arrecifes3, por ejemplo, mediante la detección de biomarcadores metabólicos de estrés18,19 y para examinar el potencial de las estrategias de gestión activa, como los subsidios nutricionales21.
Separar las células huésped y simbionte y analizar sus perfiles de metabolitos de forma independiente, en lugar de juntas como el holobionte, puede proporcionar más información sobre las interacciones de la pareja, los estados fisiológicos y metabólicos independientes y los posibles mecanismos moleculares de adaptación 11,12,22,23,24. Sin separar el coral y las Symbiodiniaceae, es casi imposible dilucidar la contribución y el metabolismo de los corales y/o Symbiodiniaceae de forma independiente, excepto con la reconstrucción compleja del genoma y el modelado metabólico25, pero esto aún no se ha aplicado a la simbiosis coral-dinoflagelado. Además, intentar extraer información sobre el metabolismo individual del huésped o del simbionte de algas a partir del perfil de metabolitos del holobionte puede dar lugar a interpretaciones erróneas.
Por ejemplo, hasta hace poco, se pensaba que la presencia de ácidos grasos poliinsaturados C18:3n-6, C18:4n-3 y C16 en extractos de tejidos de corales y holobiontes se derivaba del simbionte de las algas, ya que se suponía que los corales no poseían las ωx desaturasas esenciales para la producción de ácidos grasos omega-3 (ω3); sin embargo, la evidencia genómica reciente sugiere que múltiples cnidarios tienen la capacidad de producir AGPI ω3 de novo y biosintetizar aún más AGPI26 de cadena larga ω3. La combinación de GC-MS con marcaje isotópico estable (p. ej., 13 C-bicarbonato, NaH 13CO 3) se puede utilizar para rastrear el destino del carbono fijado fotosintéticamente a través de las redes metabólicas de holobiontes de coral tanto en condiciones de control como en respuesta a factores estresantes externos27,28. Sin embargo, un paso crítico en el seguimiento del destino de 13 C es la separación del tejido de coral de las células de algas, solo entonces se puede asignar inequívocamente la presencia de un compuesto marcado con 13C en la fracción huésped del coral como un metabolito derivado de Symbiodiniaceae translocado al coral o un producto aguas abajo de un compuesto marcado translocado. Esta técnica ha demostrado su poder al desafiar la suposición sostenida durante mucho tiempo de que el glicerol es la forma primaria en la que el fotosintato se transloca del simbionte al huésped29, así como al dilucidar cómo cambia el flujo nutricional entre socios durante el blanqueamiento27,28 y en respuesta a especies de Symbiodiniaceae incompatibles11.
Si bien la decisión de separar los tejidos depende principalmente de la pregunta de investigación, es importante tener en cuenta la practicidad, la confiabilidad y los posibles impactos metabólicos de este enfoque. Aquí, proporcionamos métodos detallados y demostrados para la extracción de metabolitos del holobionte, así como de las fracciones separadas del huésped y del simbionte. Comparamos los perfiles de metabolitos del huésped y del simbionte de forma independiente y cómo se comparan estos perfiles con el perfil de metabolitos del holobionte.
Access restricted. Please log in or start a trial to view this content.
Protocolo
NOTA: El diseño experimental, la recolección de muestras y el almacenamiento se han descrito en detalle en otro lugar 2,30,31. La aprobación del permiso para la recolección de corales silvestres debe obtenerse antes de la recolección y experimentación. Las muestras aquí fueron colectadas de colonias de Montipora mollis (color verde-morfo) importadas de Batavia Coral Farms (Geraldton, WA), originalmente recolectadas de un arrecife frente a las Islas Abrohlos (Australia Occidental; 28°52'43.3"S 114°00'17.0"E) a una profundidad de 1 m bajo la Licencia de Acuicultura AQ1643. Antes del muestreo, las colonias se mantuvieron en un acuario de 800 L a 35 PSU, bajo luz azul y blanca a 150 μmol de fotones·m−2·s−1, y a 25 °C ± 0,5 °C durante 3 meses. Los fragmentos de coral (~5cm2, N = 6) se congelaron en nitrógeno líquido y se almacenaron a -80 °C hasta su procesamiento.
1. Preparación de las soluciones y equipos de extracción
- Al menos 1 día antes de la extracción del tejido de coral, prepare las soluciones y el equipo de extracción.
- Enfríe previamente agua ultrapura en cristalería limpia y sin detergente a 4 °C.
- Mezcle metanol 100% de grado LC con una concentración final de 10 μg·mL−1 de patrón interno apropiado (p. ej., 13C6 sorbitol).
- Cree una solución de extracción de metanol al 50 % utilizando la mitad de metanol de grado LC al 100 % y la mitad de agua ultrapura. Almacenar ambas soluciones de metanol a -20 °C.
NOTA: Para ayudar a prevenir la degradación de los metabolitos, se recomienda realizar los pasos de procesamiento de muestras en lotes de cinco fragmentos de coral a la vez, con un espacio en blanco biológico adicional (solo agua) (muestras totales N = 6). Una vez que cada muestra de coral se ha separado en las dos fracciones (tejido huésped de coral, en adelante "Huésped", y células de microalgas, en adelante "Simbionte"), el número total de muestras en un lote de procesamiento será de 12.
2. Extinción del metabolismo de los corales
NOTA: El diseño experimental, la recolección de muestras y el almacenamiento se han descrito en detalle en otro lugar 2,30,31. Sin embargo, debe tenerse en cuenta que el tiempo que se tarda en apagar el metabolismo (es decir, el tiempo que transcurre entre la recolección y la preservación de la muestra de coral) es fundamental para capturar la respuesta original30. Conservar la muestra lo antes posible después de la recolección para evitar cambios en la composición del metabolito debido a la degradación de la muestra o a respuestas fisiológicas no objetivo32.
- Coloque el fragmento de coral en una bolsa estéril de recolección de muestras y drene el exceso de agua de mar tanto como sea posible. Sumerja la muestra en nitrógeno líquido durante un mínimo de 30 s. Traslade las muestras lo antes posible a un congelador a -80 °C para su almacenamiento.
NOTA: Las muestras se pueden congelar a -80 °C en recipientes con bloqueo de luz hasta su procesamiento, evitando los ciclos de congelación y descongelación.
3. Eliminación de tejido coralino del esqueleto
NOTA: Las muestras deben mantenerse en hielo (4 °C) en todo momento para garantizar que estén simultáneamente en forma líquida y evitar el metabolismo continuo.
- Coloque una bolsa de recolección de muestras limpia y estéril sobre hielo para que la bolsa esté estable y abierta sobre el hielo en un pozo poco profundo, pero no esté sumergida en el hielo. Añadir 10 ml de agua ultrapura fría (4 °C) a la bolsa.
NOTA: Esto ayudará a evitar la congelación y descongelación repetida del fragmento de coral debido al aire frío presurizado y al hielo circundante. - Seleccione un fragmento de coral con pinzas esterilizadas y enjuague con agua ultrapura fría (4 °C) utilizando una pipeta Pasteur estéril hasta que no queden residuos de agua de mar. Sumerja el fragmento de coral enjuagado en la bolsa que contiene los 10 ml de agua ultrapura.
NOTA: Este enjuague es fundamental para eliminar cualquier sal residual que interfiera con el análisis posterior. Evite el contacto de las manos con el agua o el fragmento de coral a través de la bolsa para mantener la muestra a 4 °C. - Pegue una punta de pipeta estéril de 1 ml sobre el extremo de una pistola de aire comprimido con cinta aislante, con ~5 mm cortado en el extremo de la punta (Figura 1A).
- Apunte la pistola de aire comprimido sobre el fragmento de coral con la bolsa medio sellada y el flujo de aire en bajo-medio para eliminar suavemente el tejido fomentando un movimiento circular del agua sobre el fragmento de coral.
- Después de ~ 3 minutos, o cuando parezca que se ha eliminado todo el tejido del esqueleto, apague el aire y retire el aerógrafo. Selle completamente la bolsa.
- Apriete todo el tejido de coral extraído en una esquina inferior de la bolsa. Corta la esquina opuesta y vierte suavemente el contenido de la bolsa en un tubo de 15 ml con hielo.
4. Homogeneización opcional
NOTA: Algunas especies de coral son más viscosas que otras, lo que significa que el aerógrafo eliminará el tejido en grupos en lugar de en una suspensión. Si se observan grumos de tejido en el homogeneizado con aerógrafo, se puede añadir un paso de homogeneización a 4 °C para todas las muestras.
- Limpie un homogeneizador mecánico de dientes de sierra dos veces con metanol al 70% a 4 °C y finalmente con agua ultrapura a 4 °C.
- Homogeneizar la muestra de coral en un tubo de 15 ml durante ~1 min hasta que la muestra esté completamente homogeneizada y no se vean grumos.
- Limpie el homogeneizador como en el paso 4.1 entre cada muestra. Mantenga el tiempo de homogeneización constante en todas las muestras.
5. Recogida de muestras para la normalización
- Recolectar una alícuota de 1,000 μL del tejido homogeneizado para los recuentos celulares de Symbiodiniaceae, el análisis del contenido de proteínas del tejido huésped de coral y la estimación de clorofila. Conservar a -20 °C hasta que esté listo para analizar (sección 10).
6. Separación opcional del tejido huésped del coral-células Symbiodiniaceae
- Centrifugar el homogeneizado de coral a 2.500 × g durante 5 min a 4 °C utilizando una centrífuga refrigerada.
NOTA: Esta velocidad es óptima para separar las células Symbiodiniaceae más pesadas, manteniendo intactas sus paredes celulares, del tejido huésped, que está suspendido en el sobrenadante. - Retire el sobrenadante que contiene el material huésped y colóquelo en un nuevo tubo de 15 ml.
NOTA: Los lípidos del tejido huésped suelen formar una estrecha capa rosa/blanca en la parte superior de las células simbiontes. Esta capa se puede recolectar junto con el sobrenadante huésped soluble mediante pipeteo (Figura 1B). - Vórtice vigorosamente el huésped durante exactamente 1 minuto. Mantenga la muestra de gránulos de algas y la muestra del sobrenadante en hielo.
- Añadir 2 ml de agua ultrapura a 4 °C al gránulo de algas. Vórtice vigorosamente durante exactamente 2 minutos para resuspender el pellet.
NOTA: Si no se recolectaron fragmentos individuales de 1 cm de la colonia de coral para el genotipado de Symbiodinaiceae, se puede recolectar aquí una alícuota de 200 μL de la suspensión celular de Symbiodinaiceae, conservarla en la solución tampón de ADN preferida y almacenarla como se describe en Thurber et al.30 para el genotipado de Symbiodiniaceae (por ejemplo, según González-Pech et al.12). - Repita los pasos 6.1 a 6.4 una vez más.
NOTA: La separación fiable del huésped y el simbionte depende de la biomasa y la especie de coral, ya que algunas especies pueden ser más viscosas que otras. Se recomienda un mínimo de tres pasos de lavado, pero esto se puede aumentar dependiendo del éxito de la separación. Repita los pasos de lavado 4.7-4.9 hasta que no se puedan ver células de Symbiodiniaceae en la parte inferior de la fracción del huésped y hasta que la fracción de Symbiodiniaceae esté visiblemente libre de material del huésped (p. ej., sin capa blanca en la parte superior) (Figura 1). - Retire el sobrenadante que contiene el material huésped y colóquelo en un nuevo tubo de 15 ml.
- Retenga el gránulo de simbionte en el tubo de 15 ml.
7. Secado de muestras
- Congelar el homogeneizado holobionte o las fracciones separadas del huésped y de Symbiodiniaceae, a -80 °C durante ~120 min. Liofilizar las muestras durante la noche con un vacío de 0,01 mbar a -85 °C.
NOTA: Para evitar la pérdida de muestras durante la liofilización, se recomienda utilizar una tapa cortada de otro tubo estéril, o parafilm estéril, con un orificio de ~2 mm perforado cuidadosamente con una aguja estéril de 25 G. - Cuando esté seco, usando una balanza de laboratorio, pese uno de los siguientes: 1) 25 mg del holobionte; 2) 15 mg de la fracción simbionte; o 3) 30 mg del tejido huésped de cada muestra en tubos de microcentrífuga separados de 2 ml sin plastificante.
NOTA: Paso crítico: La optimización de la biomasa para la extracción es esencial para garantizar que el GC-MS no se sobrecargue y al mismo tiempo garantizar una señal suficiente. El material de coral seco es muy estático. Para evitar la pérdida de muestras, utilice dispositivos antiestáticos para eliminar las cargas electrostáticas de las muestras y los recipientes de pesaje. Una alternativa simple y rentable es colocar una toallita para secadora de ropa debajo del tubo de muestra. El gránulo de simbionte seco se puede cortar al peso deseado con una cuchilla estéril.
8. Extracciones intracelulares de metabolitos
- Extracción intracelular de metabolitos a partir de holobionte liofilizado:
- Añadir 400 μL de metanol 100% frío (−20 °C) con patrón/es interno/s (IS; 13C6 sorbitol y/o 13C5-15 N valina, a 10μM) a cada tubo.
- Agregue una pequeña cantidad de perlas de vidrio lavadas con ácido de 710-1,180 μm (~ 10 mg) a cada muestra. Colocar en un molino de bolas a 50 Hz durante 3 min en un inserto de molino de bolas preenfriado (−20 °C).
- Añadir 600 μL adicionales de metanol 100% frío (−20 °C) con ISs (13 C6 sorbitol y/o 13C 5-15 N valina, a 10μM) a cada tubo.
- Vórtice para mezclar durante 1 min. Colocar en una coctelera a 4 °C durante 30 min.
- Extracción intracelular de metabolitos de células Symbiodiniaceae liofilizadas separadas:
- Añadir 200 μL de metanol 100% frío (−20 °C) con ISs (13 C6 sorbitol y/o 13C 5-15 N valina, a 10μM) al material seco de Symbiodiniaceae.
- Agregue una pequeña cantidad de perlas de vidrio lavadas con ácido de 710-1,180 μm (~ 10 mg). Colocar en un molino de bolas a 50 Hz durante 3 min en un inserto de molino de bolas preenfriado (−20 °C).
- Añadir otros 800 μL de metanol 100% frío (−20 °C) con IS y vórtice durante 30 s.
- Extracción intracelular de metabolitos del tejido liofilizado separado del huésped:
- Añadir 1 mL de metanol de grado LC 100% frío (−20 °C) que contiene IS (13 C6 sorbitol y/o 13C 5-15 N valina, a 10μM) al material huésped seco.
- Vórtice para mezclar durante 20 s. Colocar en un soporte de tubo flotante en un baño de sonicación a 4 °C durante 30 min.
9. Purificación del extracto de metabolitos
- Centrifugar las muestras (holobionte/huésped/simbionte) a 3.000 × g durante 30 min a 4 °C.
- Transfiera todo el sobrenadante a un nuevo tubo de microcentrífuga de 2 ml, teniendo cuidado de no alterar el gránulo de restos celulares.
NOTA: Estos son los extractos semipolares. Estos pueden mantenerse en hielo temporalmente, pero almacenarse a largo plazo a -80 °C en la oscuridad. - A los restos celulares restantes, añadir 1.000 μL de metanol frío al 50% (-20 °C). Vórtice vigorosamente durante 1 minuto para volver a suspender.
- Centrifugar las muestras a 3.000 × g durante 30 min a 4 °C.
- Recoja y agrupe el sobrenadante (extractos polares) con los extractos semipolares de la misma muestra.
NOTA: Los restos celulares pueden almacenarse a -80 °C y utilizarse para la normalización del contenido de proteínas (sección 11). - Centrifugar los extractos agrupados a 16.100 g durante 15 min para eliminar todos los precipitados y trasladar el sobrenadante a un nuevo tubo de microcentrífuga sin plastificante (2 mL).
NOTA: Los extractos de muestra pueden almacenarse a -80 °C en la oscuridad. - Cuando esté listo para analizar, alícuota 50 μL de cada extracto en un inserto de vidrio. Concentrar durante 30 min a 30 °C con un concentrador de vacío. Repita cuatro veces más (para 250 μL de extracto seco total).
NOTA: Las muestras secas se pueden almacenar a temperatura ambiente en condiciones desecantes hasta el análisis.
10. Derivatización de metabolitos
NOTA: Se utiliza un proceso de derivatización en línea de dos pasos para la metoximación y trimetisililación de los metabolitos polares.
- Añadir 25 μL de clorhidrato de metoxiamina (30 mg/mL en piridina) a cada muestra.
- Agitar a 37 °C en un agitador orbital ajustado a 750 rpm durante 2 h.
- Añadir 25 μL de N,O-bis (trimetilsilil)trifluoroacetamida + trimeticlorosilano a cada muestra.
- Agitar de nuevo a 37 °C y 750 rpm durante 1 h.
- Deje que las muestras se equilibren a temperatura ambiente durante 1 h antes de inyectar 1 μL en una proporción de división de 1:10 en el GC.
11. Análisis de cromatografía de gases-espectrometría de masas
NOTA: El espectrómetro de masas debe ajustarse de acuerdo con las recomendaciones del fabricante utilizando tris-(perfluorobutil)-amina (CF43).
- Utilice helio de ultra alta pureza como gas portador a un caudal de columna constante de 1 mL/min.
- Utilice una columna DB-5 de 30 m con un espesor de película de 1 μm y un diámetro interno de 0,25 mm.
- Programa de hornos GC
- Ajuste la temperatura de entrada a 280 °C.
- Comience con la inyección a una temperatura del horno de 100 °C y manténgala durante 4 min.
- Aumente la temperatura en 10 °C/min hasta 320 °C y manténgala durante 11 min.
- Parámetros del espectrómetro de masas
- Ajuste la línea de transferencia MS a 280 °C y ajuste la fuente de iones a 200 °C.
- Utilice argón como gas de celda de colisión para generar el ion producto de monitoreo de reacción múltiple (MRM).
- Logre la detección de metabolitos en relación con una biblioteca MRM segmentada en el tiempo que contiene objetivos MRM.
12. Recuentos de células simbiodiniáceas, análisis del contenido de proteínas del tejido huésped de coral y estimación de clorofila
- Recuentos de células de Symbiodiniaceae:
- Tome una alícuota del homogeneizado del tejido coralino.
- Centrifugar las muestras a 2.000 × g para granular las algas.
- Retire el sobrenadante de ~ 200 μL del gránulo de algas y colóquelo en un nuevo tubo de microcentrífuga.
NOTA: Esta será la muestra de proteína que se utilizará para normalizar los datos; guárdelo a -20 °C antes de analizarlo, si es necesario. - Vuelva a suspender el gránulo de algas en 1 ml de agua de mar filtrada pipeteando suavemente hacia arriba y hacia abajo. Si es necesario, diluya la suspensión de algas para facilitar el recuento de células.
- Realice un recuento de células con un hemocitómetro bajo un microscopio óptico añadiendo 10 μL a una de las cámaras. Complete de 8 a 10 recuentos por muestra.
NOTA: También se pueden aplicar métodos alternativos para contar las células de algas cuando estén disponibles (p. ej., citometría de flujo, microscopía confocal de alto rendimiento). - Calcular la concentración de las células simbiontes (mL−1), teniendo en cuenta los factores de dilución utilizados.
- Determinación del contenido de proteínas
- Cuantificar el contenido de proteínas de la muestra (por ejemplo, a través del ensayo colorimétrico de Bradford, descrito inicialmente por Bradford et al.33, o el ensayo de Lowry34,35, cuyo protocolo se ha descrito para cnidarios en otros lugares 36).
- Extracción de clorofila a
- Use un gránulo de celda de ~ 200, 000 celdas, congeladas o frescas.
- Transfiera cada gránulo de algas a 2 ml de dimetilformamida (DMF) en un vial de centelleo de vidrio e incube en la oscuridad a 4 °C durante 48 h.
NOTA: El DMF es tóxico y cancerígeno, por lo que la preparación de la muestra debe completarse bajo una campana extractora lo más oscura posible y con hielo. Si hay <200.000 células, use menos DMF. - Centrifugar durante 3 min a 16.000 × g.
- Transfiera 200 ml a una placa de pocillos UV-96 para realizar mediciones fotométricas. Ejecute cada muestra por triplicado con DMF como pieza en bruto.
- Mida la absorbancia en longitudes de onda (E) 663,8 nm, 646 nm y 750 nm. Reste la absorbancia a 750 nm de la absorbancia en las otras dos longitudes de onda.
NOTA: La medición a 750 nm corrige cualquier dispersión o turbidez en la muestra. - Calcular la concentración de clorofila a (μg/mL) utilizando la ecuación (1):
Concentración de Chl a (μg/mL) = (12,00 × E 663,8) - (3,11 × E646,8) (1)
13. Cuantificación de la biomasa celular tras extracciones de metabolitos para su normalización
NOTA: Existen dos opciones para la cuantificación de la biomasa celular que se describen a continuación: la cuantificación de la proteína relacionada con la biomasa utilizando un método colorimétrico de Bradford modificado y la medición del peso seco de los restos celulares. Cualquiera de los dos métodos es apropiado, ya que ambos ofrecen una cuantificación precisa de la biomasa celular.
- Contenido proteico de los restos celulares
- Resuspender los restos celulares congelados con 1 mL de NaOH 0,2 M e incubar las muestras a 98 °C durante 20 min.
- Enfríe las muestras en hielo durante ~ 10 minutos y centrifugue a 3.000 × g durante 5 minutos a temperatura ambiente.
- Cuantificar el contenido de proteína de la muestra (p. ej., a través del ensayo colorimétrico de Bradford, descrito inicialmente por Bradford et al.33 y modificado por Smart et al.37).
- Medición del peso seco de los restos de la célula
- Resuspender los restos celulares de la extracción de metabolitos intracelulares en agua bidestilada (~10 mL).
- Filtrar la solución al vacío utilizando un filtro de membrana prepesado (poro de 0,22 μm, 47 mm).
- Lave los tubos que contienen biomasa dos veces con agua ultrapura para asegurar la transferencia completa de biomasa al filtro de membrana.
- Retire el filtro de membrana que contiene la biomasa y séquelo con un horno microondas (baja potencia; ~250 W durante 20 min).
- Guarde el papel de filtro en un desecador durante la noche. Registre el peso seco del papel de filtro y calcule el peso seco de la biomasa restando el peso del filtro de membrana seca (utilizando un filtro de membrana seca limpio secado junto con el filtro de muestra) del peso total.
14. Análisis de datos
- Analice las dianas de metabolitos utilizando bases de datos de metabolitos en las que cada diana se compone de un MRM cuantificador y calificador.
- Inspeccione visualmente los objetivos de metabolitos detectados e intégrelos manualmente según sea necesario.
- Utilice un área de pico de metabolito para calcular la abundancia relativa de cada muestra para cada grupo. Los valores se corrigen en blanco y se normalizan para muestrear el área de pico estándar interno y luego para muestrear el contenido de proteína de desechos celulares según Smart et al.37.
- Descartar metabolitos con una desviación estándar relativa superior al 35% en todos los grupos de tratamiento (N = 23 metabolitos).
- Transforme los datos (por ejemplo, la raíz cúbica) y céntrelos en el medio; confirman una distribución normal y homogeneidad de la varianza.
- Realizar el análisis de datos (ANOVA y construcción de mapas de calor; por ejemplo, utilizando https://www.metaboanalyst.ca)38. Agrupe las muestras para examinar la variabilidad dentro del tratamiento utilizando los paquetes "cluster", "factoextra" y "klustR". Calcule el estadístico gap (un método para determinar el número óptimo de clústeres39) utilizando la función "clusGap" en R y grafique utilizando el paquete de R "tidyverse". Realizar PERMANOVAs para examinar la importancia en la separación entre los perfiles de metabolitos del tratamiento (por ejemplo, en Primer).
Access restricted. Please log in or start a trial to view this content.
Resultados
Todos los datos producidos durante este trabajo están disponibles en la información complementaria.
Separación huésped-simbionte
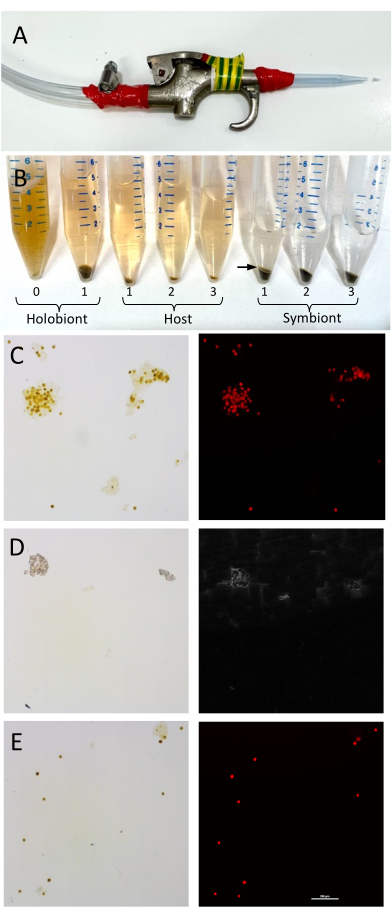
Figura 1: Configuración y validación de la separación de los tejidos del huésped de coral y las células de Symbiodiniaceae. (A
Access restricted. Please log in or start a trial to view this content.
Discusión
La separación del huésped y el simbionte se puede lograr fácil y rápidamente a través de una simple centrifugación, y los resultados aquí muestran que la separación de las fracciones puede proporcionar información valiosa indicativa de contribuciones específicas de miembros holobiontes, que pueden contribuir al análisis funcional de la salud de los corales. En los corales adultos, la síntesis de lípidos es realizada principalmente por el simbionte de algas residente 40, que suministra lípidos (por ...
Access restricted. Please log in or start a trial to view this content.
Divulgaciones
Los autores no tienen ningún conflicto de intereses que revelar.
Agradecimientos
J.L.M. recibió el apoyo de una beca de investigación del rector de UTS.
Access restricted. Please log in or start a trial to view this content.
Materiales
| Name | Company | Catalog Number | Comments |
| 100% LC-grade methanol | Merck | 439193 | LC grade essential |
| 2 mL microcentrifuge tubes, PP | Eppendorf | 30121880 | Polypropylene provides high resistance to chemicals, mechanical stress and temperature extremes |
| 2030 Shimadzu gas chromatograph | Shimadzu | GC-2030 | |
| 710-1180 µm acid-washed glass beads | Merck | G1152 | This size is optimal for breaking the Symbiodiniaceae cells |
| AOC-6000 Plus Multifunctional autosampler | Shimadzu | AOC6000 | |
| Bradford reagent | Merck | B6916 | Any protein colourimetric reagent is acceptable |
| Compressed air gun | Ozito | 6270636 | Similar design acceptable. Having a fitting to fit a 1 mL tip over is critical. |
| DB-5 column with 0.25 mm internal diameter column and 1 µm film thickness | Agilent | 122-5013 | |
| DMF | Merck | RTC000098 | |
| D-Sorbitol-6-13C and/or 13C5–15N Valine | Merck | 605514/ 600148 | Either or both internal standards can be added to the methanol. |
| Flat bottom 96-well plate | Merck | CLS3614 | |
| Glass scintillation vials | Merck | V7130 | 20 mL, with non-plastic seal |
| Immunoglogin G | Merck | 56834 | if not availbe, Bovine Serum Albumin is acceptable |
| Primer | v4 | ||
| R | v4.1.2 | ||
| Shimadzu LabSolutions Insight software | v3.6 | ||
| Sodium Hydroxide | Merck | S5881 | Pellets to make 1 M solution |
| tidyverse | v1.3.1 | R package | |
| TissueLyser LT | Qiagen | 85600 | Or similar |
| TQ8050NX triple quadrupole mass spectrometer | Shimadzu | GCMS-TQ8050 NX | |
| UV-96 well plate | Greiner | M3812 | |
| Whirl-Pak sample bag | Merck | WPB01018WA | Sample collection bag; Size: big enough to house a ~5 cm coral fragment, but not too big that the water is too spread |
Referencias
- Bundy, J. G., Davey, M. P., Viant, M. R. Environmental metabolomics: A critical review and future perspectives. Metabolomics. 5 (1), 3-21 (2008).
- Matthews, J. L., et al. The metabolic significance of symbiont community composition in the coral-algal symbiosis. Applied Environmental Metabolomics. Beale, D. J., Hillyer, K. E., Warden, A. C., Jones, O. A. H. , Academic Press. Cambridge, MA. 211-229 (2022).
- Lawson, C. A., et al. Informing coral reef conservation through metabolomic approaches. Coral Reef Conservation and Restoration in the Omics Age. Coral Reefs of the World. van Oppen, M. J. H., Aranda Lastra, M. , Springer. Cham, Switzerland. 179-202 (2022).
- LaJeunesse, T. C., et al. Systematic revision of Symbiodiniaceae highlights the antiquity and diversity of coral endosymbionts. Current Biology. 28 (16), 2570-2580 (2018).
- Rohwer, F., Seguritan, V., Azam, F., Knowlton, N. Diversity and distribution of coral-associated bacteria. Marine Ecology Progress Series. 243, 1-10 (2002).
- Maire, J., et al. Intracellular bacteria are common and taxonomically diverse in cultured and in hospite algal endosymbionts of coral reefs. The ISME Journal. 15 (7), 2028-2042 (2021).
- Hillyer, K. E., et al. Metabolite profiling of symbiont and host during thermal stress and bleaching in the coral Acropora aspera. Coral Reefs. 36, 105-118 (2016).
- Hillyer, K. E., Tumanov, S., Villas-Bôas, S., Davy, S. K. Metabolite profiling of symbiont and host during thermal stress and bleaching in a model cnidarian-dinoflagellate symbiosis. Journal of Experimental Biology. 219 (4), 516-527 (2016).
- Matthews, J. L., et al. Optimal nutrient exchange and immune responses operate in partner specificity in the cnidarian-dinoflagellate symbiosis. Proceedings of the National Academy of Sciences of the United States of America. 114 (50), 13194-13199 (2017).
- Rosset, S. L., et al. The molecular language of the cnidarian-dinoflagellate symbiosis. Trends in Microbiology. 29 (4), 320-333 (2020).
- Matthews, J. L., et al. Partner switching and metabolic flux in a model cnidarian-dinoflagellate symbiosis. Royal Society. 285 (1892), 20182336(2018).
- González-Pech, R. A., et al. Physiological factors facilitating the persistence of Pocillopora aliciae and Plesiastrea versipora in temperate reefs of south-eastern Australia under ocean warming. Coral Reefs. 41, 1239-1253 (2022).
- Williams, A., et al. Metabolomic shifts associated with heat stress in coral holobionts. Science Advances. 7 (1), (2021).
- Deutsch, J. M., et al. Metabolomics of healthy and stony coral tissue loss disease affected Montastraea cavernosa corals. Frontiers in Marine Science. 8, 1421(2021).
- Stien, D., et al. A unique approach to monitor stress in coral exposed to emerging pollutants. Scientific Reports. 10 (1), 9601(2020).
- Lohr, K. E., et al. Resolving coral photoacclimation dynamics through coupled photophysiological and metabolomic profiling. Journal of Experimental Biology. 222 (8), (2019).
- Jorissen, H., et al. Coral larval settlement preferences linked to crustose coralline algae with distinct chemical and microbial signatures. Scientific Reports. 11 (1), 14610(2021).
- Roach, T. N., Dilworth, J., Jones, A. D., Quinn, R. A., Drury, C. Metabolomic signatures of coral bleaching history. Nature Ecology & Evolution. 5 (4), 495-503 (2021).
- Parkinson, J. E., et al. Molecular tools for coral reef restoration: Beyond biomarker discovery. Conservation Letters. 13 (1), 12687(2020).
- Jiang, J., et al. How Symbiodiniaceae meets the challenges of life during coral bleaching. Coral Reefs. 40, 1339-1353 (2021).
- Guerra, F. D., Attia, M. F., Whitehead, D. C., Alexis, F. Nanotechnology for environmental remediation: materials and applications. Molecules. 23 (7), 1760(2018).
- Matthews, J. L., et al. Metabolite pools of the reef building coral Montipora capitata are unaffected by Symbiodiniaceae community composition. Coral Reefs. 39, 1727-1737 (2020).
- Papina, M., Meziane, T., van Woesik, R. Symbiotic zooxanthellae provide the host-coral Montipora digitata with polyunsaturated fatty acids. Comparative Biochemistry and Physiology Part B: Biochemistry and Molecular Biology. 135 (3), 533-537 (2003).
- Kellogg, R., Patton, J. Lipid droplets, medium of energy exchange in the symbiotic anemone Condylactis gigantea: A model coral polyp. Marine Biology. 75, 137-149 (1983).
- Ankrah, N. Y., Chouaia, B., Douglas, A. E. The cost of metabolic interactions in symbioses between insects and bacteria with reduced genomes. mBio. 9 (5), e01433(2018).
- Kabeya, N., et al. Genes for de novo biosynthesis of omega-3 polyunsaturated fatty acids are widespread in animals. Science Advances. 4 (5), (2018).
- Hillyer, K. E., Dias, D., Lutz, A., Roessner, U., Davy, S. K. 13C metabolomics reveals widespread change in carbon fate during coral bleaching. Metabolomics. 14 (1), 12(2018).
- Hillyer, K. E., Dias, D. A., Lutz, A., Roessner, U., Davy, S. K. Mapping carbon fate during bleaching in a model cnidarian symbiosis: the application of 13C metabolomics. New Phytologist. 214 (4), 1551-1562 (2017).
- Burriesci, M. S., Raab, T. K., Pringle, J. R. Evidence that glucose is the major transferred metabolite in dinoflagellate-cnidarian symbiosis. Journal of Experimental Biology. 215 (19), 3467-3477 (2012).
- Thurber, R. V., et al. Unified methods in collecting, preserving, and archiving coral bleaching and restoration specimens to increase sample utility and interdisciplinary collaboration. PeerJ. 10, 14176(2022).
- Grottoli, A. G., et al. Increasing comparability among coral bleaching experiments. Ecological Applications. 31 (4), 02262(2020).
- Mushtaq, M. Y., Choi, Y. H., Verpoorte, R., Wilson, E. G. Extraction for metabolomics: access to the metabolome. Phytochemical Analysis. 25 (4), 291-306 (2014).
- Bradford, M. M. A rapid and sensitive method for the quantitation of microgram quantities of protein utilizing the principle of protein-dye binding. Analytical Biochemistry. 72 (1), 248-254 (1976).
- Peterson, G. L., et al. A simplification of the protein assay method of Lowry et al. which is more generally applicable. Analytical Biochemistry. 83 (2), 346-356 (1977).
- Lowry, O. H., Rosebrough, N. J., Farr, A. L., Randall, R. J. Protein measurement with the Folin phenol reagent. Journal of Biological Chemistry. 193 (1), 265-275 (1951).
- Zamer, W. E., Shick, J. M., Tapley, D. W. Protein measurement and energetic considerations: Comparisons of biochemical and stoichiometric methods using bovine serum albumin and protein isolated from sea anemones. Limnology and Oceanography. 34 (1), 256-263 (1989).
- Smart, K. F., Aggio, R. B., Van Houtte, J. R., Villas-Boas, S. G. Analytical platform for metabolome analysis of microbial cells using methyl chloroformate derivatization followed by gas chromatography-mass spectrometry. Nature Protocols. 5 (10), 1709-1729 (2010).
- Pang, Z., et al. Using MetaboAnalyst 5.0 for LC-HRMS spectra processing, multi-omics integration and covariate adjustment of global metabolomics data. Nature Protocols. 17 (8), 1735-1761 (2022).
- Tibshirani, R., Walther, G., Hastie, T. Estimating the number of clusters in a data set via the gap statistic. Journal of the Royal Statistical Society: Series B (Statistical Methodology). 63 (2), 411-423 (2001).
- Chen, W. -N., et al. Diel rhythmicity of lipid-body formation in a coral-Symbiodinium endosymbiosis). Coral Reefs. 31 (2), 521-534 (2012).
- Imbs, A. Fatty acids and other lipids of corals: composition, distribution, and biosynthesis. Russian Journal of Marine Biology. 39 (3), 153-168 (2013).
- Rosset, S., et al. Lipidome analysis of Symbiodiniaceae reveals possible mechanisms of heat stress tolerance in reef coral symbionts. Coral Reefs. 38 (6), 1241-1253 (2019).
- Carreón-Palau, L., Parrish, C. C., Del Angel-Rodriguez, J. A., Perez-Espana, H. Seasonal shifts in fatty acids and sterols in sponges, corals, and bivalves, in a southern Gulf of Mexico coral reef under river influence. Coral Reefs. 40 (2), 571-593 (2021).
- Imbs, A. B., Dang, L. T. Seasonal dynamics of fatty acid biomarkers in the soft coral Sinularia flexibilis, a common species of Indo-Pacific coral reefs. Biochemical Systematics and Ecology. 96, 104246(2021).
- Oku, H., Yamashiro, H., Onaga, K., Sakai, K., Iwasaki, H. Seasonal changes in the content and composition of lipids in the coral Goniastrea aspera. Coral Reefs. 22 (1), 83-85 (2003).
- Weis, V. M. Cell biology of coral symbiosis: foundational study can inform solutions to the coral reef crisis. Integrative and Comparative Biology. 59 (4), 845-855 (2019).
- Oakley, C., Davy, S. Cell biology of coral bleaching. Coral Bleaching. van Oppen, M., Lough, J. , Springer. Cham, Switzerland. 189-211 (2018).
- Lu, W., et al. Metabolite measurement: Pitfalls to avoid and practices to follow. Annual Review of Biochemistry. 86, 277-304 (2017).
- Lawson, C. A., et al. Heat stress decreases the diversity, abundance and functional potential of coral gas emissions. Global Change Biology. 27 (4), 879-891 (2021).
- Olander, A., et al. Comparative volatilomics of coral endosymbionts from one-and comprehensive two-dimensional gas chromatography approaches. Marine Biology. 168 (5), 76(2021).
- Wuerz, M., et al. Symbiosis induces unique volatile profiles in the model cnidarian Aiptasia. Journal of Experimental Biology. 225 (19), (2022).
Access restricted. Please log in or start a trial to view this content.
Reimpresiones y Permisos
Solicitar permiso para reutilizar el texto o las figuras de este JoVE artículos
Solicitar permisoExplorar más artículos
This article has been published
Video Coming Soon
ACERCA DE JoVE
Copyright © 2025 MyJoVE Corporation. Todos los derechos reservados