Se requiere una suscripción a JoVE para ver este contenido. Inicie sesión o comience su prueba gratuita.
Method Article
Método de bioimpresión de alto rendimiento para modelar la permeabilidad vascular en placas estándar de seis pocillos con flexibilidad de tamaño y patrón
En este artículo
Resumen
Presentamos un protocolo para la producción de alto rendimiento de canales vasculares con tamaños flexibles y patrones deseados en una placa estándar de seis pocillos utilizando tecnología de bioimpresión 3D, conocida como vasos en una placa (VOP). Esta plataforma tiene el potencial de avanzar en el desarrollo de terapias para los trastornos asociados con el endotelio comprometido.
Resumen
La permeabilidad vascular es un factor clave en el desarrollo de terapias para los trastornos asociados con el endotelio comprometido, como la disfunción endotelial en las arterias coronarias y el deterioro de la función de la barrera hematoencefálica. Las técnicas de fabricación existentes no replican adecuadamente la variación geométrica de las redes vasculares en el cuerpo humano, lo que influye sustancialmente en la progresión de la enfermedad; Además, estas técnicas a menudo implican procedimientos de fabricación de varios pasos que dificultan la producción de alto rendimiento necesaria para las pruebas farmacológicas. Este artículo presenta un protocolo de bioimpresión para crear múltiples tejidos vasculares con los patrones y tamaños deseados directamente en placas estándar de seis pocillos, superando los desafíos existentes de resolución y productividad en la tecnología de bioimpresión. Se estableció un enfoque de fabricación simplificado para construir seis canales huecos y perfusibles dentro de un hidrogel, que posteriormente se recubrieron con células endoteliales de la vena umbilical humana para formar un endotelio funcional y maduro. La naturaleza controlada por ordenador de la bioimpresión 3D garantiza una alta reproducibilidad y requiere menos pasos de fabricación manual que los métodos tradicionales. Esto pone de manifiesto el potencial de VOP como plataforma eficiente y de alto rendimiento para modelar la permeabilidad vascular y avanzar en el descubrimiento de fármacos.
Introducción
La red vascular en todo el cuerpo humano funciona como una barrera de transporte crucial al regular dinámicamente el intercambio de moléculas y células entre la sangre y los tejidos circundantes. Esta regulación es esencial para prevenir el edema tisular y permitir el intercambio selectivo de nutrientes y células, apoyando así el metabolismo y la homeostasis de los tejidos1. La alteración de la permeabilidad endotelial, un factor en muchas condiciones de salud, afecta tanto a la gravedad de la enfermedad como a la eficacia del tratamiento2. El endotelio vascular actúa como una barrera selectiva, facilitando la transferencia entre vasos, tejidos y órganos. Esta regulación involucra varios mecanismos, como el filtrado básico de solutos y moléculas pequeñas, la disrupción intencional de la barrera vascular y la influencia de moléculas como prostaglandinas y factores de crecimiento en los niveles de permeabilidad3.
Los factores clave en esta regulación incluyen las uniones de células endoteliales, la migración de leucocitos y la funcionalidad de la barrera hematoencefálica4. Dada su complejidad, el proceso varía en diferentes entornos, involucrando varios tipos de vasos sanguíneos y utilizando distintas vías anatómicas. Comprender los fundamentos biológicos de la permeabilidad vascular es crucial para diseñar enfoques terapéuticos para tratar las afecciones asociadas con la permeabilidad vascular anormal. Mantener la permeabilidad vascular es crucial para la salud del sistema vascular y los tejidos circundantes; En consecuencia, el deterioro de esta función conduce a la disfunción endotelial, un estado en el que el endotelio pierde su funcionalidad normal.
La disfunción endotelial es precursora de varias enfermedades humanas prevalentes, como la hipertensión, la enfermedad de las arterias coronarias, la diabetes y el cáncer 5,6,7. Esta afección puede presentarse de varias maneras, incluyendo una disminución de la vasodilatación, un aumento de la permeabilidad de los vasos y una tendencia hacia un estado proinflamatorio. Este estado patológico es la etapa más temprana de varios problemas cardiovasculares críticos, como la enfermedad de las arterias coronarias, el accidente cerebrovascular y la enfermedad arterial periférica8, que continúan siendo las principales causas de mortalidad en los Estados Unidos1. La disfunción endotelial afecta a la salud cardiovascular, así como a la barrera hematoencefálica (BHE) y desempeña un papel importante en la progresión de diversos trastornos neurológicos. La disfunción puede aumentar la permeabilidad de la BBB, permitiendo así que las toxinas, los patógenos y las células inmunitarias se infiltren en el sistema nervioso central y contribuyan a trastornos neurológicos como el accidente cerebrovascular, la enfermedad de Alzheimer, la esclerosis múltiple y las infeccionescerebrales.
La disfunción endotelial en la diabetes se caracteriza por el compromiso de la capacidad del endotelio para regular el tono vascular y producir mediadores vasodilatadores, como el óxido nítrico, lo que conduce a una vasodilatación alterada10. Esta condición se ve exacerbada por vías inducidas por la hiperglucemia, como la activación de la proteína quinasa C y el estrés oxidativo, contribuyendo significativamente a la progresión de la enfermedad vascular diabética11. Además, se ha descubierto que un entorno inflamatorio mejora la adhesión de las células tumorales a las células endoteliales microvasculares del cerebro, mientras que se ha informado que un endotelio permeable es un factor importante en la metástasis del cáncer12,13. Se ha descubierto que la geometría de los vasos sanguíneos influye directamente en la metástasis del cáncer cerebral. Las células tumorales se adhieren preferentemente a las áreas de mayor curvatura de los vasos sanguíneos7. Este hallazgo subraya la importancia de la geometría vascular en la metástasis del cáncer. Más importante aún, en condiciones como la fibrosis y el cáncer, la alteración de la función de la barrera endotelial no solo desempeña un papel en el desarrollo de la enfermedad, sino que también dificulta la efectividad del tratamiento al dificultar la administración adecuada de medicamentos14. La investigación sobre la permeabilidad vascular es crucial para avanzar en el tratamiento de las enfermedades cardiovasculares y ofrecer información sobre el manejo de otras enfermedades que implican una función vascular comprometida.
Dado el papel crucial de la permeabilidad vascular en la salud y la enfermedad, una considerable cantidad de investigación se ha centrado en examinar la naturaleza selectiva de la barrera endotelial para el desarrollo terapéutico mediante el uso de modelos animales, junto con plataformas tradicionales de pruebas in vitro en 2D y 3D. Sin embargo, los modelos animales tienen limitaciones debido a las diferencias específicas de cada especie y a cuestiones éticas, así como a los altos costos15,16. Por ejemplo, Pfizer, en 2004, declaró que durante los 10 años anteriores, había gastado más de 2.000 millones de dólares en desarrollos de fármacos que mostraban efectos prometedores en modelos animales, pero que finalmente fracasaronen las etapas avanzadas de pruebas en humanos. Además, los modelos 2D tradicionales no imitan con precisión la arquitectura tridimensional (3D) y la compleja estructura geométrica de los canales vasculares.
Con los avances en las tecnologías de biofabricación, se han realizado grandes esfuerzos para fabricar canales vasculares mientras se recapitula la arquitectura 3D. Los canales vasculares a microescala se pueden fabricar de manera efectiva dentro de chips microfluídicos mediante el uso de litografía blanda, lo que ofrece una ventaja del análisis en tiempo real18,19. Se pueden utilizar métodos alternativos, como la fundición en hidrogel o el envoltorio de láminas de celdas alrededor de un molde o mandril, para crear estructuras tubulares independientes con el diámetro deseado20,21. Sin embargo, estos métodos tienen limitaciones; Por ejemplo, los chips microfluídicos están restringidos a configuraciones de microcanales, y la fundición de hidrogel alrededor de un molde no replica eficazmente múltiples geometrías.
Con la aparición de la tecnología de bioimpresión3D 22, se ha hecho posible replicar geometrías complejas mediante el depósito preciso de diversos materiales de hidrogel basados en matriz extracelular (ECM)23,24. Algunos métodos de bioimpresión, como los que utilizan boquillas dispuestas concéntricamente, por ejemplo, coaxial y triaxial25,26, no pueden crear tubos bifurcados; Sin embargo, las estructuras complejas se pueden lograr con métodos de patrones de sacrificio27. No se ha demostrado que ninguno de estos métodos de bioimpresión permita un modelado in vitro de alto rendimiento, un requisito crucial para la investigación farmacológica en el descubrimiento de fármacos. En este trabajo, presentamos un método para fabricar eficientemente canales vasculares endotelizados con un control eficiente sobre las dimensiones.
Establecimos un enfoque sencillo utilizando placas de seis pocillos disponibles en el mercado, combinadas con un método de patrón de sacrificio en el que una bioimpresora fabrica canales vasculares de los tamaños y patrones deseados dentro de un hidrogel ECM. Se sembraron células endoteliales de la vena umbilical humana (HUVEC) para endotelizar estos canales y evaluar la funcionalidad del endotelio a través de un ensayo de permeabilidad. Este diseño permite la perfusión sin bomba mediante la creación de depósitos de medios a ambos lados del canal y utiliza el flujo impulsado por la gravedad con la ayuda de un balancín 2D de uso común para imitar la cultura dinámica. Este enfoque elimina la necesidad de bombas peristálticas y facilita la escalabilidad de esta plataforma para aplicaciones de alto rendimiento. La naturaleza controlada por ordenador de la tecnología de bioimpresión 3D también agiliza el proceso de fabricación, disminuyendo así la probabilidad de errores durante la fabricación. El modelo VOP se muestra prometedor como una herramienta valiosa para las pruebas farmacológicas en el descubrimiento de fármacos.
Protocolo
1. Generación de código G para la bioimpresora
- Para generar y visualizar la ruta de impresión, visite una herramienta de simulación de código G en línea (por ejemplo, NCviewer).
- Haga clic en el icono Nuevo archivo en la interfaz para crear un nuevo archivo de código G.
- Genere una ruta de impresión escribiendo manualmente los comandos de código G para el canal de sacrificio y la cámara de silicio. Utilice las dimensiones de una placa estándar de seis pocillos como referencia para crear la geometría.
NOTA: El código G utilizado aquí se basa en el código de control numérico por computadora (CNC). Las funciones de cada comando se proporcionan en la Tabla Suplementaria S1. Se seleccionó el formato de placa de seis pocillos debido a su compatibilidad con los lectores de microplacas comerciales y las configuraciones de microscopía y su capacidad para acomodar volúmenes adecuados de medio para apoyar la maduración del endotelio, minimizando así la necesidad de cambios frecuentes de medio. Este protocolo de fabricación también se puede adaptar para su uso con otras placas de pocillos estándar. - Una vez completado el código G, haga clic en el icono Guardar archivo en la interfaz para descargar el archivo con una extensión .nc.
NOTA: Se puede utilizar cualquier otro algoritmo de generación de código G disponible para generar las rutas de impresión. La geometría del canal vascular se puede manipular en este código G.
2. Preparación de tintas de sacrificio y de cámara de silicona
NOTA: Las fuentes de todos los materiales utilizados en este protocolo se enumeran en la Tabla de Materiales.
- Combine dos tipos de polímeros de silicona, SE1700 y polidimetilsiloxano (PDMS), en una proporción de 10:2. Agregue el agente de curado de cada polímero en una proporción de 10:1, polímero a agente de curado.
- Utilice un mezclador planetario para mezclar y desgasificar completamente la mezcla de polímeros a 2.000 rpm.
- Con una espátula, transfiera el polímero de silicona mezclado a una jeringa desechable de 10 ml. Centrifugar la jeringa cargada a 400 × g durante 3 min a 5 °C para garantizar una consistencia uniforme y evitar burbujas durante la impresión.
NOTA: La tinta de la cámara debe usarse dentro de las 2 horas posteriores a la adición de los agentes de curado para garantizar una calidad de impresión óptima. Guarde la jeringa a 5 °C mientras la prepara para la impresión. Este proceso ayuda a ralentizar el curado de la tinta, que de otro modo podría alterar los parámetros de impresión. - Pesar Pluronic F-127 (PF127) para preparar una solución madre al 40% (p/v) de PF127 en agua destilada.
- Mezclar la solución PF127 en una batidora planetaria durante 3 min a 400 × g para lograr la homogeneidad. Mantenga la mezcla homogeneizada a 4 °C para la disolución completa de PF127.
- Prepare una solución madre de trombina de 1.000 unidades/mL en solución salina tamponada con fosfato (DPBS) de Dulbecco.
NOTA: Almacene la solución madre de trombina en alícuotas de 100 μL para evitar ciclos repetidos de congelación y descongelación. Las alícuotas deben almacenarse a -20 °C durante no más de 6 meses. - Antes de imprimir, prepare la tinta de sacrificio mezclando trombina en una dilución 1:10 con PF127 hasta una concentración de trabajo final de 36% (p/v) para PF127 y 100 unidades/mL para trombina. Para preparar 1 ml de tinta de sacrificio, mezcle 100 μl de solución madre de trombina con 900 μl de solución madre PF127.
NOTA: Al preparar la tinta de sacrificio para imprimir una sola plancha, un volumen total de 1 mL es más que suficiente.
3. Proceso de fabricación
- Antes de comenzar el proceso de fabricación, trate una placa de seis pocillos con plasma de oxígeno (O2) a una potencia de 100 vatios durante 1 minuto.
- Siga el procedimiento descrito en la sección 2 para preparar tanto las tintas de sacrificio como las de silicona, asegurándose de que las tintas estén libres de burbujas y se mezclen homogéneamente para una impresión uniforme. Cargue con cuidado las tintas en el cabezal de impresión de la bioimpresora. Ajuste la temperatura del cabezal de la bioimpresora a 37 °C para la tinta de sacrificio y a 5 °C para la tinta de silicona.
- Coloque una boquilla cónica de rosca doble de doble tornillo de 22 G en la jeringa de silicona. Para la tinta de sacrificio, elija el tamaño de la boquilla de acuerdo con el diámetro de canal deseado.
NOTA: Aquí, demostramos tres tamaños de boquillas: 18 G, 20 G y 22 G. Los parámetros de impresión óptimos, incluida la presión de impresión y la velocidad del cabezal de impresión, se describen en la Tabla 1. - Cargue el código G deseado y pulse la función servo ready en la interfaz de software de la bioimpresora durante 3 s. Coloque la placa en la plataforma en el punto de inicio del código G y haga clic en iniciar para iniciar el proceso de impresión.
NOTA: Normalmente, la fabricación de una placa que contiene seis cámaras requiere aproximadamente 1 h y 10 min. El paso 3.4, que implica la carga y ejecución del código G, está sujeto a variaciones en función de la bioimpresora específica utilizada. Asegúrese de que se mantengan las condiciones estériles mientras se utiliza la bioimpresora para evitar la contaminación. - Coloque una tapa sobre la placa y transfiera la placa a una incubadora de CO2 humidificada a 37 °C durante 72 h para curar las cámaras de silicona.
NOTA: Aunque el curado del silicona puede ocurrir a un ritmo más lento dentro de la incubadora, la placa no debe colocarse dentro de un horno seco.
4. Preparación de hidrogel e inclusión de canales
- Prepare un tubo cónico de 50 mL que contenga 20 mL de 1x PBS. Coloque 0,01 g de fenil-2,4,6-trimetilbenzoilfosfinato de litio (LAP) en el tubo cónico para hacer una solución de LAP al 0,05% (p/v). Vórdelo hasta que el polvo se disuelva por completo.
NOTA: Envuelva el tubo cónico en papel de aluminio para evitar la exposición a la luz. Almacene la solución madre de LAP a 4 °C. - Añadir 3 g de metacrilato de gelatina (GelMA) y 0,2 g de fibrinógeno a 20 mL de solución de LAP para conseguir una concentración final de 15% de GelMA y 1% de fibrinógeno (denominado GelFib). Coloque la mezcla en un baño de agua a 37 °C y mezcle periódicamente en vórtice hasta que la solución se disuelva por completo.
- Después de la fabricación, como se describe en la Sección 3, agregue 300 μL de GelFib precalentado en cada cámara de hidrogel para incrustar el patrón de sacrificio. Reticulación rápida del GelMA con luz ultravioleta (UV) a una longitud de onda de 405 nm con una intensidad de 85 mW/cm2 durante 120 s. Repita este procedimiento para todos los demás pozos.
NOTA: El fibrinógeno se entrecruza rápidamente al entrar en contacto con el patrón de sacrificio que contiene trombina. Recomendamos agregar hidrogel y realizar la reticulación UV individualmente para cada pocillo para evitar la gelificación no deseada de GelMA a temperatura ambiente. Además, se deben mantener condiciones estériles para evitar la contaminación durante el proceso de curado UV. - Agregue 1 mL de DPBS a cada lado del canal vascular en cada pocillo y mantenga la placa a 4 °C durante 15 min para licuar el PF127.
- Después de 15 minutos, succione el DPBS y repita el paso 4.5 3 veces para completar el lavado de PF127.
- Antes de introducir las células en los canales, perfunda DMEM F12 que contiene un 1% de Matrigel durante 30 minutos a través de los canales para mejorar la adhesión celular.
5. Cultura HUVEC
- Precaliente el medio de crecimiento de células endoteliales (ECGM) en un baño de agua a 37 °C durante 30 min.
- Mientras tanto, recupere un vial de HUVEC criopreservados del tanque de nitrógeno, afloje suavemente la tapa del vial y luego vuelva a apretarla para liberar nitrógeno de las roscas. Descongele inmediatamente las células sumergiendo el vial en un baño de agua a 37 °C durante 2 min, asegurándose de que quede una pequeña cantidad de hielo dentro del vial. Enjuague el vial con etanol al 70% para evitar la contaminación.
NOTA: Use gafas de seguridad cuando recupere celdas del tanque de nitrógeno. La tapa del vial debe mantenerse por encima del nivel del agua durante este proceso. - Prepare un tubo cónico de 15 mL que contenga 5 mL de ECGM precalentado. Con una micropipeta, transfiera con cuidado las células descongeladas del vial al tubo cónico. Para asegurarse de que no queden células, agregue 1 ml de medio fresco precalentado al criovial, enjuague el interior y transfiera las células restantes al tubo cónico.
- Centrifugar el tubo cónico a 200 × g durante 3 min para obtener un pellet de celda. Deseche el sobrenadante, vuelva a suspender las células en 10 mL de medio fresco, transfiera las células a un matraz T75 y coloque el matraz dentro de una incubadora de CO2 humidificada a 37 °C.
NOTA: Este paso es importante para eliminar el dimetilsulfóxido presente en el medio de congelación en el criovial mediante centrifugación. - Refresque el medio cada dos días hasta que las células alcancen el 80-90% de confluencia.
6. Endotelización de canales
- Precaliente ECGM, DPBS, solución neutralizante de tripsina y ácido etilendiaminotetraacético (TE) de tripsina en un baño de agua a 37 °C durante 30 min.
- Con una confluencia del 90%, enjuague las células en un matraz T75 con 10 mL de DPBS, agregue 1 mL de TE al 0,25% al matraz e incube durante 3 min.
- Golpee suavemente los lados del matraz y agregue 5 mL de solución neutralizante de tripsina para neutralizar el TE. Transfiera las células a un tubo cónico de 15 mL. Utilice 5 ml de ECGM fresco para recoger las células restantes y añadirlas al tubo cónico.
- Centrifugar el tubo cónico a 250 × g durante 3 min para recoger el pellet de la célula.
- Deseche el sobrenadante y vuelva a suspender el pellet celular en 1 mL de ECGM fresco. Cuente las células con un hemocitómetro y repita el paso 6.4 para obtener una pastilla de células. Resuspenda 3 millones de células en 90 μL de ECGM fresco.
- Antes de introducir la suspensión celular en el canal, aspire brevemente el canal para despejar el lumen.
NOTA: Evite la succión prolongada del canal para evitar dañar su integridad. - Cargue suavemente el canal con una suspensión de celdas a una densidad de siembra de 0,5 millones de celdas por pocillo. Utilice una micropipeta para añadir ~15 μL de esta suspensión para llenar el canal.
NOTA: La densidad de siembra puede variar dependiendo del tamaño del canal. Esta densidad está optimizada para un canal impreso con una boquilla de 20 G y un diámetro interno de aproximadamente 900 μm. - Coloque la placa plana dentro de la incubadora durante 2 h. Posteriormente, invierta la placa a 180°, manteniéndola en posición plana durante las siguientes 2 h.
- Después de 4 h, lavar el canal con DPBS para eliminar las células no adherentes y muertas. Agregue 2 mL de ECGM fresco a cada pocillo (1 mL a cada lado del canal). Inicie el cultivo dinámico en un balancín con un ángulo de inclinación de 10° y 5 rpm colocando la placa en el balancín con los canales paralelos a la dirección de balanceo. Refresque el medio de crecimiento cada dos días.
NOTA: El cultivo dinámico mejora el intercambio de medios entre los reservorios y los canales y ayuda a que las células proliferen durante la noche.
7. Evaluación de la maduración del endotelio
- Precaliente ECGM y DPBS en un baño de agua a 37 °C durante 30 min y reactivo Cell Counting Kit-8 (CCK8) a temperatura ambiente.
- Prepare una solución de trabajo de CCK8 mezclando 100 μL de reactivo CCK8 con 1 mL de ECGM fresco para cada pocillo. Mientras trabaja para una placa/canal de 6, prepare 600 μL de reactivo CCK8 combinándolo con 6 mL de ECGM fresco.
- Retire el medio de crecimiento por succión y enjuague los canales con DPBS. Agregue 1 mL de solución de trabajo CCK8 a cada pocillo y deje que la placa permanezca plana dentro de la incubadora durante 30 minutos. Después, inicie el cultivo dinámico en un balancín como se describe en el paso 6.9 y continúe este proceso durante las próximas 3 h.
- Después de 3 h, retire el contenido de cada pocillo inclinando la placa hacia un lado y transfiéralos a una nueva placa de seis pocillos. Enjuague los canales con DPBS y agregue medio fresco.
NOTA: Cubra la placa con papel de aluminio hasta la medición de la absorbancia. Mantenga un volumen de reactivo constante en todos los pocillos para garantizar lecturas uniformes. Durante el pipeteo, evite cuidadosamente introducir burbujas de aire, que pueden alterar la precisión de las lecturas de densidad óptica. - Después de agitar suavemente la placa durante 15 s para garantizar una mezcla uniforme de los colores, utilice un lector de microplacas para medir la absorbancia a 450 nm.
- Repita este procedimiento en intervalos de tiempo predefinidos. Calcule la densidad óptica media para cada punto de tiempo y trace una curva de crecimiento en un software de gráficos. Esta curva indica la maduración relativa del endotelio a lo largo del tiempo.
8. Ensayo de permeabilidad
- Retire el medio de un pozo de interés.
NOTA: Para el ensayo de permeabilidad, se recomienda procesar cada pocillo por separado para evitar que otros canales se sequen, lo que podría alterar su permeabilidad vascular. - Prepare 6 mL de solución de 0,1 mg/mL de dextrano conjugado con FITC disolviendo 70 kDa de dextrano FITC en DPBS.
NOTA: Prepare una solución madre de 20 mg/mL de dextrano FITC disolviendo 100 mg de dextrano FITC en 5 mL de DPBS. Después de vorexizar suavemente la solución, alícuota 500 μL en tubos de 1,5 mL para evitar ciclos repetidos de congelación y descongelación. Estas alícuotas pueden almacenarse a -20 °C durante un máximo de 6 meses. Antes de realizar el ensayo, diluya la solución madre hasta una concentración de trabajo de 0,1 mg/ml. - Coloque la placa firmemente en la platina del microscopio y ajuste el aumento del objetivo en el modo de contraste de fase para garantizar una visibilidad clara de la pared del canal en la región de interés, junto con el gel ubicado cerca, dentro del campo de visión.
NOTA: Para una evaluación efectiva de la permeabilidad, intente maximizar el área del gel que rodea la región de interés en el campo de visión; Este aspecto es clave para un seguimiento preciso del transporte de dextrano. - Después de enfocar el área deseada, cambie del contraste de fase al modo de fluorescencia. En la pestaña de adquisición de imágenes , agregue FITC en el canal de campo amplio y adquiera una imagen antes de agregar la solución de dextrano, para calcular la intensidad de fluorescencia de fondo. Luego, agregue 1 mL de solución de trabajo de dextrano FITC a un lado del canal y deje que la solución fluya hacia el otro lado del pozo, impulsada por la diferencia de presión hidrostática.
- Adquiera imágenes a intervalos de tiempo predeterminados, con más frecuencia para los canales con alta permeabilidad y con menos frecuencia para aquellos con menor permeabilidad.
9. Medición de la intensidad de fluorescencia en ImageJ
- En el software de análisis de imágenes ImageJ, mida la intensidad en el punto de tiempo inicial (It1), la intensidad promedio observada en el punto de tiempo posterior (It2) y la intensidad debida al ruido de fondo (Ib), como se describe a continuación. Utilice la ecuación (1) para calcular el coeficiente de permeabilidad (Pd). T1 y T2 se refieren a los puntos de tiempo inicial y posterior de la adquisición de imágenes.
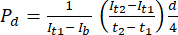 (1)
(1)- Inicie ImageJ y abra la imagen adquirida en el punto de tiempo inicial.
- Establezca la escala en ImageJ. Vaya a Analizar | Establecer escala. Introduzca la escala y la unidad de medida conocidas.
- Seleccione la herramienta rectángulo y dibuje un rectángulo sobre el área del gel donde se requiere la medición de la intensidad de fluorescencia.
- Vaya a Analizar | Establezca Mediciones y asegúrese de que el valor medio de gris esté marcado.
NOTA: Esta opción mide la intensidad media dentro del área seleccionada. Se pueden seleccionar otros parámetros según sea necesario para el análisis dado. - Con el área aún seleccionada, vaya a Analizar | Mida o simplemente presione M. Espere a que se abra una ventana de resultados que muestra la intensidad de fluorescencia media y cualquier otro parámetro seleccionado.
- Realice tres mediciones y calcule el valor medio de la intensidad de fluorescencia en una hoja de cálculo.
- Repita este procedimiento para las imágenes capturadas en el punto de tiempo posterior t2, así como las tomadas antes de la adición de la solución de dextrano para el cálculo de la intensidad de fluorescencia en el punto de tiempo posterior, para determinar la fluorescencia de fondo.
Resultados
La plataforma VOP, con flexibilidad de tamaño y patrón, se fabricó con un sistema de bioimpresión de múltiples cabezales. Los canales, tanto huecos como con capacidad de perfusión, se sembraron con HUVEC para facilitar la endotelización y posteriormente se evaluaron con un ensayo de permeabilidad (Figura 1A). Para demostrar la capacidad de fabricación multiescala de este método, imprimimos tres configuraciones distintas: recta, bifurcada y enrevesad...
Discusión
Aprovechando la precisión, la automatización y la naturaleza controlada por computadora de la tecnología de bioimpresión 3D, establecimos un método simplificado para fabricar canales vasculares en placas estándar de seis pocillos, que se eligieron por su compatibilidad con lectores de microplacas comerciales y configuraciones de imágenes de microscopio. El diseño de la placa puede acomodar canales de varios tamaños y un volumen suficiente de medios para el crecimiento de canales...
Divulgaciones
Los autores declaran no tener intereses financieros contrapuestos.
Agradecimientos
Este trabajo fue apoyado por las subvenciones de la Fundación Nacional de Investigación de Corea (NRF) financiadas por el gobierno de Corea (Ministerio de Ciencia y TIC, MSIT) [No. NRF-2019R1C1C1009606; No. 2020R1A5A8018367; y No. RS-2024-00423107]. Esta investigación fue apoyada por el Programa de Desarrollo de Tecnología Bio y Médica de la NRF financiadas por el MSIT [No. NRF-2022M3A9E4017151 y No. NRF-2022M3A9E4082654]. Este trabajo contó con el apoyo del Programa de Innovación Tecnológica [Nº 20015148] y el Proyecto Alquimista [Nº 20012378] financiado por el Ministerio de Comercio, Industria y Energía (MOTIE, Corea). Este trabajo también contó con el apoyo del Instituto Coreano de Planificación y Evaluación de Tecnología en Alimentos, Agricultura y Silvicultura (IPET) a través del Programa de Tecnologías de Convergencia Agrícola y Alimentaria para el Desarrollo de Recursos Humanos de Investigación, financiado por el Ministerio de Agricultura, Alimentación y Asuntos Rurales (MAFRA) [No. RS-2024-00397026].
Materiales
| Name | Company | Catalog Number | Comments |
| 10 mL Serological Pipette | SPL | SPL 91010 | |
| 10 mL syringe | Shinchang Medical | ||
| 15 mL conical tube | SPL | 50015 | |
| 3D Bioprinter | T&R Biofab | 3DX-Printer | |
| 6-well plate | SPL | 37206 | |
| Biological Safety Cabinets | CHC LAB | PCHC-777A2-04, | |
| Brightfield Inverted Microscopes | Leica | DMi1 | |
| Cell Counting Kit (CCK8) | GlpBio | GK10001 | |
| Cell Counting Kit (CCK8) | GlpBio | GK10001 | |
| Cell Culture Flask 75T | SPL | 70075 | |
| Corning Matrigel Growth Factor Reduced (GFR) Basement Membrane Matrix, LDEV-free, 10 mL | Corning | 354230 | |
| Distilled water | |||
| DMEM/F12 | Gibco | 11320033 | |
| DMSO, Cell Culture Grade | Sigma aldrich | D2438 | |
| Dow-Corning, PDMS-Sylgard 184a Kit | DOW | DC-184 | |
| DOWSIL SE 1700 Clear W/C 1.1 KG Kit | DOW | 2924404 | |
| D-PBS - 1x | Welgene | LB001-01 | |
| Endothelial Cell Growth Medium MV 2 (Ready to use) | Promocell | C-22022 | |
| Eppendorf Micro pipette(1000,200,100,20,10) | eppendorf | ||
| Ethyl Alcohol 99.9% | Duksan | D5 | |
| Excel | Microsoft | ||
| Fibrinogen from bovine plasma | Sigma Aldrich | F8630-1G | |
| FITC Dextran 70 kDa | Sigma Aldrich | 46945-100MG-F | |
| Fluorescent beads (1.0 μm, green) | Sigma Aldrich | L1030-1ML | |
| GelMA-powder (Gelatin methacrylate) 50 g | 3D Materials | 20JT29 | |
| Gibco, Recovery Cell Culture Freezing Medium, 50 mL | Gibco | ||
| HUVECs (Human Umbillical Vein Endothelial Cells) | Promocell | ||
| ImageJ software | NIH | ||
| Incubator | Thermo SCIENTIFIC | Forma STERI-CYCLE i160 CO2 Incubator | |
| Invitrogen, Live/dead viability/cytotoxicity Kit (for mammalian cells) | Thermo Fisher | L3224 | |
| Lithium Phenyl (2,4,6-trimethylbenzoyl) phosphate powder | Tokoyo Chemical Industry CO. | 85073-19-4 | |
| Marienfeld Superior, Counting chamber cover | Marienfeld Superior | ||
| Marienfeld Superior, Hemocytometer, cell counting chamber | Marienfeld Superior | HSU-0650030 | |
| Microcentrifuge | eppendorf | Centrifuge 5920 R | |
| NCViewer.com | |||
| Nitrogen tank | WORTHINGTON INDUSTRIES | LS750 | |
| Omnicure UV Laser | EXCELITAS | SERIES 1500 | |
| Parafilm M | amcor | PM-996 | |
| Penicillin-Streptomycin Solution (100x) | GenDEPOT | CA005-010 | |
| Planetary Mixer | THINKY CORPORATION, japan | ARE-310 | |
| Plasma treatment machine | FEMTO SCIENCE | CUTE-1MPR | |
| Pluronic F-127 | Sigma aldrich | P2443-250G | |
| Pre-made buffer, (P2007-1) 10x PBS | Biosesang | PR4007-100-00 | |
| Reagent storage cabinet | ZIO FILTER TECH | SC2-30F-1306D1-BC | |
| Real time Live cell Imaging Microscope | Carl ZEISS | ||
| Refrigerator | SAMSUNG | RT50K6035SL | |
| ROCKER 2D digital | IKA | 4003000 | |
| Scoop-Spatula | CacheBy | SL-SCO7001-EA | |
| sigma,Trypsin-EDTA solition, 0.25% | Sigma aldrich | T4049-100ML | |
| Sodium Dodecyl Sulfate (SDS) | Thermo Fisher scientific | 151-21-3 | |
| Syringe Barrel Tip Cap | FISNAR | 3051806 | |
| Tally counter | Control Company | C23-147-050 | |
| Tapered Nozzle (18 G) | Mushashi | TPND-18G-U | |
| Tapered Nozzle (22 G) | Mushashi | TPND-22G-U | |
| Tapered nozzle 20 G | Musashi | TPND-20G-U | |
| Thrombin from bovine plasma | Sigma Aldrich | T7326-1KU | |
| Timer, 4-channel | ETL | SL.Tim3005 | |
| Trypan Blue Solution 0.4% | Gibco | 15250061 | |
| Trypsin Neutralizing Solution | Promocell | C-41120 | |
| UG 24 mL UG ointment jar | Yamayu | No. 3-53 | |
| UG 58 mL UG ointment jar | Yamayu | No. 3-55 | |
| Water Bath | DAIHAN Scientific | WB-11 | |
| Weight machine | Sartorius | bce2241-1skr |
Referencias
- O'Connor, C., Brady, E., Zheng, Y., Moore, E., Stevens, K. R. Engineering the multiscale complexity of vascular networks. Nat Rev Mater. 7 (9), 702-716 (2022).
- Claesson-Welsh, L., Dejana, E., McDonald, D. M. Permeability of the Endothelial Barrier: Identifying and Reconciling Controversies. Trends Mol Med. 27 (4), 314-331 (2021).
- Claesson-Welsh, L. Vascular permeability-the essentials. Ups J Med Sci. 120 (3), (2015).
- Wautier, J. -. L., Wautier, M. -. P. Vascular Permeability in Diseases. Int. J. Mol. Sci. 23 (7), (2022).
- Higashi, Y., Kihara, Y., Noma, K. Endothelial dysfunction and hypertension in aging. Hypertens Res. 35 (11), (2012).
- Gallo, G., Volpe, M., Savoia, C. Endothelial dysfunction in hypertension: current concepts and clinical implications. Front Med (Lausanne). 8, 798958 (2022).
- Park, W., Lee, J. -. S., Gao, G., Kim, B. S., Cho, D. -. W. 3D bioprinted multilayered cerebrovascular conduits to study cancer extravasation mechanism related with vascular geometry. Nat Commun. 14 (1), 7696 (2023).
- Sun, H. -. J., Wu, Z. -. Y., Nie, X. -. W., Bian, J. -. S. Role of endothelial dysfunction in cardiovascular diseases: the link between inflammation and hydrogen sulfide. Front Pharmacol. 10, 1568 (2020).
- Yuan, Y., Sun, J., Dong, Q., Cui, M. Blood-brain barrier endothelial cells in neurodegenerative diseases: Signals from the "barrier.". Front Neurosci. 17, 1047778 (2023).
- Hadi, H. A., Suwaidi, J. A. Endothelial dysfunction in diabetes mellitus. Vasc Health Risk Manag. 3 (6), 853-876 (2007).
- De Vriese, A. S., Verbeuren, T. J., Van de Voorde, J., Lameire, N. H., Vanhoutte, P. M. Endothelial dysfunction in diabetes. Br J Pharmacol. 130 (5), 963-974 (2000).
- Wang, K., et al. Inflammatory environment promotes the adhesion of tumor cells to brain microvascular endothelial cells. Front Oncol. 11, 691771 (2021).
- Tiwary, S., et al. Metastatic brain tumors disrupt the blood-brain barrier and alter lipid metabolism by inhibiting expression of the endothelial cell fatty acid transporter Mfsd2a. Sci Rep. 8 (1), 8267 (2018).
- Chauhan, V. P., Stylianopoulos, T., Boucher, Y., Jain, R. K. Delivery of molecular and nanoscale medicine to tumors: transport barriers and strategies. Annu Rev Chem Biomol Eng. 2 (1), 281-298 (2011).
- Van Norman, G. A. Limitations of animal studies for predicting toxicity in clinical trials: Is it time to rethink our current approach. JACC Basic Transl Sci. 4 (7), 845-854 (2019).
- Morgan, S. J., et al. Use of animal models of human disease for nonclinical safety assessment of novel pharmaceuticals. Toxicol Pathol. 41 (3), 508-518 (2013).
- Can Pfizer deliver. MIT Technology Review Available from: https://www.technologyreview.com/2004/02/01/233321/can-pfizer-deliver/ (2004)
- Raasch, M., et al. Microfluidically supported biochip design for culture of endothelial cell layers with improved perfusion conditions. Biofabrication. 7 (1), 015013 (2015).
- Xu, Z., et al. Design and construction of a multi-organ microfluidic chip mimicking the in vivo microenvironment of lung cancer metastasis. ACS Appl Mater Interfaces. 8 (39), 25840-25847 (2016).
- Strobel, H. A., et al. Assembly of tissue-engineered blood vessels with spatially controlled heterogeneities. Tissue Eng Part A. 24 (19-20), 1492-1503 (2018).
- Atchison, L., Zhang, H., Cao, K., Truskey, G. A. A Tissue engineered blood vessel model of Hutchinson-Gilford Progeria Syndrome using human iPSC-derived smooth muscle sells. Sci Rep. 7 (1), 8168 (2017).
- Ronaldson-Bouchard, K., Vunjak-Novakovic, G. Organs-on-a-Chip: A fast track for engineered human tissues in drug development. Cell Stem Cell. 22 (3), 310-324 (2018).
- Gold, K. A., et al. 3D bioprinted multicellular vascular models. Adv Healthc Mater. 10 (21), 2101141 (2021).
- Tabriz, A. G., Hermida, M. A., Leslie, N. R., Shu, W. Three-dimensional bioprinting of complex cell laden alginate hydrogel structures. Biofabrication. 7 (4), 045012 (2015).
- Gao, G., et al. Tissue engineered bio-blood-vessels constructed using a tissue-specific bioink and 3D coaxial cell printing technique: a novel therapy for ischemic disease. Adv. Funct. Mater. 27 (33), 1700798 (2017).
- Cho, W. -. W., Ahn, M., Kim, B. S., Cho, D. -. W. Blood-lymphatic integrated system with heterogeneous melanoma spheroids via in-bath three-dimensional bioprinting for modelling of combinational targeted therapy. Adv Sci (Weinh). 9 (29), 2202093 (2022).
- Kolesky, D. B., et al. 3D bioprinting of vascularized, heterogeneous cell-laden tissue constructs. Adv Mater. 26 (19), 3124-3130 (2014).
- Polacheck, W. J., Kutys, M. L., Tefft, J. B., Chen, C. S. Microfabricated blood vessels for modeling the vascular transport barrier. Nat Protoc. 14 (5), 1425-1454 (2019).
- Li, H., et al. Expanding sacrificially printed microfluidic channel-embedded paper devices for construction of volumetric tissue models in vitro. Biofabrication. 12 (4), 045027 (2020).
- Gao, G., Park, J. Y., Kim, B. S., Jang, J., Cho, D. Coaxial cell printing of freestanding, perfusable, and functional in vitro vascular models for recapitulation of native vascular endothelium pathophysiology. Adv Healthc Mater. 7 (23), 1801102 (2018).
- Farasatkia, A., Kharaziha, M., Ashrafizadeh, F., Salehi, S. Transparent silk/gelatin methacrylate (GelMA) fibrillar film for corneal regeneration. Mater Sci Eng C Mater Biol Appl. 120, 111744 (2021).
- Duong, V. T., et al. Double-layered blood vessels over 3 mm in diameter extruded by the inverse-gravity technique. Biofabrication. 15 (4), 045022 (2023).
- Luo, L., et al. Application of bioactive hydrogels combined with dental pulp stem cells for the repair of large gap peripheral nerve injuries. Bioact Mater. 6 (3), 638-654 (2021).
- Zhu, M., et al. Gelatin methacryloyl and its hydrogels with an exceptional degree of controllability and batch-to-batch consistency. Sci Rep. 9 (1), 6863 (2019).
- Wang, Y., et al. Development of a photo-crosslinking, biodegradable GelMA/PEGDA hydrogel for guided bone regeneration materials. Materials. 11 (8), 1345 (2018).
- Han, Y., et al. Biomimetic injectable hydrogel microspheres with enhanced lubrication and controllable drug release for the treatment of osteoarthritis. Bioact Mater. 6 (10), 3596-3607 (2021).
- Bupphathong, S., et al. Gelatin methacrylate hydrogel for tissue engineering applications-a review on material modifications. Pharmaceuticals. 15 (2), 171 (2022).
- Wu, Z., et al. Microfluidic printing of tunable hollow microfibers for vascular tissue engineering. Adv Mater Technol. 6 (8), 2000683 (2021).
- Medina-Leyte, D. J., Domínguez-Pérez, M., Mercado, I., Villarreal-Molina, M. T., Jacobo-Albavera, L. Use of human umbilical vein endothelial cells (HUVEC) as a model to study cardiovascular disease: a review. Appl. Sci. 10 (3), 938 (2020).
- Khattak, S. F., Bhatia, S. R., Roberts, S. C. Pluronic F127 as a cell encapsulation material: utilization of membrane-stabilizing agents. Tissue Eng. 11 (5-6), 974-983 (2005).
- Jia, W., et al. Direct 3D bioprinting of perfusable vascular constructs using a blend bioink. Biomaterials. 106, 58-68 (2016).
- Kim, S. -. J., et al. Bioprinting methods for fabricating in vitro tubular blood vessel models. Cyborg Bionic Syst. 4, 0043 (2023).
- Maji, S., Lee, M., Lee, J., Lee, J., Lee, H. Development of lumen-based perfusable 3D liver in vitro model using single-step bioprinting with composite bioinks. Mater Today Bio. 21, 100723 (2023).
- Pauty, J., et al. A vascular permeability assay using an in vitro human microvessel model mimicking the inflammatory condition. Nanotheranostics. 1 (1), 103-113 (2017).
- van Duinen, V., et al. 96 perfusable blood vessels to study vascular permeability in vitro. Sci Rep. 7 (1), 18071 (2017).
- Pink, D. B. S., Schulte, W., Parseghian, M. H., Zijlstra, A., Lewis, J. D. Real-time visualization and quantitation of vascular permeability in vivo: implications for drug delivery. PLoS ONE. 7 (3), e33760 (2012).
- Filippi, M., et al. Perfusable biohybrid designs for bioprinted skeletal muscle tissue. AAdv Healthc Mater. 12 (18), 2300151 (2023).
- Zhang, F., Lin, D. S. Y., Rajasekar, S., Sotra, A., Zhang, B. Pump-less platform enables long-term recirculating perfusion of 3D printed tubular tissues. Adv Healthc Mater. 12 (27), 2300423 (2023).
Reimpresiones y Permisos
Solicitar permiso para reutilizar el texto o las figuras de este JoVE artículos
Solicitar permisoExplorar más artículos
This article has been published
Video Coming Soon
ACERCA DE JoVE
Copyright © 2025 MyJoVE Corporation. Todos los derechos reservados