Esecuzione di reazioni al di sotto della temperatura ambiente
Panoramica
Fonte: Laboratorio della Dott.ssa Dana Lashley - College of William and Mary
Dimostrazione di: Matt Smith
Quando si formano nuovi legami nel corso di una reazione chimica, è necessario che le specie coinvolte (atomi o molecole) si avvicinino molto strettamente e si scontrino l'una con l'altra. Le collisioni tra queste specie sono più frequenti ed efficaci quanto maggiore è la velocità con cui queste molecole si muovono. Una regola empirica ampiamente utilizzata, che ha le sue radici nell'equazione di Arrhenius1, afferma che l'aumento della temperatura di 10 K raddoppierà approssimativamente la velocità di una reazione, e l'aumento della temperatura di 20 K quadruplicherà la velocità:
(1) 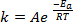
L'equazione (1) si trova spesso nella sua forma logaritmica:
(2) 
dove k è la velocità della reazione chimica, A è il fattore di frequenza (relativo alla frequenza delle collisioni molecolari), Ea è l'energia di attivazione richiesta per la reazione, R è la costante ideale del gas e T è la temperatura alla quale avviesi la reazione.
Una temperatura più elevata significa quindi che una reazione viene completata molto più velocemente. Tuttavia, in alcuni casi è auspicabile effettuare reazioni a basse temperature, nonostante l'effetto di abbassamento sulla velocità della reazione. Alcuni scenari a questo proposito sono elaborati più avanti.
Quando è utile eseguire una reazione al di sotto della temperatura ambiente, i chimici usano bagni di raffreddamento per mantenere una certa temperatura o intervallo di temperatura. Le reazioni vengono raffreddate alla temperatura desiderata posizionando il pallone di reazione all'interno di un bagno di raffreddamento appropriato. I reagenti nella reazione non entrano mai in contatto diretto con le sostanze chimiche nel bagno di raffreddamento. Il bagno di raffreddamento può essere costituito da un singolo componente criogenico (raffreddamento) (come ghiaccio, ghiaccio secco o azoto liquido) o può essere una miscela del componente criogenico con un determinato solvente e/o un sale additivo. Lo scopo del solvente è quello di trasferire efficacemente la temperatura dell'agente di raffreddamento al pallone di reazione e lo scopo dell'additivo è quello di abbassare (o deprimere) il punto di congelamento della miscela. (Si noti che è possibile che una sostanza sia sia un solvente che un additivo.)
Procedura
Configurazione del bagno di raffreddamento
Per un allestimento generale, preparare il bagno di raffreddamento preferito come descritto di seguito e immergere il pallone di reazione nel bagno (Figura 1). Non riempire il recipiente del bagno fino in fondo, ma lasciare abbastanza spazio per consentire l'immersione del pallone di reazione.
Nota: se la reazione è sensibile all'umidità, prestare molta attenzione quando si aggiungono reage
Applicazione e Riepilogo
Quando è utile eseguire una reazione a bassa temperatura?
Per rispondere a questa domanda esaminiamo quattro diverse applicazioni:
Applicazione 1. A volte le reazioni sono troppo vigorose ed esotermiche e la miscela di reazione deve essere raffreddata per evitare fuoriuscite e accumuli di pressione dovuti allo sviluppo di gas. Una reazione altamente esotermica può anche diventare un pericolo per la sicurezza in quanto la miscela di reazione può ...
Riferimenti
- Gordon, A. J., Ford, R. A. The Chemist's Companion - A Handbook of Practical Data, Techniques, and References. Chapter 11 (1973) ISBN: 978-0-471-31590-2.
- Rondeau, R. E. Slush baths. J. Chem. Eng. Data. 11, 124 (1966)
Vai a...
Video da questa raccolta:

Now Playing
Esecuzione di reazioni al di sotto della temperatura ambiente
Organic Chemistry
70.7K Visualizzazioni

Introduzione alla catalisi
Organic Chemistry
34.5K Visualizzazioni

Assemblaggio di un sistema a riflusso per reazioni chimiche riscaldate
Organic Chemistry
167.9K Visualizzazioni

Trasferimento di solventi tramite linea Schlenk
Organic Chemistry
41.7K Visualizzazioni

Degasaggio di liquidi con ciclo freeze-pump-thaw
Organic Chemistry
56.3K Visualizzazioni

Preparazione di reagenti anidri e relativa strumentazione
Organic Chemistry
79.4K Visualizzazioni

Purificazione di composti tramite ricristallizzazione
Organic Chemistry
709.4K Visualizzazioni

Separazione di miscele tramite precipitazione
Organic Chemistry
157.8K Visualizzazioni

Estrazione solido-liquido (lisciviazione)
Organic Chemistry
238.0K Visualizzazioni

Rimozione dei solventi con evaporatore rotante
Organic Chemistry
212.9K Visualizzazioni

Distillazione frazionata
Organic Chemistry
334.7K Visualizzazioni

Preparazione di cristalli per l'analisi mediante diffrazione dei raggi X
Organic Chemistry
32.4K Visualizzazioni

Performing 1D Thin Layer Chromatography
Organic Chemistry
289.9K Visualizzazioni

Cromatografia su colonna
Organic Chemistry
360.5K Visualizzazioni

Spettroscopia a risonanza magnetica nucleare (NMR)
Organic Chemistry
248.4K Visualizzazioni
