このコンテンツを視聴するには、JoVE 購読が必要です。 サインイン又は無料トライアルを申し込む。
Method Article
げっ歯類モデルにおける神経筋接合部伝達を評価するための刺激単繊維筋電図法 (SFEMG)
要約
この研究では、げっ歯類モデルにおける神経筋接合部(NMJ)伝達の in vivo 測定を可能にする洗練された単繊維筋電図(SFEMG)プロトコルを示します。ラット腓腹筋のNMJ伝達変動と機能不全を定量化できるように、SFEMG技術への段階的なアプローチが説明されています。
要約
神経系と筋肉の間の最終的な接続として、神経筋接合部(NMJ)での伝達は正常な運動機能にとって重要です。単線維筋電図検査 (SFEMG) は、臨床的に関連性があり感度の高い技術であり、 随意収縮または神経刺激中の単一筋線維活動電位反応を測定して NMJ 伝達を評価します。NMJ伝送の評価と定量化には、ジッターとブロッキングの2つのパラメーターが含まれます。ジッターとは、連続するシングルファイバー活動電位(SFAP)間のタイミング(遅延)の変動を指します。ブロッキングは、NMJ 送信が SFAP 応答を開始できなかったことを示します。SFEMGは臨床現場では定評があり感度の高い検査ですが、前臨床研究への応用は比較的まれです。このレポートでは、げっ歯類モデルのジッターとブロッキングを定量化するために、刺激SFEMGを実行する際に採用された手順と基準を概説しています。この手法は、健康、老化、および疾患の文脈におけるNMJ機能についての洞察を得るために、前臨床および臨床研究で使用することができます。
概要
シングルファイバー筋電図法(SFEMG)は、1960年代にStålbergとEkstedtによって最初に開発され、主に筋肉疲労を研究するために、個々の筋繊維からの活動電位を特定および分析しました1。SFEMG は、神経筋接合部 (NMJ) 伝達の評価に最も感度の高い臨床手法です 2.SFEMGは、シングルファイバー活動電位(SFAP)3を選択的に記録することによって行われます。NMJの伝達は、老化4,5や重症筋無力症や筋萎縮性側索硬化症6などのさまざまな神経筋障害などの要因によって損なわれる可能性があります。さらに、虚血、温度の変動、神経筋遮断薬の使用などの状態は、NMJ伝達の変動の増加とNMJ障害の発生によって現れる、NMJ伝達の欠損を引き起こす可能性があります2。
SFEMGの記録には、刺激SFEMGと自発SFEMGの2つのアプローチがあります。随意 SFEMG には、自発的活性化中にテストされる筋肉に挿入された同心円針電極を使用して、同じ運動軸索によって供給される 2 つの NMJ からの SFAP を記録することが含まれます7。したがって、自発的なSFEMGは被験者からの協力を必要とし、低閾値運動単位(弱い収縮中に活性化される運動単位)のみを評価できます3。刺激SFEMGは、一対の刺激電極を使用して運動軸索を刺激しながら、SFEMG針電極をテスト対象の筋肉に挿入してSFAPを記録します7。
自発的SFEMGと誘導SFEMGの両方で、ジッターとブロッキングは、NMJ伝送8を評価および定量化するために使用される2つのパラメータである。ジッターは、連続する SFAP 間のタイミング(遅延)の変動を表します。自発的なSFEMGでは、50〜100回の連続放電中のSFAPのペア(同じモーター軸索から供給される)間の遅延差を評価することにより、ジッターが定量化されます。刺激SFEMG中、ジッターは、50〜100回の連続放電中の刺激タイミングとSFAPの開始との間の遅延差を評価することにより定量化されます。ブロッキングは、NMJ送信がSFAP応答をトリガーできなかったことを示し、自発的なSFEMG中のSFAPの各ペアの有無、または刺激されたSFEMG中の各NMJの有無として定量化できます2,7。
SFEMGは臨床現場で確立された感度の高い検査ですが、前臨床研究で適用されることはめったにありません4,5,9,10,11,12,13,14,15,16,17,18 .このレポートでは、前臨床げっ歯類モデルでSFEMG記録を実行および分析するためのアプローチについて概説します。さらに、非脱分極性神経筋遮断薬であるロクロニウムの投与後のNMJ伝達の障害を示すSFEMGに関する代表的な所見を強調する代表的なデータを提示します。
プロトコル
すべてのプロトコルは、ミズーリ大学の動物管理および使用委員会によって定められた規則に従って承認され、実施されました。
1.動物の準備と麻酔投与
- 適切な個人用保護具を着用してください。
- 手順の前に、ラットの体重を測定して、体重ベースの薬と人工呼吸器の設定に適した用量を決定します。
- 3%〜5%の吸入イソフルランで麻酔を誘発します。.適切なレベルの麻酔が確立されたら、ラットを腹臥位に置き、1%〜3%の吸入イソフルランで麻酔を維持します。
- 鉗子で後肢のフットパッドをそっと押して、離脱反応がないことを観察することにより、麻酔の深さの適切性を確認します。
- 体温を37°Cに保ちます。
- 獣医師が認めた石油系の軟膏を目に塗り、乾燥を防ぎます。呼吸数を観察し、鉗子を使用してフットパッドに圧力を加えるときの離脱反応を評価することにより、麻酔の深さを監視します。
- バリカンを使用して評価する後肢を剃ります。適切な脱毛後、粘着テープを使用して、足首を約90°背屈に固定し、膝を伸展させ、股関節を外転させた状態で、研究する手足を配置します。
- 実験全体を通してラットの呼吸と心拍数を継続的に監視します。
注:心拍数の増加は、麻酔薬の深さが不十分であることを示す指標として一般的に使用されます。 - イソフルランを投与してラットを安楽死させます。5%以上の用量で、少なくとも3分間呼吸が止まるまで。斬首による安楽死を確認します。
2. 電極の配置とセットアップ
注:坐骨神経と腓腹筋のNMJ伝達は、筋電図(EMG)システムを使用して評価されます。 資料の表を参照してください。
- 陰極で坐骨神経を近位後肢の領域に刺激するための一対の絶縁された28G単極針を挿入しますが、陽極は仙骨を覆う皮下組織内に近位にあります。
- 坐骨神経や他の隣接する構造への直接的な害を避けるために、刺激電極が坐骨神経のすぐ近くに、または過度に深く配置されていないことを確認してください。
- 反対側の後肢または尾に使い捨ての接地電極を置きます。
- プラチナイリジウム材料で作られた記録面を特徴とする、単繊維筋電図用に特別に設計された27ゲージ、25mmの針電極を右の腓腹筋に慎重に配置します。無菌性を維持するために、各使用前にSFEMG電極がオートクレーブされていることを確認してください。
- SFEMG針電極を腓腹筋線維と平行に挿入して、単一線維活動電位(SFAP)を捕捉します。
- SFEMG針を筋肉内に挿入して操作する間は、筋肉の損傷を避けてください。
3. 刺激型シングルファイバー筋電図法(SFEMG)の手技
- 0.3〜10 mAの強度範囲と0.1 msのパルス持続時間を使用して、10 Hzの周波数で右の坐骨神経に定電流刺激を加えます。
- 1 kHzの低周波フィルターと10kHzの高周波フィルター内でフィルター設定を構成します。ゲインを分割あたり200μVから1000μVに調整して、電位の視覚化を容易にします。掃引速度を分割あたり500μsに設定します。
- 刺激強度を調整して、記録とその後の分析のためにSFAPをトリガーおよび分離します。
- 応答をSFAPとして識別および解析するには、以下の特定の基準が満たされていることを確認してください:ベースラインピークから負の相までの立ち上がり時間が500 μs未満であること、最小振幅(ベースラインピークから負)が少なくとも200 μVであること、および応答が一貫してオールオアナッシングの動作(応答間の安定したサイズと形状)を示すことを確認してください。
注:繰り返し発生する応答は、ノッチや変曲点のない一貫した上向きのフェーズを示すことが不可欠です。最後の基準は、高品質の信号と複数の信号の合計を区別するために重要であることに注意してください。
- 応答をSFAPとして識別および解析するには、以下の特定の基準が満たされていることを確認してください:ベースラインピークから負の相までの立ち上がり時間が500 μs未満であること、最小振幅(ベースラインピークから負)が少なくとも200 μVであること、および応答が一貫してオールオアナッシングの動作(応答間の安定したサイズと形状)を示すことを確認してください。
- 少なくとも 50 回の刺激 (50 から 100 回の刺激) に続く連続放電間の SFAP 遅延 (刺激と SFAP の負のピークの上昇フェーズとの間の時間) の変動性であるジッターを計算し、ブロッキングを評価および定量化します。
注:ブロッキングは、各シナプスでの有無、または単一繊維の活動電位生成をトリガーしない刺激の割合として評価できます。ジッターは、次の式7 を使用して計算されます(ジッターは通常、クリニックの筋電図システムによって自動的に計算されます)。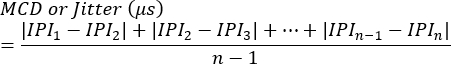
MCD = 連続差の平均値
IPI = インターポテンシャルインターバル - 追加の SFAP 応答に対してこのプロセスを繰り返します。平均して、各動物の 10 個のシナプスを評価してジッターを計算し、その後、動物あたりの平均値を決定します。
- ジッターが4μs未満のSFAPを解析から除外して、直接的な筋肉刺激11によって誘発された可能性のある電位を含めるのを防ぎます。
- 断続的なブロッキングを示す電位を記録する場合は、刺激強度を上げて、SFAPの失敗が最大以下の刺激に起因していないことを確認します。
結果
NMJ伝送障害の状況でジッターとブロッキングの増加を実証するために、ロクロニウムの静脈内投与の有無にかかわらず、刺激SFEMGを実施しました。ロクロニウムは、手術や医療処置中に筋肉麻痺を誘発するために臨床現場で広く使用されている、中作用型の非脱分極性神経筋遮断薬です。これは、NMJ19でニコチン性アセチルコリン受容体に競合的に?...
ディスカッション
SFEMGは、自己免疫疾患、後天性NMJ疾患、および遺伝的形態が疑われる患者の診断検査に一般的に使用されます。SFEMGは、NMJ障害である重症筋無力症20,21の診断に最も感度の高い検査と考えられています。反復神経刺激(RNS)は、臨床診断検査でより一般的に使用される別の方法であり、一連の刺激で末梢神経を刺激し、神経支?...
開示事項
W. David Arnoldは、NMD PharmaとAvidity Biosciencesから研究資金を受け取り、NMD Pharma、Avidity Biosciences、Dyne Therapeutics、Novartis、Design Therapeutics、Catalyst Pharmaceuticalsのコンサルティングを行っています。
謝辞
著者らは、ロクロニウムの投与に関する貴重なアドバイスを提供してくださったNMD PharmaのMartin Brandhøj Skov博士と、計算の支援をいただいたストーニーブルック大学生物医学工学科のArash Karimiに感謝します。この研究は、NIHからWDA(R01AG067758およびR01AG078129)への資金提供によって部分的に支援されました。
資料
| Name | Company | Catalog Number | Comments |
| 27 G Reusable Single Fiber Needle Electrode | Technomed | 202860-000 | singlefiber recording electrode |
| 2 mL Glass Syringe | Kent Scientific Corporation | SOMNO-2ML | |
| Detachable Cable | Technomed | 202845-0000 | to connect the recorder electrode to the electrodiagnostic machine |
| Disposable 2" x 2" disc electrode with leads | Cadwell | 302290-000 | ground electrode |
| disposable monopolar needles 28 G | Technomed | 202270-000 | cathode and anode stimulating electrodes |
| EMG needle cable (Amp/stim switch box) | Cadwell | 190266-200 | to connect monopolar electrodes to electrodiagnostic stimulator |
| Helping Hands alligator clip with iron base | Radio Shack | 64-079 | Maintaining recording electrode placement |
| Isoflurane (250 mL bottle) | Piramal Healthcare | NA | |
| monoject curved tip irrigating syringe | Covidien | 81412012 | utilized for application of electrode gel |
| PhysioSuite Physiological Monitoring System with RightTemp Homeothermic Warming | Kent Scientific Corporation | PS-RT | Includes infrared warming pad, rectal probe, and pad temperature probe |
| Pro trimmer Pet Grooming Kit | Oster | 078577-010-003 | clippers for hair removal |
| Rat Endotracheal Tubes (16 G) | Kent Scientific Corporation | ||
| Rocoronium Bromide | Sigma | PHR2397-500MG | neuromuscular blocker agent |
| Sierra Summit EMG system | Cadwell Industries, Inc., Kennewick, WA | NA | portable electrodiagnostic system |
| SomnoSuite Low-Flow Digital Anesthesia System | Kent Scientific Corporation | SOMNO | Includes anti-spill, anti-vapor bottle top adapter; Y adapter tubing; charcoal scavenging filter |
| Veterinarian petroleum-based ophthalmic ointment | Puralube | 26870 | applied during anesthesia to avoid corneal injury |
参考文献
- Stalberg, E. Propagation velocity in human muscle fibers in situ. Acta Physiol Scand Suppl. 287, 1-112 (1966).
- Stålberg, E., Trontelj, J. V. The study of normal and abnormal neuromuscular transmission with single fibre electromyography. J Neurosci Methods. 74 (2), 145-154 (1997).
- Sanders, D. B., et al. Guidelines for single fiber EMG. Clin Neurophysiol. 130 (8), 1417-1439 (2019).
- Chugh, D., et al. Neuromuscular junction transmission failure is a late phenotype in aging mice. Neurobiol Aging. 86, 182-190 (2020).
- Padilla, C. J., et al. Profiling age-related muscle weakness and wasting: Neuromuscular junction transmission as a driver of age-related physical decline. GeroScience. 43 (3), 1265-1281 (2021).
- Selvan, V. A. Single-fiber EMG: A review. Ann Indian Acad Neurol. 14 (1), 64-67 (2011).
- Sanders, D. B., Kouyoumdjian, J. A., Stålberg, E. V. Single fiber electromyography and measuring jitter with concentric needle electrodes. Muscle Nerve. 66 (2), 118-130 (2022).
- Juel, V. C. Single fiber electromyography. Handb Clin Neurol. 160, 303-310 (2019).
- Chung, T., et al. Evidence for dying-back axonal degeneration in age-associated skeletal muscle decline. Muscle Nerve. 55 (6), 894-901 (2017).
- Iyer, C. C., et al. Follistatin-induced muscle hypertrophy in aged mice improves neuromuscular junction innervation and function. Neurobiol Aging. 104, 32-41 (2021).
- Meekins, G. D., Carter, G. T., Emery, M. J., Weiss, M. D. Axonal degeneration in the trembler-j mouse demonstrated by stimulated single-fiber electromyography. Muscle Nerve. 36 (1), 81-86 (2007).
- Gooch, C. L., Mosier, D. R. Stimulated single fiber electromyography in the mouse: Techniques and normative data. Muscle Nerve. 24 (7), 941-945 (2001).
- Chung, T., Tian, Y., Walston, J., Hoke, A. Increased single-fiber jitter level is associated with reduction in motor function with aging. Am J Phys Med Rehabil. 97 (8), 551-556 (2018).
- Sokolow, S., et al. Impaired neuromuscular transmission and skeletal muscle fiber necrosis in mice lacking na/ca exchanger 3. J Clin Investig. 113 (2), 265-273 (2004).
- Añor, S., et al. Evaluation of jitter by stimulated single-fiber electromyography in normal dogs. J Vet Intern Med. 17 (4), 545-550 (2003).
- Mizrachi, T., et al. NMO-IgG and AQP4 peptide can induce aggravation of eamg and immune-mediated muscle weakness. J Immunol Res. 2018, 5389282 (2018).
- Lin, T. S., Cheng, T. J. Stimulated single-fiber electromyography in the rat. Muscle Nerve. 21 (4), 482-489 (1998).
- Finley, D. B., Wang, X., Graff, J. E., Herr, D. W. Single fiber electromyographic jitter and detection of acute changes in neuromuscular function in young and adult rats. J Pharmacol Toxicol Methods. 59 (2), 108-119 (2009).
- Khan, Z. H., Hajipour, A., Zebardast, J., Alomairi, S. R. Muscle relaxants in anesthesia practice: A narrative review. Arch Anesthesiol Crit Care. 4 (4), 547-552 (2018).
- Padua, L., Caliandro, P., Stålberg, E. A novel approach to the measurement of motor conduction velocity using a single fibre emg electrode. Clin Neurophysiol. 118 (9), 1985-1990 (2007).
- Khoo, A., Hay Mar, H., Borghi, M. V., Catania, S. Electrophysiologic evaluation of myasthenia gravis and its mimics: Real-world experience with single-fiber electromyography. Hosp Pract. 50 (5), 373-378 (2022).
- Nannan, G., et al. A role of lamin a/c in preventing neuromuscular junction decline in mice. J Neurosci. 40 (38), 7203 (2020).
- Alley, D. E., et al. Grip strength cutpoints for the identification of clinically relevant weakness. J Gerontol A Biol Sci Med Sci. 69 (5), 559-566 (2014).
- Juel, V. C. Clinical Neurophysiology of Neuromuscular Junction Disease. Handbook of Clinical Neurology. 161, 291-303 (2019).
- Rich, M. M. The control of neuromuscular transmission in health and disease. Neuroscientist. 12 (2), 134-142 (2006).
- Juel, V. C. Evaluation of neuromuscular junction disorders in the electromyography laboratory. Neurol Clin. 30 (2), 621-639 (2012).
- Arnold, W. D., Clark, B. C. Neuromuscular junction transmission failure in aging and sarcopenia: The nexus of the neurological and muscular systems. Ageing Res Rev. 89, 101966 (2023).
- Kokubun, N. Reference values for concentric needle single fiber EMG. Rinsho Shinkeigaku. 52 (11), 1246-1248 (2012).
- Testelmans, D., et al. Rocuronium exacerbates mechanical ventilation-induced diaphragm dysfunction in rats. Crit Care Med. 34 (12), 3018-3023 (2006).
- Suzuki, K., et al. Intravenous infusion of rocuronium bromide prolongs emergence from propofol anesthesia in rats. PLoS One. 16 (2), e0246858 (2021).
- Stålberg, E., et al. Reference values for jitter recorded by concentric needle electrodes in healthy controls: A multicenter study. Muscle Nerve. 53 (3), 351-362 (2016).
転載および許可
このJoVE論文のテキスト又は図を再利用するための許可を申請します
許可を申請さらに記事を探す
This article has been published
Video Coming Soon
Copyright © 2023 MyJoVE Corporation. All rights reserved