Method Article
단일 단계 및 반자동 Heparin Affinity Chromatography Protocol을 통한 Adeno-associated viral vectors 분리
* 이 저자들은 동등하게 기여했습니다
요약
이 원고는 최적화된 헤파린 기반 친화성 크로마토그래피 방법을 사용하여 아데노 관련 바이러스 벡터의 생성 및 정제를 위한 자세한 프로토콜을 설명합니다. 간단하고 확장 가능하며 비용 효율적인 접근 방식을 제시하여 초원심분리가 필요하지 않습니다. 생성된 벡터는 높은 순도와 생물학적 활성을 나타내며 전임상 연구에서 그 가치를 입증합니다.
초록
아데노 관련 바이러스(AAV)는 in vivo 유전자 전달을 위한 점점 더 가치 있는 벡터가 되었으며 현재 인간 임상 시험을 진행 중입니다. 그러나 AAV를 정제하는 데 일반적으로 사용되는 방법은 염화세슘 또는 요오드릭산올 밀도 구배 초원심분리를 사용합니다. 이러한 방법의 장점에도 불구하고 이러한 방법은 시간이 많이 걸리고 확장성이 제한되며 종종 순도가 낮은 벡터를 생성하게 됩니다. 이러한 제약을 극복하기 위해 연구자들은 크로마토그래피 기술에 관심을 기울이고 있습니다. 여기에서는 AAV 정제를 위한 보편적인 캡처 단계 역할을 하는 최적화된 헤파린 기반 친화성 크로마토그래피 프로토콜을 제시합니다.
이 방법은 헤파란 설페이트 프로테오글리칸에 대한 AAV 혈청형 2(AAV2)의 내적 친화도에 의존합니다. 구체적으로, 이 프로토콜은 원하는 AAV 캡시드 단백질을 AAV2의 단백질과 인코딩하는 플라스미드의 동시 transfection을 수반하며, 이를 통해 두 부모 혈청형의 특성을 결합한 모자이크 AAV 벡터를 생성합니다. 간단히 말해서, 생산자 세포의 용해 후 AAV 입자를 포함하는 혼합물은 표준 고속 단백질 액체 크로마토그래피(FPLC) 시스템을 사용하여 최적화된 단일 단계 헤파린 친화성 크로마토그래피 프로토콜에 따라 직접 정제됩니다. 정제된 AAV 입자는 이후에 농축되고 순도 및 생물학적 활성 측면에서 포괄적인 특성 분석이 거쳐집니다. 이 프로토콜은 초원심분리 및 그래디언트 없이 수행할 수 있는 간단하고 확장 가능한 접근법을 제공하여 깨끗하고 높은 바이러스 역가를 생성합니다.
서문
아데노 관련 바이러스(AAV) 벡터는 현재 유전자 치료 연구에서 가장 유망한 전달 시스템 중 하나로 자리매김하고 있습니다. 1965년1년에 처음 확인된 AAV는 직경이 약 25nm인 이십면체 단백질 캡시드를 가진 작고 외피가 없는 바이러스로, 단일 가닥 DNA 게놈을 가지고 있습니다. AAV는 단순 헤르페스 바이러스 또는 더 빈번하게는 아데노 바이러스와 같은 도우미 바이러스와의 동시 감염에 대한 독특한 의존성으로 인해 Parvoviridae 계열과 Dependoparvovirus 속에 속합니다.
AAV의 4.7 킬로베이스 게놈은 특징적인 T자형 헤어핀 말단을 형성하는 2개의 ITR(Inverted Terminal Repeat)이 측면에 있는 2개의 ORF(Open Reading Frame)로 구성되어 있습니다4. ITR은 AAV 패키징, 복제 및 적분에 중요한 유일한 시스 작용 요소이므로 재조합 AAV(rAAV) 벡터에서 유지되는 유일한 AAV 염기서열입니다. 이 시스템에서는 벡터 생산에 필요한 유전자가 트랜스로 별도로 공급되어 관심 유전자가 바이러스 캡시드 5,6 내부에 패키징될 수 있습니다.
각 바이러스 유전자는 대체 스플라이싱(alternative splicing)과 스타트 코돈(start codon)을 통해 서로 다른 단백질을 코드화합니다. Rep ORF 내에서 4개의 비구조적 단백질(Rep40, Rep52, Rep68 및 Rep78)이 암호화되어 바이러스 DNA 7,8의 복제, 부위 특이적 통합 및 캡슐화에 중요한 역할을 합니다. Cap ORF는 N 말단에서 서로 다른 3개의 구조 단백질(VP1, VP2 및 VP3)이 조립되어 1:1:10 4,9의 비율로 60-mer 바이러스 캡시드를 형성하기 위한 템플릿 역할을 합니다. 또한, 비전통적 CUG 시작 코돈과 함께 Cap 유전자에 중첩된 선택적 ORF는 어셈블리 활성화 단백질(AAP)을 인코딩합니다. 이 핵 단백질은 새로 합성된 캡시드 단백질 VP1-3과 상호 작용하여 캡시드 조립체10,11을 촉진하는 것으로 나타났습니다.
캡시드의 아미노산 서열의 차이는 자연적으로 발생하는 11개의 AAV 혈청형과 인간 및 비인간 영장류 조직에서 분리된 100개 이상의 변이체를 설명합니다 7,12,13. 구조적으로 가변적인 영역의 형태 변화는 서로 다른 균주에서 유래한 캡시드의 뚜렷한 항원 특성과 수용체 결합 특이성을 좌우합니다. 그 결과 서로 다른 포유류 장기에 걸쳐 뚜렷한 조직 영양성(tissue tropisms)과 형질도입 효율(transduction efficiency)이 발생한다14.
rAAV의 초기 생산 방법은 보조 목적으로 아데노바이러스 감염에 의존하였다 15,16,17,18,19. 효율적이고 일반적으로 대규모로 쉽게 생산할 수 있음에도 불구하고 이 감염으로 인해 몇 가지 문제가 발생합니다. 불활성화를 위한 정제 및 열 변성 단계 후에도 아데노바이러스 입자가 AAV 제제에 여전히 존재할 수 있으며, 이는 원치 않는 안전성 문제를 구성할 수 있습니다20. 더욱이, 변성된 아데노바이러스 단백질의 존재는 임상적 사용에 허용되지 않습니다. 다른 생산 전략은 Rep/Cap 및 전이유전자를 표적 세포(21) 또는 바큘로바이러스-곤충 세포 시스템(22)으로 가져오도록 조작된 재조합 헤르페스 단순 헤르페스 바이러스 균주를 이용한다. 이러한 시스템은 확장성 및 GMP 호환성 측면에서 이점을 제공하지만 여전히 유사한 문제에 직면해 있습니다.
rAAV 생산을 위한 삼중 형질주입 방법은 이러한 문제를 쉽게 극복하기 위해 일반적으로 채택되어 왔습니다. 간단히 말해서, rAAV 어셈블리는 다음을 암호화하는 3개의 플라스미드를 가진 세포의 일시적인 transfection에 의존합니다: 1) 야생형 AAV2 게놈(pITR)의 ITR 사이에 패킹된 전이유전자 발현 카세트; 2) 복제 및 virion 조립(pAAV-RC)에 필요한 Rep/Cap 서열; 3) 최소 아데노바이러스 단백질(E1A, E1B, E4 및 E2A)과 도우미 효과(pHelper)에 필요한 아데노바이러스 바이러스 관련 RNA6,20,23. 플라스미드 transfection 방법은 전임상 연구에서 rAAV 생산을 위한 단순성과 유연성을 제공하지만, 이러한 절차는 대규모 생산에 적용할 때 확장성 및 재현성 측면에서 한계가 있습니다. 대안적인 접근법으로, 벡터 구조체와 함께 AAV Rep/Cap 유전자 또는 Rep/Cap을 안정적으로 발현하는 AAV 생산자 세포주(부착 성장 및 현탁 성장 모두)를 사용하여 rAAV 생산을 달성할 수 있습니다. 이러한 시스템에서 아데노바이러스 도우미 유전자는 플라스미드 transfection을 통해 도입됩니다. 이 전략은 세포 배양 공정의 확장성을 향상시키지만 기술적으로 복잡하고 시간이 많이 걸립니다 21,24,25.
두 경우 모두, 생산자 세포는 용해되고 하나 또는 여러 정제 단계를 거칩니다. 현재, rAAV를 정제하는 주요 방법에는 염화 세슘(CsCl) 또는 요오드옥산올 초고속 밀도 구배 원심분리의 사용이 포함되며, 그 후 크로마토그래피 기술에 의한 또는 그렇지 않은 방법이 있습니다26. 바이러스 침전을 위한 원래 정제 방법은 황산암모늄을 사용한 후 CsCl 그래디언트를 통해 2회 또는 3회의 초원심분리를 사용했습니다. 이 공정의 주요 장점은 모든 혈청형을 정제할 수 있는 가능성과 다양한 밀도에 따라 빈 캡시드에서 전체 입자를 물리적으로 분리할 수 있는 기능을 포함합니다. 그러나 이 방법은 정교하고 시간이 많이 걸리며 확장성이 제한되어 종종 수율이 낮고 시료 품질이 낮습니다 27,28,29,30. 더욱이, 생리학적 완충액에 대한 투석은 CsCl이 포유류에 가할 수 있는 독성 효과로 인해 생체 내 연구 전에 종종 필요합니다.
요오딕사놀은 또한 rAAV 벡터를 정제하기 위한 대체 이소삼투압 구배 매체로 사용되었으며, 안전성 및 벡터 효능 관점에서 CsCl에 비해 장점이 있습니다. 그러나 CsCl과 마찬가지로 요오딕사놀 방법은 세포 배양 용해물의 로딩 용량(따라서 rAAV 정제의 확장성)과 관련된 몇 가지 단점이 있으며 시간과 비용이 많이 드는 방법으로 남아 있습니다30,31.
이러한 제약을 극복하기 위해 연구자들은 크로마토그래피 기술에 관심을 돌렸습니다. 이와 관련하여 친화성, 소수성 또는 이온 교환 크로마토그래피 방법을 통합하는 여러 정제 방법이 개발되었습니다. 이러한 방법은 자연 수용체를 포함한 특정 혈청형의 생화학적 특성, 또는 바이러스 입자(32)의 전하 특성에 의존한다. 예를 들어, AAV2, AAV3, AAV6 및 AAV13이 헤파란 설페이트 프로테오글리칸(HSPG)에 바람직하게 결합한다는 발견은 친화성 크로마토그래피 정제에서 밀접하게 관련된 헤파린을 사용할 수 있는 가능성을 열었습니다. 그러나, HSPG에 대한 결합 부위는 혈청형에 따라 다를 수 있으며, 이는 AAV 부착 및 표적 세포의 감염을 매개하는 다양한 방식으로 작용할 수있다 2,33,34,35,36. 반면에 AAV1, AAV5 및 AAV6은 N 결합 시알산(SA)에 결합하는 반면 AAV4는 O 결합 SA 2,14,34를 사용합니다. 동일한 이론적 근거에 따라, SA37에 고도로 농축된 포유류 단백질인 뮤신(mucin)의 사용을 기반으로 rAAV5 정제를 위한 단일 단계 친화성 크로마토그래피 프로토콜도 개발되었습니다. 헤파린 기반 기술과 마찬가지로 이 정제도 생성되는 특정 혈청형에 따라 달라집니다. 헤파린과 뮤신 외에도 A20 단클론 항체 및 카멜리드 단일 도메인 항체(AVB Sepharose 및 POROS CaptureSelect)22,23,38,39,40,41과 같은 다른 리간드가 친화성 크로마토그래피를 위해 탐색되었습니다. 기존의 정제 방법을 개선하기 위한 다른 혁신적인 전략에는 특정 결합 에피토프를 제시하기 위해 rAAV 캡시드에 작은 변형을 도입하는 것이 포함됩니다. 예를 들어, 헥사-히스티딘 태그 또는 비오틴화된 rAAV는 해당 에피토프(각각 니켈 니트릴로트리아세트산 및 아비딘 수지)를 표적으로 하는 리간드를 사용하여 정제할 수 있습니다.42,43,44.
rAAV의 원하는 특성을 넓히기 위한 노력의 일환으로, 연구자들은 캡시드를 혼합하여 바이러스를 교차 드레싱했습니다. 이는 생산 중에 두 개의 별개의 AAV 혈청형에서 캡시드 유전자를 등몰 또는 다른 비율로 공급함으로써 달성되며, 서로 다른 혈청형 34,45,46,47,48,49,50의 캡시드 소단위체의 혼합물로 구성된 캡시드 구조를 생성합니다 . 이전 연구에서는 AAV2와 AAV1(1:1 비율) 및 AAV2와 AAV9(1:1 비율)의 캡시드 단백질을 함께 발현하면 각각 모자이크 rAAV1/2 및 rAAV2/9 벡터가 생성된다는 물리적 증거를 제공합니다(45,46,48). 모자이크 rAAV 생성의 주요 이점은 다양한 AAV 혈청형의 유리한 형질을 통합할 수 있는 능력으로, rAAV 생산 중에 유용한 다른 특성을 유지하면서 전이유전자 발현 및 영양성에서 시너지 효과를 개선합니다. 흥미롭게도, 어떤 모자이크 변이체들은 심지어 부모 바이러스 46,47,49 와서와는 다른 새로운 특성을 나타내기도 한다. AAV2의 헤파린 결합 능력을 이용함으로써, 모자이크 rAAV 벡터는 잠재적으로 AAV2를 유도 진화 및/또는 합리적 설계에 의해 생성된 다른 천연 또는 새로운 AAV 캡시드와 혼합하여 생성 및 정제할 수 있습니다. 그럼에도 불구하고 이전 연구에서는 모자이크 벡터를 조립하려고 할 때 capsid subunit 호환성의 중요성을 강조했습니다. 예를 들어, Rabinowitz와 동료들은 AAV1, AAV2 및 AAV3의 transcapsidation이 모자이크 캡시드의 효율적인 공동 조립으로 이어졌지만, 이러한 혈청형과 AAV4의 교차 드레싱이 안정적인 virions 34,45,47의 생성을 방해한다는 것을 입증했습니다. 또한, AAV1, AAV2 및 AAV3는 AAV5와의 호환성이 낮았는데, 이는 이러한 캡시드를 서로 다른 비율로 혼합할 때 얻어지는 감소된 바이러스 역가를 감안할 때 그렇습니다. 흥미롭게도, 모자이크 rAAV2/5는 헤파린 결합 특성이 감소한 반면, 부모 AAV5와 같은 뮤신 결합 능력은 유지했습니다. 그러나 3:1 비율의 rAAV3/5는 헤파린과 뮤신에 대한 이중 결합을 보존했습니다. 전반적으로, 향상된 transduction, specific tropism 또는 낮은 immunogenicity를 가진 새로운 모자이크 rAAV의 생성은 캡시드 조립 및 수용체 상호 작용에 대한 우리의 이해에 큰 도움이 될 수 있으며, 특정 조합은 여전히 철저한 조사와 최적화가 필요합니다.
본 연구에서는 최적화된 헤파린 친화성 크로마토그래피 방법을 사용하여 rAAV의 생산 및 정제를 위한 단계별 프로토콜을 설명합니다. rAAV는 일시적인 transfection에 의해 생성되며 고속 단백질 액체 크로마토그래피(FPLC) 시스템을 사용하여 정제됩니다. 선택된 정제 분획의 농축 후, 생성된 바이러스 스톡은 역가, 순도, 고유한 물리적 특성 및 in vitro 및 in vivo 생물학적 활성의 측면에서 특성화됩니다. 개념 증명(PoC)으로서, 모자이크 rAAV1/2 및 rAAV2/9 벡터 생성을 위한 이 프로토콜의 개선 사항과 적용 가능성을 입증합니다. 각 혈청형의 선택은 현저하게 다른 트로피즘을 기반으로 했으며, 이는 잠재적으로 모자이크 버전에도 고유한 특성을 부여할 수 있습니다. 중추신경계(CNS)에 대한 전반적인 중간 정도의 영양성을 가진 AAV 혈청형 1은 뉴런과 신경교세포를 transduction할 수 있는 능력을 가지고 있으며(정도는 덜하지만) in vivo 2,7,8에서 전방 및 역행 방향으로 축삭 수송을 겪습니다. 또한, AAV 혈청형 9는 혈액-뇌 장벽을 통과하고 신생아 및 성인 마우스 모두에서 CNS를 표적으로 하는 자연적인 능력 때문에 선택되었습니다51,52. 마지막으로, AAV 혈청형 2는 헤파린에 결합하는 능력을 고려하여 선택되었으며, 이는 친화성 크로마토그래피33을 가능하게 했습니다. 정제된 rAAV1/2 및 rAAV2/9 입자는 두 부모 AAV 혈청형의 특성을 결합하여 CNS 45,46,48,49의 transduction에 적합한 벡터를 구성합니다.
프로토콜
참고: 프로토콜을 요약하는 그림은 그림 1 을 참조하십시오. 이 프로토콜에 사용된 모든 재료, 기기 및 시약에 대한 자세한 내용은 재료 표를 참조하십시오. 세포 및 바이러스와 관련된 모든 작업은 세포주의 유지 관리를 위해 정기적으로 사용되는 것과 분리된 전용 생물안전 캐비닛 및 인큐베이터에서 수행해야 합니다. 배양된 세포 및 바이러스와 접촉하는 장비 및 시약은 멸균 상태여야 합니다. 바이러스에 오염된 유해 시약 및 물질의 폐기는 물질안전보건자료와 각 기관의 환경 보건 및 안전 사무소에서 제공하는 국가 법률 및 지침에 따라 수행되어야 합니다. 2019년 4월 현재, 재조합 또는 합성 핵산 분자와 관련된 연구에 대한 NIH 지침은 모든 AAV 혈청형과 재조합 또는 합성 AAV 구조체를 위험 그룹 1 제제(건강한 성인의 질병과 관련이 없음)로 분류합니다. 이 분류는 전이유전자가 잠재적으로 종양유발 유전자 산물 또는 독소를 암호화하지 않고, 조성물이 도우미 바이러스 없이 생산되는 경우에 적용된다.
동물과 관련된 모든 실험은 2013년 포르투갈 법률(법령 113/2013)로 전환된 실험실 동물의 관리 및 사용에 대한 유럽 연합 공동체 지침(2010/63/EU)에 따라 수행되었습니다. 또한, 동물 시술은 코임브라 대학교 허가 동물 시설의 의과 대학 및 신경 과학 및 세포 생물학 센터의 동물 복지 책임 기관에서 승인했습니다. 연구원들은 실험을 수행하기 위해 포르투갈 당국(Direcção Geral de Alimentação e Veterinária, Lisbon, Portugal)으로부터 적절한 교육(FELASA 인증 과정)과 인증을 받았습니다.
1. 플라스미드 구조체
- maxiprep endotoxin-free 키트에 대한 제조업체의 지침에 따라 다음 플라스미드의 상당한 양의 DNA를 분리하고 정제하십시오: i) pITR: 관심 전달 벡터; ii) pAAV-RC 플라스미드: AAV2 Rep 및 Cap 서열(36)을 포함하는 pRV1; iii) pAAV-RC 플라스미드: AAV1 Rep 및 Cap 서열(36)을 포함하는 pH21; iv) pAAV-RC 플라스미드: AAV2 Rep 및 AAV9 Cap 서열을 포함하는 pAAV2/9n; v) pHelper: pFdelta6, Adenovirus-helper plasmid36.
- 권장되는 효소 제한(enzymatic restrictions)을 수행하여 생성된 플라스미드의 무결성을 스크리닝한다36. ITR53,54의 불안정한 부분 내에서 두 번 절단하는 제한 엔도뉴클레아제인 SmaI로 분해하여 pITR 플라스미드의 무결성을 모니터링합니다.
참고: ITR은 매우 불안정하고 결실에 취약하기 때문에 이러한 부위에서 재결합을 최소화하기 위해 SURE 2 supercompetent cell을 사용하는 것이 좋습니다.
2. 세포 배양
- 배양 인간 배아 신장 293, Dulbecco의 DMEM(Modified Eagle Medium) 고포도당에서 SV40 거대 T 항원(HEK293T) 세포주를 안정적으로 발현하고, 37°C에서 5% CO2가 포함된 가습된 분위기 하에서 5%CO2를 포함하는 가습 분위기에서 발현합니다.
- 멸균 1x 인산염 완충 식염수(PBS), pH 7.4를 사용하여 세포를 세척한 후 0.05% 트립신-에틸렌디아민테트라아세트산(EDTA)을 첨가합니다.
알림: 과도한 수의 통과(최대 20개)를 거친 셀을 사용하지 마십시오. 세포 배양에서 마이코플라스마 오염을 정기적으로 테스트합니다.
3. 일시적인 transfection에 의한 rAAV 생산
- 1일차: 셀 도금
- 각 바이러스 생산에 대해 HEK293T 세포를 transfection 전날 10.5 × 106 cell의 밀도로 22mL의 보충된 배양 배지에 담아 10개의 처리된 배양 접시(직경 15cm)에 플레이트하고 세포가 70%-80% 합류하고 transfection 준비가 될 때까지 24시간 동안 배양합니다.
- 2일차: 폴리에틸렌이민(PEI)을 사용한 세포 형질주입
- 각 바이러스 생산(접시 10.5회에 해당)에 대해 마이크로 원심분리 튜브에 다음 transfection 혼합물을 설정합니다: 54.6 μg의 pITR; pRV1 45.675μg; 45.675 μg의 pH21 또는 pAAV2/9n; 109.2μg의 pFdelta6. 두드려서 섞는다.
- 혼합물을 50mL 원심분리 튜브에 있는 4.557mL의 보충되지 않은 DMEM에 추가합니다. 두드려서 섞는다.
- 1.365mg/mL(pH 7.4)에서 멸균 PEI 용액 1.365mL를 한 방울씩 추가합니다. 두드려서 섞는다. DNA-PEI 복합체가 형성될 수 있도록 실온에서 10분 동안 배양합니다.
- 이 혼합물을 231mL의 예열된 보충 DMEM에 첨가하십시오. 각 접시의 전체 배양 배지를 이 transfection 혼합물 22mL로 교체합니다. 48시간 동안 세포를 배양합니다.
알림: 이 단계는 셀 분리를 방지하기 위해 주의해서 수행해야 합니다.
- 4일차: 세포 채취
- pITR이 형광 리포터를 인코딩할 때 형광 현미경으로 transfection된 세포를 시각화합니다.
- 각 접시의 배지를 50mL 원심분리기 튜브에 모으고 800× g 에서 10분 동안 원심분리합니다. 상층액을 버립니다.
참고: 이 단계는 선택 사항이며 매우 높은 밀도로 인해 분리되었을 수 있는 transfection된 세포를 복구하는 것을 목표로 합니다. - 각 플레이트에 예열된 PBS 10mL를 추가합니다. 셀 스크레이퍼로 셀을 부드럽게 제거하고 3.3.2단계에서 50mL 원심분리기 튜브에 현탁액을 수집합니다.
- 추가 5mL의 PBS로 한 번에 10개의 접시를 세척하고 현탁액을 3.3.3단계에서 50mL 원심분리기 튜브로 옮깁니다. 800 × g 에서 10 분 동안 세포를 펠렛하고 상층액을 버립니다.
- 세포 펠릿을 -80 °C에서 동결합니다.
알림: 세포 펠릿은 몇 달 동안 보관할 수 있습니다(일시 중지 지점).
4. rAAV 추출 및 FPLC 정제
- 5일차: 세포 용해물 준비
- 세포 펠릿을 실온에서 해동합니다. 150mM 염화나트륨(NaCl) 및 20mM Tris, pH 8.0을 포함하는 멸균 완충액 100mL에 10개의 접시에서 수집된 세포를 초순수(유형 I) 물에 재현탁시킵니다. 균일한 현탁액을 보장하기 위해 위아래로 피펫팅하여 현탁액을 혼합합니다.
- 초순수에 10% 데옥시콜산나트륨의 갓 준비된 멸균 용액 12.5mL를 첨가하여 세포 용해를 유도합니다. 위아래로 피펫팅하여 혼합합니다.
알림: 물질안전보건자료(Material Safety Data Sheet) 및 기관의 환경 보건 및 안전 사무소(Environmental Health and Safety Office)에서 제공하는 지침에 따라 데옥시콜산나트륨 및 이와 접촉하는 물질을 폐기하십시오. 이 분말을 취급하는 동안 안면 마스크를 착용하는 것도 권장됩니다. 혼합 후 용액은 점성이 높아집니다. - 이전 혼합물에 27μL의 벤조나제 뉴클레아제를 추가합니다. 샘플이 더 이상 점성이 없을 때까지 위아래로 피펫팅하여 철저히 혼합합니다. 37°C에서 1시간 동안 배양하고 10분마다 소용돌이를 수행합니다.
참고: 이 엔도뉴클레아제는 단백질 분해 활성을 나타내지 않고 모든 형태의 DNA와 RNA를 효율적으로 분해할 수 있습니다. - 3,000× g 의 온도에서 25°C에서 60분 동안 혼합물을 원심분리하여 세포 파편을 제거합니다. 0.45μm 멸균 폴리비닐리덴 디플루오라이드(PVDF) 주사기 필터로 상층액을 여과하고 새 멸균 용기에 옮깁니다.
참고: 이 중요한 단계는 대부분의 세포 파편이 제거되도록 하여 크로마토그래피 컬럼의 막힘을 방지합니다. 분석을 위해 이 혼합물의 작은 부분 표본을 저장합니다(선택적 단계).
- 5일차(계속): rAAV의 헤파린 컬럼 정제
참고: 시료 적용은 시료 펌프 또는 시스템의 일부로 50mL 또는 150mL 슈퍼루프를 사용하여 수행할 수 있습니다. 낮은 온도에서 더 많은 공기가 용해되기 때문에 완충액과 용액(일반적으로 4°C에서 보관)이 FPLC 시스템에서 사용하기 전에 실온에 적응할 수 있는 충분한 시간을 허용하는 것이 중요합니다.- 선택 사항: 시스템을 장기간 보관한 경우 수동 지침 또는 사전 정의된 시스템 현장 청소(시스템 CIP) 방법을 사용하여 시스템과 모든 입구를 새로 준비된 보관 용액(20% 에탄올)으로 채우십시오.
- 수동 지침 또는 사전 정의된 시스템 CIP 방법을 사용하여 멸균 초순수로 액체 흐름 경로를 완전히 세척합니다.
- 1mL의 사전 포장된 헤파린 컬럼을 연결하고, 압력 알람을 설정하고, 1mL/분의 유속으로 5개의 컬럼 부피(CV)의 초순수로 세척합니다.
- 버퍼 트레이의 용액을 초순수에서 유입구 A(초순수에서 100mM NaCl 및 20mM Tris, pH 8의 멸균 용액)로 전환하고 입구 B(시스템 펌프 B)의 경우 완충 B(초순수에서 500mM NaCl 및 20mM Tris, pH 8의 멸균 용액)로 전환합니다. 시스템에 샘플 펌프가 있는 경우 샘플 입구 밸브의 버퍼 입구를 버퍼 A에 놓습니다.
- 시스템 펌프 B를 버퍼 B로 세척하고 나머지 액체 흐름 경로를 버퍼 A로 채웁니다.
알림: 필요한 경우 흐름 경로에서 컬럼을 분리했다가 나중에 다시 연결하십시오. - 샘플 입구 밸브(예: S1)에서 샘플 입구 튜브를 삽입합니다.ample, 4.1.4단계에서 얻은 바이러스 제제가 있는 용기에 넣습니다. (세포 용해물 준비에서). 시료 용액을 사용하여 시료 주입구 S1에서 주입 밸브까지의 흐름 경로를 프라이밍합니다. 또는 50mL 주사기를 사용하여 rAAV가 포함된 샘플로 50mL 또는 150mL 슈퍼루프를 충전합니다.
- 1mL/분의 속도로 완충액 B의 12.5%를 사용하여 총 5개의 CV 부피로 컬럼을 평형화합니다.
- 시료 펌프( 공기 센서를 사용하여 모든 시료 주입 선택) 또는 슈퍼루프를 사용하여 0.5mL/min의 속도로 시료의 총 부피를 컬럼에 적용하고 새 멸균 용기의 배출 포트를 사용하여 플로우스루를 수집합니다.
알림: 과압 방지를 위한 흐름 제어 기능이 활성화되면 컬럼이 막히는 경우 흐름이 자동으로 감소합니다. 유속이 0.5mL/분 미만으로 크게 떨어지면 시료 적용을 중단하고 2-5CV의 완충액 A로 세척한 다음 시료 적용을 재개합니다. - 20CV의 완충액 A로 1mL/분으로 컬럼을 세척하고 배출 포트를 사용하여 플로우스루를 수집합니다.
- 다음 방법으로 1mL/min의 속도로 시료를 용리합니다: i) 5개의 CV에 대해 완충액 B의 50%를 목표로 하는 선형 그래디언트; ii) 5개의 CV 동안 버퍼 B의 90%를 목표로 하는 단계; iii) 5개의 CV 동안 버퍼 B의 100%를 목표로 하는 단계.
- 분획 분취기와 저잔류 미세 원심분리 튜브(2mL)를 사용하여 용출된 시료를 1mL 분획으로 수집하고 -20°C에서 보관합니다.
참고: rAAV 분획은 몇 주(일시 중지 지점) 동안 저장될 수 있습니다. - 5개의 CV에 대해 12.5%의 완충액 B와 1mL/분으로 컬럼을 다시 평형화합니다.
- 버퍼 용액의 주입구를 초순수로 전환하고 5개의 CV에 대해 1mL/분으로 컬럼을 세척합니다.
- 주입구를 초순수에서 20% 에탄올로 전환하고 5개의 CV에 대해 1mL/분으로 컬럼을 세척합니다. 컬럼을 분리하고 4°C에서 보관합니다.
참고: 동일한 rAAV 혈청형 및 전이유전자를 사용하는 경우 다른 주요 세척 및 위생 절차 없이 컬럼을 여러 번 재사용할 수 있습니다. - 수동 지침 또는 사전 정의된 시스템 CIP 방법을 사용하여 20% 에탄올로 액체 흐름 경로를 완전히 세척합니다.
5. 정제된 rAAV의 농도
- 6일차: 집중 단계 1
- 100kDa 분자량 컷오프가 있는 15mL 원심 필터 장치를 사용하여 rAAV를 농축합니다. rAAVs(FPLC 분획 7 - 16)를 포함하는 원하는 분획을 15mL 원심 필터 장치에 로드하고 실온에서 2분 동안 2,000× g 으로 원심분리합니다. 필터 장치의 농축 부피가 약 500μL인지 확인하십시오. 농축된 부피가 500μL를 크게 초과하는 경우 원하는 부피에 도달할 때까지 1분 간격으로 원심분리 단계를 반복합니다.
- 6일차(계속): 버퍼 교환
- rAAV가 들어 있는 원심 필터 장치에 제균 PBS 1mL를 추가합니다. 필터를 위아래로 조심스럽게 피펫팅하여 세척합니다. 최종 부피가 500 μL에 도달할 때까지 1분 간격으로 2,000 × g 으로 원심분리합니다.
- 6일차(계속): 집중 단계 2
- 이전 단계에서 얻은 500μL의 농축된 rAAV를 100kDa 분자량 컷오프가 있는 0.5mL 원심 필터 장치로 옮기고 6,000× g 에서 1분 동안 원심분리합니다. 필요한 경우 최종 부피가 100μL 미만이 될 때까지 원심분리 단계를 반복합니다.
- 6일차(계속): 회복
- 농축된 rAAV를 회수하려면 필터 장치를 새 미세 원심분리기 수집 튜브에 거꾸로 놓습니다. 캡이 중앙을 향하도록 하여 튜브를 마이크로 원심분리기에 놓고 플로우 챔버 내부에서 장기간 회전을 수행하여 농축된 rAAV를 장치에서 마이크로 원심분리기 튜브로 전달합니다. 또는 1,000× g 에서 2분 동안 원심분리합니다.
- 멸균 Pluronic F-68 0.001%(선택 사항)를 보충하십시오.
참고: Pluronic F-68은 미국 식품의약국(FDA)에서 인체 사용을 승인한 비이온성 계면활성제로, 희석 준비, 주사기 로딩 및 전달 장비55,56 중에 사용되는 재료(플라스틱) 표면과의 상호 작용을 방지하여 rAAV의 손실을 완화할 수 있습니다. - rAAV를 저잔류 마이크로 원심분리기 튜브에 분취하고 -80°C(일시 중지 지점)에서 보관합니다.
6. 정제된 rAAV의 정량화
- 6일차(계속): 상용 키트를 사용하고 제조업체의 지침에 따라 실시간 정량적 중합효소 연쇄 반응(RT-qPCR)으로 바이러스 게놈/μL(vg/μL)로 발현되는 rAAV 제제의 역가를 결정합니다.
- rAAV 입자 용액을 DNase I과 함께 37°C에서 20분 동안 배양합니다.
참고: 이 절차는 숙주 세포에서 유래한 유리 게놈 DNA 및 플라스미드 DNA의 분해를 촉진하여 온전한 rAAV 입자 내부의 핵산 서열만 보존되도록 합니다. - 95°C에서 10분 동안 DNase I을 가열 비활성화합니다.
- Lysis Buffer를 추가하고 70°C에서 10분 동안 배양하여 rAAV 입자 단백질의 열 변성을 촉진합니다.
- RT-qPCR로 진행하기 전에 얻은 rAAV 게놈 용액을 희석 완충액에 희석합니다. 키트와 함께 제공된 양성 대조군의 직렬로 희석된 표준물질 세트(2 × 107 vg/μL에서 2 × 102 vg/μL까지)를 준비합니다.
- 12.5 μL의 Taq II 믹스, 0.5 μL의 희석된 프라이머 믹스, 7 μL의 물 및 5 μL의 희석된 rAAV DNA(미지 AAV 샘플 및 6.1.4단계의 표준물질)를 포함하는 반응 혼합물을 수행합니다.
- 95°C에서 2분 동안 1주기(초기 변성), 95°C에서 5초(변성) 동안 40주기, 30초 동안 60°C(어닐링, 확장 및 플레이트 판독) 프로토콜을 사용하여 Real-Time PCR 검출 시스템에서 RT-qPCR을 수행한 후 용융 곡선 분석을 수행합니다.
- rAAV 시료 전처리로 인한 희석 계수를 고려하여 표준 곡선(선형 회귀선)에서 절대 시료 농도를 계산합니다.
참고: 바이러스 게놈 수의 정량화는 AAV2의 ITR 염기서열(키트에서 제공하는 프라이머의 표적 염기서열)의 증폭을 통해 이루어집니다.
- rAAV 입자 용액을 DNase I과 함께 37°C에서 20분 동안 배양합니다.
7. SDS-PAGE, Coomassie 블루 염색 및 웨스턴 블롯
- 6x 샘플 버퍼 (0.5 M Tris-HCl / 0.4 % 도데 실 설페이트 (SDS) pH 6.8, 30 % 글리세롤, 10 % SDS, 0.6 M 디티 오트레이톨 (DTT), 0.012 % 브로 모페놀 블루)를 첨가하고 샘플을 95 ° C에서 5 분 동안 배양하여 각 샘플 (각 FPLC 분획, 플로우 스루, 프리 컬럼 샘플 및 최종 농축 제품의 총 2.3 × 1010 vg)을 변성시키고 샘플을 배양합니다.
- 변성된 샘플(48μL)을 SDS-폴리아크릴아미드 겔(4% 스태킹 및 10% 분해 겔)에 로드하고 단백질 사다리에 인접한 100V에서 70분 동안 전기영동 분리를 수행합니다.
- 단백질 분석
알림: Coomassie blue 염색 또는 western blotting을 수행할 수 있습니다.- 쿠마시 블루 스테인닝
- 단백질 밴드를 시각화하려면 50% 메탄올과 10% 아세트산 빙하에 용해된 0.25% Coomassie blue G250 용액으로 10분 동안 겔을 염색합니다.
- 배경이 낮은 투명한 띠가 보일 때까지 25% 메탄올과 5% 아세트산 빙하를 함유한 용액으로 겔 탈색을 여러 번 수행합니다.
- 적절한 이미징 시스템을 사용하여 이미지를 캡처합니다.
- 웨스턴 블롯
- 표준 프로토콜에 따라 단백질을 PVDF 멤브레인으로 옮깁니다.
- TBS-T(트리스 완충 식염수 0.1% 트윈 20)에 희석한 5% 무지방 우유에 실온에서 1시간 동안 배양하여 멤브레인을 차단합니다.
- 4 °C에서 하룻밤 배양을 위해 다음 기본 항체(차단 용액에 희석)를 사용하십시오: 마우스 monoclonal anti-AAV, VP1, VP2, VP3 항체 (B1, 1:1,000) 또는 마우스 monoclonal anti-AAV, VP1, VP2 항체 (A69, 1:1,000).
- TBS-T에서 3 x 15분 동안 멤브레인을 세척하고 실온에서 2시간 동안 알칼리성 인산가수분해효소 결합 염소 항마우스 2차 항체(1:10,000)로 배양합니다.
- TBS-T에서 3 x 15분 동안 멤브레인을 세척합니다. 향상된 화학형광 기질(ECF)을 추가하고 화학형광 이미징으로 단백질 밴드를 시각화할 수 있습니다.
- 쿠마시 블루 스테인닝
8. 투과 전자 현미경 (TEM)
- rAAV 샘플 한 방울 위에 Formvar-carbon-coated 200 메쉬 그리드를 거꾸로 놓고 1분 동안 가라앉힙니다.
- 물 한 방울로 그리드를 씻고 여과지로 여분의 액체를 말리십시오.
- 1% 우라닐 아세테이트 용액(pH 7)으로 그리드를 1분 동안 음의 염색하여 바이러스 입자를 고정하고 대조합니다.
- 물 한 방울로 그리드를 씻고 여과지로 여분의 액체를 말리십시오.
- 투과 전자 현미경에서 샘플을 검사합니다.
참고: 높은 염 농도는 rAAV가 그리드에 결합하는 데 직접적인 영향을 미칠 수 있으며 결정과 같은 구조의 시각화로 이어질 수 있습니다.
9. 연속 자외선-가시광선 흡수, 정적 광 산란 및 동적 광 산란 분석
- 96웰 정량 플레이트에서 2μL의 rAAV 샘플과 2μL의 PBS를 로드하여 버퍼 블랭크로 사용합니다(중복으로 수행).
- 클라이언트 분석 소프트웨어에서 AAV Quant 애플리케이션을 사용하여 샘플의 이름을 플레이트의 올바른 위치에 배치하고 AAV 혈청형을 선택한 후 Next(다음)를 클릭합니다.
- 96웰 정량 플레이트를 전용 장비에 로드하고 데이터 수집을 위한 플레이트 판독을 진행합니다.
10. In vitro transduction 어세이
- 다양한 세포주를 사용하여 rAAV의 transduction 효율을 신속하게 분석할 수 있습니다.
- 위에서 설명한 대로 10% 소 태아 혈청 및 1% 페니실린-스트렙토마이신이 보충된 DMEM 고포도당을 사용하여 24웰 플레이트(137,500 cells/well 밀도)와 마우스 neuroblastoma-2A(Neuro2a) 세포주에서 24-well 플레이트(137,500 cells/well 밀도)와 마우스 neuroblastoma-2A(Neuro2a) 세포주를 균등하게 파HEK293T종합니다. 세포가 37 % CO2 를 포함하는 가습 된 분위기에서 5 ° C에서 밤새 부착되도록합니다.
- 각 웰에서 컨디셔닝된 매체(24웰 플레이트에서 250μL, 8웰 챔버 슬라이드에서 50μL)를 수집하고 나중에 사용할 수 있도록 4°C에서 보관합니다.
- 다음 rAAV 제제를 각 웰에 추가하고 5%CO2 분위기에서 37°C에서 24시간 동안 세포를 배양합니다.
- FPLC 수집 분획 F2-F16 50μL를 추가하고 24웰 플레이트에 도HEK293T된 세포에 플로우스루를 추가합니다.
- 50 μL의 PBS에 희석된 농축된 rAAV의 총 5.5 × 109 vg를 24웰 플레이트에 도금된 Neuro2a 세포에 추가합니다(세포에 50 μL의 PBS를 추가하여 음성 대조군 웰 포함).
- 25 μL의 PBS에 희석된 농축된 rAAV의 총 2.75 × 109 vg를 8-웰 챔버 슬라이드에 도금된 Neuro2a 세포에 추가합니다(세포에 50 μL의 PBS를 추가하여 음성 제어 조건 포함).
- 이전에 저장된 컨디셔닝된 배지(단계 10.1.2)를 각 웰에 추가하고 24시간 동안 배양합니다.
- 배지를 버리고 PBS로 세포를 2번 세척합니다.
- 37°C로 예열된 PBS에서 4% 자당이 보충된 4% 파라포름알데히드(PFA) 용액을 각 웰에 추가하고 실온에서 20분 동안 배양합니다.
- PBS로 2회 세척하고 이미징이 수행될 때까지(일시 중지 지점) 4°C에서 보관합니다.
- 10x/0.30 대물렌즈가 장착된 도립 형광 현미경 또는 40x/1.4 Oil DIC 대물렌즈가 장착된 도립 공초점 현미경에서 이미지를 획득할 수 있습니다.
- in vivo 환경에 대한 보다 관련성 있고 반영적인 모델을 얻으려면 다음과 같이 primary neuronal cultures를 사용하십시오.
- 이전에 Santos et al.에 의해 설명된 대로 대뇌 피질 뉴런의 1차 배양을 준비합니다.57. 간단히 말해서, 12웰 플레이트에 200,000세포/mL를 파종하고 in vitro 16까지 배양액을 유지합니다.
- 각 웰에서 조절된 매체(100μL)를 수집하고 나중에 사용할 수 있도록 4°C에서 보관합니다.
- 테스트할 rAAV를 각 웰에 추가합니다: 총 2.75 × 109 vg의 농축된 rAAV를 25 μL의 PBS에 희석합니다(음성 대조군 포함: PBS 25 μL). 5%CO2 분위기에서 37°C에서 24시간 동안 배양합니다.
- 이전에 보관된 컨디셔닝된 배지를 추가하고 24시간 동안 배양합니다.
- 각 웰의 매체를 버리고 PBS로 2번 세척합니다.
- 10.1.6단계에서 설명한 대로 PBS에서 4% PFA/4% 자당으로 세포를 고정합니다. PBS로 2번 세탁하세요.
- 실온에서 10분 동안 Alexa Fluor 633과 접합한 5μg/mL의 밀 배아 응집체(WGA)로 각 웰을 배양합니다(선택 단계: 대신 면역세포화학 수행). PBS로 2번 세탁하세요.
- PBS의 0.25% Triton X-100에서 실온에서 5분 동안 배양합니다. PBS로 씻으십시오.
- 실온에서 4',6-diamidino-2-phenylindole(DAPI)과 함께 5분 동안 배양합니다. PBS로 2번 세탁하세요.
- 40x/0.95 대물렌즈가 장착된 도립 형광 현미경 또는 40x/1.4 Oil DIC 대물렌즈가 장착된 도립 형광 현미경에서 이미지를 획득할 수 있습니다.
11. 생체 내 실험
참고: 동물들은 12시간 밝음/어둠 주기로 유지되는 온도 조절실에 수용되었습니다. 음식과 물은 임시로 제공되었습니다. 동물의 고통을 최소화하기 위해 모든 노력을 기울였습니다.
- 소뇌에 입체적 주입
- 기화기에 연결된 챔버에서 산소(0.8L/min)가 있는 상태에서 2% 이소플루란을 흡입하여 9주 된 C57BL/6 동물을 마취합니다.
- 마취된 동물을 입체 장치(35°C로 데워진 패드 위)에 넣고 이소플루란 마스크를 동물의 코에 넣습니다. 이소플루란 수치를 1.3-1.7%로 낮춥니다.
참고: 진행하기 전에 동물이 올바르게 마취되었는지 확인하십시오(양쪽 뒷다리의 굴곡에 대한 반사 상실). - 각막이 건조해지지 않도록 윤활제 눈 연고를 바르고 동물에게 승인된 진통제를 주사합니다.
알림: 모든 후속 단계는 멸균 조건에서 수행해야 합니다. - 동물의 머리 털을 면도하고 수술 부위를 소독한 후 두개골을 노출시키고 10μL 해밀턴 주사기에 연결된 30G의 뭉툭한 끝 주사 바늘 끝을 브레그마 바로 위에 놓습니다(입체 좌표 계산을 위해 브레그마를 0으로 사용).
- 바늘을 원하는 좌표로 이동하고 바늘이 들어갈 두개골에 구멍을 뚫습니다.
참고: 이 연구의 틀에서는 단일 주사가 소뇌 중앙에서 수행되었습니다. - 자동 주입기를 사용하여 PBS에 희석된 총 8 × 109 vg를 포함하는 rAAV 용액 4μL를 0.5μL/min의 주입 속도로 주입합니다. bregma에서 계산 된 다음 좌표를 사용하여 성인 C57BL / 6 마우스의 소뇌 중앙에서 단일 주입을 수행하십시오. 전후 : -6.5 mm; 측면: 0mm; 복부 : -2.9 mm.
알림: 이 좌표는 사용 중인 동물의 마우스 변형, 성별 및 연령에 따라 다를 수 있습니다. - 역류를 최소화하고 바이러스 벡터 확산을 허용하려면 주입이 완료되면 주사기 바늘을 이 좌표에 3분 동안 그대로 둔 다음 천천히 0.3mm 집어넣고 마우스 뇌에서 완전히 제거하기 전에 추가로 2분 동안 제자리에 두십시오.
- 절개 부위를 봉합하고 소독제(예: 10 % 포비돈 요오드)로 청소합니다.
- 동물들을 집 우리로 돌려보내기 전에 마취에서 회복할 수 있도록 하십시오.
- 조직 채취 및 준비
참고: 이 실험에서는 주입 후 12주 후에 형질도입 수준이 관찰되었지만, 주입 후 4주 이내에 동일한 절차를 평가할 수 있습니다.- 자일라진/케타민(체중 8/160mg/kg)의 과다 투여에 대한 복강 내 투여로 동물을 말기 마취합니다.
- 2.5mL/분의 속도로 6분 동안 얼음처럼 차가운 PBS로 동물에게 심혈관 관류한 다음 갓 준비된 얼음처럼 차가운 4% PFA 용액으로 동일한 속도로 10분 동안 관류합니다.
- 절제된 뇌를 실온에서 하룻밤 동안 4% PFA에 후치한 다음 동결 보호를 위해 25% 자당/PBS 용액으로 옮깁니다. 뇌가 가라앉으면(약 48시간 후) -80 °C에서 보관합니다.
- -21°C에서 cryostat를 사용하여 30μm 두께의 연속 시상 절편을 절단합니다. 각 동물에 대해 뇌 반구의 96개 시상 절편을 해부학적 시리즈로 PBS에서 0.05% 아지드화나트륨이 보충된 자유 부동 절편으로 수집합니다. 추가 처리가 될 때까지 4 °C에서 보관하십시오.
- 표준 형광 면역조직화학(immunohistochemistry)
- 동물당 240μm의 거리에서 8개의 시상 섹션을 선택합니다.
- 차단/투과화 용액(PBS에 10% 정상 염소 혈청(NGS)을 함유한 0.1% Triton X-100)에서 자유 부유 섹션을 실온에서 1시간 동안 배양합니다.
- 4 °C에서 닭 다클론 항-GFP 일차 항체(1:1,000)로 절편을 밤새 배양합니다.
- PBS에서 3 x 15분 동안 세척하고 Alexa Fluor 488 fluorophore(1:200)에 접합된 2차 항체 goat polyclonal anti-chicken 항체를 사용하여 실온에서 2시간 동안 절편을 배양합니다.
- PBS에서 3 x 15분 동안 세척합니다. 실온에서 5분 동안 DAPI로 배양합니다.
- PBS에서 3 x 15분 동안 세척합니다. 젤라틴 코팅된 슬라이드에 섹션을 배치하고 형광 장착 매체로 커버슬립합니다.
- 20x/0.8 대물렌즈가 장착된 슬라이드 스캐너 형광 현미경에서 이미지를 획득합니다.
결과
이 연구에서는 중추신경계(예: AAV1 및 AAV9)를 표적화하고 형질도입할 가능성이 있는 모자이크 rAAV(그림 1에 요약)의 생산, 정제 및 특성화를 위한 자세한 프로토콜을 제시하며, 동시에 헤파린 친화성 크로마토그래피 정제(AAV2)에 적합합니다. 이를 위해 천연 AAV 혈청형 1, 2, 9의 캡시드를 사용하여 모자이크 rAAV1/2 및 rAAV2/9 벡터를 개발했습니다.
시작하기 전에 플라스미드 제제의 구조적 무결성을 스크리닝했습니다. 클로닝 단편의 올바른 삽입을 검증하는 데 필요한 분해 외에도 잠재적인 ITR 결실/삽입을 검출하기 위해 pITR 플라스미드를 일관되게 스크리닝하는 것이 필수적입니다. 예를 들어, pITR 플라스미드의 상이한 클론에서 ITR의 무결성은 제한효소 SmaI를 사용한 플라스미드 분해 후에 모니터링하였다(보충 그림 S1).
두 가지 유형의 모자이크 벡터는 표준 transfection 방법6에 따라 각각의 AAV capsid plasmids를 1:1 비율로 co-transfection하여 생성하였다. 간단히 말해서, HEK293T 세포는 i) ITR(pITR) 염기서열 사이에 패킹된 관심 전이유전자를 포함하는 플라스미드, ii) AAV2 및 AAV1 또는 AAV9의 야생형 AAV 게놈 Rep 및 Cap ORF(pAAV-RC 플라스미드)를 포함하는 플라스미드, iii) 아데노바이러스 단백질(E1A, E1B, E4 및 E2A) 및 도우미 기능(pHelper)에 필수적인 아데노바이러스 바이러스 관련 RNA를 코드화하는 플라스미드로 transfection되었습니다. 48시간 후, 세포를 6,36 수확하고, FPLC 시스템을 사용하여 친화성 크로마토그래피에 의해 세포 균질액으로부터 rAAV를 정제하였다. 그림 2A에 나타난 바와 같이, 컬럼 평형화(평형 단계) 후, rAAV를 함유한 세포 용해물을 컬럼에 적용하였다(샘플 로딩). 헤파린33에 대한 rAAV2의 자연적인 친화력으로 인해 rAAV는 컬럼의 수지에 결합하는 반면, 다른 구성 요소는 실행 중인 버퍼에서 수행되고 UV 모니터(플로우스루)에 의해 감지되어 흡광도가 증가했습니다. 이어서 컬럼을 세척하고(세척 단계) 최종적으로 NaCl 농도를 증가시켜 rAAV를 용출했습니다(용리 단계). 용출된 바이러스는 UV 모니터로 검출하고 1mL 분획으로 수집했습니다.
rAAV1/2 및 rAAV2/9의 대표적인 용리 피크 프로필은 각각 그림 2B 및 보충 그림 S2A에 나와 있으며, 서로 다른 바이러스 배치가 분획 F7에서 시작하여 F16까지 단일 피크를 일관되게 나타냅니다. 피크 높이는 rAAV 생산에 따라 가변적이며, 일반적으로 피크가 높을수록 rAAV 수율이 높아집니다. 생성된 rAAV1/2 및 rAAV2/9의 각 분획은 바이러스 역가를 평가하기 위해 RT-qPCR로 특성화했습니다(그림 2C 및 보충 그림 S2B).
용출된 물질의 순도를 특성화하기 위해 각 분획 및 각 플로우스루의 40μL를 10% SDS-폴리아크릴아미드 겔 전기영동으로 검사했습니다(rAAV1/2의 경우 그림 2D 및 rAAV2/9의 경우 보충 그림 S2C ). Coomassie blue 염색은 Van Vliet와 동료14가 이전에 설명한 바와 같이 AAV의 VP1 (87 kDa), VP2 (72 kDa) 및 VP3 (62 kDa) 캡시드 단백질에 해당하는 분자량을 가진 분획 F7-F16의 3 가지 주요 밴드를 드러냈습니다. 두 경우 모두에서, 그리고 UV 흡광도, RT-qPCR 및 겔 밴드 강도에 기초하여, 대부분의 모자이크 rAAVs는 분획 F7 및 F8에 존재하며 분획 F9-F16에서 점차적으로 감소하기 시작한다는 것이 분명합니다. 3개의 바이러스 캡시드 단백질 외에도, 대략 17kDa 크기의 또 다른 단백질(또는 단백질)이 분획 F8-F16에서 검출되었다.
이 공-정제 단백질(들)을 제거하기 위해, 분획 F7-16을 이어서 100 KDa 원심 필터 유닛을 사용하여 여과 및 농축하고, 최종 rAAV 역가를 RT-qPCR에 의해 측정하였다(rAAV1/2에 대한 그림 3A,B 참조). rAAV 생산의 최종 수율은 pITR의 길이와 복잡성, ITR 염기서열의 무결성, 세포 배양 조건(예: 세포 통로 수) 및 transfection 효율 24,58,59,60,61에 따라 달라집니다. 그럼에도 불구하고 최종 역가는 0.5mL 원심 필터 장치를 사용하여 rAAV 준비의 여러 원심분리를 수행하여 조정할 수 있습니다(농도 단계 2). 이 프로토콜에 따라 50 - 100 μL 범위의 최종 부피에 대한 농도는 일반적으로 2 × 109 및 5 ×10 10 vg/μL 사이로 구성됩니다(참조된 적정 키트를 사용하여 정량화).
그런 다음 최종 rAAV 제제의 순도를 10% SDS-폴리아크릴아미드 겔에서 평가했습니다. 그림 3C에서 볼 수 있듯이 rAAV1/2 제제에서 rAAVs 캡시드 단백질을 나타내는 3개의 띠만 관찰되었으며 검출 가능한 공동 정제 단백질은 확인되지 않았습니다. 이러한 결과는 rAAV2/9에 대해 수득된 결과와 일치하였다(보충 그림 S2C). rAAV1/2 및 rAAV2/9 벡터의 식별을 확인하고 순도를 추가로 특성화하기 위해 바이러스 분획 및 농축 스톡을 특이 항체 B1(보충 숫자 S3A 및 추가 그림 S4A) 및 A69(추가 그림 S3B 및 추가 그림 S4B)와 함께 웨스턴 블롯으로 분석했습니다. 항체 B1은 대부분의 AAV 혈청형62의 모든 VP 단백질에 공통적인 C-말단 에피토프를 인식하는 반면, 클론 A69는 VP1 및 VP263의 에피토프만 인식합니다. 그럼에도 불구하고 분자량이 VP3(<62kDa)보다 낮은 일부 희미한 띠도 B1 및 A69 라벨링에서 감지할 수 있습니다.
구조적 형태를 특성화하고 rAAV의 순도를 추가로 평가하기 위해 바이러스 입자를 TEM으로 직접 시각화했습니다. 이 기법은 바이러스 샘플의 샘플 무결성 및 순도를 평가하는 표준 절차로, 빈 및 전체 rAAV 입자의 정량화와 샘플 29,64,65,66,67의 오염 평가를 가능하게 합니다. 그림 3D에서 볼 수 있듯이 직경이 ~25nm인 많은 양의 rAAV 입자를 깨끗한 배경에서 관찰할 수 있습니다. 전자 밀도가 높은 중심이 있는 빈 입자(검은색 화살표)와 전체 벡터(흰색 화살표)도 시료 필드 전체에서 관찰할 수 있습니다.
또한 자외선-가시광선(UV-Vis) 분광법, 정적 광 산란(SLS) 및 동적 광 산란(DLS)68을 결합한 플랫폼인 Stunner를 사용하여 정제된 rAAV의 품질 관리를 수행했습니다. 각 샘플에 대해 단백질, ssDNA의 총량, 흡수 불순물 및 배경 탁도를 UV-Vis 분광법으로 측정했습니다(그림 3E 및 보충 그림 S5A). 그런 다음 SLS와 DLS를 적용하여 rAAV 캡시드의 광 산란 거동을 평가했습니다. AAV의 평균 직경이 25nm라는 점을 감안할 때 15-45nm 직경 범위 내의 입자는 온전한 것으로 간주됩니다. 큰 입자는 전형적으로 바이러스 응집체를 나타내고, 더 작은 모든 것은 조립되지 않은 캡시드 단백질(68)을 포함하여 가장 가능성이 높은 작은 입자를 포함한다. rAAV1/2의 경우, 30nm에서 온전한 캡시드 입자에 해당하는 단일 피크가 관찰되었으며(그림 3F), 응집체 강도는 0%, 소입자 강도는 0%였습니다. rAAV2/9 제제의 경우, 78%의 캡시드 강도를 나타내는 30nm에서의 피크도 검출되었습니다(보충 그림 S5B). 이 샘플의 경우 작은 입자 강도가 0%였음에도 불구하고 22%의 응집체 강도가 측정되었으며(회색으로 표시), 평균 직경이 620nm인 대형 응집체(19.9%)가 주요 기여(보충 그림 S5B)했습니다. UV-Vis 분광법과 SLS 및 DLS 정보의 조합을 통해 Stunner는 그림 3G 및 보충 그림 S5C 에 표시된 두 가지 바이러스 제제에 대한 전체 총 캡시드 역가, 전체 캡시드 역가, 유리 및 응집된 단백질, 유리 및 응집된 ssDNA를 밝혔습니다(각 그림 범례에 표시된 특정 값).
이와 동시에 개발된 모자이크 AAV 벡터의 생물학적 활성을 평가하기 위해 HEK293T 세포에 rAAV1/2 또는 rAAV2/9 제제의 각 FPLC 획득 분획(F2-F16) 50μL를 감염시켰습니다. rAAV1/2 벡터는 CMV 프로모터(pAAV-CMV-ssGFP)의 제어 하에 단일 가닥 녹색 형광 단백질(GFP)을 인코딩하고, rAAV2/9 벡터는 CMV 프로모터(pAAV-CMV-scGFP53)의 제어 하에 자기 보완적 GFP를 인코딩하기 때문에, 감염 후 48시간 후에 이들 세포에서 직접 GFP 형광을 검사하였다(보충 그림 S6 및 보충 그림 S7). RT-qPCR, Coomassie blue 및 western blot에 대한 이전 관찰과 일관되게 바이러스 분획 F7 및 F8에 대해 가장 높은 감염성 수준이 달성되었으며 분획 F9에서 F16까지 점차 감소했습니다.
한외여과 및 농축 단계 후에도 rAAV의 생물학적 활성이 유지되는지 확인하기 위해, 24-웰 플레이트와 8-웰 챔버 슬라이드 모두에 도톰된 Neuro2A 세포를 CMV 프로모터(pAAV-CMV-scGFP53)의 제어 하에 scGFP를 인코딩하는 농축된 rAAV1/2 벡터로 감염시켰다. 명시야 및 형광 이미지는 감염 후 48시간 후에 획득했습니다(고해상도 이미지의 경우 그림 4A,B).
보다 관련성 있고 반사적인 세포 모델에서 생성된 rAAV의 감염 능력을 조사하기 위해 피질의 반밀도 1차 신경 세포 배양을 12웰 플레이트에 파종하고 이전에 사용된 rAAV1/2 - CMV-scGFP에 감염시켰습니다. 감염 후 48시간 후, 세포를 고정하고 DAPI 및 WGA로 라벨링하고 Alexa Fluor 633으로 접합했습니다. 고정 세포를 라벨링하는 데 널리 사용되는 렉틴. 그림 4C,D에 표시된 이미지는 Zeiss Axio Observer Z1과 Zeiss 컨포칼 LSM 710으로 획득한 것입니다. 직접 GFP 형광에 의해 이 그림에서 묘사된 바와 같이, 집중된 모자이크 바이러스는 신경 세포를 위한 그들의 유전자 전달 재산을 보존합니다.
시험관 내에서 순도, 물리적 특성 및 기능성 측면에서 모자이크 rAAV를 특성화한 후, 다음으로 정제된 rAAV1/2 모자이크 벡터를 사용하여 C57BL/6 마우스의 소뇌를 transduction할 수 있는 가능성을 평가했습니다. 이를 위해 9주 된 마우스에서 입체탁스 주입을 수행하고 12주 후에 GFP 발현을 평가했습니다. 예상한 바와 같이, PBS로 주입된 동물은 GFP immunolabeling에 형광을 나타내지 않았다. 시냅신 1 프로모터(rAAV1/2 - Syn-ssGFP)의 제어 하에 GFP를 인코딩하는 rAAV1/2 벡터를 주입한 마우스의 형광 이미지는 rAAV1/2 벡터가 소뇌의 여러 영역, 즉 심부 소뇌핵(DCN) 영역과 소뇌의 다른 소엽을 성공적으로 transduction했음을 보여주었습니다(그림 5). 이러한 결과는 포유류의 뇌에서 전이유전자의 발현이 연장됨을 보여줍니다(12주).
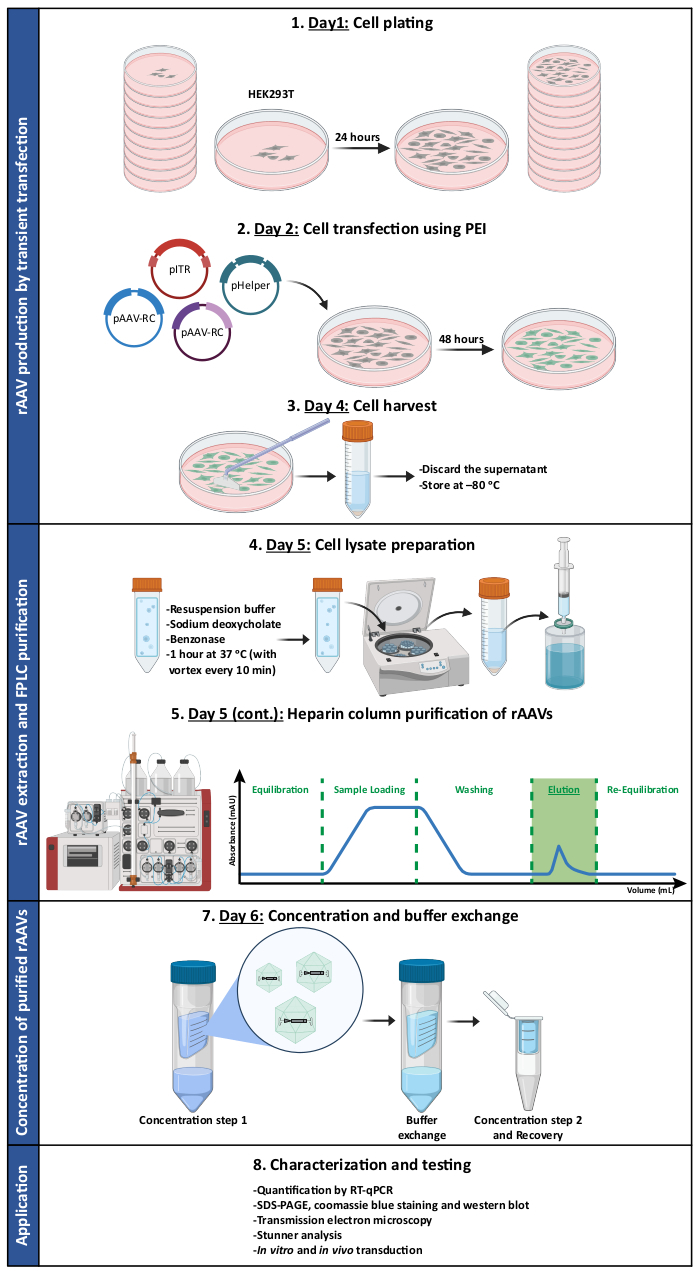
그림 1: rAAV 생산 및 정제 프로토콜의 개략도. rAAV는 폴리에틸렌이민(PEI)을 사용하여 HEK293T 세포의 일시적인 형질주입에 의해 생성됩니다. 그 후, 세포를 채취 및 용해하고 친화성 크로마토그래피를 통해 세포 균질액에서 rAAV를 정제합니다. 그런 다음 rAAV를 함유한 수집된 분획을 농축하고 최종 바이러스 스톡을 역가, 순도, 형태학적 특징 및 생물학적 활성성 측면에서 특성화합니다. 약어: rAAV = 재조합 아데노 관련 바이러스; PEI = 폴리에틸렌민; RT-qPCR = 실시간 정량적 중합효소 연쇄 반응; SDS-PAGE = 소듐 도데 실 설페이트 - 폴리 아크릴 아미드 겔 전기 영동. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
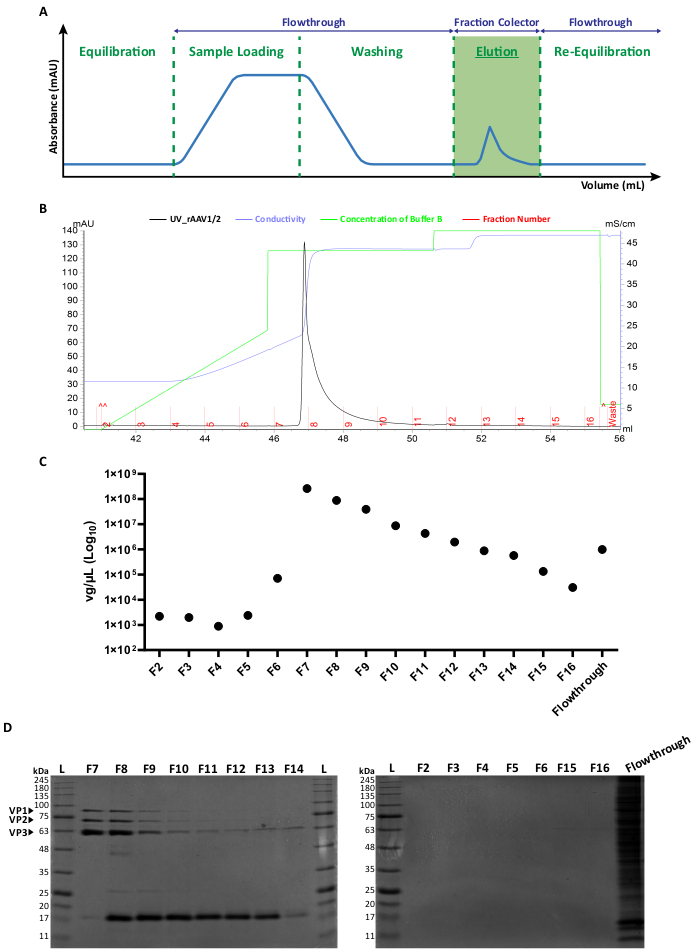
그림 2: FPLC 정제 프로토콜 및 rAAV1/2의 대표적인 용리 프로파일. (A) 전체 크로마토그램 프로파일의 개략도로, rAAV 정제 공정의 여러 단계를 보여줍니다. 컬럼 평형 단계 후에 샘플이 적용됩니다. 그런 다음 컬럼을 세척하고 NaCl의 농도를 증가시켜 용출을 수행합니다. 용리된 바이러스의 결합되지 않은 물질(플로우스루)과 1mL 분획을 수집하여 분석합니다. 280nm에서 흡광도는 mAU로 표시되고 x축은 부피(mL)를 나타냅니다. (B) rAAV1/2 용리 피크(검은색)를 보여주는 확대 부분 크로마토그램과 해당 분수 번호(F2-F16) 및 폐기물(빨간색으로 표시). 방출된 완충액 B 농도와 전도도(mS/cm로 표시)도 각각 녹색과 자주색으로 표시됩니다. (C) 친화성 정제(F2-F16) 및 플로우 스루 중에 수집된 각 분획의 RT-qPCR. vg/μL 단위의 역가는 로그 눈금으로 표시됩니다. (D) 수집된 바이러스 분획의 SDS-PAGE 분석. 용출 단계(F2-F16)에서 각 분획의 동일한 부피(40μL) 및 각각의 플로우스루를 10% SDS-폴리아크릴아미드 겔에 로드하고 분리했습니다. 단백질 밴드는 Coomassie blue 염색으로 시각화되었습니다. AAV 캡시드 단백질 VP1, VP2 및 VP3에 해당하는 띠가 표시됩니다. 표준 단백질 크기 사다리는 (L)로 지정되며 해당 분자량도 표시됩니다. 약어: rAAV = 재조합 아데노 관련 바이러스; RT-qPCR = 실시간 정량적 중합효소 연쇄 반응; SDS-PAGE = 소듐 도데 실 설페이트 - 폴리 아크릴 아미드 겔 전기 영동. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
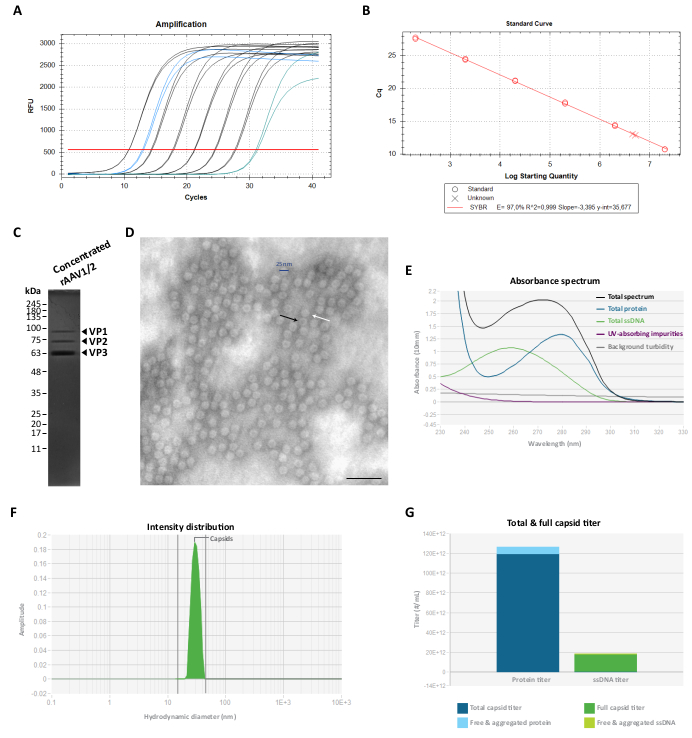
그림 3: 농축된 rAAV1/2 벡터의 특성화. (A) 농축된 rAAV1/2 샘플(파란색)의 증폭 곡선, 2 × 107 vg/μL에서 2 × 102 vg/μL(검은색) 및 템플릿 없는 대조군(녹색)까지 연속적으로 희석된 표준물질, RT-qPCR 중에 얻어짐. (B) rAAV 샘플의 역가를 vg/μL 단위로 측정하기 위한 표준 곡선(선형 회귀). (C) 농축된 바이러스 입자의 SDS-PAGE 분석. 총 2.3 × 1010 vg의 농축 스톡을 겔에 고였습니다. (D) 직경이 ~25-30nm인 rAAV1/2 입자의 투과 전자 현미경 이미지. 전자 밀도가 높은 중심이 있는 빈 입자(검은색 화살표로 표시)는 전체 캡시드(흰색 화살표로 표시)와 구별할 수 있습니다. 스케일 바 = 100nm. (E) Stunner로 측정한 rAAV1/2 제제의 흡광도 스펙트럼(검은색). 단백질(파란색), ssDNA(녹색), 기타 UV 흡수 화합물 또는 불순물(보라색) 및 배경 탁도(회색)의 기여도도 표시됩니다. (F) Stunner로 측정한 30nm에서 단일 피크를 가진 rAAV1/2의 DLS 강도 분포. 100%의 캡시드 산란 강도는 15 - 45 nm(녹색 음영)에서 곡선 아래 면적을 측정하여 측정되었습니다. (G) 1.19 ×10 14 cp/mL(진한 파란색)의 총 캡시드 역가 및 1.73 ×10 13 vg/mL(짙은 녹색)의 전체 캡시드 역가를 나타내는 rAAV1/2 벡터 제제의 충격 분석. 7.16 × 1012 cp/mL 당량(연한 파란색)의 유리 및 응집된 단백질과 1.04 × 1012 vg/mL 당량(연한 녹색)의 유리 응집된 ssDNA도 측정되었습니다. 약어: rAAV = 재조합 아데노 관련 바이러스; RT-qPCR = 실시간 정량적 중합효소 연쇄 반응; SDS-PAGE = 소듐 도데 실 설페이트 - 폴리 아크릴 아미드 겔 전기 영동; ssDNA = 단일 가닥 DNA; DLS = 동적 광 산란. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
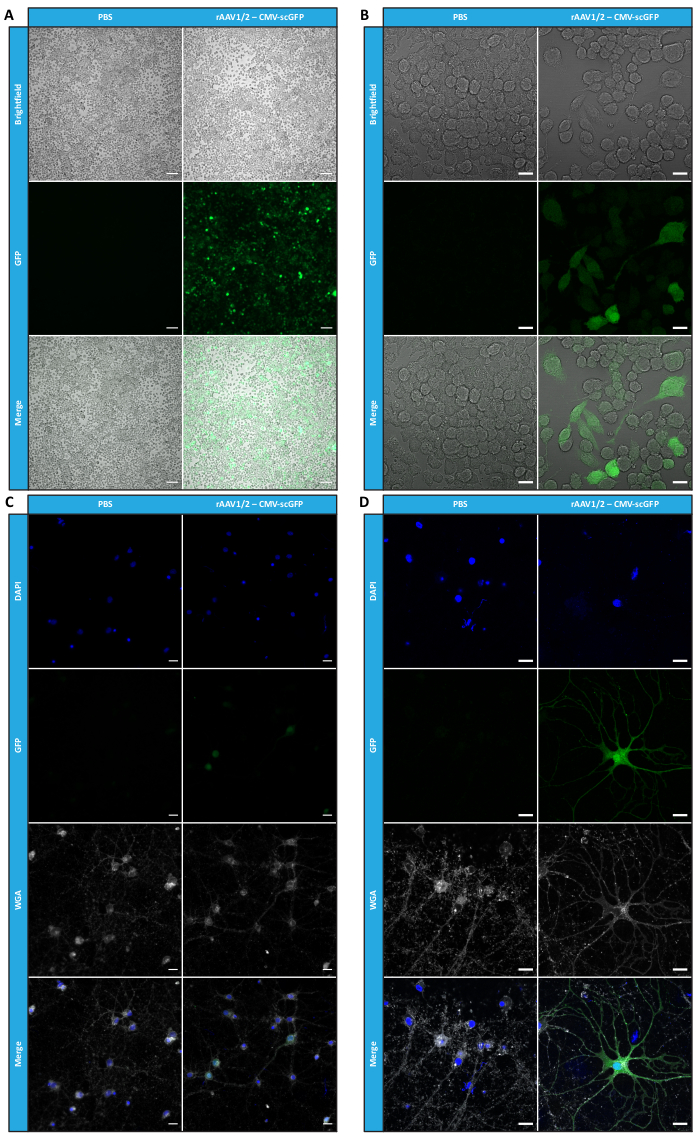
그림 4: 농축된 rAAV1/2 샘플의 체외 감염성 평가. (A) Neuro2A 세포는 rAAV1/2 - CMV-scGFP에 감염되었거나 음성 대조군으로서 동등한 부피의 PBS로 배양되었습니다. 감염 후 48시간 동안 촬영한 세포의 명시야 및 형광 이미지. 이미지는 Zeiss Axio Observer Z1(10x 대물렌즈)에서 획득했습니다. 스케일 바 = 100 μm. (B) rAAV1/2 - CMV-scGFP 감염 후 48시간 후 Neuro2A 세포의 상세 이미지. 이미지는 Zeiss LSM 710(40x 대물렌즈)에서 획득했습니다. 스케일 바 = 20 μm. (C) rAAV1/2 - CMV-scGFP에 감염되거나 동일한 부피의 PBS로 배양되어 음성 대조군 역할을 하는 반밀도 일차 신경 세포 배양. 세포는 핵 염색(파란색의 DAPI) 및 멤브레인 염색(흰색의 WGA)으로 라벨링되었습니다. 이미지는 Zeiss Axio Observer Z1(40x 대물렌즈)에서 획득했습니다. 스케일 바 = 20 μm. (D) rAAV1/2 - CMV-scGFP 감염 후 48시간 후 반밀집된 1차 신경 세포 배양의 상세 이미지. 이미지는 Zeiss LSM 710(40x 대물렌즈)에서 획득했습니다. 스케일 바 = 20 μm. 약어: rAAV = 재조합 아데노 관련 바이러스; CMV = 거대세포바이러스; scGFP = 자기 보완 녹색 형광 단백질; PBS = 인산염 완충 식염수; DAPI = 4', 6- 디아 미디노 -2- 페닐 린돌; WGA = 밀 배아 응집체. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
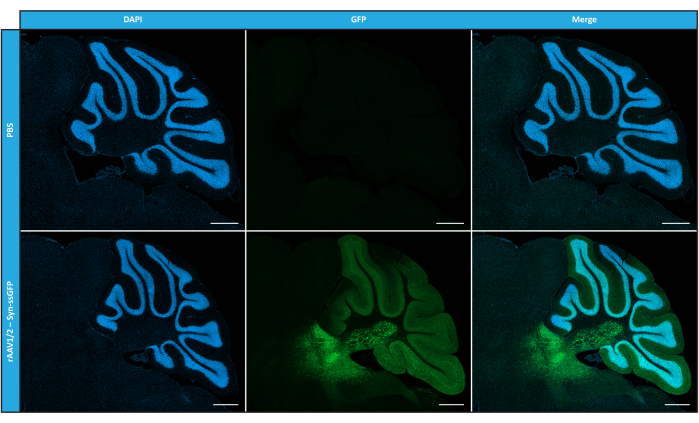
그림 5: 실질내 주입 후 rAAV1/2의 In vivo transduction 효율. 소뇌에서 rAAV1/2 - Syn-ssGFP의 중앙 주입 시 소뇌 전체에 걸쳐 널리 퍼진 GFP 발현(녹색)을 보여주는 대표적인 면역형광 이미지. 핵은 DAPI(파란색)로 염색하였다. 스케일 바 = 500 μm. 약어: rAAV = 재조합 아데노 관련 바이러스; syn = 시냅신 1; ssGFP = 단일 가닥 녹색 형광 단백질; DAPI = 4', 6- 디아 미디노 -2- 페닐 린돌; PBS = 인산염 완충 식염수. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
보충 그림 S1: SmaI로 절단된 rAAV 벡터 플라스미드의 아가로스 겔 분석. pITR의 6개 클론(C1-C6)을 SmaI 제한 효소(레인 2, 4, 6, 8, 10 및 12)로 절단하고, 이는 각 반전 말단 반복 내에서 두 번 절단합니다. 이 경우, 이 pITR의 완전한 분해는 두 개의 밴드(3,796 bp 및 3,013 bp)를 생성할 것으로 예상됩니다. 성공적인 제제(C1, C3, C4 및 C5)에서는 부분 분해로 인한 6809bp의 띠가 여전히 보입니다(전체의 ~5%). ITR 재조합을 사용한 제제에서는 비율이 역전되거나(C2) 분해가 발생하지 않았습니다(C6). 각각의 비분해 클론도 제시됩니다(레인 3, 5, 7, 9, 11, 13). 약어: rAAV = 재조합 아데노 관련 바이러스; ITR = 반전 단자 반복. 이 파일을 다운로드하려면 여기를 클릭하십시오.
보충 그림 S2: 헤파린 기반 친화성 크로마토그래피에 의한 rAAV2/9 정제. (A) NaCl 농도 증가에 따른 단일 피크(검은색)를 나타내는 rAAV2/9의 용리 프로파일. 수집된 분획은 그래프 하단에 빨간색으로 표시된 숫자(2-16)로 표시되며, 280nm에서의 흡광도는 mAU로, 전도도는 mS/cm로 표시, x축은 mL 단위의 부피를 나타냅니다. (B) 각 통합 분획(F2-F16) 및 플로우스루에 대해 RT-qPCR로 정량화된 rAAV 역가. 값은 로그 눈금으로 표시됩니다. (C) SDS-PAGE 및 Coomassie blue 염색에 의한 순도 분석. 각 분획(F2-F16)의 동일한 부피(40μL)와 각각의 플로우스루를 10% SDS-PAGE에 로드하고 분리했습니다. 농축된 스톡을 RT-qPCR로 정량하고, 2.3 × 1010 vg를 40 μL의 PBS에 희석하고 겔에 합하였다. 단백질 밴드는 Coomassie blue 염색으로 시각화되었습니다. AAV 캡시드 단백질(VP1, VP2 및 VP3)이 표시됩니다. 표준 단백질 크기 사다리는 (L)로 지정되며 해당 분자량도 표시됩니다. 약어: rAAV = 재조합 아데노 관련 바이러스; RT-qPCR = 실시간 정량적 중합효소 연쇄 반응; SDS-PAGE = 소듐 도데 실 설페이트 - 폴리 아크릴 아미드 겔 전기 영동. 이 파일을 다운로드하려면 여기를 클릭하십시오.
보충 그림 S3: FPLC로 정제된 rAAV1/2 벡터의 웨스턴 블롯 분석. (A) 수집된 분획 및 농축된 rAAV1/2 벡터를 SDS-PAGE 겔에서 분리하고 VP1, VP2 및 VP3 캡시드 단백질을 인식하는 마우스 단클론 항-AAV 항체(B1)로 조사했습니다. (B) 수집된 분획 및 농축된 rAAV1/2 벡터를 SDS-PAGE 겔에서 분리하고 VP1 및 VP2 캡시드 단백질을 인식하는 마우스 단클론 항-AAV 항체(A69)로 조사했습니다. 약어: rAAV = 재조합 아데노 관련 바이러스; FPLC = 고속 단백질 액체 크로마토그래피; SDS-PAGE = 소듐 도데 실 설페이트 - 폴리 아크릴 아미드 겔 전기 영동; L = 표준 단백질 크기 사다리. 이 파일을 다운로드하려면 여기를 클릭하십시오.
보충 그림 S4: FPLC로 정제된 rAAV2/9 벡터의 웨스턴 블롯 분석. (A) 수집된 분획 및 농축된 rAAV2/9 벡터를 SDS-PAGE 겔에서 분리하고 VP1, VP2 및 VP3 캡시드 단백질을 인식하는 마우스 단클론 항-AAV 항체(B1)로 조사했습니다. (B) 수집된 분획 및 농축된 rAAV2/9 벡터를 SDS-PAGE 겔에서 분리하고 VP1 및 VP2 캡시드 단백질을 인식하는 마우스 단클론 항-AAV 항체(A69)로 조사했습니다. 약어: rAAV = 재조합 아데노 관련 바이러스; FPLC = 고속 단백질 액체 크로마토그래피; SDS-PAGE = 소듐 도데 실 설페이트 - 폴리 아크릴 아미드 겔 전기 영동; L = 표준 단백질 크기 사다리. 이 파일을 다운로드하려면 여기를 클릭하십시오.
보충 그림 S5: Stunner를 통한 rAAV2/9 벡터 정량 및 특성화. (A) Stunner로 측정한 rAAV2/9 벡터의 흡광도 스펙트럼(검은색). 단백질(파란색), ssDNA(녹색), 기타 UV 흡수 화합물 또는 불순물(보라색) 및 배경 탁도(회색)의 기여도도 표시됩니다. (B) 15 - 45 nm(녹색 음영)의 곡선 아래 면적을 측정하여 측정한 캡시드 산란 강도 78%에 해당하는 30nm에서 주요 피크를 갖는 rAAV2/9의 DLS 강도 분포. 22%의 총 응집체 강도(회색 음영)도 측정되었으며, 평균 직경이 620nm인 대형 응집체(19.9%)의 주요 기여도도 측정되었습니다. (C) 2.18 ×10 14 cp/mL(진한 파란색)의 총 캡시드 역가 및 2.35 ×10 13 vg/mL(짙은 녹색)의 전체 캡시드 역가를 나타내는 rAAV2/9 벡터 제제의 기절 분석. 2.92 × 1013 cp/mL 당량(연한 파란색)의 유리 및 응집된 단백질과 3.14 ×10 12 vg/mL 당량(연한 녹색)의 유리 및 응집된 ssDNA도 이 제제에서 측정되었습니다. 약어: rAAV = 재조합 아데노 관련 바이러스; ssDNA = 단일 가닥 DNA; DLS = 동적 광 산란. 이 파일을 다운로드하려면 여기를 클릭하십시오.
보충 그림 S6: rAAV1/2의 정제된 분획의 시험관 내 형질도입 효율 및 생존력. ssGFP(rAAV1/2 - CMV-ssGFP)를 인코딩하는 rAAV1/2 벡터의 50μL의 FPLC 분획으로 형질도입 후 48시간 후 GFP(direct fluorescence)를 발현하는 HEK293T 세포. 스케일 바 = 100 μm. 약어: rAAV = 재조합 아데노 관련 바이러스; FPLC = 고속 단백질 액체 크로마토그래피; ssGFP = 단일 가닥 녹색 형광 단백질. 이 파일을 다운로드하려면 여기를 클릭하십시오.
보충 그림 S7: rAAV2/9의 정제된 분획의 시험관 내 형질도입 효율 및 생존력. HEK293T 세포는 CMV 프로모터의 제어 하에 각 FPLC 분획(F2-F16) 또는 rAAV2/9 벡터 인코딩 scGFP의 플로우스루 50μL에 감염되었습니다. GFP 발현 세포는 감염 후 48시간 동안 시각화되었습니다. 스케일 바 = 100 μm. 약어: rAAV = 재조합 아데노 관련 바이러스; FPLC = 고속 단백질 액체 크로마토그래피; scGFP = 자기 보완 녹색 형광 단백질; CMV = 거대세포바이러스. 이 파일을 다운로드하려면 여기를 클릭하십시오.
토론
빠르게 확장되고 있는 AAV vector toolkit은 다양한 투여 경로를 통해 광범위한 세포 유형에 대한 가장 유망한 유전자 전달 시스템 중 하나가 되었습니다. 이 연구에서 우리는 전임상 연구에서 그 가치를 입증할 수 있는 모자이크 rAAV 벡터의 생산, 정제 및 특성화를 위한 개선된 프로토콜을 개발하는 것을 목표로 했습니다. 이를 위해 rAAV1/2 및 rAAV2/9 모자이크 벡터의 생성이 여기에 설명되어 있지만, 표준 rAAV2 벡터를 정제하기 위해 절차를 적용할 수도 있습니다(데이터는 표시되지 않음).
Mosaic rAAV는 PEI를 transfection 시약으로 사용하는 최적화된 transfection 방법에 따라 생산되었습니다. 일시적인 transfection 방법은 유연성과 속도가 뛰어나 초기 단계의 전임상 연구에서 상당한 이점이 있기 때문에 선택되었습니다. 특정 전이유전자 및 혈청형이 검증되면, 감염 과정에 의해 제공되는 추가 유전자와 함께 특정 Rep/Cap 유전자의 subset을 발현하는 안정적인 transfected 세포주를 구축함으로써 생산 시스템을 미세 조정하여 더 나은 확장성과 비용 효율성을 달성할 수 있습니다24. 칼슘-인산염 transfection과 비교했을 때, PEI는 몇 가지 장점이 있습니다. 이 제품은 안정적이고 비용 효율적인 transfection 시약으로 더 넓은 pH 범위 내에서 효과적으로 작동합니다. 또한, 형질주입 후 세포 배지를 변경할 필요가 없어 비용 및 작업량 모두를 현저히 줄일 수 있다69.
CsCl 또는 요오드릭사놀 그래디언트에 의해 부과된 일부 제한을 우회하기 위해 생성된 rAAV를 친화성 크로마토그래피로 수확하고 정제했습니다. 이 전략은 초원심분리 및 그래디언트 없이 수행할 수 있는 간단하고 확장 가능한 접근법을 제공하여 깨끗하고 높은 바이러스 역가를 생성합니다. 실제로, FPLC 시스템을 사용하는 크로마토그래피 기술은 베드 높이가 더 높은 컬럼에 더 많은 수지 부피를 충전하여 자동화하고 확장할 수 있습니다. 본 명세서에 기술된 프로토콜은 5mL HiTrap Heparin HP 컬럼을 통합하도록 쉽게 조정할 수 있습니다(데이터는 표시되지 않음). 또한 헤파린 컬럼은 여러 번 재사용할 수 있으므로 이 방법의 비용 효율성에 기여합니다.
그런 다음 정제된 rAAV를 역가, 순도, 형태학적 특징 및 생물학적 활성의 측면에서 특성화했습니다. 흥미롭게도, Coomassie blue 염색에서 3 가지 전형적인 바이러스 캡시드 단백질 외에도 약 17 kDa의 띠가 F8-F16 분획에서 검출되었습니다. 그러나, 이 밴드는 rAAV의 농축 단계 후에 더 이상 존재하지 않는다. 더욱이, 분자량이 VP3 (<62 kDa)보다 낮은 일부 희미한 띠도 B1 및 A69 라벨링에서 검출될 수 있으며, 이는 이들이 VP1, VP2 및 VP3 캡시드 단백질(70)의 단편일 수 있음을 시사한다. 또 다른 가능성은 이들이 실제로 페리틴(ferritin) 또는 AAV 캡시드 단백질과 유사한 단백질 지문을 공유하고 AAV 생물학에 관여할 수 있는 폴리펩티드를 가진 다른 세포 단백질과 같은 다른 공동 정제 단백질일 수 있다는 것이다 26,71,72.
TEM 및 충격기 분석은 또한 다양한 생산 전반에 걸쳐 다양한 수준에서 빈 입자의 존재를 밝혀냈습니다. 유사하게, 다른 연구에서는 이전에 형질주입 또는 감염 방법에 의해 제조된 rAAV에 대한 가변적이고 높은 수준(>65%)의 빈 캡시드 생성을 보고하였다24,73. rAAV 생성의 메커니즘은 새로 합성된 VP 단백질에서 빈 캡시드를 빠르게 형성하는 것으로 시작하여 Rep단백질 74,75에 의해 매개되는 미리 형성된 캡시드로 게놈 패키징의 느린 속도 제한 단계가 뒤따릅니다. 따라서, 빈 캡시드는 rAAV 생산에서 생성되지만, 빈 캡시드와 전체 캡시드의 비율은 관심 전이유전자의 크기 및 서열 및 세포 배양 조건에 따라 달라질 수 있다58,73. 빈 캡시드는 관심 게놈이 없기 때문에 치료 효과를 제공할 수 없고 잠재적으로 선천성 또는 적응 면역 반응을 증가시킬 수 있기 때문에 몇 가지 우려를 불러일으킵니다. 그러나, 일부 보고는 또한 그들의 비율을 조정함으로써, 빈 AAV 캡시드가 AAV-특이적 중화항체에 대한 매우 효과적인 미끼 역할을 할 수 있고, 따라서 형질도입 효율을 증가시킬 수 있음을 보여주었다 60,76,77. 빈 캡시드의 존재가 결정적으로 해롭고 전체 벡터에 비해 빈 입자의 음이온 특성이 약간 덜한 경우, 잠재적인 해결책은 음이온 교환 크로마토그래피 기술(64)을 사용하여 두 번째 연마 정제 단계를 수행하는 것을 포함할 수 있습니다.
이 연구는 또한 생성된 모자이크 rAAV가 rAAV1/2의 두개내 주입 시 체외 신경 세포 배양뿐만 아니라 CNS도 효율적으로 transduction할 수 있다는 설득력 있는 증거를 제공합니다. 전반적으로, 이러한 결과는 설명된 생산 및 정제 프로토콜이 고순도의 생물학적 활성 rAAV를 6일 이내에 바로 사용할 수 있게 하며, 전임상 연구에서 rAAV를 생성하기 위한 다재다능하고 비용 효율적인 방법임을 시사합니다.
공개
저자는 이해 상충이 없음을 선언합니다.
감사의 말
rAAV의 TEM 분석과 관련하여 Coimbra Institute for Clinical and Biomedical Research(iCBR) 및 Center for Innovative Biomedicine and Biotechnology(CIBB)의 Mónica Zuzarte 박사가 제공한 협력, 통찰력 및 기술 지원에 감사드립니다. 우리는 코임브라 대학교(CNC-UC)의 신경과학 및 세포 생물학 센터와 코임브라 대학교(IIIUC)의 학제 간 연구 연구소의 Dominique Fernandes 박사에게 주요 신경 세포 배양 실험에 대한 귀중한 기술 지원과 통찰력에 대해 감사를 표합니다. 이 연구에 필수적인 pRV1, pH21 및 pFdelta6 플라스미드는 University of Aberdeen의 생명과학 및 의과대학 의과대학의 Christina McClure 박사에 의해 아낌없이 제공되었으며, 이에 대해 감사드립니다. 이 작업은 Centro 2020 지역 운영 프로그램을 통해 유럽 지역 개발 기금(ERDF)의 자금 지원을 받았습니다. COMPETE 2020 - 경쟁력 및 국제화를 위한 운영 프로그램, FCT - Fundação para a Ciência e a Tecnologia를 통한 포르투갈 국가 기금 프로젝트: UIDB/04539/2020, UIDP/04539/2020, LA/P/0058/2020, ViraVector(CENTRO-01-0145-FEDER-022095), Imagene(PTDC/BBB-NAN/0932/2014 | POCI-01-0145-FEDER-016807), 재설정 - IDT-COP(CENTRO-01-0247-FEDER-070162), SARS-CoV-2(CENTRO-01-01D2-FEDER-000002), BDforMJD(CENTRO-01-0145-FEDER-181240), ModelPolyQ2.0(CENTRO-01-0145-FEDER-181258), MJDEDIT(CENTRO-01-0145-FEDER-181266); 미국 포르투갈 생물 의학 연구 기금 (APBRF) 및 Richard Chin and Lily Lock Machado-Joseph Disease Research Fund, ARDAT에 의해 IMI2 JU 그랜트 계약에 따라 EU 및 EFPIA의 지원을 받는 945473 없음; GeneT- 팀 구성 프로젝트는 유럽 연합의 Horizon Europe 프로그램에서 지원101059981. M.M.L.은 2021.05776.BD 의 지원을 받았습니다. C.H.는 2021.06939.BD 의 지원을 받았습니다. A.C.S.는 2020.07721.BD 에 의해 지원되었습니다. D.D.L.은 2020.09668.BD 에 의해 지원되었으며, 그림 1 은 BioRender.com 를 사용하여 생성되었다.
자료
| Name | Company | Catalog Number | Comments |
| 10% povidone-iodine | Medline | MDS093943 | |
| 12-well plates | Thermo Scientific | 11889684 | |
| 24-well plates | VWR | 734-2325 | |
| 4’,6-diamidino-2-phenylindole (DAPI) | Invitrogen | D1306 | |
| 96-well Stunner plate | Unchained Labs | 701-2025 | 96-well quantification plate for the consecutive ultraviolet-visible light absorption, static light scattering, and dynamic light scattering analysis of rAAV samples |
| AAVpro Titration Kit (for Real-Time PCR) Ver.2 | Takara | 6233 | For determining the titer of AAV using RT-qPCR. This kit contains DNase I, Lysis Buffer, Dilution Buffer, positive control, Taq II mix, primer forward, primer reverse, water |
| Acetic acid glacial | Fisher Chemical | A/0360/PB17 | |
| ÄKTA pure 25 | Cytiva | 29018224 | FPLC system controlled by UNICORN software, version 6.3 |
| Alkaline phosphatase-linked goat anti-mouse | Invitrogen | 31328 | |
| Amicon ultra-0.5 centrifugal filter unit | Merck Millipore | UFC5100 | |
| Amicon ultra-15 centrifugal filter unit | Merck Millipore | UFC9100 | |
| Benzonase Nuclease | Merck Millipore | E1014 | |
| Bromophenol blue | Sigma-Aldrich | B0126 | |
| CFX96 Real-Time PCR detection system | Biorad | 184-5096 | |
| ChemiDoc Touch Imaging System | Bio-Rad Laboratories | 1708370 | |
| Chicken polyclonal anti-GFP primary antibody | Abcam | ab13970 | |
| Coomassie Blue G250 | Fisher Chemical | C/P541/46 | |
| Dithiothreitol (DTT) | Fisher Bioreagents | BP17225 | |
| DMEM | Sigma-Aldrich | D5796 | |
| ECF Substrate for Western Blotting | Cytiva | RPN5785 | |
| FastDigest SmaI | Thermo Scientific | FD0663 | |
| FEI-Tecnai G2 Spirit Biotwin | FEI | Biotwin | Transmission electron microscope |
| Fetal bovine serum | Biowest | S1810 | |
| Fluorescence mounting medium | Dako | S3023 | |
| Formvar-carbon coated 200 mesh grid | TAAB Laboratories Equipment | F077/025 | |
| Gas evacuation apparatus | RWD | R546W | |
| Glycerol | Fisher BioReagents | 10021083 | |
| Goat polyclonal anti-chicken antibody, Alexa Fluor 488 | Invitrogen | A-11039 | |
| Hamilton needle 30G, Small Hub RN Needle, 25 mm, PST3 | Hamilton | 7803-07 | |
| Hamilton syringe (10 µL) | Hamilton | 7653-01 | |
| HEK293T | American Type Culture Collection | CRL-11268 | |
| HiTrap Heparin HP 1 x 5 mL | Cytiva | 17040701 | Pre-packed heparin column |
| HiTrap Heparin HP 5 x 1 mL | Cytiva | 17040601 | Pre-packed heparin column |
| Immobilon-P PVDF Membrane | Merck Millipore | IPVH00010 | |
| Isoflurane | Braun | 469860 | |
| Ketamine | Dechra Pharmaceuticals | N/A | Nimatek |
| Low-retention microcentrifuge tubes (2 mL) | Fisher Scientific | 11906965 | |
| Lunatic & Stunner Client software | Unchained Labs | N/A | Client analysis software version 8.0.1.235. Software for the consecutive ultraviolet-visible light absorption, static light scattering, and dynamic light scattering analysis of rAAV samples |
| Methanol | Fisher Chemical | M/4000/FP21 | |
| Mouse monoclonal anti-AAV, VP1, VP2 antibody (A69) | American Research Products | 03-61057 | |
| Mouse monoclonal anti-AAV, VP1, VP2, VP3 antibody (B1) | American Research Products | 03-61058 | |
| Neuro2a | American Type Culture Collection | CCL-131 | |
| Normal goat serum | Gibco | 16210064 | |
| NucleoBond Xtra Maxi EF | Macherey-Nagel | 12738422 | |
| NZYColour Protein Marker II | NZYtech | MB09002 | |
| pAAV-CMV-scGFP | Addgene | 32396 | Addgene plasmid # 32396; http://n2t.net/addgene:32396; RRID:Addgene_32396 |
| pAAV-CMV-ssGFP | Addgene | 105530 | Addgene plasmid # 105530; http://n2t.net/addgene:105530; RRID:Addgene_105530 |
| pAAV2/9n | Addgene | 112865 | Addgene plasmid # 112865; http://n2t.net/addgene:112865; RRID:Addgene_112865 |
| Paraformaldehyde | Acros Organics | 10342243 | |
| PBS | Fisher BioReagents | BP2438 | |
| Penicillin-streptomycin | Gibco | 15140-122 | |
| Pluronic F-68 Non-ionic Surfactant (100x) | Gibco | 24040032 | |
| Polyethylenimine MAX, MW 40,000 | Polysciences Europe | 24765 | |
| R500 Series Compact Small Animal Anesthesia Machine - Isoflurane | RWD | N/A | |
| Sample Inlet Valve V9-IS | Cytiva | 29027746 | |
| Sample pump P9-S | Cytiva | 29027745 | |
| Sodium azide | Sigma-Aldrich | S2002 | |
| Sodium chloride | Fisher Scientific | 10428420 | |
| Sodium deoxycholate | Sigma-Aldrich | D6750 | |
| Sodium dodecyl sulfate (SDS) | Fisher Bioreagents | BP166 | |
| Sterile PVDF syringe filter | Fisher Scientific | 15191499 | |
| Stunner Platform | Unchained Labs | 700-2002 | Equipment for the consecutive ultraviolet-visible light absorption, static light scattering, and dynamic light scattering analysis of rAAV samples |
| Superloop 150 mL | Cytiva | 18-1023-85 | |
| Superloop 50 mL | Cytiva | 18-1113-82 | |
| SURE 2 supercompetent cells | Stratagene, Agilent Technologies | HPA200152 | |
| Treated culture dishes | Corning | 734-1711 | |
| Tris base | Fisher BioReagents | BP152 | |
| Tris hydrochloride | Fisher BioReagents | BP153 | |
| Triton X-100 | Sigma-Aldrich | T8787 | |
| Trypsin-EDTA | Gibco | 25200-072 | |
| Wheat Germ Agglutinin (WGA) conjugated with Alexa Fluor 633 | Invitrogen | W21404 | |
| Xylazine | Dechra Pharmaceuticals | N/A | Sedaxylan |
| Zeiss Axio Observer Z1 | Carl Zeiss Microscopy GmbH | N/A | Inverted fluorescence microscope equiped with an EC Plan-Neofluar 10x/0.30 objective and a Plan-Apochromat 40x/0.95 objective |
| Zeiss Axio Scan.Z1 | Carl Zeiss Microscopy GmbH | N/A | Slide scanner fluorescence microscope equipped with a Plan-Apochromat 20x/0.8 objective |
| Zeiss LSM 710 | Carl Zeiss Microscopy GmbH | N/A | Inverted confocal microscope equipped with a Plan-Apochromat 40x/1.4 Oil DIC objective |
| µ-Slide 8 well Ibidi | Ibidi | 80826 | 8-well chamber slide |
참고문헌
- Atchison, R. W., Casto, B. C., Hammon, W. M. Adenovirus-associated defective virus particles. Science. 149 (3685), 754-756 (1965).
- Murlidharan, G., Samulski, R. J., Asokan, A. Biology of adeno-associated viral vectors in the central nervous system. Front Mol Neurosci. 7, 1-9 (2014).
- Muzyczka, N. Use of Adeno-Associated Virus as a General Transduction Vector for Mammalian Cells. Viral Expression Vectors. 158, 97-129 (1992).
- Goncalves, M. A. F. V Adeno-associated virus: from defective virus to effective vector. Virol J. 2, 43(2005).
- Flotte, T. R. Gene therapy progress and prospects: recombinant adeno-associated virus (rAAV) vectors. Gene Ther. 11 (10), 805-810 (2004).
- Grieger, J. C., Choi, V. W., Samulski, R. J. Production and characterization of adeno-associated viral vectors. Nat Protoc. 1 (3), 1412-1428 (2006).
- Ojala, D. S., Amara, D. P., Schaffer, D. V Adeno-Associated Virus Vectors and Neurological Gene Therapy. Neuroscientist. 21 (1), 84-98 (2014).
- Saraiva, J., Nobre, R. J., Pereira de Almeida, L. Gene therapy for the CNS using AAVs: The impact of systemic delivery by AAV9. Journal of Controlled Release. 241, 94-109 (2016).
- Agbandje-McKenna, M., Kleinschmidt, J. AAV capsid structure and cell interactions. Methods Mol Biol. 807, 47-92 (2011).
- Sonntag, F., Schmidt, K., Kleinschmidt, J. A. A viral assembly factor promotes AAV2 capsid formation in the nucleolus. Proc Natl Acad Sci U S A. 107 (22), 10220-10225 (2010).
- Sonntag, F., et al. The assembly-activating protein promotes capsid assembly of different adeno-associated virus serotypes. J Virol. 85 (23), 12686-12697 (2011).
- Gao, G., et al. Clades of Adeno-associated viruses are widely disseminated in human tissues. J Virol. 78 (12), 6381-6388 (2004).
- Gao, G., Vandenberghe, L. H., Wilson, J. M. New recombinant serotypes of AAV vectors. Curr Gene Ther. 5 (3), 285-297 (2005).
- Van Vliet, K. M., Blouin, V., Brument, N., Agbandje-McKenna, M., Snyder, R. O. The role of the adeno-associated virus capsid in gene transfer. Methods Mol Biol. 437, 51-91 (2008).
- Clark, K. R., Voulgaropoulou, F., Fraley, D. M., Johnson, P. R. Cell lines for the production of recombinant adeno-associated virus. Hum Gene Ther. 6 (10), 1329-1341 (1995).
- Inoue, N., Russell, D. W. Packaging cells based on inducible gene amplification for the production of adeno-associated virus vectors. J Virol. 72 (9), 7024-7031 (1998).
- Liu, X., Voulgaropoulou, F., Chen, R., Johnson, P. R., Clark, K. R. Selective Rep-Cap gene amplification as a mechanism for high-titer recombinant AAV production from stable cell lines. Mol Ther. 2 (4), 394-403 (2000).
- Mathews, L. C., Gray, J. T., Gallagher, M. R., Snyder, R. O. [23] Recombinant adeno-associated viral vector production using stable packaging and producer cell lines. Methods Enzymol. 346, 393-413 (2002).
- Gao, G., et al. Purification of recombinant adeno-associated virus vectors by column chromatography and its performance in vivo. Hum Gene Ther. 11 (15), 2079-2091 (2000).
- Xiao, X., Li, J., Samulski, R. J. Production of high-titer recombinant adeno-associated virus vectors in the absence of helper adenovirus. J Virol. 72 (3), 2224-2232 (1998).
- Aponte-Ubillus, J. J., et al. Molecular design for recombinant adeno-associated virus (rAAV) vector production. Appl Microbiol Biotechnol. 102 (3), 1045-1054 (2018).
- Smith, R. H., Levy, J. R., Kotin, R. M. A simplified baculovirus-AAV expression vector system coupled with one-step affinity purification yields high-titer rAAV stocks from insect cells. Mol Ther. 17 (11), 1888-1896 (2009).
- Grimm, D., Kern, A., Rittner, K., Kleinschmidt, J. A. Novel tools for production and purification of recombinant adenoassociated virus vectors. Hum Gene Ther. 9 (18), 2745-2760 (1998).
- Wright, J. F. Transient transfection methods for clinical adeno-associated viral vector production. Hum Gene Ther. 20 (7), 698-706 (2009).
- Yuan, Z., Qiao, C., Hu, P., Li, J., Xiao, X. A versatile adeno-associated virus vector producer cell line method for scalable vector production of different serotypes. Hum Gene Ther. 22 (5), 613-624 (2011).
- Strobel, B., Miller, F. D., Rist, W., Lamla, T. Comparative analysis of cesium chloride- and iodixanol-based purification of recombinant adeno-associated viral vectors for preclinical applications. Hum Gene Ther Methods. 26 (4), 147-157 (2015).
- Zolotukhin, S., et al. Recombinant adeno-associated virus purification using novel methods improves infectious titer and yield. Gene Ther. 6 (6), 973-985 (1999).
- Anderson, R., Macdonald, I., Corbett, T., Whiteway, A., Prentice, H. G. A method for the preparation of highly purified adeno-associated virus using affinity column chromatography, protease digestion and solvent extraction. J Virol Methods. 85 (1-2), 23-34 (2000).
- Okada, T., et al. Scalable purification of adeno-associated virus serotype 1 (AAV1) and AAV8 vectors, using dual ion-exchange adsorptive membranes. Hum Gene Ther. 20 (9), 1013-1021 (2009).
- Guo, P., et al. Rapid and simplified purification of recombinant adeno-associated virus. J Virol Methods. 183 (2), 139-146 (2012).
- Lock, M., et al. Rapid, simple, and versatile manufacturing of recombinant adeno-associated viral vectors at scale. Hum Gene Ther. 21 (10), 1259-1271 (2010).
- Wang, L., Blouin, V., Brument, N., Bello-Roufai, M., Francois, A. Production and Purification of Recombinant Adeno-Associated Vectors. Adeno-Associated Virus: Methods and Protocols. 807, 361-404 (2011).
- Summerford, C., Samulski, R. J. Membrane-associated heparan sulfate proteoglycan is a receptor for adeno-associated virus type 2 virions. J Virol. 72 (2), 1438-1445 (1998).
- Wu, Z., Asokan, A., Samulski, R. J. Adeno-associated Virus Serotypes: Vector Toolkit for Human Gene Therapy. Molecular Therapy. 14 (3), 316-327 (2006).
- Mietzsch, M., Broecker, F., Reinhardt, A., Seeberger, P. H., Heilbronn, R. Differential adeno-associated virus serotype-specific interaction patterns with synthetic heparins and other glycans. J Virol. 88 (5), 2991-3003 (2014).
- McClure, C., Cole, K. L. H., Wulff, P., Klugmann, M., Murray, A. J. Production and titering of recombinant adeno-associated viral vectors. JoVE. (57), e3348(2011).
- Auricchio, A., O’Connor, E., Hildinger, M., Wilson, J. M. A single-step affinity column for purification of serotype-5 based adeno-associated viral vectors. Mol Ther. 4 (4), 372-374 (2001).
- Wang, Q., et al. Identification of an adeno-associated virus binding epitope for AVB sepharose affinity resin. Mol Ther Methods Clin Dev. 2, 15040(2015).
- Mietzsch, M., et al. OneBac: platform for scalable and high-titer production of adeno-associated virus serotype 1–12 vectors for gene therapy. Hum Gene Ther. 25 (3), 212-222 (2014).
- Mietzsch, M., et al. Characterization of AAV-specific affinity ligands: consequences for vector purification and development strategies. Mol Ther Methods Clin Dev. 19, 362-373 (2020).
- Florea, M., et al. High-efficiency purification of divergent AAV serotypes using AAVX affinity chromatography. Mol Ther Methods Clin Dev. 28, 146-159 (2023).
- Koerber, J. T., Jang, J. -H., Yu, J. H., Kane, R. S., Schaffer, D. V. Engineering adeno-associated virus for one-Step purification via immobilized metal affinity chromatography. Hum Gene Ther. 18 (4), 367-378 (2007).
- Zhang, H. -G., et al. Addition of six-His-tagged peptide to the C terminus of adeno-associated virus VP3 does not affect viral tropism or production. J Virol. 76 (23), 12023-12031 (2002).
- Arnold, G. S., Sasser, A. K., Stachler, M. D., Bartlett, J. S. Metabolic biotinylation provides a unique platform for the purification and targeting of multiple AAV vector serotypes. Mol Ther. 14 (1), 97-106 (2006).
- Rabinowitz, J. E., et al. Cross-dressing the virion: the transcapsidation of adeno-associated virus serotypes functionally defines subgroups. J Virol. 78 (9), 4421-4432 (2004).
- Hauck, B., Chen, L., Xiao, W. Generation and characterization of chimeric recombinant AAV vectors. Mol Ther. 7 (3), 419-425 (2003).
- Choi, V., McCarty, D., Samulski, R. AAV hybrid serotypes: improved vectors for gene delivery. Curr Gene Ther. 5 (3), 299-310 (2005).
- Nonnenmacher, M., van Bakel, H., Hajjar, R. J., Weber, T. High capsid–genome correlation facilitates creation of AAV libraries for directed evolution. Mol Ther. 23 (4), 675-682 (2015).
- Kimura, K., et al. A mosaic adeno-associated virus vector as a versatile tool that exhibits high levels of transgene expression and neuron specificity in primate brain. Nat Commun. 14 (1), 4762(2023).
- Issa, S. S., Shaimardanova, A. A., Solovyeva, V. V., Rizvanov, A. A. Various AAV serotypes and their applications in gene therapy: an overview. Cells. 12 (5), 785(2023).
- Foust, K. D., et al. Intravascular AAV9 preferentially targets neonatal neurons and adult astrocytes. Nat Biotechnol. 27 (1), 59-65 (2009).
- Lopes, M. M., et al. A new protocol for whole-brain biodistribution analysis of AAVs by tissue clearing, light-sheet microscopy and semi-automated spatial quantification. Gene Ther. 29 (12), 665-679 (2022).
- Gray, J. T., Zolotukhin, S. Design and construction of functional AAV vectors. Methods Mol Biol. 807, 25-46 (2011).
- Choi, V. W., Asokan, A., Haberman, R. A., Samulski, R. J. Production of recombinant adeno-associated viral vectors. Curr Protoc Hum Genet. , Chapter 12, Unit 12.9-12.9.21 (2007).
- Bennicelli, J., et al. Reversal of blindness in animal models of leber congenital amaurosis using optimized AAV2-mediated gene transfer. Mol Ther. 16 (3), 458-465 (2008).
- Fischer, M. D., Hickey, D. G., Singh, M. S., MacLaren, R. E. Evaluation of an optimized injection system for retinal gene therapy in human patients. Hum Gene Ther Methods. 27 (4), 150-158 (2016).
- Santos, S. D., et al. Contactin-associated protein 1 (Caspr1) regulates the traffic and synaptic content of α-amino-3-hydroxy-5-methyl-4-isoxazolepropionic acid (AMPA)-type glutamate receptors. J Biol Chem. 287 (9), 6868-6877 (2012).
- Sommer, J. M., et al. Quantification of adeno-associated virus particles and empty capsids by optical density measurement. Mol Ther. 7 (1), 122-128 (2003).
- Dong, B., Nakai, H., Xiao, W. Characterization of genome integrity for oversized recombinant AAV vector. Mol Ther. 18 (1), 87-92 (2010).
- Wright, J. F. AAV empty capsids: For better or for worse. Mol Ther. 22 (1), 1-2 (2014).
- Asaad, W., et al. AAV genome modification for efficient AAV production. Heliyon. 9 (4), e15071(2023).
- Wobus, C. E., et al. Monoclonal antibodies against the adeno-associated virus type 2 (AAV-2) capsid: epitope mapping and identification of capsid domains involved in AAV-2-cell interaction and neutralization of AAV-2 infection. J Virol. 74 (19), 9281-9293 (2000).
- Wistuba, A., Kern, A., Weger, S., Grimm, D., Kleinschmidt, J. A. Subcellular compartmentalization of adeno-associated virus type 2 assembly. J Virol. 71 (2), 1341-1352 (1997).
- Qu, G., et al. Separation of adeno-associated virus type 2 empty particles from genome containing vectors by anion-exchange column chromatography. J Virol Methods. 140 (1-2), 183-192 (2007).
- Brument, N., et al. A versatile and scalable two-step ion-exchange chromatography process for the purification of recombinant adeno-associated virus serotypes-2 and -5. Mol Ther. 6 (5), 678-686 (2002).
- Potter, M., et al. A simplified purification protocol for recombinant adeno-associated virus vectors. Mol Ther Methods Clin Dev. 1, 14034(2014).
- Dobnik, D., et al. Accurate quantification and characterization of adeno-associated viral vectors. Front Microbiol. 10, 1570(2019).
- Yang, Q. -E., et al. Rapid quality control assessment of adeno-associated virus vectors via Stunner. GEN Biotechnology. 1 (3), 300-310 (2022).
- Huang, X., et al. AAV2 production with optimized N/P ratio and PEI-mediated transfection results in low toxicity and high titer for in vitro and in vivo applications. J Virol Methods. 193 (2), 270-277 (2013).
- Salganik, M., et al. Evidence for pH-dependent protease activity in the adeno-associated virus capsid. J Virol. 86 (21), 11877-11885 (2012).
- Dong, B., et al. Proteomics analysis of co-purifying cellular proteins associated with rAAV vectors. PLoS One. 9 (2), e86453(2014).
- Grieger, J. C., Soltys, S. M., Samulski, R. J. Production of recombinant adeno-associated virus vectors using suspension HEK293 cells and continuous harvest of vector from the culture media for GMP FIX and FLT1 clinical vector. Mol Ther. 24 (2), 287-297 (2016).
- Wright, J. Product-related impurities in clinical-grade recombinant AAV vectors: characterization and risk assessment. Biomedicines. 2 (1), 80-97 (2014).
- Bennett, A., Mietzsch, M., Agbandje-McKenna, M. Understanding capsid assembly and genome packaging for adeno-associated viruses. Future Virol. 12 (6), 283-297 (2017).
- Myers, M. W., Carter, B. J. Assembly of adeno-associated virus. Virology. 102 (1), 71-82 (1980).
- Mingozzi, F., et al. Overcoming preexisting humoral immunity to AAV using capsid decoys. Sci Transl Med. 5 (194), (2013).
- Hoffman, B. E., Herzog, R. W. Covert warfare against the immune system: decoy capsids, stealth genomes, and suppressors. Mol Ther. 21 (9), 1648-1650 (2013).
재인쇄 및 허가
JoVE'article의 텍스트 или 그림을 다시 사용하시려면 허가 살펴보기
허가 살펴보기더 많은 기사 탐색
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. 판권 소유