JoVE 비디오를 활용하시려면 도서관을 통한 기관 구독이 필요합니다. 전체 비디오를 보시려면 로그인하거나 무료 트라이얼을 시작하세요.
Method Article
인간 근육 간 지방 조직에서 핵 분리 및 다운스트림 단일 핵 RNA 염기서열분석
요약
근육 간 지방 조직(IMAT)의 생물학은 인체 조직의 접근성이 제한되어 있기 때문에 대부분 탐구되지 않았습니다. 여기에서는 이 고유한 지방 저장소의 세포 구성을 식별하기 위해 단일 핵 RNA 염기서열 분석을 위한 냉동 인간 IMAT의 핵 분리 및 라이브러리 준비에 대한 자세한 프로토콜을 제시합니다.
초록
근육 간 지방 조직(IMAT)은 근육 섬유 사이에 위치한 상대적으로 연구가 덜 된 지방 저장소입니다. IMAT 함량은 연령과 BMI에 따라 증가하며 대사 및 근육 퇴행성 질환과 관련이 있습니다. 그러나 IMAT의 생물학적 특성과 주변 근섬유와의 상호 작용에 대한 이해는 심각하게 부족합니다. 최근 몇 년 동안 단세포 및 핵 RNA 염기서열 분석은 여러 인간 조직의 세포 유형 특이적 아틀라스를 제공했습니다. 그러나 인간 IMAT의 세포 구성은 인간의 생검 수집에 대한 접근성의 본질적인 문제로 인해 대부분 탐구되지 않은 상태로 남아 있습니다. 수집되는 조직의 양이 제한되어 있을 뿐만 아니라 인간 IMAT의 처리는 골격근 조직 및 근막에 근접하기 때문에 복잡합니다. 지방세포의 지질이 풍부한 특성으로 인해 단세포 분리와 호환되지 않습니다. 따라서 단일 핵 RNA 염기서열 분석은 단일 세포 분해능에서 고차원 전사체학을 얻는 데 최적이며 IMAT의 정확한 세포 구성을 포함하여 이 저장소의 생물학을 밝힐 수 있는 잠재력을 제공합니다. 여기에서는 단일 핵 RNA 염기서열분석을 위한 냉동 인간 IMAT의 핵 분리 및 라이브러리 준비에 대한 자세한 프로토콜을 제시합니다. 이 프로토콜은 액적 기반 접근 방식을 사용하여 수천 개의 핵을 프로파일링할 수 있도록 하여 희귀하고 풍부하지 않은 세포 유형을 검출할 수 있는 능력을 제공합니다.
서문
근육 간 지방 조직(IMAT)은 근섬유 사이 및 주변에 존재하는 이소성 지방 저장소입니다1. Goodpaster et al.의 최근 문헌고찰에서 자세히 설명한 바와 같이, IMAT는 고해상도 컴퓨터 단층 촬영(CT) 및 자기 공명 영상(MRI)을 사용하여 검출할 수 있으며(그림 1A, B) 전신의 근섬유 주변과 내에서 발견된다1. IMAT의 양은 개인마다 크게 다르며 BMI, 연령, 성별, 인종 및 좌식 생활의 영향을 받습니다 2,3,4. 또한, IMAT 침착은 근육퇴행과 관련된 병리학적 조건에서 흔히 볼 수 있으며5, 수많은 연구에서 비만, 제2형 당뇨병, 대사 증후군 및 인슐린 저항성이 있는 개인에서 IMAT 질량이 증가하는 것을 보고했습니다 6,7,8,9. 그럼에도 불구하고 IMAT의 세포 및 생물학적 특성은 이제 막 밝혀지기 시작했습니다. 제한된 접근성과 IMAT 위치 및 체내 함량의 다양성으로 인해 이 독특한 지방 저장소2에서 샘플을 수집하는 데 어려움을 겪었습니다. 더욱이, 샘플은 채취 시 골격근(SM)에 쉽게 '오염'되어 서로 다른 조직의 생물학적 기여도를 분리하는 것을 해독하기 어렵습니다(그림 1C). 이를 위해 지난 10년 동안 상당한 주목을 받은 단일핵 RNA 염기서열분석(snRNA-seq)은 단세포 분해능으로 IMAT 및 SM 유래 유전자 발현 패턴을 분리할 수 있는 이상적인 방법론입니다. 더욱이, 핵 분리는 지질이 많이 함유된 지방세포가 크기 때문에 지방 조직에 특히 유용하며, 이는 세포의 무결성을 손상시키지 않고 단세포 현탁액으로 해리할 수 없습니다. 마지막으로, 이 기술은 IMAT 특이적 지방세포의 새로운 마커를 발견하고, 다양한 전구 세포 집단의 구성 및 존재를 밝혀내고, 병리학적 및 정상 조건에서 세포 구성의 변화를 연구할 수 있는 잠재력을 가지고 있습니다.
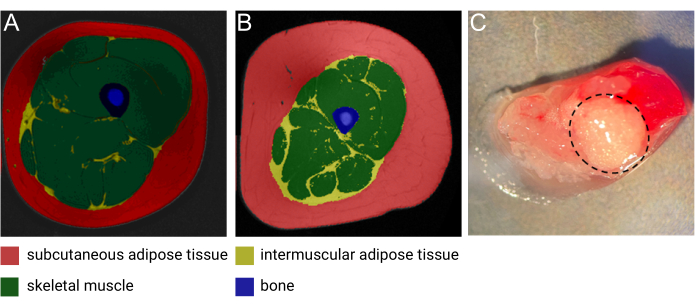
그림 1: IMAT 이미지. (A) 마른 중년 여성과 (B) 비만이 있는 중년 남성의 IMAT의 대표적인 자기 공명(MRI) 이미지. 빨간색: 피하 지방 조직, 노란색: 근육 간 지방 조직, 녹색: 골격근, 파란색: 뼈. 이미지 제공: Heather Cornnell, AdventHealth Translational Research Institute. (C) IMAT가 있는 신선한 조직 샘플(검은색 점선으로 둘러싸임). 이미지 제공: Meghan Hopf, AdventHealth Translational Research Institute 및 Bryan Bergman, University of Colorado. 이 그림은 Goodpaster et al.1의 허가를 받아 수정되었습니다. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
단세포(sc) 및 snRNA-seq10를 사용하여 돼지, 닭 및 소의 육류(특히 IMAT)의 마블링을 조사하는 축산업에서 많은 연구가 발표되었습니다. 이러한 연구는 지방 세포의 여러 하위 집단과 IMAT11,12,13의 잠재적 전구 세포의 마커를 확인했습니다. 그러나 이러한 세포 조성이 인간 IMAT로 변환되는지 여부는 알려져 있지 않습니다. 우리가 아는 한, 고관절 골관절염이 있는 남성 환자로부터 얻은 지방 침윤을 동반한 인간 근육의 세포 이질성을 조사한 연구는 단 한 건에 불과하며, snRNA-seq14를 사용했다. 연구자들은 myonuclei14의 큰 집단 내에서 작은 지방 세포 집단과 여러 섬유 지방 원생 전구 세포(FAP) 하위 집단을 보고했습니다. 본 연구는 snRNA-seq를 이용하여 인체 근육에서 수동으로 절개한 IMAT를 세포 조성을 직접 조사하는 방법을 최초로 개발한 것입니다.
중요한 것은 사용 가능한 조직의 양과 특정 조직의 물리적 특성에 따라 최적의 처리 단계가 결정되기 때문에 snRNA-seq 프로토콜은 연구 대상 조직에 맞게 맞춤화되어야 한다는 것입니다. IMAT의 조직 수율은 일반적으로 작으며 초음파 유도 생검을 수행할 때에도 50mg을 초과하지 않는 경우가 많습니다. 따라서 이 희소한 조직을 적절하게 처리하는 것이 필수적입니다. 우리는 이 프로토콜이 인간 IMAT를 연구하는 연구자들에게 귀중한 자원이 될 것이라고 믿습니다.
Access restricted. Please log in or start a trial to view this content.
프로토콜
이 프로토콜에 사용된 샘플은 SOMMA(Study of Muscle, Mobility, and Aging)15의 일부로, WCG(Western IRB-Copernicus Group) Institutional Review Board의 승인을 받았으며 헬싱키 선언에 따라 수행되었습니다. 참가자는 연구 참여에 대해 정보에 입각한 서면 동의서를 제공했습니다.
참고 : 이 프로토콜은 나노웰 기반 플랫폼(16)에서 100mg의 인간 복부 피하 지방 조직을 사용하는 이전 프로토콜에서 조정되었습니다. 현재 프로토콜은 액적 기반 플랫폼을 사용하여 50mg의 인간 IMAT 및 라이브러리 준비에 최적화되어 있습니다. 비인간 IMAT 또는 기타 지방 저장소로부터의 핵 분리를 위해 이 프로토콜의 추가 최적화가 필요할 수 있습니다.
1. 완충액 및 시약의 제조(표 1 및 표 2)
참고: 실험 당일에 완충액을 새로 준비하고 재사용하지 마십시오.
- 원심분리기를 4°C로 사전 냉각합니다.
- 균질화 완충액과 핵 분리 배지를 준비합니다.
- 두 개의 얼음 양동이를 구하고 2 x 15mL 코니컬 튜브를 미리 냉각합니다.
- 균질화 완충액(HB)에 대한 모든 시약을 표 1에 나열된 순서대로 15mL 코니컬 튜브에 혼합합니다. 얼음 위에 두십시오. 소용돌이로 섞는다.
- 표 2의 순서 목록에 있는 15mL 원뿔형 튜브에 핵 분리 배지(NIM)용 모든 시약을 혼합합니다. 얼음 위에 두십시오. 소용돌이로 섞는다.
- 100 μL의 Triton X-100 - 900 μL의 뉴클레아제가 없는 물을 첨가하여 10% Triton-X를 제조합니다. 적절한 혼합을 보장하기 위해 소용돌이. 실온(RT)에서 보관하십시오.
| 시약 | 부피 (μL) | 최종 농도 (mM) | |
| 1배 | 2배 | ||
| 1개 m MgCl2 | 10 | 20 | 5 |
| 1M 트리스 버퍼, pH 8.0 | 20 | 40 | 10 |
| 2개 M KCl | 25 | 50 | 25 |
| 1.5m 자당 (-4oC) | 334 | 668 | 250 |
| 1mM 디티에이트 | 2 | 4 | 0.001 (~1 μM) |
| 100x 프로테아제 억제제 | 20 | 40 | 1배 |
| 슈퍼아신 20 U/μL | 40 | 80 | 0.4 U/μL |
| 뉴클레아제가 없는 물 | 1549 | 3098 | - |
| 총 볼륨 | 2000 | 4000 | - |
표 1: 균질화 완충액(HB). 얼음 위에 두십시오. 소용돌이로 섞는다.
| 시약 | 부피 (μL) | 최종 농도 (mM) | |
| 1배 | 2배 | ||
| 에디타 | 0.4 | 0.8 | 0.1 |
| Ribolock RNAse 억제제(40U/μL) | 40 | 80 | 0.8 U/μL |
| 1% BSA-PBS(-/-) | 1959.6 | 3919.2 | - |
| 총 볼륨 | 2000 | 4000 | - |
표 2: 핵 분리 매체(NIM). 얼음 위에 두십시오. 소용돌이로 섞는다.
2. 동결 조직의 분쇄 (그림 2A)
- 균질화를 위해 워크스테이션을 설정합니다.
- 캐니스터에 액체 질소(LN2)를 채웁니다.
주의 : LN2 로 작업할 때는 항상 고글과 냉동 장갑을 착용하십시오. - 자동 디운서용 박격포 2개, 유봉 1개, 마이크로 스쿱 주걱 1개, 유리 도운 1개, 스테인리스 스틸 유봉 1개를 얻습니다.
- 자동 디스펜서를 설정합니다.
- 비커에 얼음을 채우고 유리 뭉치를 미리 식힙니다.
- 캐니스터에 액체 질소(LN2)를 채웁니다.
- 2개의 모르타르(유봉과 주걱 포함)에 LN2 를 채워 기구를 식힙니다. LN2 를 증발시키고 반복하십시오.
- 기기가 냉각되는 동안 유리 dounce에 1mL의 HB를 추가합니다.
- 두 모르타르에 LN2 를 마지막으로 한 번 더 채우고 50mg IMAT 샘플을 모르타르 중 하나에 붓습니다.
- 유봉을 사용하여 IMAT를 조직 조각을 부드럽게 눌러 작은 조각으로 부수어 분쇄합니다. 모든 조각이 분쇄되었는지 확인하십시오.
- LN2 는 조직을 분쇄하는 동안 천천히 증발합니다. 조직이 제대로 분쇄되고 LN2 모르타르의 1/4 - 1/2이 여전히 남아 있으면 모르타르를 모르타르 가장자리 쪽으로 기울여 입술로 분쇄 된 조직을 수집합니다. LN2 를 완전히 증발시키십시오.
- 마지막 LN2 가 증발 한 직후, 분쇄 된 조직을 1 mL의 HB가 들어있는 유리 dounce에 퍼 넣습니다.
3. 분쇄된 조직의 균질화
- 자동 디운서를 사용하여 분쇄된 조직을 균질화합니다. 유리 뭉치를 스테인리스 스틸 유봉을 앞뒤로 앞으로 10번 친 다음 반대 방향으로 10번 칩니다.
- 균질화 후 용액이 탁하고 눈에 보이는 조직 조각이 없는지 확인하십시오. 연한 분홍색은 근육 조직의 오염으로 인해 종종 예상됩니다.
- 균질액을 얼음 위에서 사전 냉각된 1.7mL 저결합 튜브로 옮깁니다.
- 400μL의 HB를 사용하여 dounce를 헹구어 모든 재료가 전달되었는지 확인하고 튜브에 추가합니다.
알림: 한 번에 두 개의 샘플을 처리할 수 있습니다. 이렇게하려면 HB와 NIM의 양을 두 배로 늘리십시오. 하나의 조직 샘플을 분쇄 및 균질화한 후 즉시 두 번째 조직 샘플을 분쇄 및 균질화하여 분리 및 세척 단계를 병렬로 수행할 수 있습니다.
4. 핵 분리 및 청소(그림 2B)
- 14μL의 Triton-X(10%)를 균질액에 첨가하여 0.1% 농도를 만듭니다.
- 튜브를 얼음 위와 어두운 곳에 10-15분 동안 유지하면서 3분마다 소용돌이를 일으킵니다.
- 50mL 코니컬 튜브에 각각 100μL의 RT DPBS로 100μm 및 40μm 세포 스트레이너 1개(샘플당)를 사전 적십니다.
- 100μm 셀 스트레이너를 통해 균질액을 여과합니다.
- 1.7mL 튜브를 400μL의 HB로 헹구고 100μm 세포 여과기를 통해 여과합니다.
- 다음으로, 40μm 셀 스트레이너를 통해 용액을 여과합니다.
- 각 튜브의 ~900 μL에 해당하는 두 개의 사전 냉각된 1.7 mL low-bind tube에 동일한 양의 용액을 옮깁니다.
- 4°C에서 2700 x g 에서 10분 동안 튜브를 원심분리합니다. 원심분리 후 작은 펠릿이 보여야 합니다.
- 상단 지질층과 나머지 상층액을 제거하고 버리고 첫 번째 튜브에서 ~50μL 용액을 남깁니다.
- 두 번째 튜브에 대해 반복합니다.
- 위아래로 20배 부드럽게 피펫팅하여 첫 번째 튜브에 펠릿을 완전히 재현탁하고 새로운 1.7mL 저결합 튜브로 옮깁니다. 거품을 만들지 마십시오.
- 두 번째 튜브에 대해 이 절차를 반복하고 재현탁 용액을 동일한 튜브로 옮깁니다.
- 500 μL의 NIM을 추가하고 피펫팅과 혼합합니다.
- 1000 x g 의 저울로 튜브를 4°C에서 10분 동안 원심분리합니다.
- ~50μL를 남기고 상층액을 제거하고 펠릿이 다시 부유될 때까지 위아래로 부드럽게 피펫팅합니다. 선택적으로, 튜브 측면에 약간의 지질 잔여물이 남아 있는 경우 재현탁 펠릿을 새 깨끗한 튜브로 옮깁니다.
- 200 μL의 NIM을 추가하고 피펫팅으로 혼합합니다.
5. 핵 염색 및 계수(그림 2C 및 그림 3)
참고 : 카운팅을 용이하게 하려면 자동 셀 카운터에서 '핵 카운팅' 프로토콜을 설정하십시오. 이는 명시야와 DAPI 채널을 조정하면 카운팅에 큰 영향을 미칠 수 있습니다. 파편이 아닌 핵만 포집되도록 채널을 조정합니다. 명시야 채널이 DAPI 염색이 있는 '물체'만 표시하는지 확인하십시오.
- 살아있는 세포 염색 용액 1방울을 넣고 어두운 곳에서 얼음 위에 15분 동안 그대로 둡니다.
- 30μm 셀 스트레이너를 통해 용액을 여과합니다.
- 피펫팅으로 핵 용액을 혼합하고 10μL의 용액을 세포 계수 챔버 슬라이드에 추가합니다.
- 자동화된 세포 계수기를 사용하여 핵을 계수합니다.
참고: 최적의 농도는 1.0 x 106/mL에 해당하는 1000 nuclei/μL입니다.- 단일 핵 방울을 생성하기 위한 칩을 막을 수 있으므로 핵 덩어리가 없는지 확인하십시오(그림 3).
- 핵 농도가 충분히 높지 않으면 1000 x g 에서 용액을 4°C에서 10분 동안 스핀다운하여 펠릿을 얻고 상층액을 제거한 다음 더 작은 부피로 재현탁합니다.
- 용액의 이물질 정도가 높으면 핵 용액을 더 큰 부피의 NIM(즉, 1mL)에 재현탁시키고 30μm 셀 스트레이너를 통해 다시 여과합니다. 그런 다음 4 °C에서 10 분 동안 1000 x g 에서 스핀 다운하고 핵 농도와 관련하여 적절한 부피로 재현 탁합니다.
- 핵 농도를 얻은 후 라이브러리 준비의 첫 번째 단계로 바로 진행합니다.
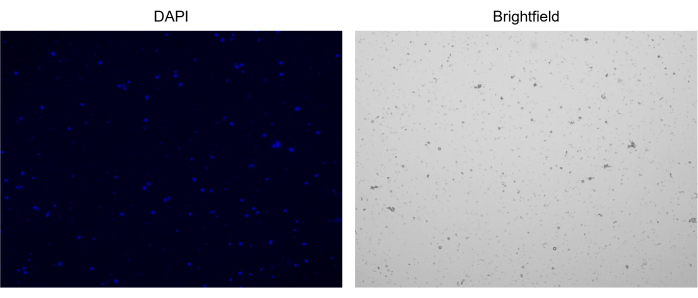
그림 3: 분리된 핵의 염색. NucBlue/DAPI로 염색된 핵의 세포 계수기 이미지(왼쪽 이미지) 및 해당 명시야 이미지(오른쪽 이미지). 소량의 파편이 존재한다는 것은 명시야 이미지에서 분명합니다. 여기에 사용된 자동화된 셀 카운터에는 축척 막대를 포함할 수 있는 옵션이 없습니다. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
6. 라이브러리 준비 및 염기서열분석 파라미터
- 제공자의 웹페이지17에서 사용할 수 있는 액적 기반 단일 핵 접근법을 사용하여 라이브러리 준비를 위한 철저한 프로토콜을 참조하십시오.
- 10,000개의 목표 핵 회수를 목표로 합니다. 그러나 높은 수준의 파편이나 깨지기 쉬운 핵이 있는 샘플의 경우 회수되는 핵의 수가 더 적을 것으로 예상됩니다.
- 2.3단계 후 최대 72시간 동안 샘플을 4°C에서 보관합니다. 라이브러리 준비 프로토콜에서 더 많은 샘플의 처리를 병렬로 결합합니다. 2일 연속으로 2.3단계까지 2개의 샘플을 처리하고, 3일째 되는 날에는 라이브러리 준비 프로토콜에서 3단계 이후의 4개 샘플을 함께 처리하여 이 작업을 수행합니다.
- 염기서열분석 매개변수: 핵당 50,000개의 paired-end read를 목표로 하는 염기서열분석 플랫폼에서의 염기서열분석.
참고: 이 프로토콜에 제시된 데이터는 핵당 50,000개의 paired-end read를 목표로 NovaSeq 6000 플랫폼에서 시퀀싱되었습니다.
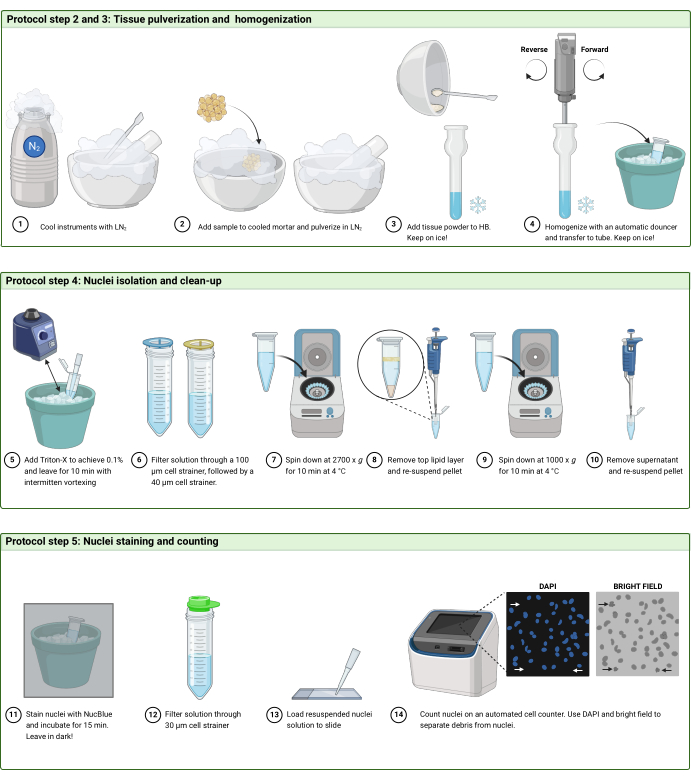
그림 2: 프로토콜 워크플로우. 프로토콜의 (A) 2단계 및 3단계, (B) 4단계 및 (C) 5단계의 워크플로우를 도식화한 그림입니다. 피규어는 BioRender.com 로 만들어졌습니다. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
7. 데이터 처리 및 분석
참고 : 이 프로토콜에서는 결과 시퀀싱 데이터를 처리하는 데 사용되는 권장 소프트웨어 및 R 패키지 중 일부를 간략하게 소개하고 초기 전처리 이후의 단계에 초점을 맞춥니다(표 3). 이 연구는 그림 4에서 일반적인 품질 관리(QC) 메트릭과 UMAP(Uniform Manifold Approximation and Projection)의 예를 제공합니다. 그러나 생물정보학적 분석에 대한 심층적인 설명은 이 프로토콜의 범위를 벗어납니다. 따라서 독자는 Heumos et al.18의 단일 세포 분석 모범 사례에 대한 최근 검토를 참조할 수 있습니다.
- 염기서열분석 데이터의 전처리
- 판독된 단일 핵을 인간 참조 게놈 GRCh38에 매핑합니다.
- 카운트에 인트론 읽기를 포함합니다.
- Seurat R 패키지19를 사용하여 데이터의 QC 및 필터링을 수행합니다.
- 검출된 유전자의 log(10) 수를 검출된 판독 횟수로 나누어 세포 복잡성 점수를 계산합니다.
- 히스토그램 또는 바이올린 플롯을 사용하여 핵당 검출된 유전자 수, 미토콘드리아 판독 비율, 세포 복잡성 점수를 포함한 가장 중요한 QC 지표를 플롯합니다.
- 핵당 유전자가 200개 미만 또는 10,000개 이상이고, 미토콘드리아 판독률이 10% 이상이며, 복잡성 점수가 0.8 미만인 핵을 필터링합니다.
- 데이터를 정규화하고 차원 축소를 수행합니다.
- Seurat의 SCTransform 함수를 사용하여 2000개의 변수 특징을 사용하여 데이터를 정규화합니다.
- Seurat R 패키지의 RunPCA, FindNeighbors, FindClusters 및 RunUMAP 함수를 사용하여 데이터를 클러스터링합니다.
- UMAP을 플로팅하여 데이터의 군집화를 시각화합니다.
- DoubletFinder R 패키지20을 사용하여 예측된 doublet을 필터링하고 데이터를 다시 클러스터링합니다.
- 조직에 존재할 것으로 예상되는 세포 유형의 알려진 유전자 마커를 사용하거나(지도 접근법) 클러스터 간에 다르게 발현된 상위 5개의 유전자를 기반으로 클러스터에 주석을 달 수 있습니다(비지도 접근 방식).
- decontX21을 사용하여 주변 RNA 오염 정도를 측정하고 주변 RNA에 대한 유전자 발현 매트릭스를 조정합니다.
- 원시 유전자 매트릭스를 배경으로 포함합니다.
- 나중에 데이터를 탐색할 수 있도록 Seurat 객체를 저장합니다.
참고: QC 및 클러스터링 분석을 위한 코드는 보충 파일 1에서 사용할 수 있습니다.
| 데이터 워크플로우에 사용되는 소프트웨어/R 패키지 | 대체 소프트웨어/패키지 | 처리 단계 |
| 셀레인저 | STARsolo, 칼리스토 | 트리밍, 정렬, 매핑 |
| 쇠라(Seurat) | SingleCellExperiment, 셀레인저 | QC, 분석 및 데이터 탐색 |
| 더블릿파인더 | scds, scdblFinder, 스크러블릿 | 이중선 검출 |
| 디콘트엑스 | 수프X, 셀벤더 | 주변 RNA 조정 |
표 3: 데이터 워크플로우를 위한 소프트웨어/도구.
Access restricted. Please log in or start a trial to view this content.
결과
이 워크플로우는 단일 핵 분해능에서 유전자 발현 프로필을 얻기 위해 냉동된 인간 IMAT 샘플을 처리하도록 설계되어 세포 유형 식별을 가능하게 합니다. 여기에서는 SOMMA 연구 참가자의 대표적인 IMAT 샘플 하나를 제시합니다.
snRNA-seq 데이터 분석의 첫 번째 단계는 데이터 세트에서 잠재적으로 제거해야 하는 저품질 핵을 식별하기 위해 데이터의 품질을 평가하는 것입니다. 중?...
Access restricted. Please log in or start a trial to view this content.
토론
IMAT를 사용하는 데에는 몇 가지 내재된 과제가 있습니다. 접근성이 제한적인 것 외에도 시료 물질의 수율이 매우 드문 경우가 많으며 골격근의 "오염"을 피하는 것은 거의 불가능합니다. 최고 품질의 검체를 얻기 위해서는 생검 바늘을 삽입할 때 근육 근막을 관통하고(피하 지방 조직이 수집되지 않도록 주의) 채취 직후 현미경으로 검체를 절개하여 가능한 한 많은 근육 조직을 제거한 후 조직학, ?...
Access restricted. Please log in or start a trial to view this content.
공개
저자는 밝힐 것이 없습니다.
감사의 말
저자들은 MoTrIMAT 연구(R01AG077956)에서 그림 1C의 IMAT 생검 이미지를 제공한 콜로라도 대학의 Bryan Bergman 박사에게 감사를 표합니다. 우리는 근육, 이동성 및 노화 연구(Study of Muscle, Mobility and Aging)에서 대표 결과 섹션에 데이터가 표시되는 IMAT 샘플을 제공해 주셔서 감사합니다. 미국 국립노화연구소(National Institute on Aging, NIA)는 근육, 이동성 및 노화 연구(SOMMA; R01AG059416) 및 그 보조 연구인 SOMMA AT(R01AG066474) 및 SOMMA Knee OA(R01AG070647). 연구 인프라 지원은 피츠버그 대학교(P30AG024827) 및 웨이크 포레스트 대학교(P30AG021332)의 NIA Claude D. Pepper Older American Independence Centers와 웨이크 포레스트 대학교(UL1 0TR001420)의 National Center for Advancing Translational Science의 자금 지원을 받는 임상 및 중개 과학 연구소(Clinical and Translational Science Institutes)에서 부분적으로 자금을 지원했습니다.
Access restricted. Please log in or start a trial to view this content.
자료
| Name | Company | Catalog Number | Comments |
| 0.2 µm corning syringe filters | Millipore Sigma | CLS431229 | |
| 1.7 mL DNA LoBind tubes | Eppendorf | 22431021 | low-bind tubes |
| 10% Tween 20 | Bio-Rad | 1662404 | |
| 100x protease inhibitor | Thermo Fisher Scientific | 78437 | |
| 10X Magnetic Separator | 10X Genomics | 230003 | |
| 10X Vortex Adapter | 10X Genomics | 330002 | |
| 15 mL canonical tubes | Sarstedt | 6,25,54,502 | |
| 2100 Bioanalyzer | Agilent | G2939BA | |
| 50 mL conical tubes | Sarstedt | 6,25,47,254 | |
| CellRanger | Genomics | N/A | |
| Chromium iX accesory kit | 10X Genomics | PN1000323 | |
| Chromium iX Controller | 10X Genomics | PN1000326 | |
| Chromium Next GEM Chip G Single Cell Kit | 10X Genomics | PN1000127 | |
| Chromium Next GEM Single Cell 3' Gel Bead Kit v3.1 | 10X Genomics | PN1000129 | |
| Chromium Next GEM Single Cell GEM Kit v3.1 | 10X Genomics | PN1000130 | |
| Countess 3 Automated Cell Counter | Thermo Fisher Scientific | AMQAX2000 | Automated cell counter |
| Countess cell counting chamber slides | Thermo Fisher Scientific | C10228 | |
| DoubletFinder | R | N/A | |
| DPBS (no calcium, no magnesium) | Thermo Fisher Scientific | 14190144 | |
| DTT | Thermo Fisher Scientific | R0861 | |
| Dual Index Kit TT Set A, 96 rxns | 10X Genomics | PN1000215 | |
| Dynabeads MyOne SILANE | 10X Genomics | PN2000048 | |
| Falcon 100 µm Cell strainer | Corning Life Science | 352360 | |
| Falcon 40 µm Cell strainer | Corning Life Science | 352340 | |
| Glycerin (glycerol), 50% (v/v) Aqueous Solution | Ricca Chemical Company | 3290-32 | |
| KCL | Thermo Fisher Scientific | AM9640G | |
| Library Construction Kit v3.1 | 10X Genomics | PN1000196 | |
| MACS SmartStrainers (30µm) | Miltenyi Biotec | 130-098-458 | |
| Mastercycler Nexus Gradient Thermal cycler | Eppendorf | 6331000017 | |
| MgCl2 | Ambion | AM9530G | |
| Mortar and pestel | Health care logistics | 14075 | |
| NucBlue Live Ready Probes Reagent | Thermo Fisher Scientific | R37605 | |
| Nuclease Free Water (not DEPC treated) | Thermo Fisher Scientific | AM9930 | |
| Probumin Bovine Serum Albumin Fatty Acid Free, Powder | Sigma-Aldrich | 820024 | |
| Qiagen Buffer EB | Qiagen | 19086 | |
| Ribolock RNAse inhibitor | Thermo Fisher Scientific | EO0382 | |
| Seurat | R | N/A | |
| Sucrose | Sigma-Aldrich | S0389 | |
| SUPERasin 20 U/µL | Thermo Fisher Scientific | AM2695 | |
| ThermoMixer C | Eppendorf | 5382000015 | |
| Tissue homogenizer | Glass-Col | 099C K54 | |
| Tris buffer pH 8.0 | Thermo Fisher Scientific | AM9855G | |
| Triton X-100 | Thermo Fisher Scientific | AC327372500 | |
| UltraPure 0.5M EDTA pH 8.0 | Gibco | 15575020 |
참고문헌
- Goodpaster, B. H., Bergman, B. C., Brennan, A. M., Sparks, L. M. Intermuscular adipose tissue in metabolic disease. Nat Rev Endocrinol. 19 (5), 285-298 (2023).
- Sparks, L. M., Goodpaster, B. H., Bergman, B. C. The metabolic significance of intermuscular adipose tissue: Is IMAT a friend or a foe to metabolic health. Diabetes. 70 (11), 2457-2467 (2021).
- Gallagher, D., et al. Adipose tissue in muscle: A novel depot similar in size to visceral adipose tissue. Am J Clin Nutr. 81 (4), 903-910 (2005).
- Manini, T. M., et al. Reduced physical activity increases intermuscular adipose tissue in healthy young adults. Am J Clin Nutr. 85 (2), 377-384 (2007).
- Addison, O., Marcus, R. L., LaStayo, P. C., Ryan, A. S. Intermuscular fat: A review of the consequences and causes. Int J Endocrinol. 2014, 309570(2014).
- Goodpaster, B. H., et al. Obesity, regional body fat distribution, and the metabolic syndrome in older men and women. Arch Intern Med. 165 (7), 777-783 (2005).
- Goodpaster, B. H., Thaete, F. L., Kelley, D. E. Thigh adipose tissue distribution is associated with insulin resistance in obesity and in type 2 diabetes mellitus. Am J Clin Nutr. 71 (4), 885-892 (2000).
- Goodpaster, B. H., et al. Association between regional adipose tissue distribution and both type 2 diabetes and impaired glucose tolerance in elderly men. Diabetes Care. 26 (2), 372-379 (2003).
- Sachs, S., et al. Intermuscular adipose tissue directly modulates skeletal muscle insulin sensitivity in humans. Am J Physiol Endocrinol Metab. 316 (5), E866-E879 (2019).
- Ford, H., Liu, Q., Fu, X., Strieder-Barboza, C. White adipose tissue heterogeneity in the single-cell era: From mice and humans to cattle. Biology (Basel). 12 (10), 1289(2023).
- Wang, L., et al. Single-nucleus and bulk RNA sequencing reveal cellular and transcriptional mechanisms underlying lipid dynamics in high marbled pork. NPJ Sci Food. 7 (1), 23(2023).
- Li, J., et al. Identification of diverse cell populations in skeletal muscles and biomarkers for intramuscular fat of chicken by single-cell RNA sequencing. BMC Genomics. 21 (1), 752(2020).
- Lyu, P., Qi, Y., Tu, Z. J., Jiang, H. Single-cell RNA sequencing reveals heterogeneity of cultured bovine satellite cells. Front Genet. 12, 742077(2021).
- Fitzgerald, G., et al. MME+ fibro-adipogenic progenitors are the dominant adipogenic population during fatty infiltration in human skeletal muscle. Commun Biol. 6 (1), 111(2023).
- Cummings, S. R., et al. The study of muscle, mobility and aging (SOMMA): A unique cohort study about the cellular biology of aging and age-related loss of mobility. J Gerontol A Biol Sci Med Sci. 78 (11), 2083-2093 (2023).
- Whytock, K. L., et al. Isolation of nuclei from frozen human subcutaneous adipose tissue for full-length single-nuclei transcriptional profiling. STAR Protoc. 4 (1), 102054(2023).
- 10x Genomics. Chromium Single Cell 3' Reagent Kits User Guide (v3.1 Chemistry Dual Index), Document Number CG000315 RevE. , Available from: https://cdn.10xgenomics.com/image/upload/v1668017706/support-documents/CG000315_ChromiumNextGEMSingleCell3-_GeneExpression_v3.1_DualIndex__RevE.pdf (2022).
- Heumos, L., et al. Best practices for single-cell analysis across modalities. Nat Rev Genet. 24 (1), 550-572 (2023).
- Hao, Y., et al. Dictionary learning for integrative, multimodal and scalable single-cell analysis. Nat Biotechnol. 42 (2), 293-304 (2023).
- McGinnis, C. S., Murrow, L. M., Gartner, Z. J. DoubletFinder: Doublet detection in single-cell RNA sequencing data using artificial nearest neighbors. Cell Syst. 8 (4), 329-337 (2019).
- Yang, S., et al. Decontamination of ambient RNA in single-cell RNA-seq with DecontX. Genome Biol. 21 (2), 57(2020).
- Common considerations for quality control filters for single cell RNA-seq data. 10X Genomics. , Available from: https://www.10xgenomics.com/analysis-guides/common-considerations-for-quality-control-filters-for-single-cell-rna-seq-data (2022).
- Luecken, M. D., Theis, F. J. Current best practices in single-cell RNA-seq analysis: a tutorial. Mol Syst Biol. 15 (6), e8746(2019).
- Emont, M. P., et al. A single-cell atlas of human and mouse white adipose tissue. Nature. 603 (7903), 926-933 (2022).
- Hildreth, A. D., et al. Single-cell sequencing of human white adipose tissue identifies new cell states in health and obesity. Nat Immunol. 22 (5), 639-653 (2021).
- Whytock, K. L., et al. Single cell full-length transcriptome of human subcutaneous adipose tissue reveals unique and heterogeneous cell populations. iScience. 25 (8), 104772(2022).
- Probst, V., et al. Benchmarking full-length transcript single cell mRNA sequencing protocols. BMC Genomics. 23 (1), 860(2022).
- CG000148 Rev A Technical Note - Resolving cell types as a function of read depth and cell number. Technical note. 10X Genomics. , Available from: https://assets.ctfassets.net/an68im79xiti/6gDArDPBTOg4IIkYEO2Sis/803be2286bb a5ca67f353e6baf68d276/CG000148_10x_Technical _Note_Resolving_Cell_Types_as_Function_of_ Read_Depth_Cell_Number_RevA.pdf (2018).
- Gupta, A., et al. Characterization of transcript enrichment and detection bias in single-nucleus RNA-seq for mapping of distinct human adipocyte lineages. Genome Res. 32 (2), 242-257 (2022).
- Bakken, T. E., et al. Single-nucleus and single-cell transcriptomes compared in matched cortical cell types. PLoS One. 13 (12), e0209648(2018).
- Wu, H., Kirita, Y., Donnelly, E. L., Humphreys, B. D. Advantages of single-nucleus over single-cell RNA sequencing of adult kidney: Rare cell types and novel cell states revealed in fibrosis. J Am Soc Nephrol. 30 (1), 23-32 (2019).
- Kim, N., Kang, H., Jo, A., Yoo, S. -A., Lee, H. -O. Perspectives on single-nucleus RNA sequencing in different cell types and tissues. J Pathol Transl Med. 57 (1), 52-59 (2023).
- Avila Cobos, F., Alquicira-Hernandez, J., Powell, J. E., Mestdagh, P., De Preter, K. Benchmarking of cell type deconvolution pipelines for transcriptomics data. Nat Commun. 11 (1), 5650(2020).
Access restricted. Please log in or start a trial to view this content.
재인쇄 및 허가
JoVE'article의 텍스트 или 그림을 다시 사용하시려면 허가 살펴보기
허가 살펴보기This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. 판권 소유