É necessária uma assinatura da JoVE para visualizar este conteúdo. Faça login ou comece sua avaliação gratuita.
Method Article
Um método passo-a-passo para a reconstituição de um transportador ABC em partículas lipídicas Nanodisc
Neste Artigo
Resumo
Nanodiscs são pequenas partículas discóides que incorporam proteínas de membrana em um pequeno pedaço de bicamada de fosfolipídios. Nós fornecemos um protocolo visual que mostra a incorporação passo-a-passo do transportador MalFGK2 em um disco.
Resumo
O nanodisc é uma partícula discoidal (~ 10-12 nm grande) que as proteínas de membrana armadilha em um pequeno pedaço de bicamada de fosfolipídios. O nanodisc é uma opção particularmente atraente para o estudo de proteínas de membrana, especialmente no contexto de interacção ligando-receptor. O método pioneiro Sligar e colegas baseia-se nas propriedades anfipáticas de uma engenharia altamente helicoidal uma proteína derivada do andaime apolipoproteína A1. As faces hidrofóbicas da proteína andaime interagir com os acilo gordos de cadeias laterais na bicamada lipídica que as regiões polares enfrentam o meio ambiente aquoso. As análises de proteínas de membrana em nanodiscs têm vantagens significativas sobre os lipossomas porque as partículas são pequenas, homogénea e solúvel em água. Além disso, os métodos bioquímicos e biofísicos normalmente reservadas para proteínas solúveis pode ser aplicada, e a partir de ambos os lados da membrana. Neste protocolo visual, apresenta-se uma reconstituição passo-a-passo de uma caracte bemterizada transportador ABC bacteriana, o macho-MalFGK complexo 2. A formação do disco é um processo de auto-montagem, que depende de interacções hidrofóbicas que têm lugar durante a remoção progressiva do detergente. Descrevem-se os passos essenciais e destaca-se a importância de escolher a proporção entre proteína e lípido-correcta, a fim de limitar a formação de agregados maiores e polidispersos lipossoma partículas semelhantes. Qualidade simples controles, tais como cromatografia de filtração em gel, electroforese em gel nativa e espectroscopia de dispersão de luz dinâmica garantir que os discos foram correctamente reconstituído.
Protocolo
Processo geral de reconstituição
O processo de reconstituição é iniciado por mistura da proteína de membrana de andaime (MSP) purificado com o MalFGK complexo 2, na presença de detergente solubilizados fosfolípidos. O passo é seguido pela remoção lenta do detergente por um material adsorvente chamado poliestireno Bio-Beads ou Amberlite (Figura 1). O processo de auto-montagem ocorre provavelmente devido às interacções entre os fosfolípidos apolares hidrofóbicas, o MalFGK dois complexos e a superfície da proteína MSP anfipática. O produto final é uma partícula discóide feito de duas moléculas de invólucro em torno do MSP 2 MalFGK complexo. As partículas são separadas a partir dos aductos e agregados por ultracentrifugação e cromatografia de exclusão de tamanho analítica. As partículas são caracterizadas por electroforese em gel nativa e espectroscopia de espalhamento dinâmico da luz.
título "> Preparação 1. Andaime da Membrana Proteínas, MSP- A sua marcada com MSP (versão MSP1D1 1) é produzido a partir do plasmídeo em E. pMSP1D1 coli BL21 (DE3), induzida em OD 600 ~ 0,5 com 0,5 mM de isopropil β-D-1-tiogalactopiranósido durante 3 horas a 37 ° C.
- As células são colhidas por centrifugação a 5000 xg durante 10 min a 4 ° C e ressuspensas em tampão contendo 100 TSG10 fluoreto de fenilmetano uM.
- As células são lisadas com uma prensa francesa (3x) a 8000 psi e o material insolúvel é removido por centrifugação a 5000 xg durante 10 min a 4 ° C. A fracção solúvel contendo o MSP é isolado por ultra-centrifugação a 125.000 xg durante 45 min.
- A MSP é purificado por cromatografia de níquel-quelante usando ~ 1,5 ml de Ni Sepharose HP em TSG10 buffer. Os contaminantes são removidos por lavagem com TSG10 tampão contendo 50 mM de imidazole. A MSP é eluída com TSG10 tampão contendo 600 mMimidazole. A proteína purificada é dialisada em TSG10 tampão e armazenado em -70 ° C a uma concentração de proteína de ~ 10-15 mg / ml.
2. Preparação do Complexo 2 MalFGK
- O MalFGK complexo 2, his-etiquetadas no terminal C de Malk, é expressa a partir do plasmídeo pBAD22-FGK em E. coli BL21 (DE3) e induzido a OD 600 ~ 0,5 com 0,2% de L-arabinose, durante 3 horas a 37 ° C.
- Seguindo a lise das células e centrifugação, tal como no passo 1.3, o sedimento de membrana foi ressuspenso em TSG20 tampão a uma concentração final de 5 mg / ml. O material é solubilizado com 1% w / v de n-dodecil-β-maltopyranoside (DDM), durante 3 horas a 4 ° C com agitação suave.
- O material insolúvel é removido por ultra-centrifugação como descrito no passo 1.3 e o sobrenadante contendo o solubilizado MalFGK complexa 2 é recolhido e purificado como descrito no passo 1.4, mas sem diálise.
- Further purificação é alcançada por cromatografia de filtração em gel em tampão TSGD num Superdex 200 HR 10/300 coluna a uma taxa de fluxo de 0,5 ml / min.
3. Preparação de Fosfolípidos
- Uma E. coli total de lípidos extrair dissolvido em clorofórmio é separada em alíquotas de 1000 nmol em tubos de microcentrífuga de tampa roscada. O solvente é evaporado sob uma corrente suave de azoto e secou-se ainda mais durante a noite num exsicador de vácuo.
- A película de lípido é dissolvido em tampão TS a 5 nM de concentração final e agitadas vigorosamente e sonicada. Os lípidos dissolvidos aparece ligeiramente opaca, devido à sua insolubilidade em geral em tampão TS aquosa, mas deve permanecer em suspensão. DDM é adicionado a uma concentração final de 0,5% (~ 10 mM), em que a solução se torne clara.
- A mistura lipídica é colocada num banho de água e de impulsos ultra-sons durante 5 vezes para ~ 5 seg. A mistura lipídica é armazenado a 4 ° C por um período máximo de 1 week.
4. Preparação de Bio-Beads
- Aproximadamente 10-15 ml (volume seco) Bio-Beads é colocado dentro de um tubo de 50 ml.
- As esferas são lavadas, sucessivamente, com 50 ml de metanol a 100%, etanol a 95%, H 2 O milliQ, e finalmente tampão TS (duas vezes cada).
- As pérolas lavadas são armazenadas a 4 ° C em tampão TS ~ 10 ml.
5. Reconstituição Nanodisc
- A MSP é diluída em tampão TSGD na concentração final de ~ 7 mg / ml (~ 0,3 mM).
- ~ Nmol 2 de purificado MalFGK complexo 2 são misturados numa relação proteína: lípido de 1:3:60 ou 1:3:400 em tampão TSGD: MSP. A concentração final é de 6 uM MalFGK 2, 18 | iM de MSP e lípidos uM 360 (1:3:60) ou 2,4 mM de lípidos (1:3:400). O volume final é de 300 uL. A concentração final de DDM é de 0,08% (~ 1,6 mM). A concentração final de glicerol depende da quantidade de lípido adicionado, mas permanece em torno de 5-10% v / v
- ~ 50 ul de Bio-Bead suspensão é adicionado ao tubo, e a mistura é incubada durante a noite numa mesa oscilante, a 4 ° C.
- As esferas são sedimentadas por gravidade e a solução é pipetada através de uma ponta estreita para evitar tanto Bio-Beads possível.
- Grande precipitados são removidos por ultra-centrifugação a 100.000 xg durante 20 min. Os discos são purificados por cromatografia de filtração em gel como descrito no passo 2.4 em TSG10 buffer. As fracções contendo os discos são reunidas e uma parte alíquota deve ser re-injectada na mesma coluna de filtração em gel para testar a estabilidade da preparação.
- Os discos purificados podem armazenado a -70 ° C por um período de tempo prolongado. Seguindo o descongelamento em gelo, os discos devem ser submetidas a ultra-centrifugação como descrito no passo 5.5 para remover precipitados potencial. Uma alíquota deve ser analisada por cromatografia de filtração em gel para assegurar que a agregação ou precipitação significativa não ocorreu durante o descongelamentoprocesso.
6. Eletroforese em gel nativo
- 1 uM de nanodiscs (~ 0,2 mg / ml) são analisadas por PAGE nativa 6, 7 (Tris-HCl pH 8,8, 4-12%) para avaliar a qualidade da reconstituição (Figura 3A).
- A ligação de MalE (1 uM) para o complexo de 2-MalFGK reconstituída em nanodiscs é também avaliada por PAGE-nativo (Figura 3A).
- Após a electroforese, o gel é corado com azul de Coomassie durante 10 min, e descorados durante ~ 1 hora.
7. Espalhamento de luz dinâmico (DLS)
- Nanodiscs são purificados por cromatografia de filtração em gel como descrito no passo 2.4 em TSG10 tampão utilizando uma coluna Superdex 200 HR 10/300 coluna com um caudal de 0,1 ml / min. As fracções contendo nanodiscs são reunidas e concentradas até ~ 10 mg / ml com um filtro Amicon centrífuga.
- A amostra é filtrada duas vezes (filtro de 0,22 nm) antes da análise por DLS usandoum Dynapro nanostar instrumento (Wyatt Technology), em um volume de 1 ul interior da cuvete de quartzo. Os dados são ajustados usando o software DINÂMICA (Wyatt Technology) para estimar o diâmetro e peso molecular das partículas.
8. Medidas ATPase
- A actividade de ATPase de MalFGK 2-reconstituídos nanodiscs é determinada utilizando um ensaio colorimétrico 8.
- 1 uM de discos purificadas e 1 mM de ATP são misturados com quantidades crescentes de MalE C e incubado a 37 ° C durante 20 min. A libertação de fosfato inorgânico é medida a 660 nm.
- A quantidade de fosfato libertado é comparada com uma curva padrão gerada com uma solução padrão de fósforo.
9. Resultados representativos
Os nanodiscs são purificados por cromatografia de filtração em gel (Figura 2A, à esquerda). O cromatograma mostra que a maioria do d reconstituídoISCs eluir (preto traço) como um único pico, enquanto que os discos feitos com lípidos em excesso (vermelho traço) eluem no volume vazio e como uma série de picos largos. A qualidade dos nanodiscs é ainda analisada por electroforese em gel nativa e espectroscopia de espalhamento dinâmico da luz (DLS). Discos adequadamente reconstituídas migrar como uma banda acentuada no gel enquanto aquelas reconstituída, na presença de um excesso de lípidos migrar como uma mancha (Figura 2A, à direita). A análise por DLS mostra que a população seja homogénea disco com um diâmetro médio de 11,4 nm (Figura 2B). Os discos reconstituídos têm um peso molecular aparente de 215 kDa com base na aproximação DLS. As amostras reconstituídas, na presença de excesso de lipídeos exibem largamente distribuído raios em torno de 100 nm, o que é típico para as amostras não homogéneos.
A qualidade da 2 MalFGK complexo é avaliada por electroforese em gel nativa e a sua actividade ATPase pelamedições (Figura 3). A proteína de ligação à maltose MalE liga com uma afinidade maior para o transportador 2 MalFGK 9, 10. Usando a electroforese não desnaturante em gel, é possível detectar um complexo entre o macho ea MalFGK 2 (Figura 3A). A estimulação da actividade de ATPase Malk 2 por MalE é mostrado na Figura 3B.
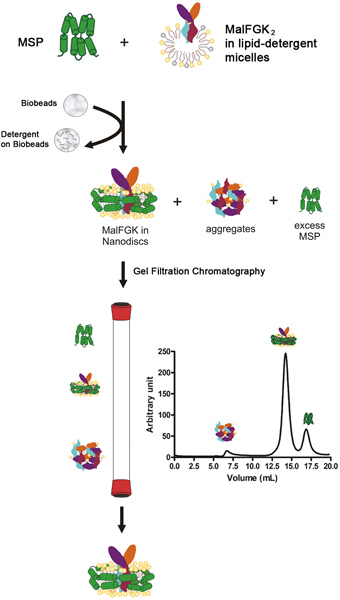
Figura 1. Fluxograma típico para o protocolo de reconstituição.
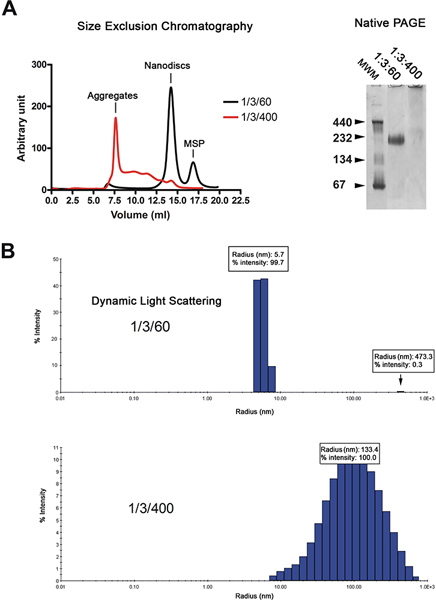
Figura 2. O controle de qualidade da preparação nanodisc. A. A análise de filtração em gel (Superdex 200 HR 10/300 coluna) das nanodiscs reconstituídos em relação lípido baixa (1/3/60; traço negro) ou a razão de lípidos elevados (1/3/400; traço vermelho). Electroforese em gel nativo de preparação do mesmo disco. MolOs marcadores de peso ecular em kDa é indicado. B. análise dinâmica de espalhamento de luz da preparação mesmo disco. Clique aqui para ver maior figura .

Figura 3. Análise da MalFGK 2 nanodisc-partículas. A. Análise de gel mudança do sexo masculino incubadas com quantidades crescentes de MalFGK 2-nanodisc partículas. B. A actividade ATPase da MalFGK 2-nanodisc partículas em função da concentração de MalE.
Discussão
Descreve-se um procedimento simples para a reconstituição do transportador de maltose em nanodiscs. O transportador é ATPase ativa e da interação com o macho parceiro solúvel ligação pode ser recriado (Figura 3). A reconstituição bem sucedida do transportador em nanodiscs abrir o caminho para análise biofísica e bioquímica suplementar. De interesse particular será a análise sistemática da ATPase Malk e maltose a actividade de transporte de detergente, lipossomas e nanodiscs. Transportado...
Divulgações
Não há conflitos de interesse declarados.
Agradecimentos
Este trabalho foi financiado pelo Instituto Canadense de Pesquisa em Saúde. CSC foi financiado por uma bolsa de pós-doutorado de Ciências Naturais e Engenharia do Canadá. FD é um Tier II Cátedra de Pesquisa do Canadá.
Materiais
| Name | Company | Catalog Number | Comments | ||||||||||||||||||||||||||||||
| Nome do reagente | Companhia | Número de catálogo | Comentários | ||||||||||||||||||||||||||||||
| Amicon Ultra-4 50K filtro centrífugo | Millipore | UFC805008 | Siga o protocolo do fabricante para o uso adequado | ||||||||||||||||||||||||||||||
| Bio-Beads SM-2 Adsorvente | Bio-Rad | 152-3920 | |||||||||||||||||||||||||||||||
| E. coli lipídios totais | Lipídios Avanti Polar | 100500C | Dissolvido em clorofórmio, como apropriado para tratar um solvente orgânico | ||||||||||||||||||||||||||||||
| Ni Sepharose HP resina | GE Healthcare | 17-5268-01 | |||||||||||||||||||||||||||||||
| Solução padrão de fósforo | Sigma-Aldrich | P3869 | |||||||||||||||||||||||||||||||
| pMSP1D1 | Addgene | 20061 | |||||||||||||||||||||||||||||||
| Superdex 200 HR 10/300 | GE Healthcare | 17-5172-01 | |||||||||||||||||||||||||||||||
| Reagentes tabela I. Específicos. | |||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||
Referências
- Denisov, I. G., Ginkova, Y. V., Lazarides, A. A., Sligar, S. G. Directed self-assembly of monodisperse phospholipid bilayer Nanodiscs with controlled size. J. Am. Chem. Soc. 126, 3477-3487 (2004).
- Boldog, T., Grimme, S., Li, M., Sligar, S. G., Hazelbauer, G. L. Nanodiscs separate chemoreceptor oligomeric states and reveal their signaling properties. Proc. Natl. Acad. Sci. USA. 103, 11509-11514 (2006).
- Bass, B. J., Denisov, I. G., Sligar, S. G. Homotropic cooperativity of monomeric cytochrome P450 3A4 in a nanoscale native bilayer environment. J. Biol. Chem. 282, 7066-7076 (2007).
- Alami, M., Dalal, K., Lelj-Garolla, B., Sligar, S. G., Duong, F. Nanodiscs unravel the interaction between the SecYEG channel and its cytosolic partner SecA. EMBO J. 26, 1995-2004 (2007).
- Mi, L. -. Z., Grey, M. J., Nishida, N., Walz, T., Lu, C., Springer, T. A. Functional and structural stability of the epidermal growth factor receptor in detergent micelles and phospholipid nanodiscs. Biochemistry. 47, 10314-10323 (2008).
- Schägger, H., Cramer, W. A., von Jagow, G. Analysis of molecular masses and oligomeric states of protein complexes by blue native electrophoresis and isolation of membrane protein complexes by two-dimensional native electrophoresis. Anal. Biochem. 217, 220-230 (1994).
- Dalal, K., Duong, F. Reconstitution of the SecY translocon in Nanodiscs. Methods Mol. Biol. 619, 145-156 (2010).
- Lanzetta, P. A., Alvarez, L. J., Reinach, P. S., Candia, O. A. An improved assay for nanomole amounts of inorganic phosphate. Anal. Biochem. 100, 95-97 (1979).
- Davidson, A. L., Dassa, E., Orelle, C., Chen, J. Structure, function and evolution of bacterial ATP-binding cassette systems. Microbiol. Mol. Biol. Rev. 72, 317-364 (2008).
- Bordignon, E., Grote, M., Schneider, E. The maltose ATP-binding cassette transporter in the 21st century-towards a structural dynamic perspective on its mode of action. Mol. Microbiol. 77, 1354-1366 (2010).
- Alvarez, F. J., Orelle, C., Davidson, A. L. Functional reconstitution of an ABC transporter for use in electron paramagnetic resonance spectroscopy. J. Am. Chem. Soc. 132, 9513-9515 (2010).
- Ritchie, T. K., Grinkova, Y. V., Bayburt, T. H., Denisov, I. G., Zolnerciks, J. K., Atkins, W. M., Sligar, S. G. Reconstitution of membrane proteins in phospholipid bilayer Nanodiscs. Methods Enzymol. 464, 211-231 (2009).
- Glück, J. M., Koenig, B. W., Willbold, D. Nanodiscs allow the use of integral membrane proteins as analytes in surface plasmon resonance studies. Anal. Biochem. 408, 46-52 (2011).
- Wan, C. -. P. L., Chiu, M. H., Wu, X., Lee, S. K., Prenner, E. J., Weers, P. M. M. Apolipoprotein-induced conversion of phosphatidylcholine bilayer vesicles into nanodisks. Biochim. Biophys. Acta (BBA). 1808, 606-613 (2011).
- Nath, A., Trexler, A. J., Koo, P. K., Miranker, A. D., Atkins, W. M., Rhoades, E. Single-molecule fluorescence spectroscopy using phospholipid bilayer Nanodiscs. Methods Enzymol. 472, 89-117 (2010).
- Denisov, I. G., Sligar, S. G. Cytochromes P450 in Nanodiscs. Biochim. Biophys. Acta. 1814, 223-229 (2011).
- Zhang, X. X., Chan, C. S., Bao, H., Fang, Y., Foster, L. J., Duong, F. Nanodiscs and SILAC-based mass spectrometry to identify a membrane protein interactome. J. Proteome Res. , (2011).
Reimpressões e Permissões
Solicitar permissão para reutilizar o texto ou figuras deste artigo JoVE
Solicitar PermissãoThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Todos os direitos reservados