JoVE 비디오를 활용하시려면 도서관을 통한 기관 구독이 필요합니다. 전체 비디오를 보시려면 로그인하거나 무료 트라이얼을 시작하세요.
Method Article
Nanodisc 지질 입자로 ABC의 전송의 Reconstitution을위한 단계별 방법
요약
Nanodiscs는 인지질 이중층의 작은 패치로 막 단백질을 포함 작은 원반 모양의 입자입니다. 우리는 디스크에 MalFGK2 수송의 단계별 설립을 보여줍니다 시각적 프로토콜을 제공합니다.
초록
nanodisc는 discoidal 입자 (~ 10-12 nm의 넓은)는 트랩 막 단백질 인지질 이중층의 작은 패치로.입니다 nanodisc 특히 리간드 - 수용체 상호 작용의 맥락에서, 막 단백질을 공부에 특히 매력적인 옵션입니다. 방법은 Sligar에 의해 개척 및 동료는 apolipoprotein A1에서 파생 설계 높은 - 나선형 비계 단백질의 amphipathic 특성에 기반을두고 있습니다. 극지방의 수성 환경에 직면 반면 비계 단백질의 소수성 얼굴은 지질 이중층의 지방산 아실 사이드 체인과 상호 작용할 수 있습니다. 입자가 작은 균질하고 수용성이기 때문에 nanodiscs의 막 단백질의 분석은 리포좀에 비해 상당한 장점이 있습니다. 또한, 일반적으로 수용성 단백질에 예약 생화학 및 biophysical 방법이 적용하고 막 양쪽에서 할 수 있습니다. 이 시각 프로토콜에서, 우리는 잘 charac의 단계별로 reconstitution을 제시terized 세균 ABC의 전송, 남성 MalFGK이 복잡. 디스크의 형성은 세제의 진보적 인 제거에있어 소수성 상호 작용에 따라 자기 조립 과정입니다. 우리는 필수적인 단계를 설명하고 우리는 집계 및 큰 polydisperse 리포좀과 같은 입자의 형성을 제한하기 위해 올바른 단백질 - 투 - 지질의 비율을 선택의 중요성을 강조 표시합니다. 간단한 품질은 디스크가 올바르게 재구성되었는지 확인 겔 여과 크로마토 그래피, 기본 겔 전기 영동 및 동적 광 산란 분광법으로 제어합니다.
프로토콜
전체 Reconstitution 프로세스
reconstitution 과정은 세제 - solubilized phospholipids의 존재에 정화 MalFGK이 컴플렉스로 막 비계 단백질 (MSP)를 혼합하여 시작합니다. 단계는 바이오 비즈 나 Amberlite (그림 1)라는 흡착제 폴리스티렌 소재로 세제의 느린 제거을합니다. 자동 조립 공정 때문에 소수성 phospholipids, MalFGK이 복잡하고 MSP amphipathic 단백질의 표면 사이의 apolar 상호 작용의 가능성이 가장 높은 발생합니다. 최종 제품은 MalFGK이 복잡한 주변 MSP 포장의 두 분자로 만든 원반 모양의 입자입니다. 입자는 초 원심 분리 및 분석 크기 배제 크로마토 그래피에 의한 알데히드 부가 물 및 집계에서 구분됩니다. 입자는 기본 - 겔 전기 영동 및 동적 광 산란 분광법을 특징으로하고 있습니다.
막의 제목 "> 1. 준비 비계 단백질, MSP- 자신의 태그 MSP는 (버전 MSP1D1 1) E.의 플라스미드 pMSP1D1에서 생산됩니다 대장균 37 3 시간 0.5 MM 이소 프로필 β-D-1-thiogalactopyranoside와 OD 600 ~ 0.5에서 유도 BL21 (DE3) ° C.
- 셀은 4시 10 분 ° C에 5,000 XG에서 원심 분리하여 수확, 100 μM의 phenylmethanesulfonyl 불화를 포함하는 TSG10 버퍼에 resuspended 있습니다.
- 세포는 8,000 PSI에 프랑스 프레스 (3 배)으로 lysed하고 불용성 물질은 4 ° C.에서 10 분 동안 5,000 XG에서 원심 분리에 의해 제거됩니다 MSP를 포함하는 수용성 분율은 45 분에 125,000 XG에 초 원심 분리에 의해 분리된다.
- MSP는 니켈 - 상기 킬레이트 화 크로마토 그래피는 TSG10 버퍼에 ~ 1.5 ML 니켈 세 파로스 HP를 사용하여 정화되어 있습니다. 오염 물질은 50 MM 이미 다졸을 포함하는 TSG10 버퍼로 씻어 수 있습니다. MSP는 600 MM를 포함하는 TSG10 버퍼로 용출되어이미 다졸. 정화 단백질은 TSG10 버퍼에 dialyzed와 ~ 10-15 MG / ML의 단백질 농도에서 -70 ° C에 저장됩니다.
2. MalFGK이 단지의 작성
- MalFGK이 단지는 MalK의 C-말단에 자신의 태그, E.의 플라스미드 pBAD22 - FGK에서 표현됩니다 대장균 BL21 (DE3)와 37 3 시간에 0.2 % L-arabinose와 OD 600에서 ~ 0.5 유도 ° C.
- 단계 1.3에서와 같이 세포 용해 및 원심 분리 후, 막 펠릿은 5 MG / ML의 최종 농도에 TSG20 버퍼에 resuspended 있습니다. 자료는 부드러운 진동과 4에 3 시간에 1 % W / V N-dodecyl-β-maltopyranoside (DDM) ° C로 solubilized 있습니다.
- 불용성 물질은 단계 1.3에서와 같이 초 원심 분리에 의해 제거하고 표면에 뜨는는 solubilized을 포함하고 있습니다 MalFGK이 단지는 수집 단계 1.4에서와 같이 정화하지만, 투석하지 않고 있습니다.
- FurtheR 정화는 0.5 ML / 분의 유량에서 Superdex 200 HR 3백분의 10 열 TSGD 버퍼에 겔 여과 크로마토 그래피에 의해 달성된다.
3. Phospholipids의 작성
- E. 대장균 총 지방질은 클로로포름에 용해 추출하는 것은 나사 캡 microfuge 튜브 1,000 nmol aliquots로 구분됩니다. 용매는 질소의 완만 한 흐름에 따라 증발 진공 건조기에서 추가 하룻밤 건조합니다.
- 지질 필름은 5 nm의 최종 농도에서 TS 버퍼에 용해하고 힘차게 vortexed와 sonicated 수 있습니다. 용해 지질 인해 수성 TS 버퍼에서의 일반 불용성으로 약간 불투명 나타납니다,하지만 그들은 정지에 남아 있어야합니다. DDM은 해결책이 분명해진다되는 0.5 % (~ 10 ㎜)의 최종 농도에 추가됩니다.
- 지질 혼합물은 물 목욕에 배치 및 펄스는 ~ 5 초 동안 5 회에 sonicated 수 있습니다. 지질 혼합물은 1 꼬마의 최대 4 ° C에 저장됩니다K.
4. 바이오 비즈의 작성
- 약 10-15 ML은 (드라이 볼륨) 바이오 비즈는 50 ML 튜브에 배치됩니다.
- 구슬이 연속 100 % 메탄올, 95 % 에탄올, milliQ H 2 O, 그리고 마지막으로 TS 버퍼 (두 번 각)의 50 ML에 세척되어 있습니다.
- 세척 구슬은 4에 저장됩니다 ° C ~ 10 ML TS 버퍼 인치
5. Nanodisc의 Reconstitution
- MSP는 ~ 7 MG / ML (~ 0.3 ㎜)의 최종 농도에 TSGD 버퍼에 희석되어 있습니다.
- MSP : TSGD 버퍼에 1:3:60 또는 1:3:400의 지질 비율 정화 MalFGK이 복합 ~ 2 nmol은 단백질에 혼합되어 있습니다. 최종 농도는 6 μM MalFGK 2, 18 μM의 MSP와 360 μM의 지질 (1:3:60) 또는 2.4 밀리미터 지질 (1:3:400)입니다. 최종 볼륨은 300 μl입니다. 최종 DDM 농도는 0.08 % (~ 1.6 ㎜)이다. 글리세롤의 마지막 농도가 지질의 양에 따라 달라집니다 추가 주변을 5~10% V / 대 유지
- ~ 바이오 비드 정지의 50 μl는 튜브에 추가되고 혼합은 4 ° C.에 흔들 테이블에 하룻밤 incubated 수 있습니다
- 구슬이 중력에 의해 sedimented되며 솔루션은 가능한 한 많은 바이오 비즈를 피하기 위해 좁은 팁을 통해 pipetted 있습니다.
- 침전물 대형은 20 분에 100,000 XG에 초 원심 분리에 의해 제거됩니다. 디스크는 TSG10 버퍼에 단계 2.4에서와 같이 겔 여과 크로마토 그래피에 의해 정화되어 있습니다. 디스크를 포함하는 분수는 풀링하고 나누어지는이 준비의 안정성을 테스트하기 위해 동일한 겔 여과 칼럼에 다시 주입해야합니다.
- 정화 디스크는 오랜 기간 동안 -70 ° C에 저장 할 수 있습니다. 얼음에 해동 후, 디스크는 가능성이 침전물 제거하는 단계 5.5에서와 같이 초 원심 분리를 받게해야합니다. 나누어지는이 중요한 집계 나 강수량은 해동하는 동안 발생하지 않았 음을 보장하기 위해 겔 여과 크로마토 그래피에 의해 분석되어야한다과정입니다.
6. 기본 젤 전기 영동
- nanodiscs 1 μM (~ 0.2 MG / ML)은 reconstitution (그림 3A)의 품질을 평가하는 기본 PAGE 6, 7 (트리스 - HCL 산도 8.8, 4-12 %)에 의해 분석됩니다.
- 2 단지 MalFGK 남성과의 바인딩 (1 μM)가 nanodiscs에서 재구성은 기본 페이지 (그림 3A)에 의해 평가된다.
- 전기 영동 후, 젤은 10 분에 Coomassie 파란색으로 물들어있는 것, 그리고 ~ 1 시간에 destained.
7. 동적 광 분산 (DL을)
- Nanodiscs는 0.1 ML / 분의 유량에서 Superdex 200 HR 300분의 10 열을 사용하여 TSG10 버퍼에 단계 2.4에서와 같이 겔 여과 크로마토 그래피에 의해 정화되어 있습니다. nanodiscs를 포함하는 분수는 풀링과 Amicon 원심 필터 ~ 10 MG / ML에 집중되어있다.
- 샘플을 사용하여 DL을 분석하기 전에 (0.22 μm 필터) 두 번 필터링1 μl 내부 볼륨 석영 큐벳에서 DynaPro nanostar 악기 (와이어트 기술). 데이터는 직경과 입자의 분자량을 추정하기 위해 역학 소프트웨어 (와이어트 기술)를 사용하여이 마련되어 있습니다.
8. ATPase 측정
- MalFGK 2 재구성 nanodiscs의 ATPase 활동이 colorimetric 분석 8을 사용하여 결정하고 있습니다.
- 정화 디스크와 1 ㎜ ATP의 1 μM는 20 분에 대한 남성과 37 incubated ° C의 증가 금액과 함께 혼합되어 있습니다. 무기 인산염의 릴리스는 660 nm의에서 측정된다.
- 출시 인산염의 금액은 인 표준 솔루션으로 생성 된 표준 곡선과 비교됩니다.
9. 대표 결과
nanodiscs는 겔 여과 크로마토 그래피 (그림 2A, 왼쪽)에 의해 정화되어 있습니다. 크로마토 그램은 보여줍니다 재구성 D의 대부분iscs (검은 색 추적) 하나의 피크로 elute, 반면에 과잉 지질 (빨간색 추적) 무효 볼륨의 elute로하고 폭 넓은 봉우리의 연속으로 만들어 디스크. nanodiscs의 품질은 더욱 네이티브 겔 전기 영동 및 동적 광 산란 분광법 (DL을)에 의해 분석됩니다. 지질의 과잉의 존재의 재구성 사람들은 비방 (그림 2A, 오른쪽)으로 마이그레이션 반면에 적절히 재구성 디스크는 젤에 날카로운 밴드로 마이그레이션됩니다. DL을하여 분석 디스크 인구가 11.4 nm의 (그림 2B)의 평균 직경이 균일 한 것을 보여줍니다. 재구성 디스크 DL을의 근사치에 따라 215 kDa의 명백한 분자량 있습니다. 초과 지질의 면전에서 재구성 샘플은 널리 비 균일 한 샘플에 대한 일반적인입니다, 100 nm의 주위 반경을 배포 표시됩니다.
MalFGK이 단지의 품질은 ATPase의 기본 - 겔 전기 영동과 그 활동에 의해 평가된다측정 (그림 3). 말토오스 결합 단백질 남자는 MalFGK이 전송 9, 10에 높은 친 화성을 바인딩합니다. 사용하지 않는 denaturing 겔 전기 영동,이 남성과 MalFGK 2 (그림 3A) 사이에 복잡한을 감지 할 수 있습니다. 수컷이 MalK이 ATPase 활동의 자극은 그림 3B에 표시됩니다.
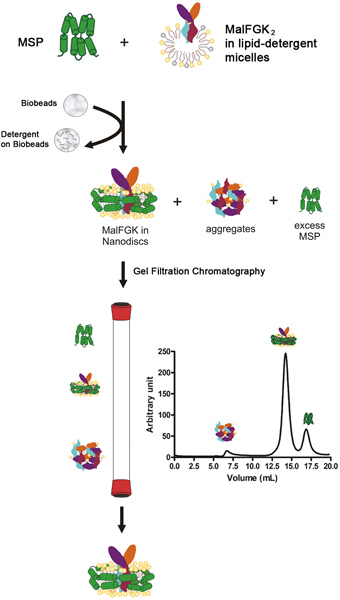
1 그림. reconstitution 프로토콜에 대한 일반적인 흐름도.
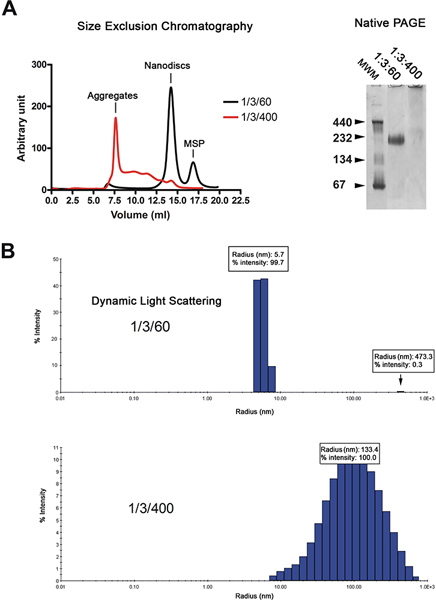
그림 2. nanodisc 준비. A. 품질 관리 또는 높은 지질 비율 (1/3/400, 붉은 색 추적), nanodiscs의 젤 여과 분석 (Superdex 200 HR 3백분의 10 열)은 낮은 지질 비율 (검은 색 추적 1/3/60)에서 재구성. 동일한 디스크 준비 기본 겔 전기 영동. 몰kDa의 ecular 중량 표시가 표시됩니다. 동일한 디스크 준비 B. 동적 광 산란 분석. 큰 그림을 보려면 여기를 클릭하십시오 .

그림 3. MalFGK 2 nanodisc 입자의 분석. A. 남성의 젤 이동 분석은 MalFGK 2 nanodisc 입자의 증가 금액과 incubated. MalFGK의 B. ATPase 활동 2 nanodisc 남성 농도의 함수로 입자.
토론
우리는 nanodiscs에 말토오스 수송의 reconstitution에 대한 간단한 절차를 설명합니다. 전송은 ATPase 활성 상태이며 수용성 바인딩 파트너 남성과의 상호 작용은 (그림 3) 재현 할 수 있습니다. nanodiscs에 전송의 성공 reconstitution 추가 biophysical 및 생화학 분석 방법을 엽니 다. 특히 관심 MalK ATPase 및 세제의 말토오스 수송 활동, 리포좀과 nanodiscs 체계적인 분석됩니다. ABC의 이동 장치는 전송 사?...
공개
관심 없음 충돌이 선언 없습니다.
감사의 말
이 작품은 건강 연구의 캐나다 연구소에 의해 지원되었다. CSC는 자연 과학 및 캐나다의 공학 연구위원회에서 박사 친목의 지원을받는되었다. FD는 등급 II 캐나다 연구 의자입니다.
자료
| Name | Company | Catalog Number | Comments | ||||||||||||||||||||||||||||||
| 시약의 이름 | 회사 | 카탈로그 번호 | 코멘트 | ||||||||||||||||||||||||||||||
| Amicon 울트라-4 50K 원심 필터 | Millipore | UFC805008 | 적절한 사용을 위해 제조업체의 규정을 따르 | ||||||||||||||||||||||||||||||
| 바이오 비즈 SM-2 흡착제 | 바이오 RAD | 152-3920 | |||||||||||||||||||||||||||||||
| 대장균 총 지질 | 벤티 폴라 지질 | 100500C | 클로로포름에 용해, 유기 용매에 따라 처리 | ||||||||||||||||||||||||||||||
| 니켈 세 파로스 HP 수지 | GE 헬스 케어 | 17-5268-01 | |||||||||||||||||||||||||||||||
| 인 표준 솔루션 | 시그마 - 알드리치 | P3869 | |||||||||||||||||||||||||||||||
| pMSP1D1 | Addgene | 20,061 | |||||||||||||||||||||||||||||||
| Superdex 200 HR 3백분의 10 | GE 헬스 케어 | 17-5172-01 | |||||||||||||||||||||||||||||||
| 표 I. 특정 시약. | |||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||
참고문헌
- Denisov, I. G., Ginkova, Y. V., Lazarides, A. A., Sligar, S. G. Directed self-assembly of monodisperse phospholipid bilayer Nanodiscs with controlled size. J. Am. Chem. Soc. 126, 3477-3487 (2004).
- Boldog, T., Grimme, S., Li, M., Sligar, S. G., Hazelbauer, G. L. Nanodiscs separate chemoreceptor oligomeric states and reveal their signaling properties. Proc. Natl. Acad. Sci. USA. 103, 11509-11514 (2006).
- Bass, B. J., Denisov, I. G., Sligar, S. G. Homotropic cooperativity of monomeric cytochrome P450 3A4 in a nanoscale native bilayer environment. J. Biol. Chem. 282, 7066-7076 (2007).
- Alami, M., Dalal, K., Lelj-Garolla, B., Sligar, S. G., Duong, F. Nanodiscs unravel the interaction between the SecYEG channel and its cytosolic partner SecA. EMBO J. 26, 1995-2004 (2007).
- Mi, L. -. Z., Grey, M. J., Nishida, N., Walz, T., Lu, C., Springer, T. A. Functional and structural stability of the epidermal growth factor receptor in detergent micelles and phospholipid nanodiscs. Biochemistry. 47, 10314-10323 (2008).
- Schägger, H., Cramer, W. A., von Jagow, G. Analysis of molecular masses and oligomeric states of protein complexes by blue native electrophoresis and isolation of membrane protein complexes by two-dimensional native electrophoresis. Anal. Biochem. 217, 220-230 (1994).
- Dalal, K., Duong, F. Reconstitution of the SecY translocon in Nanodiscs. Methods Mol. Biol. 619, 145-156 (2010).
- Lanzetta, P. A., Alvarez, L. J., Reinach, P. S., Candia, O. A. An improved assay for nanomole amounts of inorganic phosphate. Anal. Biochem. 100, 95-97 (1979).
- Davidson, A. L., Dassa, E., Orelle, C., Chen, J. Structure, function and evolution of bacterial ATP-binding cassette systems. Microbiol. Mol. Biol. Rev. 72, 317-364 (2008).
- Bordignon, E., Grote, M., Schneider, E. The maltose ATP-binding cassette transporter in the 21st century-towards a structural dynamic perspective on its mode of action. Mol. Microbiol. 77, 1354-1366 (2010).
- Alvarez, F. J., Orelle, C., Davidson, A. L. Functional reconstitution of an ABC transporter for use in electron paramagnetic resonance spectroscopy. J. Am. Chem. Soc. 132, 9513-9515 (2010).
- Ritchie, T. K., Grinkova, Y. V., Bayburt, T. H., Denisov, I. G., Zolnerciks, J. K., Atkins, W. M., Sligar, S. G. Reconstitution of membrane proteins in phospholipid bilayer Nanodiscs. Methods Enzymol. 464, 211-231 (2009).
- Glück, J. M., Koenig, B. W., Willbold, D. Nanodiscs allow the use of integral membrane proteins as analytes in surface plasmon resonance studies. Anal. Biochem. 408, 46-52 (2011).
- Wan, C. -. P. L., Chiu, M. H., Wu, X., Lee, S. K., Prenner, E. J., Weers, P. M. M. Apolipoprotein-induced conversion of phosphatidylcholine bilayer vesicles into nanodisks. Biochim. Biophys. Acta (BBA). 1808, 606-613 (2011).
- Nath, A., Trexler, A. J., Koo, P. K., Miranker, A. D., Atkins, W. M., Rhoades, E. Single-molecule fluorescence spectroscopy using phospholipid bilayer Nanodiscs. Methods Enzymol. 472, 89-117 (2010).
- Denisov, I. G., Sligar, S. G. Cytochromes P450 in Nanodiscs. Biochim. Biophys. Acta. 1814, 223-229 (2011).
- Zhang, X. X., Chan, C. S., Bao, H., Fang, Y., Foster, L. J., Duong, F. Nanodiscs and SILAC-based mass spectrometry to identify a membrane protein interactome. J. Proteome Res. , (2011).
재인쇄 및 허가
JoVE'article의 텍스트 или 그림을 다시 사용하시려면 허가 살펴보기
허가 살펴보기This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. 판권 소유