Method Article
Um método eficiente para a produção de adenovírus
Neste Artigo
Resumo
Aqui, apresentamos um protocolo para a produção de adenovírus usando o sistema pAdEasy. A tecnologia inclui a recombinação dos plasmídeos pAdEasy-1, a embalagem e amplificação do adenovírus, a purificação das partículas adenovirais do meio de cultura e lise celular, a titulação viral e o teste funcional do adenovírus.
Resumo
A transdução adenoviral tem a vantagem de uma forte e transitória indução da expressão do gene de interesse em uma ampla variedade de tipos e órgãos celulares. No entanto, a tecnologia adenoviral recombinante é trabalhosa, demorada e cara. Aqui, apresentamos um protocolo aprimorado usando o sistema pAdEasy para obter partículas adenovirais purificadas que podem induzir uma forte expressão de proteína fluorescente verde (GFP) em células transduzidas. As vantagens deste método melhorado são a preparação mais rápida e a diminuição do custo de produção em comparação com o método original desenvolvido por Bert Vogelstein. Os principais passos da tecnologia adenoviral são: (1) a recombinação do pAdTrack-GFP com o plasmídeo pAdEasy-1 na bactéria BJ5183; (2) a embalagem das partículas adenovirais; (3) a amplificação do adenovírus em células AD293; (4) a purificação das partículas adenovirais a partir do liseto celular e do meio da cultura; e (5) a titulação viral e testes funcionais do adenovírus. As melhorias no método original consistem em (i) a recombinação em BJ5183-contendo pAdEasy-1 por transformação química de bactérias; (ii) a seleção de clones recombinantes por PCR "negativo" e "positivo"; (iii) a transfecção de células AD293 utilizando o sistema de transfecção K2 para embalagem adenoviral; (iv) a precipitação com sulfato de amônio das partículas virais liberadas pelas células AD293 em meio de cultura celular; e (v) a purificação do vírus por ultracentrifugação de cloreto de césio de uma etapa. Uma forte expressão do gene de interesse (neste caso, GFP) foi obtida em diferentes tipos de células transduzidas (como hepatócitos, células endoteliais) de várias fontes (humana, bovina, murina). A transferência genética mediada por adenoviral representa uma das principais ferramentas para o desenvolvimento de terapias genéticas modernas.
Introdução
Os adenovírus são vírus não desenvolvidos contendo um nucleocapsídeo e um genoma de DNA linear de dupla cadeia1,2,3. Os adenovírus podem infectar uma ampla gama de tipos de células e a infecção não depende da divisão ativa de células hospedeiras. Após a infecção, o adenovírus introduz seu DNA genômico no núcleo celular hospedeiro, onde permanece epicosomal e é transcrito junto com os genes do hospedeiro. Assim, é atingido um risco potencial mínimo para a mutagênese insercional ou regulação oncogênica4,5,6. O genoma adenoviral não é replicado junto com o genoma hospedeiro e, portanto, os genes adenovirais são diluídos em uma população celular divisória. Entre as vantagens da transdução adenoviral, há: (i) altos níveis de expressão transgênica; (ii) redução dos riscos relacionados à integração do DNA viral no genoma hospedeiro, devido à expressão epissomal; (iii) transdução de uma grande variedade de tipos celulares divisórias e não-divisórias. A maioria dos adenovírus utilizados em pesquisas biomédicas são não replicativos, sem a região E17,8,9. Para sua produção, é necessária uma linha celular que forneça a sequência E1 (como HEK293). Além disso, uma região não essencial para o ciclo de vida viral (E3) foi suprimida para permitir a inserção de um transgene no genoma viral; outras regiões (E2 e E4) foram ainda suprimidas em alguns adenovírus, mas nesses casos, foram relatados7.
Aqui, apresentamos um protocolo aprimorado para construir, empacotar e purificar os adenovírus usando o Sistema AdEasy. Essas melhorias permitiram a embalagem do adenovírus de forma mais rápida e econômica em comparação com o método original desenvolvido por Bert Vogelstein2,10, devido às seguintes vantagens: (i) a recombinação em BJ5183-contendo pAdEasy-1 pela transformação química de bactérias; (ii) a seleção dos clones recombinantes por PCR; (iii) a transfecção de células AD293 utilizando o sistema de transfecção K2 para embalagem adenoviral; (iv) a precipitação de partículas adenovirais do meio de cultura após embalagem e amplificação virais; v A purificação adenoviral utilizando ultracentrifugação de cloreto de césio de uma etapa (CsCl).
O protocolo para a produção de adenovírus utilizando o sistema AdEasy (Figura 1) compreende as seguintes etapas:
(1) Recombinação do pAdTrack-GFP com pAdEasy-1 em bactérias BJ5183
(2) Embalagem das partículas adenovirais
(3) Amplificação do adenovírus
(4) Purificação das partículas adenovirais do meio de lise celular e cultura
(5) Titulação do Adenovírus.
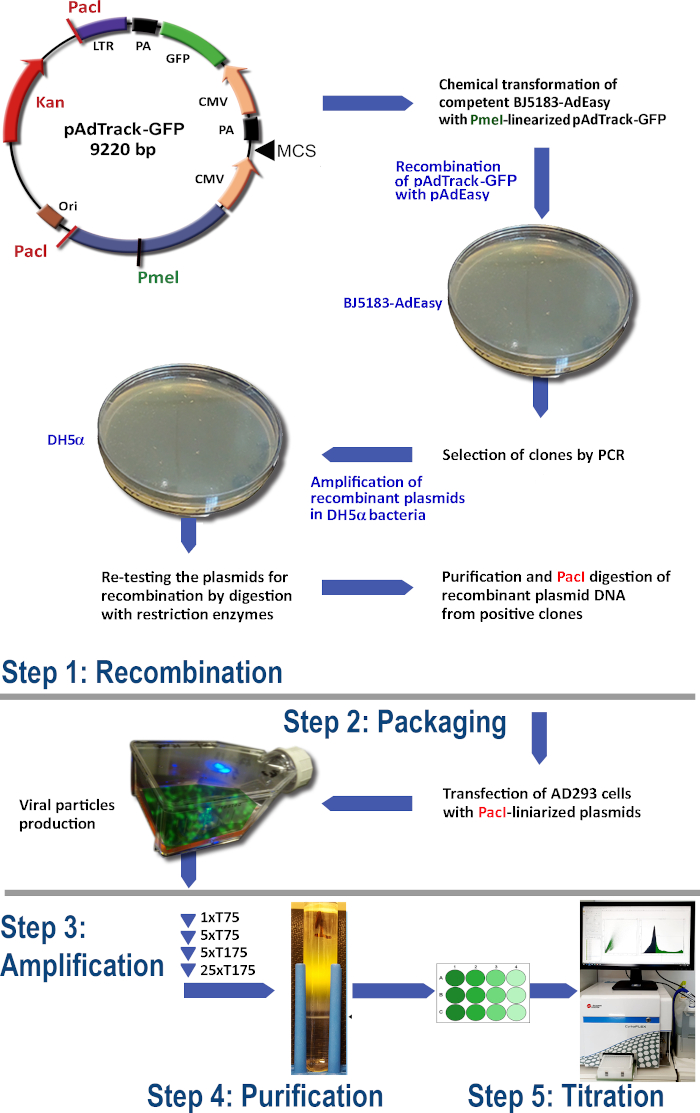
Figura 1: A tecnologia de produção de adenovírus. Os principais passos da tecnologia adenoviral são: (1) A recombinação do pAdTrack-GFP com o plasmídeo pAdEasy-1 na bactéria BJ5183. Os plasmídeos recombinados selecionados são amplificados em bactérias DH5α e, em seguida, purificados; (2) A embalagem das partículas adenovirais em células AD293, que produzem proteínas adeno-E1; (3) A amplificação do adenovírus em células AD293; (4) A purificação das partículas adenovirais do lisecelular e do meio de cultura por ultracentrifugação em um gradiente de densidade CsCl; (5) A titulação do adenovírus e dos testes funcionais. Clique aqui para ver uma versão maior desta figura.
Neste protocolo, exemplificamos a tecnologia para a produção do adenovírus, que pode induzir a expressão de GFP nas células hospedeiras. O GFP já está inserido na espinha dorsal do vetor de transporte pAdTrack-CMV (Addgene #16405), sob um segundo promotor cmv e é usado como um gene repórter(Figura 1). Por essa razão, aqui designamos o vetor pAdTrack-CMV como pAdTrack-GFP e avaliamos a expressão do GFP para fins demonstrativos. Além da expressão GFP, o sistema pode ser usado para superexpressar um gene de interesse, que pode ser clonado nos vários locais de clonagem do pAdTrack-CMV. Um gene ou um minigene clonado no pAdTrack-CMV geralmente é mais eficiente para indução de expressão em comparação com o cDNA11. Os dados mostraram uma forte expressão de GFP em células transduzidas (como hepatócitos, células endoteliais) de várias fontes (humana, bovina, murina). A transferência genética mediada por adenoviral representa uma das principais ferramentas para o desenvolvimento de terapias genéticas modernas.
Protocolo
Nota de segurança: Em geral, os adenovírus são classificados como organismos de nível 2 de biossegurança e, portanto, todas as manipulações devem ser feitas em um armário de biossegurança classe II por uma pessoa treinada, usando equipamento de proteção de risco biológico (incluindo luvas, máscara facial para aerossóis biológicos, jaleco, etc.). Todos os materiais sólidos contaminados com o adenovírus devem ser desinfetados com uma solução de alvejante de 10% para 30 min e autoclaved por 30 min a 121 °C e 1 bar. Dependendo do gene inserido, o adenovírus criado pode ter potencial perigoso e pode ser classificado em outros níveis de biossegurança.
1. Preparação experimental
- Use uma capa de cultura celular separada para manipulações adenovirais e uma incubadora separada para cada tipo de adenovírus. Use frascos T com tampas de filtro para embalagem e amplificação virais; evitar tanto quanto possíveis experimentos de transdução em placas de Petri ventiladas.
- Esvazie o capô da cultura celular após cada uso e exponha-o a UV por 15 minutos.
- Autoclave periodicamente o auxílio pipeta, pipetas e outros utensílios. Se possível, cultura em um laboratório de cultura celular separada/capuz as células para embalagens adenovirais (células AD293) e as células a serem usadas em experimentos de transdução. Lotes de adenovírus diferentes amplificados no mesmo período devem ser verificados quanto à contaminação cruzada por PCR.
- Prepare as seguintes soluções.
- Prepare o meio SOB (Caldo Super Ótimo): 20 g de triptona, 5 g de extrato de levedura, 0,5 g de NaCl (concentração final de 10 mM), 2,5 mL de 1 M KCl (concentração final de 2,5 mM), amd H2O a 1 L. Após autoclaving a 121 °C, adicione as seguintes soluções estéreis: 5 mL de 1 M MgCl2 e 5 mL de 1 M MgSO4.
- Prepare SOC (Caldo Super Ideal com repressão catabólica) médio: em 1 L estéril SOB adicione as seguintes soluções estéreis: 20 mL de glicose de 1 M, 5 mL de 1 M MgCl2 e 5 mL de 1 M MgSO4.
- Prepare a solução de precipitação: dissolva 29,5 g de acetato de potássio em 60 mL de H2O, adicione 11,5 mL de ácido acético e H2O a 100 mL.
- Prepare o tampão de resuspensão: 95 mL de 20% de glicose, 5 mL de 1 M Tris-Cl pH 8, 4 mL de 0,5 M EDTA pH 8 e adicione H2O a 200 mL.
- Solução de lise de preparação: 4,8 mL de 8,3 M NaOH, 10 mL de SDS 20% e H2O a 200 mL.
2. Recombinação do vetor viral pAdTrack-GFP com plasmídeo pAdEasy-1 em bactérias BJ5183
- Linearização do pAdTrack-GFP e purificação do plasmídeo linearizado.
- Prepare a seguinte mistura de digestão no gelo:
10 μg de pAdTrack-GFP
5 μL de tampão incolor de 10x
2 μL de Pme I
H2O de um volume final de 50 μL. - Incubar a 37 °C durante 3 horas em banho-maria.
- Inativar a 65 °C por 20 min.
- Verifique a eficiência da digestão do pAdTrack-GFP com Pme I: execute 1 μg do plasmídeo digerido em paralelo com 1 μg de plasmídeo não digerido em um gel de 0,8%.
- Prepare a seguinte mistura de digestão no gelo:
- Isolamento e purificação do DNA
NOTA: As etapas 1-6 precisam ser realizadas em um capô de fumaça.- Adicione um volume igual de fenol/clorofórmio/álcool isoamílico (25:24:1) sobre a mistura de digestão e inverta o tubo até que a mistura fique homogênea.
- Centrifugar por 3 min a 16.200 x g, e, em seguida, transferir a fase aquosa superior para um tubo de coleta.
- Adicione um volume igual de fenol/clorofórmio/álcool isoamílico (25:24:1) sobre a fase orgânica inferior e vórtice.
- Centrifugar por 3 min a 16.200 x g, e depois transferir a fase superior para o mesmo tubo de coleta.
- Adicione um volume igual de clorofórmio sobre a fase aquosa colhida no tubo de coleta e vórtice.
- Centrifugar por 3 min a 16.200 x g, e, em seguida, transferir a fase aquosa superior para um novo tubo de coleta.
- Adicione um volume de 1/10 de acetato de sódio de 3 M, e 2 volumes de frio 100% etanol e vórtice.
- Incubar por 1 hora a -70 °C ou durante a noite a -20 °C.
- Descongele a amostra no gelo e centrífuga por 10 minutos a 16.200 x g e 4 °C.
- Retire o supernascente e adicione 750 μL de 75% de etanol.
- Centrifugar por 3 min a 16.200 x g e 4 °C e remover o supernaspe.
- Gire brevemente o tubo para remover todo o supernatante e seque a pelota no capô. Não seque a pelota de DNA por muito tempo porque é complicado dissolver.
- Dissolva a pelota em 15 μL de H2O.
- Meça a concentração de DNA usando um espectrofotômetro (por exemplo, Nanodrop).
- Transformação de bactérias AdEasier-1 com pAdTrack-GFP
NOTA: Nesta etapa, ocorre a recombinação do pAdTrack-GFP com o plasmid pAdEasy-1.- Preparar o AdEasier-1 (BJ5183 contendo pAdEasy-1, Addgene #16399) bactérias químicas competentes, utilizando um kit de transformação comercial, seguindo as instruções dos fabricantes. Mantenha alíquotas de 100 μL bactérias competentes a -80 °C.
- Descongele uma alíquota de bactérias AdEasier-1 competentes no gelo e adicione 1 μg de Pme I -digerido pAdTrack-GFP purificado. Misture suavemente apertando o tubo (não encobre a mistura). Incubar por 10 minutos no gelo.
- Adicione 900 μL de soc médio e incubar por 1 hora a 37 °C com agitação.
- Microfuge por 5 min a 600 x g.
- Remova 900 μL do supernante, misture a pelota e o supernante, e semee as bactérias transformadas em placas lb-ágar com kanamicina.
- Incubar por ~16 horas a 37 °C (não exceda 18 horas).
- Seleção dos possíveis clones positivos por PCR
- Divida os palitos em duas metades e esterilize os palitos meio palitos autoclavando.
- Pegue colônias pequenas e translúcidas usando palitos estéreis.
- Brevemente, gire o palito de meio palito com bactérias em 10 μL de água (em um tubo PCR) e, em seguida, coloque o palito de meio palito em um tubo Eppendorf de 1,5 mL contendo 100 μL SOC médio com kanamicina. Incubar por 4-6 horas a 37 °C, enquanto você testa os clones por PCR "negativo" e "positivo".
- Incubar os tubos PCR contendo 10 μL de água com bactérias por 5 min a 95 °C para obter a amostra bacteriana e executar em paralelo o PCR "negativo" e "positivo".
- PCR "negativo" - para testar a integridade pAdTrack-GFP: Prepare a seguinte mistura pcr para o PCR negativo no gelo.
5 μL da amostra bacteriana
0.1 μL de primer Forward (4631 F: 5'-CAGTAGTCGGTGCTCGTCCAG)
0,1 μL de primer Reverse (5616 R: 5'-TATGGGCTGTAATGTTGTCTCC)
0,1 μL de dNTP 10 mM
3 μL de tampão de 5x
1,5 μL de MgCl2 25mM
0,1 μL de Polimerase GoTaq
H2O a um volume final de 15 μL
NOTA: O controle positivo no qual o modelo de DNA é o vetor pAdTrack-GFP deve ser incluído. - PCR "positivo" - para testar a presença do gene de interesse. Use primers específicos para o gene inserido e prepare a mistura como na etapa anterior. Os primers usados para GFP foram os seguintes:
F: 5'-CAAGGACGACGGCAACTACA
R: 5'-ATGGGGGTGTTCTGCTGGTA - Execute paralelamente o PCR "negativo" e o "positivo". O Programa PCR é: 5 min, 95 °C; 40 ciclos das seguintes etapas: 30 seg, 95 °C; 30 seg, 68 °C; 1 min, 72 °C; alongamento final: 10 min, 72 °C.
NOTA: Adapte a temperatura de ressaramento para amplificar o gene de interesse. - Avalie os produtos PCR em um gel de 1% de agarose e faça a seleção dos clones.
- Considere para processar ainda mais os clones que não dão produtos pcr para o "PCR negativo" e o produto PCR específico após o "PCR positivo".
- Cresça as culturas bacterianas de clones recombinantes selecionados
- Diluir as culturas dos supostos clones positivos (resultou na etapa 2.4.3.) em 4 mL de soc médio com kanamicina, e incuba-los durante a noite a 37°C com agitação.
- Isolamento do DNA plasmídeo da bactéria AdEasier-1 (Miniprep usando lise alcalina)
- Transfira 1,5 mL de cultura bacteriana em tubos de microcentrifuuge, centrífuga por 1 min a 16.200 x g,e remova o sobrenante.
- Transfira outra cultura bacteriana de 1,5 mL no mesmo tubo, repita a centrifugação e remova o sobrenante.
- Adicione 200 μL de tampão de resuspensão (50 mM de glicose, 10 mM EDTA, 25 mM Tris-HCl pH 8).
- Adicione 200 μL de solução de lise (0,2 N NaOH, 1% SDS), misture suavemente invertendo o tubo.
- Adicione 200 μL de solução de precipitação (60 mL de acetato de potássio de 5 M, 11,5 mL de ácido acético glacial, adicione H2O até 100 mL) e misture suavemente invertendo o tubo.
- Centrífuga por 3 min a 16.200 x g.
- Transfira o supernascer em um novo tubo de microcentrifuuge, adicione 500 μL isopropanol, misture e incuba por 20 minutos no gelo.
- Centrifugar por 15 min a 16.200 x g e adicionar 500 μL de 75% de etanol.
- Centrifugar por 10 min a 16.200 x g e remover o supernaspeso.
- Centrífuga por 3 min a 16.200 x g,remova o supernascente e adicione 15 μL de H2O.
- Amplificação, isolamento e retestagem dos plasmídeos recombinados
- Transformação de bactérias DH5α com o DNA isolado das células AdEasier-1.
- Prepare as bactérias competentes DH5α utilizando o kit de transformação comercial, seguindo as instruções dos fabricantes.
- Descongele 100 μL de bactérias competentes dh5α no gelo, adicione o DNA recombinante e incubar 10 minutos no gelo. Em seguida, semeou a bactéria em placas de ágar LB com kanamicina.
- Incubar a 37 °C durante a noite.
- Pegue várias colônias e cresça cada uma em 2 mL de meio LB com kanamicina, a 37 °C, durante a noite, com agitação.
- Isole o DNA (Miniprep usando lise alcalina) e resuspenda o DNA obtido em 25 μL H2O.
- Confirme os clones positivos por digestão enzimática.
- Prepare a seguinte mistura no gelo:
5 μL de DNA recombinante
1,5 μL de 10x tampão incolor
0,5 μL de Hind III ou Pst I
H2O a um volume final de 15 μL - Incubar a 37 °C por 30 min.
NOTA: Como controle, digerir também os plasmídeos pAdTrack-GFP e pAdEasy-1. - Em cada amostra adicione 3 μL de tampão de carregamento Sx6 com RNase A (se o RNase A não estiver presente nos buffers miniprep).
- Execute os fragmentos de DNA digeridos em 1% de eletroforese de gel agarose.
NOTA: O padrão de digestão de um clone positivo inclui a maioria dos fragmentos do plasmídeo pAdEasy digerido, revelando a recombinação pAdEasy com o vetor pAdTrack. O gene de interesse deve ser evidenciado pela digestão com as enzimas de restrição usadas para clonagem.
- Prepare a seguinte mistura no gelo:
- Preparação de DNA plasmídeo (grau de transfecção) para embalagem de adenovírus.
- Cresça uma cultura de 200 mL de bactérias a partir de um clone positivo para isolar o DNA plasmídeo.
- Isole o DNA plasmídeo usando um kit comercial para DNA plasmid Midiprep (por exemplo, Qiagen Plasmid Midi Kit) seguindo as instruções do fabricante.
- Transformação de bactérias DH5α com o DNA isolado das células AdEasier-1.
3. Embalando as partículas adenovirais
- Dia 1º. Sementes as células AD293
- Lave as células AD293 com PBS e incuba-as com 0,125% de Trypsin por 2-5 min a 37 °C.
- Recolher as células em meio frio com soro.
- Centrifugar por 5 min a 400 x g a 4 °C.
- Resuspend as células em médio com soro e semente as células a uma densidade de ~2 x 106/T25 frasco. De preferência, use um frasco com um filtro.
- Dia 1º. Digerir o DNA recombinante com Pac I
- Prepare a seguinte mistura:
6 μL de DNA recombinante (1 μg/μL)
2 μL de Pac I
2,5 μL de 10x tampão incolor
H2O a um volume final de 25 μL - Incubar por 3h (ou durante a noite) a 37 °C e, em seguida, inativar a enzima a 65 °C por 20 min.
- Precipitação de DNA com etanol: adicione 2,5 μL de (1/10 v/v) 3 M de acetato de sódio e 2-3 volumes de 100% etanol. Incubação por 30 min a -70 °C ou durante a noite a -20 °C.
- Centrifugar a 16.200 x g por 30 min a 4 °C e resuspensar a pelota em água estéril.
- Prepare a seguinte mistura:
- Dia 2: Transfecção de células AD293 usando reagente K2
- Adicione 40 μL de Multiplicador K2 sobre as células, duas horas antes da transfecção.
- Preparar soluções A e B:
Solução A: Adicione 6 μg de DNA linearizado Pac l em 260 μL de Opti-MEM.
Solução B: Adicione 21,6 μL de Reagente K2 em 248,4 μL de Opti-MEM. - Adicione a solução A sobre a solução B e misture suavemente por pipetação.
- Incubar a mistura por 20 minutos em temperatura ambiente. Adicione a mistura dropwise A e B às células.
- Dia 3-11: Monitore a expressão GFP por microscopia de fluorescência
NOTA: As células devem parecer verdes na microscopia de fluorescência e devem se desprender gradualmente. - Dia 11: Colher as partículas adenovirais de F1
- Colete as células separadas e o meio em um tubo de 50 mL, raspe as células aderentes e adicione-as no mesmo tubo.
- Centrífuga por 5 min a 400 x g, colete o supernasce em um novo tubo e resuspense a pelota celular em 0,5 mL de PBS.
- Interrupção celular
- Transfira a suspensão celular em um tubo de microcentrífuga.
- Realize três ciclos de congelamento/degelo (congelar em nitrogênio líquido ou a -80 °C /descongelar a 37 °C para máxima de 7 min).
- Passe as células quebradas através de uma agulha de seringa de 23 G três vezes.
- Remova os detritos celulares por centrifugação a 9.600 x g por 12 min.
- Transfira o supernatante para o tubo de 50 mL com o meio coletado.
4. Amplificação do adenovírus
NOTA: Se as células AD293 não atingirem a confluência necessária, as alíquotas dos estoques adenovirais (lisato obtidos das células produtoras de vírus) a serem armazenadas para infecção podem ser armazenadas a -80 °C.
- Prepare as partículas adenovirais F2.
- Semente as células AD293 em um frasco T75 (5 x 106 células/frasco).
- Infectar ~90% células AD293 confluentes usando as partículas adenovirais F1: adicione a homo homogeneizar a célula e o meio do frasco T25 sobre as células cultivadas no frasco T75.
- Monitore a expressão GFP por microscopia de fluorescência.
- Colher as células produtoras de vírus quando ~90% do AD 293 transduzido for destacado (~ o5º dia após a transdução). Mantenha a cultura celular média a 4 °C.
- Interrompa as células (da mesma forma com as de F1) em PBS de 1 mL.
- Prepare as partículas adenovirais F3.
- Infectar ~90% células AD293 confluentes semeadas em frasco T175 com partículas adenovirais F2 e o meio de cultura celular das partículas adenovirais F2.
- Colher as células (~5 dias após a transdução).
- Interrompa as células (da mesma forma com as de F1) em 2 mL de PBS.
- Prepare as partículas adenovirais F4.
- Infecte 5 frascos T175 contendo ~90% de células AD293 confluentes com partículas adenovirais F3 e meio de cultura celular.
- Colher as células (~5 dias após a transdução).
- Interrompa as células (da mesma forma com as de F1) em 3 mL de PBS.
- Prepare as partículas adenovirais F5.
- Infecte 25 frascos T175 contendo ~90% de células AD293 confluentes com estoque adenoviral F4 e meio de cultura celular.
5. Purificação do adenovírus do meio de lise celular e cultura
- Colhendo as células produtoras de vírus e o meio cultural.
- Colher as células AD293 de F5 após 5 dias de transdução.
- Guarde o meio em uma garrafa estéril para precipitação das partículas adenovirais.
NOTA: Mantenha o meio na geladeira até a purificação do adenovírus. - Centrifugar as células a 400 x g, por 5 min, a 4 oC.
- Resuspense a última pelota em 5 mL de 10 mM Tris HCl, pH 8 com 2 mM MgCl2.
- Aliquotar a suspensão em tubos de 1,5 mL.
- Interrompa as células (da mesma forma com as da F1): três ciclos de congelamento/descongelamento.
NOTA: Se a ultracentrifugação não puder ser realizada imediatamente, mantenha as amostras a -80 °C. - Passe a suspensão da célula através de uma agulha de seringa 23G por três vezes.
- Centrifugar o homogeneizar a 9 600 x g, por 12 min.
- Salve o supernatante para purificação do adenovírus pela ultracentrifugação de gradiente CsCl.
- Precipitação do adenovírus liberado no meio da cultura.
- Traga a garrafa com meio de cultura celular salva à temperatura ambiente.
- Adicione 121 g de sulfato de amônio a cada 500 mL de meio de cultura celular (a saturação da solução deve ser entre 40 a 42%).
- Misture cuidadosamente até que o sulfato de amônio esteja completamente dissolvido.
- Incubar por um mínimo de 2,5 horas em temperatura ambiente.
- Centrífuga a 1600 x g, por 15 min, a 22 oC e salvar a pelota.
- Resuspense a pelota em 4 mL de 10mM Tris HCl pH 8 com 2mM MgCl2; esta suspensão deve ser purificada imediatamente pela ultracentrifugação gradiente CsCl.
NOTA: Se a etapa de purificação não puder ser realizada posteriormente, dilísse durante a noite a pelota resuspended contra 10mM Tris HCl, pH 8 com 2mM MgCl2.
- Purificação de adenovírus por ultracentrifugação.
- Prepare um gradiente CsCl descontínuo em tubos de polipropileno para rotor SW41Ti. Adicione 3 mL de 765 mg/mL CsCl (alta densidade: 1,4 g/L) na parte inferior do tubo. Adicione lentamente 3 mL de 288,5 mg/mL CsCl (baixa densidade: 1,2 g/L) em cima da primeira camada CsCl.
- Sobrepor suavemente 3 - 4 mL de suspensão de partícula adenoviral liberada das células ou precipitada do meio de cultura celular (como descrito anteriormente) em cima do gradiente.
- Encha os tubos com óleo mineral e coloque os tubos nos baldes frios de SW41Ti.
- Equilibre os tubos. Certifique-se de que os tubos de polipropileno preenchidos estejam carregados simetricamente no rotor. Coloque o rotor no ultracentrifuge.
- Centrifugar a 210.000 x g e 4 °C, durante 18 horas, sem freio.
- Coloque os tubos de ultracentrifutura em um suporte com um papel preto atrás para obter as bandas.
- Descarte a fase superior clara, os detritos celulares e a faixa superior em um recipiente de resíduos com a solução de branqueamento.
- Colher a faixa mais baixa que contém o adenovírus completo (~700 μL - 1 mL) em um tubo estéril de 1,5 mL e mantê-lo no gelo.
- Pré-molhado um de diálise no tampão de diálise (10 mM Tris-Cl tampão pH 8, 2 mM MgCl2).
- Injete o adenovírus purificado no de diálise usando uma seringa de 2 mL.
- Dilíque durante a noite contra 10 mM Tris-Cl tampão pH 8, 2 mM MgCl2 (altere o buffer de diálise 3 - 4 vezes).
- Retire o estoque adenoviral do de diálise em alíquotas de 10 a 100 μL.
- Adicione sacarose a 4% de concentração final a alíquotas virais (para crioproteção).
- Armazenar alíquotas a -80 °C.
6. Titulação de Adenovírus
- Dia 1: Chapeamento das células
- Semente as células AD293 a uma densidade de 2,5 × 105 células por poço (em uma placa de cultura de 12 poços) em 1 mL meio de crescimento completo, como mostrado na Figura 2. Certifique-se de que as células estão espalhadas uniformemente em cada poço para uma determinação precisa de titer.
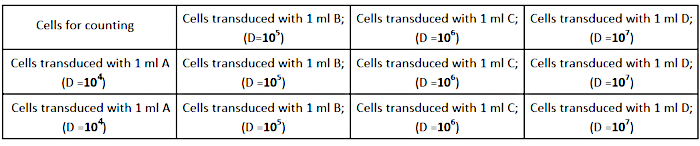
Figura 2: Desenho da placa de titulação. Clique aqui para ver uma versão maior desta figura.
- Dia 2: Transdução de células
- Retire as células de um poço com trippsina e conte-as. Observe este número porque ele será usado para calcular o título viral.
- Realizar diluições seriais (1/104; 1/105; 1/106; 1/107) do estoque viral em 1 mL de meio de crescimento completo da seguinte forma:
- 1/103: diluição do estoque do vírus - adicionar 2 μL de estoque viral a 1998 μL de meio completo.
- 1/104: Faça 1:10 diluição de 1/103 diluindo 120 μL a 1080 μL de médio completo (A).
- 1/105: Faça 1:10 diluição de B diluindo 120 μL de A a 1080 μL de médio completo (B).
- 1/106: Faça 1:10 diluição de C diluindo 120 μL de B a 1080 μL de médio completo (C).
- 1/107: Faça 1:10 diluição de D diluindo 120 μL de C a 1080 μL de médio completo (D).
NOTA: Prepare 3 tubos de cada diluição (A, B, C, D) para realizar o experimento em triplicados. - Remova o meio de cultura celular dos poços e adicione as diluições preparadas do vírus, conforme mostrado na Figura 2.
- Dia 3: Monitorando a expressão GFP
- Verifique se os poços estão à frente da presença de células verdes usando um microscópio de fluorescência.
- Dia 4: Análise de citometria de fluxo de células GFP positivos
- Prepare e rotule doze tubos de 1,5 mL.
- Colete o meio de cultura celular (juntamente com as células separadas) em tubos de 1,5 mL e mantenha-os no gelo.
- Adicione 200 μL de trippsina em cada poço.
- Incubar a placa por 2 - 3 min a 37 °C na incubadora de CO2.
- Colher as células nos mesmos tubos de Eppendorf com o meio de cultura celular. Mantenha os tubos no gelo.
- Pelota as células a 400 x g, por 5 min, a 4 °C.
- Remova o supernante; manter os tubos no gelo.
- Resuspensar a pelota em 250 μL de PBS + 2% FBS; manter os tubos no gelo.
- Transfira a suspensão celular em tubos de citometria de fluxo ou placa.
- Execute as amostras em um citómetro de fluxo registrando a fluorescência das células expressas GFP.
Cálculo de Titer: As amostras com células positivas de 5 a 20% de GFP da população-mãe devem ser levadas em conta para o cálculo do título viral usando a seguinte fórmula:
Titer (TU/mL) = D x F/100 x C/V
D = fator de diluição
F = percentual de células positivas / 100
C = número de células / bem
V = volume de inóculo viral
7. Transdução adenoviral de células-alvo e testes da expressão proteica induzida
- Dia 1: Semeando as células
- Semear as células-alvo garantindo que elas se espalhem uniformemente nos poços.
- Dia 2: Transdução das células
- Retire as células alvo de um poço e conte-as.
- Calcule o volume adequado de suspensão adenoviral necessário para transduturar as células com o número desejado de partículas infecciosas por célula.
- Adicione a quantidade correspondente de suspensão viral às células-alvo.
- Dia 3: Remoção da suspensão viral e verificação da expressão GFP
- Substitua o meio de cultura celular contendo partículas adenovirais por meio fresco.
- Verifique a expressão GFP no microscópio de fluorescência.
Resultados
Modificamos e melhoramos o protocolo original de Vogelstein, a fim de alcançar uma produção de adenovírus mais rápida e eficiente. Primeiro, revisamos a metodologia para obter uma seleção mais fácil de recombinantes. Após a recombinação, os clones bacterianos BJ5183 foram testados por "PCR negativo" para avaliar a integridade do pAdTrack-GFP como um indicador da falta de recombinação(Figura 3A), ou por "PCR positivo" para identificar o gene de interesse, assimilado em nosso caso ao GFP(Figura 3B). Tanto em PCRs "negativos" quanto "positivos", usamos pAdTrack-GFP como modelo de controle, o que deu uma banda de 986 bp para integridade pAdTrack(Figura 3A, faixa 1), e uma banda de 264 bp para GFP(Figura 3B, faixa 3). Os primers usados para o "PCR negativo" foram projetados para amplificar um fragmento de 986 bp contendo o site pmeI em pAdTrack-GFP. Este fragmento de DNA é drasticamente aumentado após a recombinação e não é amplificado nos clones recombinantes positivos. Clones negativos para recombinação, nos quais o pAdTrack-GFP permaneceu intacto, estão representados nas Figuras 3A, faixas 3, 4 e 6. Os primers se acotoram nas sequências de DNA adjacentes ao local de recombinação. Potenciais clones recombinantes positivos(Figura 3A, faixas 2 e 5) expressaram GFP como mostrado nas Figuras 3B,faixa 1 e 2. O DNA plasmídeo desses clones foi isolado e usado para a transformação de DH5α para obter uma maior quantidade de DNA. Estes plasmídeos recombinantes pré-selecionados amplificados em DH5α foram então testados por digestão enzimática. Na Figura 3C-E são ilustrados os resultados da digestão enzimática de um clone recombinante-positivo digerido com enzimas hind III, PstI, restrição bamHI(Figura 3C, D, E pista 2). Os padrões de digestão hindiii e PstI do clone recombinante foram semelhantes aos obtidos para pAdEasy-1 desde que hindiII e PstI cortaram o pAdEasy-1 plasmídeo 24 e 25 vezes, respectivamente, (Figura 3C e D, pista 3); HindIII cortou uma vez e PstI cortou quatro vezes o vetor pAdTrack-GFP(Figura 3C e D, faixa 1). BamHI cortou duas vezes o vetor pAdEasy-1(Figura 3C, faixa 3) e uma vez pAdTrack-GFP(Figura 3C, faixa 1).
O PACI cortou um fragmento de 4,5 kb do plasmídeo recombinante(Figura 3F, faixa 2), um fragmento de 2863 bp de pAdTrack-GFP(Figura 3F, faixa 1), e linearizou o vetor pAdEasy-1(Figura 3F, faixa 3). A escada de DNA está representada na Figura 3C-F,nas faixas 4. O plasmídeo recombinante foi digerido com Pac I para uso posterior para transfecção AD293.
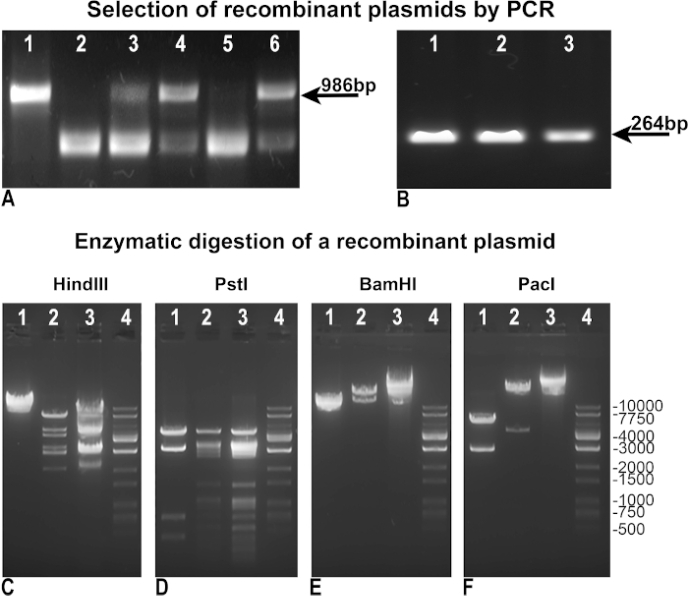
Figura 3: A recombinação do pAdTrack-GFP com o plasmídeo pAdEasy-1. Os plasmídeos obtidos após a recombinação do pAdTrack-GFP e pAdEasy-1 foram testados por PCR "negativo" para a integridade pAdTrack-GFP (A). Os clones não recombinantes foram evidenciados pela presença de uma banda de 986 bp correspondente à sequência amplificada do plasmídeo pAdTrack-GFP (A, faixas 3, 4 e 6). Os clones potencialmente positivos para recombinação (A, faixas 2 e 5) também foram obtidos. Quando o vetor pAdTrack-GFP foi usado como modelo, uma faixa de 986 bp para pAdTrack-GFP (A, pista 1) foi obtida. Os clones recombinantes potencialmente positivos foram testados para a expressão GFP por PCR "positivo" (B); uma faixa de 264 bp aparece tanto para clones potencialmente recombinados (B, lane 1 e 2), bem como para o plasmídeo pAdTrack-GFP. O DNA de um potencial clone recombinante foi testado com enzima de restrição hindiii, PstI, BamHI e PacI (C-F, faixas 2). Nos controles, o vetor pAdEasy-1 (C-F, faixas 3) e o plasmídeo pAdTrack-GFP (C-F, faixas 1) foram digeridos com as mesmas enzimas. A escada de DNA está representada na faixa C-F 4. Clique aqui para ver uma versão maior desta figura.
As embalagens adenovirais e a amplificação foram realizadas em células AD293. As partículas adenovirais (AdV-GFP) foram purificadas do liseato celular AD293, bem como do meio de cultura celular, onde foram liberadas pelas células infectadas. Para concentrar o adenovírus encontrado no meio de cultura celular, as partículas foram precipitadas com sulfato de amônio e depois resuspended em 10 mM Tris HCl pH 8 com 2 mM MgCl2, o mesmo tampão usado para a lise celular. Posteriormente, as partículas adenovirais do lisecelular e do meio de cultura foram purificadas pela ultracentrifugação de gradiente de CsCl. Após a ultracentrifugação, obteve-se uma forte faixa de AdV-GFP purificada, como mostrado na Figura 4.

Figura 4: A purificação adenoviral por ultracentrifugação em um gradiente de CsCl descontínuo. A célula homogenetada e o adenovírus precipitado do meio foram submetidos à ultracentrifugação em um gradiente descontínuo formado por soluções CsCl de baixa e alta densidade. Fortes bandas de Adenovírus GFP foram evidenciadas em ambos os casos. Clique aqui para ver uma versão maior desta figura.
Para determinar o título viral expresso em unidades transdutoras por um mL (TU/mL), as células AD293 foram infectadas com diluições seriais do AdV-GFP. Após 48 horas, as células infectadas expressaram GFP, em correlação inversa com o fator de diluição da suspensão viral. Isso foi observado pela microscopia de fluorescência e o percentual de células GFP positivos foi determinado pela citometria de fluxo(Figura 5). Para calcular o título, considerou-se a diluição viral que induziu 5 - 20% das células GFP-positivas(Figura 5C). Normalmente, obtemos um título viral de ~1010 (TU/mL) para GFP-adenovírus.
Abaixo, fornecemos um exemplo de cálculo de titânulo adenoviral para um lote adenoviral específico no qual 3000000 células (C) foram transduzidas com solução adenoviral de 1 mL (V), em um fator de diluição de10 6 (D), para o qual 6% foram obtidas células GFP-positivas (F):
Titer (TU/mL) = D x F/100 x C/V = 106 x 6/100 x 300000/1 = 1,8 x 1010 TU/mL
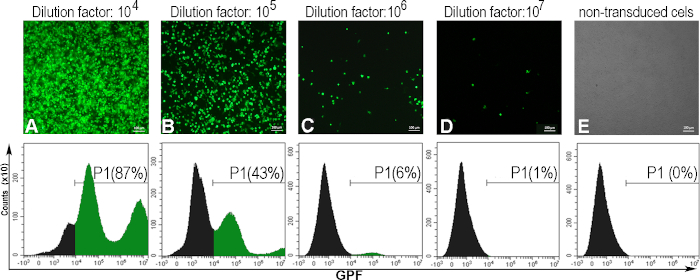
Figura 5: A avaliação do título adenoviral. As células AD293 foram infectadas com várias diluições adenovirais. Quarenta e oito horas depois, as células foram observadas por microscopia de fluorescência e analisadas por citometria de fluxo para determinar a porcentagem de células positivas de GFP induzidas por diferentes diluições adenovirais (A-D). Para estabelecer o portão para citometria de fluxo, também foram analisadas células não transduzidas (E). O título calculado para o fator de diluição 106, quando 6% das células eram GFP positivas foi 1,8 x 1010 TU/mL. Para painéis A-E, barras: 100μm. Clique aqui para ver uma versão maior desta figura.
Para testar o potencial de transdução do adenovírus preparado, foram utilizadas quatro linhas celulares: células endoteliais humanas (EA.hy926), células endoteliais aórticas bovinas (BAEC), hepatocitos murinas (Hepa 1-6) e células estrômicas mesenquimais murinas (MSC). As células endoteliais (EA.hy926 e BAEC) foram transduzidas com 25 TU/células, os hepatócitos foram transduzidos com 5 TU/célula e MSC foram transduzidos com 250 TU/cell.
Aqui está um exemplo de como o volume de suspensão adenoviral necessário para infectar 3 x 106 células com 25 TU/célula, utilizando a suspensão adenoviral com 1,8 x 1010 TU/mL, foi calculado.
Para 1 célula ................. 25 TU
3 x 106 células .............. x TU  x=75 x 106 TU
x=75 x 106 TU
Se o estoque viral contiver
1.8 x 1010 TU .............. 1 mL
75 x 106 TU ........... y mL  y= 4,2 x 10-3 mL = 4,2μL de estoque viral
y= 4,2 x 10-3 mL = 4,2μL de estoque viral
Quarenta e oito horas após a transdução, as células foram analisadas por microscopia de fluorescência. Como mostrado na Figura 6, as células endoteliais humanas ou bovinas foram transduzidas com boa eficiência (~50%) para 25 TU/cell (Figura 6 EA.hy926 e BAEC). Hepatócitos murinos (Hepa 1-6) foram eficientemente transduzidos pelo adenovírus a uma baixa quantidade de partículas de adenovírus (5 TU/célula), mas também são sensíveis ao adenovírus, uma vez que uma maior porcentagem de células mortas (células pi-positivas) foi registrada (~16%) em comparação com os outros tipos de células. As células estromais mesenquimais foram as mais difíceis de transduzir (Figura 6),devido à falta de receptores adenovirais específicos (dados inéditos).
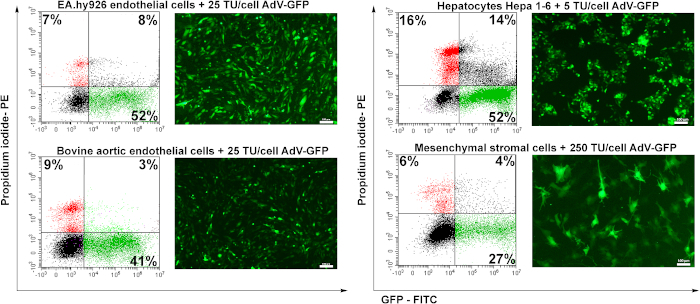
Figura 6: A infectividade do adenovírus e a indução da expressão GFP em células transduzidas. As células endoteliais humanas (EA.hy926), as células endoteliais aórticas bovinas (BAEC), os hepatócitos murinas (Hepa 1-6) e as células estrânicas mesenquimais (MSC) foram transduzidas com a quantidade indicada de adenovírus. O GFP foi detectado por microscopia de fluorescência e a porcentagem das células positivas do GFP foi analisada por citometria de fluxo. Células pi-positivas determinadas pela citometria de fluxo mostram a mortalidade celular determinada pela transdução viral. As células eA.hy926, as células endoteliais aórticas bovinas e as células Hepa 1-6 foram altamente transduzidas pelo adenovírus, o rendimento da transdução variando de 41 a 52%. Para o MSC, uma maior quantidade de vírus (250 TU/células) induziu apenas 27% de GFP positivo das células transduzidas. Barras: 100μm. Clique aqui para ver uma versão maior desta figura.
Discussão
Adenovírus recombinantes são uma ferramenta versátil para entrega e expressão genética12,13,14. Para induzir forte expressão proteica por transdução adenoviral, a sequência de codificação do gene de interesse é inserida no genoma do adenovírus. O sistema adenoviral AdEasy, desenvolvido no laboratório de Bert Vogelstein, compreende um plasmídeo de espinha dorsal (pAdEasy-1) contendo a maior parte do genoma do sorotipo 5 do adenovírus selvagem, e um vetor (pAdTrack), projetado para clonagem genética2,10. A exclusão dos genes adenovirais E1 (responsável pela montagem de partículas infecciosas do vírus) e E3 (proteínas de codificação envolvidas na evasão da imunidade hospedeira) criaram um espaço no genoma adenoviral, no qual um gene de interesse de 6,5-7,5 kb pode ser inserido2,3. Este tamanho é suficiente para muitos genes, especialmente para aqueles com introns mais curtos15,16,17. Há também pesquisadores relatando a produção de adenovírus portadores do CDNA de um transgene18,19,20. No entanto, obtivemos um menor rendimento de expressão transgênica para adenovírus portadores de cDNA do que para seus homólogos carregando um gene ou um mini-gene (dados não mostrados).
Melhorar e adaptar os métodos anteriores2,10,14,18,21, a tecnologia para a produção adenoviral requer um menor tempo, menor custo e menos esforço. O DNA adenoviral de comprimento completo é obtido por recombinação entre o vetor da nave auxiliar e o plasmídeo pAdEasy-1 na recombinação homóloga propensa a tensão E. coli, BJ5183. O protocolo implica a transformação química das células AdEasier-1 (bactérias BJ5183 contendo pAdEasy-1). Essa técnica não requer um eletroporador que pode não estar disponível em alguns laboratórios, é muito simples, aumenta o rendimento de recombinação, e reduz o tempo necessário para obter células competentes e realizar a transformação. A pré-seleção de clones recombinantes realizados pelo PCR diminui ainda mais o tempo e facilita todo o procedimento. Um procedimento semelhante foi usado por Zhao e colegas de trabalho22, no entanto, no protocolo, otimizamos as sequências dos primers.
Para a embalagem e amplificação do GFP-adenovírus, foi utilizada uma linha de células derivadas HEK293, ou seja, células AD293, que são mais aderentes à placa de cultura. Outras linhas celulares comumente utilizadas para produção adenoviral são as seguintes: 911, 293FT, pTG6559 (derivado A549), PER. C6 (derivado her), GH329 (derivado HeLa), N52. E6, e HeLa-E123,24,25,26. Em nossas mãos, não houve melhora na produção adenoviral quando foram utilizadas 911 células (dados não apresentados). A transfecção de células AD293 com o plasmídeo recombinante usando reagente K2 aumentou muito a eficiência da etapa de embalagem viral. Após a produção de adenovírus, até ~70% do adenovírus ainda está dentro das células e é liberado por três ciclos de congelamento e descongelamento. Aumentar o número de ciclos não é adequado porque destrói o adenovírus.
Ao longo do processo de produção adenoviral rotineiro, inúmeras partículas virais são liberadas no meio da cultura celular. Descartar esse meio de cultura celular durante a colheita das células AD293 infectadas resultaria em uma importante perda viral. Otimizamos o protocolo descrito por Schagen e colegas de trabalho para purificar as partículas adenovirais do meio de cultura celular por precipitação com sulfato de amônio27. Este método tem maior eficiência na recuperação do adenovírus do meio de cultura celular em comparação com o método que utiliza polietilenoglicol 28. O adenovírus precipitado deve ser purificado imediatamente por ultracentrifugação ou mantido na geladeira por alguns dias, mas somente após a diálise, para remover o excesso de sal. Manter o precipitado por mais de algumas horas sem diálise é prejudicial ao vírus.
A purificação das partículas adenovirais por ultracentrifugação realizada em uma etapa reduz a manipulação do estoque adenoviral e facilita o procedimento em comparação com os protocolos usando sucessivas etapas de ultracentrifugação14,29. A diálise do adenovírus purificado é necessária para remover cloreto de césio que pode afetar ainda mais a transdução. No protocolo, utilizamos tampão Tris contendo MgCl2, mas não sacarose para diálise, uma vez que requer uma enorme quantidade injustificada de sacarose que é necessária de outra forma como um conservante para congelamento. Assim, adicionamos sacarose mais tarde, diretamente nos estoques adenovirais preparados para o congelamento. Para evitar o congelamento frequente e o descongelamento do adenovírus purificado, é aconselhável aliquotar os estoques adenovirais e armazená-los a -80 °C. O título adenoviral foi avaliado pela citometria de fluxo considerando o gene repórter do GFP e a porcentagem de células transduzidas para uma diluição viral específica. Este método é mais rápido em comparação com o clássico "ensaio de placa" e é mais confiável em comparação com a avaliação das proteínas capsíides (por vários métodos como ELISA ou citometria de fluxo) que não revela a capacidade de infecção das partículas adenovirais. No entanto, a quantificação baseada em ELISA, Q-PCR ou ensaio de placa usando kits disponíveis comercialmente são métodos alternativos, especialmente úteis para a titulação de adenovírus que não contêm um rastreador fluorescente.
Considerando que os adenovírus pAdTrack são derivados do sorotipo 5 de adenovírus humanos que é reconhecido pelos Receptores de Coxsackievirus e Adenovirus (CAR), demonstramos a capacidade do GFP-adenovirus para transduzir células de origem humana (células endoteliais), mas também células de outras origens: bovinos (células endoteliais) e murina (células estrômicas mesenquimais e hepatócitos). Os dados mostraram que o GFP-adenovírus pode induzir um alto nível de expressão de um transgene.
Em conclusão, otimizamos essa tecnologia laboriosa para reduzir o tempo, os custos e o esforço necessário para obter as partículas adenovirais. O adenovírus preparado é capaz de infectar vários tipos de células e induzir a expressão do gene de interesse. Este protocolo pode ser usado em uma variedade de experimentos, uma vez que a transferência genética mediada por adenoviral representa uma das principais ferramentas para o desenvolvimento de terapias genéticas modernas.
ABREVIATURAS: AdV-GFP, partículas adenovirais; BAEC, células endoteliais aórticas bovinas; CsCL, cloreto de césio; GFP, proteína fluorescente verde; MSC, células estromais mesenquimais; TU, unidades transdutoras.
Divulgações
Os autores não têm nada a revelar.
Agradecimentos
Este trabalho foi apoiado por um Projeto co-financiado pelo Fundo Europeu de Desenvolvimento Regional através do Programa Operacional de Competitividade 2014-2020 (POC-A.1-A.1.1.4-E-2015, ID: P_37_668; sigla DIABETER), uma bolsa do Ministério romeno de Pesquisa e Inovação PCCDI- UEFISCDI, Projeto número PN-III-P1-1.2-PCCDI-2017-0697 dentro do PNCD III e pela Academia Romena. Os autores agradecem a Kyriakos Kypreos (Universidade de Patras, Grécia) por seus conselhos generosos e relevantes, Ovidiu Croitoru (Universidade de Belas Artes, Bucareste, Romênia) por filmagens, edição de filmes e design gráfico, e Mihaela Bratu por assistência técnica.
Materiais
| Name | Company | Catalog Number | Comments |
| AD293 cells | Agilent Technologies | 240085 | |
| AdEasier-1 cells | Addgene | 16399 | |
| Agarose I (for electrophoresis) | Thermo Scientific | 17850 | |
| Ammonium sulfate | Sigma | A4418 | |
| Ampicillin sodium salt | Sigma | A0166 | |
| BamH I | Thermo Scientific | FD0054 | |
| Cell culture plates 100 mm | Eppendorf | 30702115 | |
| Cesium chloride | Sigma | L4036 | |
| DH5alpha bacteria | Thermo Scientific | 18265017 | |
| DMEM (GlutaMAX, 4.5g/L D-Glucose) | Gibco | 3240-027 | |
| EA.hy926 cells | ATCC | CRL-2922 | |
| EDTA | Sigma | E5134 | |
| Ethanol (99.8%) | Roth | 5054.2 | |
| Fetal Bovine Serum | Sigma | F7524 | |
| Flasks T25, T75, T175 | Eppendorf | 30712129 | |
| Glucose | Sigma | G7021 | |
| Hepa 1-6 murine hepatocytes | ATCC | CRL-1830 | |
| Hind III | Thermo Scientific | FD0504 | |
| Kanamycin Sulfate | Thermo Scientific | 15160054 | |
| K2 Transfection System | Biontex | T060-5.0 | |
| LB medium | Formedium | LBx0102 | |
| LB-agar | Formedium | LBx0202 | |
| Mix & Go E. coli Transformation kit | Zymo Research | T3001 | |
| Midori Green Advanced DNA stain | Nippon Genetics Europe | MG-04 | |
| NaOH | Sigma | S8045 | |
| Opti-MEM | Thermo Scientific | 31985070 | |
| Pac I | Thermo Scientific | FD2204 | |
| pAdEasy-1 | Addgene | 16400 | |
| pAdTrack-CMV | Addgene | 16405 | |
| Phenol:chloroform:isoamyl alcohol (24:24:1) | Invitrogen | 15593-031 | |
| Polymerase GoTaq | Promega | M3005 | |
| Pme I (Mss I) | Thermo Scientific | FD1344 | |
| Potassium acetate | VWR Chemicals | 43065P | |
| Pst I | Thermo Scientific | FD0614 | |
| Qiagen Midi Prep kit | Qiagen | 12125 | |
| Cell Scraper | TPP | 99003 | |
| SDS | Thermo Scientific | 28365 | |
| Slide-A-Lyzer dialysis cassettes | Thermo Scientific | 66330 | |
| Sodium pyruvate | SIGMA | P5280-100G | |
| Syringe with 23G neeedle | B Braun | 464BR | |
| Tris HCl | Sigma | 1185-53-1 | |
| Trypan blue | Roth | CN76.1 | |
| Tubes 50ml | TPP | 91050 | |
| Ultra-Clear Tubes (14x89 mm) | Beckman Coulter | 344059 | |
| Centrifuge (refrigerated) | Sigma Sartorius | 3-19KS | |
| HeraeusFresco 17 Microcentrifuge | Thermo Scientific | 75002420 | |
| Ultracentrifuge with SW41Ti rotor | Beckman Coulter | Optima L-80 XP | |
| Culture Hood | Thermo Scientific | Class II | |
| Pipettes (0-2µl, 1-10µl, 2-20µl, 10-100µl, 20-200µl, 100-1000µl) | Thermo Scientific | ||
| Dry Block Heating Thermostat | Biosan | TDB-120 | |
| Thermocycle | SensoQuest | 012-103 | |
| Water Bath | Memmert | WNB 14 |
Referências
- Lee, C. S., et al. Adenovirus-Mediated Gene Delivery: Potential Applications for Gene and Cell-Based Therapies in the New Era of Personalized Medicine. Genes and Diseases. 4 (2), 43-63 (2017).
- He, T. C., et al. A simplified system for generating recombinant adenoviruses. Proceedings of the National Academy of Sciences of the United States of America. 95 (5), 2509-2514 (1998).
- Russell, W. C. Update on adenovirus and its vectors. The Journal of General Virology. 81, 2573-2604 (2000).
- Rauschhuber, C., Noske, N., Ehrhardt, A. New insights into stability of recombinant adenovirus vector genomes in mammalian cells. European Journal of Cell Biology. 91 (1), 2-9 (2012).
- Saha, B., Wong, C. M., Parks, R. J. The adenovirus genome contributes to the structural stability of the virion. Viruses. 6 (9), 3563-3583 (2014).
- Kreppel, F., Kochanek, S. Modification of adenovirus gene transfer vectors with synthetic polymers: a scientific review and technical guide. Molecular Therapy: the Journal of the American Society of Gene Therapy. 16 (1), 16-29 (2008).
- Dormond, E., Perrier, M., Kamen, A. From the first to the third generation adenoviral vector: what parameters are governing the production yield. Biotechnol Advances. 27 (2), 133-144 (2009).
- Parks, R. J., et al. A helper-dependent adenovirus vector system: removal of helper virus by Cre-mediated excision of the viral packaging signal. Proceedings of the National Academy of Sciences of the United States of America. 93 (24), 13565-13570 (1996).
- Jager, L., Ehrhardt, A. Emerging adenoviral vectors for stable correction of genetic disorders. Current Gene Therapy. 7 (4), 272-283 (2007).
- Luo, J., et al. A protocol for rapid generation of recombinant adenoviruses using the AdEasy system. Nature Protocols. 2 (5), 1236-1247 (2007).
- Dumitrescu, M., et al. Adenovirus-Mediated FasL Minigene Transfer Endows Transduced Cells with Killer Potential. International Journal of Molecular Sciences. 21 (17), (2020).
- Campos, S. K., Barry, M. A. Current advances and future challenges in Adenoviral vector biology and targeting. Current Gene Therapy. 7 (3), 189-204 (2007).
- Khare, R., Chen, C. Y., Weaver, E. A., Barry, M. A. Advances and future challenges in adenoviral vector pharmacology and targeting. Current Gene Therapy. 11 (4), 241-258 (2011).
- Jager, L., et al. A rapid protocol for construction and production of high-capacity adenoviral vectors. Nature Protocols. 4 (4), 547-564 (2009).
- Zvintzou, E., et al. Pleiotropic effects of apolipoprotein C3 on HDL functionality and adipose tissue metabolic activity. Journal of Lipid Research. 58 (9), 1869-1883 (2017).
- Karavia, E. A., et al. Apolipoprotein A-I modulates processes associated with diet-induced nonalcoholic fatty liver disease in mice. Molecular Medicine. 18, 901-912 (2012).
- Lampropoulou, A., Zannis, V. I., Kypreos, K. E. Pharmacodynamic and pharmacokinetic analysis of apoE4 [L261A, W264A, F265A, L268A, V269A], a recombinant apolipoprotein E variant with improved biological properties. Biochemical Pharmacology. 84 (11), 1451-1458 (2012).
- Zheng, S. Y., Li, D. C., Zhang, Z. D., Zhao, J., Ge, J. F. Adenovirus-mediated FasL gene transfer into human gastric carcinoma. World Journal of Gastroenterology. 11 (22), 3446-3450 (2005).
- Ambar, B. B., et al. Treatment of experimental glioma by administration of adenoviral vectors expressing Fas ligand. Human Gene Therapy. 10 (10), 1641-1648 (1999).
- Okuyama, T., et al. Efficient Fas-ligand gene expression in rodent liver after intravenous injection of a recombinant adenovirus by the use of a Cre-mediated switching system. Gene Therapy. 5 (8), 1047-1053 (1998).
- van Dijk, K. W., Kypreos, K. E., Fallaux, F. J., Hageman, J. Adenovirus-mediated gene transfer. Methods in Molecular Biology. 693, 321-343 (2011).
- Zhao, Y. D., Li, T., Huang, G. A simple negative selection method to identify adenovirus recombinants using colony PCR. Electronic Journal of Biotechnology, North America. 17 (1), 46-49 (2014).
- Kovesdi, I., Hedley, S. J. Adenoviral producer cells. Viruses. 2 (8), 1681-1703 (2010).
- Lin, X. Construction of new retroviral producer cells from adenoviral and retroviral vectors. Gene Therapy. 5 (9), 1251-1258 (1998).
- Fallaux, F. J., et al. Characterization of 911: a new helper cell line for the titration and propagation of early region 1-deleted adenoviral vectors. Human Gene Therapy. 7 (2), 215-222 (1996).
- Altaras, N. E., et al. Production and formulation of adenovirus vectors. Advances in Biochemical Engineering/ Biotechnology. 99, 193-260 (2005).
- Schagen, F. H., et al. Ammonium sulphate precipitation of recombinant adenovirus from culture medium: an easy method to increase the total virus yield. Gene Therapy. 7 (18), 1570-1574 (2000).
- Colombet, J., et al. Virioplankton 'pegylation': use of PEG (polyethylene glycol) to concentrate and purify viruses in pelagic ecosystems. Journal of Microbiological Methods. 71 (3), 212-219 (2007).
- Kypreos, K. E., van Dijk, K. W., van Der Zee, A., Havekes, L. M., Zannis, V. I. Domains of apolipoprotein E contributing to triglyceride and cholesterol homeostasis in vivo. Carboxyl-terminal region 203-299 promotes hepatic very low density lipoprotein-triglyceride secretion. Journal of Biological Chemistry. 276 (23), 19778-19786 (2001).
Reimpressões e Permissões
Solicitar permissão para reutilizar o texto ou figuras deste artigo JoVE
Solicitar PermissãoThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Todos os direitos reservados