Для просмотра этого контента требуется подписка на Jove Войдите в систему или начните бесплатную пробную версию.
Method Article
Идентификация и характеристика иммуногенных видов РНК в АЛЛЕРГЕНах HDM, которые модулируют воспаление эозинофилических легких
В этой статье
Резюме
Экологические аллергены, такие как клещи домашней пыли (HDM) часто содержат микробные вещества, которые активируют врожденные иммунные реакции для регулирования аллергического воспаления. Представленный здесь протокол демонстрирует идентификацию видов дстрНК в аллергенах HDM и характеристику их иммуногенной деятельности при модуляции эозинофильного воспаления легких.
Аннотация
Экологические аллергены, такие как клещи домашней пыли (HDM) часто находятся в сложных формах, содержащих как аллергические белки, которые приводят аномальные реакции типа 2 и микробных веществ, которые вызывают врожденные иммунные реакции. Эти аллерген-ассоциированные микробные компоненты играют важную роль в регулировании развития типа 2 воспалительных заболеваний, таких как аллергическая астма. Однако основополагающие механизмы остаются в значительной степени неопределенными. Представленный здесь протокол определяет структурные характеристики и активность аллерген-ассоциированной иммуностимуляторной РНК. В частности, общие аллергены рассматриваются на наличие двухцепочечная РНК (dsRNA) видов, которые могут стимулировать ответы ИФН в легких и сдерживать развитие тяжелой эозинофилии легких в мышиной модели Индуцированной ХДС аллергической астмы. Здесь мы включили следующие три анализа: Dot пятно, чтобы показать структуры DSRNA в общей РНК, изолированные от аллергенов, включая вид HDM, RT-qPCR для измерения деятельности HDM РНК в интерферон стимулирующих генов (ISGs) выражение в легких мыши и анализ FACS для определения влияния HDM РНК на количество эозинофилов в BAL и легких, соответственно.
Введение
Основываясь на гипотезе гигиены, первоначально предложенной Strachan1, раннее воздействие детей на экологические микробные факторы, такие как эндотоксин может защитить от развития аллергических расстройств2,3. Во время микробных инфекций, например, вирусных инфекций, врожденное иммунное обнаружение иностранных нуклеиновых кислот (РНК/ДНК) вызывает у хозяина защитные реакции4,,5,,6. Однако существование и распространенность иммуногенных нуклеиновых кислот, таких как длинные двуцепоченные РНК (dsRNA) видов в клещах домашней пыли (HDM) или других аллергенов насекомых остаются неизвестными. Этот протокол был разработан, чтобы определить, содержит ли HDM или аллергенов насекомых и неразвимов длинную дстрянк, которые могут активировать защитный иммунный ответ, чтобы противодействовать развитию тяжелого эозинофильного воспаления легких в мышиной модели аллергической астмы. Здесь мы предоставляем три простых и быстрых метода для оценки структурных детерминантов в общей РНК HDM, которые необходимы для регулирования аллергена индуцированного эозинофильного воспаления легких.
Слизистая иммунная система является крупнейшим иммунным органом в организме и служит первой линией защиты хозяина от микробных инфекций и аллергических оскорблений7,,8. Длинная dsRNA, репликация промежуточных многих вирусов, как известно, функционировать как патоген-ассоциированных молекулярной картины (PAMP), чтобы мощно стимулировать врожденные реакции через Toll как рецептор 3 (TLR3), чтобы вызвать выражение интерферона стимулировали гены (ISGs)9,10,11,12,13,14., Недавно мы показали, что HDM общей РНК содержит dsRNA структур, которые upregulated выражение ISGs и снижение тяжелой эозинофильных воспаление легких при введении через интракачельной привиливания в мурин модель аллергической астмы индуцированных HDM экстракты15. Тяжесть воспаления легких определяется путем анализа типов иммунных клеток в бронхоалвой лаваге (BAL) и легочной ткани через цитометрию потока16,,17,,18,19,20.
Этот протокол включает в себя три анализа: 1) быстрое обнаружение структур dsRNA с РНК точка пятно с помощью мыши моноклонального антитела J2, который специально связывается с dsRNA (40bp) в последовательности независимой манере; 2) быстрая оценка in vivo эффектов иммуностимуляторной РНК в легких мыши путем измерения индукции ISGs с помощью РТ-qPCR; 3) точная количественная количественная оценка эозинофилов в BAL и легких в контексте воспаления легких, вызванного HDM, с помощью анализа цитометрии потока.
Вышеупомянутые анализы могут быть использованы для изучения не только аллергических заболеваний легких, но и респираторных бактериальных и вирусных инфекций. Например, dsRNA специфические антитела J2 также могут быть использованы в других приложениях, таких как хроматография иммуноафизменности, иммуногистохимия, фермент-связанный иммуносорбент анализ (ELISA) и иммуносументирование21,22,23. Кроме того, несколько приложений вниз по течению сбора жидкости BAL могут быть использованы для количественной оценки растворимого содержимого, таких как цитокины и хемокины с использованием ELISA, и транскрипционное профилирование клеток в дыхательных путях (например, альвеолярные макрофаги). Хотя Есть целый ряд протоколов, доступных в литературе для оценки состояния легких, большинство из этих протоколов часто сосредоточены на целевой проверки. Описанные здесь процедуры могут быть применены для выявления компонентов экологических аллергенов, которые важны для регулирования развития аллергических заболеваний.
протокол
Экспериментальные процедуры, описанные здесь, были одобрены Институциональным комитетом по уходу за животными и использованию Техасского университета в Сан-Антонио.
1. Точка пятно, чтобы показать наличие структур dsRNA в HDM общей РНК
- Полная изоляция РНК от аллергенов, насекомых и аллергенов, не являя насекомых
- Положите HDM, насекомых или не насекомых животных, собранных живыми или полученными коммерчески в 50 мЛ труб, и быстро заморозить с жидкостью-N2. Затем храните при -70 градусов по Цельсию для последующей полной изоляции РНК.
ПРИМЕЧАНИЕ: В этом эксперименте, HDM, насекомых и не насекомых животных были выбраны, потому что они, как известно, общие источники аллергенов. Кроме того, иммуностимуляторная функция их РНК остается неясной. - Перенесите надлежащее количество (эквивалентно 100 мл в объеме или меньше) HDM, насекомых или животных, не содержащих насекомых, хранящихся при -70 градусов по Цельсию, в трубку объемом 2 мл, содержащую бисер (1,4 мм керамические сферы), затем замораживайте трубки в контейнере liquid-N2 в течение 10 минут.
- Для полной изоляции РНК, добавить 1 мЛ guanidinium thiocyanate основе РНК изоляционный реагент24 к каждой трубке, а затем разорвать насекомых и не-насекомых мелких животных с высокоэнергетических клеточных разрушителей на максимальной скорости 45 с и холод на льду. Повторите этот шаг дважды.
- Перенесите раствор с шага 1.1.3 в новую трубку 1,5 мл и добавьте 200 мл хлороформа в каждую трубку и вихрь. Центрифуги трубы на 14000 х г в течение 14 мин при 4 градусов по Цельсию.
- После завершения центрифугации перенесите верхнюю аквеевую фазу (200 мл) в новую трубку 1,5 мл, содержащую 500 мл изопропанола для осадки гранул РНК. Не нарушайте межфаз. Рекомендуемое соотношение объема верхней фазы по сравнению с изопропанолом составляет 1:2,5 соотношения.
- Смешайте по нежному вихрю, затем центрифуги трубы на 14000 х г в течение 14 мин при 4 градусов по Цельсию.
- Аспирировать супернатанта с осторожностью, затем мыть гранулы РНК с 500 мл 75% этанола и центрифуги на 7500 х г в течение 10 мин при 4 градусов по Цельсию. Удалите всю жидкость с осторожностью, высушите гранулы и растворите гранулы РНК с 20-50 л RNase-free H2O.
- Измерьте концентрацию РНК с помощью спектрофотометра, используя следующие параметры:
- Откройте связанное программное обеспечение и выберите тип нуклеиновых кислот для измерения. Измените тип образца на РНК.
- Выполните пустое измерение с 1-2 мл RNase-бесплатно H2O. Протрите RNase-бесплатно H2O. Теперь прибор готов к измерению.
- Загрузите 1-2 л образца РНК и измерьте концентрацию РНК (мкг/л).
ПРИМЕЧАНИЕ: Соотношение абсорбции на уровне 260 и 280 нм (A260/280) на уровне 2,0 (1,9-2,2) принято как "чистое" для РНК. Если не обрабатывается немедленно, хранить образцы РНК при -70 градусов по Цельсию и избежать замораживания-оттепели циклов сохранить РНК нетронутыми.
- Положите HDM, насекомых или не насекомых животных, собранных живыми или полученными коммерчески в 50 мЛ труб, и быстро заморозить с жидкостью-N2. Затем храните при -70 градусов по Цельсию для последующей полной изоляции РНК.
- Обнаружение структуры dsRNA в общей РНК с использованием dsRNA специфического антитела J2
- Подготовьте два 20 мл образцов РНК (200 нг/л). Один с RNase-III лечения (1 мл для 1 мкг РНК, инкубировать при 37 градусов по Цельсию в течение 60 мин), а другой без RNase-III лечения.
ПРИМЕЧАНИЕ: RNase III используется здесь, чтобы специально деградировать dsRNA, но не одноцепочечную РНК25. - Используйте карандаш, чтобы нарисовать сетки, где образцы РНК будут смыты на мембране.
- Найдите 2 л из 200 нг/л образца РНК на положительно заряженной нейлоновой мембране.
- Перекрестная ссылка образцов на мембрану на 1200 микроджоулей х 100 в УФ-кросслинкер. Повторите шаги 1.2.3 и 1.2.4 больше в месте образца. Это приведет к общей сложности 0,8 мкг за помарку.
ПРИМЕЧАНИЕ: Не замечайте более 2 МЛ образца РНК на мембране одновременно. - Блок неспецифическая привязка с 5% молока в TBS-T на 1 ч с встряхиванием при комнатной температуре. Снимите блокирующий раствор с шага 1.2.5 и добавьте антитела anti-dsRNA J2 при разбавлении 1:1,000 в 1% молоке в TBS-T и инкубировать на ночь с встряхиванием при 4 градусах Цельсия.
- Вымойте мембрану с TBS-T в течение 5 минут и повторите этот шаг в течение 3 раз. Добавьте вторичное антитело (щелочный фосфатаза-конъюгированный анти-мышеловатый IgG, разбавленный в 1% молоке 1:5,000) и инкубировать в течение 1 ч на шейкере при комнатной температуре. Вымойте мембрану с TBS-T в течение 5 мин и повторите этот шаг в течение 3x.
- Добавьте субстрат (BCIP/NBT) и инкубировать в течение 5-15 мин до тех пор, пока не будет виден желаемый сигнал.
- Остановить реакцию путем полоски мембраны с ddH2O.
- Высушите мембрану на тканевых бумагах и сфотографируйте с помощью смартфона (репрезентативный результат показан на рисунке 1).
- Подготовьте два 20 мл образцов РНК (200 нг/л). Один с RNase-III лечения (1 мл для 1 мкг РНК, инкубировать при 37 градусов по Цельсию в течение 60 мин), а другой без RNase-III лечения.
2. RT-qPCR для измерения способности HDM общей РНК в стимулировании экспрессии легких ISGs
- Изоляция РНК от тканей легких мышей
ПРИМЕЧАНИЕ: Мыши (женщины, 8-12 недель, C57BL/6J) поддерживались в конкретных условиях, свободных от патогенов.- Кратко анестезировать животное с изофлураном и вводить через интрачеальную закамупочку с 5 мкг (разбавленным в 80 МЛ PBS) РНК HDM обработанных с или без RNase III.
- После 16-18 ч после лечения РНК HDM, пожертвовать мышь CO2 ингаляции в течение нескольких минут. Затем поместите мышь на платформу и контактные конечности с иглами.
- Дезинфицировать мышь с 70% этанола затем сократить кожу, начиная от живота до шеи с стерилизованными ножницами.
- Исправить кожу с иглами и сократить ребра подвергать легких. Удалите все легкие и вымыть их с холодной PBS. Поместите легкие на тканевые бумаги и акцизный один маленький кусочек каждого легкого-лепестка в трубку 2 мл, содержащую бисер (200-300 мл в объеме, 1,4 мм керамических сфер).
ПРИМЕЧАНИЕ: Цель использования керамических бусинок заключается в том, чтобы измельчить целые ткани легких - Заморозить образцы легких, поместив трубки в контейнер жидкости-N2 в течение 10 минут.
- Добавьте 500 мл реагента РНК на основе гуанидининия тинацианата в каждую трубку и разбейте ткани легких гогенизатором на 45 с. Холод на льду между каждым шагом. Повторите этот шаг дважды.
- Следуйте шагам 1.1.4- 1.1.7 для изоляции РНК легких.
- Воздух-сухой гранулы и растворить гранулы РНК с надлежащим количеством RNase-бесплатно H2O (20-30 мл).
- Измерьте концентрацию РНК, описанную в шаге 1.1.8.
- RT-qPCR определяет способность РНК HDM в стимулировании экспрессии генов легких.
- Используя 100 нг/л РНК, извлеченную из легочных тканей в качестве шаблона, выполняйте синтез кДНК в соответствии с протоколом26.
- Настройка реакции RT-qPCR на 10 мл/год для 384-хорошо пластины с использованием cDNA генерируется выше и ген-специфических праймер пар (Таблица 1 и Таблица 2).
- Печать скважин плотно с прозрачной клейкой пленкой и вихрь пластины для 30 с. Спин пластины на 1000 х г на 30 с для сбора образцов в нижней части скважин.
- Загрузите пластину на аппарат RT-qPCR и начните работать с реакцией RT-qPCR с помощью протокола теплового цикла(таблица 3).
- Экспорт результатов в файл электронной таблицы или анализ данных с помощью программного обеспечения, предоставляемого производством после завершения программы (репрезентативный результат отображается на рисунке 2).
3. Анализ FACS для определения влияния РНК HDM на инфильтрацию эозинофилов в BAL и легких
- Сбор жидкости BAL для анализа FACS
- Euthanize мышей (женщины, 8-12 недель, C57BL/6J), которые были обработаны с экстрактами аллергена HDM (согласно экспериментальному дизайну показаны в рисунке 3B) путем вдыхания CO2.
- Поместите мышь на платформу и контактные конечности с иглами.
- Дезинфицировать мышь 70% этанолом. Используйте ножницы, чтобы вырезать кожу от верхней части живота до шеи.
- Аккуратно, потяните слюнные железы и стернохоидной мышцы тщательно друг от друга с помощью щипцов, чтобы разоблачить трахею. Поместите нейлоновую струну (10 см) под трахею с помощью щипцов.
- Сделать разрез в трахее (2 мм под гортани) достаточно, чтобы вставить канюлю. Не прорезайте трахею. Узел строки вокруг трахеи и канюлы.
- Загрузите шприц с 1 мл ИЗ-ЗА ИДТА и прикрепите его к концу канюли. Введите 1 мЛ ИЗ-ЗАТА в легкие и полностью аспирировать раствор. Аккуратно отсоедините шприц от канюли и перенесите раствор в трубку 15 мЛ на льду.
- Перезагрузите шприц со свежим PBS-EDTA и повторите этот шаг 2x.
- Центрифуга трубки, содержащей объединенный BAL, полученную в шаге 3.1.7, чтобы гранулировать клетки при 500 х г в течение 7 мин при 4 градусов по Цельсию. Запишите объем жидкости BAL, затем перенесите супернатант на две 1,5 мЛ труб, не нарушая гранулы.
ПРИМЕЧАНИЕ: Супернатант BAL может храниться при уровне -70 градусов по Цельсию для будущего анализа, например, ELISA. - В случае, если в грануле присутствуют РБК из-за сильного воспаления легких, после удаления супернатанта добавьте 500 мл буфера лизиса РБК и хорошо перемешайте при повторном рецусепенсе. Перенесите раствор в новую трубку 1,5 мл и центрифугу в течение 7 минут со скоростью 500 х г при 4 градусов по Цельсию.
- Удалите супернатант и повторно осуществите гранулы в 150 мл буфера FACS.
- Перенесите 150 МЛ повторного образца в 96-хорошо пластины и центрифуги пластины в течение 7 минут со скоростью 500 х г при 4 градусов по Цельсию.
- Быстро, инвертировать пластины на ткани документы для сбора клеток, проживающих в нижней части колодцев.
- Окрашивать клетки антителами в буфер FACS в присутствии 2,4G2 блокирующих антител (2,5 мкг / 100 мл). Инкубировать пластину при комнатной температуре в течение 30 минут в темном месте.
- После окрашивания, центрифуга пластины гранулы клетки на 500 х г в течение 7 мин при 4 градусов по Цельсию.
- Удалите раствор окрашивания путем инвертирования пластины на бумаге, затем промыть путем повторного времени с 100 МЛ буфера FACS. Далее, центрифуга пластины снова на 500 х г в течение 7 минут при 4 градусов по Цельсию и удалить буфер FACS путем инвертирования пластины на бумаге ткани.
- Повторные образцы в 150 МЛ буфера FACS и перенос образцов в трубы FACS, содержащие 350 МЛ буфера FACS. Добавьте 25 ЗЛ подсчета бисера к каждому образцу. Образцы теперь готовы к анализу цитометрии потока.
ПРИМЕЧАНИЕ: Различные типы клеток в жидкости BAL были помечены антителами, как указано. Подсчет бисера были добавлены до запуска FACS. Данные о цитометрии потока анализировались с помощью коммерчески доступного программного обеспечения. Обратитесь к рисунку 3 и таблице 4 для стратегии gating.
- Переваривание легочной ткани для анализа FACS
- Следуйте шагам 3.1.1 - 3.1.3.
- Вырезать кожу, начиная от живота до шеи с стерилизованными ножницами. Исправить кожу с иглами и сократить ребра подвергать легких.
- Удалите все легкие и вымыть их с холодной PBS. Поместите образцы в трубку 1,5 мл, содержащую 50 мл раствора пищеварения легких.
- Измельчить ткани легких на мелкие кусочки с изогнутыми ножницами. Перенесите ткани легких в 6-хорошую пластину, затем добавьте 8 мл раствора пищеварения легких. Поместите тарелку на шейкер в инкубаторе 37 градусов по Цельсию в течение 45 минут.
- После инкубации используйте верхнюю часть 1,5 мЛ трубки для измельчения легочных тканей. Поместите 70-м секорсы на новую 6-скважинную пластину и нанесите образец через фильтр 0,22 мкм.
- Перенесите фильтрованный раствор в трубку 15 мЛ, затем центрифуж трубки при 500 х г в течение 7 минут при 4 градусов по Цельсию. Аспирировать супернатанта и перезарядить гранулы в 1 мл буфера лизиса РБК и оставить его на льду в течение 3 мин.
- Перенесите образец в трубку 1,5 мл и центрифугу при 500 х г в течение 7 минут при 4 градусах Цельсия. Повторите 2x
- Вымойте клетки легких 2x с буфером 1 mL FACS. Аспирировать супернатант и resuspend гранулы в 1 мл буфера FACS, а затем передать 100 мл образца в 96 хорошо пластины.
- Центрифуга пластины в течение 7 мин со скоростью 500 х г при 4 градусов по Цельсию. Следуйте шагам, описанным в сборе жидкости BAL для анализа FACS (3.1.13 до 3.1.16), чтобы испачкать клетки переваренных образцов легочной ткани.
ПРИМЕЧАНИЕ: Эозинофилы в легких были помечены антителами, как указано, а затем смешаны с подсчетом бисера для дальнейшего анализа FACS. Данные о цитометрии потока были проанализированы с помощью связанного программного обеспечения. Обратитесь к рисунку 3 для оценки HDM РНК-индуцированных иммунных реакций.
4. Статистический анализ
- Выполните статистический анализ с использованием коммерчески доступного программного обеспечения.
- Определите значения p по неокрашенным двуххвостым тестом Student t для сравнения двух групп.
- Рассчитайте абсолютные числа эозинофилов на основе эталонных бусин (верхняя панель) с помощью формулы
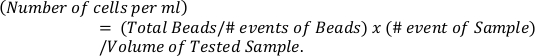
- Определите значения p двусторонним тестом ANOVA и Sidak для сравнения более двух групп.
- Рассмотрим значение p меньше 0,05 как статистически значимое. Значения p указаны на участках, как зп й lt;0.05, Зрхтт;0,01, Зл-пт;0,001, и ЗРХТ;0.0001.
ПРИМЕЧАНИЕ: Все рецепты буфера приведены в таблице 5.
Результаты
Присутствие длинных структур dsRNA в HDM, насекомых и не насекомых мелких животных было исследовано точка пятно с использованием DSRNA-специфических мыши моноклонального антитела J2 (40bp). RNase III был использован для переваривания dsRNA в 12-15 bp dsRNA фрагменты, которые были необнаружимы J2(р?...
Обсуждение
Текущий протокол описывает, как оценить иммуностимуляторные свойства аллерген-ассоциированной микробной РНК и их влияние на развитие эозинофильного воспаления легких в мышиной модели аллергической астмы. Хотя длинные dsRNAs известны как репликации промежуточных многих вирусов, которы...
Раскрытие информации
Нам нечего раскрывать.
Благодарности
Мы благодарим г-жу Карлу Горену за техническую помощь в цитометрии потока. L.S. поддерживается Китайским советом стипендий и Провинциальным инновационным фондом провинции Хунань для аспирантов (CX201713068). H.H.A. поддерживается кафедрой клинических лабораторных наук, Колледжем прикладных медицинских наук, Университетом Джуфа, Сакака, Саудовская Аравия. X.D.L. поддерживается UT здравоохранения Сан-Антонио школа медицины стартап-фонд и Макс и Минней Voelcker фонда.
Материалы
| Name | Company | Catalog Number | Comments |
| 0.40 µm Falcon Cell Strainer | Thermo Fisher Scientific | 08-771-1 | |
| 1 mL syringes | Henke Sass Wolf | 5010.200V0 | |
| 15 mL Tube | TH.Geyer | 7696702 | |
| 50 mL Tube | TH.Geyer | 7696705 | |
| 70% ethanol | Decon Labs | 2701 | |
| Absolute Counting Beads | Life Technologies Europe B.V. | C36950 | |
| ACK-RBC lysing buffer | Lonza | 10-548E | |
| Amersham Hybond-N+ Membrane | GE Healthcare | RPN203B | |
| Ant | San Antonio | Note: Locally collected | |
| Antibody dilution buffer | (see Table 5 for recipe) | ||
| Anti-Mouse CD11b V450 Rat (clone M1/70) | BD Bioscience | 560456 | 1 to 200 dilution |
| Anti-Mouse CD11c PE-Cy7 (clone N418) | BioLegend | 117317 | 1 to 200 dilution |
| Anti-Mouse CD19 Alexa Flour 647 (clone 1D3) | eBioscience | 15-0193-81 | 1 to 200 dilution |
| Anti-Mouse CD3e APC (clone 145-2C11) | Invitrogen | 15-0031-81 | 1 to 200 dilution |
| Anti-Mouse CD45 APC-Cy7 (clone: 30-F11) | BioLegend | 103130 | 1 to 200 dilution |
| Anti-Mouse Fixable Viabillity Dye eFluor 506 | Invitrogen | 65-0866-14 | 1 to 200 dilution |
| Anti-Mouse IgG (H+L), AP Conjugate | Promega | S3721 | |
| Anti-Mouse Ly-6G FITC (clone RB6-8C5) | Invitrogen | 11-5931-82 | 1 to 200 dilution |
| Anti-Mouse MHC II APC-eFluor 780 (clone M5/114.15.2) | eBioscience | 47-5321-80 | 1 to 200 dilution |
| Anti-Mouse Siglec-F PE (clone E50-2440) | BD Pharmingen | 552126 | 1 to 200 dilution |
| BCIP/NBT substrate | Thermo Fisher Scientific | PI34042 | |
| Blocking Buffer | (see Table 5 for recipe) | ||
| Cannual, 20G X 1.5” | CADENCE SCIENCE | 9920 | |
| Centrifuge | Thermo Fisher Scientific | 75004030 | |
| CFX384 Touch Real-Time PCR Detection System | Bio-Rad Laboratories | 1855485 | |
| Chloroform | Thermo Fisher Scientific | C298-500 | |
| Cockroach | Greer Laboratories | B26 | |
| Counting beads | Thermo Fisher Scientific | 01-1234-42 | |
| D. farinae | Greer Laboratories | B81 | |
| D. pteronyssinus | Greer Laboratories | B82 | |
| Denville Cell Culture Plates with lid, 96 well cell culture plate | Thomas Scientific | 1156F03 | |
| Digital Dry Bath - Four Blocks | Universal Medical, Inc. | BSH1004 | |
| Earthworm | San Antonio | Note: Locally collected | |
| Ethylenediaminetetraacetic acid (EDTA) | Sigma-Aldrich | E6511 | |
| FACS buffer | (see recipe in Table 5) | ||
| Falcon Round-Bottom Polypropylene Tubes, 5 mL | STEMCELLTM TECHNOLOGIES | 38056 | |
| Flow cytometer (BD FACS Celesta) | BD Biosciences | ||
| Fly | Greer Laboratories | B8 | |
| Forceps | Roboz Surgical Instrument | RS-5135 | |
| Hemocytometer | Hausser Scientific | 3110 | |
| HT-DNA | Sigma | D6898 | |
| In Vivo MAb anti-mouse CD16/CD32 (clone: 2.4G2) | Bio X Cell | BE0307 | |
| iScript cDNA Synthesis Kit | Bio-Rad Laboratories | 1708891 | |
| Isoflurane | Abbott Labs | sc-363629Rx | |
| Isopropanol | Thermo Fisher Scientific | BP2618500 | |
| J2 anti-dsRNA monoclonal antibody | SCICONS | 10010200 | |
| Lung digestion solution | (see recipe in Table 5) | ||
| Lysing Matrix D | MP Biomedicals | 116913050-CF | |
| Lysing Matrix D, 2 mL tube | MP Biomedicals | SKU:116913100 | |
| Mice (female, 8-12 weeks old, C57BL/6J) | Jackson Laboratory | #000664 | |
| Microcentrifuge tube 1.5 mL | Sigma-Aldrich | 30120.094 | |
| Microscope | Olympus | CK30 | |
| Mini-BeadBeater | Homogenizers | SKU:BS:607 | |
| Mini-Beadbeater-16 | Biospec | 607 | |
| Mosquito | Greer Laboratories | B55 | |
| NanoDrop 2000C | Thermo Scientific Spectophotometer Medex Supply | TSCND2000C | |
| Needle, 21 G x 1 1/2 in | BD Biosciences | 305167 | |
| Non-fat milk | Bio-Rad Laboratories | 1706404 | |
| Nylon string | Dynarex | 3243 | |
| Phosphate-buffered Saline (PBS) | Lonza | BE17-516F | |
| RNase III | Thermo Fisher Scientific | AM2290 | |
| RNase T1 | Thermo Fisher Scientific | AM2283 | |
| Scissors | Roboz Surgical Instrument | RS-6802 | |
| Shaker or Small laboratory mixer | Boekel Scientific | 201100 | |
| SPHERO AccuCount Fluorescent | Spherotech | ACFP-70-5 | 1 to 10 dilution |
| Spider | San Antonio | Note: Locally collected | |
| TBS | (see recipe in Table 5) | ||
| TBS-T | (see recipe in Table 5) | ||
| Total cell medium | (see recipe in Table 5) | ||
| TRIzol Reagent | Thermo Fisher Scientific | 15596018 | |
| Tween 20 | Sigma-Aldrich | P9416 | |
| UV Stratalinker 2400 UV | LabX | 20447 | |
| Wasp | San Antonio | Note: Locally collected |
Ссылки
- Strachan, D. P. Hay fever, hygiene, and household size. BMJ. 299, 1259-1260 (1989).
- Schuijs, M. J., et al. Farm dust and endotoxin protect against allergy through A20 induction in lung epithelial cells. Science. 349, 1106-1110 (2015).
- Stein, M. M., et al. Innate Immunity and Asthma Risk in Amish and Hutterite Farm Children. New England Journal of Medicine. 375, 411-421 (2016).
- Roers, A., Hiller, B., Hornung, V. Recognition of Endogenous Nucleic Acids by the Innate Immune System. Immunity. 44, 739-754 (2016).
- Schlee, M., Hartmann, G. Discriminating self from non-self in nucleic acid sensing. Nature Reviews Immunology. 16, 566-580 (2016).
- Wu, J., Chen, Z. J. Innate immune sensing and signaling of cytosolic nucleic acids. Annual Reviews Immunology. 32, 461-488 (2014).
- O'Hara, A. M., Shanahan, F. The gut flora as a forgotten organ. EMBO Reports. 7 (7), 688-693 (2006).
- . Focused Meeting 2018: Microbes and Mucosal Surfaces Available from: https://microbiologysociety.org/event/society-events-and-meetings/focused-meeting-2018-microbes-and-mucosal-surfaces.html (2018)
- Weber, F., et al. Double-stranded RNA is produced by positive-strand RNA viruses and DNA viruses but not in detectable amounts by negative-strand RNA viruses. Journal of Virology. 80, 5059-5064 (2006).
- Barral, P. M., et al. Functions of the cytoplasmic RNA sensors RIG-I and MDA-5: Key regulators of innate immunity. Pharmacology and Therapeutics. 124, 219-234 (2009).
- Netea, M. G., et al. From the Th1/Th2 paradigm towards a Toll-like receptor/T-helper bias. Antimicrobial Agents and Chemotherapy. 49, 3991-3996 (2005).
- McNally, B., et al. Intranasal administration of dsRNA analog poly(I:C) induces interferon-alpha receptor-dependent accumulation of antigen experienced T cells in the airways. PLoS One. 7, 51351 (2012).
- Seya, T., Takeda, Y., Matsumoto, M. Tumor vaccines with dsRNA adjuvant ARNAX induces antigen-specific tumor shrinkage without cytokinemia. Oncoimmunology. 5, 1043506 (2016).
- Toussi, D. N., Massari, P. Immune Adjuvant Effect of molecularly defined Toll-Like Receptor Ligands. Vaccines (Basel). 2, 323-353 (2014).
- She, L., et al. Immune Sensing of Aeroallergen-Associated Double-Stranded RNA Triggers an IFN Response and Modulates Type 2 Lung Inflammation. Journal of Immunology. 203, 2520-2531 (2019).
- Fujimoto, Y., et al. Pulmonary inflammation and cytokine dynamics of bronchoalveolar lavage fluid from a mouse model of bronchial asthma during A(H1N1)pdm09 influenza infection. Science Reports. 7, 9128 (2017).
- Yao, Y., et al. Induction of Autonomous Memory Alveolar Macrophages Requires T Cell Help and Is Critical to Trained Immunity. Cell. 175, 1634-1650 (2018).
- Dua, K., Shukla, S. D., Hansbro, P. M. Aspiration techniques for bronchoalveolar lavage in translational respiratory research: Paving the way to develop novel therapeutic moieties. Journal of Biological Methods. 4, 73 (2017).
- Van Hoecke, L., et al. Bronchoalveolar Lavage of Murine Lungs to Analyze Inflammatory Cell Infiltration. Journal of Visualized Experiments. (123), e55398 (2017).
- Salahuddin, S., et al. Processing of Bronchoalveolar Lavage Fluid and Matched Blood for Alveolar Macrophage and CD4+ T-cell Immunophenotyping and HIV Reservoir Assessment. Journal of Visualized Experiments. (148), e59427 (2019).
- Son, K. N., Liang, Z., Lipton, H. L. Double-Stranded RNA Is Detected by Immunofluorescence Analysis in RNA and DNA Virus Infections, Including Those by Negative-Stranded RNA Viruses. Journal of Virology. 89, 9383-9392 (2015).
- Monsion, B., et al. Efficient Detection of Long dsRNA in Vitro and in Vivo Using the dsRNA Binding Domain from FHV B2 Protein. Front Plant Sci. 9, 70 (2018).
- Redente, E. F., et al. Age and sex dimorphisms contribute to the severity of bleomycin-induced lung injury and fibrosis. American Journal of Physiology-Lung Cellular and Molecular Physiology. 301, 510-518 (2011).
- Card, J. W., et al. Gender differences in murine airway responsiveness and lipopolysaccharide-induced inflammation. Journal of Immunology. 177, 621-630 (2006).
- Gueders, M. M., et al. Mouse models of asthma: a comparison between C57BL/6 and BALB/c strains regarding bronchial responsiveness, inflammation, and cytokine production. Inflammation Research. 58, 845-854 (2009).
Перепечатки и разрешения
Запросить разрешение на использование текста или рисунков этого JoVE статьи
Запросить разрешениеThis article has been published
Video Coming Soon
Авторские права © 2025 MyJoVE Corporation. Все права защищены